107644

Ciepło mieszania jest ujemne; - reakcja egzotermiczna;
Objętość roztworu jest mniejsza od objętości roztworów czystych;
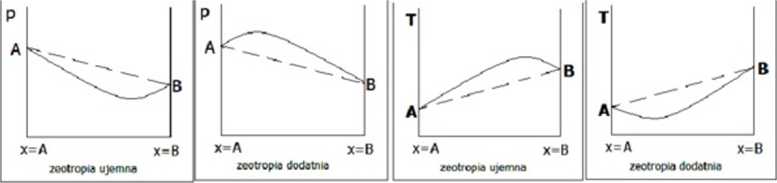
Destylacja jest procesem fizykochemicznym. Polega on na ogrzewaniu roztworu wieloskładnikowego do temperanny wrzenia pod stałym lub programowym ciśnieniem. W wyniku ogrzewania roztworu doskonałego mieszanina zaczyna wrceć. Wytworzona para zawiera więcej składnika bardziej lotnego tuż roztwór wyjściowy. Z paty po skropleniu powstaje kondensator o niższej temperaturze wrzenia.W wyniku powtarzających się procesów kondensacji i wrzenia można dokonać całkowitego rozdziału substancji niezbędnych warunkiem stosowania taj metody jest, aby skład pary różnił się od składu cieczy.
2. CEL ĆWICZENIA:
Celem ćwiczenia jest sporządzenie wykresu równowagowego temperatur wrzenia badanych roztworów w funkcji składu cieczy i pary, z uwzględnieniem temperatur wtzenia czystych składników, a także porównanie kizywej doświadczalnej z teoretyczną krzywą równowagową ciecz-para.
3. ZADANE PARAMETRY:
Dane są czyste substancje: heksan i toluen, a także roztwory toluen-heksan o określonych ułamkach molowych każdego składnika: x. Należy przeprowadzić destylację podanych mieszanin, a następnie metodą refraktometryczną określić stężenie poszczególnych składników w cieczy podestylacyjnej i kondensacie pary, aby w ten sposób określić krzywą równowagową ciecz-para. Do skonstruowania wykresu potrzebne też są temperanny wtzenia każdej mieszaniny. Krzywą teoretyczną konstruuje się ze znajomości m.iii ciśnienia panującego w otoczeniu układu badawczego.
4. SPOSÓB WYKONANIA ĆWICZENIA:
1. Przygotowanie zestawu i roztworu do destylacji - napełnienie aparam ok 35 ml roztworu o zadanym składzie, uruchomienie przepływu wody przez chłodnicę, podłączenie układu grzewczego.
2. Powolne doprowadzenie układu do wrzenia, kontrolowanie prawidłowej cyrkulacji cieczy (poprzez zawór trójdrożny) i chłodzenie par w chłodnicy zwrotnej.
3. Odczytanie temperatury wrzenia z dokładnością 0.1 st. Ć. po ustabilizowaniu się procesu wrzenia (czyli po około 15-tu minutach). Prowadzenie procesu jeszcze przez ok 5-10 minut.
4. Odłączenie układu grzewczego, zebranie cieczy (która przestała wrzeć) oraz kondensam pary do osobnych, czystych, suchych i zamykanych naczynek
5. Zebrane ciecze ostudzić do temperatury otoczenia, zmierzyć współczynnik załamania światła (a tym samym określić ułamki molowe składników), ciecze zlać do wyjściowego naczynia celem ich powtórnego użycia.
6. Ponadto odczytuje się ciśnienie panujące w pracowni, w czasie przeprowadzania doświadczenia.
Pomiarów dokonuje się dla każdego stężenia.
|
Objętość Toluenu |
Objętość Heksanu |
Ułamek mol. toluenu |
Ułamek mol. heksanu | |
|
HEKSAN-TOLUEN 6:5 |
15,8 cm3 |
19,2 cm3 |
0,45 |
0,55 |
|
HEKSAN-TOLUEN 1:1 |
17,4 cm3 |
17,6 cm3 |
0.5 |
0.5 |
|
HEKSAN-TOLUEN 2:1 |
12 cm3 |
23 cm3 |
0,34 |
0,66 |
2
Wyszukiwarka
Podobne podstrony:
ZaA5 Uwzględnić reakcje spalania z zad.4 jeżeli udział powietrza w mieszaninie jest o 5% większy od
Kwas siarkowy. Mieszanina SO3 i H2O w stosunku 1:1 to monohydrat. Jeżeli stosunek ten jest mniejszy
PB040198 Potencjał chemiczny rozpuszczalnika w roztworze uf (p. T. xr )= uf (p. T)+ RTIn xr < uf
Zdjęcie0544 Masa producentów w oceanie jest mniejsza od mas> organizmów, które się nią zvw lą&nbs
Slajd26 Ciecz zwilżająca ciecz zwilża ciało stale jeśli jej energia powierzchniowa właściwa jes
statystyka skrypt�47 Świadczy też o tym wartość p ■ 0,0000, która jest mniejsza od przyjętej wartośc
img56 LIS POLARNY (A!opex lagopus) Jest mniejszy od zwykłego rudego lisa. Zamieszkuje Północną Amery
skanowanie0066 ^3))Energia Ej jest zawsze większa od energii Ev C) Energia E, raz jest mniejsza od e
skanuj0004 (1045x1600) Powierzchnia przyśrodkowa jest mniejsza od omawianej sylwety zęba i ogranicze
http ://l ay er. uci. agh. edu. pl/ maglay/wrona sów jest mniejszy od czasu propagacji sygnału w bra
140 Monika Jeziorska jest mniejsza od OB, właściciele mają bodziec do odmowy zapłaty i przekazania b
Zadanie 4.3. (0-4) Para (liczba 1, słowo 1) jest mniejsza od pary (liczba!, slowo2 gdy: -
Untitled16 186 II. Klasyczna myśl ekonomia, Malthus i Marks prognozy jest mniejsze od jedności. Tak
więcej podobnych podstron