Antybiotyk |
β-laktamowe |
||||
|
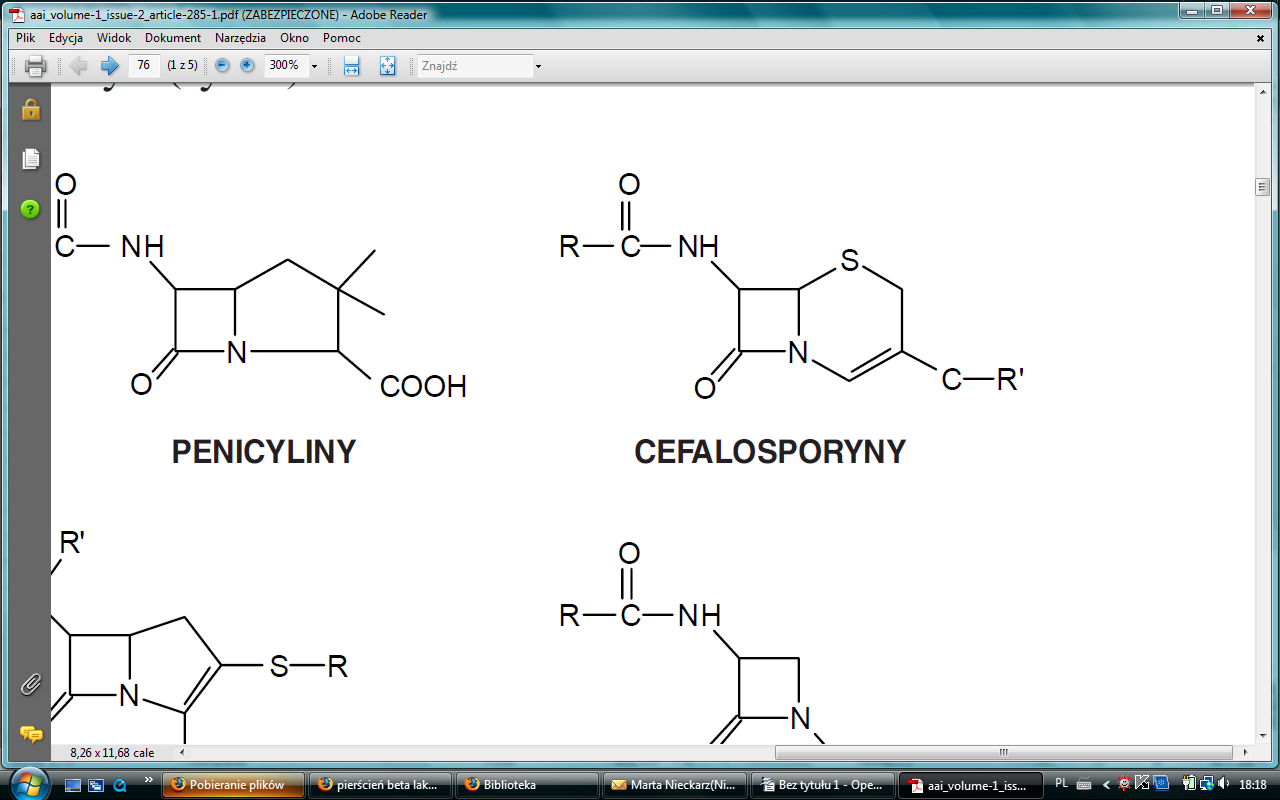
Penicyliny |
Cefalosporyny |
Metabolity Streptomyces: Cefamycyny Kwas klawulanowy Tienamycyna |
||
Wzór |
|
|
Kwas klawulanowy - inhibitor β-laktamaz |
||
Układ |
penam |
cef-3-em |
monocykliczny |
||
Pierścienie |
β-laktamowy + tiazolidynowy |
β-laktamowy + dihydrotiazynowy |
pojedynczy β-laktamowy |
||
Producent: |
Penicillium chrysogenum |
Acremonium chrysogenum (=Cephalosporium acremonium) |
Streptomyces sp. |
||
Naturalne antybiotyki: |
Penicylina benzylowa G Penicylina fenoksymetylowa V |
Cefalosporyna C |
|
||
Związki do syntezy półsyn. pochodnych: |
Acylaza penicylinowa
|
Cefamycyna C |
|
||
Półsyntetyczne pochodne: |
II generacji: metycylina III generacji: ampicylina, amoksycylina (Augmentin) IV generacji: karbenicylina, piperacylina |
I generacji: cefalotyna, cefalorydyna II generacji: cefoksytyna (cefamycyna) |
|
||
Mechanizm działania: |
→ inhibicja III etapu biosyntezy peptydoglikanu (przebiega z udziałem białek PBP) poprzez nieodwracalne wiązanie się antybiotyku z PBP |
||||
Mechanizm oporności: |
|
||||
Chemiczne modyfikacje: |
W pozycji C-6 pierścienia β-latamowego |
W pozycji C-7 pierścienia β-latamowego W pozycji C-3 pierścienia dihydrotiazynowego |
|
||
Antybiotyk |
Chinony |
|
|
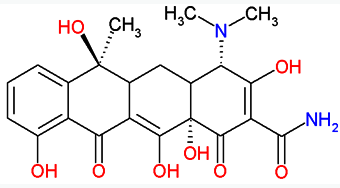
Tetracyklina |
Antracyklina |
Wzór |
|
|
Budowa: |
Układ czteropierścieniowy (oktahydronaftacenu) pozycje 5,6,7 podlegają modyfikacjom |
Układ czteropierścieniowy + grupa glikozylowa |
Producenci: |
Streptomyces aureofaciens Streptomyces rimosus |
Streptomyces purpurascens Streptomyces peucetius Streptomyces galileus |
Naturalne antybiotyki: |
chlorotetracyklina oksytetracyklina tetracyklina |
daunorubicyna doksorubicyna |
Półsyntetyczne pochodne: |
metacyklina, doksycyklina, minocyklina syntetyczna pochodna → tiatetracyklina |
|
Biosynteza: |
→ szlak poliketydowy |
→ szlak poliketydowy |
Mechanizm działania: |
|
|
Skutki uboczne: |
|
|
Mechanizm oporności: |
- zmiany sekwencji AA białek rybosomu - ograniczone przenikanie przez pompy (niespecyficzne) - mechanizmy oporności specyficznej - efflux (aktywne usuwanie tetracykliny) - enzymatyczna inaktywacja |
|
Antybiotyk |
Makrocykliczne |
|||||
|
Makrolidy → erytromycyna |
Ansamycyny → ryfamycyny |
||||
Wzór |
|
|
||||
Budowa: |
14 członowy pierścień makrolidowy + pochodne deoksycukrów |
Mostek ansa łączący dwa przeciwległe brzegi układu cyklicznego: naftalenu i pierścienia furanowego |
||||
Producenci |
Saccharopolyspora erytrea |
Amycolatopsis mediterranei |
||||
Naturalne antybiotyki |
Erytromycyna A (gram+) |
Ryfamycyna: A, B, C, D, E + O, S, SV, Y, G (gram+, prątki gruźlicy) |
||||
Biosynteza |
→ szlak poliketydowy |
→ szlak poliketydowy |
||||
Półsyntetyczne pochodne |
(gram+, gram-, H.pylori, C.jejuni)
|
(gram+, gram-) |
||||
Mech. działania |
→ hamuje translację - wiąże się z podjednostką 50S rybosomu, zablokowane wiązanie z tRNA |
→ zatrzymanie syntezy RNA przez zablokowanie polimerazy RNA |
||||
Mech. oporności |
- metylacja 23S rRNA - modyfikacja białek L4 i L22 w 50S rybosomu - enzymatyczna inaktywacja leku aktywne usuwanie przez pompy |
- mutacje punktowe i delecje w genie rpoB podjednostki β polimerazy RNA
|
||||
Biosynteza |
Prekursory: propionylo-CoA, metylomalonylo-CoA kondensują, następnie cyklizacja → erytromycyna D ważne enzymy: kinaza propionianowa, karboksylaza propionylo-CoA |
Kondensacja aktywowanych kw. org. (podjednostki octanowe i propionowe dołączane do kwasu 3-amino-5-hydroksybenzoesowego) (dodajemy barbiturany) |
||||
Inne: |
Erytromycyna A:B:C (50:1:5) |
Modyfikacje genetyczne:
|
||||
Antybiotyk |
Aminoglikozydy |
|||||
|
Streptomycyna |
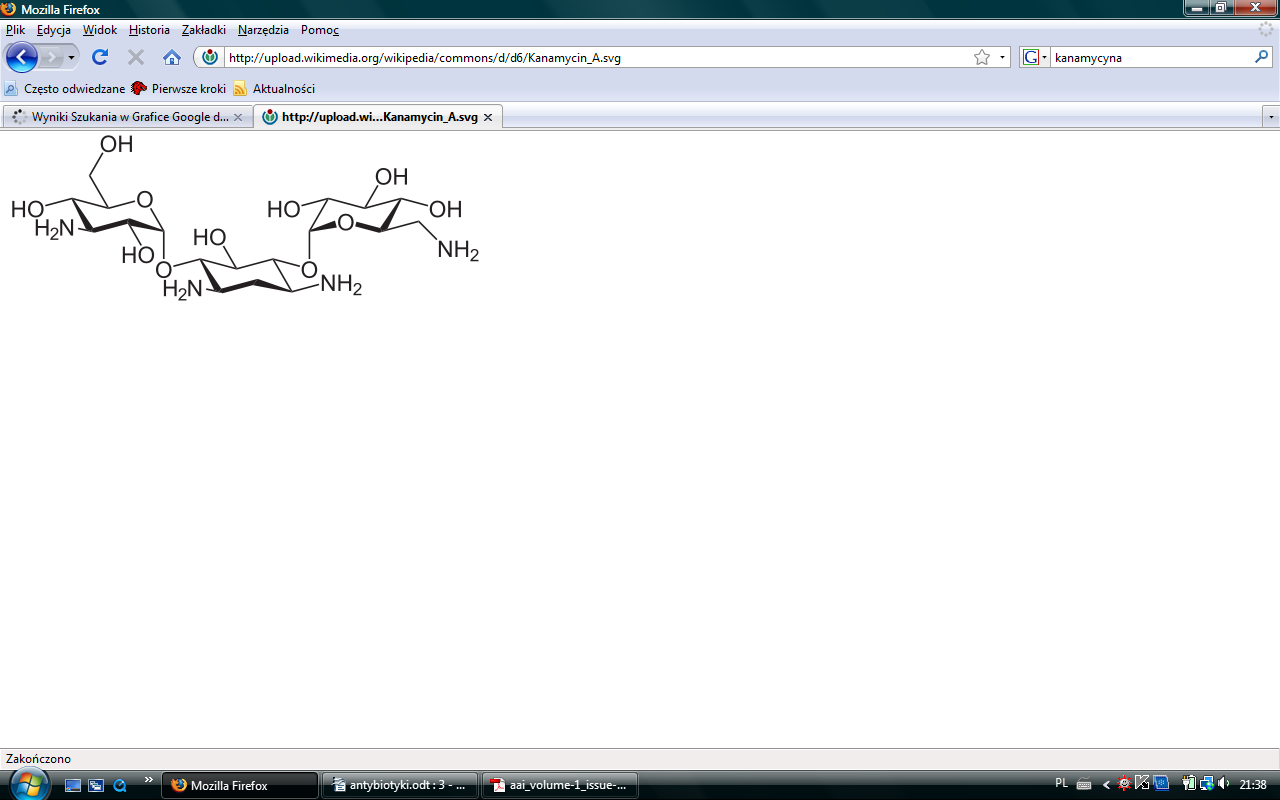
Kanamycyna |
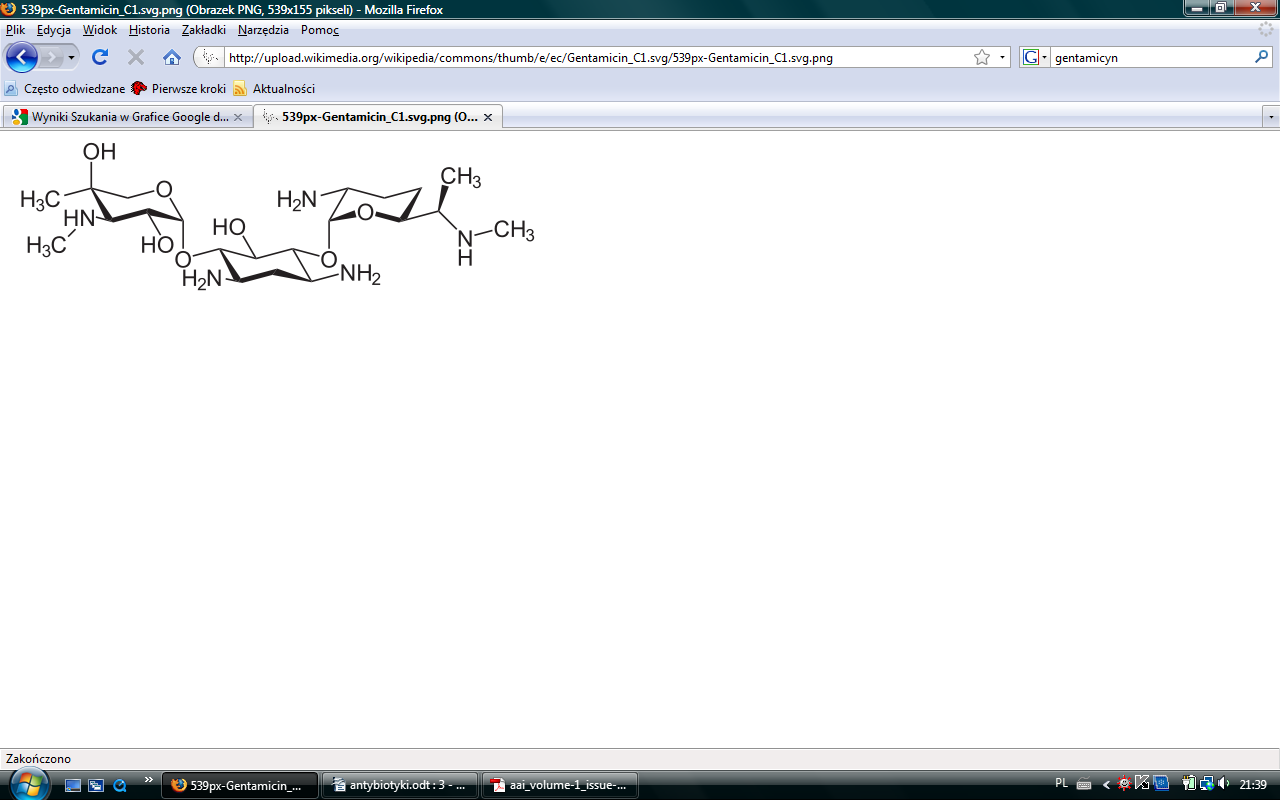
Gentamicyna |
|||
Wzór |
|
1957r. |
1963r. |
|||
Producenci |
Strepromyces grisens |
Strepromyces kanamyceticus |
Micromonospora purpurea (grzyb) |
|||
Budowa: |
Część niecukrowa =aminocyklitol (aglikon) + reszty cukrowe/aminocukrowe
grupa I: streptomycyna - ma aminocyklitol streptydyny grupa II - kanamycyna, gentamycyna - ma 2-deoksystreptaminę |
|||||
Naturalne |
Streptomycyna, kanamycyna, gentamicyna |
|||||
Półsyntetyczne |
Amikacyna - pochodna kanamycyny Dibekacyna retylmycyna izepamycyna |
|||||
Mechanizmdziałania |
- zahamowanie translacji - aktywnośc wobec 30S rybosomu - blokowanie dekodowania (oddziaływanie kodon-antykodon) - aminoglikozyd stanowi zawadę steryczną |
|||||
Mechanizm oporności patogenu |
|
|||||
Mechanizmoporności producenta |
|
|||||
Aktywność |
Streptomycyna - M. tuberculosis Gentamicyna - szerokie spektrum, Enterobacteriaceae, P. aeruginosa bakterie gramujemne |
|||||
Skutki uboczne |
Ototoksyczność (uszkodzenie narządu słuchu), nefrotoksyczność (uszkodzenia nerek) |
|||||
Biogeneza |
Glukoza → fosforan streptydyny → fosforan dihydroksystreptydyny → N-metylo-L-glukozamina → fosforan dihydrostreptomycyny → transport poza komórkę → defosforylacja → streptomycyna |
|||||
Regulacja produkcji |
Dwie fazy:
→ regulacja czynnikiem A (powoduje wzrost produkcji str) |
|||||
|
Polipeptydowe |
||
Budowa |
- Złożona - Łańcuchy zbudowane z reszt L-i D-aminokwasów - Kilka- kilka tys. Da - Peptydy liniowe/cykliczne - Nie są syntetyzowane na rybosomach - Synteza z udziałem enzymów |
||
Producenci: |
Bacillus brevis - gramicydyna B. lichniformis - bacytracyna B. polymyxa - polimyksyna (lipopeptyd) |
||
Synteza |
NRPS (=nierybosomalna synteza peptydów) → kompleks anzymatyczny z kilku modułów → w każdym module 3 domeny:
→ białko PCP dostarcza reszt aminoacylowych |
||
Cel |
- błona cytoplazmatyczna (tworzą pory powodując wyciek) - wyjątek glikopeptydowe
|
||
Glikopeptydowe |
Lantybiotyki |
||
1956r. - wankomycyna 1978r. - teikoplanina → na gram + (są duże, i nie mogą penetrować przez błonę gram -) |
Gram+ i gram - dopuszczona do przemysłu spożywczego jako inhiitor wzrostu drobnoustrojów |
||
Wankomycyna - Streptomyces orientalis |
Nizyna - Lactococcus lactis |
||
|
Część cukrowa → toksyczność wanko |
Dimer z liniowych podjednostek z 34 AA |
|
|
Silnie modyfikowana |
Nizyna A, Z, S |
|
|
Cel działania: peptydoglikan, etap biosyntezy → wiąże się do 2 AA w mostku penapeptydowym , hamuje przyłączanie PBP |
Układ lantioniny (między Ala-Ala i Ala-kw. Aminomasłowy) - mostki siarczkowe → nadają opornośc na działanie proteaz |
|
|
Mechanizm oporności: zamiana reszty D-Ala na resztę mleczanową w penapeptydzie |
Nietypowe antybiotyki: DHA (dehydroalanina) i DHB (dehydrobutyryna) |
|
|
|
Cel: degradacja błony cytoplazmatycznej |
|
|
|
Biosynteza: odcięcie końca N po przejsciu przez błonę → modyfikacje → aktywna cząsteczka antybiotyku |
|
Wyszukiwarka
Podobne podstrony:
antybiotyki B laktamowe
antybiotyki b laktamy id 623641 Nieznany (2)
MECHANIZMY OPORNOŚCI NA ANTYBIOTYKI β LAKTAMOWE
W10 SZ W10 Chemioterapia zakażeń?kteryjnych, sulfonamidy, antybiotyki ß laktamowe (Daro)
13. oznaczanie wrażliwości na antybiotyki beta laktamowe, Biologia UMCS, IIº, I semestr, Mikrobiolog
ANTYBIOTYKI BETA LAKTAMOWE
Antybiotyki beta laktamowe, penicyliny ppt
W 42 Antybiotyki beta laktamowe oraz inne inhibitory
Antybiotyki Beta laktamowe
więcej podobnych podstron