606616430
(1930) 23
PRZEMYSŁ CHEMICZNY
185
zenie przy określonym naprężeniu rozciągającym27). Współczynnik temperaturowy wulkanizacji waha się w granicach: 1,9—2,8, a zatem odpowiada wartości ustalonej przez V a n't H o f f a dla reakcyj chemicznych przebiegających w temperaturach niezbyt wysokich. Podane powyżej wyniki studiów warunków kinetycznych reakcji wulkanizacji nie mogą służyć za podstawę do określenia zachodzących przemian; wydaje się jednak jasnym, iż wulkanizacja jest wynikiem kilku jednocześnie przebiegających reakcyj, których kierunek zależy między innymi od składu mieszaniny wulkanizowanej. Również wyniki badań termochemicz-nych, ze względu na wielorakość przemian mających miejsce w czasie wulkanizacji nie wyświetlają należycie tego procesu. Zastosowanie prawa Hessa i pierwszej zasady termodynamiki przy studiach teoretycznych sumarycznych efektów cieplnych, lub też wyników otrzymanych drogą pośrednią (przez spalanie mieszanin kauczuku surowego z siarką i odpowiednich mieszanek zwulkanizowanych) natrafią na znaczne trudności, chociażby ze względu na ilość składników układów rozpatrywanych. Dodać należy, że wulkanizacja kauczuku związana jest naogól z dodatnim sumarycznym efektem cieplnym; w mieszaninach o niewielkim początkowym stężeniu siarki ilość ciepła wyzwalanego jest nieznaczna28). Według wyników pewnych prac Blake’a29) sumaryczny efekt cieplny przy tworzeniu się miękkiej gumy zwulkanizowanej ma być nawet równy zeru. Wyniki te jednak nie zostały potwierdzone przez dalsze badania prowadzone przez tegoż autora30) i być może oparte zostały na mylnej interpretacji danych liczbowych, jak to wskazali Lewis i współpracownicy31). Tworzenie się ebonitu związane jest ze znacznym dodatnim efektem cieplnym.
Gdy wziąść pod uwagę podstawowy element budowy cząstki węglowodoru kauczukowego:
— CHS — CH = C — CHi —
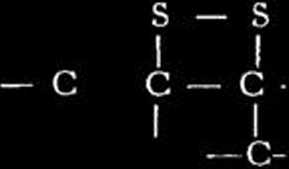
(tworzenie dwusiarczków)
4
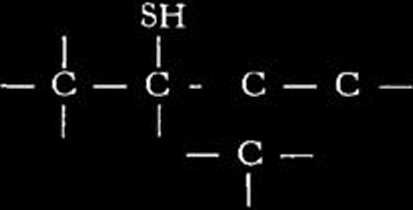
(tworzenie reszt merkapto—)
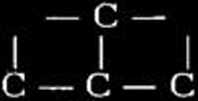
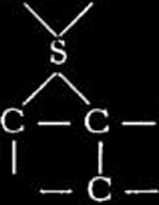
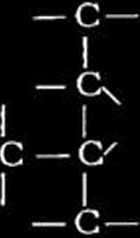
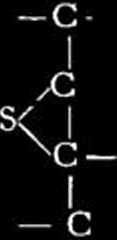
Jeśli chodzi o możliwości reakcyj w które wchodzi więce niż jedna cząstka węglowodoru, to odpowiadają im między innymi schematy następujące:
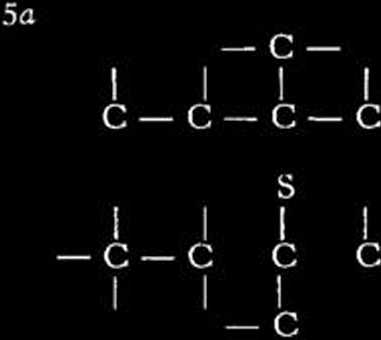
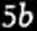

C
5 c
CH,
I
C
i rozważyć jakie są możliwości reakcji z siarką, to dojść można między innymi do schematów następujących:
\a — S--, ,-S---- --S
lilii
— G — C — C — C — C — C — C —
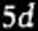
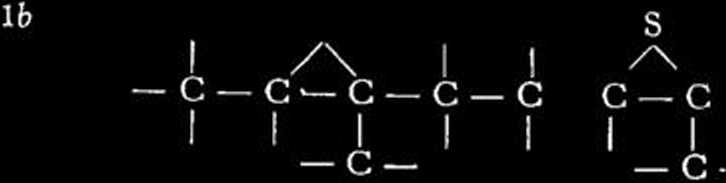
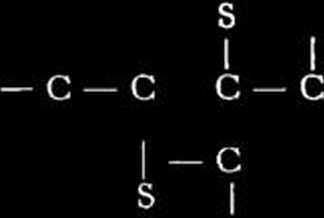
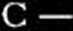
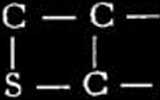
(wytwarzanie wewnątrzcząsteczkowych „mostków” siarkowych);
2a S 2 b S — S

(tworzenie tioozonidów lub izotioozonidów)
|
1 | |
|
1 1 |
s |
r?) L i i c I, Trans. Inst. Rubber Ind. 12, 161 (1936). *8) E e r k s. J. Soc. Chem. Ind. 45, 142T (1926); r o y a b e. Rubber Chem. Tech. 3, 384 (1930)
,#) Ind, Eng. Chem. 22, 741 (1930)
") Ind. Eng. Chem. 26, 1283 (1934)
ll)
(tworzenie między cząsteczkowych „mostków” siarkowych i kondensacja)
Wyszukiwarka
Podobne podstrony:
(1939) 23 PRZEMYSŁ CHEMICZNY179 runkach laboratoryjnych, zwłaszcza przy koksowaniu w ty-gielku, gdy
(1939) 23 PRZEMYŚL CHEMICZNY183 czukowy, przy czym przebiegające reakcje wydają się być nieodwracaln
(1939) 23 PRZEMYŚL CHEMICZNY175Lepkość ciał wysokocząsteczkowych, szczególnie celulozy1* Sur la
(1939) 23 PRZEMYŚL CHEMICZNY181 zaobserwowano, że krzywe te (rycina 2) są tym bardziej wypukłe, im b
(1939) 23 PRZEMYSŁ CHEMICZNY189 w czasie wulkanizacji. Reakcje te jednak uważane są za zjawiska
(1U39) 23 PRZEMYŚL CHEMICZNY191 z odszczepieniem reszt aryloaminowych i podstawieniem ich grupami
U939) 23 PRZEMYSŁ CHEMICZNY193 Pan Prezydent wyraził swą zgodę na objęcie Wysokiego Protektoratu nad
rI930) 23 PRZEMYSŁ CHEMICZNY195 Na Kongresie obecni będą najwybitniejsi przedstawiciele wiedzy
(1939) 23 PRZEMYŚL CHEMICZNY 163 cylinder wysokości 70 mm o średnicy wewnętrznej 80 mm i zewnętrznej
(1039) 23 PRZEMYSŁ CHEMICZNY165 szybkiego wzrostu w tym czasie temperatury retortki (krzywa na rycin
(1939) 23 PRZEMYŚL CHEMICZNY 107 Zcl ujaitobt Aa 0 005% ZcLLuo-i-tobc Aa 0,0 03 % P-łW^pitsiac/L $0
176 PRZEMYSŁ CHEMICZNY 23 (1939; przy porównaniu z równaniem Staudingerał,l: wynika, że VQ jest
180 PRZEMYŚL CHEMICZNY 23 (1930) istnieje między kontrakcją a stopniem spękania koksu. Im większa je
181 PRZEMYSŁ CHEMICZNY 23 (1939) jest do reakcyj chemicznych opartych na zmianie stopnia nienasyceni
192 PRZEMYSŁ CHEMICZNY 23 (1939) ków studiujących chemię wynosiła 19, w roku następnym 30, a w r. 18
196 PRZEMYŚL CHEMICZNY 23 (1939) które mają postać naczyń włoskowatych; z miejsc tych są nie do
16*2 PRZEMYŚL CHEMICZNY 23 (1939) TABLICA 1. Procentowa zawartość koksu surowego L. p. Węgiel
164 23 (1939) PRZEMYSŁ CHEMICZNY Rycina 4. na skutek rozkładowych procesów pirogcne-tycznycli z
166 PRZEMYSŁ CHEMICZNY 23 (1939)Wpływ manganu zawartego w kredzie na processtarzenia się
więcej podobnych podstron