Biotechnologia ścieków
Hydroliza związków wielkocząsteczkowych

Hydroliza związków wielkocząsteczkowych
Sposób zaliczenia:
Ocena końcowa = 2/3 oceny z egzaminu + 1/3 oceny z
laboratorium
Pozytywną ocenę z egzaminu wolno poprawiać jeden raz.
Ocena niedostateczna z egzaminu jest brana pod uwagę
przy liczeniu oceny końcowej z wyjątkiem oceny
niedostatecznej uzyskanej z egzaminu zerowego.

Hydroliza związków wielkocząsteczkowych
Literatura do wykorzystania:
1.
Janusz Łomotowski, Adam Szpindor: Nowoczesne systemy
oczyszczania ścieków, Arkady, Warszawa, 1999.
2.
Mogens Henze, Poul Harremoës, Jes la Cour Jansen, Eric
Arvin: Oczyszczanie ścieków procesy biologiczne i chemiczne,
Wydawnictwo Politechniki Świętokrzyskiej, Kielce 2000.
3.
Metcalf & Eddy: Wastewater Engineering treatment, disposal,
and reuse, McGraw – Hill, third edition 1991 i późniejsze
wydania
4.
Mieczysław K. Błaszczyk: Mikroorganizmy w ochronie
środowiska, PWN, Warszawa, 2007.
Inne podręczniki oraz publikacje naukowe

Hydroliza związków wielkocząsteczkowych
Zakres wykładów:
Hydroliza związków wielkocząsteczkowych,
Beztlenowe oczyszczanie ścieków
Nitryfikacja, denitryfikacja, beztlenowa deamonifikacja
(Anammox)
Biologiczna defosfatacja,
Przemiany związków siarki w oczyszczaniu ścieków
Unieszkodliwianie osadów ściekowych

Hydroliza związków wielkocząsteczkowych
Zakres laboratorium:
(4 godziny tygodniowo)
1.
Zajęcia organizacyjne (podział na sekcje, BHP)
2.
Charakterystyka ścieków I
3.
Charakterystyka ścieków II
4.
Oczyszczanie ścieków w złożu wieżowym
5.
Oczyszczanie ścieków w złożu tarczowym
6.
Oczyszczanie ścieków w reaktorze pełnego wymieszania

7. Właściwości sedymentacyjne osadu czynnego
8. Oczyszczanie ścieków w reaktorach membranowych
9. Reaktor SBR I; usuwanie związków organicznych
10. Reaktor SBR II; usuwanie zawiązków azotu (nitryfikacja)
11. Reaktor SBR III; usuwanie związków fosforu i azotu
(denitryfikacja)
12. Zajęcia przeznaczone na odrabianie zajęć laboratoryjnych
13. Kolokwium zaliczeniowe
14. Zaliczenie
Hydroliza związków wielkocząsteczkowych
A
B
C
E
D
G
F
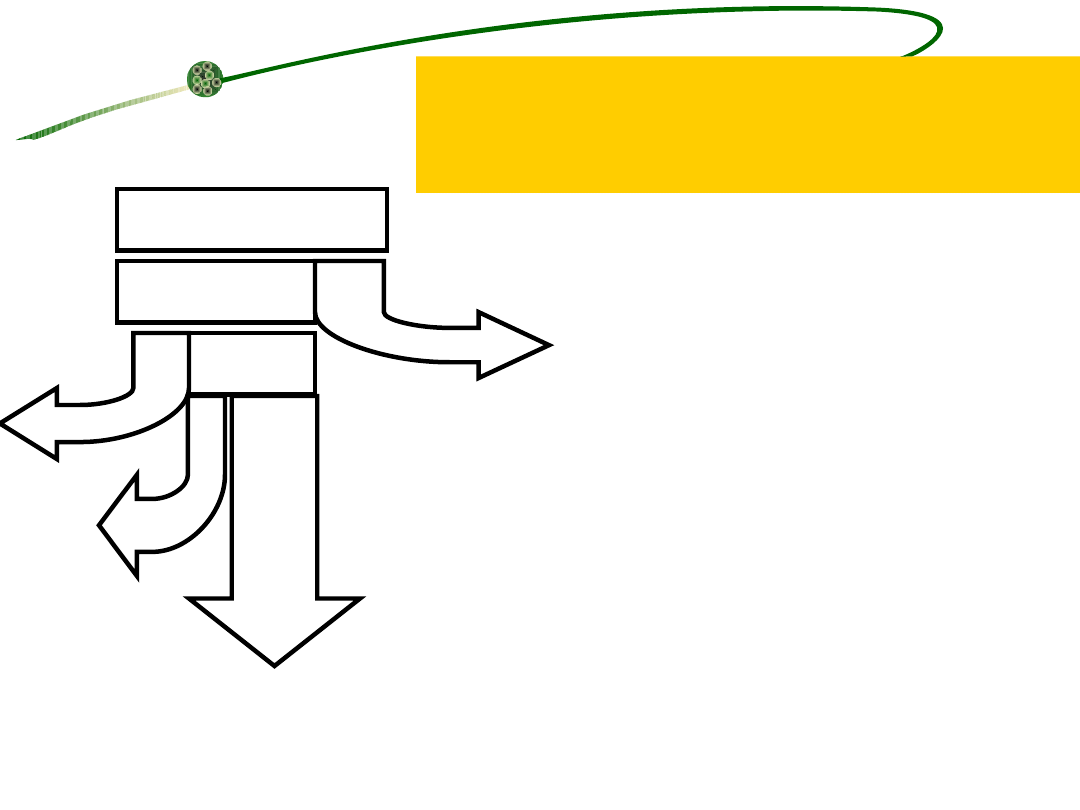
A – zanieczyszczenia doprowadzane,
B –zanieczyszczenia zatrzymane na
powierzchni mikroorganizmów,
C – zanieczyszczenia odprowadzane z
oczyszczonymi ściekami,
D – zanieczyszczenia utlenione do CO
2
,
H
2
O i innych produktów końcowych,
E – zanieczyszczenia asymilowane w
postaci przyrostu biomasy,
F – autooksydacja mikroorganizmów do
CO
2
, H
2
O i innych produktów
końcowych,
G – nadmiar mikroorganizmów

Hydroliza związków wielkocząsteczkowych
W ściekach większość związków organicznych
występuje w formie koloidalnej i zawiesiny. W surowych
ściekach bytowo-gospodarczych stanowią one aż 60 –
70% ładunku zanieczyszczeń organicznych. Po
osadniku wstępnym stanowią 40 – 50% związków
organicznych.
Stałe cząsteczki organiczne są szybko sorbowane
przez kłaczki osadu czynnego, ale ich rozkład jest
wolny. Umożliwia go hydroliza, która czyni je
dostępnymi dla mikroorganizmów.

Hydroliza związków wielkocząsteczkowych
Hydroliza jest jednym z najwolniejszych
procesów w oczyszczaniu ścieków.
Hydrolazy są enzymami katalizującymi proces
hydrolizy. Przecinają wiązania wstawiając
cząsteczki wody.
Hydroliza związków wielkocząsteczkowych
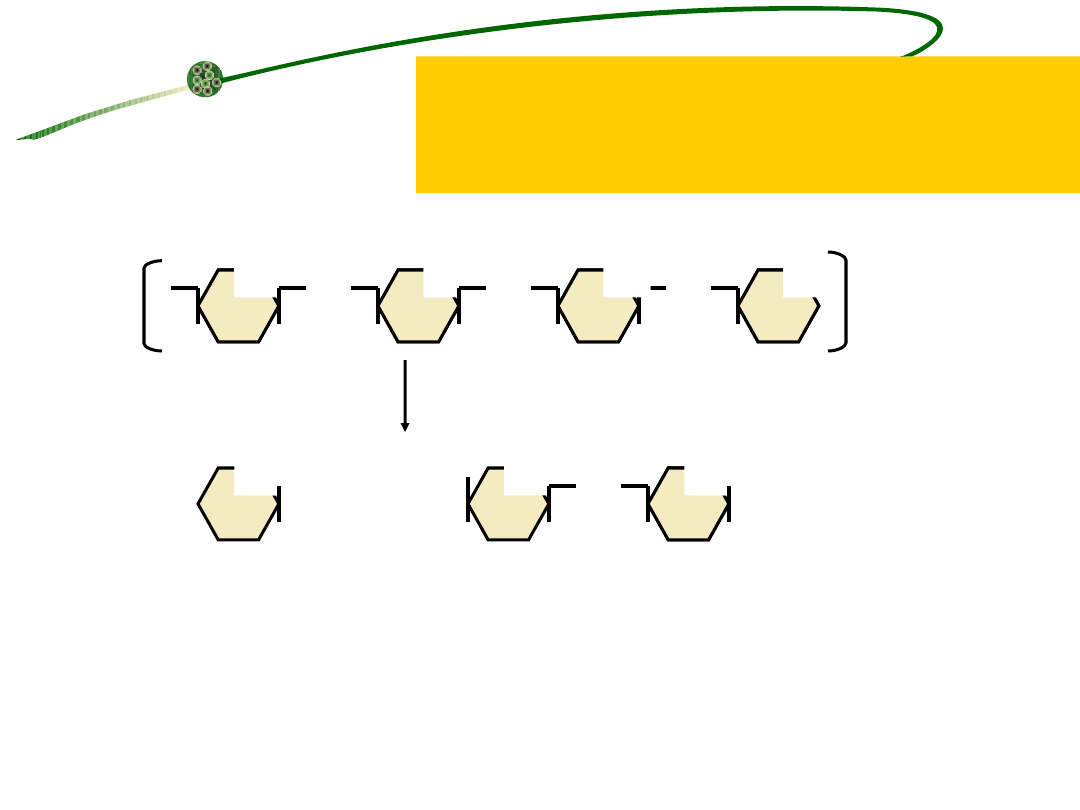
enzym rozkładający wielocukry
O
O
O
n
O
O OH
O
O
O
O
O
O OH
O
O
Duże cząsteczki wielocukrów są rozkładane do pojedynczych
cukrów lub do mniejszych cząsteczek.
Hydroliza związków wielkocząsteczkowych
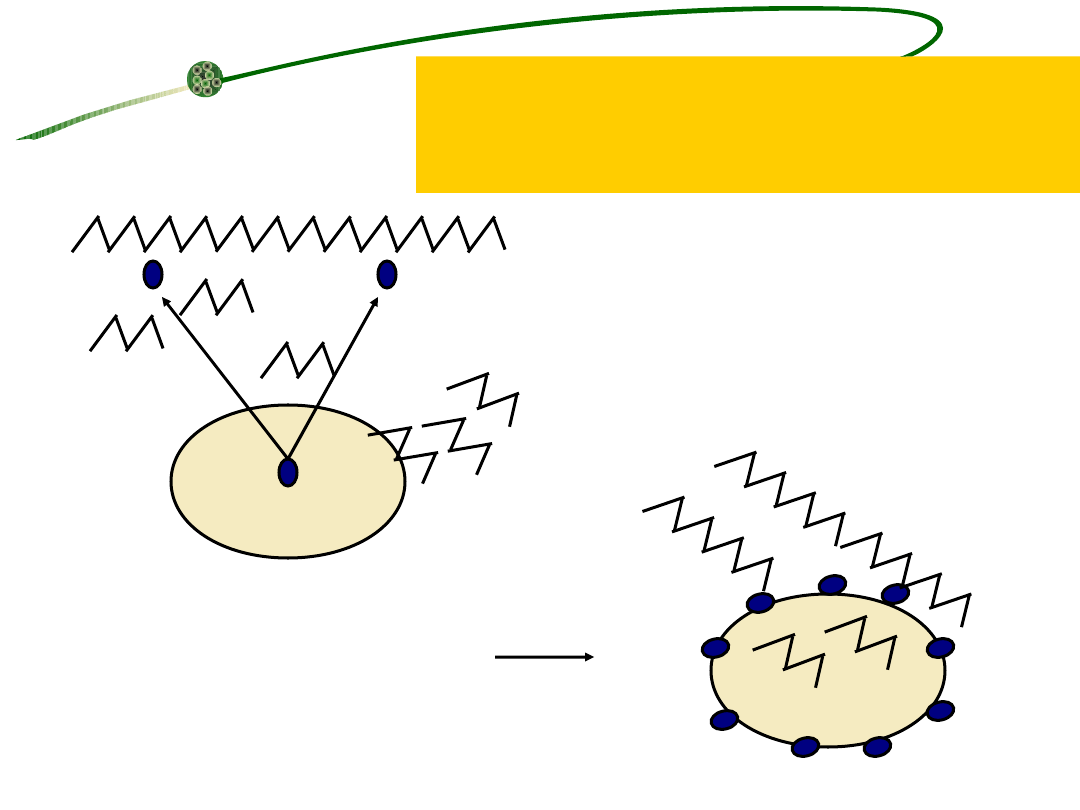
enzymy zewnątrzkomórkowe
enzymy związane z
powierzchnią komórki
Gdy konkurenci mogą przejąć
produkty hydrolizy

Hydroliza związków wielkocząsteczkowych
Hydrolazy to np.: lipazy, fosfatazy, proteazy,
celulazy.
Najszybciej hydrolizowane są białka, potem
tłuszcze, a następnie węglowodany.
Skład cząstek zawiesiny oraz rozmiar cząstek
mają wpływ na szybkość hydrolizy. Małe
cząsteczki są hydrolizowane szybciej niż duże.
Szybkość hydrolizy zależy też od akceptora
elektronów oraz od sił ścinających.

Hydroliza związków wielkocząsteczkowych
Nie ma jednego, uniwersalnego sposobu
ilościowego opisu szybkości hydrolizy. Do opisu
hydrolizy wykorzystywane są:
kinetyka reakcji pierwszego rzędu,
kinetyka reakcji zależna od powierzchni,
kinetyka reakcji drugiego rzędu.

Hydroliza związków wielkocząsteczkowych
Kinetyka pierwszego rzędu przy stałym pH i stałej
temperaturze:
dF/dt = -K
H
F
F – stężenie substratu (stałych cząsteczek organicznych),
kg/m
3
;
t – czas, dni;
K
H
– stała szybkości hydrolizy, 1/dzień.
Różne wartości K
H
z powodu zmiennego rozkładu rozmiaru
cząstek.

Hydroliza związków wielkocząsteczkowych
Ponieważ kinetyka hydrolizy opisana równaniem
reakcji pierwszego rzędu nie bierze pod uwagę
powierzchni substratu, wielkość stałej hydrolizy
nie może być ekstrapolowana na inne podobne
substraty jeśli rozkład wielkości cząsteczek jest
nieporównywalny. Wtedy przy wykorzystywaniu
modelu reakcji pierwszego rzędu stała hydrolizy
musi być wyznaczana eksperymentalnie dla
każdego substratu.

Hydroliza związków wielkocząsteczkowych
Kinetyka reakcji limitowanej powierzchnią
Cząsteczki substratu są całkowicie pokryte
bakteriami, które wydzielają enzymy. Ponieważ
enzymy są obecne w nadmiarze, szybkość
hydrolizy jest stała w przeliczeniu na jednostkę
powierzchni dostępną dla hydrolizy.
Stała hydrolizy jest niezależna od rozmiaru
cząsteczki substratu.

Hydroliza związków wielkocząsteczkowych
dM/dt = - K
sbk
A
M – masa substratu, kg;
t – czas, dni;
K
sbk
– stała hydrolizy (zależnej od powierzchni),
kg/m
2
dzień;
A – powierzchnia dostępna dla hydrolizy, m
2
.

Hydroliza związków wielkocząsteczkowych
Bardzo często zakłada się, że cząsteczki mają
kształt kulisty i są rozkładane od zewnątrz.
Wtedy masa całkowita przyjmuje wartość:
4πR
3
nρ/3 gdzie n – liczba cząsteczek,
ρ – gęstość cząsteczek,
a całkowita powierzchnia 4πnR
2
.

Hydroliza związków wielkocząsteczkowych
Po podstawieniu do równania dM/dt = - K
sbk
A
Zmniejszenie średniego promienia w czasie można
opisać następująco:
R
t
= R
0
– K
sbk
t/ρ,
R
t
– średni promień cząsteczki po czasie t, m;
R
0
- średni promień cząsteczki w czasie t = 0, m.
Model ten pozwala ocenić zmiany w rozkładzie
wielkości cząstek w trakcie hydrolizy.

Hydroliza związków wielkocząsteczkowych
Założenie dodatkowe, to, że liczba cząsteczek się nie
zmienia i są one całkowicie biodegradowalne.
Jeżeli cząsteczki w trakcie hydrolizy rozpadają się na
mniejsze, to teoretycznie wzrasta powierzchnia i rośnie
szybkość hydrolizy.
Praktyka wykazuje jednak, że szybkość hydrolizy maleje
wraz z wydłużaniem czasu hydrolizy i rozpad
cząsteczek nie generuje wzrostu powierzchni dostępnej
dla hydrolizy ponieważ mniejsze cząsteczki składają się
z substancji słabiej biodegradowalnej.
Hydroliza związków wielkocząsteczkowych
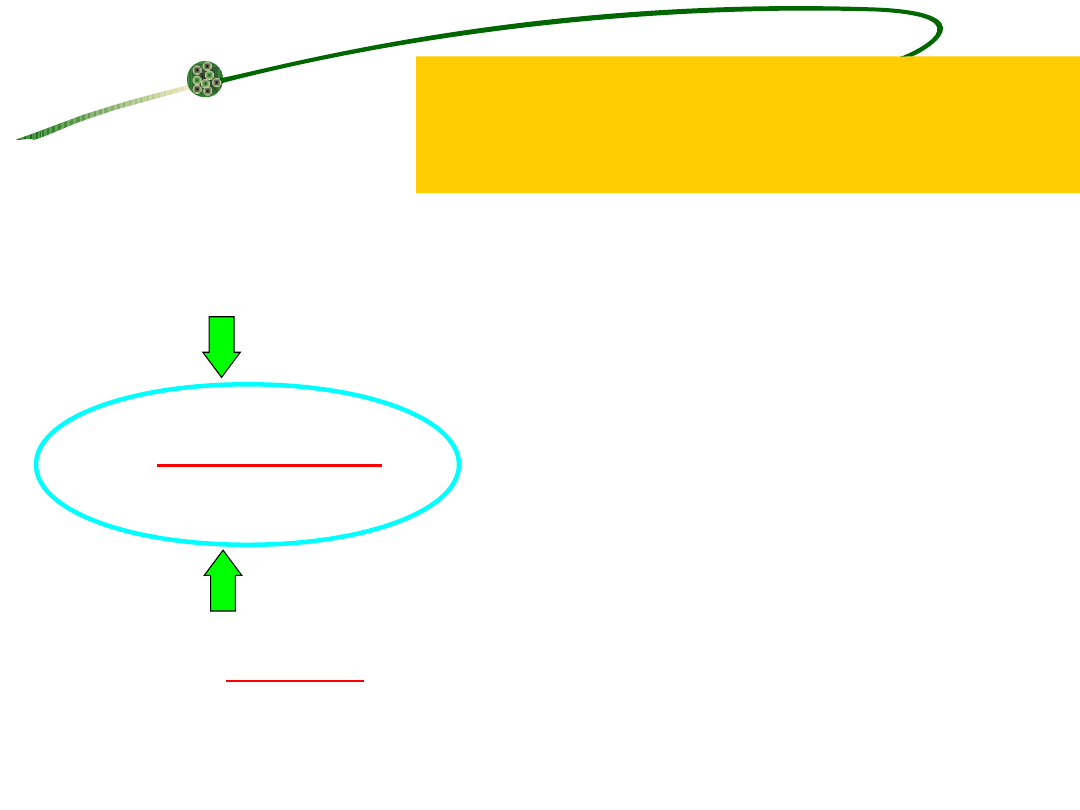
Wzrost mikroorganizmów osadu czynnego limitowany substratem
r = µ · X
µ = µ
m
S
K
s
+ S
r =
µ
m
· S · X
K
s
+ S
r – szybkość wzrostu
mikroorganizmów, g sm/ l·s,
µ - specyficzna szybkość wzrostu,
d
-1
,
X- zawartość biomasy, g sm/l,
µ
m
– maksymalna specyficzna
szybkość wzrostu, d
-1
,
K
s
– stała saturacji dla danego
substratu, mg/l,
S – stężenie substratu
limitującego wzrost
mikroorganizmów, mg/l,

Hydroliza związków wielkocząsteczkowych
r = -Y · r
s
Y – współczynnik przyrostu
biomasy,
g sm/ g BZT
5,
r
s
– szybkość zużycia
substratu, mg/l·s,
r – szybkość wzrostu
mikroorganizmów,
g sm/ l·s,
r
s
= -
r
Y
= -
µ
m
· S · X
Y · (K
s
+ S)
Hydroliza związków wielkocząsteczkowych
W osadzie czynnym można zastosować wzór zaproponowany przez
Stenstroma, odnoszący się do szybkości przyrostu aktywnej
biomasy na zawiesinie organicznej :
r
s
fs
r
s
m
a
a
x
x
K
x
x
dt
dx
x
/
/
1
+
= µ
X
a
– zawartość aktywnej
biomasy, mg smo/l,
X
s
– „stężenie” pobranego
substratu, mg smo/l,
X
r
– zawartość zawiesiny
organicznej, mg smo/l,
µ
m
- maksymalna specyficzna
szybkość wzrostu, d
-1
,
K
fs
- stała saturacji dla
danego substratu,
X
r
= X
p
+ X
b
X
p
– zawiesina organiczna, mg smo/l,
X
b
– biomasa w reaktorze, mg smo/l
Hydroliza związków wielkocząsteczkowych
Modyfikacja równania uwzględniająca kinetykę hydrolizy
limitowanej powierzchnią:
n
a
s
fs
n
a
s
m
a
a
X
X
K
X
X
dt
dX
X
/
/
1
+
=
µ
n – współczynnik,
zależny od stosunku
objętości komórki do
jej powierzchni
Założenia:
n = 1,
X
s
= X
pd
„stężenie” zawiesiny organicznej
ulegającej biodegradacji, mg smo/l
Hydroliza związków wielkocząsteczkowych
Równanie można przekształcić zgodnie
z zależnością:
r = -Y · r
s
a
pd
fs
pd
m
pd
X
X
K
X
Y
dt
dX
/
1
+
=
µ
Y - współczynnik
przyrostu biomasy,
g sm/ g BZT
5
Z równania tego można wyprowadzić wzór dla kinetyki
pierwszego rzędu. Jeśli X
pd
/X
a
« K
fs
, to wyrażenie to
można pominąć i wzór przybierze postać:
Hydroliza związków wielkocząsteczkowych
fs
pd
m
pd
K
X
Y
dt
dX
µ
1
=
Wielkość stała – stała
szybkości hydrolizy –
K
p
’
, 1/dzień
pd
p
pd
X
K
dt
dX
'
−
=
Równanie przybiera postać:
K
p
’
– zależy od
zawartości biomasy

Hydroliza związków wielkocząsteczkowych
Zaproponowano wprowadzenie specyficznej stałej
szybkości hydrolizy K
p
= K
p
’
/X
a
, 1/mg dzień.
Równanie przybiera wówczas postać:
a
pd
p
pd
X
X
K
dt
dX
−
=

Hydroliza związków wielkocząsteczkowych
Degradowalna część zawiesiny X
pd
w reaktorze o przepływie ciągłym
t
X
f
X
X
p
nd
p
pd
θ
0
−
=
f
nd
– nie ulegająca biodegradacji frakcja zawiesiny w dopływie,
θ – wiek osadu, dni,
X
p
0
– zawartość zawiesiny organicznej w dopływie, mg smo/l

Hydroliza związków wielkocząsteczkowych
Aktywna biomasa w reaktorze o przepływie ciągłym
θ
b
X
X
b
a
2
,
0
1
8
,
0
+
=
X
b
– zawartość biomasy w reaktorze, mg smo/l,
b – współczynnik rozkładu biomasy na skutek
endogennej respiracji (autooksydacji), 1/dzień

Hydroliza związków wielkocząsteczkowych
Aktywna biomasa w reaktorze okresowym
(wprowadzona do reaktora okresowego z reaktora o
przepływie ciągłym)
)
(
2
,
0
1
8
,
0
0
t
b
X
X
b
a
+
+
=
θ
X
b
– zawartość biomasy w reaktorze, mg smo/l,
b – współczynnik rozkładu biomasy na skutek
endogennej respiracji (autooksydacji), 1/dzień,
θ
0
– wiek osadu, przy którym biomasa powstała w
reaktorze o przepływie ciągłym, dni

Hydroliza związków wielkocząsteczkowych
Szybkość rozkładu biomasy
a
b
bX
dt
dX
−
=
)
(
2
,
0
1
8
,
0
0
t
b
X
b
dt
b
dX
b
+
+
−
=
θ
stąd
Równanie to pozwala wyznaczyć wartość
współczynnika b
Document Outline
- Slajd 1
- Slajd 2
- Slajd 3
- Slajd 4
- Slajd 5
- Slajd 6
- Slajd 7
- Slajd 8
- Slajd 9
- Slajd 10
- Slajd 11
- Slajd 12
- Slajd 13
- Slajd 14
- Slajd 15
- Slajd 16
- Slajd 17
- Slajd 18
- Slajd 19
- Slajd 20
- Slajd 21
- Slajd 22
- Slajd 23
- Slajd 24
- Slajd 25
- Slajd 26
- Slajd 27
- Slajd 28
- Slajd 29
- Slajd 30
- Slajd 31
Wyszukiwarka
Podobne podstrony:
Hydroliza zwiazkow wielkoczasteczkowych 1
Hydroliza zwiazkow wielkoczasteczkowych 1
Wyznaczanie masy cząsteczkowej związków wielkocząsteczkowych, Studia, Politechnika
IDENTYFIKACJA ZWIĄZKÓW WIELKOCZĄSTECZKOWYCH, Politechnika, Sprawozdania, projekty, wyklady, Techniki
Wyznaczanie masy cząsteczkowej związków wielkocząsteczkowych
Chemia labolatorium, Hydroliza2, Hydroliza - reakcja niektórych zwiazków chemicznych z wodą, która p
Związki wodowskazów rzeki Narwi - praca 4, hydrologia
Charakterystyka technologiczna produkcji wielkotonażowych związków organicznych w UE
Poliuretany są wielkocząsteczkowymi związkami
identyfikacja wielkopierścienowych związków za pomocą chrmoatrogafi
4 Linie wpływu wielkości statycznych w ustrojach prętowych
wyklad 13nowy Wyznaczanie wielkości fizykochemicznych z pomiarów SEM
izomeria zwiazkow organicznych
Ostre Zatrucie Związkami Rtęci
3 ch org zwiazki funkcyjne
7 władza w bliskim związku
zwiazki kompleksowe 2
więcej podobnych podstron