Przykładowe pytani egzaminacyjne:
1. Wykorzystując odpowiednie związki Grignarda zaproponuj metody syntezy następujących alkoholi:
a) 1-fenylo-1-propanol, b) 2-fenylo-2-propanol, c) 1-fenylo-2-propanol, d) 3-fenylo-1-propanol,
e) trifenylometanol.
2.Napisz równania reakcji cykloheksanolu z następującymi reagentami:
a) stęż. H2SO4, ogrzewanie, b) CrO3 / H2SO4, d) HBr, e) Na, f) CH3COOH / H![]()
.
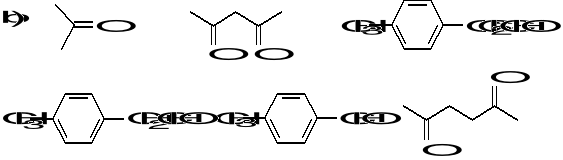
3.Które z poniższych związków mogą tworzyć formę enolową? Przedstaw jej wzór.
a) benzofenon, cykloheksanon, 2,2,4,4-tetrametylo-3-pentanon, aldehyd
benzoesowy
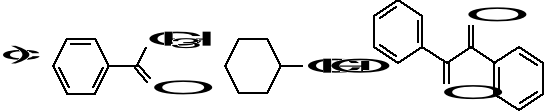
4.Które z poniższych związków (podać ich nazwy systematyczne) ulegają reakcji aldolowej?
5. Jakie czynniki wpływają na właściwości kwasowe kwasów karboksylowych? Uporządkuj poniższe triady według wzrastającej kwasowości. Odpowiedź uzasadnij.
a) octowy, trichlorooctowy, chlorooctowy,
b) 2-bromopropanowy, propanowy, 3-bromopropanowy,
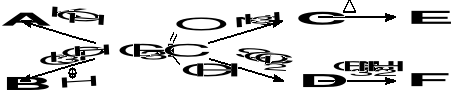
6. Napisz wzory związków A-F:
7. Z trzech zamieszczonych pod równaniem reagentów wybierz reagent najkorzystniejszy do przeprowadzenia każdej z podanych reakcji:
a) CH3-CH3 ![]()
CH3-CH2Cl
1) HCl / ZnCl2 / ; 2) PCl3 ; 3) Cl2 / h
b) (CH3)2CH-CH2OH ![]()
(CH3)2CH-CH2Br
1) Br2 ,CCl4 ; 2) Br2 / h ; 3) HBr
Używając odpowiedniego skrótu literowego określ mechanizm tych reakcji.
8.Napisz wzory głównych produktów i nazwij mechanizmy reakcji:
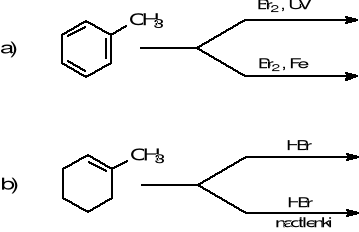
W punkcie b) określ, która z reakcji przebiega zgodnie z regułą Markownikowa
9B. Trimirystyna to stały tłuszcz - główny składnik lipidowy gałki muszkatołowej. W wyniku hydrolizy trimirystyna daje glicerol i kwas tetradekanowy (mirystynowy) w stosunku molowym 1 : 3. Przedstaw wzorem strukturę trimirystyny
10B.Napisz równanie reakcji katalitycznego uwodornienia (H2 / Ni) trioleinianu glicerolu (trioleiny). Nazwij produkt i wyjaśnij, czy będzie miał on wyższą, czy też niższą temperaturę topnienia od substratu.
11B. Triacyloglicerydy, jeśli zawierają dwa lub trzy różne kwasy tłuszczowe mogą wykazywać czynność optyczną.
a) Przedstaw strukturę optycznie czynnego triacyloglicerydu zawierającego 1 mol kwasu mirystynowego i 2 mole kwasu oleinowego.
b) Przedstaw strukturę optycznie nieczynnego triacyloglicerydu o składzie identycznym jak w punkcie (a).
12B.Co oznacza skrót NNKT oraz skróty anglojęzyczne: EFA, PUFA, CLA. Podaj przykłady związków przypisywanych każdej z tych grup.
13.Izopren to niewystępujący w stanie wolnym w naturze formalny monomer terpenów. Przedstaw jego wzór i podaj systematyczną nazwę.
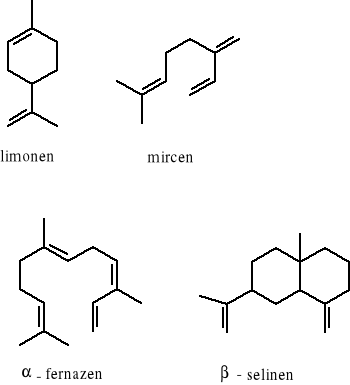
14.W poniższych związkach (należą one do izoprenoidów) zaznacz wszystkie jednostki izoprenowe
15B. Przedstaw projekcję Fischera aldehydu D-glicerynowego. Określ jego konfigurację absolutną (zaznacz kolejność podstawników).
16B. Narysuj projekcje Fischera enancjomerów D-glukozy i D-fruktozy. Do jakiego szeregu konfiguracyjnego należą te enancjomery ?
17B. Ile centrów chiralności posiada: a) aldotetroza, b) ketotetroza? Ile jest możliwych stereoizomerycznych aldotetroz, ile ketotetroz? Przedstaw ich projekcje Fischera.
18B. Oto wzór D-erytrozy. Określ konfigurację centrów chiralności, narysuj jej enancjomer i diastereoizomer. Czy D-erytritol (alditol) otrzymany w wyniku redukcji grupy karbonylowej erytrozy jest optycznie czynny?
19B. Narysuj wzory Fischera wszystkich stereoizomerycznych D-aldopentoz. Przedstaw też wzory produktów ich utleniania rozc. HNO3. Które z otrzymanych kwasów aldarowych będą optycznie nieczynne?
20B.Galaktozę różni od glukozy konfiguracja na czwartym atomie węgla. Narysuj wzór: a) D-galaktozy, b) L-galaktozy, c) -L-galaktopiranozy, d) -D-galaktofuranozy.
21B.Niżej podany jest wzór -D-allopiranozy. Narysuj: a) -L-allopiranozę, b) D-allozę w projekcji Fischera, c) metylo- -D-allopiranozyd.
22B.Konkretnymi przykładami zilustruj: a) anomery, b) epimery, c) -glikozyd, d) L-aldopentoza, f) próba Tollensa, h) dezoksysacharyd
23.W reakcji 100 g acetonu i 200 g alkoholu metylowego powstało 100 g 2,2-di-metoksypropanu. Oblicz wydajność tej reakcji.
Masy molowe:.aceton 58 g/mol, metanol 32 g/mol, produkt 104 g/mol.
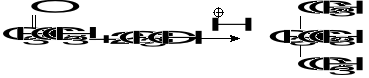
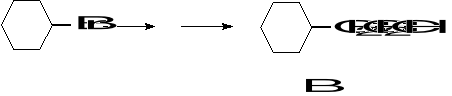
24.Wiedząc ,że wydajność poniższej syntezy wynosi 55% , oblicz , z jakiej ilości bromocykloheksanu należy wyjść, aby otrzymać 100 g alkoholu B.
25.Oblicz, ile benzenu trzeba użyć do dwuetapowej syntezy prowadzącej przez toluen do kwasu benzoesowego, w celu otrzymania 200 kg kwasu benzoesowego. Wydajność pierwszego etapu wynosi 70% a drugiego 90%.
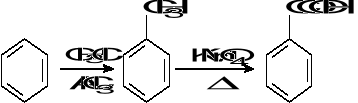
26.Oblicz ile meta-nitrobenzoesanu metylu otrzymano w reakcji syntezy tego związku, jeżeli do reakcji użyto 6,3 cm3 benzoesanu metylu o gęstości 1,08 g/cm3, a reakcja przebiegła z 75% wydajnością. Odczynniki nieorganiczne zastosowano w nadmiarze.
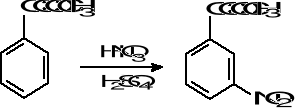
27.W wyniku reakcji 100 g kwasu benzoesowego C6H5COOH i 200 cm3 etanolu C2H5OH o gęstości 0,78 g/cm3 otrzymano 110 cm3 benzoesanu etylu C6H5COOC2H5 (d = 0,87 g/cm3). Napisz równanie zachodzącej reakcji i oblicz jej wydajność.
28.Propen (22,4 dm3) przepuszczono przez 200 cm3 1 molowego roztworu bromu w rozpuszczalniku organicznym (np. CCl4). Otrzymano 15 g produktu. Oblicz wydajność tej reakcji.
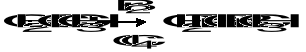
29.Skręcalność właściwa (S) (+)-2 butanolu jest równa [α]D = + 13,50. Oblicz wartość odczytanej na polarymetrze skręcalności tego związku, wiedzą, że gęstość 2-butanolu wynosi 0,808 g/cm3, a pomiaru dokonano w rurce polarymetrycznej od długości 2 dm. Jaką skręcalność wykaże enancjomer tego związku przy pomiarze dokonanym w rurce o długości 10 cm?
30.Oblicz jaką skręcalność zaobserwujesz na polarymetrze skoro naważkę 0,1 mola D-glukozy (masa molowa 180 g/mol; [α]D = +52,5o ) rozpuszczono w H2O w kolbce miarowej o pojemności 100 cm3 a pomiaru dokonano w rurce o długości 20 cm.
31.Oblicz skręcalność właściwą roztworu cukru C6H12O6, którego 1 molowy roztwór wykazuje skręcalność α = + 9,45 0, przy pomiarze prowadzonym z zastosowaniem rurki polarymetrycznej o długości 10 cm.
38.Oblicz ile gramów D-mannozy (równowagowa skręcalność właściwa [α]D = + 14,2o) rozpuszczono w kolbie miarowej o pojemności 0,25 dm3, jeśli zmierzona skręcalność wynosiła dokładnie α = +1,00o. Użyta rurka polarymetryczna miała długość 2,5 cm.
32.(R )-(-)-karwon olejek eteryczny ekstrahowany z liści mięty, odpowiedzialny za jej zapach ma skręcalność właściwą [α]D = - 61o. Podaj jaką skręcalność wykaże roztwór 2 g karwonu w 10ml alkoholu etylowego i umieszczony w rurce polarymetrycznej o długości 5 cm.
33.(R)-(+)-limonen jest olejkiem eterycznym obecnym w skórkach owoców cytrusowych. Oblicz skręcalność właściwą limonenu, jeżeli wiadomo, że roztwór zawierający 3 g tego związku w 15 ml alkoholu etylowego umieszczony w rurce polarymetrycznej o długości 5 cm wykazywał skręcalność α = + 12,3o.
34.Oblicz, ile moli D-glukozy należy użyć w celu przygotowania 4 dm3 roztworu (masa molowa glukozy180 g/mol, skręcalność właściwa [α]D = + 52,5o), który po umieszczeniu w rurce polarymetrycznej o długości 10 cm wykazał skręcalność α = + 18,90.
35.Oblicz stężenie molowe roztworu cukru C6H12O6, którego roztwór wykazuje skręcalność α = + 18,900, przy pomiarze prowadzonym z zastosowaniem rurki polarymetrycznej o długości 5 cm. Skręcalność właściwa cukru [α]D = + 52,5o
36.Oblicz skręcalność właściwą [α]D pirokalciferolu, skoro roztwór 248 mg tego związku w chloroformie, znajdujący się w kolbie miarowej o pojemności 10cm3, umieszczony w rurce polarymetrycznej o długości 5 cm, wykazuje skręcalność α = + 6,350.
37. Jaki jest najprostszy wzór empiryczny związku C8H16O2? Oblicz jego skład procentowy.
38.Jaki jest najprostszy wzór empiryczny związków o składzie procentowym:
a) 77,38% C, 7,58% H oraz 15,04% N,
b) 45,45%C oraz 6,10%H ?
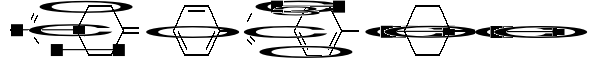
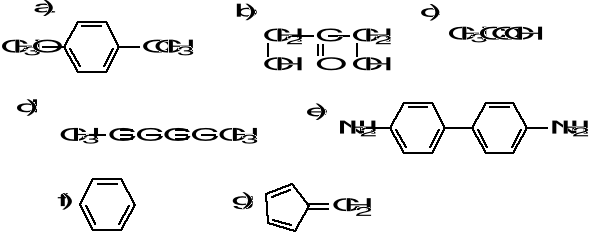
39.Oblicz stopień nienasycenia dla poniższych związków :
40.Węglowodór C9H16 ma dwa stopnie nienasycenia. Podaj przykłady takich izomerów tego węglowodoru, które zawierałyby:
a) dwa nasycone pierścienie, b) jeden nienasycony pierścień, c) jeden nasycony pierścień i jedno podwójne wiązanie, d) dwa podwójne wiązania, e) jedno potrójne wiązanie.
41.Oblicz empiryczny wzór sumaryczny związków o składzie procentowym:
A) 40,0% C, 6,7% H
B) 78,9% C, 10,6% H.
Wiedząc, że masa molowa związku odpowiadającego składowi a) wynosi 90 g/mol, a masa molowa związku o składzie b) 152 g/mol podaj sumaryczne wzory rzeczywiste obu związków oraz zaproponuj po jednym wzorze strukturalnym dla każdego z tych przypadków.
42.Podaj wzór sumaryczny i zaproponuj wzór strukturalny związku zawierającego 64,48% C i 13,61% H. Masa molowa 74 g/mol. Nazwij ten związek. Wskaż grupę funkcyjną.
43.Podaj wzór sumaryczny i zaproponuj wzór strukturalny związku zawierającego 62,04% C i 10,41% H. Masa molowa 58 g/mol. Nazwij ten związek. Wskaż grupę funkcyjną.
43.Podaj wzór sumaryczny i zaproponuj wzór strukturalny związku zawierającego 77,77% C i 7,41%H. Masa molowa 108 g/mol. W strukturze tego związku jest pierścień benzenowy. Czy przedstawiony związek reaguje z 2,4-dinitro-fenylohydrazyną? Nazwij ten związek. Wskaż grupę funkcyjną.
44. Związek o składzie pierwiastkowym C = 69, 72% i H = 11,70% daje pozytywny wynik reakcji z 2,4-dinitrofenylohydrazyną oraz negatywny wynik próby Tollensa. Wzór empiryczny tego związku odpowiada jego wzorowi rzeczywistemu. Podaj wzory strukturalne oraz nazwy systematyczne przynajmniej dwóch związków spełniających podane warunki. (W obliczeniach przyjmij zaokrąglone do jedności masy pierwiastków).
45.Wymień poznane klasy związków organicznych, zilustruj każdą klasę dwoma konkretnymi przykładami podając wzory i nazwy odpowiednich związków.
46.Napisz wzory strukturalne podanych związków, wskaż ich grupy funkcyjne, podaj do jakich klas należą i nazwij je systematycznie oraz zwyczajowo (jeżeli znasz nazwę zwyczajową):
CH3(CH2)2CH3, C2H4, CH3CHO, C3H7COOH, H2NCH2COOH, HCOOC2H5, CH3NH2, CH2=CHCH=CH2, C6H6, CH3CH2CH2OH, C2H5Br, C2H2, CH3CONH2 .Określ hybrydyzację atomów węgla, azotu i tlenu w tych związkach.
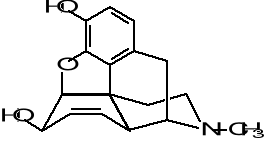
47.W cząsteczce morfiny wskaż znane grupy funkcyjne, typy wiązań oraz elementy struktury:
48.Istnieje wiele izomerycznych związków o sumarycznym wzorze C5H10O. Napisz odpowiadające temu wzorowi sumarycznemu wzory strukturalne następujących związków: a) aldehydu b) ketonu c) nasyconego eteru d) nasyconego alkoholu e) nienasyconego alkoholu.
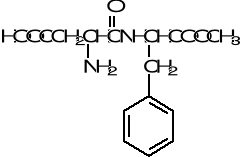
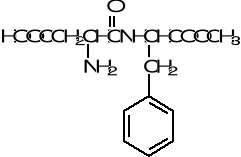
49.W cząsteczce podanego związku wskaż grupy funkcyjne, podaj po jednym przykładzie związku (wzór i nazwa) zawierającego wskazane grupy funkcyjne, określ klasy związków organicznych, do której te związki należą. Wskaż grupy, które mogą ulec: a) hydrolizie zasadowej, b) estryfikacji lub transestryfikacji, c) redukcji d) utlenianiu e) substytucji elektrofilowej aromatycznej.
50B. Odpowiednimi przykładami zilustruj pojęcia: trigliceryd charakterystyczny dla tłuszczów roślinnych, cukier redukujący, monoterpen, D-aminokwas, disacharyd, hemiacetal, peptyd, L-ketopentoza, D-aldoza, kwas aldonowy, kwas aldarowy, wosk, CLA, NIKT, nasycony kwas tłuszczowy, nienasycony kwas tłuszczowy, glukoza, fruktoza, ryboza, Ala-Ala, trieleinian glicerolu, tripalmitynian glicerolu
51B.Wskaż biocząsteczki, w których występuje: wiązanie estrowe, wiązanie amidowe, wiązanie eterowe (hemiacetalowe lub acetalowe). Podaj przykłady konkretnych związków zawierających wymienione wiązania. Tam gdzie potrafisz napisz wzór odpowiedniego związku.
52.Odpowiednimi przykładami zilustruj pojęcia: C-H kwas, kwas karboksylowy, hydroksykwas, kwas aromatyczny, kwas Brønsteda, kwas Lewisa, sprzężony kwas, mocny kwas, słaby kwas, NNKT, CLA.
53.Reakcja 2,3-dimetylo-1-butenu z HBr prowadzi do bromoalkanu C6H13Br. Pod wpływem KOH w metanolu ten bromoalkan tworzy węglowodór, który jest izomeryczny z wyjściowym alkenem. Jaka jest struktura tego węglowodoru i według jakiego mechanizmu tworzy się on z bromoalkanu?
54.Przykładami odpowiednich par związków zilustruj pojęcia: izomery grup funkcyjnych, izomery Z i E, enancjomery, izomery szkieletowe, izomery pozycyjne, izomery cis-trans, konformery, tautomery.
55.Istnieje wiele izomerycznych związków o sumarycznym wzorze C6H12O. Napisz odpowiadające temu wzorowi sumarycznemu wzory strukturalne następujących związków: a) aldehydu b) ketonu c) związku optycznie czynnego d) izomeru E e) izomeru cis.
56.Dwa steroizomeryczne alkeny dają w wyniku ozonolizy i następnie hydrolizy powstałego ozonku w obecności czynnika redukującego (Zn) następujące produkty: 2-metylopropanal i etanal. Podaj wzory i nazwy systematyczne tych alkenów.
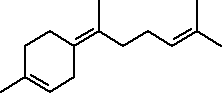
57.γ-Bisabolen należy do seskwiterpenów. Zaznacz na podanym wzorze jednostki izoprenowe (odseparuj je wyraźnie). Jaki związek jest formalnym monomerem terpenów - narysuj jego wzór i podaj nazwę systematyczną.
58.Terpeny dają się formalnie „rozłożyć” bez reszty na jednostki izoprenowe (C5). Narysuj szkieletowy wzór 1-etylo-2,2-dimetylocyklopentanu. Związek ten ma tylko 9 atomów węgla. Monoterpeny zwierają 10 atomów węgla. Spróbuj teraz przez dorysowanie w odpowiednim położeniu tylko jednego dodatkowego wiązania węgiel - węgiel (jako pojedynczej kreski), „otrzymać” węglowodór, który można zaliczyć do izoprenoidów. Odseparuj wyraźnie na wzorze jednostki izoprenowe. Czy istnieje więcej niż jedna możliwa struktura tego monoterpenu?
59.Wykorzystując wiedzę zdobytą na ćwiczeniach i wykładach z chemii organicznej podaj sposoby pozwalające na:
odróżnienie fruktozy od kwasu benzoesowego (obie substancje są ciałami stałymi) popowiedż test rozpuszczalnośći;
odróżnienie aldehydu D-glicerynowego (nazwa systematyczna: 2,3-dihydroksypropanal) od równomolowej mieszaniny aldehydu D i L glicerynowego (obie substancje są cieczami); podpowiedż - polarymetria
odróżnienie 1-pentanolu od pentanu (oba związki są cieczami); (test rozpuszczalności)
odróżnienie kwasu octowego od trietyloaminy (oba związki są cieczmi) (test rop[uszczalności]
Podaj wzory wymienionych związków. Tam gdzie jest to uzasadnione napisz stosowne reakcje chemiczne.
60B.Podaj sposób pozwalający na:
odróżnienie glicyny od proliny (oba związki są ciałami stałymi)
odróżnienie toluenu od cykloheksanolu (obydwa związki są cieczami)
odróżnienie tłuszczu roślinnego od tłuszczu zwierzęcego
odróżnienie glukozy od sacharozy (oba związki są ciałami stałymi)
Tam gdzie jest to uzasadnione napisz stosowne reakcje chemiczne.
61.Wskaż i uzasadnij każdą odpowiedź jednym zdaniem, który z wymienionych w podanych parach związków będzie:
miał wyższą temperaturę wrzenia: pentan czy 2,2-dimetylopropanol?
mocniejszym kwasem: kwas propanowy czy alkohol benzylowy?
łatwiej ulegał reakcji SEAr: anilina (aminobenzen) czy benzen?
ulegał reakcji wg mechanizmu SN1: 1-bromopropan czy 2-metylo-2-bromo-propan?
mocniejszą zasadą: dimetyloamina czy anilina?
Przy każdej odpowiedzi napisz wzory strukturalne wymienionych związków.
62.Narysuj wzory wymienionych związków. Wskaż i uzasadnij każdą odpowiedź jednym zdaniem, który z wymienionych w podanych parach związków będzie:
a)miał wyższą temperaturę wrzenia: etanol czy eter dimetylowy?
b)optycznie czynny: kwas 2-hydroksypropanowy czy kwas 3-hydroksypropan-owy?
c)łatwiej ulegał reakcji eliminacji: 2-metylo-2-butanol czy 1-pentanol?
d)wstępował sam ze sobą w reakcję aldolową: aldehyd benzoesowy czy butanal?
e)mocniejszą zasadą: dimetyloamina czy amoniak?
63.Wskaż i uzasadnij jednym zdaniem, który z wymienionych w parach związków:
a) będzie miał wyższą temperaturę wrzenia - chlorometan czy metanol?
b) wykaże większy moment dipolowy - chlorometan czy dichlorometan?
c) ulega reakcji Cannizzaro - acetaldehyd czy benzaldehyd?
64B.Wyjaśnij, dlaczego glicyna jest substancją krystaliczną (temp. topnienia 2620C) a jej ester metylowy jest cieczą (temp. wrzenia 1300C). Podaj wzory produktów reakcji glicyny z kwasem solnym, wodorotlenkiem sodu i kwasem azotowym (III). Jak wykrywamy aminokwasy?
65.Wśród poznanych klas związków wymień te, których cząsteczki są zdolne do tworzenia asocjatów. Odpowiednimi szkicami zilustruj powstawanie wiązań wodorowych dla przykładowych reprezentantów tych klas. Jaki jest wpływ tworzenia wiązań wodorowych na właściwości fizyczne tych związków?
66.Napisz wzory podanych związków i uszereguj je zgodnie z malejącą temperaturą wrzenia: butan, etan, 1-butanol, 2-metylopropan, kwas butanowy, eter dietylowy, etanol. Wśród podanych związków wskaż te, które są zdolne do tworzenia wiązań wodorowych z cząsteczkami H2O oraz te, które są zdolne do tworzenia asocjatów (czyli wiązań wodorowych same ze sobą). Wymień jeszcze inne klasy związków organicznych zdolnych do tworzenia asocjatów.
67.Napisz wzory sprzężonych zasad dla: kwasu octowego, fenolu, 2-nitrofenolu, wody, butanolu, kwasu trichlorooctowego. Podaj reakcje wymienionych kwasów Brønsteda (jeżeli zachodzą) z metalicznym sodem, roztworem NaOH i NaHCO3.
68.Przedstaw wszystkie wiązania wodorowe, które mogą zostać utworzone w roztworze wodnym zawierającym metanol i aceton. Jaka jest moc wiązań wodorowych w porównaniu z kowalencyjnym?
69.Uszereguj poniższe związki według malejącej kwasowości: HCl, C2H5OH, H2O, CH3COOH, CH3NH2, CF3COOH, C6H5OH, C2H2, C2H4.
70.Dla każdego z podanych związków: etanal, etyn, kwas etanowy, etanol, etyloamina napisz wzór sprzężonej z nim zasady Brønsteda. Wykorzystując dowolne dwie pary napisz równanie reakcji kwas - zasada. Wskaż kierunek przebiegu tej reakcji.
71B.Odpowiednimi przykładami zilustruj: a) enancjomery, b) diastereoizomery, c) węglowodór o konfiguracji absolutnej S, d) halogenopochodną o konfiguracji absolutnej R, e) L-aminokwas, f) L-ketoheksozę, g) związek mezo.
72.Napisz wzór i zaznacz centrum chiralności w kwasie 2-hydroksypropanowym (kwas mlekowy). Narysuj przestrzennie i w postaci wzoru Fischera enancjomer S tego hydroksykwasu. Zaznacz starszeństwo podstawników zgodnie z regułami CIP. W oparciu o narysowany wzór Fischera zdecyduj, czy związek ten ma konfigurację względną D czy L.
73.Narysuj wzór przestrzenny (S)-4-bromo-1-pentenu. Zaznacz starszeństwo podstawników. Czy związek ten zachowa czynność optyczną po uwodornieniu wiązania podwójnego? Odpowiedź uzasadnij.
74B. Alanina jest związkiem dwufunkcyjnym. Napisz wzór tego związku i przedstaw w jakiej formie będzie występował ten aminokwas w pH 2, pH = pI i pH 13. Podaj wzory strukturalne dipeptydów AlaGly i GlyAla. Czy związki te są optycznie czynne? Jak można przekonać się o ich czynności optycznej? Czy jest zależność stereoizomeryczna między tymi dipeptydami?
75B.Nazwa systematyczna aminokwasu fenyloalaniny (Phe) brzmi: kwas 2-amino-3-fenylopropanowy. Przedstaw w jakiej formie będzie występował ten aminokwas w pH 2, pH = pI i pH 13. Narysuj dipeptyd, zbudowany z fenyloalaniny. Zaznacz wiązanie peptydowe. Używając skrótu trzyliterowego oznaczającego fenyloalaninę napisz wszystkie możliwe dipeptydy, które mogą powstać w mieszaninie racemicznej tego aminokwasu. Wskaż wśród nich enacjomery.
76B.Aspartam (wzór poniżej), niskokaloryczny środek słodzący ( NutraSweet®) jest w istocie estrem metylowym dipeptydu: α-Asp-Phe-OCH3. Wskaż (obrysuj wszystkie atomy) grupę karboksylową, estrową i wiązanie peptydowe. Zaznacz węgle asymetryczne (*). Wiedząc, że aminokwasy wchodzące w jego skład mają konfigurację L określ konfigurację absolutną (R,S) na jednym z centrów asymetrii. Napisz wzory produktów pełnej hydrolizy aspartamu w żołądku (pH~3).
77B.Hydroliza zasadowa dwóch tłuszczów (A i B) daje oleinian sodu (C18H33O2Na) i palmitynian sodu (C16H31O2Na). Do utwardzenia 1 mola tłuszczu A niezbędne jest użycie 22,4 dm3 wodoru, natomiast do utwardzenia 1 mola tłuszczu B niezbędne jest użycie 2 moli wodoru. Wiadomo, że obydwa tłuszcze są optycznie czynne. Zaproponuj wzory tłuszczu A i tłuszczu B. Dla jednego z nich napisz wyżej wymienione reakcje.
78.Narysuj wzór 3-chlorocykloheksanonu. Zaznacz w tym związku centrum stereogeniczne. Określ konfigurację absolutną tego centrum chiralności (koniecznie ustal i zaznacz na podanym wzorze kolejność podstawników zgodnie z regułami CIP). Zdecyduj, czy redukcja tego związku do chlorocykloheksanu wpłynie na czynność optyczną tego związku?
79B.Poniżej przedstawiono wzór aldoheksozy o nazwie L-altroza w projekcji Fischera. Narysuj wzór D-altrozy i przedstaw wzory taflowe obu anomerów jej formy piranozowej. Wskaż w nich węgiel anomeryczny.
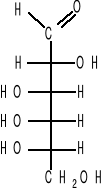
80B.Poniżej podano wzór idozy w formie piranozowej. Rozstrzygnij, czy jest to D czy L heksoza ? Jaki to anomer? Zaznacz węgle chiralne. Dla wybranego centrum chiralności określ kolejność podstawników zgodnie z regułami CIP i oznacz konfigurację absolutną.
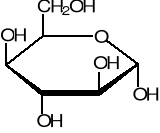
81.Podaj przykłady (równania konkretnej reakcji, bez mechanizmów) ilustrujące reakcje substytucji: a) nukleofilowej SN b) rodnikowej SR c) elektrofilowej SE. Nazwij substraty i produkty tych reakcji.
82.Odpowiednimi przykładami zilustruj reakcje addycji a) nukleofilowej AN, b) addycji elektrofilowej AE, c) addycji rodnikowej AR. Zilustruj także reakcję eliminacji E. Nazwij substraty i produkty tych reakcji.
83.Wyjaśnij znaczenie poszczególnych symboli w skrótach: SEAr, SR, SN1, AE, AN, E. Dla jednego z tych oznaczeń zaproponuj równanie konkretnej reakcji. Nazwij substraty i produkty tej reakcji.
84.Odpowiednimi konkretnymi przykładami zilustruj: a) reakcję regioselektywną b) reakcję stereoselektywną. Nazwij substraty i produkty tych reakcji.
85.Odpowiednimi przykładami równań reakcji zilustruj reakcję; a) przebiegającą zgodnie z regułą Markownikowa b) przebiegającą zgodnie z regułą Zajcewa.
86.Dla pięciu wybranych klas związków zaproponuj przynajmniej jedną metodę syntezy oraz przynajmniej jedną reakcję, której ulegają te związki. Zilustruj te reakcje dla konkretnego przedstawiciela danej klasy związków. Nazwij substraty i produkty tych reakcji.
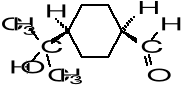
87.Poniższy aldehyd o zapachu konwalii jest stosowany w perfumerii ( związek ten o konfiguracji trans nie posiada zapachu). Napisz produkty jego reakcji: a) z 2,4-di-nitrofenylohydrazyną, b) z HCN, c) z nadmiarem alkoholu etylowego w obecności H2SO4 , d) z kwasem benzoesowym w obecności H2SO4, e) ogrzewanie produktu reakcji (b) z H3O![]()
.
88B.Tłuszcze są estrami gliceryny i wyższych kwasów tłuszczowych. Dla dowolnych, ale odpowiednich tłuszczów napisz reakcję hydrolizy i utwardzania. Nazwij produkty tych reakcji. W jakich warunkach reakcja hydrolizy estrów jest reakcją nieodwracalną? Przedstaw dokładny mechanizm tej reakcji dla mrówczanu metylu.
89B.Podaj wzór strukturalny trioleinianu glicerolu oraz wzory i nazwy związków A, B i C w poniższym schemacie:
![]()
90B.β-Alanina (kwas 3-aminopropanowy) jest izomerem kwasu 2-aminopropanowego (alaniny). Napisz wzory tych związków, wskaż ich grupy funkcyjne. Do jakiej klasy związków można je zaliczyć? Który z tych związków jest typowym składnikiem białek? Wyjaśnij, co oznacza zapis Ala-Ala, Ala-β-Ala i β-Ala-β-Ala. Napisz wzory tych dipeptydów.
91B.Wykorzystując naturalne aminokwasy: serynę HOCH2CH(NH2)COOH, cysteinę HSCH2CH(NH2)COOH i glicynę (kwas 2-aminooctowy) przedstaw wzór dowolnego tripeptydu. Wskaż aminokwas C-końcowy i N-końcowy. Zaznacz wiązania peptydowe. Jaki wpływ na strukturę białek ma obecność dodatkowych grup funkcyjnych w serynie i cysteinie?
92B.D-Ksyloza jest epimerem C-3 D-rybozy. Podaj wzór tetrozy, z której w wyniku syntezy Kilianiego-Fischera można otrzymać D-ksylozę. Czy ryboza też może być otrzymana z tego samego monosacharydu? Napisz wzory produktów reakcji D-ksylozy z wodą bromową, kwasem azotowym i borowodorkiem sodu.
Wyszukiwarka
Podobne podstrony:
Przykladowy egzamin chemia organiczna - ICiP - 2010-zima. , Egzamin
Egzamin Chemia organiczna zestawy 1 8
EgzaminMikrobPytania2008, chemia organiczna, biologia ewolucyjna-wykłady, genetyka, biologia komórki
egzamin d, chemia organiczna
Przykładowe pytania egzamin chemia
opracowane pytania egzaminacyjne chemia
mechanizmy do egzaminu, chemia organiczna
Pytania Wykład 5 Chemia organiczna aromaty
Test A Egzamin Chemia organiczna! 06 2008
pytania egzamin chemia fizyczna 08 2009
Egzamin Chemia organiczna zestawy
Przykladowy egzamin chemia organiczna - ICiP - 2010-zima. , Egzamin
Egzamin Chemia organiczna zestawy 1 8
Pytania Egzamin chemia
Egzamin Chemia Organiczna Jerzy Zoń
Chemia organiczna pytania na egzamin
więcej podobnych podstron