
KARDIOLOGIA PRAKTYCZNA
DLA LEKARZY RODZINNYCH
I STUDENTÓW MEDYCYNY
TOM III
Część 1
CHOROBA NIEDOKRWIENNA SERCA
Pod redakcją:
Mirosława Dłużniewskiego
Artura Mamcarza
Patryka Krzyżaka
AKADEMIA MEDYCZNA
WARSZAWA 2003

© Copyright by Mirosław Dłużniewski, Artur Mamcarz
& Patryk Krzyżak
ISBN 83-88559-85-0
Recenzent:
Prof. dr hab. n. med. Grzegorz Opolski
Druk i oprawa:
B-2 Sp. z o.o.
Projekt graficzny serii:
Urszula Janiszewska
Korekta:
Magdalena Zielonka
Katedra i Klinika Kardiologii
II Wydziału Lekarskiego Akademii Medycznej w Warszawie
ul. Kondratowicza 8, 03-242 Warszawa
tel.: (22) 326 58 24, fax: (22) 326 58 26
web site: www.amkard.waw.pl
e-mail: klinika@amkard.waw.pl

KARDIOLOGIA PRAKTYCZNA
DLA LEKARZY RODZINNYCH
I STUDENTÓW MEDYCYNY
TOM III
Część 1
CHOROBA NIEDOKRWIENNA SERCA

Autorzy:
Dr n. med. Wojciech Braksator
Lek. med. Ewa Burbicka
Lek. med. Marek Chmielewski
Lek. med. Agnieszka Cudnoch-Jędrzejewska
1
Lek. med. Katarzyna Cybulska
Prof. dr hab. n. med. Mirosław Dłużniewski
Lek. med. Agnieszka Domagała
Lek. med. Włodzimierz Gierlak
Dr n. med. Iwonna Grzywanowska-Łaniewska
Lek. med. Maciej Janiszewski
Lek. med. Liliana Kostana
Lek. med. Edyta Kostarska-Srokosz
Dr n. med. Małgorzata Kozłowska-Wojciechowska
2
Dr n. med. Jarosław Król
Dr n. med. Hubert Krysztofiak
3
Lek. med. Patryk Krzyżak
Prof. dr hab. n. med. Jerzy Kuch
Dr hab. n. med. Marek Kuch
Mgr Magdalena Makarewicz-Wujec
2
Dr hab. n. med. Artur Mamcarz
Prof. dr hab. Marek Naruszewicz
4
Lek. med. Agnieszka Petrykowska
Dr n. med. Witold Pikto-Pietkiewicz
Lek. med. Katarzyna Sadkowska
Dr n. med. Jacek Sawicki
Dr n. med. Teresa Serwecińska
Prof. dr hab. n. med. Kazimierz B. Suwalski
5
Lek. med. Piotr Suwalski
5
Dr n. med. Joanna Syska-Sumińska
Dr n. med. Edmund Szczepańczyk
Prof. dr hab. n. med. Ewa Szczepańska-Sadowska
1
Dr n. med. Andrzej Światowiec
Lek. med. Monika Tomaszewska-Kiecana
Dr hab. n. med. Adam Witkowski
6
Lek. med. Karol Wrzosek

z Katedry i Kliniki Kardiologii II Wydziału Lekarskiego AM w Warszawie
1
z Katedry i Zakładu Fizjologii Doświadczalnej i Klinicznej AM w Warszawie
2
z Zakładu Upowszechniania Wiedzy o Żywności i Żywieniu Instytutu
Żywności i Żywienia
3
z Zakładu Fizjologii Stosowanej Instytutu-Centrum Medycyny Doświad-
czalnej i Klinicznej PAN
4
z Centrum Badań nad Miażdżycą Pomorskiej AM w Szczecinie
5
z Oddziału Klinicznego Kardiochirurgii Katedry i Kliniki Chorób Wewnętrz-
nych i Kardiologii AM w Warszawie
6
z Instytutu Kardiologii w Aninie


Szanowne Koleżanki, Szanowni Koledzy!
Nasi młodsi Koledzy Studenci!
To już trzeci tom „Kardiologii Praktycznej” poświęcony „Chorobie niedokr-
wiennej serca”. Zaczynamy od fizjologii krążenia wieńcowego, rozdziału na-
pisanego „gościnnie” przez Panią Doktor Agnieszkę Cudnoch-Jędrzejewską
i Panią Profesor Ewę Szczepańską-Sadowską, którym chciałbym w tym miejscu
serdecznie podziękować za bardzo ciekawe ujęcie tematu.
Kolejnym ekspertem zaproszonym do udziału w tej części „Kardiologii
Praktycznej” jest Pani Doktor Małgorzata Kozłowska-Wojciechowska, a jej roz-
działy o wpływie żywienia w zapobieganiu i leczeniu ChNS za pomocą diety są
ogromnie cenne dla lekarzy praktyków – dziękujemy.
Bardzo potrzebny pogląd fizjologa klinicznego na skuteczność i bezpie-
czeństwo wysiłku fizycznego w ChNS prezentuje Pan Doktor Hubert Krzyszto-
fiak – za cenne uwagi dziękujemy.
Niewątpliwie cenne rozważania na temat tej trudnej choroby są udziałem
kolejnego Gościa, Pana Profesora Kazimierza Suwalskiego – „Kardiochirurgia
w zasięgu ręki” – bardzo dziękujemy Panu Profesorowi nie tylko za ten roz-
dział, ale także, a może przede wszystkim, za wykłady w naszej Podyplomowej
Szkole Kardiologicznej. Już ponad 1000 uczestników miało szansę wysłuchać
świetnego, pełnego chirurgicznej ekspresji, znakomicie przyjmowanego wykła-
du Pana Profesora.
Tajemnice dynamicznie rozwijającej się „Kardiologii inwazyjnej” przedstawia
nam kolejny ulubiony Wykładowca Szkoły Kardiologicznej – Pan Docent
Adam Witkowski. Wiedza o tym, jak dziś można pomóc pacjentowi z ChNS,
przy pomocy talentu i doświadczenia kardiologa inwazyjnego jest obowiązkową
i fascynującą lekturą dla praktyka – dziękujemy Panu Docentowi.
Wreszcie, trwająca już lata próba odkrycia tajemnicy rozwoju zmian w naczy-
niach – wybitny Ekspert w tej dziedzinie Profesor Marek Naruszewicz – praw-
dziwy „Naukowiec”, próbuje przybliżyć nam – klinicznym praktykom – subtel-
ności patogenezy miażdżycy. Temat ten jest także znakomicie przyjmowany
– dzięki talentowi Wykładowcy – przez Słuchaczy Szkoły. Dziękujemy Panie
Profesorze.
Jakie jeszcze rozdziały przygotowaliśmy w tym wydaniu o „Chorobie niedokr-
wiennej serca”?
1
Od etiopatogenezy miażdżycy do patogenezy choroby niedokrwiennej
serca – czy już naprawdę coś wiemy? Jeśli tak, to jak zrozumieć, rozpoz-
nać i w końcu, co najważniejsze, jak leczyć chorobę wieńcową spowo-
dowaną miażdżycą naczyń wieńcowych? Jak leczyć dolegliwości wieńcowe,
gdy nie znajdujemy zmian w naczyniach nasierdziowych, tak jak ma to
miejsce w zespole X? Jakie znaczenie ma „nieme niedokrwienie” – choro-
ba wieńcowa bez bólu, ale z konsekwencjami!?
Próbujemy wyjaśnić te ciekawe dla badacza i trudne dla klinicysty różnice.
Przedstawiamy też, pomimo istniejących standardów, dyskusyjne proble-
my postępowania w ostrych zespołach wieńcowych – kogo leczyć jeszcze
farmakologicznie, kogo już za pomocą nowoczesnych technik kardiologii
interwencyjnej.
Przedstawiamy odrębności choroby niedokrwiennej serca u kobiet, u osób
starszych i u chorych z cukrzycą – mówimy o jednej, ale jakże różnej choro-
bie, u różnych osób ze zróżnicowaną diagnostyką i postępowaniem.
Koleżanki i Koledzy Studenci!
W czasie zajęć w naszej Klinice spotykacie na co dzień chorych z chorobą
niedokrwienną serca: po zawale serca, po ostrym zespole wieńcowym, z bólami
typowymi i bez takich dolegliwości. Mówimy o chorobie wieńcowej stabilnej
i niestabilnej, o niemym niedokrwieniu i zespole X.
Na pierwszy rzut oka to ta sama, a przecież nie taka sama choroba – oto ko-
lejny dowód, że kardiologia jest ciekawa i co ważniejsze, że postęp w rozumie-
niu patogenezy tej choroby i, a może przede wszystkim, w leczeniu nowoczes-
nym i bardzo skutecznym – może być także Waszym udziałem.
Powtarzam to, co pisałem już wcześniej NAPRAWDĘ WARTO – to specjali-
zacja fascynująca dziś i obiecująca na przyszłość dla Was i Waszych Pacjentów.
Z życzeniami satysfakcji z kolejnego tomu „Kardiologii praktycznej”
Prof. dr hab. n. med. Mirosław Dłużniewski
2

PS
Z obowiązku, ale także z powodu dużej satysfakcji i z przyjemnością pragnę
podkreślić, że kolejny, trzeci już tom tego wydania ukaże się dzięki wsparciu
firmy Schwarz Pharma, Firmy świetnie i wytrwale rozumiejącej, że wspólnie
działamy dla dobra naszych Pacjentów! Z nadzieją na kolejne tomy bardzo
dziękujemy.
Tom ten nie powstałby bez udziału naszych Gości – znakomitych ekspertów:
Pani Dr Agnieszki Cudnoch-Jędrzejewskiej
Pani Dr n. med. Małgorzaty Kozłowskiej-Wojciechowskiej
Pani Mgr Magdaleny Makarewicz-Wujec
Pani Prof. dr hab. med. Ewy Szczepańskiej-Sadowskiej
Pana Dr. n. med. Huberta Krysztofiaka
Pana Prof. dr. hab. med. Marka Naruszewicza
Pana Prof. dr. hab. med. Kazimierza Suwalskiego
Pana Dr. Piotra Suwalskiego
Pana Doc. dr. hab. med. Adama Witkowskiego
Za trud włożony w przygotowanie swoich rozdziałów serdecznie dziękuję,
Prof. dr hab. n. med. Mirosław Dłużniewski
3

4
SPIS TREŚCI
Część 1
1. Krążenie wieńcowe – podstawy fizjologiczne i patofizjologiczne
Agnieszka Cudnoch-Jędrzejewska,
Ewa Szczepańska-Sadowska
5
2. Patogeneza miażdżycy, nowe koncepcje w świetle badań
podstawowych i klinicznych
Marek Naruszewicz
26
3. Epidemiologia choroby niedokrwiennej serca
Andrzej Światowiec, Patryk Krzyżak
38
4. Choroba niedokrwienna serca – podstawowe mechanizmy
i definicje. Implikacje dla lekarza praktyka
Mirosław Dłużniewski
51
5. Co należy robić, aby uniknąć choroby niedokrwiennej serca?
Prewencja pierwotna
Witold Pikto-Pietkiewicz, Artur Mamcarz
61
6. Postępowanie dietetyczne w chorobie niedokrwiennej serca
Małgorzata Kozłowska-Wojciechowska
89
7. Rola kwasów tłuszczowych, steroli i stanoli
w zapobieganiu miażdżycy
Małgorzata Kozłowska-Wojciechowska,
Magdalena Makarewicz-Wujec
106
8. Aktywność fizyczna w profilaktyce choroby
niedokrwiennej serca – recepta na wysiłek
Hubert Krysztofiak, Artur Mamcarz
125
9. Zasady diagnostyki nieinwazyjnej w chorobie
niedokrwiennej serca – standard postępowania
Wojciech Braksator, Artur Mamcarz, Joanna Syska-Sumińska,
Jarosław Król
151
10. Leczenie choroby niedokrwiennej serca
– jak powinien wyglądać standard?
Jarosław Król, Monika Tomaszewska-Kiecana,
Mirosław Dłużniewski
163
11. Stabilna dusznica bolesna
Joanna Syska-Sumińska, Iwonna Grzywanowska-Łaniewska,
Mirosław Dłużniewski
174
I.
KRĄŻENIE WIEŃCOWE – PODSTAWY
FIZJOLOGICZNE I PATOFIZJOLOGICZNE
Agnieszka Cudnoch-Jędrzejewska, Ewa Szczepańska-Sadowska
ANATOMIA FUNKCJONALNA NACZYŃ WIEŃCOWYCH
Zaopatrzenie w krew tętniczą
Krew dostarczana jest do serca przez dwie główne tętnice wieńcowe, wy-
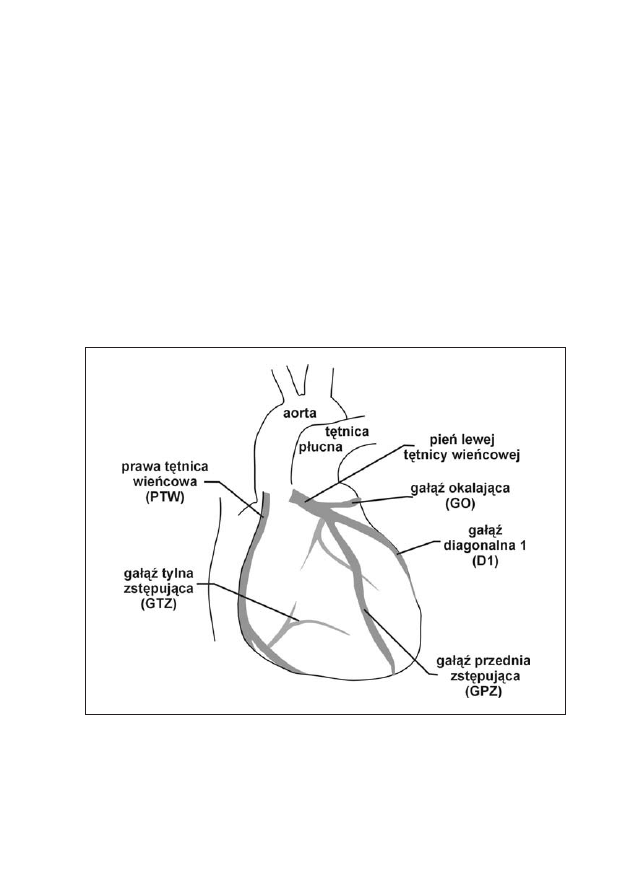
chodzące z aorty tuż poniżej zastawki aortalnej (ryc. 1). Krew płynie przez te
tętnice przez cały czas trwania cyklu hemodynamicznego serca, dzięki zawi-
rowaniom prądów krwi, które odsuwają płatki zastawek półksiężycowatych
aorty od ujścia tętnic wieńcowych.
Prawa tętnica wieńcowa jest naczyniem dominującym w 50% przypadków,
a lewa tylko w 20%. U pozostałych osób przepływ krwi przez obie tętnice
jest jednakowy.
5
Rycina 1: Tętnice wieńcowe i ich główne odgałęzienia

Prawa tętnica wieńcowa
Prawa tętnica wieńcowa biegnie w dół i na prawo w bruździe wieńcowej,
oddając odgałęzienia do prawego przedsionka i prawej komory. W 70%
przypadków przebiega ona wzdłuż dolnego brzegu lewej komory oddając ga-
łąź tylną zstępującą, zaopatrującą tylną część przegrody międzykomorowej
oraz odgałęzienia do lewej komory, zaopatrujące tylną ścianę serca.
Węzeł zatokowy i przedsionkowo-komorowy są zazwyczaj zaopatrywane
przez prawą tętnicę wieńcową, stąd ostre niedokrwienie wywołane zmniej-
szeniem przepływu przez to naczynie może doprowadzić do wystąpienia bra-
dykardii lub bloku przedsionkowo-komorowego różnego stopnia.
Lewa tętnica wieńcowa
Lewa tętnica wieńcowa zaopatruje w krew dolną część ściany lewej komo-
ry i tylną część przegrody. Zbudowana jest z pnia, który posiada dwie głów-
ne gałęzie:
Główne odgałęzienia tętnic wieńcowych wysyłają w kierunku wsierdzia
liczne tętnice o przekroju 100-300 nm nazywane przeszywającymi, które
przebiegają przez osierdzie, mięsień sercowy i wsierdzie prostopadle do dłu-
giej osi okrężnie ułożonych włókien mięśnia sercowego. Są to naczynia prze-
wodzące, których rola polega na szybkim dostarczeniu krwi do głębszych
warstw mięśnia sercowego. Naczynia te oddają na poziomie poszczególnych
warstw mięśnia sercowego liczne mniejsze tętnice i tętniczki o średnicy
10-100 nm. Tętniczki, łączą się ze sobą za pomocą naczyń włosowatych, wy-
twarzających sieci tętnicze ułożone prawie równolegle do powierzchni ścia-
ny serca. Najlepiej rozwiniętą sieć naczyń włosowatych stanowi splot pod-
wsierdziowy, położony bezpośrednio pod wsierdziem. Przepływ krwi przez
łożysko naczyń wieńcowych jest głównie regulowany przez zmiany napięcia
zwieraczy przedwłośniczkowych.
6
• gałąź przednia zstępująca biegnie w bruździe międzykomorowej
i zaopatruje ścianę przednią lewej komory i część przegrody
międzykomorowej;
• gałąź okalająca przebiega w bruździe wieńcowej lewej,
dostarczając krew do lewego przedsionka i lewej komory
(w 30% przypadków dzieli się na gałąź zstępującą tylną, która
z kolei zaopatruje w krew dolną część ściany lewej komory i tylną
część przegrody międzykomorowej).
Przepływ krwi przez naczynia włosowate
Jednolita dystrybucja przepływu wieńcowego między poszczególnymi czę-
ściami mięśnia sercowego jest możliwa dzięki licznym zespoleniom, łączą-
cym naczynia włosowate, zwłaszcza w przegrodzie międzykomorowej. Tęt-
niczki wieńcowe nie są więc tętnicami końcowymi z anatomicznego punktu
widzenia. Jednak pod względem funkcji fizjologicznej należą one do naczyń
końcowych, bowiem łączące je zespolenia nie mogą zapewnić dostatecznego
ukrwienia obocznego mięśniowi sercowemu podczas niedostatecznego za-
opatrzenia w tlen. Krew przepływająca przez splot podwsierdziowy kontak-
tuje się z krwią komór serca. Napływ krwi z komór serca nie przekracza 2%
całkowitego zaopatrzenia serca w krew, ale mimo to odgrywa on istotną ro-
lę w dostarczaniu krwi do włókien Purkinjego i strun ścięgnistych.
Odpływ krwi żylnej
Główna część krwi żylnej z mięśnia sercowego odprowadzana jest do pra-
wego przedsionka za pośrednictwem zatoki wieńcowej. W procesie tym bio-
rą udział zarówno drobne żyły wieńcowe, jak i naczynia tętnicze otwierające
się bezpośrednio do zatoki wieńcowej lub komór serca.
FIZJOLOGIA KRĄŻENIA WIEŃCOWEGO
Przepływ wieńcowy w spoczynku stanowi 4-5% pojemności minutowej ser-
ca (225 ml/min). U osób zdrowych podczas wysiłku fizycznego może wzro-
snąć nawet kilkakrotnie (650-900 ml/min).
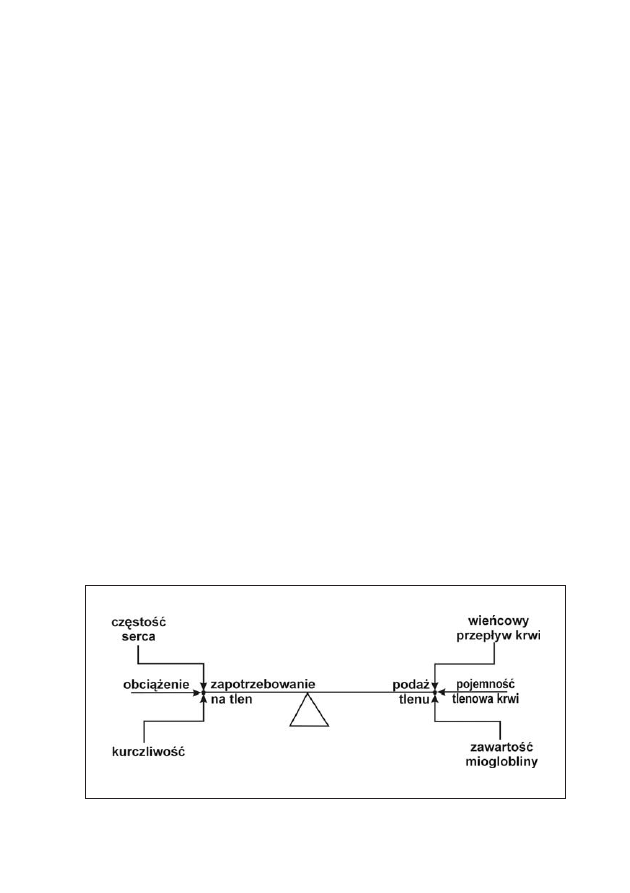
Podstawowym zadaniem krążenia wieńcowego jest zaopatrzenie serca
w krew proporcjonalnie do jego zapotrzebowania na tlen (ryc. 2).
7
Rycina 2: Równowaga pomiędzy zapotrzebowaniem i zaopatrzeniem w tlen mięśnia sercowego

Główną siłę napędową dla przepływu krwi przez krążenie wieńcowe stano-
wi gradient ciśnień pomiędzy początkowym odcinkiem tętnic wieńcowych
(tzn. średnim ciśnieniem w aorcie), a miejscem odpływu krwi żylnej (tzn.
prawym przedsionkiem). Ze względu na bardzo niskie ciśnienie w prawym
przedsionku przyjmuje się, że ciśnienie perfuzyjne krążenia wieńcowego jest
zbliżone do średniego ciśnienia panującego w aorcie.
Fizyczne determinanty przepływu wieńcowego
Przepływ przez naczynia wieńcowe podlega prawom hydrodynamiki, po-
dobnie jak wszystkie łożyska naczyniowe ustroju. Przepływ cieczy (Q), po-
dobnie jak przepływ prądu elektrycznego opisywany jest przez prawo Ohma,
dotyczące przepływu prądu elektrycznego, jest wprost proporcjonalny do
różnicy ciśnień (DP) między początkiem i końcem odcinka układu naczy-
niowego i odwrotnie proporcjonalny do oporu (R) stawianego przez ten
układ.
Opór, jaki stawia płynąca ciecz, definiuje prawo Poiseuile'a równaniem:
8
m l
p r
4
gdzie
m = lepkość krwi, l = długość naczynia, r = promień naczynia
Z równania tego wynika, że jedynym parametrem podlegającym dużej, dy-
namicznej zmianie w krążeniu wieńcowym jest promień naczyniowy. Zmia-
na średnicy tętnicy wieńcowej, spowodowana zmianą napięcia mięśni gład-
kich ściany tego naczynia, zwężeniem jego światła spowodowanym
obecnością blaszki miażdżycowej lub działaniem obu tych czynników jedno-
cześnie, wpływa wyraźnie na opór naczyniowy i przepływ wieńcowy.
Naczynia krążenia wieńcowego wytwarzają opór dla przepływu, różny
w poszczególnych segmentach naczyniowych. Tętnice nasierdziowe i odcho-
dzące od nich tętnice przeszywające stanowią mniej niż 20% całkowitego
oporu naczyniowego krążenia wieńcowego. Od nich z kolei odchodzą arte-
riole odpowiedzialne za 50-60% tego oporu. Pozostała cześć oporu dla prze-
pływu wieńcowego powstaje w naczyniach włosowatych. Nierównomierny
rozkład oporu naczyniowego jest spowodowany, obok przyczyn anatomicz-
nych, dodatkowo wzrostem czynnego napięcia mięśniówki gładkiej w naczy-
niach mikrokrążenia.
Wyróżniamy dwie składowe oporu naczyniowego determinujące spadek
przepływu wieńcowego:
8

Fazowe zmiany przepływu wieńcowego
Fazowość przepływu dotyczy głównie naczyń zaopatrujących mięsień le-
wej komory, gdzie w przeciwieństwie do innych obszarów naczyniowych krą-
żenia dużego, przepływ osiąga najwyższą wartość w czasie rozkurczu, a naj-
niższą w ostatnim okresie skurczu izometrycznego. Wysoka wartość
przepływu wieńcowego w czasie rozkurczu spowodowana jest spadkiem opo-
ru zewnątrznaczyniowego w tej fazie cyklu hemodynamicznego (spadek ci-
śnienia wewnątrzkomorowego oraz ciśnienia tkankowego w mięśniu serco-
wym).
Przyczyną niskiej wartości przepływu w czasie skurczu izowolumetrycznego
jest uciśnięcie naczyń śródmięśniowych przez wzrost ciśnienia tkankowego
spowodowany skurczem mięśnia sercowego i wzrostem ciśnienia wewnątrz-
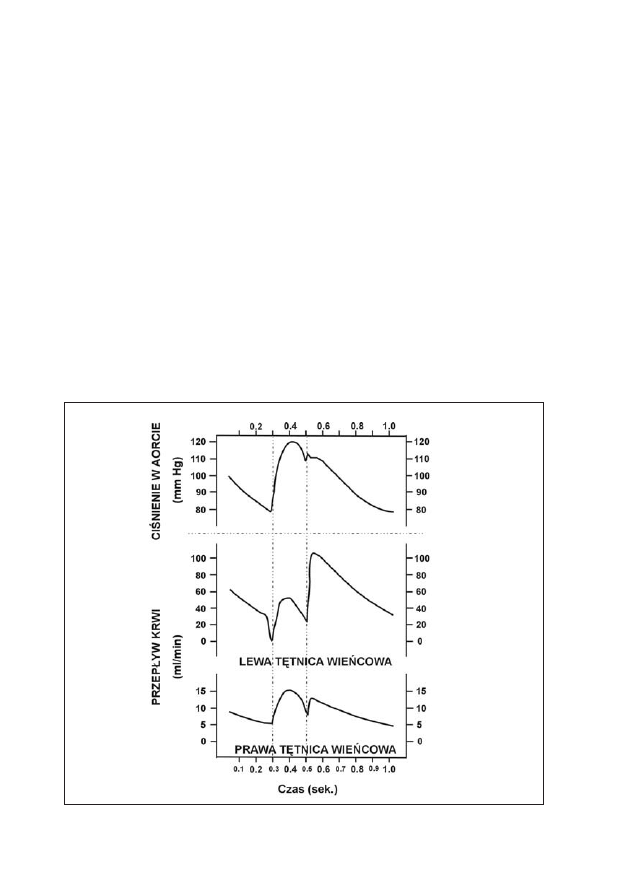
komorowego (ryc. 3). Należy pamiętać, że wysokość ciśnienia tkankowego
wywierającego ucisk na naczynia wieńcowe maleje w kierunku bardziej po-
wierzchownych warstw mięśnia lewej komory. Z tego powodu przepływ
w tym obszarze jest utrzymany w czasie całego cyklu hemodynamicznego ser-
ca, w przeciwieństwie do warstwy podwsierdziowej, gdzie w końcowej fazie
skurczu izometrycznego maleje on do wartości bliskich zeru.
U osób zdrowych ograniczenie przepływu wieńcowego, które ma miejsce
podczas skurczu, zostaje całkowicie skompensowane podczas rozkurczu.
Kompensacja taka występuje nawet w warunkach wysiłku fizycznego, kiedy
znacznie wzrasta siła skurczu mięśnia sercowego i zapotrzebowanie serca na
tlen. Najwyższy przepływ w rozkurczu występuje wówczas w warstwach pod-
9
• bierny opór zewnątrznaczyniowy – spowodowany uciskiem
kurczących się włókien mięśnia sercowego na sąsiadujące
naczynia wieńcowe oraz dodatkowo w czasie skurczu
izowolumetrycznego ciśnieniem krwi napierającej na ściany
komór; opór zewnątrznaczyniowy ma największą wartość
w warstwie podwsierdziowej mięśnia sercowego lewej komory
(najsilniejszy ucisk kurczących się włókien i ciśnienia krwi
w komorze) oraz systematycznie maleje w kierunku nasierdzia;
opór zewnątrznaczyniowy podlega rytmicznym zmianom podczas
cyklu hemodynamicznego serca, co z kolei pociąga za sobą fazowe
zmiany przepływu wieńcowego;
• aktywny opór wewnątrznaczyniowy – polega na zmianach napięcia
mięśni gładkich naczyń wieńcowych pod wpływem czynników
metabolicznych i neurohormonalnych.
wsierdziowych, w których jego upośledzenie podczas skurczu było najwięk-
sze. Skrócenie fazy rozkurczu podczas cyklu hemodynamicznego (tachykar-
dia) lub obniżenie ciśnienia rozkurczowego w aorcie (niedomykalność lub
stenoza zastawki aortalnej) pogarszają warunki przepływu krwi w krążeniu
wieńcowym w fazie rozkurczu i mogą mieć poważne implikacje kliniczne.
Czynnikiem utrudniającym kompensacyjne zwiększenie przepływu krwi
w naczyniach wieńcowych podczas rozkurczu jest również podwyższenie ci-
śnienia wewnątrzkomorowego w końcowej fazie rozkurczu lewej komory
(LVEDP). Może to mieć miejsce w niewydolności lewej komory lub wadach
zastawki aortalnej. Przy braku kompensacji rozkurczowej przepływu wień-
cowego najbardziej zagrożona niedokrwieniem jest podwsierdziowa warstwa
mięśnia sercowego, w której warunki przepływu podczas skurczu były naj-
gorsze. Dlatego też najczęściej w tej okolicy występuje zawał serca.
W zdrowym sercu wpływ oporu zewnątrznaczyniowego na przepływ wień-
cowy jest dodatkowo kompensowany czynnym rozkurczem mięśni gładkich
naczyń (wyjaśnienie niżej), ale w obszarze bez rezerwy wazodylatacyjnej
(w tzw. naczyniu stenotycznym) nie ma takiej możliwości.
10
Rycina 3: Przepływ krwi przez lewą i prawą tętnicę wieńcową podczas cyklu hemodynamicznego serca
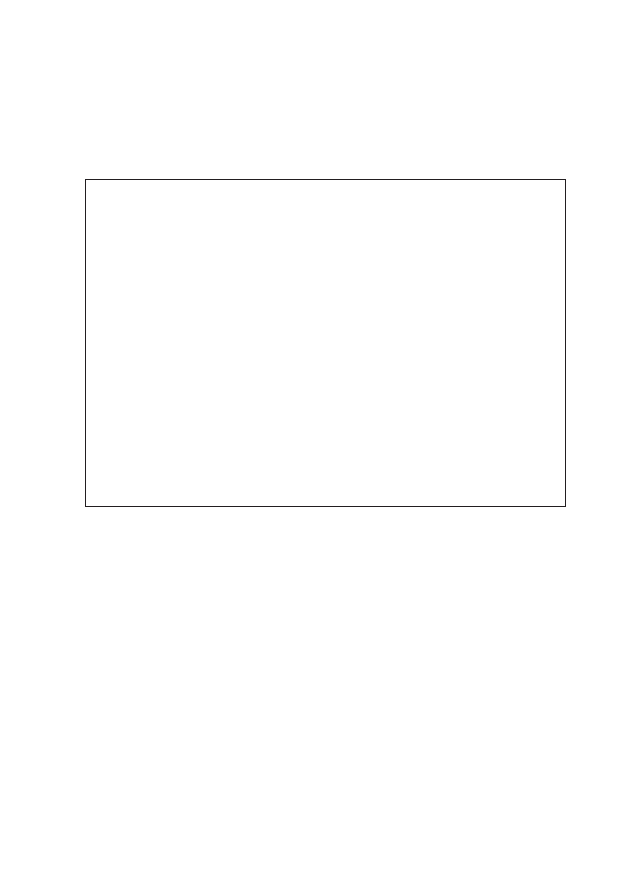
Wydajność transportu wieńcowego
Zdolność krążenia wieńcowego do zaopatrywania serca w składniki od-
żywcze i usuwania z niego produktów przemiany materii nazywana jest wy-
dajnością transportu. Zależy on od dwóch parametrów – pojemności prze-
pływu i pojemności wymiany:
REGULACJA KRĄŻENIA WIEŃCOWEGO
Regulacja krótkoterminowa
Stan czynny napięcia ściany naczynia, tzw. tonus naczyniowy, jest wypad-
kową działania czynników miogennych, metabolicznych, neurogennych, hor-
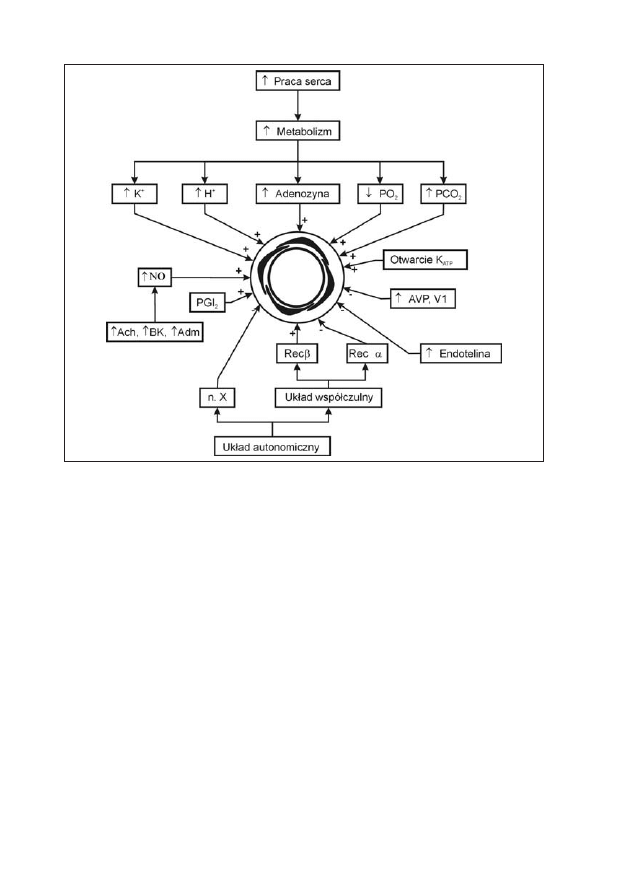
monalnych i humoralnych (ryc. 4). Regulacja nerwowo-humoralna odgrywa
niewielką rolę w zdrowym sercu.
Autoregulacja przepływu wieńcowego
Regulacja miogenna zależy od właściwości komórek mięśni gładkich
w ścianie naczynia, które kurczą się w odpowiedzi na rozciąganie. Skurcz
jest proporcjonalny do wzrostu ciśnienia transmuralnego (działającego w po-
przek ściany naczynia i rozciągającego je) i powoduje odpowiednie zmniej-
szenie światła naczyń i wzrost oporu naczyniowego. Dzięki temu przepływ
11
• pojemność przepływu określana jest na podstawie przepływu krwi
podczas maksymalnego rozszerzenia naczyń wieńcowych.
Wyznacza ona tzw. rezerwę wieńcową – różnicę pomiędzy
aktualnym, ustalonym przepływem wieńcowym, a przepływem
przez maksymalnie rozszerzone naczynia (potencjalna zdolność
do zwiększenia przepływu krwi w danym obszarze);
rezerwa wieńcowa jest znacznie mniejsza w podwsierdziowych niż
w podnasierdziowych warstwach komór mięśnia sercowego;
rezerwa wieńcowa może być trwale zmniejszona nie tylko przez
wzrost aktualnego przepływu, ale i przez zmniejszenie przepływu
maksymalnego. Powodem takiego zmniejszenia bywają zmiany
patologiczne występujące w naczyniach wieńcowych, np.
w przebiegu niewydolności serca, polegające na odkładaniu się
tkanki łącznej w ścianie naczynia, co z kolei prowadzi do
zgrubienia ścian i zmniejszenia ich podatności;
• pojemność wymiany zależy od przepuszczalności i powierzchni na-
czyń włosowatych w mikrokrążeniu wieńcowym.
krwi utrzymywany jest na stałym poziomie w pewnych granicach zmian ci-
śnienia perfuzyjnego. Zjawisko to, które odbiega od opisywanej wcześniej
(wynikającej z prawa Ohma) proporcjonalności zmian przepływu i ciśnienia
tętniczego, określono pojęciem autoregulacji. Autoregulacja przepływu
wieńcowego ma na celu przede wszystkim uniezależnienie mięśnia sercowe-
go od wahań ciśnienia krwi. Nie dotyczy ona zakresu bardzo niskich i wyso-
kich wartości ciśnienia perfuzyjnego.
Autoregulacja występuje w naczyniach wieńcowych z zachowaną rezerwą
wieńcową. W przypadkach, w których dochodzi do zwiększenia perfuzji wień-
cowej kosztem rezerwy wieńcowej (wysiłek fizyczny, niedokrwistość, obniżenie
ciśnienia parcjalnego tlenu we wdychanym powietrzu), dolna granica autore-
gulacji przesuwa się w kierunku wyższych wartości ciśnienia. Powoduje to
wzrost ryzyka niedokrwienia warstwy podwsierdziowej, w szczególności w sytu-
acji zwężenia naczynia wieńcowego. Do przesunięcia granic autoregulacji
w kierunku wyższych wartości dochodzi również w nadciśnieniu tętniczym.
12
Rycina 4: Schemat krótkoterminowej regulacji przepływu wieńcowego
AVP – wazopresyna; Adm – adrenomodullina; Ach – acetylocholina; BK – bradykinina; NO – tlenek azo-
tu; V
1
– receptory wazopresyny; PGI
2
– prostacyklina

Mechanizm autoregulacji nie jest do końca poznany. Starsze hipotezy za-
kładały, że zasadniczą przyczyną zjawiska autoregulacji jest otwarcie pod
wpływem rozciągnięcia ściany miocytów kanałów wapniowych wrażliwych na
rozciąganie. Wzrasta wówczas napływ jonów wapnia i zostaje zapoczątko-
wany skurcz. Obecnie przypisuje się również w tym procesie rolę ATP-zale-
żnym kanałom potasowym. Zamknięcie tych kanałów przez ATP powoduje
zmniejszenie wypływu jonów potasu i depolaryzuje błonę komórkową, co
ułatwia z kolei napływ jonów wapnia przez kanały zależne od potencjału
i skurcz mięśni gładkich. Przedłużający się skurcz naczyń i nagromadzenie
ADP i adenozyny powoduje z kolei otwarcie kanałów K
ATP
, rozkurcz mię-
śni gładkich i polepszenie przepływu.
Regulacja metaboliczna
Regulacja metaboliczna dotyczy naczyń o średnicy mniejszej niż 100 µm,
tzn. mających bliski kontakt z miocytami serca. Polega ona na dostosowaniu
przepływu do aktualnych potrzeb metabolicznych serca poprzez uwalniane
podczas jego pracy produktów przemiany materii o działaniu wazodylata-
cyjnym.
Zapotrzebowanie energetyczne serca
Serce wykorzystuje głównie energię pochodzącą z przemian tlenowych.
Ponieważ ma ono znikome możliwości magazynowania energii, wytwarza-
nie ATP musi nadążać za jego zużyciem. W spoczynku mięsień sercowy po-
chłania 6-8 ml/100 g/min O
2
, co stanowi 11% tlenu pobieranego przez cały
organizm (przeciętne zużycie tlenu w organizmie człowieka wynosi
0,4 ml/100 g/min). Warunkiem utrzymania bilansu energetycznego, a przez
to sprawności hemodynamicznej serca, jest zachowanie równowagi pomię-
dzy zaopatrzeniem i zużyciem tlenu przez ten narząd. Stąd pochłanianie tle-
nu oceniane podczas badania spiroergometrycznego stanowi obecnie naj-
bardziej wiarygodny parametr oceny wydatku energetycznego serca, a także
pośrednio jego wydolności.
Większość tlenu pochłanianego przez serce jest zużywana podczas pracy
związanej z hemodynamiką samego serca (tab. 1). Praca mechaniczna zwią-
zana z pracą zewnętrzną tego narządu zmienia się w zależności od rytmu
serca, naprężenia i kurczliwości mięśnia sercowego. Dlatego też leki działają-
ce na powyższe parametry, takie jak np.
b-adrenolityki czy antagoniści kana-
łów wapniowych, umożliwiają zmniejszenie pochłaniania tlenu. Do najwięk-
szego zużycia energii dochodzi jednak podczas skurczu izowolumetrycznego
(praca wewnętrzna), co z kolei – jak to przedstawiono wyżej – powoduje naj-
13

większe ograniczenie zapotrzebowania na tlen w warstwie podwsierdziowej
(najwyższy wzrost oporu zewnątrznaczyniowego).
Substraty energetyczne
Substratami energetycznymi mięśnia sercowego mogą być wolne kwasy
tłuszczowe, glukoza, mleczany, ciała ketonowe i aminokwasy. W warunkach
tlenowych dochodzi jednak do wykorzystania głównie wolnych kwasów tłusz-
czowych. Ich utlenianie dostarcza 60-70% energii. Pozostała część pochodzi
z fosforylacji oksydatywnej i glikolizy beztlenowej glukozy i glikogenu. Serce
wykorzystuje większość tlenu dostarczonego przez krążenie wieńcowe już
w warunkach spoczynkowych (70%), dlatego też przy dalszym wzroście za-
potrzebowania na tlen konieczne jest zwiększenie przepływu wieńcowego.
W zdrowym sercu obserwuje się liniowy wzrost przepływu wieńcowego wraz
ze wzrostem obciążenia serca pracą.
W warunkach niedostatecznego zaopatrzenia w tlen wzrasta znaczenie gli-
kolizy beztlenowej. Dochodzi wówczas do zwiększonego rozpadu glikoge-
nu. Ilość energii powstającej podczas przemian beztlenowych jest jednak
bardzo ograniczona i w warunkach niedokrwienia wystarcza jedynie na kilka
faz cyklu hemodynamicznego. Dłuższe niedokrwienie powoduje zaburzenie
przepływu wieńcowego. Dodatkowo procesy anaerobowe nasilają produk-
cję mleczanów, powodując obniżenie pH, co z kolei upośledza kurczliwość
miocytów i nasila istniejącą już najczęściej martwicę. W tabeli 2 przedsta-
wiono czynniki, które rozszerzają naczynia wieńcowe. W prawidłowo funk-
cjonującym krążeniu wieńcowym w dostosowaniu przepływu wieńcowego do
zwiększonych potrzeb metabolicznych współuczestniczą prawdopodobnie
jednocześnie: zwiększone wytwarzanie CO
2
, wzrost stężenia jonów potasu,
adenozyny i obniżenie ciśnienia parcjalnego tlenu w sąsiedztwie miocytów.
Potas uwalniany jest z komórek mięśnia sercowego podczas skurczu. Jego
działanie naczyniorozszerzające może mieć znaczenie zwłaszcza podczas ta-
chykardii, kiedy na skutek krótkiego okresu repolaryzacji stężenie jonów K
+
14
Tabela 1: Pochłanianie tlenu przez mięsień sercowy w zależności od potrzeb energetycznych
RODZAJ CZYNNOŚCI
POCHŁANIANIE TLENU [%]
przemiana podstawowa
15
aktywacja elektryczna
5
praca mechaniczna
80

w przestrzeni zewnątrzkomórkowej nie może zostać wyrównane i wzrasta do
10-15 mmol/l. Niedokrwienie i uszkodzenie komórek mięśnia sercowego po-
woduje uwolnienie i znacznie większy wzrost stężenia jonów potasu. Niedo-
krwienie powoduje również zwiększenie hipoksji, wzrost stężenia adenozyny,
ciśnienia parcjalnego CO
2
, nagromadzenie kwaśnych metabolitów i obniże-
nie pH. Czynniki te powodują zaburzenia przewodzenia pobudzeń w ukła-
dzie przewodzącym i w mięśniu sercowym oraz zaburzenia regulacji krążenia
wieńcowego.
Regulacja śródbłonkowa
Komórki śródbłonka, które wyściełają ściany naczyń krwionośnych wytwa-
rzają związki odgrywające ważną rolę w miejscowej regulacji przepływu
wieńcowego. Najważniejsze znaczenie naczyniorozszerzające ma tlenek azo-
tu (NO), powstający w wyniku działania syntazy śródbłonkowej (NOS 3) na
L-argininę. Głównym czynnikiem zwiększającym wytwarzanie NO jest
wzrost szybkości przepływu krwi w naczyniach, który łączy się ze zwiększe-
niem siły ścinającej (
t). Siła ta jest wprost proporcjonalna do szybkości stru-
mienia krwi i jej lepkości i odwrotnie proporcjonalna do trzeciej potęgi pro-
mienia naczynia. Rozszerzenie tętniczek przez opisane wyżej czynniki
metaboliczne powoduje zwiększenie szybkości przepływu krwi i uwolnienie
NO ze śródbłonka w wyższych segmentach naczyniowych. Dzięki silnemu
wazodylatacyjnemu działaniu NO ułatwiony jest dopływ krwi do znajdują-
cych się poniżej małych tętniczek i naczyń włosowatych serca. W warunkach
fizjologicznych wytwarzanie tlenku azotu w sercu utrzymywane jest na nie-
wielkim, ale stałym poziomie, co powoduje toniczny rozkurcz naczyń wień-
15
Tabela 2: Główne czynniki wpływające na metaboliczną i śródbłonkową regulację przepływu
wieńcowego
CZYNNIKI ZWIĘKSZAJĄCE PRZEPŁYW WIEŃCOWY
• hipoksja;
• hiperkapnia;
• hiperkaliemia;
• kwasica;
• wzrost osmolarności;
• adenozyna;
• tlenek azotu;
• prostacyklina.

cowych. Podczas wzmożonej pracy, a tym samym w warunkach nasilonego
metabolizmu mięśnia sercowego, np. podczas wysiłku fizycznego, dochodzi
do zwiększenia szybkości przepływu, wzrostu siły ścinającej i zwiększenia
uwalniania NO, który wpływa na sąsiadujące naczynia. W ten sposób wzrost
przepływu spowodowany początkowo czynnikami metabolicznymi jest wtór-
nie wspomagany przez uwalniany ze śródbłonka tlenek azotu.
Do związków rozszerzających naczynia wieńcowe, uwalnianych przez ko-
mórki sródbłonka pod wpływem siły ścinającej należy także prostacyklina.
Inne związki naczyniorozszerzające, takie jak np. acetylocholina, bradyki-
nina, adrenomedullina wywierają swoje działanie naczyniorozkurczowe na
naczynia wieńcowe również za pośrednictwem tlenku azotu.
W chorobie niedokrwiennej serca, hipercholesterolemii, nadciśnieniu tęt-
niczym, cukrzycy czy niewydolności serca dochodzi do upośledzenia wytwa-
rzania tlenku azotu, co umożliwia uzyskanie przewagi przez czynniki naczy-
niokurczące. Powoduje to ograniczenie rezerwy wieńcowej i ogranicza
zdolność regulacji metabolicznej.
Regulacja neurogenna
Serce jest unerwione przez neurony układu autonomicznego. Wpływ te-
go układu na napięcie mięśni gładkich naczyń wieńcowych jest stosunkowo
niewielki.
• Działanie bezpośrednie
Układ współczulny: W naczyniach wieńcowych występują receptory
a- i ß-ad-
renergiczne. Pobudzenie receptorów ß odpowiada za rozszerzenie naczyń,
natomiast stymulacja receptorów
a, znajdujących się głównie w warstwie
podnasierdziowej, wywołuje działanie naczyniozwężające i może spowodo-
wać spadek przepływu wieńcowego nawet do 30%. U osób zdrowych działa-
nie to jest kompensowane przez działanie śródbłonkowych czynników na-
czyniorozszerzających. W chorobie niedokrwiennej przy uszkodzonym
śródbłonku stymulacja układu współczulnego może spowodować ból wień-
cowy.
Układ przywspółczulny: Unerwienie przywspółczulne ogranicza się do
małych naczyń, położonych obwodowo w stosunku do tętnic nasierdziowych,
które rozszerzają się podczas aktywacji baroreceptorów i chemoreceptorów.
16

• Działanie pośrednie
Wpływ pośredni układu autonomicznego na przepływ wieńcowy związany
jest z regulacją pracy serca. Aktywacja układu współczulnego wywołuje przy-
śpieszenie częstości serca i wzrost kurczliwości mięśnia sercowego, co wtór-
nie prowadzi do wzrostu pracy serca i pochłaniania tlenu, a tym samym
wzrostu przepływu wieńcowego. Pobudzenie układu przywspółczulnego
zwalnia częstość pobudzeń generowanych w sercu zmniejszając jego pracę
i zapotrzebowanie na tlen.
Odruchowa regulacja przepływu wieńcowego
• Odruchy z baroreceptorów i chemoreceptorów
Pobudzenie receptorów w obrębie łuku aorty i zatoki tętnicy szyjnej po-
woduje rozszerzenie naczyń wieńcowych (redukcja tonicznego wpływu na-
czyniozwężającego układu współczulnego).
• Ekspozycja na zimno
U chorych z chorobą niedokrwienną serca ekspozycja na zimno powoduje
wzrost wieńcowego oporu naczyniowego. Jest to spowodowane stymulacją
układu współczulnego i pobudzeniem receptorów znajdujących się na na-
czyniach wieńcowych, co prowadzi do zmniejszenia przepływu i często do
pojawienia się bólu wieńcowego.
DŁUGOTERMINOWA REGULACJA PRZEPŁYWU WIEŃCOWEGO
Regulacja długoterminowa polega na długotrwałych zmianach bioche-
micznych i strukturalnych wpływających na wydolność transportu wieńco-
wego.
Trening fizyczny
U osób zdrowych intensywny, regularny trening fizyczny prowadzi do
przerostu mięśnia sercowego, któremu towarzyszą zmiany adaptacyjne
w krążeniu wieńcowym umożliwiające poprawę wydolności transportu wień-
cowego.
Wzrost rezerwy wieńcowego przepływu krwi spowodowany treningiem wy-
siłkowym jest możliwy dzięki zmianom zachodzącym w budowie naczyń
wieńcowych, jak również dzięki usprawnieniu mechanizmów kontrolujących
17

przepływ. Przebudowa może dotyczyć różnych segmentów naczyń krwiono-
śnych, w zależności od okresu życia, w jakim rozpoczęto trening. W przebie-
gu treningu dochodzi również do aktywacji niektórych mechanizmów neuro-
humoralnych. Do czynników ułatwiających przystosowanie krążenia
wieńcowego do wysiłków fizycznych należy wzrost aktywności układu współ-
czulnego i zwiększenie reaktywności naczyń wieńcowych na działanie związ-
ków naczyniorozszerzających. Główną przyczyną lepszej tolerancji wysiłków
fizycznych są jednak adaptacyjne zmiany obwodowe w mięśniach szkieleto-
wych i układzie ruchowym umożliwiające wykonanie tej samej pracy fizycz-
nej przy mniejszym koszcie energetycznym i mniejszym obciążeniu serca
pracą. Dzięki temu wykonywanie wysiłków fizycznych wymaga mniejszego
wzrostu przepływu wieńcowego.
Patologiczny przerost mięśnia sercowego
W licznych jednostkach chorobowych, takich jak nadciśnienie tętnicze czy
wady zastawkowe, dochodzi do przerostu mięśnia sercowego, a tym samym
również do zmian adaptacyjnych w krążeniu wieńcowym. Przy dużym prze-
roście mięśnia sercowego adaptacja krążenia wieńcowego może być nieade-
kwatna w stosunku do aktualnego zapotrzebowania na tlen. Dochodzi wów-
czas do zmniejszenia rezerwy wieńcowej, co w początkowym okresie objawia
się jedynie w warunkach wzmożonej pracy mięśnia sercowego, np. podczas
wysiłku fizycznego. Z czasem jednak prowadzi także do niedokrwienia mię-
śnia sercowego w spoczynku.
PATOFIZJOLOGIA KRĄŻENIA WIEŃCOWEGO
Niedokrwienie a hipoksja – definicje
Niedokrwienie serca pojawia się przy braku równowagi między aktualnym
zapotrzebowaniem serca na tlen, a dopływem utlenowanej krwi. Najczęst-
szą przyczyną takiego stanu są zmiany w samych naczyniach wieńcowych
(przede wszystkim miażdżyca). Inną przyczyną niedokrwienia może być
znaczny spadek ciśnienia perfuzyjnego w krążeniu wieńcowym spowodowa-
ny spadkiem ciśnienia układowego (krwotok, hipotonia ortostatyczna,
wstrząs endotoksyczny). Obniżenie ciśnienia układowego może ujawnić ist-
niejące już, ale bezobjawowe zaburzenia ukrwienia mięśnia sercowego spo-
wodowane chorobą wieńcową. Pojawieniu się niedokrwienia może również
sprzyjać wzrost ciśnienia końcowo-rozkurczowego w lewej komorze serca,
w niewydolności lewej komory lub wadach zastawki aortalnej. Fragment
mięśnia sercowego traktujemy jako fizjologicznie niedokrwiony, jeśli nie jest
18

w nim możliwe zapewnienie homeostazy tlenowej i prawidłowej funkcji skur-
czowej. Najlepszym wskaźnikiem wydajności przepływu krwi w krążeniu
wieńcowym jest rezerwa wieńcowa. Do zmniejszenia rezerwy dochodzi już
po zmniejszeniu światła naczynia o 30-40%, natomiast spoczynkowy prze-
pływ wieńcowy zostaje zredukowany dopiero po zmniejszeniu światła naczy-
nia wieńcowego o 85%. Rozróżniamy niedokrwienie:
Hipoksja polega na niewystarczającym zaopatrzeniu w tlen w stosunku do
zapotrzebowania i może wystąpić przy prawidłowej rezerwie wieńcowej. Po-
woduje ona zaburzenia procesów biochemicznych, elektrycznych i funkcji
mechanicznej serca. Niedokrwieniu zawsze towarzyszy hipoksja. Hipoksja
może jednak również występować w obecności prawidłowego przepływu
wieńcowego (np. w niedokrwistości, czy na znacznych wysokościach). Nie-
dokrwienie bardziej uszkadza mięsień sercowy niż sama hipoksja, bowiem
dodatkowo prowadzi do gromadzenia powstałych podczas przemian meta-
bolicznych szkodliwych substancji, które nie mogą być odprowadzone z mię-
śnia sercowego przez krew.
Patogeneza niedokrwienia mięśnia sercowego
• Powstanie blaszki miażdżycowej – zmiany wolno postępujące
Miażdżyca stanowi najczęstszą przyczynę niedokrwienia mięśnia sercowe-
go. Początkowo dochodzi do odłożenia w ścianie naczyniowej cholesterolu
i innych związków tłuszczowych oraz związków wapnia, które wytwarzają
blaszkę miażdżycową, ulegającą wtórnie zwłóknieniu. Stopniowy rozwój
blaszki może zostać na każdym etapie przerwany przez rozerwanie pokrywy
włóknistej, co prowadzi do powstania szczeliny w blaszce lub jej pęknięcia.
Pęknięcie blaszki oznacza utratę ochronnej, działającej przeciwzakrzepowo
warstwy błony wewnętrznej i kontakt krwi w świetle naczynia z trombogenną
19
• względne – dopływ krwi jest prawidłowy jedynie w spoczynku,
natomiast nie wzrasta adekwatnie do zapotrzebowania na tlen
podczas zwiększonego obciążenia (np. podczas wysiłku fizyczne-
go); niedokrwienie względne świadczy o braku lub ograniczeniu
rezerwy wieńcowej;
• bezwzględne – polegające na zmniejszeniu dopływu krwi do serca
już w warunkach spoczynkowych;
• całkowite – polegające na zatrzymaniu dopływu krwi do mięśnia
sercowego.
zawartością blaszki. Powoduje to jej dalsze powiększanie się na skutek ab-
sorpcji na powierzchni płytek, krwinek i włóknika i w efekcie powstanie ro-
snącego zakrzepu. Zmiany rozrostowe w ścianie naczynia i w samej blaszce
są przyspieszane przez wytwarzane w komórkach ściany naczyń, krwinkach
i płytkach krwi czynniki wzrostu, takie jak czynnik płytkopochodny (PDGF),
fibroblastopochodny (FGF) i czynniki transformujące (TGF). Skrzeplina
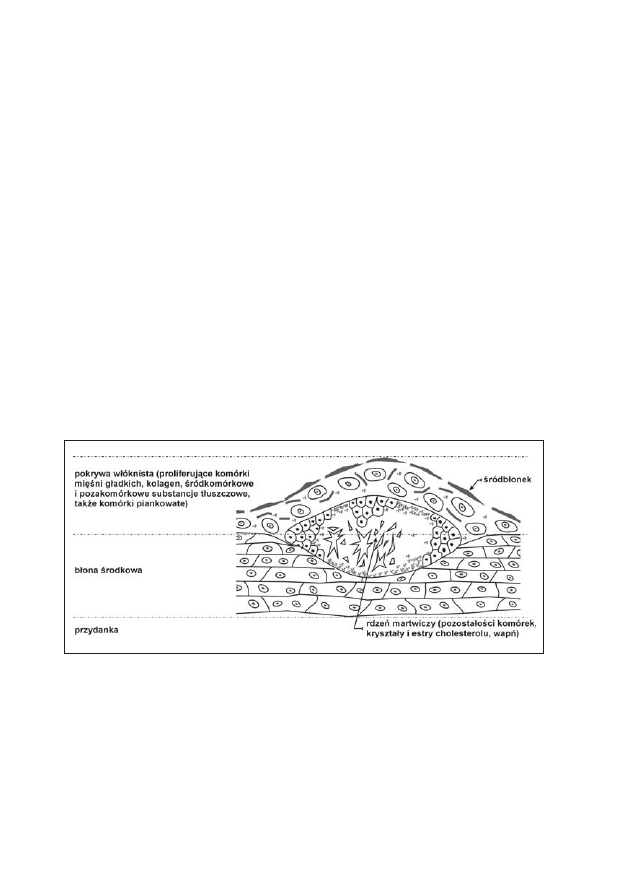
może się szerzyć do światła, zamykając je całkowicie lub częściowo (ryc. 5).
Wyniki badań przeprowadzonych na zwierzętach wskazują, że zwężenie
średnicy światła przez blaszkę miażdżycową poniżej 50-60% ogranicza prze-
pływ nawet przy maksymalnym rozkurczu, niemniej przepływ spoczynkowy
nie jest upośledzony, dopóki nie wystąpi zwężenie 80-90%.
Rozwój blaszki miażdżycowej powoduje najczęściej mniejsze ograniczenie
rezerwy wieńcowej, niż wynikałoby to z ograniczenia przepływu przez miaż-
dżycowo zwężone naczynie. Dochodzi bowiem do rozwoju krążenia obocz-
nego, mogącego częściowo kompensować obniżenie przepływu wieńcowe-
go. Rolą krążenia obocznego jest zapobieganie rozwojowi zawału lub
ograniczenie jego rozmiarów. Dlatego bardziej burzliwy przebieg zawału
mięśnia sercowego znacznie częściej spotyka się u ludzi młodych, u których
krążenie oboczne nie zdążyło się jeszcze dobrze rozwinąć.
• Nagłe zamknięcie tętnicy wieńcowej
Zator tętnicy wieńcowej, powstający w wyniku oderwania się zakrzepu od
położonej powyżej blaszki miażdżycowej stanowi najczęstszą przyczynę na-
głego zamknięcia się naczynia. Pęknięcie blaszki miażdżycowej może zostać
przyspieszone przez gwałtowny wzrost ciśnienia lub szybkości przepływu
krwi. Światło tętnicy wieńcowej może być również zamknięte przez zakrzepy
20
Rycina 5: Struktura blaszki miażdżycowej

przyścienne powstałe w lewym przedsionku lub komorze. Utrzymanie się
wystarczająco długo naczyniowego skurczu tętnicy wieńcowej (tzw. wazo-
spazm naczyniowy) także może przyczynić się do nagłego zamknięcia światła
naczynia. Przebieg kliniczny nagłego zamknięcia światła tętnicy wieńcowej
jest zazwyczaj bardzo dramatyczny z powodu braku czasu na rozwój krążenia
obocznego.
Następstwa niedokrwienia mięśnia sercowego
• Zawał mięśnia sercowego
Długo trwające lub bardziej nasilone niedokrwienie, niemożliwe do nor-
malizacji podczas reperfuzji doprowadza do nieuniknionej martwicy mięśnia
sercowego zwanej zawałem serca (dopływ krwi poniżej 1,3 ml/100 g/min).
Proces ten może zachodzić w ciągu minut od momentu wystąpienia niedo-
krwienia lub pojawić się dopiero po kilku godzinach, w zależności od tempa
przemian metabolicznych i rozmiaru zwężonego naczynia. Paradoksalnie nie
ma jednak zależności pomiędzy stopniem zwężenia tętnicy a prawdopodo-
bieństwem wystąpienia zawału. Poszczególne miocyty mogą wykazywać róż-
ny stopień wrażliwości na niedokrwienie. Już po 8-10 sekundach od zatrzy-
mania dopływu krwi, dochodzi do przesunięcia procesów przemiany materii
z torów tlenowych na beztlenowe. Po 15 minutach wzrasta liczba recepto-
rów
b-adrenergicznych na kardiomiocytach i ich wrażliwość na działanie
b-agonistów. Stopniowo dochodzi do aktywacji procesów zapalnych i apo-
ptozy komórek. Po upływie 40-60 minut, brak jest wiązań wysokoenergetycz-
nych, dochodzi do obniżenia pH, obrzmienia komórek, uszkodzenia mito-
chondriów i sarkolemmy. Nasilenie tych odpowiedzi może być różne,
w zależności od przyczyn niedokrwienia. Wydaje się, że większość miocytów
przeżywa niedokrwienie do 15 minut, stąd reperfuzja w tym okresie całkowi-
cie zapobiega wystąpieniu zawału serca, ale może prowadzić do innych ro-
dzajów następstw niedokrwienia, przebiegających zazwyczaj w dwóch posta-
ciach: ogłuszenia i hibernacji. W niektórych sytuacjach procesy te mogą
w siebie wzajemnie przechodzić.
W obszarze zawału można zawsze wyróżnić strefę całkowitego niedo-
krwienia i strefę brzegową, do której dopływa pewna ilość krwi drogą połą-
czeń obocznych. W warunkach podstawowych strefa brzegowa może być wy-
starczająco zaopatrzona w tlen, jednak podczas zwiększenia pracy serca (np.
podczas wysiłku fizycznego lub pobudzenia układu współczulnego przez
stres) krew odpływa ze strefy brzegowej do innych rozszerzonych naczyń
mięśnia sercowego (tzw. podkradanie krwi), co powoduje powiększenie stre-
21

fy bezwzględnego niedokrwienia i zwiększa zagrożenie poszerzeniem strefy
zawałowej.
• Ogłuszenie mięśnia sercowego
Zarówno ciężkie niedokrwienie, jak i hipoksja, nie trwające na tyle długo,
aby doprowadzić do nieodwracalnego uszkodzenia komórek serca, powodu-
je ogłuszenie (stunning) mięśnia sercowego. Ogłuszeniem nazywamy zabu-
rzenia kurczliwości lub zdolności relaksacyjnych miocytów, występujące
w następstwie nagłych pojedynczych lub powtarzających się epizodów nie-
dokrwienia (np. w niestabilnej chorobie wieńcowej). Reperfuzja prowadzi
wówczas do podjęcia czynności przez komórki serca, ich funkcja nie zostaje
jednak w pełni przywrócona, a praca serca charakteryzuje się przetrwałą dys-
funkcją skurczową i zmniejszonym pobieraniem tlenu. Obserwuje się wzrost
przepuszczalności ścian naczyń oraz obrzęk komórek przestrzeni zewnątrz-
komórkowej spowodowany działaniem wolnych rodników tlenowych, po-
wstałych na skutek reperfuzji i ponownego dowozu tlenu. Prowadzi to do
zaburzeń funkcji pompy sodowo-potasowej, wapniowej i wodorowej oraz
wymiany sód/wapń. Ostatecznym wynikiem tych zaburzeń jest nadmierna
akumulacja jonów wapnia i sodu w komórkach mięśnia sercowego, z jedno-
czasowym zmniejszeniem wrażliwości układów kurczliwych na jony wapnia.
To przemijające przeładowanie komórek wapniem prowadzi do aktywacji
układów enzymatycznych, uszkadzających włókna mięśnia sercowego. Ogłu-
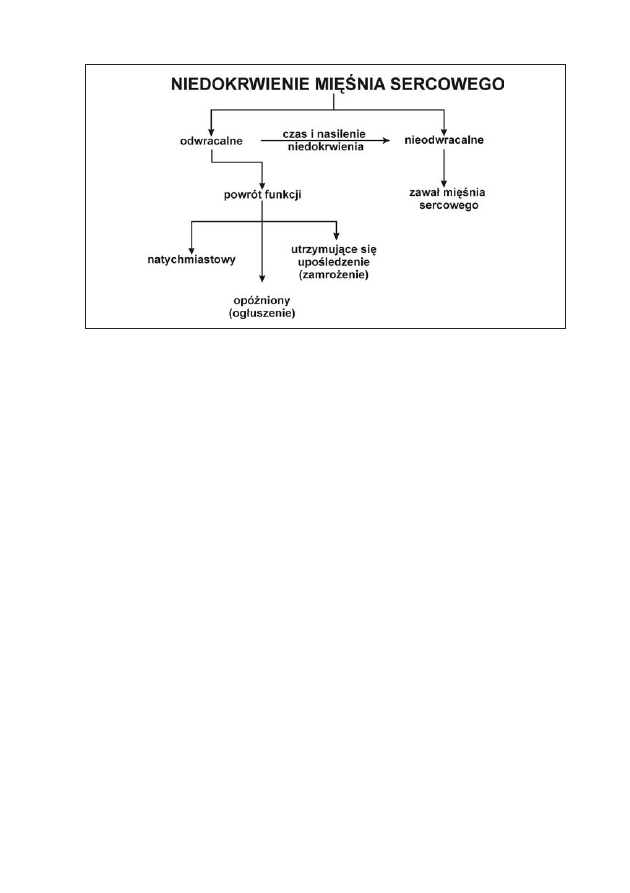
szenie może ustąpić samoistnie lub może przekształcić się w zamrożenie
(ryc. 6). Poddanie pacjenta wczesnej angioplastyce lub CABG (coronary ar-
tery bypass graft) stopniowo w ciągu tygodni powoduje pełne przywrócenie
kurczliwości w ogłuszonym obszarze mięśnia sercowego. Uważa się, że leki
inotropowo dodatnie, także mogą przezwyciężyć ogłuszenie, a przeciwutle-
niacze nawet zapobiec jego wystąpieniu.
• Zamrożenie mięśnia sercowego (hibernacja)
Zjawisko długotrwałego zaburzenia kurczliwości mięśnia sercowego, poja-
wiające się w postaci nie kurczących się lub słabo kurczących się niedosta-
tecznie perfundowanych obszarów zostało nazwane zamrożeniem mięśnia
sercowego. Jest ono uważane za przejaw adaptacji fizjologicznej do chro-
nicznego niedokrwienia. Obszary „zamrożone” są trudne do różnicowania
z obszarem hipo- lub akinezy pozawałowej. Dopiero rewaskularyzacja umoż-
liwia prawidłową interpretację zmian, bowiem w jej trakcie dochodzi do po-
prawy kurczliwości w mięśniu zamrożonym. Należy podkreślić, że o ile
w mięśniu ogłuszonym nie ma charakterystycznych zmian histopatologicz-
22
nych, stanowiących adaptację do zmian metabolicznych, to podczas procesu
zamrożenia dochodzi m.in. do przyjęcia postaci płodowej przez białka włó-
kien mięśniowych, zwiększonej ekspresji przedsionkowego peptydu natriure-
tycznego (ANP) w kardiomiocytach komór i wzmożonego gromadzenia gli-
kogenu. Umożliwia to utrzymanie miocytów przy życiu, jednak ze znacznym
ograniczeniem ich kurczliwości. W interpretacji znaczenia procesu zamro-
żenia to przewlekłe ograniczenie kurczliwości nie jest rozważane jako wynik
długotrwałego niedoboru energii, lecz jako zjawisko regulacyjne, które po-
zwala uniknąć bieżącego niedoboru energii, który mógłby spowodować mar-
twicę, i tym samym utrzymać żywotność mięśnia sercowego.
Hibernacja może być bezpośrednią konsekwencją niedokrwienia lub mo-
że pojawić się w następstwie ogłuszenia (ryc. 6) Warto pamiętać, że niedo-
krwienie mięśnia sercowego, nie przerwane w odpowiednim momencie, do-
prowadza nieuchronnie do śmierci komórki, ale reperfuzja niezbędna do
przeżycia komórek także niesie ze sobą pewne ryzyko związane z ogłusze-
niem lub zamrożeniem i wymaga ostrożnego postępowania terapeutycznego
w tym okresie.
23
Rycina 6: Skutki niedokrwienia mięśnia sercowego

KARDIOPROTEKCJA I JEJ MECHANIZMY
Kardioprotekcja – polega na uruchomieniu mechanizmów wspomagają-
cych reperfuzję w celu:
Rozważając mechanizmy kardioprotekcji nie można pominąć zdolności
adaptacyjnych samego mięśnia sercowego do ograniczania skutków niedo-
krwienia, przejawiające się w postaci tzw. zjawiska hartowania (preconditio-
ning). Polega ono na zwiększonej tolerancji niedokrwienia po powtarzają-
cych się epizodach niedokrwienia. Mechanizm tego zjawiska polega na
zwiększaniu się podatności naczyń wieńcowych serca na działanie czynników
naczyniorozszerzających wskutek otwarcia kanałów potasowych. W wyniku
niedostatecznego dowozu tlenu w mięśniu sercowym maleje stężenie ATP,
a wzrasta stężenie adenozyny, która otwiera kanały K
ATP
. Przypuszczalnie
w zjawisku hartowania odgrywa również rolę bradykinina, działająca za po-
średnictwem receptorów
b
2
. Dzięki hartowaniu, bardziej efektywne jest roz-
szerzenie naczyń strefy brzeżnej w trakcie długotrwałego niedokrwienia, co
najczęściej prowadzi do ograniczenia obszaru zawału mięśnia sercowego lub
nawet zapobiega jego wystąpieniu.
Niektórzy badacze uznają także ogłuszenie i zamrożenie mięśnia serco-
wego za endogenne mechanizmy kardioprotekcyjne; ogłuszenie w ostrym
niedokrwieniu, a zamrożenie w przewlekłym.
Kardioprotekcja metaboliczna i farmakologiczna – są to działania z ze-
wnątrz organizmu, wspomagające mechanizmy endogenne i stanowiące
ukierunkowaną i w wielu przypadkach skuteczną metodę naprawczą.
Powszechnie wiadomo, że zastosowanie mieszanki polaryzującej GIK (glu-
koza, insulina, potas) w umiarkowanym niedokrwieniu, bądź w niedokrwie-
niu towarzyszącym reperfuzji, umożliwia zwiększenie rezerwy energetycz-
nej. Tradycyjne formy terapii stabilnej choroby niedokrwiennej serca czy
zawału serca polegają m.in. na poprawie dostarczenia tlenu do niedokrwio-
nego mięśnia sercowego (mechaniczne metody udrożnienia, związki naczy-
niorozszerzające) i obniżaniu jego zapotrzebowania na tlen (
b-adrenolity-
24
• zmniejszenia zakresu nieodwracalnego uszkodzenia zdolności
serca do skurczu;
• ograniczenia nieodwracalnego uszkodzenia miocytów
– zmniejszenie strefy zawałowej;
• zmniejszenia zaburzeń bioelektrycznych – ograniczenie
podatności na arytmię;
• poprawy przepływu wieńcowego.

ki). Ostatnie badania zarówno eksperymentalne, jak i kliniczne potwierdzi-
ły, że przesunięcie głównego źródła energii w niedokrwionym mięśniu serco-
wym z kwasów tłuszczowych w kierunku metabolizmu glukozy, może stano-
wić efektywne przyszłościowe postępowanie terapeutyczne.
Zapamiętaj!
1. Podstawowym zadaniem krążenia wieńcowego jest zaopatrzenie mięśnia
sercowego w krew proporcjonalnie do jego zapotrzebowania na tlen.
2. Rezerwa wieńcowa to potencjalna zdolność krążenia wieńcowego do zwięk-
szenia przepływu krwi, np. podczas wysiłku fizycznego.
3. Krążenie wieńcowe podlega regulacji miogennej, metabolicznej i neurohu-
moralnej.
4. Niedokrwienie mięśnia sercowego to brak równowagi między aktualnym za-
potrzebowaniem na tlen mięśnia serowego, a dopływem krwi utlenowanej.
5. Najczęstszą przyczyną niedokrwienia mięśnia sercowego jest powstanie
blaszki miażdżycowej.
6. Zawał mięśnia sercowego stanowi następstwo długotrwałego niedokrwie-
nia, prowadzącego do martwicy mięśnia sercowego.
7. Kardioprotekcją nazywamy reakcje ochronne ze strony mięśnia sercowego,
ułatwiające jego funkcję lub przeżycie, np. w warunkach niedokrwienia.
Polecane lektury:
M. Berne, M. N. Levy, R. M. Koeppen, B. A. Stanton: Physiology, Mosby,
Philadelphia 1998.
A. Beręsewicz, M. Mączewski: Regulacja krążenia wieńcowego w normie
i w chorobie wieńcowej. W: Choroba niedokrwienna serca. Fundacja dla
serca. Red. M. Dłużniewski, Warszawa 1998.
J. D. Hosenpud, B. H. Greenberg: Congestive Heart Failure. Lippincott
Williams and Wilkins, Philadelphia 2000.
A. Januszewicz, W. Januszewicz, E. Szczepańska-Sadowska, M. Sznajder-
man: Nadciśnienie tętnicze. Medycyna Praktyczna, Kraków 2000.
J. Kupersmith: Farmakoterapia chorób serca, Wrocław 1998.
J. McGeown: Physiology, Belfast 2002.
E. Szczepańska-Sadowska: Seminaria z fizjologii, część 2, AM Warszawa 2001.
25

II.
PATOGENEZA MIAŻDŻYCY, NOWE KONCEPCJE
W ŚWIETLE BADAŃ PODSTAWOWYCH
I KLINICZNYCH
Marek Naruszewicz
Widoczny postęp w leczeniu chorób układu krążenia, który nastąpił
w ostatniej dekadzie nie może jednak przesłaniać faktu, że w roku 2003
w USA wystąpi półtora miliona zawałów serca i siedemset tysięcy udarów
mózgu. Jest to wymierny skutek starzenia się tej populacji, a także efekt bra-
ku odpowiednich działań diagnostycznych i leczniczych. Takie działania bo-
wiem należy podejmować już w dzieciństwie, gdyż miażdżyca jest procesem
powolnym i z reguły nie dającym żadnych objawów przed wystąpieniem
ostrego incydentu wieńcowego.
Znamy już teoretycznie ponad 200 różnych czynników, które mogą inicjo-
wać i nasilać proces aterogenezy, a więc powodować akumulację choleste-
rolu w tętnicach, często nawet wtedy, gdy jego poziom w osoczu nie prze-
kracza pożądanej wartości, tj. 200 mg/dL i nie towarzyszy temu nadciśnienie
tętnicze lub cukrzyca typu 2. Świadczy to o tym, że nie można już dalej igno-
rować tych czynników, w tym genetycznych, które w połączeniu z wadliwym
sposobem żywienia zwiększają skłonność do miażdżycy. Zagadnieniami cze-
kającymi więc na szybkie rozwiązanie są przede wszystkim te, które dadzą
odpowiedź, jakimi metodami, jak wcześnie i jakim kosztem (cost effective-
ness) należy je wykrywać. Na to pytanie postaram się odpowiedzieć w niniej-
szym rozdziale, przedstawiając pokrótce także historię badań nad miażdży-
cą i ich perspektywy wynikające z osiągnięć biologii molekularnej i genetyki.
ZARYS HISTORII BADAŃ NAD MIAŻDŻYCĄ
Wbrew ogólnie przyjętym poglądom, że miażdżyca jest atrybutem ostat-
niego stulecia naszej cywilizacji, zmiany charakterystyczne dla ogniska atero-
matycznego wykryto u mumii egipskich. Sądząc także z opisów historycz-
nych, wielu wielmoży i dostojników kościelnych miało objawy chorób układu
krążenia i były one prawdopodobną przyczyną ich zgonów. Z dużym praw-
dopodobieństwem można sądzić, że powodem tego był ułatwiony dostęp do
żywności, brak ruchu i związana z tym otyłość, a więc czynniki ryzyka rozpo-
wszechnione obecnie i to niezależnie od pozycji społecznej.
Na fakt, że patogeneza miażdżycy jest procesem złożonym i wieloprzyczy-
nowym, wskazywali już pierwsi badacze tego zagadnienia w XIX stuleciu, tj.
Von Rokitanski i Virchow. O wyjątkowej celności tych obserwacji świadczy
26

fakt, że zawarte w nich sugestie są wciąż aktualne i stanowią podstawę do
proponowanej obecnie zunifikowanej teorii rozwoju miażdżycy. Połączyła
ona dwie przeciwstawne hipotezy, tj. Rokitanskiego o udziale substancji
obecnych w krążeniu w tworzeniu zmian naczyniowych i Virchova o podłożu
zapalnym ogniska ateromatycznego. Dalszym kamieniem milowym na dro-
dze wykrywania czynników etiologicznych miażdżycy były badania Anichko-
va i Khalatova nad patogenną rolą cholesterolu. Prawie trzydzieści pięć lat
później Gofman i współpracownicy wyizolowali metodą ultrawirowania – li-
poproteiny transportujące cholesterol i inne lipidy, tj. VLDL, HDL i LDL.
Ich elektroforetyczny rozdział na agarozie pozwolił Fredriksonowi na po-
czątku lat sześćdziesiątych podzielić zaburzenia gospodarki lipidowej na 5 ty-
pów hiperlipidemii. W międzyczasie, tj. w roku 1949 Duquid opublikował
pracę sugerującą, że agregujące płytki krwi i powstały skrzep naczyniowy po-
wodują uszkodzenie śródbłonka naczyniowego, z dalszymi konsekwencjami
dla rozwoju miażdżycy. Przygotował on w ten sposób grunt pod aktualną do
dziś hipotezę „odpowiedzi na uszkodzenie” wysuniętą przez Rossa i Glom-
seta w połowie lat siedemdziesiątych. Należy dodać, że Ross był także od-
krywcą czynnika mitogennego syntetyzowanego przez płytki krwi stymulu-
jącego proliferację komórek mięśni gładkich, czyli tzw. płytkowego czynnika
wzrostu (PDGF). Jego wykrycie wyjaśniło również częściowo sens hipotezy
monoklonalnej miażdżycy, którą lansował Benditt, a zakładała ona, że ist-
nieją bliżej nieokreślone czynniki (bakterie, wirusy, chemikalia), które nasi-
lają rozrost komórek mięśni gładkich pogrubiając ścianę naczynia.
Prawdziwy przełom w badaniach nad miażdżycą rozpoczął się jednak w la-
tach osiemdziesiątych wraz z rozwojem genetyki i biologii molekularnej. Wy-
krycie receptora dla lipoproteiny LDL i szlaku przemian metabolicznych
cholesterolu w komórce przyniosło profesorom Goldsteinowi i Brownowi
Nagrodę Nobla w dziedzinie medycyny w roku 1985. Ich zasługą było także
zbadanie akumulacji cholesterolu w ścianie naczyniowej, która zachodzi
w makrofagach posiadających tzw. scavenger receptor (wymiatający) dla
zmodyfikowanych biologicznie LDL. Natomiast Henriksen i Steinberg
stwierdzili, że w wyniku wzajemnej interakcji komórek ściany naczyniowej
i LDL dochodzi do utlenienia tej frakcji, która dopiero wtedy staje się ligan-
dem dla makrofagów, posiadających zdolność gromadzenia lipidów i two-
rzenia komórek piankowatych będących podstawą wczesnych zmian miaż-
dżycowych.
Niestety, często popełnianym błędem jest niedostrzeganie nurtu badań nad
patofizjologią śródbłonka naczyniowego, a przecież jego wpływ na rozwój
miażdżycy trudno przecenić. Stąd chciałbym przypomnieć wyróżnione Na-
grodą Nobla badania J. Vane'a, z którym współpracował R. Gryglewski. Zba-
27

dali oni istotę interakcji pomiędzy płytkami krwi a ścianą naczynia, co dopro-
wadziło do wykrycia prostacykliny i tromboksanu. Należy również wspomnieć
Furchgotta i Zawadzkiego, którzy stwierdzili istnienie czynnika pochodzenia
śródbłonkowego – „relaksującego” ścianę naczyniową (EDRF). Wkrótce po-
tem wykazano, że w istocie jest to tlenek azotu (NO) syntetyzowany zarówno
w ścianie naczyniowej, jak i płytkach krwi z L-argininy.
Tak oto wydawało się, że byliśmy stosunkowo blisko zamknięcia historii
badań nad miażdżycą i rozwiązania problemów związanych z jej zapobiega-
niem i leczeniem. Niestety tak się nie stało, gdyż powstały zupełnie nowe za-
gadnienia, jak np. restenoza naczyniowa po zabiegach PTCA, zamykanie się
pomostów aortalno-wieńcowych po operacjach kardiochirurgicznych, czy
niemożność zahamowania progresji miażdżycy przeciętnie u ponad 40% pa-
cjentów, pomimo stosowanych zabiegów leczniczych. Ten katalog powyż-
szych problemów wymaga więc nowych badań zarówno podstawowych, jak
i klinicznych.
Na ich podstawie wiemy już dzisiaj, że niezbędnym elementem inicjują-
cym proces aterogenezy jest zarówno uszkodzenie śródbłonka tętnic, jak
i biologiczna modyfikacja cząstek LDL zawierających cholesterol. Jednak-
że omawiając najnowsze osiągnięcia w zakresie molekularnych podstaw
miażdżycy nie należy odbiegać od realiów związanych z poszczególnymi eta-
pami jej rozwoju.
I tak, według popularnego podziału zaproponowanego przez Stary’ego roz-
różniamy obecnie VI typów zmian naczyniowych, z których typ I – initial le-
sion (zmiana początkowa) i typ II – fatty streak (pasmo tłuszczowe) dają pod-
stawę do rozpoznania wczesnych zmian miażdżycowych, charakteryzujących
się obecnością obładowanych lipidami komórek piankowatych w błonie we-
wnętrznej naczynia. Obecność tych wczesnych zmian wykazuje się autopsyj-
nie w naczyniach wieńcowych u prawie 45% noworodków, z tym że mają one
tendencję do późniejszego zanikania. Natomiast typ II jest już rozpoznawal-
ny u większości dzieci pomiędzy 2. a 15. rokiem życia, głównie w łuku aorty
i w miejscach szczególnie podatnych na rozwój miażdżycy, tj. w obrębie roz-
gałęzień naczyń tętniczych.
Za niezwykle istotną z punktu widzenia wczesnej profilaktyki chorób ukła-
du krążenia, należy uznać obserwację wskazującą, że zmiany typu II poja-
wiające się w ekscentrycznie pogrubiałej błonie wewnętrznej naczyń mogą
ulegać zarówno progresji – tzw. typ IIa, jak i zahamowaniu – tj. typ IIb.
Czynnikiem, który decyduje o dalszym przebiegu zmian miażdżycowych jest
przewlekły stan zapalny śródbłonka. Stan ten indukowany jest przez nad-
miar krążących lipoprotein, ale także przez wysoki poziom homocysteiny,
28

angiotensyny II, tlenkowej hemoglobiny. Ta ostatnia jest następstwem pale-
nia tytoniu, czy też toksycznych lipidowych nadtlenków pochodzących z utle-
nionych kwasów tłuszczowych, powstających w przetworzonej termicznie
żywności. Dodatkowym czynnikiem nasilającym stan zapalny mogą być wiru-
sy, szczególnie typu Herpes oraz bakterie, np. Chlamydia pneumoniae, któ-
rych obecność w ścianie naczynia stwierdza się coraz częściej u pacjentów
operowanych z powodu niedrożności naczyń wieńcowych.
Konsekwencją przewlekłego lokalnego stanu zapalnego jest aktywacja ko-
mórek śródbłonka i następowa adhezja mononuklearnych leukocytów, tj.
limfocytów T i monocytów. Jest to proces złożony i wynika z pobudzenia
i zwiększenia ekspresji specyficznych genów odpowiedzialnych za produk-
cję błonowych glikoprotein, tj. selektyny E, immunoglobuliny ICAM-1 i gli-
koproteiny VCAM-1. Obecność tych cząstek adhezyjnych stwierdza się we
wczesnych stadiach miażdżycy zarówno u ludzi, jak i u zwierząt doświadczal-
nych, którym podaje się dietę wzbogaconą w cholesterol. Wiadomo już tak-
że, że bezpośrednim czynnikiem aktywującym produkcję adhezyn przez
śródbłonek jest czynnik martwicy guza (TNF-
a) i interleukina-1b (IL-1b),
a więc swoiste mediatory odpowiedzi zapalnej i immunologicznej. Rolę
TNF-
a jako stymulatora rozwoju miażdżycy u ludzi potwierdzono obecnie
w badaniach klinicznych, obserwując jej zwiększoną produkcję u pacjentów
z zaostrzoną chorobą niedokrwienną serca. Podobne obserwacje dotyczą
IL-1
b, która indukuje komórki śródbłonka do syntezy białek macierzy po-
zakomórkowej, zwiększa przepuszczalność naczyń oraz ich właściwości pro-
trombotyczne.
Mając zarysowany obraz czynników indukujących stan zapalny śródbłonka,
prześledzimy obecnie poszczególne fazy tworzenia się wczesnych zmian,
szczególnie z punktu widzenia powstania komórek piankowatych. I tak,
w wyniku pobudzenia komórek śródbłonka, wzrasta wielokrotnie ich prze-
puszczalność i może dochodzić do nadmiernego gromadzenia się lipoprote-
in LDL i Lp (a) w przestrzeni podśródbłonkowej, gdzie są wiązane przez ich
nośnik białkowy, tj. apolipoproteinę B (apo B) z proteoglikanami macierzy.
Wprawdzie ten proces zapobiega przechodzeniu lipoprotein do głębszych
warstw naczynia, ale powoduje, że ich retencja przedłuża się z 6-7 godzin
(jak to jest w normalnym naczyniu) do nawet 7 dni w miejscu miażdżycowo
zmienionym. To z kolei naraża wspomniane klasy lipoprotein na działania
różnych czynników aktywnych biologicznie, z których na czoło wysuwają się
wolne rodniki tlenowe, enzymy proteolityczne, a także podwyższone stężenie
glukozy i homocysteiny. Jednak do najlepiej poznanych modyfikacji biolo-
gicznych LDL, jak i Lp (a) należy proces ich utleniania poprzez komórki
ściany naczynia, a także przez napływowe monocyty-makrofagi. Powstają
29

wtedy wysoce aterogenne cząsteczki lipoprotein, których obecność we
wszystkich stadiach miażdżycy obserwowano w badaniach post mortem
i ex-vivo.
Wiemy już obecnie, że oksydacja LDL przebiega stopniowo, i że naj-
pierw powstają tzw. minimalnie zmodyfikowane cząsteczki MM-LDL, któ-
re są jednak już bardzo aktywne promiażdżycowo. Stwierdzono bowiem,
że MM-LDL powodują wzrost stężenia cAMP w komórkach śródbłonka,
co świadczy o ich pobudzeniu i skutkuje uwalnianiem czynnika chemotok-
sycznego monocytów (MCP-1), czynnika stymulującego kolonie makrofa-
gów (M-CSF), a także szeregu innych selektyn i chemokinin. To w konse-
kwencji prowadzi do napływu nowej generacji monocytów do ściany
naczynia oraz ich następowego przenikania i gromadzenia pod warstwą
śródbłonka. Tak duża koncentracja komórek stanu zapalnego powstająca
lokalnie w naczyniu, skutkuje silnie zaznaczonym stresem oksydacyjnym,
któremu nie jest w stanie przeciwdziałać zarówno obecność umieszczonych
pozakomórkowo enzymów antyoksydacyjnych (np. dysmutazy ponadtlen-
kowej), jak i naturalnych antyoksydantów będących częścią składową fazy
lipidowej LDL i Lp (a), tj. witaminy E, koenzymu Q10 i karotenoidów. To
właśnie stopniowe, trwające nawet kilka dni, wyczerpywanie się zasobów
wspomnianych antyoksydantów w tych lipoproteinach, prowadzi do całko-
witego wolnorodnikowego utleniania wielonienasyconych kwasów tłusz-
czowych, będących częścią składową ich lipidów, tj. fosfolipidów i estrów
cholesterolu. Powstające z nich cytotoksyczne aldehydy modyfikują apo-
-B-LDL, co z kolei całkowicie hamuje komórkową degradację tej frakcji
na drodze fizjologicznego receptora. Natomiast tak zmodyfikowana frakcja
LDL (ox-LDL) zaczyna być aktywnie pobierana poprzez receptory tzw.
wymiatające (scavenger) i/lub na drodze fagocytozy, głównie poprzez mo-
nocyty i makrofagi. To one bowiem są odpowiedzialne za usuwanie ze ścia-
ny naczynia wszelkich produktów apoptozy komórkowej, ale także i pato-
logicznie zmienionych lipoprotein. Niestety jednak w przypadku procesu
aterogenezy, makrofagi przyswajając nadmiar ox-LDL tracą swoją mobil-
ność i stają się integralną częścią ściany naczynia, transformując się do tzw.
komórek piankowatych, zawierających w cytoplazmie charakterystyczne
złogi estrów cholesterolu.
W następnej fazie procesu miażdżycowego często dochodzi do nekrozy
komórek piankowatych pod wpływem cytotoksycznych związków powstałych
w wyniku utleniania LDL, np. 7
a-hydroperoksycholesterolu, 7-ketocholeste-
rolu i 4-hydroksyneonalu. Prowadzi to do powstawania pozakomórkowego
rdzenia lipidowego charakteryzującego typ III i IV zmian miażdżycowych,
pojawiających się w czasie trzeciej dekady życia. Ponieważ te zmiany skut-
30

kują pogrubieniem ekscentrycznym ściany naczynia w kierunku przydanki,
to są one często niezauważalne i z reguły nie dają objawów klinicznych. Jed-
nak przy utrzymującym się przewlekle wysokim stężeniu lipidów w osoczu,
dochodzi do dalszej progresji tych zmian, a w szczególności do zmiany feno-
typu miocytów w ognisku miażdżycowym. Komórki te bowiem zaczynają
w stanie fazy syntetyzującej migrować w kierunku śródbłonka, gdzie są bar-
dziej podatne na czynniki proliferacyjne, np. na płytkowy czynnik wzrostu
PDGF. Zaobserwowano także, że miocyty syntetyzują zwiększone ilości
IL-1 i TNF-
a oraz kolagenu i elastyny. Ten proces prowadzi do generowania
typu Va zmian miażdżycowych, który cechuje się pojawieniem się blaszki
włóknistej – fibroatheroma, oraz lokalnej stenozy, rzadko jednak przekracza-
jącej 30-50% światła naczynia w IV dekadzie życia.
Jednak u osób posiadających kilka nakładających się na siebie czynni-
ków ryzyka, może dojść do destabilizacji blaszki miażdżycowej i jej pęknię-
cia na granicy z niezmienionym śródbłonkiem. Bezpośrednią przyczyną ta-
kiego powikłania jest przewlekły proces zapalny powiązany ze zwiększoną
ilością LDL w krążeniu, a w przypadku hipertrójglicerydemii lub hiperlipi-
demii mieszanej – także z retencją w osoczu tzw. remnantów (częściowo
zdegradowanych) chylomikronów i VLDL. Istotną obserwacją kliniczną
ostatnich lat było stwierdzenie, że w tego typu zaburzeniach lipidowych to-
warzyszących często oporności tkankowej na insulinę, tj. w otyłości, cukrzy-
cy typu 2 i zespole polimetabolicznym, występują wysoce aterogenne czą-
steczki LDL o odmiennej strukturze. Są one mniejsze, wzbogacone
w apoB i bardziej podatne na utlenianie, gdyż jak to wykazaliśmy w na-
szych badaniach, zawierają mniej witaminy E w fazie lipidowej. Coraz czę-
ściej wskazuje się także na fakt, że wysoki poziom homocysteiny może
przyśpieszać pękanie blaszki miażdżycowej i tworzenie zakrzepu na jej po-
wierzchni.
Nie ulega jednak dziś wątpliwości, że to obecność makrofagów i limfocy-
tów T w zmianach typu IV i V i uwalnianie z tych komórek enzymów prote-
olitycznych – metaloproteinaz, tj. kolagenazy i elastazy – jest bezpośrednią
przyczyną osłabienia struktury blaszki. Stwarza to bezpośrednie zagrożenie
tworzeniem się zakrzepu, gdyż w miejscu uszkodzenia obserwujemy zmniej-
szenie syntezy prostacykliny, inhibitorów układu krzepnięcia, np. antytrom-
biny III, kompleksu trombomodulina-białko C i tkankowego aktywatora pla-
zminogenu (t-PA). Dodatkowym czynnikiem, który może nasilać proces
trombogenezy jest podwyższony poziom fibrynogenu i Lp (a). Proces gwał-
townego wykrzepiania jest bezpośrednią przyczyną ostrych incydentów wień-
cowych, zawału serca i udaru mózgu. Wydaje się, że niezależnym stymula-
torem stanów prozakrzepowych może być także wzrost poziomu czynnika
31

tkankowego (TF) oraz czynnika VII w śródbłonku naczynia, bezpośrednio
stykającego się z pękniętą blaszką miażdżycową. Bowiem stres oksydacyjny
towarzyszący stale procesom progresji miażdżycy powoduje, że w komór-
kach śródbłonka dochodzi do aktywacji jądrowego czynnika transkrypcyjne-
go, tj. NF-KB, który z kolei pobudza ekspresję wielu genów odpowiedzial-
nych za protrombotyczne i antyfibrynolityczne właściwości tych komórek
i jest bezpośrednią przyczyną nasilonej ich apoptozy.
Można więc spróbować postawić hipotezę, że czynniki, które na poziomie
molekularnym hamują aktywację NF-KB, mogą również przeciwdziałać roz-
wojowi miażdżycy.
Ostatnio okazało się, że powszechnie obecnie stosowane statyny, oprócz
swojego, tzw. lipidowego punktu uchwytu, mogą poprzez kilka różnych me-
chanizmów pleotropowych, tj. pierwotnie niezaplanowanych, wpływać po-
średnio na czynniki transkrypcyjne. Ta grupa leków bowiem, blokując syn-
tezę wewnątrzkomórkowego cholesterolu poprzez wpływ na aktywność
reduktazy HMG-CoA, oddziałuje również na system prenylacji i farnelizacji
białek sygnalnych G, takich jak p21Rac, Ras i Rho. Kontrolują one zarówno
funkcję wielu błonowych receptorów komórkowych, jak i aktywność enzy-
mów, w tym na przykład oksydazy NADPH, która jest odpowiedzialna za
produkcję jonów ponadtlenkowych, biorących udział w procesie utleniania
LDL przez komórki ściany naczynia i to z kolei może wpływać na poziom
NF-KB w komórkach śródbłonka.
We wspólnych, pionierskich badaniach z grupą prof. J. Davignona z Mont-
realu wykazałem, że simwastatyna w stężeniu adekwatnym do obserwowa-
nego we krwi ludzi leczonych tym lekiem, skutecznie obniża oksydację LDL
przez pobudzone monocyty-makrofagi in vitro. Było to bezpośrednio związa-
ne ze zmniejszoną prenylacją białka G. Nasze obserwacje zostały potwier-
dzone kilka lat później w eksperymentach in vivo, gdzie wykazano, że lipofil-
ne statyny mogą hamować aktywność oksydazy NADPH.
Inny ciekawy mechanizm antyoksydacyjnego działania ma atorwastatyna.
Między innymi grupa prof. Avirama z Hajfy wykazała, że metabolity ator-
wastatyny mają wysoką aktywność w bezpośrednim wychwytywaniu wolnych
rodników tlenowych, co ma istotny wpływ na stopień oksydacji LDL przez
makrofagi. Prawdopodobnie dodatkowym efektem antyoksydacyjnego dzia-
łania statyn, jest ich wpływ odtwarzający zdolności rozkurczowe śródbłonka
naczyniowego. Wykazano bowiem, że atorwastatyna i simwastatyna podwyż-
szają aktywności syntazy tlenku azotu w warunkach in vitro nawet wtedy, gdy
komórki śródbłonka były wcześniej inkubowane z ox-LDL. Ten sam efekt
relaksacyjny statyn wykazano także w bezpośrednich badaniach klinicznych
32

i jest on obserwowany nawet po miesiącu przyjmowania leków i to w najniż-
szych ze stosowanych powszechnie dawek.
Coraz częściej wspomina się również, że przeciwmiażdżycowe, pleotropo-
we działanie statyn, szczególnie litofilnych, tj. lowastatyny, simwastatyny
i atorwastatyny jest związane z hamowaniem procesu proliferacji komórek
mięśni gładkich. Jednak trzeba stwierdzić, że przy użyciu tej grupy leków nie
udało się zahamować procesu restenozy naczyniowej po zabiegach angio-
plastyki wieńcowej.
Nie ulega jednak wątpliwości, że statyny mogą hamować procesy zapalne
w blaszce miażdżycowej, co między innymi wykazano wielokrotnie w bada-
niach klinicznych nad prawastatyną. Ta jedyna statyna rozpuszczalna w śro-
dowisku wodnym jest bardzo skuteczna w obniżaniu poziomu fibrynogenu
i białka CRP, co może mieć związek z wpływem prawastatyny na syntezę in-
terleukiny-6 w wątrobie, a więc w organie, gdzie ten lek jest praktycznie cał-
kowicie katabolizowany.
Wymierne z punktu widzenia klinicznego są również wyniki wpływu pra-
wastatyny na zmniejszenie ilości odrzutów po transplantacji serca.
Dla środowiska kardiologów inwazyjnych, najważniejszym z mechanizmów
pleotropowego działania statyn jest ich wpływ na stabilizację blaszki miaż-
dżycowej i przeciwdziałanie tworzeniu się zakrzepu na śródbłonku naczyń.
Jak już wspomniano, głównym czynnikiem destabilizacji płytki miażdżyco-
wej jest w niej obecność makrofagów, które produkując kolagenazy i elasta-
zy powodują osłabienie struktury blaszki, co grozi jej pękaniem.
Na destabilizację płytki miażdżycowej i na tzw. nagłą śmierć sercową mo-
że wpływać także podwyższony poziom homocysteiny we krwi.
Po raz pierwszy, aterogenne działanie homocysteiny wykryto u dzieci
z genetycznym niedoborem syntazy cystationowej lub reduktazy mety-
loczterohydrofolianowej. Typowe zmiany miażdżycowe rozwijają się
u nich nie tylko w naczyniach wieńcowych, ale także w nerkowych, mó-
zgowych i obwodowych. Można więc mówić o stadium uogólnionej miaż-
dżycy i to z wyraźnie zaznaczonymi zaburzeniami w układzie krzepnię-
cia. Jeśli natomiast chodzi o populację ogólną, to do wzrostu stężenia
homocysteiny we krwi może dochodzić w wyniku nadmiernego spożycia
w diecie mięsa i jego przetworów będących źródłem metioniny. Towarzy-
szy temu z reguły niedobór witamin grupy B, a w szczególności B
6
i B
12
oraz kwasu foliowego, wpływających na katabolizm homocysteiny po-
przez jej konwersję do cystationiny. Uważa się obecnie, że homocysteina
ma zdolność uszkadzania śródbłonka naczyniowego, a także zwiększania
33

degradacji elastyny w błonie wewnętrznej, co przyspiesza procesy włók-
nienia i kalcyfikacji.
Badania własne wykazały także, że tiolakton homocysteiny ma zdolność
modyfikacji lipoprotein poprzez przyłączanie się do wolnych grup lizyno-
wych apolipoproteiny B, co powoduje zwiększoną agregację cząsteczek
LDL. Bezpośrednich dowodów na aterogenne działania homocysteiny do-
starczają nam jednak głównie badania prospektywne. I tak w jednym z nich
stwierdzono, że wśród 15 tysięcy mężczyzn-lekarzy, wykryte przypadki hiper-
homocysteinemii wiązały się z trzykrotnym wzrostem ryzyka zawału serca.
Również przyspieszony rozwój miażdżycy u chorych z przewlekłą niewydol-
nością nerek może mieć związek z przewlekłym podwyższeniem homocy-
steiny we krwi tych ludzi.
Podsumowując należy stwierdzić, że stopień progresji miażdżycy induko-
wanej czy to przez cholesterol, czy też przez homocysteinę – ulega swoistej
regulacji poprzez fizjologiczny proces ochronny związany ze zwrotnym trans-
portem cholesterolu do wątroby poprzez frakcje HDL.
Omawiając, z konieczności w sposób skrótowy, zwrotny transport chole-
sterolu z tkanek obwodowych do wątroby należy wskazać, że jest on regulo-
wany poprzez ekspresję genu odpowiedzialnego za syntezę białka nośniko-
wego, tj. apolipoproteiny A-I. To bowiem dzięki temu nośnikowi i wysokiej
zawartości fosfolipidów, frakcja HDL ma zdolność pobierania z cytoplazmy,
czy też z błony komórkowej makrofagów i/lub komórek mięśni gładkich nad-
miaru cholesterolu, aby po jego estryfikacji za pomocą enzymu lecytynowo-
-cholesterolowej transferazy kwasów tłuszczowych (LCAT) przekazać go wą-
trobie lub włączyć do wtórnego obiegu w lipoproteinach VLDL i LDL.
Wykazano już, że niska ekspresja genu regulującego syntezę apo A-I jest ści-
śle powiązana z niską aktywnością enzymu lipazy lipoproteinowej, co z kolei
wiąże się z hipertrójglicerydemią i/lub upośledzeniem katabolizmu chylomi-
kronów podczas lipemii pokarmowej. Jest przy tym faktem powszechnie zna-
nym, że większa część pacjentów z chorobą niedokrwienną serca i z ewident-
ną normolipemią, podczas obciążenia tłuszczem egzogennym wykazuje ich
upośledzoną eliminację z krążenia. Za ten stan w wielu przypadkach odpo-
wiedzialna może być mutacja genu zawiadującego nie tylko syntezą lipazy,
ale także jej katalityczną aktywnością. W tych wcale nierzadkich przypad-
kach możliwość interwencji ogranicza się tylko do eliminacji innych czynni-
ków ryzyka, np. wysokich LDL, jednakże często w populacji, za spadek po-
ziomu HDL odpowiada niska aktywność fizyczna i otyłość, palenie tytoniu,
a także niektóre leki z grupy
b-adrenolityków. Należy w tym miejscu wspo-
mnieć, że umiarkowane picie alkoholu, tj. poniżej 23 g dziennie może zwięk-
34

szyć syntezę HDL, ale wyłącznie u ludzi zdrowych, bez tendencji do hiper-
trójglicerydemii środowiskowej.
Nie ulega dziś już żadnej wątpliwości, że niski poziom HDL podnoszą naj-
efektywniej leki z grupy fibratów i kwas nikotynowy. I tak z badań klinicz-
nych wynika, że wzrost stężenia cholesterolu HDL o 6% powoduje spadek
śmiertelności z powodu choroby niedokrwiennej serca o 21%.
Wymiernym wynikiem postępu badań nad patogenezą miażdżycy jest zna-
czący spadek umieralności na chorobę niedokrwienną serca w USA, Kana-
dzie, a także w wielu państwach Europy Zachodniej. Z pewnością niemały
wpływ na te korzystne zmiany miał jakościowy postęp w opiece kardiologicz-
nej, w tym rozwój metod inwazyjnych, jak przezskórna angioplastyka, pomo-
stowanie naczyń wieńcowych oraz nowe generacje leków trombolitycznych.
Nie można jednak ignorować faktu, że towarzyszyła temu pozytywna zmiana
w stylu życia zachodnich populacji, a więc drastyczne ograniczenie palenia
tytoniu i odwrót od przyzwyczajeń żywieniowych, a szczególnie zastąpienie
tłuszczów pochodzenia zwierzęcego tłuszczami roślinnymi. Podobne tenden-
cje obserwujemy od dwóch lat w naszym kraju, który wraz z innymi krajami
Europy Środkowej na początku lat dziewięćdziesiątych zajmował czołowe
miejsce na świecie, jeśli chodzi o epidemię chorób układu krążenia, bo prze-
cież nie chodzi tu tylko o zawały serca, ale także o udary mózgu. Jednak ze
względu na bardzo ograniczone nakłady na naszą służbę zdrowia, trzeba po-
ważnie zastanowić się nad taktyką walki z miażdżycą w Polsce. Najbardziej
realne wydaje się wyłonienie osób tzw. grupy wysokiego ryzyka oraz wdroże-
nie wśród nich aktywnych metod wczesnej profilaktyki, nie wyłączając z niej
dzieci w wieku szkolnym. Bowiem z wielu badań wynika, że najbliższe po-
tomstwo ludzi, u których wystąpiły objawy ChNS przed 55. rokiem życia, po-
siada często więcej niż jeden genetyczny czynnik ryzyka miażdżycy, który ob-
jawia się z reguły pomiędzy 7. a 11. rokiem życia. Jeśli więc u członków rodzin
„wysokiego ryzyka” stwierdzimy genetycznie uwarunkowaną heterozygotycz-
ną formę hipercholesterolemii lub wysoki poziom apoB i Lp(a), mutację ge-
nu konwertującego angiotensynę albo genu odpowiedzialnego za lipazę li-
poproteinową, należy wówczas zrobić wszystko co możliwe, aby właśnie
u tych osób ograniczyć inne potencjalne czynniki ryzyka pochodzenia śro-
dowiskowego. Jest to bowiem w pełni możliwe przy odpowiedniej motywacji
i wiedzy, o czym świadczą doświadczenia z Finlandii. Natomiast stosowanie
metod z zakresu inżynierii genetycznej, jako niezwykle kosztowne i obcią-
żone wciąż brakiem wystarczającej wiedzy na temat konsekwencji takiego
postępowania w dalszej przyszłości, należy pozostawić do dyspozycji dla wy-
jątkowo rzadkich przypadków homozygotycznych defektów. Jest jednak fak-
tem godnym odnotowania, że pierwsze doświadczenia w zakresie wprowa-
35

dzenia do organizmu ludzkiego genu odpowiedzialnego za aktywność recep-
tora LDL mamy już za sobą i otuchą napawają nas wyniki wskazujące, że
dzięki temu w rodzinnej hipercholesterolemii udało się efektywnie obniżyć
stężenie cholesterolu.
Podsumowując należy stwierdzić, że dla populacji ogólnej najlepszym
i najtańszym środkiem walki z miażdżycą pozostanie jeszcze na długie lata
prawidłowa dieta – najlepiej typu śródziemnomorskiego, aktywność fizyczna
i umiejętność pokonywania stresu związanego z dniem codziennym.
Zapamiętaj!
1. Miażdżyca jest procesem wieloczynnikowym. Zwrócili już na to uwagę wy-
bitni badacze XIX wieku – Von Rokitanski i Virchow.
2. Zasadniczą rolę w patogenezie miażdżycy odgrywa proces zapalny induko-
wany przez lipidy. Opinię taką przedstawił Virchow przed 150 laty – jest ona
ciągle aktualna.
3. Ważnym nurtem poszukiwań patogenetycznych były i są badania nad funk-
cją i dysfunkcją śródbłonka naczyniowego – odkrycia z tego zakresu uho-
norowano Nagrodą Nobla (tlenek azotu – EDRF – NO).
4. Wiemy już dzisiaj, że niezbędnym elementem inicjującym proces ateroge-
nezy jest zarówno uszkodzenie śródbłonka tętnic, jak i biologiczna modyfi-
kacja cząstek LDL zawierających cholesterol.
5. Czynnikiem, który decyduje o dalszym przebiegu zmian miażdżycowych jest
przewlekły stan zapalny śródbłonka indukowany zarówno przez nadmiar
krążących lipoprotein, jak i przez wysoki poziom homocysteiny, angiotensy-
ny II, tlenkowej hemoglobiny, będącej następstwem palenia tytoniu czy też
toksycznych lipidowych nadtlenków.
6. Dodatkowym czynnikiem nasilającym stan zapalny mogą być wirusy, szcze-
gólnie typu Herpes oraz bakterie np. Chlamydia pneumoniae.
7. Konsekwencją przewlekłego lokalnego stanu zapalnego jest aktywacja ko-
mórek śródbłonka i następowa adhezja mononuklearnych leukocytów, tj.
limfocytów T i monocytów. W łańcuchu patogenetycznym udział biorą na
różnym etapie różne związki, cząsteczki, substancje (selektyny E, immu-
noglobuliny ICAM-1 i glikoproteiny VCAM-1, czynnik martwicy guza –
TNF-
a i interleukina-1b – IL-1b).
8. Dysponujemy dziś silną bronią przeciwmiażdżycową (statyny, fibraty), wyko-
rzystując nie tylko lipidowe, ale także pleotropowe mechanizmy ich działania
(przeciwzapalne, przeciwzakrzepowe, antyproliferacyjne, antyoksydacyjne itd.).
36

9. Najsilniejszą bronią jest jednak odpowiedni styl życia – odpowiednia dieta,
aktywność fizyczna, radzenie sobie ze stresem. Skuteczna modyfikacja tych
elementów, to wyzwanie dla kardiologii XXI wieku.
Warto przeczytać:
B. Thurberg, T. Collins: The nuclear factor-kappa B/inhibitor of kappa B
autoregulatory system and atherosclerosis. Curr Opin Lipidiol 1998; 9: 387-
396.
M. de Lorgeril, P. Salen, J. L. Martin i wsp.: Mediterranean diet, traditio-
nal risk factors and the rate of cardiovascular complications after myocardial
infarction: final report of the Lyon Diet Heart Study. Circulation 1999; 99:
779-785.
S. M. Grundy, T. Bazzarre, J. Cleeman i wsp.: Prevention Conference V:
beyond secondary prevention: identifying the high-risk patient for primary pre-
vention: medical office assessment: Writing Group I. Circulation 2000; 101:
E3-E11.
R. Ross: Atherosclerosis: an inflammatory disease. N Engl J Med 1999; 340:
115-136.
L. Robbie, P. Libby: Inflammation and atherothrombosis. Ann N Y Acad
Sci 2001; 947: 147-179.
P. Libby, Y. J. Geng, M. Aikawa i wsp.: Macrophages and atherosclerotic
plaque stability. Curr Opin Lipidol 1996; 7: 330-335.
A. von Eckardstein, J. R. Nofer, G. Assmann: High density lipoprotein and
arteriosclerosis. Role of cholesterol efflux and reverse cholesterol transport.
Arterioscler Thromb Vasc Biol 2001; 21: 13-27.
M. Takemoto, J. K. Liao: Pleiotropic effects of 3-hydroxy-3methylglutaryl co-
enzyme a reductase inhibitors. Arterioscler Thromb Vasc Biol 2001; 21:
1712-1719.
H. B. Rubins, S. J. Robins, D. Collins i wsp.: Gemfibrozil for the secondary
prevention of coronary heart disease in men with low levels of high-density li-
poprotein cholesterol: Veterans Affairs High-Density Lipoprotein Cholesterol
Intervention Trial Study Group. N Engl J Med 1999; 341: 410-418.
37

III.
EPIDEMIOLOGIA CHOROBY NIEDOKRWIENNEJ
SERCA
Andrzej Światowiec, Patryk Krzyżak
Współczesna epidemiologia jest nauką zajmującą się badaniem czynników
związanych z występowaniem i rozprzestrzenianiem się chorób i stanów pa-
tologicznych oraz zapobieganiem i zwalczaniem tych zjawisk.
Epidemiologia chorób układu krążenia rozwinęła się w ostatnim pięćdzie-
sięcioleciu, a choroba niedokrwienna serca (ChNS) była początkowo po-
strzegana jako choroba ludzi zamożnych. Obecnie dominuje pogląd, że wy-
stępowanie ChNS uzależnione jest przede wszystkim od trzech czynników:
żywienia, palenia papierosów oraz związanych z warunkami ekonomiczny-
mi. Jest faktem, że choroba ta staje się główną przyczyną zgonów w krajach
rozwijających się; w krajach bogatych występuje częściej wśród ludzi bied-
nych, a regres ChNS następuje głównie w grupie ludzi o wysokim standar-
dzie ekonomicznym.
Badania epidemiologiczne możemy podzielić na trzy zasadnicze rodzaje:
badania opisowe – oceniające aktualny stan zdrowia populacji na podstawie
przeprowadzanych badań przekrojowych, określających częstość występo-
wania chorób w danym społeczeństwie oraz ich zmienność w czasie, w wy-
niku przeprowadzanych badań długoterminowych określających zachoro-
walność, umieralność i śmiertelność w badanej populacji;
badania analityczne – będące próbą określenia czynników wpływających na
rozwój danej choroby oraz jej naturalny przebieg. Są to badania retrospek-
tywne poszukujące różnic w występowaniu czynników mogących wpływać na
rozwój choroby zarówno wśród osób chorych, jak i zdrowych oraz badania
prospektywne, śledzące zachorowalność w grupie osób zdrowych obarczo-
nych czynnikiem wpływającym prawdopodobnie na rozwój choroby. W ba-
daniu retrospektywnym najistotniejsza jest hipoteza, że częstość występowa-
nia danego czynnika chorobotwórczego będzie większa w populacji osób
chorych niż zdrowych. Z kolei w badaniu prospektywnym dominantą jest
czynnik chorobotwórczy (hipotetycznie zachorowalność będzie większa
w populacji osób obarczonych tym czynnikiem). Badanie retrospektywne jest
prostsze i tańsze, ale obarczone większym błędem. Ideałem badania anali-
tycznego jest badanie prospektywne, które jest jednak rozciągnięte w cza-
sie, a co za tym idzie wymaga dużego wysiłku organizacyjnego i jest kosz-
towne;
38
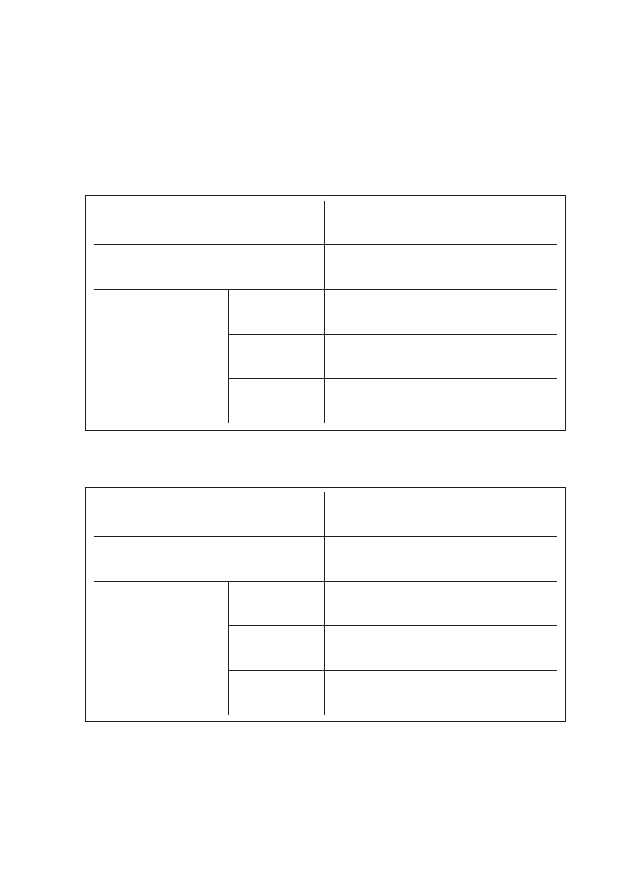
badania eksperymentalne – weryfikujące hipotezy o skuteczności podejmo-
wanych działań leczniczych i profilaktycznych.
Dla uporządkowania podstawowych pojęć opisujących wskaźniki epide-
miologiczne, przedstawiono je w kolejnych tabelach (tab. 1-4):
39
Tabela 1: Współczynniki opisujące chorobowość
CHOROBOWOŚĆ
WSPÓŁCZYNNIKI
/PRZYKŁADY
OGÓLNA
liczba chorych
/liczba ludności
SZCZEGÓŁOWA
wg wieku
liczba chorych <40 r.ż.
/liczba ludności <40 r.ż.
wg przyczyny
liczba chorych na X
/liczba ludności
wg płci
liczba chorych kobiet
/liczba kobiet
Tabela 2: Współczynniki opisujące zachorowalność (zapadalność)
ZACHOROWALNOŚĆ
WSPÓŁCZYNNIKI
/PRZYKŁADY
OGÓLNA
liczba chorych
/liczba ludności
SZCZEGÓŁOWA
wg wieku
liczba nowych zachorowań <40 r.ż.
/liczba ludności <40 r.ż.
wg przyczyny
liczba nowych zachorowań na
chorobę X/liczba ludności
wg płci
liczba nowych zachorowań kobiet
/liczba kobiet

Badania epidemiologiczne ChNS związane są przede wszystkim z Framin-
gham. Wśród mieszkańców tego niewielkiego miasteczka w pobliżu Bostonu,
w latach czterdziestych XX wieku podjęto pionierskie, długoterminowe ba-
dania mające na celu opisanie zachorowalności i umieralności na ChNS oraz
ustalenie przyczyn jej występowania. Wyniki tego badania określiły czynniki
ryzyka ChNS i miały kapitalny wpływ na dalsze prace badawcze na całym
świecie. Początkowo były to badania opisowe, ale już w latach sześćdziesią-
tych dominowały badania analityczne. Wyniki przeprowadzonych w tym cza-
sie badań prospektywnych ujawniły istotną rolę nikotyny, lipidów, diety, cu-
krzycy, otyłości, nadciśnienia tętniczego, alkoholu, braku aktywności
fizycznej w rozwoju ChNS. W latach siedemdziesiątych prowadzono już ba-
40
Tabela 3: Współczynniki opisujące umieralność
UMIERALNOŚĆ
WSPÓŁCZYNNIKI
/PRZYKŁADY
OGÓLNA
liczba zgonów/liczba ludności
SZCZEGÓŁOWA
wg wieku
liczba zgonów <40 r.ż.
/liczba ludności <40 r.ż.
wg przyczyny
liczba zgonów z powodu X
/liczba ludności
wg płci
liczba zgonów kobiet
/liczba kobiet
Tabela 4: Współczynniki opisujące śmiertelność
ŚMIERTELNOŚĆ
WSPÓŁCZYNNIKI
/PRZYKŁADY
OGÓLNA
liczba zgonów/liczba chorych
SZCZEGÓŁOWA
wg wieku
liczba zgonów <40 r.ż.
/liczba chorych <40 r.ż.
wg przyczyny
liczba zgonów z powodu X
/liczba chorych z powodu X
wg płci
liczba zgonów kobiet
/liczba chorych kobiet

dania eksperymentalne, których celem była ocena wpływu farmakoterapii
nadciśnienia tętniczego na częstość występowania jego powikłań (zawału
serca, udaru mózgu, nagłego zgonu, niewydolności serca i nerek), wpływu
prewencji na zachorowalność na ChNS oraz wpływu terapii na śmiertelność
w zawale serca i prewencję nagłego zgonu sercowego.
Umieralność z powodu ChNS jest wypadkową zachorowalności i śmiertel-
ności w przebiegu choroby. Zachorowalność na ChNS, w tym na zawał serca,
jest wynikiem wpływu czynników warunkujących rozwój miażdżycy tętnic
wieńcowych (czynników ryzyka). Śmiertelność jest uwarunkowana jakością
opieki medycznej.
Dzięki wdrożeniu narodowych programów prewencyjnych (modyfikacja
stylu życia, co wpływa bezpośrednio na czynniki ryzyka) i poprawie opieki
medycznej, początkowo w USA, a następnie w innych krajach, obserwuje się
spadek umieralności spowodowanej ChNS. Obserwowany w USA w latach
1968-75, spadek umieralności z powodu ChNS aż o 60% był wynikiem zmia-
ny stylu życia, a złożyło się na to głównie zmniejszenie palenia tytoniu, obni-
żenie przeciętnego poziomu cholesterolu całkowitego (dieta zwyczajowa)
oraz poprawa kontroli ciśnienia tętniczego. Pomimo że umieralność z po-
wodu ChNS zmniejsza się w większości uprzemysłowionych krajów świata
od połowy lat siedemdziesiątych, w Polsce wzrastała do 1991 roku i wzrost
ten należał do najwyższych w świecie (spośród krajów publikujących wiary-
godne dane wyprzedzały nas tylko Węgry). W latach 1970-1990 umieralność
z powodu ChNS w Polsce wśród populacji w wieku 35-64 lat wzrosła o 102%
u mężczyzn i o 160% u kobiet. Od 1990 roku obserwuje się w Polsce spadek
tej umieralności (w latach 1990-1996 o 25% u mężczyzn i 23% u kobiet),
niemniej w 1996 roku nadal była ona wyższa niż w roku 1970, a przeciętna
długość trwania życia w Polsce była niższa niż w większości krajów zachod-
nioeuropejskich o ok. 9 lat dla mężczyzn i 6 lat dla kobiet.
W 1996 roku, umieralność w Polsce z powodu chorób układu krążenia wy-
niosła 37% całkowitej umieralności mężczyzn w wieku 35-64 lat i odpowied-
nio 33% kobiet. Z tych danych wynika, że w Polsce, co trzeci zgon wśród po-
pulacji w wieku średnim, jest wynikiem chorób układu krążenia. Trzeba
w tym miejscu zaznaczyć, że niski odsetek badań autopsyjnych w Polsce
wpływa ujemnie na powyższe dane – uważa się, że umieralność spowodowa-
na chorobami układu krążenia jest w Polsce niedoszacowana.
Przez wiele lat zachorowalność i umieralność na zawał serca oceniana by-
ła w Polsce na podstawie rejestrów szpitalnych, co wynikało z błędnego zało-
żenia, iż wszyscy pacjenci z ostrym zawałem serca są hospitalizowani. Z da-
nych publikowanych na podstawie wieloletniej obserwacji w ramach
41

wielkiego międzynarodowego programu WHO MONICA wynika, że zacho-
rowania na zawał serca zakończone zgonem przed hospitalizacją (zgony
przedszpitalne) stanowią około 75% wszystkich zgonów z powodu zawału
serca w okresie 28 dni od zachorowania. Według danych pochodzących
z prowadzonego pod kierunkiem prof. Rywika programu Pol-MONICA (da-
ne z lat 1984-1994) zachorowalność na zawał serca wśród osób w wieku 35-
64 lata wynosi w Warszawie 628/100 tys. u mężczyzn i 242/100 tys. u kobiet.
Od roku 1990 notuje się spadek tej zachorowalności o 33% u obu płci.
W porównaniu z danymi międzynarodowymi (WHO MONICA) wartości te
należą do przeciętnych. Śmiertelność ogólna w zawale serca, w pierwszych
28 dniach od zachorowania, wynosiła w Warszawie (dla tej samej populacji)
41-45% u mężczyzn i 32-37% u kobiet, przy czym śmiertelność szpitalna
w zawale serca wynosiła 16% u mężczyzn i 12% u kobiet, a przedszpitalna
odpowiednio 35% i 23%. Podkreślenia wymaga fakt, iż u mężczyzn wykazy-
wała ona tendencję wzrostową. W porównaniu z danymi międzynarodowy-
mi, wartości te należą do ponadprzeciętnych. Tak wysoka śmiertelność
przedszpitalna w populacji Warszawy spowodowana była istotnym opóźnie-
niem hospitalizacji – w pierwszej godzinie zawału hospitalizowano zaledwie
12% chorych, natomiast po 24 godzinach od zachorowania aż 17%. Czas ho-
spitalizacji zależy zarówno od sprawności organizacyjnej służb medycznych,
jak i od świadomości (poziomu edukacji) chorego i jego rodziny.
Reasumując, w populacji polskiej notuje się raczej wysokie wartości współ-
czynników umieralności z powodu ChNS i zawału serca, pomimo zaobser-
wowanego spadku ich wartości w ostatnich latach (spośród krajów Europy
Centralnej i Wschodniej, spadek umieralności zanotowano jedynie w Polsce
i Czechach). Utrzymuje się nadumieralność mężczyzn w stosunku do kobiet.
Zachorowalność na zawał serca w Polsce szacuje się na ok. 100 tys. osób
rocznie.
Stopień zagrożenia ChNS (zachorowalność) w danej populacji wiąże się
z oceną czynników ryzyka i określeniem tzw. ryzyka globalnego. Jak wspo-
mniano wyżej, pojęcie czynnika ryzyka znane jest od czasów słynnego już ba-
dania populacyjnego w Framingham. Aktualnie w piśmiennictwie świato-
wym występuje 246 różnych czynników, które korelowały z wystąpieniem
ChNS (wg opracowania Hopkinsa i Williama z 1981 roku). Główne czynni-
ki ryzyka ChNS można obecnie uporządkować w trzech następujących gru-
pach (tab. 5):
42

Czynniki socjalne mają wpływ na nasze zachowania, a czynniki behawio-
ralne do pewnego stopnia wpływają na somatyczne. Opierając się na wielo-
letnich doświadczeniach z Framingham uznano, że czynniki ryzyka wpływają
na rozwój ChNS w każdym wieku i u obu płci, ale z różną siłą. Przykładowo
palenie papierosów wywiera bardziej niekorzystny wpływ u mężczyzn, a cu-
krzyca i niski poziom HDL-cholesterolu u kobiet, przy czym zaburzenia lipi-
dowe i nietolerancja glukozy zmniejszają swój wpływ wraz z wiekiem. Nato-
miast otyłość, nadciśnienie tętnicze i mała aktywność fizyczna mają wysoce
niekorzystny wpływ na rozwój ChNS w każdym wieku. Problem ten omówio-
no szeroko w rozdziale na temat prewencji pierwotnej.
PALENIE PAPIEROSÓW
W populacji Warszawy w 1993 roku (program Pol-MONICA), papierosy
paliło 50% mężczyzn i 33% kobiet. Spośród 40 populacji objętych progra-
mem WHO MONICA, odsetek palących mężczyzn w Polsce był najwyższy,
a kobiety ustępowały jedynie badanym populacjom w Danii i Islandii. Na
przykład na Litwie paliło papierosy tylko 4% kobiet. Ryzyko zgonu u osób
wypalających więcej niż 15 papierosów dziennie, w porównaniu z osobami
niepalącymi wzrasta u mężczyzn o 63%, a u kobiet o 75% (należy jednak pa-
miętać, że ryzyko dotyczy w tym przypadku nie tylko ChNS, ale i chorób
płuc, tętnic obwodowych i udarów mózgu).
43
Tabela 5: Czynniki ryzyka choroby niedokrwiennej serca
CZYNNIKI
SOCJALNE
CZYNNIKI
BEHAWIORALNE
CZYNNIKI
SOMATYCZNE
• poziom
wykształcenia;
• praca i stres
związany z pracą;
• aktywność fizyczna
w pracy;
• dochód;
• stan cywilny;
• zadowolenie
z kontaktów
społecznych i życia
rodzinnego.
• typ A zachowań;
• palenie papierosów;
• zwyczajowa dieta;
• spożycie alkoholu;
• aktywność fizyczna;
• zaburzenia snu.
• nadciśnienie
tętnicze;
• hiper-
cholesterolemia;
• otyłość;
• cukrzyca.

W roku 2002, w trakcie Kongresów Kardiologicznych, zostały przedsta-
wione badania Zdrojewskiego i wsp. NATPOL III PLUS (publikacje są w fa-
zie redakcyjnej, dane prezentujemy dzięki uprzejmości autorów projektu),
oceniające rozpowszechnienie głównych czynników ryzyka chorób sercowo-
-naczyniowych w Polsce. Jest to reprezentatywna próba dla populacji pol-
skiej w wieku 18-94 lat, przeprowadzona we współpracy z sopockim PBS,
z maksymalnym błędem statystycznym ± 2,0%. Zgodnie z przedstawionymi
w tym badaniu wynikami, osoby palące w naszym kraju stanowią aktualnie
33% populacji, a spośród 67% niepalących – 22% to byli palacze.
ZABURZENIA LIPIDOWE
Pożądane stężenie cholesterolu całkowitego wynosi < 200 mg%
(< 5,2 mmol/L). W roku 1993 w populacji Pol-MONICA, wartości takie
stwierdzano jedynie u 30% mężczyzn i 33% kobiet. Wśród osób z hipercho-
lesterolemią dominowało stężenie w przedziale 200-250 mg% (5,2-6,7
mmol/L), a więc tzw. hipercholesterolemia środowiskowa, będąca głównie
konsekwencją błędów w zwyczajowej diecie. Na tle populacji objętych pro-
gramem WHO MONICA odsetek znaczącej hipercholesterolemii był w Pol-
sce niewielki.
Z kolei średnie wartości HDL-cholesterolu były w populacji Pol-MONICA
dość duże: wartości niskie, tzn. < 39 mg% (< 1,0 mmol/L), stwierdzano
w 1993 roku u 11% mężczyzn i 4% kobiet. Na podstawie wieloletnich badań
oceniono, że ryzyko zgonu jest odwrotnie proporcjonalne do stwierdzanych
wartości HDL-cholesterolu i dla mężczyzn z wartościami < 45 mg%
(< 1,2 mmol/L), jest ono o 25% większe niż przy wartościach > 55 mg%
(>1,4 mmol/L). U kobiet różnica ryzyka zgonu pomiędzy wartościami
< 52 mg% (< 1,3 mmol/L), a > 62 mg% (> 1,6 mmol/L) wynosi aż 68%.
Reasumując, w badaniu Pol-MONICA odsetek populacji w średnim wieku
z zaburzeniami lipidowymi był dość wysoki, wynosił ok. 70% i w obserwacji
10-letniej nie wykazywał tendencji do poprawy. Hipercholesterolemia mie-
szana stanowiła ok. 30%, a dominowała czysta hipercholesterolemia. Czysta
hipertrójglicerydemia stanowiła bardzo niewielki odsetek całości zaburzeń
lipidowych.
Rozpowszechnienie poszczególnych rodzajów zaburzeń lipidowych w ba-
daniu NATPOL III PLUS przedstawiono w kolejnych tabelach (tab. 6, 7, 8,
9, 10).
44
45
Tabela 6: Hipercholesterolemia – rozkład w populacji wg płci (wg T. Zdrojewskiego)
Cholesterol
całkowity [mg%]
Kobiety
[%]
Mężczyźni
[%]
Ogółem
[%]
< 200
46,5
49,0
47,5
200-249
37,0
35,0
36,0
250-299
12,5
13,0
13,0
³ 300
4,0
3,0
3,5
Tabela 7: Rozpowszechnienie hipercholesterolemii wg grup wiekowych (wg T. Zdrojewskiego)
Cholesterol
całkowity
[mg%]
Wiek
18-30 lat
[%]
Wiek
31-44 lata
[%]
Wiek
45-64 lata
[%]
Wiek
>64 lat
[%]
< 200
74,5
51,0
32,5
30,0
200-249
20,5
37,0
43,5
44,0
250-259
3,0
10,0
19,0
19,5
³ 300
2,0
2,0
5,0
6,5
Tabela 9: HDL-cholesterol – rozkład w populacji wg płci (wg T. Zdrojewskiego)
Cholesterol
HDL [mg%]
Kobiety
[%]
Mężczyźni
[%]
Ogółem
[%]
³ 40
94,5
83,5
89,0
< 40
5,5
16,5
11,0
Tabela 8: LDL-cholesterol – rozkład w populacji wg płci (wg T. Zdrojewskiego)
Cholesterol LDL
[mg%]
Kobiety
[%]
Mężczyźni
[%]
Ogółem
[%]
< 115
43,0
43,0
43,0
115-134
21,5
21,0
21,5
³ 135
35,5
36,0
35,5
NADCIŚNIENIE TĘTNICZE
Jeden z najczęściej występujących i najgroźniejszych czynników ryzyka wy-
stąpienia nie tylko ChNS i zawału serca, ale również niewydolności serca
i nerek, udaru mózgu, tętniaka aorty i chorób tętnic obwodowych. Według
oszacowań amerykańskich, jeżeli ryzyko zgonu przy ciśnieniu skurczowym
równym 120 mm Hg przyjmie się za 1,0, to przy ciśnieniu 165 mm Hg ryzyko
wynosi już 1,94, natomiast przy ciśnieniu 195 mm Hg już 2,86.
W populacji Pol-MONICA (wiek 35-64 lat) w 1984 roku, częstość wystę-
powania nadciśnienia tętniczego wynosiła 39% u mężczyzn i 34% u kobiet
i do roku 1993 obniżyła się odpowiednio do 30% i 25%. Trzeba jednak pa-
miętać, że w tym samym okresie oszacowano, iż w populacji polskiej 46%
mężczyzn nie wiedziało o tym, że cierpi na nadciśnienie, 30% mężczyzn po-
mimo wiedzy o tym nie podjęło żadnego leczenia, a 20% podjęło nieskutecz-
ne leczenie. W 1993 roku, zaledwie 4% mężczyzn z nadciśnieniem tętniczym
miało właściwie kontrolowane ciśnienie. U kobiet odsetki te wynosiły odpo-
wiednio 31%, 24% i 36% – prawidłową kontrolę ciśnienia stwierdzano u 9%
kobiet.
Warto dodać, że nadciśnienie tętnicze najczęściej współistnieje z innymi
czynnikami ryzyka – otyłością, cukrzycą i hiperlipidemią. Jedynie u 15% cho-
rych na nadciśnienie nie stwierdza się innych czynników ryzyka.
W badaniu NATPOL III PLUS dokonano aktualnej oceny rozpowszech-
nienia nadciśnienia tętniczego w Polsce w 2002 roku.
46
Tabela 10: Trójglicerydy – rozkład w populacji wg płci (wg T. Zdrojewskiego)
Trójglicerydy
[mg%]
Kobiety
[%]
Mężczyźni
[%]
Ogółem
[%]
< 150
77,0
62,5
70,0
150-199
12,5
16,0
14,0
³ 200
10,5
21,5
16,0
Kryteria diagnostyczne:
Ciśnienie optymalne: <120/80 mm Hg – stwierdzono u 20%;
Ciśnienie prawidłowe <130/85 mm Hg – stwierdzono u 21%;
Ciśnienie wysokie prawidłowe: 130-139/85-89 mm Hg
– stwierdzono u 30%;
Nadciśnienie:
³ 140/90 mm Hg – stwierdzono u 29%.

Liczba dorosłych mieszkańców Polski wynosi 29 mln. Zgodnie z powyższy-
mi danymi na nadciśnienie tętnicze choruje w Polsce 8,4 mln osób, a zagro-
żonych nadciśnieniem (kategoria – wysokie prawidłowe) jest dalszych 8,7
mln osób.
Ocena skuteczności leczenia wypadła następująco:
Wobec powyższych danych interesujący jest fakt, że 62% badanych dekla-
ruje systematyczne przyjmowanie leków. Ciekawie też wygląda struktura
przyjmowanych leków hipotensyjnych w Polsce – okazuje się, że ACE-I
przyjmuje 59% chorych na nadciśnienie tętnicze, beta-adrenolityki 40% cho-
rych, antagonistów kanałów wapniowych 34%, diuretyki 24%, rezerpinę 2%
zaś inne leki 3%.
OTYŁOŚĆ
W badanej populacji Warszawy w latach 1984-93 (program Pol-MONICA),
u obu płci utrzymywał się wysoki odsetek osób z nadwagą (body mass index –
BMI > 25,0) – u mężczyzn wynosił 67%, a u kobiet 75%. Dane te dotyczą
osób w średnim wieku (35-64 lat). Otyłość – tzn. BMI
³ 30,0 – stwierdzano
u 20% mężczyzn i 29% kobiet. Jednocześnie zaczęto obserwować korzystne
zjawiska w sposobie odżywiania się naszego społeczeństwa, choć struktura
energetyczna diety nie ulegała znaczącym zmianom. Białko było dostarczy-
cielem 14% energii (przy zaleceniach WHO 10-15%), węglowodany 45-47%
energii (zalecenia WHO 55-75%, w tym cukrów prostych do 10%), a tłusz-
cze 39-41% energii (zalecenia WHO 15-30%, w tym z tłuszczów nasyconych
maks. 7-8%, a z wielonienasyconych maks. 3-7%). W Polsce odsetek tłusz-
czów nasyconych utrzymywał się jednak niezmiennie na wysokim poziomie
i wynosił 14-15%, a wielonienasyconych na poziomie 5-6%. Zmniejszyło się
też wyraźnie spożycie cholesterolu – u mężczyzn o 31% do poziomu 433 mg
dziennie (przy zaleceniach WHO do 300 mg), a u kobiet o 36% do pozio-
mu 284 mg dziennie. Ogólnie rzecz biorąc w obserwacji 10-letniej w Polsce,
dieta zwyczajowa zaczęła ulegać korzystnym przemianom – wskaźnik atero-
genności diety wg Keksa, obniżył się o 12-17%.
W badaniu NATPOL III PLUS (rok 2002) oceniano również rozpo-
wszechnienie nadwagi i otyłości w Polsce. Uzyskane dane wydają się po-
47
nadciśnienie tętnicze nie wykryte – 33%;
nadciśnienie wykryte, nie leczone – 10%;
nadciśnienie leczone nieskutecznie – 45%;
skutecznie leczone nadciśnienie tętnicze – 12%.
twierdzać obserwowane na początku lat dziewięćdziesiątych korzystne ten-
dencje. Wyniki przedstawiają się następująco (tab. 11):
Podsumowując, poziom czynników ryzyka w populacji polskiej należy oce-
nić jako wysoki, aczkolwiek w obserwacji wieloletniej obejmującej ostatnie
20-lecie, zaznaczają się korzystne tendencje wśród głównych czynników ryzy-
ka ChNS. Zmniejszenie częstości palenia tytoniu, korzystne zmiany w zwy-
czajowej diecie i zmniejszenie odsetka osób z nadwagą, lepsza wykrywalność
i kontrola nadciśnienia tętniczego, to wszystko zjawiska bardzo pozytywne.
Nie wyczerpują jednak całokształtu problemu, jako że do głównych czynni-
ków ryzyka omówionych powyżej należy zaliczyć cukrzycę (szeroko omówio-
no ten problem w innym rozdziale), ponadto brak aktywności fizycznej oraz
nie podlegający modyfikacji dodatni wywiad rodzinny. W ostatnich latach
do grupy czynników zagrożenia ChNS dołączyły nowe:
• nadreaktywność płytek krwi;
• wysoki poziom fibrynogenu i czynnika VII;
• podwyższony poziom alfa-lipoproteiny;
• insulinooporność;
• wzrost poziomu homocysteiny;
• zaburzenia genetyczne.
Walka o zmniejszenie zachorowalności i umieralności z powodu chorób
układu krążenia (w tym przede wszystkim ChNS/zawału serca) jest jak wi-
dać problemem niezwykle złożonym.
W USA w ciągu ostatnich 30 lat umieralność z powodu ChNS zmniejszyła
się o ponad 40%, a umieralność z powodu chorób mózgowo-naczyniowych
o 50%. Pomimo to choroby układu sercowo-naczyniowego są w USA przy-
czyną 42% wszystkich zgonów, co stanowi liczbę 925 tys. rocznie. Każdego
roku w USA notuje się 1,25 mln zawałów serca i 500 tys. zgonów tylko z po-
wodu ChNS (dane z 1998 roku).
48
Tabela 11: Rozpowszechnienie nadwagi i otyłości w Polsce wg badania NATPOL III PLUS (rok 2002)
BMI [kg/m
2
]
[%] populacji
NORMA
< 25,0
47
NADWAGA
25-30
34
OTYŁOŚĆ
> 30
19

Struktura zgonów w Polsce w latach 1990-2000 przedstawiała się następu-
jąco:
• choroby układu krążenia – 50%;
• choroby nowotworowe – 20%;
• zgony z innych przyczyn – 30%.
Wdrożone w wielu krajach kosztowne prace badawcze i ogólnonarodowe
programy profilaktyczne pozwoliły na ograniczenie wielu czynników ryzyka
i zmniejszenie zachorowalności, niemniej zmniejszenie umieralności z po-
wodu chorób układu krążenia pozostaje nadal jednym z największych wy-
zwań.
Zapamiętaj!
1. Zdecydowana większość czynników ryzyka ChNS poddaje się modyfikacji
i w ogromnym stopniu jest zależna od poziomu edukacji społeczeństwa.
2. Ogólna umieralność w przebiegu chorób układu krążenia jest wypadkową
zachorowalności i śmiertelności, głównie z powodu choroby niedokrwien-
nej serca i jej następstw.
3. Zachorowalność na ChNS modyfikujemy poprzez profilaktykę (ogranicza-
nie czynników ryzyka), a śmiertelność zmniejszamy usprawniając pracę
służb medycznych.
4. Liczba tzw. zgonów przedszpitalnych z powodu zawału serca od wielu lat
przewyższa liczbę zgonów wśród pacjentów hospitalizowanych z tego po-
wodu.
Warto przeczytać:
S. Rywik i wsp.: Epidemiologia chorób układu krążenia –
Program Pol-MONICA; Warszawa, Kardiologia Polska, 1996.
WHO MONICA Project (H. Tunstall-Pedoe i wsp.): Myocardial infarction
and coronary deaths in the World Health Organization MONICA Project. Re-
gistration procedure, event rates, case-fatality rates in 38 populations from 21
countries in four continents; Circulation, 1994.
M. Naruszewicz: 150 lat badań nad miażdżycą – stan obecny i perspektywy;
Polskie Archiwum Medycyny Wewnętrznej, 1997.
49

R. Kogel, M. Miller: Epidemiologia i profilaktyka choroby wieńcowej. Kar-
diologia Kliniczna – Program Samokształcenia ACC/AHA; 1997-98.
T. Zdrojewski i wsp.: Ocena rozpowszechnienia głównych czynników ryzyka
chorób sercowo-naczyniowych w Polsce – 2002 r.; Program NATPOL III
PLUS.
50

IV.
CHOROBA NIEDOKRWIENNA SERCA
– PODSTAWOWE MECHANIZMY I DEFINICJE.
IMPLIKACJE DLA LEKARZA PRAKTYKA
Mirosław Dłużniewski
Przyczyny choroby niedokrwiennej serca (ChNS) są złożone i pomimo wy-
raźnego postępu w rozumieniu patogenezy tej choroby i możliwości diagno-
stycznych, nie potrafimy wszystkiego wyjaśnić, a przede wszystkim przewi-
dzieć.
Przez lata patogeneza choroby niedokrwiennej wydawała się dla klinicy-
sty dość „łatwa” do wyobrażenia. Postępujące zmiany miażdżycowe w naczy-
niach wieńcowych, po przekroczeniu pewnego „progu”, jakim było zmniej-
szenie światła naczynia do 30-20-10%, w zależności od aktywności pacjenta
i zapotrzebowania serca na tlen, stawały się symptomatyczne, powodując
różne dolegliwości wieńcowe. Pacjent, a za nim jego lekarz wiedział, że ob-
ciążenie wysiłkiem w postaci wejścia na 2-3 piętro, przejścia określonego dy-
stansu – wywoływało ból wieńcowy. Taką postać anginy określano jako stabil-
ną chorobę wieńcową. Jeżeli dystans chromania wieńcowego się skracał,
zaczęły występować bóle spoczynkowe, to mówiliśmy o anginie niestabilnej, za-
wale zagrażającym. Skutkowało to odpowiednim postępowaniem, włączaniem
nowych leków, ale zdarzało się, że w okresie nasilenia dolegliwości dochodzi-
ło do pełnej martwicy mięśnia sercowego i rozpoznania zawału serca (ZS).
Od lat klinicyści mieli świadomość ułomności takiego rozumienia choroby
niedokrwiennej serca. Z tego powodu do kolejnych klasyfikacji postaci kli-
nicznych choroby wieńcowej dołączono ZS i nagły zgon sercowy (sudden car-
diac death – SCD). Potwierdzało to słabości rozumienia patogenezy ChNS,
bo jak prosto połączyć z jednej strony narastającą miażdżycę w naczyniach
i stopniowo nasilające się objawy kliniczne, a z drugiej strony ZS lub SCD
u osób z poczuciem pełnego zdrowia?!
Narastające doświadczenie wynikające z analizy angiogramów, wykonywa-
nych coraz częściej zarówno wśród młodszej, jak i starszej populacji, pozwo-
liło na dalszą analizę zmian w naczyniach. Okazało się, że proste rozumo-
wanie ze stopniowo narastającą miażdżycą, tak jak przedstawił to V. Fuster
na rycinie 1, nie wytrzymuje prostego przełożenia na „klinikę”.
51
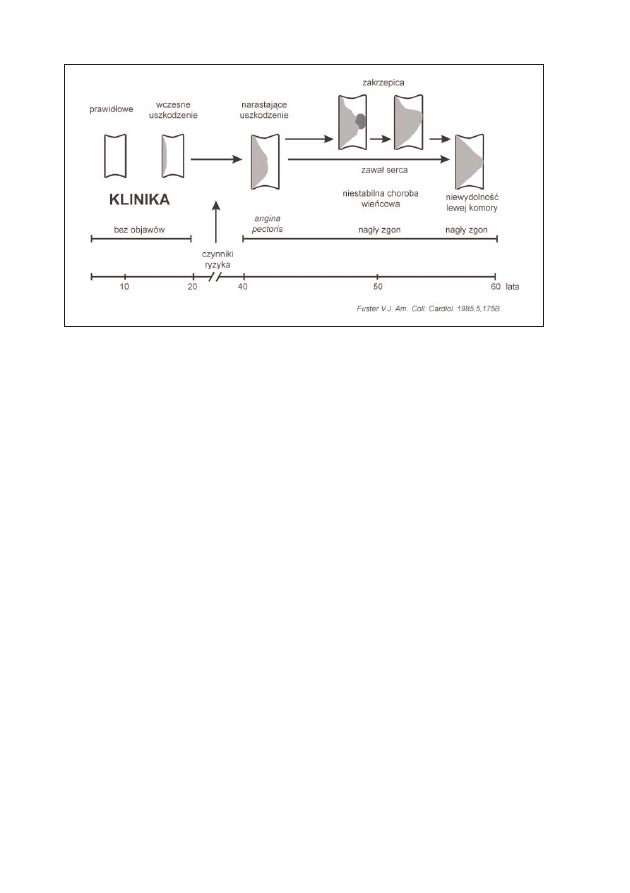
W grupie chorych z zawałem serca nie zawsze udaje się zidentyfikować
tętnicę odpowiedzialną za wystąpienie martwicy lub przeciwnie, stwierdza
się jedną jedyną zmianę krytycznie zwężającą lub zamykającą naczynie od-
powiedzialne za katastrofę wieńcową, co często trudno zrozumieć przy bra-
ku zmian w innych częściach drzewa wieńcowego.
Wśród chorych ze stabilną chorobą wieńcową, badania angiograficzne wy-
kazują niewielkie lub krytyczne zwężenia. U części pacjentów nierzadko ob-
serwuje się całkowite, nieme klinicznie zamknięcie naczynia, a u innych na-
tomiast, brak zmian miażdżycowych w nasierdziowych naczyniach
wieńcowych. W takich sytuacjach rozpoznajemy czasem – oceniając subiek-
tywnie przepływ kontrastu – tajemniczy zespół „X”.
Co zatem, pomimo tych wątpliwości, wiemy na dziś?
Zasadniczą przyczyną choroby wieńcowej jest miażdżyca tętnic wieńco-
wych – zmiany te rozwijają się prawdopodobnie już we wczesnym okresie ży-
cia. Zmiany miażdżycowe narastają w czasie, pod wpływem wielu czynników,
ale też mogą się cofać.
Rozwijające się zmiany w naczyniach wieńcowych zostały określone jako
blaszki miażdżycowe; ich liczba, stopień zaawansowania i zróżnicowania jest
przedmiotem rozległych badań i próbą wyjaśnienia wielu dotychczas niezro-
zumiałych zdarzeń klinicznych. Niestabilna blaszka miażdżycowa jest dziś
nie tylko celem badań, ale także celem interwencji metabolicznych i farma-
kologicznych. Rozwój blaszki, zarówno dla pacjenta, jak i jego lekarza, to
proces niezwykle podstępny i co gorsza, często niemy klinicznie.
52
Rycina 1: Miażdżycowe uszkodzenie tętnic wieńcowych

Mechanizmy kompensacyjne w czasie powstawania blaszki miażdżycowej
przeciwdziałają zwężeniu światła naczynia, poprzez przebudowę ściany na-
czyniowej (arterial remodeling). Proporcjonalnie do wzrostu blaszki miażdży-
cowej, ściana tętnicy poszerza się na zewnątrz, a narastająca blaszka nie
wgłębia się do światła naczynia, nie powoduje jej stenozy i może być niewi-
doczna w badaniu angiograficznym (dzieje się tak oczywiście do pewnego
momentu rozwoju blaszki). Z tego powodu badanie angiograficzne, chociaż
dalej najważniejsze w diagnostyce ChNS, pomału przestaje być złotym stan-
dardem. Ponadto staje się badaniem, które powinno raczej rozpoznawać
i pomóc zaplanować sposób leczenia ChNS, a nie fakt jej istnienia. Co to
znaczy dla lekarza praktyka? Spróbujmy w tym miejscu zastanowić się nad
prawdami – a może już tylko „mitami” kardiologii.
„ChNS MOŻNA ROZPOZNAĆ ZA POMOCĄ BADAŃ
NIEINWAZYJNYCH?!”
Otóż, już od dawna wiadomo, że żadne z badań diagnostycznych nie wy-
kryje rozwijającej się blaszki miażdżycowej, która mimo intensywnego roz-
woju nie zwęziła istotnie hemodynamicznie naczynia wieńcowego. Wszyst-
kie badania nieinwazyjne, nawet te dynamiczne – a tylko one się liczą – mają
swą czułość i specyficzność. Należy je wykonywać, ale o rozpoznaniu ChNS
powinna decydować suma informacji o chorych (ocena globalnego ryzyka),
a także wiedza i doświadczenie lekarza. Przy całym postępie wiedzy – jakże
to pozornie banalne – dalej ocena prawdopodobieństwa w oparciu na czyn-
nikach ryzyka i doświadczeniu klinicznym (nie książkowym) lekarza, decy-
duje o trafności decyzji diagnostycznych i terapeutycznych.
To czy klinicysta ma szansę wykryć objawy choroby wieńcowej, zależy tak-
że od stopnia zaawansowania i dynamiki rozwoju blaszki miażdżycowej. Nie-
istotne klinicznie zwężenie to takie, które nie powoduje żadnych dolegliwo-
ści, a badania nieinwazyjne nie pozwalają na jego wykrycie. Blaszka istotna
daje dolegliwości; im większe zwężenie, tym mniejszy wysiłek (obciążenie
serca) potrzebny do ich wywołania. Daje to szanse na wykrycie w rutyno-
wych badaniach diagnostycznych, takich jak: test wysiłkowy, perfuzja izoto-
powa, obciążenie dobutaminą. I wreszcie blaszka krytyczna, będąca często
przyczyną niestabilnej dusznicy bolesnej, rozpoznanie nie nasuwa wątpliwo-
ści – trudności praktyczne, to wybór i skuteczność leczenia.
Zmiana miażdżycowa może obejmować cały obwód naczynia – wtedy ma-
my do czynienia ze zwężeniem koncentrycznym – lub „tylko” jego część – to
zwężenie ekscentryczne. Na dynamikę zmian, a zwłaszcza stabilność lub wy-
stąpienie objawów niestabilnej dusznicy wpływa także aktualna czynność
53

śródbłonka i reaktywność mięśniówki gładkiej naczyń – wszystko to powo-
duje, że „przewidywalność” blaszki miażdżycowej dla klinicysty jest wielkim
wyzwaniem – niestety ciągle jeszcze niespełnionym.
Dalej nie wiemy – pomimo różnych logicznych koncepcji – dlaczego często
bezobjawowa zmiana miażdżycowa nabiera niebezpiecznej dynamiki? Dla-
czego „prowokuje” to powstanie skrzepliny – nagle lub w ciągu godziny –
zamykającej całkowicie światło naczynia, powodując nagłą śmierć pacjenta
w mechanizmie niedokrwienia i niestabilności elektrycznej, co prowadzi do
migotania komór lub „tylko” zawału serca.
Spróbujmy zatem uporządkować przyczyny powstania niedokrwienia mię-
śnia sercowego.
1. Zmiany miażdżycowe:
– rozwijają się podstępnie, niejasny początek;
– udowodniony związek z zaburzeniami lipidowymi, wysokim stęże-
niem cholesterolu całkowitego, frakcji LDL, trójglicerydów, z ob-
niżeniem frakcji HDL;
– coraz więcej dowodów na czynniki zapalne, „torujące” drogę
miażdżycy.
2. Czynniki dodatkowe („nagły bodziec”):
– stres fizyczny i/lub psychiczny;
– obciążenie serca („skok” ciśnienia tętniczego krwi);
– zaburzenia równowagi układu wegetatywnego.
3. Odpowiedź serca – sposób reakcji:
– zakrzep w naczyniu;
– pęknięcie blaszki miażdżycowej;
– kurcz naczyń wieńcowych.
Szacunkowe dane dotyczące naczyń odpowiedzialnych za ZS wskazują, że
mniej więcej połowa zmian miażdżycowych zwężała naczynie o mniej niż
50%. Czyżby kolejna reguła 50%? U połowy chorych dokonuje się ZS z po-
wodu katastrofy naczynia ze zwężeniem mniejszym niż 50%.
54

Dlatego to nie zawsze i nie tylko postępujące zwężenie jest odpowiedzial-
ne za powstanie ZS, a patogenetyczny mechanizm prowadzący do zmniej-
szenia przepływu wieńcowego i ostrego zespołu wieńcowego związany jest
także z ostrą zakrzepicą.
Zmiany miażdżycowe i naprężenia na jej powierzchni prowadzą do roze-
rwania włóknistej pokrywy blaszki miażdżycowej. Wrażliwe blaszki – niesta-
bilne – mają cienką wierzchnią pokrywę włóknistą, podatną na pęknięcie
i na rozerwanie, co inicjuje proces zakrzepowy i zamknięcie naczynia. Taki
mechanizm dominuje prawdopodobnie u mężczyzn, u kobiet częściej ma wy-
stępować rzadszy sposób rozrywania, polegający na powierzchniowej erozji
blaszki. Erozja błony wewnętrznej ma być mechanizmem częstszym u kobiet
przed 50 r. ż. i silnie związanym z paleniem tytoniu! Występuje prawdopo-
dobnie częściej także u chorych z cukrzycą. Natomiast rozerwanie blaszki
ma zdarzać się częściej u starszych kobiet i chorych z hipercholesterolemią.
Podobnej zależności od wieku nie obserwuje się u mężczyzn, różnice te mia-
łyby mieć związek z estrogenami, ale pogląd ten jest kontrowersyjny.
W rozważanych mechanizmach rozwoju miażdżycy bierze się od dawna
pod uwagę udział zakażenia wirusowego lub bakteryjnego, wywołanego na
przykład przez Chlamydia pneumoniae, wirus cytomegalii czy Helicobacter
pylorii. Drobnoustroje te miałyby wpływać niekorzystnie na czynność śród-
błonka lub aktywować odpowiedź zapalną, co prowadzi do rozwoju blaszki
i jej rozerwania.
Pytanie, czy choroba wieńcowa to choroba immunologiczno-zapalna,
pozostaje dalej wyzwaniem. Dowody na udział różnych patogenów bak-
teryjnych, znajdowanych w blaszkach miażdżycowych naczyń wieńcowych,
aorty piersiowej i brzusznej – u chorych z wyraźnym uszkodzeniem ścian
tętnic – wskazują, że koncepcja zapalna może dotyczyć chorych z chorobą
wieńcową, ale czy wszystkich? Tego w chwili obecnej nie wiadomo. Nato-
miast w badaniach nad udziałem tych patogenów w uszkodzeniu naczyń
wieńcowych wykazano, że im więcej przeciwciał stwierdzono we krwi – co
wskazywało na przebytą lub istniejącą infekcję – tym bardziej zaawanso-
wane były zmiany w wykonanej równolegle koronarografii. Niestety próby
leczenia antybiotykami choroby wieńcowej, nawet w wybranych grupach
chorych z potwierdzoną infekcją nie przyniosły spodziewanych (?) efek-
tów klinicznych.
Co z tego pozostało lekarzowi w codziennej praktyce? Nadzieję budzi oce-
na stanu zapalnego za pomocą białka ostrej fazy (C-reactive proteine – CRP).
Wyraźne podwyższenie wartości tego białka stwierdzono równolegle do wy-
stępowania ostrych epizodów wieńcowych. Wskazywało ono także na gorsze
55

rokowanie u osób pozornie zdrowych i na podwyższone ryzyko wystąpienia
ZS i/lub udaru mózgu w tej grupie.
Zwiększone stężenie CRP wskazuje więc na uszkodzenie serca, na udział
odpowiedzi immunologicznej w patogenezie ChNS; jest czułym wskaźni-
kiem, ale niestety również nieswoistym, zmieniającym się w każdym stanie
zapalnym. Tak więc, czynnik zapalny pozostaje ważnym, praktycznie już
możliwym do wykrycia, ale wciąż tajemniczym i trudnym do leczenia oraz
sterowania elementem patogenezy choroby wieńcowej.
Przedstawione wyżej przyczyny są ogromnym uproszczeniem, a niektóre
z wymienionych elementów nakładają się na siebie. Część z nich łatwo roz-
poznać i podejrzewać ich udział w patogenezie ChNS, inne natomiast są bar-
dziej tajemnicze.
Lekarz praktyk spotykając chorego, który ma wyraźne zaburzenia lipido-
we, nadciśnienie tętnicze, pali od lat, przekroczył 40 rok życia, a w jego ro-
dzinie występowały choroby układu sercowo-naczyniowego, z ogromnym
prawdopodobieństwem powinien podejrzewać chorobę wieńcową i możli-
wość wystąpienia w najbliższym czasie katastrofy wieńcowej. Mniejsze zna-
czenie ma fakt, że chory przy ustabilizowanym trybie życia nie odczuwa istot-
nych dolegliwości.
Lata doświadczeń i ostatnie badania, klasyfikacje Towarzystw Amerykań-
skich i Europejskich, każą ocenę globalnego ryzyka traktować jako najważ-
niejsze „badanie diagnostyczne ChNS”.
REPERFUZJA/OGŁUSZENIE/ZAMROŻENIE/HARTOWANIE
Dyskutując o mechanizmach niedokrwienia nie można nie wspomnieć
o reperfuzji – zjawisku ciekawym, dobroczynnym z jednej i bardzo niebez-
piecznym z drugiej strony. Klasyczna i najlepiej poznana reperfuzja to ta,
którą wywołuje skuteczne leczenie fibrynolityczne.
Zamknięte zakrzepem na często pękniętej blaszce miażdżycowej naczynie
powoduje ostre, ciężkie i często rozległe – co związane jest z kalibrem na-
czynia – niedokrwienie i w konsekwencji martwicę. Możliwość leczenia fi-
brynolitycznego odkryła przed klinicystami bardzo ciekawe i ważne zjawi-
sko. Skuteczne leczenie otwierające uprzednio zamknięte naczynie (TIMI 2/
TIMI 3) powoduje ponowny przepływ do niedokrwionego obszaru mięśnia
lewej komory (reperfuzja). Pomimo zachowanego przepływu i braku mar-
twicy mięśnia, utrzymują się zaburzenia kurczliwości: hipo-, akineza lewej
komory. Stan taki nazywamy ogłuszeniem miokardium.
56

Upraszczając to zjawisko na poziomie komórki, można powiedzieć, że
w wyniku reperfuzji i niedoboru tlenu dochodzi do zaburzeń funkcji siatecz-
ki sarkoplazmatycznej, zmiany wrażliwości na wapń, powstaje duża ilość tok-
sycznych rodników tlenowych, dochodzi do uszkodzenia białek, wzrasta stę-
żenie utlenowanego glutationu, co w rezultacie prowadzi do zaburzeń
kurczliwości. To, co jest ważne dla klinicystów – czas łagodzi skutki „stresu
oksydacyjnego”, białka wracają do formy zredukowanej lub są zastępowane
nowymi – kurczliwość poprawia się, a nawet wraca do normy.
Ogłuszenie, które przychodzi nagle wraz z niedokrwieniem, łatwiej rozpo-
znać, gdyż odkrycie echokardiograficzne łączy się z objawami klinicznymi.
Narastające zwężenie, powodujące przewlekłą hipoperfuzję lub nawraca-
jące epizody ogłuszenia, prowadzi do powstawania obszarów mięśnia serco-
wego słabo lub niekurczących się w ogóle – hipokineza lub akineza – zjawi-
sko to nazywamy zamrożeniem miokardium.
Przewlekle niedokrwiony mięsień żyje na ile go stać, ponieważ ma mniej
tlenu i substancji potrzebnych do sprawnego metabolizmu, „zamraża” swą
najważniejszą funkcję – kurczliwość. Po rewaskularyzacji, w obszarach tych
dochodzi do wyraźnej poprawy funkcji skurczowej.
Tłumacząc najprościej mechanizm zamrażania, należy stwierdzić, że ogra-
niczenie przepływu wieńcowego prowadzi do zaburzeń w transporcie wapnia
z równoczesną zmianą metabolizmu miocytów, spowodowaną spadkiem po-
daży tlenu („sprytny mięsień”). Nie wiemy, czy zawsze zamrożony mięsień
pod wpływem poprawy ukrwienia poprawia swoją kurczliwość. Prawdopo-
dobnie jednak zależy to od czasu trwania zamrożenia.
Podobieństwa ogłuszenia i zamrożenia są duże, a obraz zaburzeń kurczli-
wości w badaniu echokardiograficznym jest trudny do odróżnienia. Stany te
różnią się istotnie w zakresie przepływu – w mięśniu ogłuszonym jest on za-
chowany, natomiast wyraźnie ograniczony w mięśniu zamrożonym (ryc. 2).
KARDIOPROTEKCJA
Z procesami prowadzącymi do niedokrwienia wiążą się objawy mądrości
naszego organizmu. Działanie powodujące ochronę serca, ograniczające lub
zapobiegające uszkodzeniu mięśnia sercowego – to kardioprotekcja. Poję-
ciem tym obejmuje się wszelkie mechanizmy, które bezpośrednio lub po-
średnio chronią miokardium. W praktyce klinicznej najważniejsze „zadania”
kardioprotekcji, to ochrona mięśnia w czasie niedokrwienia i reperfuzji.
Wracając na chwilę do fizjologii trzeba przypomnieć, że w okresach więk-
szego przepływu wieńcowego (wysiłek, stres), dochodzi do stymulacji synte-
57
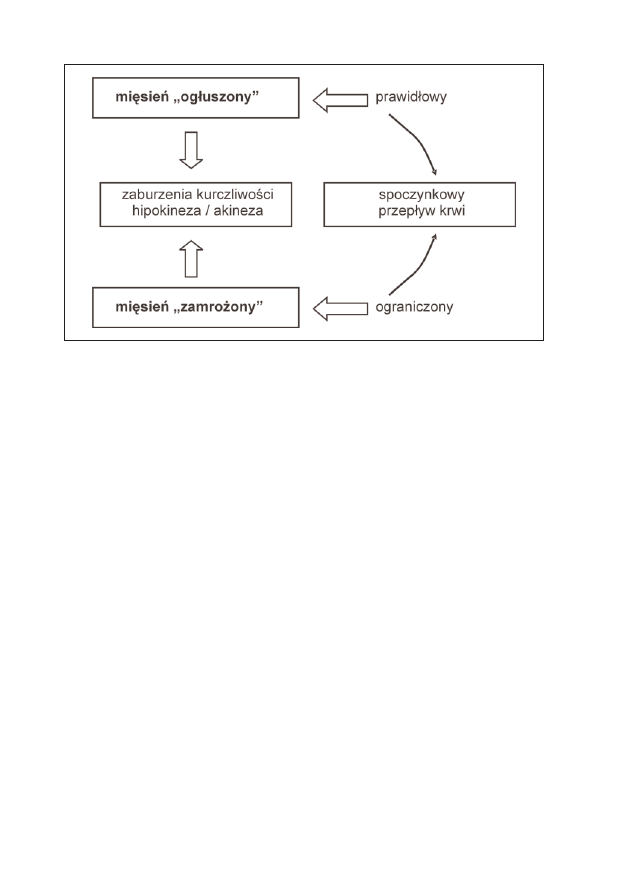
zy trójfosforanu adenozyny (ATP) potrzebnego do zaspokojenia potrzeb
metabolicznych serca. Pod wpływem niedokrwienia i niedoboru tlenu, meta-
bolizm zmienia się z tlenowej na beztlenową glikolizę, z narastaniem mlecza-
nów i kwasicy z konsekwencjami i tu włącza się endogenna kardioprotekcja –
mądra adaptacja mięśnia na przeczekanie, na uzyskanie potrzebnego czasu,
„na interwencję lekarską”.
Przedstawione wcześniej zjawiska ogłuszenia i zamrożenia mięśnia serco-
wego, to endogenna kardioprotekcja – dowód na mądrość organizmu.
Ogłuszenie chroni mięsień sercowy przed całkowitą zagładą, daje mu czas,
by mógł wrócić do normalnej czynności po ustąpieniu zaburzeń dopływu
krwi i reperfuzji. Zamrożenie chroni żywotność miokardium przez „oszczęd-
ną” kurczliwość i zmniejszenie zużycia tlenu w przewlekłych zaburzeniach
ukrwienia w zamrożonych naczyniach wieńcowych.
Kardioprotekcja, to łączne działanie wielu różnych mechanizmów, chro-
niących mikrokrążenie przed uszkodzeniem, zmniejszające zaburzenia
w przepływie tkankowym nie tylko w czasie, ale także po ustąpieniu niedo-
krwienia. W wyniku tych działań dochodzi do ograniczenia obszaru martwi-
cy po niedokrwieniu i reperfuzji. Ta reakcja adaptacyjna na niedokrwienie
określana jest jako endogenne działanie ochronne lub inaczej „precondi-
tioning” – „hartowanie przez niedokrwienie”.
Dla praktyka oznacza to, że w jakiś tajemniczy sposób, chory po pierw-
szym bólu wieńcowym, w dalszym ciągu, pomimo wykonywania podobnych
58
Rycina 2: Konsekwencja „ogłuszenia” i „zamrożenia”

wysiłków jest wolny od dolegliwości. Działanie ochronne, jakoby z udziałem
adenozyny, jest tajemnicze mimo intensywnych badań i co ciekawe, udowod-
nione dla niektórych uznanych leków wieńcowych, jak np. dla nitrogliceryny.
Chociaż przyczyną większości ostrych zespołów wieńcowych są powikła-
nia zakrzepowe miażdżycy, zamknięcie naczynia wieńcowego może być po-
wodowane innymi przyczynami: skurcz tętnicy wieńcowej, samoistne rozwar-
stwienie ściany, zatorowość, czy w końcu wspomniane wcześniej zapalenie
(„coronaritis”?), a także stany nadkrzepliwości. Wszystko to potwierdza ta-
jemniczość patogenezy tej bardzo przecież powszechnej choroby, niejedno-
krotnie o dramatycznym przebiegu.
Co te rozważania patogenetyczne o chorobie niedokrwiennej serca zna-
czą dla lekarza praktyka?
Przede wszystkim umiejętność przerwania mechanizmów „błędnego ko-
ła”. Chory z powodu narastającego znaczenia uznanych czynników ryzyka
niszczy własny śródbłonek – jego dysfunkcja sprzyja gromadzeniu się w bło-
nie wewnętrznej makrofagów i cząsteczek LDL. Makrofagi dalej uszkadza-
ją śródbłonek i są też odpowiedzialne za oksydację LDL, którego cząsteczki
dalej uszkadzają śródbłonek i „samodestrukcja” trwa.
Jak zapobiec i leczyć? Pozornie wydaje się to proste. O czynnikach ryzyka
powiedziano już wiele. Natomiast, jeśli chodzi o wybór leków wieńcowych,
warto pamiętać o lekach, które mają udowodnione działanie stabilizujące
płytkę miażdżycową i chroniące śródbłonek. Te „sprawdzone” leki to kwas
acetylosalicylowy,
bb-adrenolityki, ACE-inhibitory i statyny.
Od patogenezy po udowodnione kliniczne leczenie – o tym będą mówiły
kolejne rozdziały niniejszego opracowania.
Zapamiętaj!
1. Zmiany miażdżycowe w naczyniach wieńcowych są główną przyczyną cho-
roby niedokrwiennej serca.
2. Zaburzenia w lipidach krwi (głównie hipercholesterolemia), wysokie stęże-
nie frakcji LDL, trójglicerydów, ale i obniżenie frakcji HDL, są główną
przyczyną zmian miażdżycowych w naczyniach.
3. Czy należy wykonywać nieinwazyjne badania dla wykrycia choroby wieńco-
wej? TAK (!), z podkreśleniem wagi badań dynamicznych, pamiętając jed-
nak, że ich ujemny wynik, zwłaszcza w trakcie terapii lekami „wieńcowy-
mi”, nie wyklucza obecności zmian w naczyniach!
59

4. Najważniejszym „badaniem” dla lekarza-praktyka jest ocena globalnego
ryzyka rozwoju choroby wieńcowej – to ono powinno decydować o podej-
rzeniach choroby, decyzji o badaniach i leczeniu – często jeszcze przed ob-
jawami choroby!
Warto przeczytać:
A. Beręsewicz, M. Kurzelewski: Niestabilna blaszka miażdżycowa. Kardio-
logia Polska. 2001, 6, 431.
A. C. van der Wal, A. E. Becher: Atherosclerotic plague rupture patologic
basis of plague stability and instability. Cardiovasc. Res. 1999, 41, 334.
A. Beręsewicz: Regulacja krążenia wieńcowego w normie i w chorobie wień-
cowej. Rozdział w „Choroba niedokrwienna serca – co lekarz wiedzieć powi-
nien” – pod red. M. Dłużniewski, Warszawa 1999, 5, Fundacja „Dla Serca”.
A. P. Burke i wsp.: Effects of risk factors on the mechanism of acute throm-
bosis and sudden coronary death in women. Circulation 1998, 97, 2110.
A. P. Burke i wsp.: Coronary risk factors and plaque morphology in men with
coronary disease who died suddenly. N. Engl. J. Med. 1997, 336, 1276.
60

V.
CO NALEŻY ROBIĆ, ABY UNIKNĄĆ CHOROBY
NIEDOKRWIENNEJ SERCA?
PREWENCJA PIERWOTNA
Witold Pikto-Pietkiewicz, Artur Mamcarz
WSTĘP
Epidemia chorób układu krążenia (ChUK) stała się z całą pewnością jed-
nym z najistotniejszych wyzwań, przed jakimi stanęła medycyna XX wieku.
Narastająca szybko w pierwszej połowie ubiegłego stulecia ilość zgonów
z powodu chorób serca i naczyń stanowiła zaskoczenie i swego rodzaju za-
gadkę dla lekarzy w tym czasie. Miażdżyca, będąca obok nadciśnienia, pod-
stawową przyczyną ChUK, nie była przecież zjawiskiem nowym i wcześniej
nieznanym. Pozostawało jednak pytanie, dlaczego szybkiemu wzrostowi ule-
ga ilość zgonów sercowo-naczyniowych, będących wynikiem przyśpieszonego
rozwoju tej patologii? Wzrost zapadalności i umieralności na ChUK był
szczególnie zauważalny w krajach o wysokim poziomie rozwoju technolo-
gicznego. Szeroko zakrojone badania epidemiologiczne i kliniczne, poczy-
nając od Framingham Heart Study rozpoznały główne czynniki ryzyka ChUK,
a w szczególności czynniki determinujące zagrożenie chorobą wieńcową
(ChW). Czynniki te zdefiniowano jako czynniki ryzyka ChW. Kolejne bada-
nia pozwoliły określić wagę podstawowych czynników ryzyka, takich jak nad-
ciśnienie tętnicze, hipercholesterolemia, palenie tytoniu, czy cukrzyca. Dzię-
ki temu ustalono priorytety w zakresie postępowania zapobiegawczego.
W końcu udało się wykazać, że zwalczanie czynników ryzyka wiąże się ze
zmniejszeniem zapadalności i umieralności z powodu ChW. Rezultatem
zmian świadomości społecznej, dotyczącej zagrożenia ChUK, stały się zmia-
ny stylu życia, które wraz z postępem medycyny w zakresie rozpoznania i le-
czenia tych chorób, doprowadziły do odwrócenia niekorzystnych trendów
zapadalności i umieralności związanych z tą grupą chorób. Do najistotniej-
szych czynników, mających w tym procesie swój udział, należy zaliczyć ra-
cjonalizację żywienia, zmniejszenie odsetka ludzi palących papierosy, popra-
wę wykrywalności i efektywności leczenia nadciśnienia tętniczego oraz
hiperlipidemii, a także znaczący postęp w leczeniu samej ChW. Korzystne
zmiany trendów chorobowych związanych z ChUK, zachodzące na przeło-
mie lat sześćdziesiątych i siedemdziesiątych ubiegłego stulecia, dotyczyły
większości rozwiniętych krajów zachodniej części Europy, a także Ameryki
Północnej i Australii. W tym czasie w wielu krajach Europy Środkowo-
-Wschodniej, nastąpił dynamiczny wzrost zapadalności na ChW i związanej
61

z nią umieralności. Ten szybki wzrost zachorowalności szczególnie zaznaczył
się w Polsce, doprowadzając pod koniec lat osiemdziesiątych do nadumieral-
ności mężczyzn w średnim wieku, a w rezultacie do skrócenia średniego cza-
su życia mężczyzn. Zmiany społeczno-ekonomiczne, jakie nastąpiły w Pol-
sce w latach dziewięćdziesiątych, przyczyniły się do zahamowania tego
dramatycznego wzrostu wskaźników chorobowych związanych z ChW.
Powszechna akceptacja w środowiskach medycznych roli czynników ryzy-
ka w powstawaniu zagrożenia ChUK, a także coraz liczniejsze dowody, prze-
konujące o skuteczności metod ich zwalczania za pomocą interwencji far-
makologicznej i niefarmakologicznej, spowodowały powstanie nowej gałęzi
kardiologii zwanej kardiologią prewencyjną. Organizacja tej dziedziny me-
dycyny różni się w poszczególnych krajach dość istotnie, zależy bowiem od
zamożności poszczególnych krajów, form organizacyjnych publicznej służby
zdrowia, tradycji kulturowych i in. Niezależnie od tych różnic, kardiologia
prewencyjna powinna kierować się 3 priorytetami. Należą do nich:
Pierwszy z wymienionych priorytetów jest typową domeną codziennej
praktyki lekarzy kardiologów, a także lekarzy pierwszego kontaktu. Także
pozostałe dwa priorytety powinny być realizowane przez system publicznej
ochrony zdrowia, jednak zakres tej realizacji jest w znacznym stopniu uza-
leżniony od funduszy przeznaczanych przez państwo na ochronę zdrowia.
W krajach o szczególnie dużym zagrożeniu ChW, a do takich należy Pol-
ska, w działaniach prewencyjnych konieczne jest zastosowanie strategii po-
pulacyjnej. Strategia ta polega przede wszystkim na ograniczaniu oddziały-
wania czynników ryzyka związanych ze stylem życia. Informacje o roli tych
czynników oraz zalecenia co do ich modyfikacji powinny być kierowane do
wszystkich ludzi za pośrednictwem środków masowego przekazu, poprzez
szkoły, organizacje samorządowe i społeczne. Jednostki służby zdrowia peł-
nią w tym zakresie jedynie rolę inicjatywną i opiniotwórczą. Wyrazem dzia-
łań opiniotwórczych jest również formułowanie przez towarzystwa nauko-
we, m.in. Polskie Towarzystwo Kardiologiczne, standardów postępowania
zapobiegawczego. Standardy te służą do ustalania celów i zasad postępowa-
62
• prewencja wtórna oraz rehabilitacja chorych z objawową chorobą
wieńcową;
• wczesne rozpoznanie asymptomatycznej miażdżycy naczyń
w populacji ogólnej;
• badania przesiewowe w celu oceny ryzyka rozwoju ChW i innych
powikłań naczyniowych miażdżycy w populacji ogólnej.

nia z pacjentami zagrożonymi ChUK. Część standardów powinna być roz-
powszechniana przez środki masowego przekazu, tak aby dotrzeć do możli-
wie jak najszerszego kręgu odbiorców.
PRZEGLĄD NAJWAŻNIEJSZYCH CZYNNIKÓW RYZYKA
Badania epidemiologiczne doprowadziły do szybkiego zidentyfikowania
znacznej liczby czynników ryzyka ChW. Obecnie liczba poznanych czynni-
ków ryzyka zbliża się do 300. Zgodnie ze starą definicją Simborga, za czyn-
nik ryzyka należy uznać każdy czynnik lub cechę, występującą w populacji
ludzi „zdrowych”, której obecność wiąże się jednak ze zwiększonym ryzykiem
zachorowania lub zgonu z powodu ChW. W myśl tej definicji, czynnik ryzyka
jest pojęciem statystycznym, jednak w większości przypadków w jakimś me-
chanizmie, czasem nie do końca poznanym, wiąże się z etiopatogenezą ChW.
Z praktycznego punktu widzenia najważniejsze czynniki ryzyka podzielono
na 3 główne kategorie: czynniki dotyczące stylu życia, modyfikowalne czyn-
niki biochemiczne oraz czynniki niepoddające się modyfikacji (tab. 1).
Jak przedstawiono w tabeli 1, czynniki ryzyka można podzielić na modyfi-
kowalne, np. palenie, otyłość, nadciśnienie tętnicze oraz takie, które nie
podlegają modyfikacji, np. wiek lub płeć. Znaczna część czynników ma po-
tencjalnie charakter modyfikowalny, jednak tylko co do części z nich mamy
jednoznaczne dowody, przemawiające za skutecznością podejmowanych
działań interwencyjnych. Do czynników, o których wiadomo, że działania in-
terwencyjne, korygujące dany czynnik są skuteczne w zmniejszaniu ryzyka
rozwoju ChW, zaliczamy m.in. obniżanie stężenia cholesterolu LDL, farma-
koterapię nadciśnienia tętniczego, czy zmniejszenie występowania nałogu
palenia papierosów. Bardzo prawdopodobna wydaje się skuteczność pre-
wencyjna uzyskana poprzez dobre wyrównanie cukrzycy. Badania prospek-
tywne w prewencji pierwotnej (np. wieloletnie badanie UKPDS) nie po-
twierdzają jednak tego w sposób ostateczny. Stwierdzenie to nie dotyczy
jednak prewencji wtórnej, gdyż w tym przypadku istnieją dowody na zasad-
ność insulinoterapii w zmniejszeniu umieralności po przebytym zawale ser-
ca (badanie DIGAMI).
Pozostaje także znaczna grupa czynników ryzyka, co do których skutecz-
ność działań prewencyjnych wydaje się prawdopodobna, ze względu na po-
znane lub postulowane przesłanki patofizjologiczne, ale brak jest na to jesz-
cze dowodów, pochodzących z interwencyjnych badań klinicznych (np.
hiperhomocysteinemia, czynniki psychosocjalne).
63

DIETA – SPOSÓB ŻYWIENIA
Sposób żywienia stanowi istotny czynnik determinujący ryzyko ChW ze
względu na jego wpływ na profil lipidowy, wysokość ciśnienia tętniczego oraz
występowanie otyłości. Powszechnie znanym czynnikiem sprzyjającym miaż-
dżycy jest dieta bogata w nasycone kwasy tłuszczowe (tłuszcze zwierzęce),
podwyższająca stężenie cholesterolu LDL. Czynnikiem aterogennym jest
także spożycie kwasów tłuszczowych nienasyconych trans. W przyrodzie wy-
stępują naturalne kwasy tłuszczowe nienasycone, posiadające podwójne wią-
zania jedynie w konfiguracji cis, kwasy trans powstają zaś w procesie prze-
mysłowego utwardzania tłuszczów roślinnych. Ze względu na niekorzystne
działanie kwasów nienasyconych trans, zawartość ich w margarynach powin-
na być możliwie jak najniższa, najlepiej jeśli byłaby określona w składzie
i wyszczególniona na opakowaniu. Spożycie jedno- i wielonienasyconych
kwasów tłuszczowych cis obniża stężenie LDL cholesterolu. Wysokie spoży-
64
Tabela 1: Najważniejsze czynniki ryzyka incydentu wieńcowego
Styl życia
Cechy biochemiczne
i fizjologiczne
(poddające się
modyfikacji)
Cechy indywidualne
(niepoddające się
modyfikacji)
• dieta obfitująca
w tłuszcze
nasycone,
cholesterol
i kalorie;
• palenie tytoniu*;
• nadmierne
spożycie alkoholu;
• mała aktywność
fizyczna.
• podwyższone
stężenie
cholesterolu
(LDL)*;
• podwyższone
stężenie
trójglicerydów;
• niskie stężenie
cholesterolu HDL*;
• podwyższone
ciśnienie tętnicze*;
• otyłość;
• hiperglikemia
/cukrzyca*;
• czynniki
trombogenne;
• zwiększone stężenie
homocysteiny.
• wiek:
– mężczyzna
³ 45
lat*,
– kobieta
³ 55 lat*;
• przedwczesna
menopauza*;
• wczesne występowa-
nie w rodzinie ChW
lub innych chorób tęt-
nic na tle miażdżycy:*
– mężczyzn przed
55 r. ż.,
– kobiet przed
65 r. ż.;
• istniejąca u pacjenta
ChW lub choroby
innych tętnic na tle
miażdżycy*.
* czynniki służące do oceny ryzyka ogólnego w standardach ESC i PTK

cie węglowodanów złożonych powoduje spadek zarówno LDL, jak i HDL,
tym samym nie poprawia stosunku LDL/HDL. Problem ten omówiono
szczegółowo w innym rozdziale.
Trwa obecnie dyskusja, jaki rodzaj diety jest optymalny dla osób zagro-
żonych, u których chcielibyśmy obniżyć poziom cholesterolu LDL. W każ-
dym przypadku powinna być to dieta z niską zawartością nasyconych kwa-
sów tłuszczowych oraz nienasyconych kwasów trans. Dyskusja dotyczy
jednak tego, czy należy jako zamiennik stosować wysokie spożycie wielo-
nienasyconych kwasów tłuszczowych, czy też dieta powinna być uzupełnio-
na węglowodanami złożonymi. Stosowanie obu rodzajów diet (przykładowo:
dieta śródziemnomorska – bogata w tłuszcze nienasycone czy tradycyjna
dieta japońska – bogata w węglowodany złożone) jest związane w bada-
niach obserwacyjnych z długim przeżyciem. W chwili obecnej przeważa po-
gląd o większej przydatności diety śródziemnomorskiej (mała zawartość
mięsa czerwonego, mało kwasów tłuszczowych nasyconych, duża ilość oliwy
– kwas jednonienasycony, warzywa i owoce – antyoksydanty, wino – alko-
hol i flawonoidy).
ZABURZENIA LIPIDOWE
Cholesterol LDL
Wpływ nieprawidłowej diety, zwiększający ryzyko ChW, związany jest
głównie – jak wspominano wcześniej – z niekorzystnymi przesunięciami
w zakresie lipidów, głównie frakcji cholesterolu LDL. Zaburzenia lipidowe
nie są jednak wyłącznie wynikiem nieprawidłowej diety, mogą być także
uwarunkowane genetycznie. W przeważającym odsetku zaburzenia lipido-
we mają charakter pierwotny, należy jednak pamiętać, że mogą one być
wtórne do innych patologii (np. wysokie spożycie alkoholu, niedoczynność
tarczycy, choroby nerek i wątroby, stosowanie niektórych leków, np. beta-
-adrenolityków, diuretyków, steroidów anabolicznych i in.). Zawsze należy
wykluczyć hiperlipidemię wtórną, szczególnie przed podjęciem decyzji o le-
czeniu farmakologicznym.
Zależność pomiędzy stężeniem cholesterolu całkowitego, a ryzykiem
ChUK jest jednym z najwcześniej odkrytych czynników ryzyka. Nic w tym
dziwnego, bowiem z badań klinicznych i badań doświadczalnych wiadomo
już było wcześniej, że cholesterol jest jednym z podstawowych składników
ogniska ateromatycznego. Wiadomo też, że większą część puli cholesterolu
całkowitego stanowi aterogenna frakcja lipoprotein niskiej gęstości – low
density lipoprotein (LDL). Z tej właśnie frakcji, cholesterol przenika do ścia-
65

ny naczyniowej i odkłada się w blaszce miażdżycowej. Intensywność przeni-
kania cholesterolu do ściany naczyniowej uzależniona jest głównie od:
Przy zdrowym śródbłonku i braku stresu oksydacyjnego, prawidłowym stę-
żeniu lipoprotein LDL oraz prawidłowym ciśnieniu krwi, miażdżyca nie roz-
wija się lub rozwija się bardzo powoli. Ryzyko ChW wzrasta semilogaryt-
micznie wraz ze wzrostem stężenia cholesterolu LDL, poczynając od
wartości zdecydowanie niskich – trudno jest zatem wskazać granicę stężenia
cholesterolu LDL, poniżej której ryzyko ChW już nie zależy od jego stęże-
nia. Warto pamiętać, że stężenie cholesterolu LDL we krwi pępowinowej
noworodków wynosi poniżej 50 mg/dL, a stosunek LDL do HDL jest równy
lub większy od 1. W dalszym okresie życia następuje stopniowe zwiększanie
stężenia cholesterolu LDL, a stosunek LDL/HDL także ulega stałemu wzro-
stowi. Brak wartości progowej, oddzielającej „prawidłowe” stężenia chole-
sterolu LDL od nieprawidłowych, znajduje także odzwierciedlenie w zmie-
niających się „normach” zawartych w standardach towarzystw naukowych,
dotyczących postępowania w zakresie zaburzeń lipidowych. Warto także
podkreślić utrzymujące się pewne różnice w zakresie optymalnych lub do-
celowych stężeń LDL oraz wskazań do farmakoterapii hiperlipidemii w stan-
dardach różnych towarzystw. Problemowi docelowego, „optymalnego” stę-
żenia cholesterolu LDL, do jakiego należy dążyć u pacjentów wysokiego
ryzyka, poświęconych jest kilka trwających obecnie, dużych badań klinicz-
nych. Uzyskanie optymalnych stężeń cholesterolu LDL należy do podstawo-
wych celów prewencji zdarzeń sercowo-naczyniowych. Istnieje bardzo boga-
ta i przekonująca dokumentacja, dotycząca interwencji w tym zakresie, która
potwierdza skuteczność leczenia hipolipemizującego w hamowaniu progre-
sji miażdżycy, redukcji liczby incydentów wieńcowych, udarów mózgu,
zmniejszeniu potrzeb zabiegów rewaskularyzacyjnych. Najistotniejszą jed-
nak korzyścią postępowania hipolipemizującego jest redukcja śmiertelności
związanej z ChUK zależnymi od miażdżycy. Problem ten szeroko omówiono
w innej części niniejszego opracowania.
66
• stężenia LDL w surowicy;
• przepuszczalności ściany naczyniowej (funkcja ochronna
śródbłonka);
• ciśnienia tętniczego krwi;
• obecności czynników modyfikujących strukturę natywnych LDL.

Cholesterol HDL
Ryzyko ChW, związane z zaburzeniami lipidowymi, to nie tylko cholesterol
LDL, ale także inne lipidowe czynniki ryzyka. Zaliczamy do nich obniżone
stężenie cholesterolu zawarte w „ochronnej” frakcji lipoprotein wysokiej gę-
stości – high density lipoprotein (HDL), a także podwyższone stężenie trój-
glicerydów (TG).
Już w latach pięćdziesiątych ubiegłego stulecia, pojawiło się pierwsze do-
niesienie o związku niskich stężeń cholesterolu HDL ze zwiększonym ryzy-
kiem ChW, jednak dominujący wówczas pogląd o podstawowej roli chole-
sterolu LDL, jako czynnika ryzyka, zdeterminował badania nad prewencją
ChW w tym kierunku na wiele lat. Wyniki badań prospektywnych (m.in. ba-
dania PROCAM, Framingham Heart Study) potwierdziły w kolejnych latach
wpływ niskich stężeń cholesterolu HDL na zwiększone ryzyko ChW, nieza-
leżny od pozostałych lipidowych i nielipidowych czynników ryzyka. Co wię-
cej, okazało się, że ryzyko ChW związane z niskim stężeniem HDL jest po-
dobnie wysokie jak ryzyko wynikające z wysokich stężeń cholesterolu LDL.
Oznacza to m.in., że osoby z niskimi stężeniami HDL (<40 mg/dL), u których
uzyskano metodami farmakologicznymi bądź niefarmakologicznymi obni-
żenie stężenia cholesterolu LDL, pozostają nadal w grupie podwyższonego
ryzyka ChW ze względu na stężenie HDL. Rola lipoprotein HDL, jako czyn-
nika hamującego postęp miażdżycy, wydaje się związana z dwoma głównymi
mechanizmami: zwrotnym transportem cholesterolu z tkanek obwodowych
do wątroby (reverse cholesterol transport) oraz właściwościami antyoksyda-
cyjnymi składników tych lipoprotein. W tym kontekście, głównie wymieniany
jest enzym – paraoksonaza. Postulowane są także inne właściwości przeciw-
miażdżycowe HDL (ryc. 1). Istnieją dowody na to, że interwencja skierowa-
na na niskie stężenie HDL może być związana z redukcją ryzyka ChW. Re-
trospektywna analiza badania Helsinki Heart Study, wskazała na istotne
zmniejszenie ryzyka incydentu wieńcowego w prewencji pierwotnej u osób
z niskim wyjściowo stężeniem HDL, u których pod wpływem leczenia gem-
fibrozilem doszło do wzrostu poziomu HDL. Bardzo obiecujące są także wy-
niki prospektywnego badania VAHIT, w którym stosowano leczenie gemfi-
brozilem w prewencji wtórnej u chorych po zawale serca, z niskim stężeniem
HDL (<40 mg/dL), przy towarzyszącym „prawidłowym” stężeniu cholestero-
lu LDL (<140 mg/dL). Leczenie to, prowadzone przez 5 lat, związane było
z istotną redukcją incydentów wieńcowych (o 22%). Efekt leczenia był szcze-
gólnie wyrażony w podgrupie osób z cukrzycą (40% redukcja).
Analiza omawianych badań wskazuje na zależność stopnia redukcji ryzyka
wieńcowego od wyjściowego stężenia cholesterolu HDL – im niższe wyjścio-
67
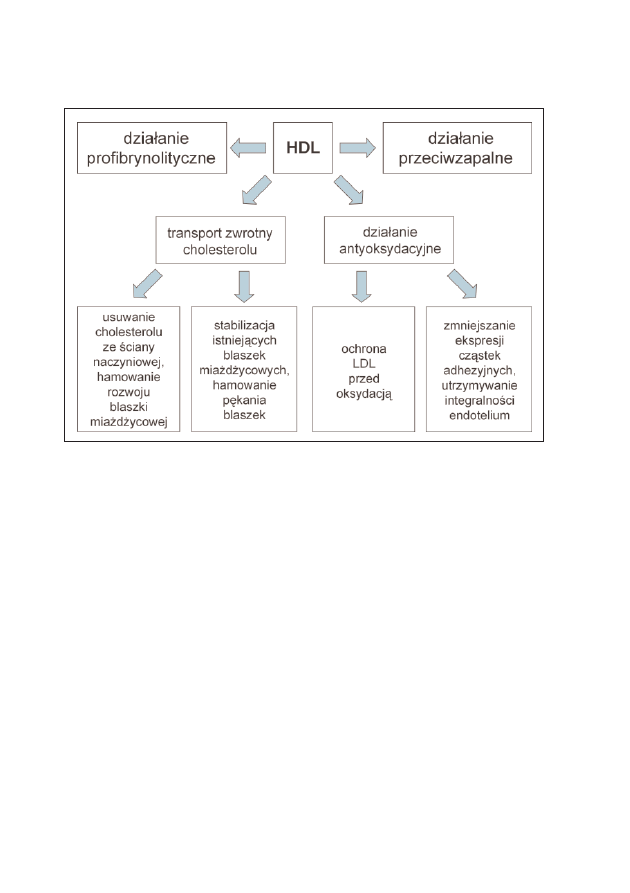
we stężenie, tym efekt prewencyjny leczenia jest większy. Wzrost stężenia
HDL o 1% związany jest 2-3% spadkiem ryzyka incydentu wieńcowego.
HIPERTRÓJGLICERYDEMIA
Przez długi czas sądzono, że ryzyko ChW, związane z podwyższonym stęże-
niem trójglicerydów (TG), wynika z częstego współistnienia hipertrójglicery-
demii (HTG) z innymi metabolicznymi czynnikami ryzyka, a przede wszyst-
kim z jej powiązania z niskim stężeniem cholesterolu HDL, a także otyłością
i cukrzycą. Istnieje ścisły związek metabolizmu cząstek HDL i VLDL. VLDL
obok chylomikronów transportują podstawową część TG w surowicy. Lipo-
proteiny o bardzo małej gęstości (very light density lipoprotein – VLDL) są
syntetyzowane w wątrobie, a następnie po wydzieleniu do krwi są szybko me-
tabolizowane przy udziale osoczowej lipazy lipoproteinowej. Istotną rolę
w metabolizmie VLDL odgrywa białko CETP. Czas półtrwania VLDL jest
krótki i wynosi poniżej 1 godziny. Utrzymujący się wzrost stężenia TG
(VLDL) w surowicy związany jest z równoległym spadkiem stężenia HDL.
Ze względu na znacznie dłuższy półokres trwania HDL, pomiar ich stęże-
nia może służyć jako długoterminowy wskaźnik zaburzeń metabolizmu TG
(podobnie jak poziom hemoglobiny glikowanej jest wskaźnikiem wyrówna-
nia cukrzycy). Lipoproteiny VLDL nie stanowią homogennego zbioru i róż-
68
Rycina 1: HDL – mechanizmy ochronne w hamowaniu ChNS

nią się pod względem składu oraz wielkości cząsteczek. Małe VLDL są ate-
rogenne, bowiem łatwiej przenikają przez śródbłonek do ściany naczynio-
wej, stając się składnikiem powstających ognisk ateromatycznych. Duże
cząstki VLDL oraz chylomikrony nie są aterogenne, toteż nawet ciężka
HTG związana z obecnością dużych cząstek nie zwiększa ryzyka ChW, może
natomiast być przyczyną ostrego zapalenia trzustki. Należy podkreślić fakt,
że nawet niewielkiemu wzrostowi stężeń TG (>150 mg/dL) towarzyszą nie-
korzystne przesunięcia w podfrakcjach LDL i HDL (gromadzenie małych
gęstych LDL, spadek stężeń HDL). HTG towarzyszy także przedłużona hi-
perlipemia poposiłkowa, co wiąże się z przedłużeniem ekspozycji ściany na-
czyniowej na działanie aterogennych remnantów chylomikronów. Oba te
zjawiska, towarzyszące łagodnej lub umiarkowanej HTG, przyczyniają się
do nasilenia tendencji promiażdżycowych. Z tego też powodu najnowsze
standardy NCEP określają jako pożądane stężenia TG <150 mg/dL.
INNE CZYNNIKI LIPIDOWE
Apolipoproteina B (apo-B) jest podstawowym białkowym składnikiem
aterogennych lipoprotein LDL i VLDL. Ze względu na fakt, że w każdej
cząsteczce aterogennych lipoprotein znajduje się tylko jedna cząsteczka
apo-B, pomiar jej stężenia jest dobrym wskaźnikiem zawartości miażdżyco-
rodnych lipoprotein w surowicy, a przez to jest istotnym markerem ryzyka
ChW.
Lipoproteina (a) – jest miażdżycorodną lipoproteiną, której stężenie jest
w znacznym stopniu determinowane genetycznie, a przez to w niewielkim
stopniu jest podatne na modyfikację. Zwiększone ryzyko rozwoju ChW
u osób z podwyższonymi stężeniami Lp (a) wymaga w związku z tym bar-
dziej intensywnego zwalczania innych, modyfikowalnych czynników ryzyka.
PALENIE TYTONIU
Palenie tytoniu jest klasycznym modyfikowalnym czynnikiem ryzyka chorób
układu sercowo-naczyniowego. Drastyczny spadek liczby palących białych
Amerykanów w latach sześćdziesiątych XX wieku (z ponad 60% do kilkunastu
procent), uważany jest za jedną z podstawowych przyczyn odwrócenia w poło-
wie lat siedemdziesiątych, wzrostowego trendu zapadalności na ChW w Sta-
nach Zjednoczonych.
Palenie tytoniu wywiera silny, miażdżycorodny wpływ poprzez wiele różnych
mechanizmów; do najważniejszych z nich należą: dysfunkcja śródbłonka, dzia-
łanie prozakrzepowe oraz niekorzystny wpływ na lipoproteiny osocza.
69

Dysfunkcja śródbłonka objawia się głównie zaburzoną funkcją wazorelak-
sacyjną, zależną od tlenku azotu. Uszkodzenie śródbłonka stanowi ponad-
to bodziec do prezentacji cząstek adhezyjnych, a w konsekwencji do przyle-
gania i penetracji monocytów do ściany naczyniowej. Jednocześnie pod
wpływem składników dymu tytoniowego, aktywacji ulega adhezja płytek oraz
uwalnianie czynników stymulujących proliferację komórek mięśniówki gład-
kiej naczyń.
Zaburzenia krzepnięcia, potęgowane przez palenie tytoniu, są zależne od
wzrostu stężenia fibrynogenu, obniżenia stężenia plazminogenu, wzrostu stę-
żenia czynnika VII, a także aktywacji płytek.
Palenie tytoniu wywiera także niekorzystny wpływ na profil lipidowy, bo-
wiem zmniejsza stężenie ochronnej frakcji cholesterolu HDL, jak również
nasila oksydacyjną modyfikację lipoprotein LDL. Ze zjawiskiem tym wiąże
się także zmniejszenie zdolności antyoksydacyjnych osocza u palaczy, m.in.
związane ze zmniejszonym stężeniem witamin antyoksydacyjnych (E i C).
Choć jest wiele prawdopodobnych mechanizmów promocji miażdżycy na
skutek palenia tytoniu, to trudno jest wskazać ten najistotniejszy. Wpływ pa-
lenia wyraża się zarówno poprzez przyspieszony rozwój blaszki miażdżyco-
wej, jak również poprzez inicjowanie procesów zakrzepowych na blaszce, co
powoduje powstanie ostrego zespołu wieńcowego (ACS). Z tym drugim me-
chanizmem związany jest fakt, że po zaprzestaniu palenia tytoniu u osób
z objawową ChW, dochodzi do szybkiej redukcji ryzyka incydentu do pozio-
mu ryzyka osób niepalących (w ciągu 2-3 lat ryzyko się zrównuje). W przy-
padku osób bez objawów ChW, czas jaki musi upłynąć od momentu rzucenia
palenia do uzyskania podobnie niskiego poziomu ryzyka, jak u niepalących
wynosi 10 lat (wpływ na rozwój samej blaszki).
Wpływ palenia papierosów przyspieszający miażdżycę, dotyczy zarówno
mężczyzn, jak i kobiet, wydaje się jednak, że nałóg ten wywiera szczególnie
szkodliwy wpływ u kobiet. Palenie bowiem znosi ochronny, hamujący przed-
wczesny rozwój ChW, wpływ profilu hormonalnego kobiet. Znany powszech-
nie jest także fakt wyjątkowo dużego ryzyka zawału serca u kobiet palących
papierosy i jednocześnie stosujących doustną hormonalną antykoncepcję.
Wpływ palenia papierosów na ryzyko ChW jest także wyraźnie modyfiko-
wany przez stężenia lipidów. Jak pokazują niektóre badania obserwacyjne,
np. w populacji Japonii, ryzyko ChW pozostaje niskie, pomimo że rozpo-
wszechnienie palenia tytoniu w tej populacji jest wysokie. Przyczyną jest za-
pewne fakt, że Japończycy, stosujący tradycyjną dietę japońską, bogatą w wę-
glowodany (ryż), mają niskie stężenie cholesterolu. Kiedy jednak następuje
zmiana diety na zbliżoną do diety zachodniej, dochodzi wówczas do wzro-
70

stu stężenia cholesterolu, a wtedy palenie tytoniu staje się podobnie silnym
czynnikiem ryzyka ChW, jak w krajach zachodnich.
Im wcześniej dochodzi do utrwalenia nałogu palenia tytoniu, tym większe
jest ryzyko chorób naczyniowych, szczególnie wtedy, jeśli palenie zostaje roz-
poczęte przed 15. rokiem życia.
ALKOHOL
Wśród czynników dotyczących stylu życia, obecnie najbardziej chyba kon-
trowersyjnym elementem jest spożycie alkoholu. Z jednej strony powszech-
nie wiadomo, że wysokie spożycie alkoholu związane jest ze zwiększonym
ryzykiem uzależnienia, jest także przyczyną wielu chorób somatycznych oraz
zwiększa ogólne ryzyko zgonu. Z drugiej strony, z dużych badań obserwa-
cyjnych płyną informacje o „protekcyjnym” wpływie spożywania alkoholu na
układ krążenia, szczególnie w aspekcie zagrożenia chorobą wieńcową. Za-
leżność umieralności ogólnej od wielkości spożycia alkoholu wykazuje
kształt krzywej J. Oznacza to, że małe lub umiarkowane spożycie alkoholu
(10-30 g czystego alkoholu dziennie, co odpowiada 1-3 standardowym „drin-
kom” – np. 1-3 kieliszki wina lub 1-3 butelki piwa – związane jest z mniej-
szą umieralnością, w stosunku do osób w ogóle niepijących. Podstawowy
udział w tej redukcji ma przede wszystkim zmniejszenie śmiertelności ser-
cowo-naczyniowej. Dalsze zwiększenie spożycia alkoholu związane jest
z szybkim wzrostem umieralności z różnych przyczyn (wypadki, choroby wą-
troby i trzustki, nowotwory, kardiomiopatia alkoholowa).
Ochronny wpływ małych dawek alkoholu na układ krążenia związany jest
prawdopodobnie z mechanizmami przeciwzakrzepowymi (działaniem anty-
agregacyjnym i profibrynolitycznym) oraz faktem podwyższenia stężeń cho-
lesterolu HDL. Efekt ten wydaje się niezależny od rodzaju spożywanego
trunku, choć istnieją wokół tego tematu kontrowersje (zwolennicy czerwone-
go wina). Nadmierne spożycie alkoholu zwiększa, jak wspominano, zagro-
żenie zgonem, także sercowo-naczyniowym. Główne przyczyny zgonu serco-
wo-naczyniowego to udar krwotoczny mózgu oraz nagły zgon sercowy.
Ze względu na to, że w skali społecznej szkodliwe skutki spożycia alkoho-
lu przeważają nad potencjalnymi korzyściami z tego płynącymi, nie wydaje
się celowe propagowanie spożywania, nawet niewielkich dawek alkoholu
w celach ochrony serca. W podejściu indywidualnym nie ma jednak powodu,
aby zakazywać spożywania alkoholu, jeżeli ilości konsumowane nie przekra-
czają 30 g alkoholu dla mężczyzny i 10-20 g dla kobiety na dzień.
71

NADCIŚNIENIE TĘTNICZE
Nadciśnienie tętnicze (NT) obok palenia tytoniu i zaburzeń lipidowych,
należy do klasycznej triady najważniejszych czynników ryzyka ChW. Ryzyko
ChW wykazuje rosnącą zależność od wielkości ciśnienia tętniczego, poczyna-
jąc od wartości niskich, uznawanych za mieszczące się w granicach normy
i ma charakter ciągły. Oznacza to, iż nie można, podobnie jak w przypadku
stężeń cholesterolu, ustalić wartości progowej dla ciśnienia tętniczego, od-
dzielającej normę od patologii. Zgodnie z ustaleniami ostatnich standardów
międzynarodowych i polskich (WHO, ISH, JNC VI, standardy PTK i PTNT)
ustalono zakres wartości ciśnienia optymalnego, wysokiego granicznego oraz
nadciśnienia tętniczego (tab. 2). Liczne badania interwencyjne w zakresie
modyfikacji stylu życia oraz z zastosowaniem farmakoterapii udowodniły, że
obniżenie ciśnienia tętniczego średnio o 5-6 mm Hg związane jest z istotnym
zmniejszeniem ryzyka nowych incydentów sercowo-naczyniowych (30-40%
redukcja ryzyka udaru mózgu, 50% redukcja ryzyka rozwoju niewydolności
serca, 15% redukcja ryzyka incydentów wieńcowych). O ile redukcja ryzyka
udaru mózgu czy niewydolności serca jest proporcjonalna do wielkości ry-
zyka, zależnego od wzrostu ciśnienia tętniczego, to w przypadku choroby
wieńcowej, obniżenie ciśnienia tętniczego nie powoduje proporcjonalnie
zbliżonej redukcji ryzyka incydentów wieńcowych (ryzyko ChW związane ze
wzrostem ciśnienia o 5-6 mm Hg wynosi 25%, redukcja – ok. 15%). Nie są
dokładnie wyjaśnione powody takiego stanu rzeczy. Postuluje się niedosza-
cowanie we wcześniejszych badaniach znaczenia nadciśnienia skurczowego,
jako czynnika o większym znaczeniu, niż nadciśnienie rozkurczowe dla ry-
zyka ChW. Być może znaczenie mają niekorzystne efekty metaboliczne,
związane ze stosowaniem w badaniach interwencyjnych nieselektywnych be-
ta-adrenolityków oraz diuretyków. Istotny może być także zbyt krótki czas
obserwacji danej kohorty dla wykazania pełnego efektu interwencji terapeu-
tycznej, związanej z nadciśnieniem tętniczym. Wydają się to potwierdzać dłu-
goletnie obserwacje populacji Framingham. Na wielkość uzyskanej redukcji
ryzyka wpływ ma także z całą pewnością efektywność leczenia NT, wyrażają-
ca się odsetkiem chorych z uzyskaną normotensją, tj. wartościami ciśnienia
tętniczego poniżej 140/90 mm Hg.
Nadciśnienie tętnicze wywiera swój aterogenny wpływ poprzez wiele me-
chanizmów, część z nich ma charakter hemodynamiczny, część zaś związana
jest z zaburzeniami humoralno-metabolicznymi. Wysokie ciśnienie wywiera
bezpośredni, uszkadzający wpływ na ścianę naczyniową, w rezultacie lipo-
proteiny niskiej gęstości (LDL) łatwiej wnikają do ściany naczyniowej. Wyso-
kie ciśnienie tętnicze może być także czynnikiem wyzwalającym pęknięcie
już wytworzonej blaszki miażdżycowej, będąc tym samym mechanizmem
72
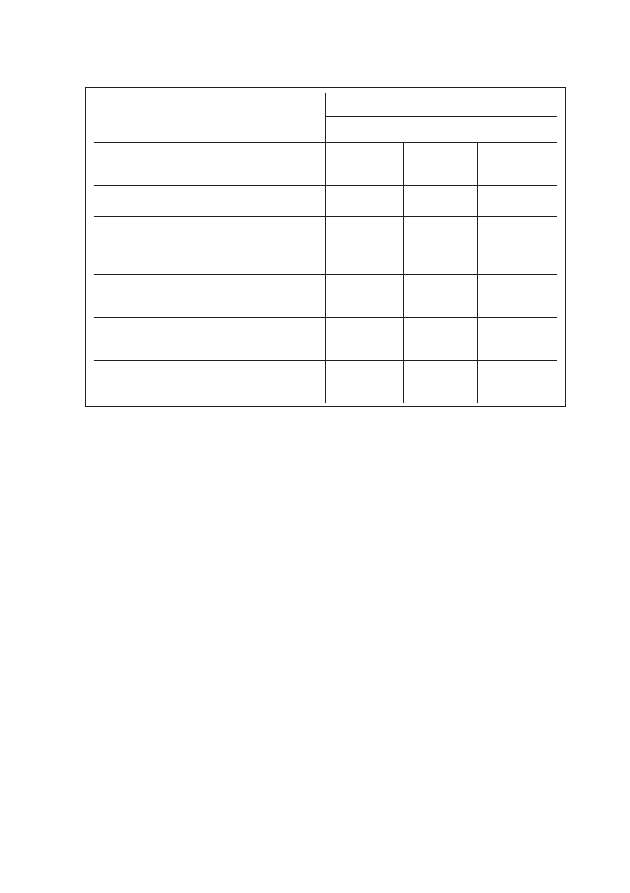
spustowym dla powstania ostrego zespołu wieńcowego. Wpływ uszkadzający
ścianę naczyniową jest związany nie tylko z wielkością ciśnienia, ale także
z licznymi mediatorami chemicznymi, odgrywającymi rolę w patogenezie sa-
mego NT, jak również w patogenezie procesu miażdżycowego w ścianie na-
czyniowej. Wśród wielu mediatorów wymienić należy przede wszystkim an-
giotensynę II, której istotna rola w wielu procesach chorobowych w układzie
sercowo-naczyniowym została udowodniona. Inne ważne substancje biolo-
gicznie aktywne to białka adhezyjne oraz endotelina. Aktywność tych i wie-
lu innych mediatorów powoduje przesunięcie równowagi w kierunku więk-
szej gotowości naczynioskurczowej oraz prowadzi do wzmożenia procesów
proliferacyjnych w ścianie naczyniowej z jednoczesną dysfunkcją wazorelak-
sacji, zależnej od śródbłonkowego tlenku azotu. Tym samym, przyśpieszeniu
ulegają mechanizmy prowadzące do powstania blaszki miażdżycowej. Two-
rzące się blaszki miażdżycowe charakteryzują się większą gotowością do pę-
kania, tzn. wykazują cechy blaszki niestabilnej (vulnerable plaque).
Nadciśnienie tętnicze jest chorobą współistniejącą często z innymi pato-
logiami, które przyspieszają proces aterogenezy. Z NT często współistnieje
otyłość, aterogenna dyslipidemia i upośledzona tolerancja glukozy, będąca
wynikiem insulinooporności. NT często, bo w ponad połowie przypadków,
towarzyszy jawnej cukrzycy, która sama w sobie stanowi pod względem ryzy-
ka naczyniowego stan równoważny z objawową ChW.
73
Tabela 2: Klasyfikacja ciśnienia tętniczego (mm Hg)
KATEGORIA
CIŚNIENIE
skurczowe rozkurczowe
prawidłowe
w tym: optymalne
<130
<120
i
i
<85
<80
wysokie prawidłowe
130-139
i/lub
85-89
nadciśnienie tętnicze
stopień 1 (łagodne)
w tym: graniczne
140-159
140-149
i/lub
i/lub
90-99
90-94
nadciśnienie tętnicze
stopień 2 (umiarkowane)
160-179
i/lub
100-109
nadciśnienie tętnicze
stopień 3 (ciężkie)
³ 180
i/lub
³ 110
izolowane nadciśnienie skurczowe
w tym: graniczne
³ 140
140-149
i
i
<90
<90

CUKRZYCA
Częstość występowania cukrzycy typu 2 wzrasta stosunkowo szybko w kra-
jach rozwiniętych. Wiąże się to m.in. ze zmianami w sposobie odżywiania,
narastającą epidemicznie częstością występowania otyłości, a także niską ak-
tywnością fizyczną. Cukrzyca zwiększa 2-4-krotnie ryzyko chorób naczynio-
wych, w wyniku przyspieszonego rozwoju miażdżycy. Zwiększone ryzyko po-
wikłań ze strony układu krążenia dotyczy zarówno osób z cukrzycą typu 1,
jak i osób z cukrzycą typu 2. Wydaje się jednak, że cukrzyca typu 2 sprzyja
w sposób szczególny rozwojowi powikłań naczyniowych miażdżycy, jest bo-
wiem skojarzona z większą ilością zaburzeń metabolicznych i hemodyna-
micznych. Nie można jednak sprowadzać ryzyka powikłań naczyniowych za-
leżnych od cukrzycy jedynie do faktu skojarzenia tej choroby z innymi
czynnikami ryzyka, bowiem hiperglikemia oraz jej konsekwencje powodują
niezależny wzrost ryzyka. Mechanizmy prowadzące do tego stanu są tylko
częściowo poznane (np. glikacja białek, oksydacja i glikacja LDL, uszkodze-
nie śródbłonka). Zwiększone ryzyko sercowo-naczyniowe, związane z cu-
krzycą jest szczególnie wysokie u kobiet. Cukrzyca wyraźnie znosi kardio-
protekcyjny wpływ hormonalnego profilu płci żeńskiej. Niewyrównane stany
hiperglikemii prowadzą do wzrostu ryzyka powikłań naczyniowych. Stany hi-
perglikemii wiążą się także z częstszym występowaniem NT i zaburzeń lipi-
dowych. Z drugiej strony, ciągle jednak nie dysponujemy całkowicie jedno-
znacznymi dowodami, które wskazałyby, że ścisła kontrola glikemii
zmniejsza ryzyko powikłań makroangiopatycznych cukrzycy (miażdżyca)
w prewencji pierwotnej.
Badania obserwacyjne chorych z cukrzycą bez współistniejącej objawowej
choroby niedokrwiennej serca wskazują, że zagrożenie zawałem serca jest
w tej grupie chorych, co najmniej tak samo duże, jak u pacjentów po przeby-
tym już zawale serca bez cukrzycy. Konsekwencją tego faktu jest powszech-
nie akceptowane stanowisko, wyrażone w standardach postępowania pre-
wencyjnego, które zalicza cukrzycę do stanów równoważnych pod względem
zagrożenia z objawową chorobą wieńcową. Z tym wiąże się zalecenie bar-
dziej agresywnego zwalczania współistniejących z cukrzycą czynników ryzyka
ChW. NT powinno być leczone bardziej rygorystycznie, niż u chorych bez
cukrzycy, a optymalne wartości ciśnienia tętniczego dla osób z cukrzycą po-
winny wynosić poniżej 130/80 mm Hg. Natomiast, jeśli cukrzycy towarzyszy
mikroalbuminuria, to należy ciśnienie obniżać do wartości poniżej 125/75
mm Hg. Zaburzenia lipidowe w cukrzycy odbiegają od typowej hiperchole-
sterolemii i najczęściej przybierają formę tzw. dyslipidemii cukrzycowej. Stan
ten charakteryzuje się podwyższeniem stężenia TG, obniżeniem stężenia
74

cholesterolu HDL oraz stosunkowo nieznacznie podwyższonymi pozioma-
mi cholesterolu LDL. Istotą zaburzeń lipidowych w cukrzycy jest kumulacja
szczególnie aterogennych form lipoprotein, takich jak małe gęste LDL
i remnanty chylomikronów, z jednoczesnym ubytkiem pełnowartościowych
ochronnych lipoprotein HDL (przewaga małych gęstych HDL). Toczy się
obecnie dyskusja, jaka forma farmakoterapii jest bardziej uzasadniona przy
takim układzie zaburzeń lipidowych (statyny czy fibraty), jednak wszyscy są
zgodni co do potrzeby rygorystycznego ich leczenia. Pierwszoplanowym ce-
lem terapii zaburzeń lipidowych pozostaje zgodnie z zaleceniami American
Diabetes Association i standardami NCEP ATP III uzyskanie u chorych na
cukrzycę stężeń cholesterolu LDL poniżej 100 mg/dL. Problem odrębności
patofizjologicznych, klinicznych i terapeutycznych u chorych z cukrzycą
i ChNS przedstawiliśmy szeroko w innym rozdziale.
OTYŁOŚĆ
Nadwaga i otyłość stanowią istotny problem zdrowotny rozwiniętych spo-
łeczeństw. Częstość występowania tych stanów stale narasta wraz z rozwo-
jem cywilizacyjnym i wzrostem zamożności społeczeństwa. W Polsce częstość
rozpoznania nadwagi lub otyłości wynosi ponad 65% zarówno u kobiet, jak
i u mężczyzn (badanie Pol-MONICA).
Prospektywne badania epidemiologiczne wskazują na zwiększone ryzyko
zgonu u osób z nadwagą lub otyłością, głównie za sprawą zwiększonego
prawdopodobieństwa zgonu sercowo-naczyniowego. Istotny wzrost ryzyka
ChUK związany jest z brzusznym typem otyłości, kiedy tkanka tłuszczowa
gromadzi się w obrębie jamy otrzewnej (otyłość centralna lub wisceralna).
Powszechnie przyjętym wskaźnikiem nadwagi/otyłości jest wskaźnik masy
ciała (Body Mass Index – BMI) wyrażony jako stosunek wagi w kg i wzrostu
w m
2
, opisujący ogólny stan zawartości tkanki tłuszczowej w organizmie.
Wartość BMI w zakresie 25-29,9 kg/m
2
oznacza nadwagę, między 30-40 –
otyłość, natomiast BMI > 40 kg/m
2
– oznacza ciężką otyłość. Wzrost ryzyka
ChUK występuje już przy niewielkim stopniu nadwagi, szczególnie gdy jest
to otyłość brzuszna. Wskaźnikiem opisującym ten typ otyłości jest pomiar
stosunku obwodu brzucha i obwodu bioder (waist-hip ratio – WHR). Wskaź-
nik WHR >1,0 u mężczyzn i > 0,85 u kobiet oznacza otyłość typu brzuszne-
go. Innym prostym parametrem opisującym ten typ otyłości jest pomiar ob-
wodu brzucha. Pomiar ten opisuje nadmiar tkanki tłuszczowej wisceralnej,
jeśli obwód brzucha przekracza 102 cm u mężczyzny i 88 cm u kobiety, przy
BMI >25 kg/m
2
.
75

Zwiększone ryzyko rozwoju chorób zależnych od miażdżycy w przypadku
otyłości wisceralnej, związane jest z całym kompleksem zaburzeń metabolicz-
nych, humoralnych i hemodynamicznych, jaki powstaje w związku z nadmier-
nym wzrostem masy ciała. Jednym z głównych mechanizmów odpowiedzial-
nych za ten stan jest insulinooporność i towarzysząca jej hiperinsulinemia.
Otyłości centralnej towarzyszy wzrost aterogennych frakcji cholesterolu
LDL, wzrost stężenia TG, spadek ochronnej frakcji HDL, nasileniu ulega
lipemia poposiłkowa, zaburzony zostaje metabolizm węglowodanów, może
wystąpić jawna cukrzyca. Wraz ze wzrostem stopnia nadwagi dochodzi do
wzrostu ciśnienia tętniczego, a w konsekwencji rozwija się nadciśnienie. Do-
chodzi także do wzrostu gotowości prozakrzepowej, za co odpowiedzialne
są: wzrost stężenia fibrynogenu, czynnika VII oraz PAI-1 (inhibitor aktywa-
tora plazminogenu-1). W latach osiemdziesiątych zespół insulinooporności
skojarzonej z hiperinsulinemią i całym powyżej opisanym kompleksem za-
burzeń metaboliczno-humoralnych został zdefiniowany i opisany przez Re-
avena jako metaboliczny zespół X. Stanowi on wyjątkowo duże zagrożenie
powikłaniami ze strony układu sercowo-naczyniowego (tab. 3). Należy pod-
kreślić, że niekorzystne zmiany metaboliczne związane z zespołem X poja-
wiają się przy nadmiernym gromadzeniu tkanki tłuszczowej w jamie otrzew-
nej, nawet wówczas, kiedy nie towarzyszy temu procesowi bezwzględny,
istotny wzrost wskaźnika BMI. Częstość występowania zespołu metabolicz-
nego narasta w społeczeństwach rozwiniętych, co wiąże się z rozpowszech-
nieniem otyłości w tych populacjach. Zmianom tym towarzyszy, w zakresie
zaburzeń lipidowych, stopniowe zmniejszanie się częstości występowania izo-
lowanej hipercholesterolemii, a coraz powszechniejsze występowanie zabu-
rzeń lipidowych, typowych dla zespołu metabolicznego, określanych jako
aterogenna dyslipidemia (tab. 4). Stąd też jednym z najistotniejszych zadań
w prewencji pierwotnej staje się walka z otyłością, która stanowi mechanizm
76
Tabela 3: Metaboliczny zespół X
• nadciśnienie tętnicze;
• otyłość;
• hiperinsulinizm i insulinooporność;
• zaburzenia tolerancji glukozy/cukrzyca;
• niskie stężenie cholesterolu HDL;
• wysokie stężenie lipoproteiny (a);
• hiperurykemia;
• nadkrzepliwość (hiperfibrynogenemia, wzrost PAI-1).
spustowy dla powstania zespołu metabolicznego, cukrzycy typu 2 oraz „ze-
społu niskiego HDL”.
CZYNNIKI NIEMODYFIKOWALNE
Wiek i płeć
Ryzyko ChW narasta wraz z wiekiem. Szczególnie dynamiczny wzrost ry-
zyka jest zauważalny u mężczyzn pomiędzy 45., a 60. rokiem życia. Ten wzrost
ryzyka uzależniony jest od nasilania się metabolicznych czynników ryzyka
w tym okresie. Dla odmiany warto podkreślić, że u osób powyżej 80. roku
życia, zarówno u kobiet, jak i u mężczyzn, wpływ poszczególnych czynników
oraz ich zsumowany efekt, zwiększający ryzyko wieńcowe nie jest już zna-
mienny.
Płeć kobieca jest czynnikiem kardioprotekcyjnym do momentu menopau-
zy, następnie ryzyko ChW u kobiet w ciągu kolejnych 10 lat szybko wyrównu-
je się z ryzykiem mężczyzn. Większość standardów przyjmuje wiek >45 lat
dla mężczyzn i >55 lat dla kobiet, jako niezależny czynnik ryzyka ChW.
Od dłuższego czasu czynione są próby stosowania hormonalnej terapii za-
stępczej w prewencji zdarzeń sercowo-naczyniowych, ale jak pokazują wyni-
ki ostatnich badań, nie ma przekonujących dowodów na skuteczność takiego
postępowania w prewencji pierwotnej i wtórnej ChW u kobiet.
Obciążający wywiad rodzinny
Wczesne (< 55. roku życia u mężczyzn, < 65. roku życia u kobiet) wystę-
powanie w rodzinie, u krewnych pierwszego stopnia, choroby wieńcowej lub
innych chorób naczyniowych na tle miażdżycy, uważane jest za silny czynnik
ryzyka ChW. Predyspozycje te są w znacznej mierze determinowane gene-
tycznie. Ta determinacja może dotyczyć ekspresji genotypowej, warunkującej
występowanie czynników ryzyka (np. geny odpowiedzialne za syntezę apo-
lipoprotein B, E, apolipoproteiny (a) i in.). Może też ona być związana z po-
77
Tabela 4: Aterogenna dyslipidemia
• cholesterol LDL: 130-159 mg/dL;
• łagodne lub umiarkowane podwyższenie stężenia trójglicerydów·
(150-200 mg/dL lub 250-500 mg/dL);
• wzrost podfrakcji małych gęstych cząsteczek LDL;
• obniżenie stężenia cholesterolu HDL.

limorfizmem niektórych genów (np. genu konwertazy angiotensyny I, angio-
tensynogenu, receptora dla angiotensyny II), modulujących wiele procesów
odpowiedzialnych za powstawanie zmian w układzie sercowo-naczyniowym
(m.in. odpowiedź zapalna, proliferacja błony wewnętrznej, przerost mię-
śniówki naczyń, przerost mięśnia sercowego) w odpowiedzi na różne bodźce
uszkadzające.
Możliwości zastosowania szerokiej diagnostyki genetycznej w prewencji
pierwotnej są jeszcze bardzo ograniczone.
INNE CZYNNIKI RYZYKA
Czynniki psychospołeczne
Sprawność radzenia sobie w sytuacjach stresowych uwarunkowana jest ce-
chami indywidualnymi oraz warunkami otoczenia. Oba aspekty funkcjono-
wania społecznego wywierają istotny wpływ na ryzyko rozwoju ChUK. Dane
z badań prospektywnych sugerują, że wpływ czynników psychosocjalnych
na ryzyko ChW jest niezależny od klasycznych czynników ryzyka, takich jak
ciśnienie tętnicze i stężenie cholesterolu LDL i HDL. Wśród indywidual-
nych cech zachowania najbardziej związane z ryzykiem ChW jest poczucie
wrogości (hostility). Występowanie depresji również zwiększa zagrożenie in-
cydentami wieńcowymi. Sposób zachowania, sprzyjający ryzyku ChW, może
również obejmować te elementy zachowania, które w bezpośredni sposób
wiążą się z klasycznymi czynnikami ryzyka (styl życia: palenie, niezdrowa
dieta, nadużywanie alkoholu, mała aktywność fizyczna). Czynniki środowi-
skowe, sprzyjające wystąpieniu ChW, związane są z warunkami wykonywania
pracy zawodowej, do których zaliczyć należy wysokie wymagania w zakresie
kompetencji w połączeniu z dużym stresem czasowym, a także niewielkie
możliwości decyzyjne dotyczące własnej pozycji zawodowej. Ryzyko ChW
wykazuje także wzrastający „gradient” w kierunku mniej zamożnych warstw
społecznych, co może być związane z warunkami pracy opisanymi powyżej,
a częściej dotyczącymi tej warstwy społecznej. Zjawisko to może też odzwier-
ciedlać niski poziom samooceny związany ze słabą zdolnością radzenia sobie
w sytuacjach stresowych, w połączeniu z wysokim poziomem wrogości
i zwiększoną częstością występowania depresji. Niski status społeczny czę-
ściej wiąże się również z niekorzystnymi nawykami, dotyczącymi sposobu od-
żywiania, paleniem tytoniu, nadużywaniem alkoholu i małą aktywnością fi-
zyczną.
W wyniku odpowiedzi behawioralnej na stres otoczenia, postulowane są
różne mechanizmy pośredniczące we wzroście ryzyka ChW. Najprawdopo-
78

dobniej mechanizmy te związane są z nieprawidłową odpowiedzią neurohu-
moralną organizmu na stres (zwiększone napięcie układu sympatycznego,
gotowość prozakrzepowa).
Mała aktywność fizyczna
Mała aktywność fizyczna jest od dawna rozpoznanym, niezależnym czyn-
nikiem ryzyka ChW. Niekorzystny wpływ braku wysiłku fizycznego zwięk-
szający ryzyko ChUK jest m.in. rezultatem obniżenia stężenia cholesterolu
HDL i zwiększenia gotowości prozakrzepowej. Mała aktywność fizyczna
często wiąże się także z otyłością, zwiększonym stężeniem TG oraz wyższy-
mi wartościami ciśnienia tętniczego. Z drugiej strony, nawet niewielki
wzrost aktywności fizycznej związany jest ze zmniejszeniem umieralności
zarówno sercowo-naczyniowej, jak i umieralności pozasercowej. Dobro-
czynny wpływ wysiłku fizycznego związany jest po części ze zmianami wspo-
mnianych wcześniej czynników metaboliczno-humoralnych, a w szczegól-
ności zapobiega powstawaniu otyłości. Ponadto pomaga zredukować
istniejącą nadwagę, wpływa korzystnie na profil lipidowy – powodując istot-
ny spadek stężenia TG, umiarkowane obniżenie stężenia LDL oraz norma-
lizację ich składu (spadek podfrakcji małych gęstych LDL) oraz wzrost
HDL. Wysiłek fizyczny powoduje także obniżenie ciśnienia tętniczego,
zwiększa aktywność przywspółczulnej składowej układu wegetatywnego, co
manifestuje się zwiększeniem zmienności rytmu serca – heart rate variabili-
ty (HRV). U osób z zespołem metabolicznym, wysiłek fizyczny redukuje in-
sulinooporność, korzystnie modyfikując tym samym osiowe zaburzenia
w tym zespole.
Wysiłek fizyczny stanowi jeden z podstawowych elementów rehabilitacji
chorych po zawale serca ze względu na wspomniane wcześniej przesłanki,
a także ze względu na korzystny wpływ na psychikę chorego (zmniejszenie
napięcia emocjonalnego, poprawa nastroju, lepsza samoocena). Choć czy-
nione były próby oceny wpływu kontrolowanego treningu fizycznego na ry-
zyko zdarzeń wieńcowych, nie ma w chwili obecnej jednoznacznych badań
potwierdzających – niezależny od innych czynników – wpływ kontrolowa-
nego treningu fizycznego na redukcję ryzyka wieńcowego u chorych po
przebytym incydencie wieńcowym (trudność z oddzieleniem efektu trenin-
gu, od zmian w zakresie innych czynników modyfikujących styl życia, m.in.
diety, redukcji masy ciała, zaprzestania palenia). Badania obserwacyjne
wskazują wyraźnie na protekcyjne działanie wysiłku fizycznego w prewen-
cji pierwotnej ChW. Aktywność fizyczna jest dziś traktowana jako lek XXI
wieku, w związku z tym poświęcamy tej kwestii dwa rozdziały tego pod-
ręcznika.
79

Czynniki trombogenne
Zwiększona gotowość zakrzepowa może stanowić czynnik wyzwalający ob-
jawy ostrego zespołu wieńcowego. Badania epidemiologiczne wskazują, że
zwiększone ryzyko incydentów wieńcowych dotyczy osób z podwyższonymi
poziomami niektórych czynników układu krzepnięcia i fibrynolizy. Szczegól-
nie wyraźny związek zagrożenia ChW dotyczy podwyższonych stężeń fibry-
nogenu. Wymienia się kilka możliwych mechanizmów, wiążących proces ate-
rotrombozy z fibrynogenem:
Przyczyny zwiększonego stężenia fibrynogenu mogą być bardzo różne, począw-
szy od uwarunkowań genetycznych, poprzez procesy zapalne. Zwiększone stęże-
nie fibrynogenu związane jest także z wiekiem, paleniem papierosów, cukrzycą,
otyłością brzuszną, zespołem metabolicznym, wysokim stężeniem TG, menopau-
zą. Odwrotna zależność występuje pomiędzy stężeniem fibrynogenu, a stężeniem
cholesterolu HDL, aktywnością fizyczną oraz przyjmowaniem estrogenów.
Mniej jednoznaczny, choć potwierdzony w niektórych badaniach, jest zwią-
zek z ryzykiem wieńcowym innych czynników układu krzepnięcia, takich jak
poziom czynnika VII, czy zwiększone stężenie inhibitora aktywatora plazmi-
nogenu 1 (PAI-1).
Stan zwiększonej gotowości płytek do agregacji może być wynikiem od-
działywania bardzo wielu czynników i z całą pewnością zwiększa zagrożenie
incydentami wieńcowymi. Dowodzi tego korzystny wpływ leków hamujących
agregację (kwas acetylosalicylowy, tiklopidyna, klopidogrel), zmniejszający
ryzyko incydentów wieńcowych w prewencji wtórnej. Nie ma jednak do-
brych, standaryzowanych metod do oceny agregacji płytek – stąd trudność
w jednoznacznej ocenie stopnia ryzyka związanego z jej zaburzeniami.
Hiperhomocysteinemia
Homocysteina jest aminokwasem powstającym w organizmie z metioniny.
Jest związkiem toksycznym i jako taki, jest szybko metabolizowana do cyste-
iny lub w procesie metylacji z powrotem przekształcana do metioniny. Ko-
faktorami tych reakcji są witaminy z grupy B (kwas foliowy, witamina B
12
,
witamina B
6
). U osób z homocysteinurią uwarunkowaną genetycznie, szybko
rozwija się zaawansowana miażdżyca. Rola homocysteiny w rozwoju miaż-
80
• wpływ na parametry reologiczne krwi;
• nasilenie agregacji płytek;
• zwiększone tworzenie trombiny;
• stymulacja migracji i proliferacji komórek mięśni gładkich tętnicy.

dżycy związana jest głównie z jej cytotoksycznym wpływem na śródbłonek
naczyniowy, a także z nasileniem pod wpływem tego aminokwasu procesów
zakrzepowych i modyfikacją lipoprotein LDL. Homocysteina podwyższa
także stężenie białka CRP.
Zwiększone stężenie homocysteiny może być uwarunkowane mutacjami ge-
nów odpowiedzialnych za metabolizm homocysteiny (reduktaza metylenotetra-
hydrofolianowa) lub nabytymi niedoborami wspomnianych witamin z grupy B.
Wyniki badań obserwacyjnych i klinicznych potwierdzają związek pomię-
dzy podwyższonymi stężeniami homocysteiny, a zwiększonym ryzykiem ChW,
a także miażdżycy w naczyniach kończyn dolnych i mózgu. Związek ten jest
nieco słabiej zaznaczony, choć nadal obecny w badaniach prospektywnych.
Hiperhomocysteinemia szczególnie wyraźnie nasila ryzyko ChW u osób palą-
cych papierosy, z nadciśnieniem tętniczym lub hiperlipidemią. Substytucja
witaminowa, a szczególnie podawanie kwasu foliowego, obniża stężenia ho-
mocysteiny (o ok. 30%). W niektórych krajach (USA) kwas foliowy dodawa-
ny jest do mąki. Nie wiadomo jednak, czy tego typu interwencja zmniejsza
zagrożenie ChW, związane z podwyższonymi stężeniami homocysteiny. Nie
są też jednoznacznie określone stężenia homocysteiny, które należy uznać za
podwyższone (stanowisko IAS: >12
mmol/l, stanowisko AHA: >10 mmol/l).
Markery zapalne
Od dawna wiadomo, że miażdżyca może być rozpatrywana jako rodzaj
przewlekłego stanu zapalnego w odpowiedzi na czynniki uszkadzające ścia-
nę naczyniową (np. zmodyfikowane lipoproteiny LDL). Aktywność procesu
zapalnego w obrębie blaszki miażdżycowej jest w znacznej części odpowie-
dzialna za powstanie niestabilności blaszki miażdżycowej. Miernikiem aktyw-
ności tego procesu może być m.in. zwiększona temperatura blaszki (blaszki
„gorące”).
CRP (C-reactive protein) należy do białek ostrej fazy, jest wydzielane przez
wątrobę pod wpływem krążących cytokin (interleukina 6). Jego niewielki,
„podprogowy” wzrost jest możliwy do wykrycia technikami oznaczeń wyso-
kiej czułości. Wydaje się prawdopodobne, że ten nieznacznie podwyższony
poziom CRP, związany jest z aktywnością procesu zapalnego w blaszce miaż-
dżycowej, a więc odzwierciedla zwiększone ryzyko jej pęknięcia i powstania
objawów ostrego zespołu wieńcowego. W ostatnich latach pojawiło się wie-
le prac wskazujących na dodatnią korelację nieswoistych wykładników sta-
nu zapalnego, takich jak białko C-reaktywne, ze zwiększonym ryzykiem incy-
dentów wieńcowych, także incydentów niedokrwiennych mózgu oraz
w naczyniach obwodowych. Z drugiej strony wykazano, że statyny poza wpły-
wem na parametry lipidowe obniżają także stężenie CRP, a spadek jego po-
81

ziomu związany jest z redukcją incydentów wieńcowych, niezależną od
zmian w stężeniach lipidów. Tym samym wykazano, że statyny posiadają do-
datkowe, nieswoiste działanie przeciwzapalne, które jest istotne dla redukcji
ryzyka wieńcowego. Także inne parametry stanu zapalnego, poczynając od
tych najprostszych jak OB, leukocytoza, stężenia fibrynogenu, poprzez po-
ziom amyloidu A, cytokin (IL-6, TNF-alfa), a także stężenia niektórych czą-
stek adhezyjnych (ICAM-1), korelują z ryzykiem incydentu wieńcowego,
wskazując wyraźnie na rolę procesu zapalnego w patogenezie ostrych zespo-
łów wieńcowych (acute coronary syndromes – ACS). Aktywacja procesów za-
palnych może być nasilana pod wpływem czynników infekcyjnych, jednak
nie ustalono jednoznacznej roli tych czynników w patogenezie ACS.
CO ZROBIĆ, ŻEBY NIE ZACHOROWAĆ
NA CHOROBĘ WIEŃCOWĄ?
Rozpoznanie czynników zwiększających zagrożenie ChW, ustalenie zasad
postępowania w celu ich redukcji, wreszcie szerokie propagowanie wiedzy
w tym zakresie, pozwoliły odwrócić narastające zagrożenie epidemią ChUK,
a ChW w szczególności. Nasza wiedza dotycząca czynników wpływających
na zagrożenie ChW podlega stałej ewolucji, prowadzi do modyfikacji obo-
wiązujących standardów postępowania, zarówno w prewencji pierwotnej, jak
i w prewencji wtórnej. Podstawą działań w prewencji pierwotnej powinna
być strategia populacyjna. Działania prewencyjne muszą objąć możliwie jak
najszersze kręgi społeczeństwa i powinny dotyczyć przede wszystkim zmian
stylu życia, a w szczególności: zmian w sposobie żywienia, redukcji palenia
papierosów, wzrostu aktywności fizycznej. W celu upowszechnienia tych za-
leceń powinny być wykorzystywane środki masowego przekazu, szkoły, or-
ganizacje społeczne.
Ustalono cele żywieniowe dla populacji krajów europejskich, określające
pożądane proporcje składników żywieniowych (tab. 5). Warunkiem ich
wprowadzenia jest popularyzacja praktycznej wiedzy na temat zdrowej diety
(ryc. 2) oraz upowszechnienie innych zachowań prozdrowotnych. W naszym
zespole opracowaliśmy „dekalog kardiologiczny” (tab. 6), ważne jest jednak
przede wszystkim, aby stosować jego zalecenia.
Bardzo istotnym elementem prozdrowotnego stylu życia jest odpowiednio
wysoki poziom aktywności fizycznej. Należy w związku z tym promować pro-
gramy treningowe i stwarzać warunki dla szerokiego z nich korzystania, za-
równo przez ludzi zdrowych, jak i przez osoby z obecną już ChW. Duża ak-
tywność fizyczna (tygodniowy wydatek energetyczny 1500-2000 kcal) jest
obok diety, optymalną metodą walki z kompleksem metabolicznych czynni-
ków (zaburzenia lipidowe, insulinooporność, zmniejszenie gotowości proza-
82
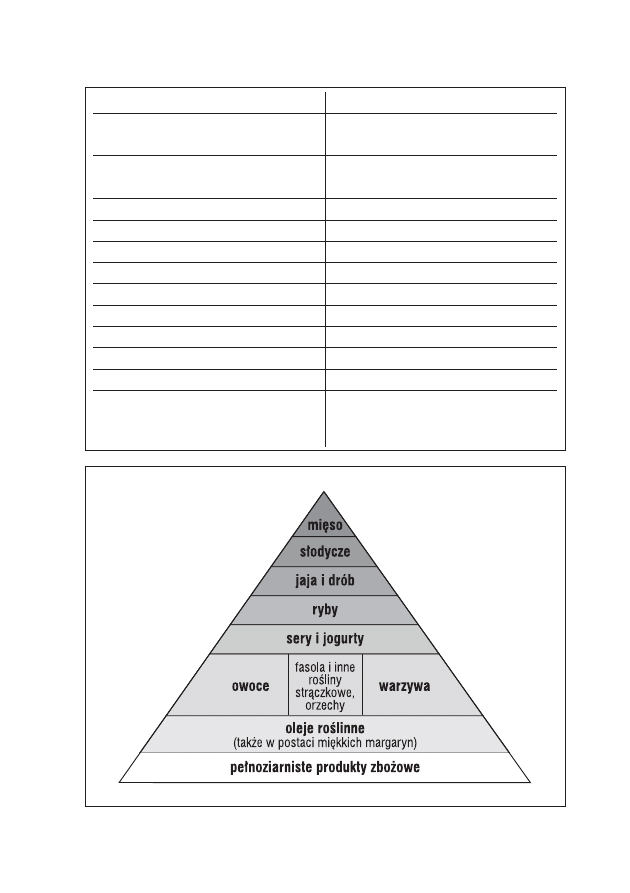
83
Tabela 5: Cele żywieniowe dla populacji krajów europejskich
tłuszcz całkowity
< 30% energii (cel ostateczny)
nasycone kwasy tłuszczowe
(łącznie z kwasami trans)
< 10% energii
nienasycone kw. tłuszczowe
w tym kwasy wielonienasycone
< 20% energii
(cel ostateczny) 3-7% energii
kwasy tłuszczowe trans
obniżyć spożycie
cholesterol
< 300 mg/dzień
skrobia
> 50% energii
cukry proste
obniżyć spożycie
błonnik pokarmowy
27-40 g/dzień
sól
< 6 g/dzień
leguminy, orzechy, nasiona
> 30 g/dzień
owoce i warzywa
> 400 g/dzień
ryby
> 20 g/dzień
mięso i produkty mleczarskie
zmniejszyć spożycie tłustych mięs
i pełnotłustych produktów
mleczarskich, jeżeli jest wysokie
Rycina 2: Piramida zdrowego żywienia

krzepowej). Poza tym stanowi także element niefarmakologicznego lecze-
nia nadciśnienia tętniczego, szczególnie jego postaci łagodnej, a więc tej,
z którą spotykamy się najczęściej.
Istotnym elementem w postępowaniu niefarmakologicznym, zarówno
w przypadku ustalonego NT, jak również w jego prewencji, jest ogranicze-
nie spożycia sodu, natomiast zwiększenie w diecie zawartości potasu, a tak-
że wapnia i magnezu. Należy również ograniczać spożycie alkoholu.
Trzeba dążyć do ograniczenia nałogu palenia tytoniu poprzez akcje oświa-
towe, odpowiednią politykę cenową kształtującą sprzedaż papierosów oraz
tworzenie poradni przeciwtytoniowych.
84
Tabela 6: „Dekalog kardiologiczny”
1 NIE PAL – nikotyna zwiększa ryzyko miażdżycy,
choroby wieńcowej, zawału serca, chorób nowotworowych.
2 UNIKAJ NADMIARU ALKOHOLU – jeśli czasem sięgniesz po
kieliszek – wybierz czerwone wino.
3 ODŻYWIAJ SIĘ ZDROWO – jedz mniej tłuszczów
zwierzęcych, mięsa i słodyczy, a więcej ryb, owoców i warzyw.
4 ZWIĘKSZ AKTYWNOŚĆ RUCHOWĄ – korzystaj z roweru,
biegaj, graj w tenisa. Wybierz sport, który najbardziej Ci
odpowiada, bądź w tym systematyczny.
5 ZWAŻ SIĘ – gdy masz nadwagę, spróbuj z nią sobie radzić.
Wyznacz cele (waga należna) i terminy – nie spiesz się, ważne,
by redukcja wagi była trwała, nie szybka.
6 NIE OSIĄGAJ SUKCESÓW ZA KAŻDĄ CENĘ (ZDROWIA)
– rywalizuj mądrze, nie walcz, poszukaj radości także poza pracą
(rodzina, hobby).
7 SPRÓBUJ RADZIĆ SOBIE ZE STRESEM – gdy masz
trudności, poradź się psychologa.
8 ZBADAJ POZIOM CHOLESTEROLU I CUKRU – konsultuj
wyniki z lekarzem.
9 CZĘSTO MIERZ CIŚNIENIE TĘTNICZE – skorzystaj
z porady lekarza, gdy jest podwyższone. Systematycznie przyjmuj
leki, nigdy nie odstawiaj ich sam.
10 SKORZYSTAJ Z BADAŃ KARDIOLOGICZNYCH – po tym
„przeglądzie” lekarz poradzi Ci, co masz zmienić.
Szereg prospektywnych badań udowodniło, że pomimo silnych przesłanek
teoretycznych i doświadczalnych, stosowanie witamin antyoksydacyjnych
w postaci suplementów żywieniowych, nie przynosi żadnych korzyści i nie
zmniejsza ryzyka ChW lub innych chorób naczyniowych, co więcej – stoso-
wanie tych witamin może być w niektórych sytuacjach wręcz szkodliwe. Dla-
tego w chwili obecnej, jedyne zalecenie dotyczące antyoksydantów, określa
potrzebę stosowania ich w postaci naturalnej, jako elementu diety (dieta bo-
gata w warzywa i owoce, dieta śródziemnomorska).
Kolejnym ważnym celem w prewencji pierwotnej jest wyselekcjonowanie gru-
py osób podwyższonego ryzyka ChW. W tym celu należy wykonywać badania
przesiewowe, ukierunkowane na podstawowe czynniki ryzyka, przede wszyst-
kim na wykrycie zaburzeń lipidowych i NT. NT jest bardzo powszechne (ponad
połowa dorosłej populacji), ciągle jednak daleko niewystarczająca jest skutecz-
ność jego rozpoznawania oraz leczenia. W badaniu Pol-MONICA skuteczność
leczenia NT wyniosła mniej niż 10%! Należy więc pamiętać o tym, aby w trak-
cie rutynowej wizyty lekarskiej, dokonywać pomiaru ciśnienia tętniczego. Co
5 lat należy także dokonywać u osób dorosłych (> 20 r. ż.) pomiaru stężenia
cholesterolu całkowitego. Konieczne jest oznaczenie pełnego profilu lipidowe-
go u osób z cholesterolem całkowitym > 230 mg/dL, w przypadkach współist-
niejącego NT, otyłości, cukrzycy, a także palenia papierosów. W chwili obec-
nej rutynowo oznaczany jest cholesterol całkowity, stężenie HDL oraz TG.
85
Tabela 7: Kategorie ryzyka epizodu wieńcowego
RYZYKO
ŁAGODNE
RYZYKO
UMIARKO-
WANE
RYZYKO
DUŻE
RYZYKO
BARDZO DUŻE
• jeden
lub dwa
łagodne
czynniki
ryzyka
• jeden
umiarkowany
czynnik
ryzyka
• jeden silny
czynnik
ryzyka
lub
• dwa
umiarkowane
czynniki
ryzyka
• przynajmniej jeden
bardzo silny
czynnik ryzyka
(głównie ChNS)
lub
• przynajmniej dwa
silne czynniki ryzyka
lub
• przynajmniej trzy
umiarkowane
czynniki ryzyka
86
Tabela 8: Podział czynników ryzyka
CZYNNIKI
RYZYKA
ŁAGODNE
• LDL: 130-159 mg/dL (3,4-4,1 mmol/L);
(TC: 200-239 mg/dL; 5,2-6,2 mmol/L);
• RRs: 140-159 mm Hg,
i/lub
• RRd: 90-99 mm Hg.
UMIARKOWANE
• palenie papierosów;
• LDL: 160-210 mg/dL (4,1-5,4 mmol/L),
(TC: 240-300 mg/dL; 6,2-7,8 mmol/L);
• HDL:
£ 35 mg/dL u mężczyzn (0,9 mmol/L),
£ 40 mg/dL u kobiet (1,0 mmol/L);
• RRs: 160-179 mm Hg, i/lub·RRd: 100-109 mm Hg,
– mężczyzna
³ 45 lat,
– kobieta
³ 55 lat,
– przedwczesna menopauza,
– przedwczesne występowanie IHD lub chorób
tętnic obwodowych na tle miażdżycy
u krewnych 1. stopnia,
– krewni mężczyźni < 55 r. życia,
– krewne kobiety < 65 r. życia.
SILNE
• 20 lub więcej papierosów dziennie;
• LDL-chol: > 210 mg/dl (5,4 mmol/L),
(TC: >300 mg/dL; 7,8 mmol/L);
• RRs
³ 180 mm Hg,
i/lub
• RRd
³ 110 mm Hg.
BARDZO SILNE
• choroba niedokrwienna serca;
• klinicznie udokumentowane choroby innych tętnic;
• hiperlipidemia rodzinna;
• cukrzyca.
RRs – ciśnienie tętnicze skurczowe; RRd – ciśnienie tętnicze rozkurczowe

Stężenie cholesterolu LDL obliczane jest ze wzoru Friedewalda, o ile stężenie
TG nie przekracza 400 mg/dL. Do oznaczeń stężenia TG wymagane jest, aby
pacjent był co najmniej 14 godzin na czczo. W przypadku oznaczania stężeń
cholesterolu nie jest to konieczne, ale trzeba pamiętać, że jego stężenie obniża
się w przypadku ostrych chorób zakaźnych, po operacjach i po zawale serca,
powracając do stanu wyjściowego dopiero po ok. 6 tygodniach.
W określonych grupach ryzyka, celowe może być także oznaczanie przygodnej
glikemii lub wykonywanie testu obciążenia glukozą w celu wykrycia cukrzycy.
Do niedawna o tym, na ile intensywne powinno być postępowanie zapobie-
gawcze, decydował fakt przebycia ostrego epizodu wieńcowego lub obecność
objawów ChW. W ten sposób prewencję dzielono arbitralnie – na pierwotną
(przed wystąpieniem incydentu wieńcowego) oraz wtórną (po incydencie). Po-
dział ten do pewnego stopnia był uzasadniony, bowiem chorzy po zawale serca
są grupą, w której ryzyko wystąpienia kolejnych epizodów wieńcowych jest
szczególnie wysokie. Dziś jednak wiadomo, że ograniczenie intensywnych dzia-
łań prewencyjnych jedynie do tej grupy pozostawia poza takim działaniem inne
grupy chorych, których zagrożenie jest równie wysokie. Obecna strategia postę-
powania polega na indywidualnej ocenie całościowego (globalnego) ryzyka dla
każdego pacjenta, w oparciu na wynikach wieloletnich prospektywnych badań
populacyjnych (np. Framingham Study). Opracowane na tej podstawie algoryt-
my pozwalają oszacować 10-letnie ryzyko wystąpienia epizodu wieńcowego,
w oparciu na szeregu obecnych (lub nieobecnych) u danego pacjenta czynników
ryzyka. Istotne w tej ocenie jest uwzględnienie obecności kilku czynników, nawet
o niewielkim nasileniu, gdyż ich współistnienie często powoduje podobne lub
większe zagrożenie ChW, niż pojedynczy, nawet bardzo silny, czynnik ryzyka.
Przydzielenie na tej podstawie pacjenta do grupy wysokiego, umiarkowanego
lub niskiego ryzyka, determinuje intensywność działań prewencyjnych, a przede
wszystkim wskazania do leczenia farmakologicznego (np. leczenie hipolipemizu-
jące, farmakoterapia NT, leczenie przeciwpłytkowe) (tab. 7, 8). Określenie po-
ziomu ryzyka ogólnego determinuje cele terapeutyczne w zakresie poszczegól-
nych czynników ryzyka (np. docelowe stężenia lipidów), określa czas, w jakim
należy wprowadzić interwencję farmakologiczną i wskazuje, jak intensywne po-
winno być to leczenie. Problemem w powszechnym zastosowaniu wypracowa-
nych algorytmów oceny ryzyka (np. algorytmu Framingham) pozostaje brak
możliwości odniesienia ich do każdej populacji (w szczególności dotyczy to Eu-
ropy, gdzie stopień ryzyka istotnie różni poszczególne kraje). Należy także pod-
kreślić potrzebę unifikacji standardów poszczególnych towarzystw naukowych,
które w chwili obecnej różnią się stanowiskami. Wyniki nowych, dużych badań
klinicznych, powodują konieczność aktualizacji dotychczasowych standardów
po to, by skuteczność działań prewencyjnych była coraz większa.
87

Zapamiętaj!
1. Prewencja pierwotna to zespół działań, zmierzających do zmniejszenia ry-
zyka zachorowania, poprzez ograniczanie obecności lub natężenia czynni-
ków ryzyka choroby w populacji.
2. Zidentyfikowano wiele czynników ryzyka ChNS; najistotniejsze z nich to
nadciśnienie tętnicze, zaburzenia lipidowe, palenie tytoniu, cukrzyca, oty-
łość, mała aktywność fizyczna.
3. Udokumentowano ponad wszelką wątpliwość, że walka z czynnikami ry-
zyka ogranicza prawdopodobieństwo zachorowania na wszystkie postacie
kliniczne miażdżycy.
4. Prewencja pierwotna to nie tylko działania farmakologiczne (leczenie cu-
krzycy, hiperlipidemii, nadciśnienia tętniczego – mamy tu wiele bardzo sku-
tecznych leków), ale przede wszystkim działania niefarmakologiczne (walka
z nałogiem palenia tytoniu, zwiększenie aktywności fizycznej, odpowiedni
sposób żywienia); działania te muszą wspierać interwencję farmakolo-
giczną.
5. Prewencja pierwotna możliwa jest wtedy, gdy współpracować będą lekarze, me-
dia, nauczyciele, działacze społeczni, politycy – tylko wówczas przyniesie to spek-
takularne efekty, ograniczy zachorowania i wydłuży życie naszych pacjentów.
Warto przeczytać:
Prevention of coronary heart disease in clinical practice. Recomendations of
the Second Joint Task Force of European and other Societies on Corona-
ry Prevention. Eur. Heart J. 1998; 19: 1434-1503.
Profilaktyka choroby niedokrwiennej serca. Rekomendacje Komisji Profi-
laktyki Polskiego Towarzystwa Kardiologicznego. Kardiologia Polska 2000;
53 suplement.
Executive Summary of the Third Report of the National Cholesterol Educa-
tion Program (NCEP) Expert Panel on Detection, Evaluation and Treatment
of High Blood Cholesterol in Adults (Adult Treatment Panel). JAMA 2001;
285: 2486-2497.
American Diabetes Association: Management of dyslipidemia in adults with
diabetes. Diabetes Care 2001; 24 (supl. 1): 558.
Kardiologia prewencyjna. Red. M. Naruszewicz; Warszawa, 2003.
88

VI.
POSTĘPOWANIE DIETETYCZNE
W CHOROBIE NIEDOKRWIENNEJ SERCA
Małgorzata Kozłowska-Wojciechowska
Prawidłowe żywienie jest jedną z najważniejszych metod profilaktyki miaż-
dżycy i jej klinicznych powikłań. Dzięki zastosowaniu właściwie dobranej
diety możliwe jest obniżenie stężenia lipidów w surowicy, ciśnienia tętnicze-
go oraz stężenia fibrynogenu. Ponadto, dobór właściwych proporcji pomię-
dzy składnikami mineralnymi i witaminami zmniejsza podatność lipoprote-
in na oksydacyjną modyfikację oraz ułatwia utrzymanie niskich poziomów
stężeń homocysteiny. Zachowanie proporcji pomiędzy podażą energii, zgod-
ną z jej zapotrzebowaniem, a jej wydatkowaniem zapobiega nadwadze i oty-
łości, czyli kolejnym, istotnym czynnikom ryzyka nie tylko miażdżycy, ale
i cukrzycy typu 2. Wiadome jest, że cukrzyca jest silnym czynnikiem ryzyka
wczesnego rozwoju zmian miażdżycowych.
W ramach profilaktyki pierwotnej skierowanej do populacji generalnej,
istotne jest promowanie zasad prawidłowego żywienia, które jest szansą na
zmniejszenie ryzyka nie tylko choroby niedokrwiennej serca, ale również
i innych chorób dietozależnych. Natomiast w przypadku pacjentów z choro-
bą niedokrwienną serca, po przebytym zawale czy udarze konieczne jest włą-
czenie leczenia dietetycznego do terapii ogólnej choroby. W praktyce ozna-
cza to, że dieta staje się jednym z istotnych elementów leczenia, oprócz
farmakoterapii, rehabilitacji czy psychoterapii. Zalecenia dietetyczne dla pa-
cjentów są często bardziej restrykcyjne, co jednak nie oznacza, iż niemożliwe
do zastosowania.
Właściwe postępowanie diagnostyczne, zgodne z obowiązującymi standar-
dami Polskiego Towarzystwa Kardiologicznego (PTK), wymaga określenia
czynników ryzyka choroby niedokrwiennej serca, które do niej doprowadzi-
ły i/lub jej towarzyszą. Stąd, konieczne jest ustalenie rodzaju występujących
zaburzeń gospodarki lipidowej i/lub węglowodanowej, a nierzadko również
stężenia fibrynogenu, homocysteiny, czy w przypadku nadwagi lub otyłości,
ocena jej stopnia i rodzaju. Są to wszystko niezbędne informacje nie tylko
do prawidłowego leczenia, ale również prawidłowego określenia zaleceń die-
tetycznych. Ponadto, nierzadko z chorobą niedokrwienną serca współistnie-
ją inne choroby, takie jak nadciśnienie tętnicze, cukrzyca, nieprawidłowy,
siedzący tryb życia, palenie papierosów, czy wykonywanie stresującej pracy.
To kolejne czynniki, które utrudniają skuteczną terapię oraz zagrażają pro-
gresją choroby, a nawet groźnymi dla życia powikłaniami. Dlatego też,
oprócz odpowiednio dobranego leczenia farmakologicznego i dietetyczne-
89

go, należy sugerować pacjentom zmianę stylu życia, gdyż jest to czynnik, któ-
ry jak udowodniono w licznych badaniach, przynosi wymierne korzyści oraz
poprawia skuteczność terapii. Pamiętać przy tym należy, że ustalenie co-
dziennego jadłospisu nie jest rolą lekarza, lecz jest to obowiązek dietetyka.
Lekarz natomiast zobowiązany jest ustalić charakterystykę diety, jaką pa-
cjent powinien zastosować. Kolejnym obowiązkiem lekarza jest przekona-
nie pacjenta o konieczności wprowadzenia zmian w dotychczasowym stylu
życia, wskazanie mu korzyści, jakie ta zmiana powinna spowodować. Lekarz
jest autorytetem dla pacjenta; odbierany jest jako najbardziej wiarygodne
źródło informacji, dlatego tylko w gabinecie lekarskim można najlepiej pa-
cjenta przekonać, umotywować do podjęcia przez niego działań, które po-
mogą w terapii i zapewnią mu poprawę komfortu życia. Lekarz powinien
wskazać mu tę drogę oraz zasugerować kto, jak i gdzie, pomoże mu te zale-
cenia zrealizować.
ZASADY OGÓLNE
Zalecenia dietetyczne, które stanowią podstawę profilaktycznego leczenia
pacjentów z chorobą niedokrwienną serca, są w swych głównych wytycznych
zgodne z zasadami prawidłowego żywienia i sprowadzają się do zalecenia:
RODZAJ ZABURZEŃ LIPIDOWYCH
Aby rozpocząć leczenie pacjenta i określić cel, jaki należy osiągnąć, koniecz-
ne jest ustalenie typu zaburzeń lipidowych, z jakimi ma się do czynienia. Jest
to niezbędne nie tylko w ustaleniu farmakoterapii, ale również założeń le-
czenia dietetycznego. W tabeli 1 zaprezentowano klasyfikację hiperlipide-
mii, w zależności od wzrostu poziomów lipidów i lipoprotein.
90
• spożywania różnorodnych produktów;
• zbilansowania spożywanej żywności z aktywnością fizyczną w celu
utrzymania lub redukcji nadmiaru masy ciała;
• preferowania diety niskotłuszczowej, ubogiej w nasycone kwasy
tłuszczowe i cholesterol pokarmowy, poprzez ograniczanie spoży-
cia tłuszczów zwierzęcych;
• wybierania diety obfitującej w warzywa i owoce oraz pełnoziarni-
ste produkty zbożowe;
• stosowania diety o umiarkowanej zawartości cukru, soli kuchennej
i sodu oraz umiarkowanego picia alkoholu, jeśli są to pacjenci pi-
jący alkohol.

Hiperlipidemia (HLP) może być zarówno pierwotna, jak i wtórna, tzn.
występująca w przebiegu innych chorób, takich jak: niedoczynność tarczy-
cy, przewlekła niewydolność nerek, zespół nerczycowy, żółtaczka zastoino-
wa (łącznie z pierwotną marskością wątroby), szpiczak mnogi, nadużywa-
nie alkoholu, jadłowstręt psychiczny i lipodystrofia. Podwyższone poziomy
lipidów w surowicy krwi mogą występować wtórnie – w trakcie przyjmowa-
nia leków moczopędnych, beta-adrenolityków, retinoidów, kortykostery-
dów, sterydów anabolicznych lub preparatów zawierających progesteron.
Leczenie HLP wtórnej polega przede wszystkim na leczeniu choroby pod-
stawowej.
CELE LECZENIA
Celem leczenia hiperlipidemii pierwotnej powinno być osiągnięcie stężenia
cholesterolu poniżej 200 mg/dL i trójglicerydów poniżej 150 mg/dL. Jednak-
że, zgodnie ze stanowiskiem Europejskiego Towarzystwa Miażdżycowego,
ustalanie celu i sposobu leczenia musi zostać określone zgodnie z indywidu-
alnym ryzykiem pacjenta. Zależy ono od obecności lub nieobecności choro-
by niedokrwiennej serca, rodzinnego jej występowania lub nie, obecności
choroby naczyń obwodowych lub mózgowych oraz od liczby współtowarzy-
szących i stopnia zaawansowania pozostałych czynników ryzyka, innych niż
HLP.
Jeśli stężenie cholesterolu w surowicy krwi przed leczeniem mieści się
w granicach 200-300 mg/dL i nie występują inne, nielipidowe czynniki ryzy-
ka miażdżycy, a stężenie cholesterolu HDL wynosi ponad 58 mg/dL, to wy-
starczającym celem leczenia jest osiągnięcie stężenia cholesterolu całkowite-
go 195-230 mg/dL, a cholesterolu LDL 155-175 mg/dL. Jednakże, jeśli
91
Tabela 1: Klasyfikacja hiperlipidemii
KLASYFIKACJA
(1992 rok)
PODWYŻSZONE STĘŻENIE
lipoprotein
lipidów
hipercholesterolemia
LDL
cholesterol
hiperlipidemia
mieszana
LDL + VLDL
cholesterol
i trójglicerydy
hipertrójglicerydemia
VLDL
trójglicerydy
zespół
chylomikronemii
VLDL
chylomikrony
(w osoczu na czczo)
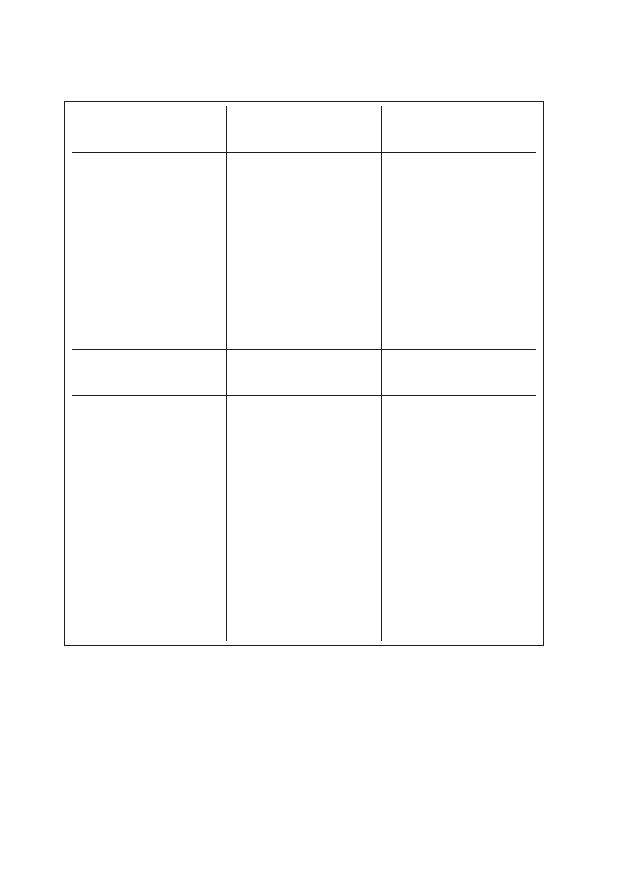
występują inne czynniki ryzyka miażdżycy towarzyszące hipercholesterole-
mii i/lub hipertrójglicerydemii, należy dążyć do osiągnięcia stężenia chole-
sterolu całkowitego, podobnie jak i stężenia trójglicerydów poniżej 200 mg/dL,
natomiast cholesterolu LDL – 115-135 mg/dL. Są to cele do osiągnięcia u lu-
dzi w ramach prewencji pierwotnej.
Według ekspertów Europejskiego Towarzystwa Miażdżycowego optymal-
ne dla regresji miażdżycy i zahamowania progresji zmian są wartości chole-
sterolu całkowitego w granicach 155-175 mg/dL, a stężenie cholesterolu
LDL nie przekraczające 95 mg/dL (2,5 mmol/l).
92
Tabela 2: Wybór metod postępowania w przypadku rozpoznania typu zaburzeń gospodarki lipidowej
(wg B. Cybulskiej i wsp., zalecenia PTK)
Hipercholesterolemia
Hiperlipidemia
mieszana
Hipertrójglice-
rydemia
• redukcja masy ciała,
jeśli istnieje taka
potrzeba;
• redukcja masy ciała;
• „korekta” przyczyn:
– kontrola cukrzycy,
– redukcja spożycia
alkoholu,
– zaprzestanie
stosowania leków
moczopędnych,
beta-adrenolityków
lub retinoidów;
• redukcja masy ciała;
• „korekta” przyczyn
(jak w hiperlipide-
mii mieszanej);
• dieta
hipolipemiczna;
• dieta
hipolipemiczna;
• dieta
hipolipemiczna;
• inhibitory reduktazy
HMG-CoA
(statyny);
• leki przerywające
krążenie kwasów
żółciowych
(żywice);
• fibraty (łagodna
i umiarkowana
hipercholesterole-
mia);
• kwas nikotynowy.
• fibraty, jeśli
dominuje wzrost
TG;
• kwas nikotynowy,
jeśli dominuje
wzrost TG;
• statyny, jeśli
dominuje wzrost
cholesterolu LDL.
• fibraty;
• kwas nikotynowy;
• oleje rybne bogate
w wielonienasycone
kwasy tłuszczowe
omega 3.

Ostatnio opublikowane zalecenia NCEP (National Cholesterol Education
Program) przedstawiają jeszcze inne cele interwencji lipidowych. Jako za-
sadniczy cel interwencji stawiają cholesterol frakcji LDL. U osób wysokiego
ryzyka (ChNS lub jej odpowiedniki) docelowym stężeniem LDL jest cholesterol
tej frakcji poniżej 100 mg/dL. Wartością progową dla interwencji farmakolo-
gicznej jest stężenie przekraczające 130 mg/dL (interwencja ta jest w wybra-
nych przypadkach możliwa przy stężeniach LDL w zakresie 100-130 mg/dL).
Przy braku klinicznej manifestacji miażdżycy, ale przy obecności dwóch czyn-
ników ryzyka docelowe wartości LDL to stężenia poniżej 130 mg/dL, a przy
obecności jednego czynnika ryzyka – poniżej 160 mg/dL. Wszyscy pacjenci
wymagają postępowania dietetycznego lub szerzej – postępowania oparte-
go na tzw. terapeutycznym stylu życia (dieta, aktywność fizyczna, redukcja
otyłości, zaprzestanie palenia tytoniu). Drugorzędowym celem leczenia jest
cholesterol frakcji HDL, którego wartość powinna przekraczać 40 mg/dL,
a u chorych z cukrzycą 45 mg/dL. Wybór leku hipolipemizującego jest zwią-
zany z oceną globalnego ryzyka, rodzajem zaburzeń i wyznaczeniem celów
terapeutycznych. Zasady tego wyboru przedstawiono w drugim tomie Kar-
diologii Praktycznej (Farmakologia Kliniczna).
W tabeli 2 przedstawiono zasady leczenia zaburzeń gospodarki lipidowej
w zależności od typu hiperlipidemii, rekomendowane przez PTK, które nie-
zależnie od rodzaju wybranej farmakoterapii, muszą być poprzedzone i współ-
leczone dietą hipolipemiczną.
DIETA HIPOLIPEMICZNA
Podstawą diety zapobiegającej powstawaniu miażdżycy lub jej progresji,
jest eliminowanie składników sprzyjających chorobie i w to miejsce zastępo-
wanie ich produktami wykazującymi korzystne oddziaływanie. W prawidło-
wej diecie przeciwmiażdżycowej na szczególną uwagę zasługują źródła po-
karmowe tłuszczów. Dieta ta wymaga właściwych proporcji w źródłach
kwasów tłuszczowych nasyconych, jednonienasyconych, wielonienasyconych
oraz trans, gdyż tłuszcze są składnikiem diety, najsilniej oddziałującym
w promowaniu lub zahamowaniu rozwoju miażdżycy. Dlatego temu zagad-
nieniu poświęcony jest odrębny rozdział. Obecnie omówione zostaną ogólne
zasady diety hipolipemicznej.
Węglowodany złożone
W diecie hipolipemicznej, zgodnej z zasadami prawidłowego żywienia,
głównym źródłem energii muszą być węglowodany złożone, które powinny
dostarczać średnio ok. 60% energii. Oznacza to, że każdy prawidłowo zesta-
93

wiony posiłek musi opierać się na produktach skrobiowych, czyli pieczywie
z grubego przemiału, razowym, kaszach, makaronach, ziemniakach oraz ro-
ślinach strączkowych. Uważa się, iż węglowodany te oprócz tego, że są naj-
zdrowszym źródłem energii, dostarczają zarazem błonnika pokarmowego,
witamin i składników mineralnych. Ponadto, im większe ich występowanie
w diecie, tym większa szansa na zmniejszenie pokarmowych źródeł nasyco-
nych kwasów tłuszczowych, które zostają nimi zastąpione. Prowadzi to do
obniżenia stężenia cholesterolu LDL, nie dzięki właściwościom hipolipe-
micznym węglowodanów złożonych, ale ich obecności w diecie.
Zależność pomiędzy spożyciem węglowodanów złożonych, a występowa-
niem choroby niedokrwiennej serca nie jest zależnością prostą, odgrywa jed-
nak zasadniczą rolę. Wielkość spożycia węglowodanów wpływa na spożycie
energii, co z kolei decyduje o nadwadze lub otyłości, szczególnie otyłości ty-
pu centralnego, która wywiera wpływ na stężenie lipidów, przede wszystkim
trójglicerydów oraz odpowiada za poziom glikemii. W wielu eksperymen-
tach stwierdzono, iż wzrostowi podaży energii z węglowodanów, głównie
o niskim indeksie glikemicznym, czyli wysokiej zawartości błonnika pokar-
mowego towarzyszy jedynie umiarkowany wzrost lipemii poposiłkowej,
w pierwszych kilku tygodniach stosowania diety, która jednak ustępuje,
w miarę stosowania takiego żywienia. Liczne badania epidemiologiczne z za-
stosowaniem diety węglowodanowej (w której znacznie przeważają węglo-
wodany złożone) pokazują, iż towarzyszą jej niskie wartości cholesterolu
w surowicy krwi. Ponadto, należy pamiętać, iż zmniejszenie udziału węglo-
wodanów w diecie pociąga za sobą wzrost spożycia tłuszczów lub białek.
U osób z hipertrójglicerydemią należy kontrolować wielkość spożycia wę-
glowodanów, szczególnie prostych (cukru i słodyczy), gdyż dieta wysokowę-
glowodanowa (udział energii z węglowodanów powyżej 60%) może przyczy-
nić się do wzrostu stężenia trójglicerydów. U tych pacjentów substytucja
wysoką podażą jedno- i wielonienasyconych kwasów tłuszczowych w diecie
może być korzystną alternatywą dla zmiany stężenia trójglicerydów. Dieta
węglowodanowa z niskim indeksem glikemicznym, czyli bogata w produkty
zbożowe z pełnego przemiału, dostarczające błonnika pokarmowego, wywo-
łuje korzystny wpływ na stężenie glukozy (obniżający), łącznie z redukowa-
niem poziomu lipidów.
Błonnik pokarmowy
Jak już wspomniano, błonnik pokarmowy dostarczany w produktach wę-
glowodanowych (szczególnie frakcja rozpuszczalna) powoduje redukcję stę-
żenia cholesterolu całkowitego i frakcji LDL.
94

Pierwsza definicja opisująca błonnik pokarmowy sprowadzała się do okre-
ślania go, jako substancji resztkowych pochodzenia roślinnego, które nie
podlegają trawieniu w przewodzie pokarmowym ssaków. Definicja ta obej-
mowała wszystkie, znane składniki określane mianem błonnika, czyli celu-
lozę, hemicelulozę, pektynę i ligniny wraz z gumami i śluzami. Według przy-
należności chemicznej są to związki organiczne, zaliczane do nieskrobiowych
polisacharydów oraz lignin. Obie definicje wskazują jednak, że błonnik po-
karmowy składa się z różnorodnych elementów strukturalnych ścian komór-
kowych roślin.
Spożywana przez człowieka żywność pochodzenia roślinnego odgrywa bar-
dzo zróżnicowaną fizjologiczną rolę, gdyż w produktach pochodzenia roślin-
nego zawarte są liczne związki, oddziałujące różnorodnie na organizm czło-
wieka. Jak pokazują badania nad składem wartości odżywczej żywności
pochodzenia roślinnego, w naszym świecie występują rośliny jadalne o zróż-
nicowanej ilości poszczególnych frakcji błonnika; dzięki temu możliwe jest
przybliżenie jego roli i znaczenia w prawidłowym odżywianiu. Pamiętać jed-
nak należy, że spożywana przez człowieka żywność pochodzenia roślinnego
poddawana jest często różnym obróbkom, czy to technologicznym, czy kuli-
narnym, w konsekwencji czego funkcja fizjologiczna, jak i zawartość poszcze-
gólnych frakcji błonnika, może ulegać zmianom.
Z powodu fizjologicznego oddziaływania błonnika w organizmie człowie-
ka, dokonano jeszcze jednego jego podziału – na frakcje rozpuszczalne i nie-
rozpuszczalne w wodzie. Błonnik rozpuszczalny to pektyny, hemicelulozy,
gumy (występują głównie w owocach i warzywach, w mniejszym stopniu pro-
duktach zbożowych, np. owsie), które podlegają bakteryjnej fermentacji
w przewodzie pokarmowym, wykazując wpływ na przemiany metaboliczne
węglowodanów i tłuszczów. Natomiast frakcję nierozpuszczalną stanowią ce-
luloza, inne hemicelulozy i ligniny (otręby pszenne, rośliny nasion strączko-
wych, kasze), które wywierają wpływ na pracę jelit, zarówno jelita cienkie-
go, jak i jelita grubego, szczególnie okrężnicy. Rola tej frakcji przyczynia się
do przyśpieszania pasażu jelitowego, zwiększania masy stolca, pochłaniania
i wiązania niektórych substancji (również toksycznych) z przewodu pokar-
mowego, a jak pokazała metaanaliza wielu badań epidemiologicznych – ist-
nieje ścisła korelacja pomiędzy zawartością błonnika pokarmowego w die-
cie, a częstością występowania raka jelita grubego.
Funkcja błonnika w prawidłowym żywieniu, to nie tylko poprawa czynno-
ści jelita grubego, poprzez skrócenie czasu pasażu, wzrost masy stolca oraz
regulację procesu defekacji, ale również jego rola w redukcji stężenia chole-
sterolu.
95

Podatność błonnika na procesy fermentacyjne pod wpływem mikroflory
jelitowej decyduje o hamowaniu wątrobowej syntezy cholesterolu. Docho-
dzi do tego dzięki powstawaniu krótkołańcuchowych kwasów tłuszczowych,
takich jak kwas octowy, propionowy, masłowy i kapronowy. Tę zdolność wy-
kazują przede wszystkim pektyna i guma guarowa. Na procesy fermentacyj-
ne całkowicie oporna jest celuloza, która nie posiada zdolności wiązania
kwasów żółciowych. Zdolność wiązania kwasów żółciowych, będących no-
śnikiem cholesterolu, sprawia, że hamowany jest ich zwrotny transport do
wątroby, co wpływa na obniżenie stężenia cholesterolu w surowicy krwi.
Wiązanie kwasów żółciowych przyczynia się również do zmniejszenia lito-
genności żółci.
Obserwacje epidemiologiczne potwierdziły, że populacje odżywiające się
pokarmem bogatym w błonnik pokarmowy mają zwykle mniejsze stężenie
cholesterolu całkowitego, a przede wszystkim cholesterolu frakcji LDL.
Stwierdzono, że warzywa, rośliny strączkowe, otręby owsiane i jęczmienne,
w których przeważają frakcje rozpuszczalne w wodzie, wykazują najskutecz-
niejszy wpływ redukujący stężenia cholesterolu w surowicy krwi. Przyjmuje
się, że zdolność obniżania cholesterolu wynosi średnio od 5-10%, jednakże
istnieją doniesienia, że przy dawkach powyżej 35 g dziennie, można obniżyć
wyjściowe wartości cholesterolu nawet o 25%. Nie stwierdzono natomiast
istotnych zmian we frakcji HDL, pod wpływem działania błonnika. Mecha-
nizm hipolipemicznego wpływu błonnika do końca nie został wyjaśniony.
Najbardziej prawdopodobny jest mechanizm wiązania kwasów żółciowych
w jelicie, jednakże są podnoszone i inne mechanizmy, jak choćby modyfika-
cja (hamowanie) syntezy cholesterolu w wątrobie poprzez krótkołańcucho-
we kwasy tłuszczowe. Przypuszcza się również, że dieta bogata w węglowoda-
ny złożone i błonnik pokarmowy powstrzymuje lipogenezę. Wynika z tego,
że oddziaływanie hipolipemiczne błonnika może być wieloczynnikowe, co
wymaga jeszcze wielu badań.
Wiele prezentowanych od lat badań wskazuje na korzystną rolę błonnika
pokarmowego w redukcji poposiłkowej glikemii oraz odpowiedzi insulino-
wej. Takie działanie błonnika obserwowano u osób zdrowych oraz u pacjen-
tów z różnymi typami cukrzycy. Stwierdzono, że błonnik opóźnia opróżnia-
nie żołądka i jelita cienkiego, powodując zwolnienie odpowiedzi
glikemicznej. Ponadto, przedłużając przebywanie pokarmów w jelitach, po-
woduje zmniejszanie wchłaniania glukozy i trójglicerydów, w efekcie zmniej-
szając zapotrzebowanie na insulinę oraz doustne środki hipoglikemizujące,
jak np. pochodne sulfonylomocznika. Jednym z mechanizmów takiego dzia-
łania jest zwiększenie lepkości treści pokarmowej, poprzez tworzenie żeli,
które zwalniają pasaż w jelicie cienkim. Wykazano, że frakcje błonnika nie-
96

rozpuszczalne w wodzie przyśpieszają, natomiast rozpuszczalne – opóźniają
pasaż treści pokarmowej przez jelito cienkie. Wynika z tego, że dla pacjen-
tów z podwyższonymi stężeniami glukozy i cholesterolu winny być polecane
przede wszystkim jarzyny liściaste, bulwiaste i korzeniowe, płatki owsiane,
mąki razowe oraz kasze i owoce, które są bogatym źródłem rozpuszczalnych
frakcji błonnika pokarmowego. Dla chorych na cukrzycę przyjmuje się, że
dobowe spożycie błonnika pokarmowego powinno wynosić nie mniej niż
15 g na 1000 kcal.
A więc pamiętajmy, że głównymi produktami, dostarczającymi węglowo-
danów złożonych są wyroby z pełnego ziarna oraz nasiona roślin strączko-
wych. Natomiast źródłem błonnika są otręby owsiane, müsli, jęczmień,
owies, nasiona roślin strączkowych, produkty sojowe, jabłka, żurawiny, po-
rzeczki i agrest i wiele innych produktów pochodzenia roślinnego. Produkty
tego typu powinno się spożywać we wszystkich posiłkach codziennie, gdyż
błonnika pokarmowego organizm człowieka nie kumuluje na zapas, a co-
dziennie potrzebuje go od 30 do 40 g.
Warzywa i owoce – źródło witamin
Dieta hipolipemiczna musi być w dużej mierze oparta na warzywach
i owocach. Jest to o tyle konieczne, że warzywa i owoce są nie tylko produk-
tami niskokalorycznymi, ułatwiającymi utrzymanie należnej masy ciała (co
w leczeniu HLP jest nieodzowne), ale są również głównymi źródłami wita-
min antyoksydacyjnych, beta-karotenu i witaminy C oraz flawonoidów. Pa-
miętać należy, że do grupy witamin antyoksydacyjnych zalicza się witaminę
E (rozpuszczalną w tłuszczach), której źródłem są przede wszystkim oleje,
ryby, orzechy, kiełki pszenicy. Nie można jednoznacznie stwierdzić, że wita-
miny te w postaci preparatów suplementujących dietę mają korzystny wpływ
w profilaktyce miażdżycy. Co więcej, istnieje wiele prac, które taką opinię
podważają. Niemniej jednak, istnieje coraz więcej danych badawczych, że
witaminy te w postaci naturalnej (czyli pochodzące z żywności) wykazują ta-
kie działanie. Witaminy te w swym działaniu chronią przed tworzeniem się
wolnych rodników tlenowych oraz ich pochodnych, jak np. nadtlenki lipido-
we i dwutlenek azotu. Znajdujemy w tej chwili coraz więcej dowodów na to,
iż witaminy antyoksydacyjne biorą istotny udział w mechanizmie obronnym
organizmu przeciwko stresowi oksydacyjnemu. Jest to o tyle istotne, iż u pa-
cjentów z hipercholesterolemią, podatność lipidów i lipoprotein osocza na
oksydatywną modyfikację (czyli zdolność tworzenia zmodyfikowanych LDL
o wysokiej aterogenności) wpływa poziom, a szczególnie niedobór witamin:
C, E i karotenoidów.
97

Takie podejście do źródeł witamin antyoksydacyjnych znajduje swoje odzwier-
ciedlenie w najnowszym stanowisku American Heart Association z 1996 ro-
ku, gdzie czytamy: „Suplementy witamin i składników mineralnych nie są
substytutem pod względem odżywczym diety, w której położono nacisk na
spożywanie owoców, warzyw i produktów z pełnego ziarna. Zaleca się, aby
witaminy antyoksydacyjne i inne składniki pokarmowe pochodziły ze źródeł
naturalnych, czyli z żywności”. W indywidualnych przypadkach pacjentów
nie wyklucza się jednak podawania poszczególnych witamin w postaci suple-
mentacji farmakologicznej. Jednakże prawidłowo zestawiona dieta powin-
na zawierać w każdym posiłku owoce i/lub warzywa, w ilości nie mniejszej
jak 400 g dziennie, a hasło „5 razy dziennie warzywa i owoce” oznacza, że
ilość posiłków dla każdego powinna wynosić pięć dziennie.
Alkohol
W ostatnich latach w wielu krajach prowadzone są dyskusje na temat
wpływu alkoholu na redukcję ryzyka miażdżycy i częstości występowania
choroby niedokrwiennej serca. W badaniach prospektywnych wykazano od-
wrotną zależność pomiędzy spożyciem alkoholu, a występowaniem miażdży-
cy zarówno u kobiet, jak i u mężczyzn. Badania te sugerują, że spożywanie
jednego-dwóch „drinków”, czyli 14-28 g etanolu dziennie, prowadzić może
do redukcji ryzyka od 30 do 50%. Dowodów na tę teorię dostarczyły badania
autopsyjne, w których wykazano mniejsze nasilenie zmian miażdżycowych
u ludzi, którzy spożywali umiarkowane ilości alkoholu. Korzystny efekt dzia-
łania alkoholu w zmniejszaniu czynników ryzyka sprowadza się do wzrostu
stężenia cholesterolu HDL oraz prawdopodobnie zmniejszenia agregacji
płytek czy nasilenia fibrynolizy.
Trwa ciągle dyskusja, któremu rodzajowi alkoholu można przypisać tę ro-
lę. Ponieważ udowodniono, iż flawonoidy wykazują działanie antyoksydacyj-
ne, a występują one przede wszystkim w czerwonym winie i ciemnym piwie,
to być może przede wszystkim te dwa gatunki alkoholu wykazują działanie
prewencyjne.
Z tego względu, iż udowodniony jest fakt szkodliwego wpływu alkoholu
na zdrowie i wywoływanie wielu śmiertelnych chorób, zalecanie picia alko-
holu, jako metody prewencyjnej, budzi wiele zastrzeżeń.
ZALECENIA DIETETYCZNE W PREWENCJI WTÓRNEJ
Działania lecznicze z zastosowaniem diety hipolipemicznej w profilaktyce
pierwotnej mają za zadanie zapobiec wystąpieniu i rozwojowi choroby nie-
dokrwiennej serca, a tym samym zawału serca, jako najgroźniejszego jej po-
98
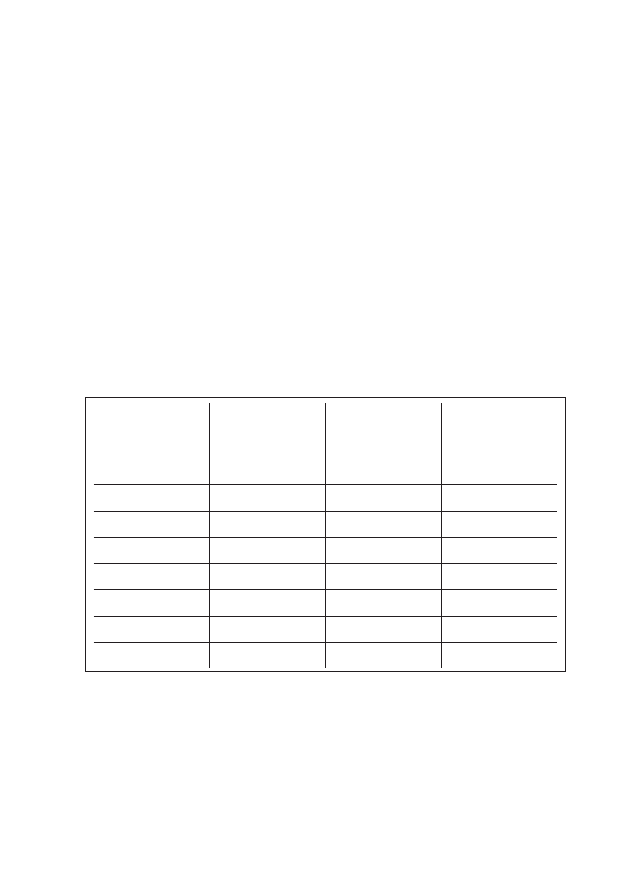
wikłania. Natomiast, w przypadku pacjentów po zawale serca, stosowanie
diety i leczenie zaburzeń gospodarki lipidowej oraz innych czynników ryzyka
ma na celu zmniejszenie powikłań choroby podstawowej, czyli zapobieganie
kolejnym zawałom. Właściwe leczenie dietetyczne pozwala zmniejszyć za-
padalność i umieralność z powodu choroby niedokrwiennej serca oraz no-
we przypadki zachorowań.
Ponieważ w prawidłowo skomponowanej diecie hipolipemicznej, bez
względu na jej kaloryczność, obowiązuje zasada ograniczania tłuszczów ogó-
łem i tłuszczów nasyconych do określonych wartości, w tabeli 3 podano wa-
gowe (w gramach) ilości tych składników, zależnie od kaloryczności diety.
Ponieważ obecnie obowiązuje w naszym kraju konieczność umieszczania na
opakowaniach produktów spożywczych informacji o zawartości tłuszczu ogó-
łem i nasyconych kwasów tłuszczowych, jeśli w danym produkcie występują,
wiedząc ile każdemu wolno ich zjeść, łatwiej obliczyć, czy wybrany produkt
nie spowoduje przekroczenia dobowego zapotrzebowania.
W tabeli 4 podano zawartość tłuszczu ogółem oraz nasyconych kwasów
tłuszczowych w wybranych produktach spożywczych, aby możliwe było zob-
razowanie istoty diet hipolipemicznych.
Ogólne zasady tworzenia diety hipocholesterolemicznej przedstawia tabe-
la 5, natomiast w tabeli 6 podano szczegółowe zalecenia tej diety.
99
Tabela 3: Dozwolone ilości tłuszczu ogółem i nasyconych kwasów tłuszczowych w zależności
od kaloryczności diety i zaleconego udziału energii z tych składników
Kaloryczność
diety
[kcal]
Tłuszcz
ogółem <30 %
[g]
Kwasy
tłuszczowe
nasycone <10%
[g]
Kwasy
tłuszczowe
nasycone <7%
[g]
1200
40 lub mniej
poniżej 13
poniżej 9
1500
50 lub mniej
poniżej 17
poniżej 12
1800
60 lub mniej
poniżej 20
poniżej 14
2000
67 lub mniej
poniżej 22
poniżej 16
2200
73 lub mniej
poniżej 24
poniżej 17
2500
83 lub mniej
poniżej 28
poniżej 19
3000
100 lub mniej
poniżej 33
poniżej 23

100
Tabela 4: Przykładowa zawartość tłuszczu ogółem i nasyconych kwasów tłuszczowych w 100 g wybra-
nych produktów (wg H. Kunachowicz i wsp. 2002)
100 g produktu
Zawartość tłuszczu
ogółem [g]
Zawartość
nasyconych
kwasów
tłuszczowych [g]
mleko 3,5%
3,5
2,10
mleko 1,5%
1,5
0,96
śmietana kremowa
30,0
17,92
masło ekstra
82,5
54,72
margaryna Flora
60,0
12,84
margaryna Planta
100,0
49,55
parówki
34,3
11,65
szynka wiejska
20,3
7,11
szynka z indyka
1,6
0,50
salceson włoski
29,3
11,38
ser Ementaler
29,7
17,74
ser twarogowy chudy
0,5
0,28
serek Fromage z czosnkiem
35,2
23,88
jaja kurze (dwa)
9,7
3,00 (cholesterolu
360 mg)
karp świeży
4,2
0,67
łosoś świeży
13,6
2,94
cielęcina
2,8
1,0
wieprzowina – karkówka
22,8
7,98
wołowina – szponder
15,7
7,52
indyk – pierś bez skóry
0,7
0,22
kurczak udko
10,2
2,88
orzechy włoskie
60,3
6,56
lody śmietankowe
8,5
5,08
czekolada gorzka
34,3
21,35
101
Tabela 5: Dieta obniżająca poziom lipidów
ZASADA
ILOŚĆ
ŹRÓDŁA
POKARMOWE
¯ tłuszczu
całkowitego
<30% energii
unikanie masła, twardych
margaryn, pełnego mleka,
śmietany, lodów, tłustych
serów, tłustego mięsa,
drobiu, ciast, „zabielaczy”
do kawy, produktów
zawierających
uwodornione oleje, olejów
palmowego i kokosowego;
¯ tłuszczu
nasyconego
7-10% energii
spożycia produktów
białkowych o małej
zawartości tłuszczów
nasyconych
ryby, kurczęta, indyki,
cielęcina, dziczyzna,
młode jagnięta;
węglowodanów
złożonych błonnika
owoców i warzyw
roślin strączkowych
około 35 g
błonnika dziennie
(połowa
z owoców
i warzyw)
wszystkie owoce łącznie
z suszonymi, świeże
i mrożone warzywa,
soczewica, suche
strączkowe, nierafinowane
produkty zbożowe, w tym
z owsa;
¯ cholesterolu
pokarmowego
< 300 mg/dzień
dopuszcza się 2 żółtka
tygodniowo i wątróbkę
2 razy w miesiącu;
umiarkowany wzrost
spożycia olejów
bogatych
w jednonienasycone
lub wielonienasycone
kwasy tłuszczowe
omega-3 i omega-6
jednonienasycone
10-15%
oliwa z oliwek, olej
słonecznikowy, sojowy
i pochodne margaryny.
wielonienasycone
7-10%
102
Tabela 6: Dieta hipolipemiczna
PRODUKTY
ZALECANE
PRODUKTY DO
SPOŻYWANIA
W UMIARKO-
WANYCH
ILOŚCIACH
PRODUKTY
PRZECIW-
WSKAZANE
produkty
zbożowe
pieczywo z pełne-
go ziarna, kasze
gruboziarniste,
owsianka,
makaron, maca,
ryż, placki
kukurydziane;
rogaliki
francuskie
(croissant);
produkty
mleczne
mleko odtłusz-
czone, sery o
niskiej zawartości
tłuszczu (np.
chudy twaróg),
jogurt bardzo
nisko tłuszczowy,
białko jaja,
substytuty jaj;
mleko półtłuste,
sery o zmniejszo-
nej zawartości
tłuszczu (np. Brie,
Camembert,
Edamski, Gouda),
jogurt niskotłusz-
czowy, dwa całe
jaja na tydzień;
pełne mleko,
mleko
skondensowane,
śmietana,
zabielacze
do kawy, sery
pełnotłuste,
jogurt
pełnotłusty;
zupy
chude wywary
mięsne, zupy
warzywne;
zupy zagęszczane,
zupy zaprawiane
śmietaną;
ryby
ryby (z rusztu,
gotowane, wędzo-
ne), unikać skóry;
ryby smażone na
właściwym oleju;
ikra, ryby smażone
na nieznanym
oleju lub tłuszczu;
skorupiaki ostrygi;
małże, homary;
krewetki, kalmary;
mięso
indyki, kurczaki,
cielęcina,
dziczyzna, króliki;
bardzo chuda wo-
łowina, szynka,
bekon, jagnięta
(1 lub 2 razy w
tygodniu), kiełba-
sa z cielęciny lub
kurczaka, wątroba
2 razy w miesiącu;
kaczki, gęsi,
mięso
z widocznym
tłuszczem,
kiełbasy, salami,
pasztety mięsne
i inne, skóra
drobiu;

tłuszcze
oleje zawierające
kwasy wieloniena-
sycone (np.
słonecznikowy,
kukurydziany,
krokoszowy, sojo-
wy), oleje zawie-
rające kwasy jed-
nonienasycone,
np. rzepakowy,
oliwa z oliwek,
margaryny
miękkie z tych
olejów, margaryny
o zmniejszonej za-
wartości tłuszczu;
masło, łój,
słonina; smalec,
tłuszcz spod
pieczeni, olej
palmowy,
margaryny
twarde, tłuszcze
uwodornione;
owoce
i warzywa
wszystkie świeże
i mrożone warzy-
wa, zwłaszcza su-
che nasiona roślin
strączkowych (fa-
sola, groch, socze-
wica), kukurydza,
ziemniaki, wszyst-
kie świeże i suszo-
ne owoce, konser-
wowane owoce
(niesłodzone);
ziemniaki lub
frytki smażone
na dozwolonym
oleju;
ziemniaki
pieczone, frytki,
warzywa lub ryż
smażone na
nieznanym lub
niewłaściwym
oleju lub tłuszczu,
solone,
konserwowane
warzywa;
desery
sorbet, galaretki,
budynie na mleku
odtłuszczonym;
lody, kremy, budy-
nie na pełnym mle-
ku, sosy na śmieta-
nie lub maśle;
wyroby
cukiernicze
ciasto drożdżowe,
nugat;
marcepany,
chałwa;
czekolada, toffi,
karmelki, batony
kokosowe;
wypieki
ciasta i ciasteczka
przygotowane na
tłuszczach
nienasyconych;
torty, przemysłowe
wyroby cukierni-
cze (ciastka, pasz-
teciki, babeczki);
103
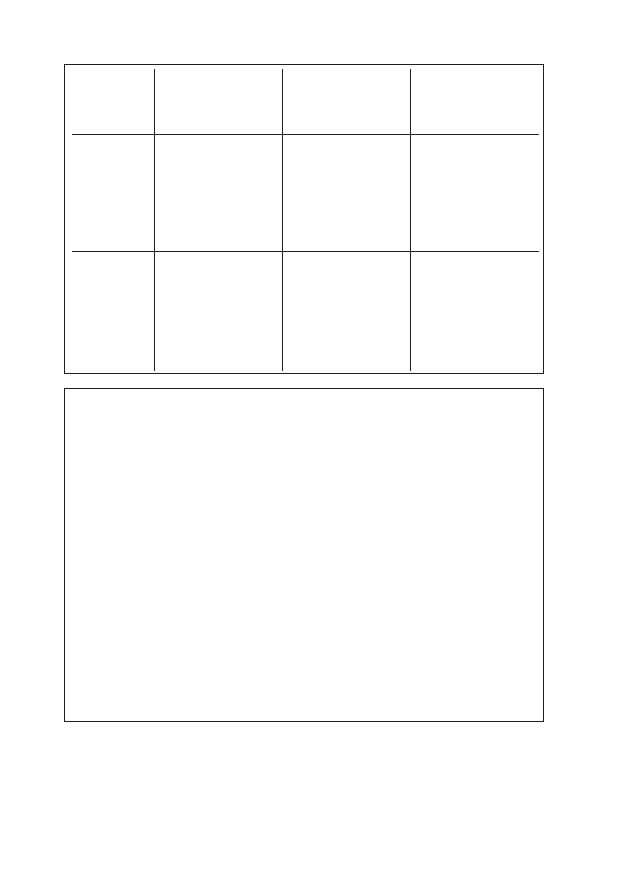
104
orzechy
orzechy włoskie,
migdały,
kasztany;
orzechy brazylij-
skie, orzeszki ziem-
ne i pistacjowe;
orzechy
kokosowe,
słone orzechy;
napoje
herbata, kawa
filtrowana lub
instant, woda,
napoje
bezalkoholowe,
bezkaloryczne;
alkohol, napoje
czekoladowe,
niskotłuszczowe;
napoje
czekoladowe,
kawa
ze śmietanką,
gotowana kawa;
sosy,
przyprawy
pieprz, musztarda,
zioła, przyprawy
korzenne.
sosy sałatkowe
niskotłuszczowe.
sól dodana, sosy
sałatkowe, kremy
sałatkowe, sosy
do mięsa i ryb za-
wierające tłuszcz,
majonezy.
• produkty zalecane cechują się niską zawartością tłuszczu
lub/i wysoką zawartością błonnika; powinny być spożywane
regularnie;
• produkty do spożywania w umiarkowanych ilościach cechują się
zawartością tłuszczów nasyconych; produkty te są dozwolone
tylko w ograniczonych ilościach, ponieważ dieta powinna być
ubogotłuszczowa np.:
–
mięso czerwone nie więcej niż 3 razy w tygodniu,
–
sery o średniej zawartości tłuszczu oraz mięsne i rybne pasty
raz w tygodniu,
–
ciasto domowe, biszkopty i wyroby cukiernicze przygotowane
z dodatkiem odpowiednich margaryn zawierających kwasy
tłuszczowe wielonienasycone lub oleje, 2 razy tygodniowo,
–
frytki i ziemniaki pieczone na właściwym oleju, raz
na 2 tygodnie;
• produkty przeciwwskazane zawierają duże ilości tłuszczów
nasyconych i/lub cholesterolu; zawsze należy ich unikać.

Zapamiętaj!
1. Nieodzownym elementem prawidłowej terapii zaburzeń gospodarki lipido-
wej, oprócz farmakoterapii, jest leczenie dietetyczne.
2. Podstawowym źródłem energii w diecie hipolipemicznej muszą być węglo-
wodany złożone o dużej zawartości błonnika pokarmowego.
3. Warzywa i owoce są najkorzystniejszym źródłem witamin antyoksydacyj-
nych i składników mineralnych w profilaktyce miażdżycy.
4. Cholesterol pokarmowy w codziennej diecie nie powinien przekraczać 300
mg, czyli powinniśmy ograniczać produkty pochodzenia zwierzęcego – pro-
dukty roślinne cholesterolu nie zawierają!
Warto przeczytać:
S. M. Grundy, G. I. Balady, M. H. Criqui i wsp.: Primary prevention of co-
ronary heart disease. Guidelines from Framingham. A statement for Health
Care Professionals from the AHA Task Force on Risk Reduction. Circula-
tion 1998; 97, 1876.
F. B. Hu, J. E. Manson, W. C. Willet: Types of dietary fat risk of coronary
heart disease: a critical review. J. Am. Coll. Nutr. 2001; 1: 5-19.
M. Kozłowska-Wojciechowska: Rola żywienia w leczeniu hipercholesterole-
mii. Farmakologia Polska, 1998; 4: 161.
Prevention of coronary heart disease in clinical practice. Recommendations
of the Second Joint Task Force of European and other Societies on Co-
ronary Prevention. Eur. Heart J. 1998; 19: 1434.
Profilaktyka choroby niedokrwiennej serca. Kardiologia Polska 2000; supl. 1.
A. S. Truswell: Meta-analysis of the cholesterol-lowering effects of dietary fi-
bre. Am. J. Clin. Nutr. 1999; 70: 942-943.
A. S. Truswell: Cereal grains and coronary heart disease. Eur. J. Clin. Nutr.
2002; 56: 1-14.
105

VII. ROLA KWASÓW TŁUSZCZOWYCH, STEROLI
I STANOLI W ZAPOBIEGANIU MIAŻDŻYCY
Małgorzata Kozłowska-Wojciechowska, Magdalena Makarewicz-Wujec
Światowa Organizacja Zdrowia (WHO) definiuje styl życia, jako sposób
bycia człowieka wynikający z wzajemnego oddziaływania warunków, w ja-
kich żyje oraz indywidualnych wzorców zachowania, określonych przez czyn-
niki społeczno-kulturowe i osobiste cechy jego charakteru.
Składowe stylu życia, wywierające niekorzystny wpływ na zdrowie człowie-
ka to przede wszystkim niewłaściwa dieta, siedzący tryb życia, używki oraz
stresy życia codziennego, którym należy przeciwdziałać wśród jak najwięk-
szej części zagrożonej populacji.
STYL ŻYCIA I SKŁADNIKI DIETY
Najnowszy raport ekspertów Światowej Organizacji Zdrowia i Organizacji
ds. Żywności i Rolnictwa (WHO/FAO 2002) przedstawia elementy stylu ży-
cia oraz składniki diety, których oddziaływanie na rozwój lub zapobieganie
chorobom układu krążenia na tle miażdżycy jest bezsporne, nie podlegające
dyskusji oraz prawdopodobne, wymagające potwierdzenia w jeszcze więk-
szej liczbie badań. Na liście tej umieszczono również tzw. czynniki możliwe,
których oddziaływanie jak dotąd potwierdzone zostało w zbyt małych, wy-
branych populacjach, co tym samym sugeruje konieczność prowadzenia dal-
szych badań. Wyniki tej analizy przedstawiono w tabeli 1.
Modyfikacja spożycia tłuszczów
W ślad za powyższym zestawieniem składowych stylu życia oraz czynni-
ków dietetycznych, eksperci FAO/WHO zaproponowali wprowadzenie
zmian w dotychczasowych zaleceniach żywieniowych dla populacji general-
nych krajów rozwiniętych, które szczególnie obejmują zalecenia w odniesie-
niu do spożycia tłuszczów. Sugerują, aby udział energii z tłuszczu ogółem,
w dziennych racjach pokarmowych pozostawić na dotychczasowym pozio-
mie, czyli w granicach od 15 do 30%, zmniejszając jednak udział energii
z nasyconych kwasów tłuszczowych do 7%, a nie jak dotąd do 10% energii.
Propozycja wprowadzenia takich zmian pokazuje, iż rola wyższego spożycia
nasyconych kwasów tłuszczowych – jako czynnika zagrażającego zdrowiu po-
pulacji – nie budzi wątpliwości. Jest to zalecenie o tyle nowe, iż dotychczas
redukcję spożycia tłuszczów nasyconych poniżej 7% zalecano w tzw. diecie
II stopnia wg AHA (American Heart Association), obejmującej udział energii
106
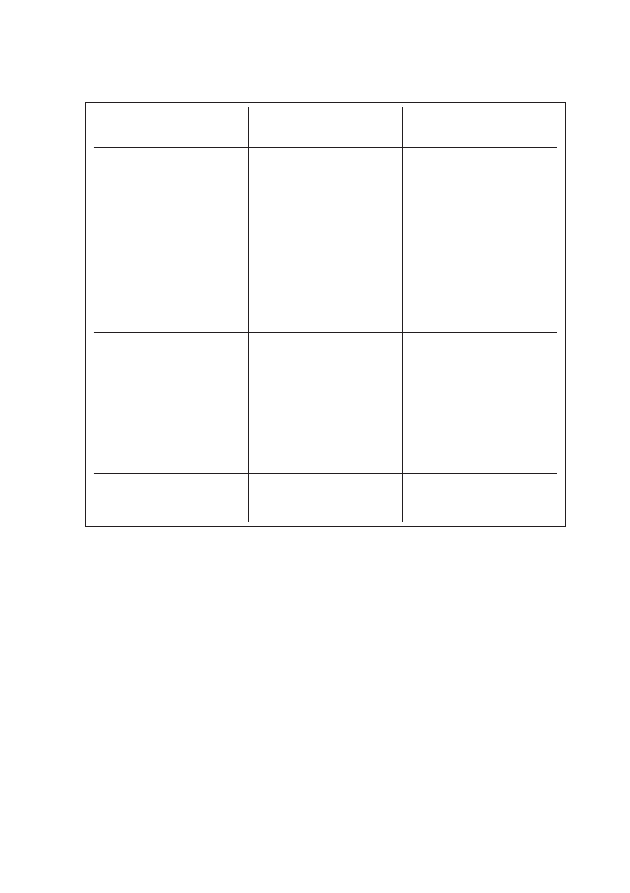
z tłuszczów < 25%, nasyconych kwasów tłuszczowych < 7%, cholesterolu
pokarmowego < 200 mg/dzień. Redukcja ta była proponowana dopiero jako
kolejny etap leczenia pacjentów z zaburzeniami lipidowymi, wówczas gdy
zastosowanie diety I stopnia (energia z tłuszczów < 30%, z nasyconych kwa-
sów tłuszczowych < 10%, cholesterolu < 300 mg/dzień) nie pozwalała osią-
gnąć pożądanych efektów. Natomiast w najnowszych zaleceniach brak jest
sugestii zmian w spożyciu cholesterolu pokarmowego, którego bezpieczna
granica nadal wynosi 300 mg/dziennie. Wytłumaczyć to można faktem, iż
cholesterol pokarmowy jako czynnik izolowany, bez jednoczesnej podaży na-
syconych kwasów tłuszczowych, u większości ludzi tylko w niewielkim stop-
niu wpływa na podniesienie stężenia cholesterolu w surowicy krwi.
Kwasy tłuszczowe typu trans
Omawiane zalecenia sugerują, aby wielkość spożycia kwasów tłuszczowych
typu trans ograniczyć do poniżej 1% udziału energii. Wynika to z faktu, iż
107
Tabela 1: Elementy stylu życia zmniejszające/zwiększające ryzyko chorób sercowo-naczyniowych
wg raportu WHO/FAO (2002 rok)
ELEMENTY
STYLU ŻYCIA
ZMNIEJSZAJĄCE
RYZYKO
ZWIĘKSZAJĄCE
RYZYKO
BEZSPORNE
• owoce i warzywa;
• ryby i oleje rybie;
• kwas linolowy;
• potas;
• małe dawki
alkoholu (ChNS);
• regularna
aktywność fizyczna;
• kwas mirystynowy
i palmitynowy;
• kwasy trans;
• wysoka podaż sodu;
• otyłość;
• nadużywanie
alkoholu (udar);
PRAWDOPODOBNE
• kwas
a-linolenowy;
• błonnik
pokarmowy;
• ziarna i orzechy;
• foliany;
• sterole i stanole;
• cholesterol
pokarmowy;
• niefiltrowana,
gotowana kawa;
• suplementacja
b-karotenem;
MOŻLIWE
• flawonoidy;
• soja.
• tłuszcze bogate
w kwas laurynowy.

ten typ kwasów tłuszczowych wywiera szczególnie niekorzystny wpływ na
profil lipidowy u ludzi, nawet bardziej szkodliwy niż kwasy tłuszczowe nasy-
cone. Spełnienie jednak tego zalecenia nastręczać może wiele trudności
w zwyczajowych modelach żywienia społeczeństw krajów uprzemysłowio-
nych. Kwasy tłuszczowe typu trans są wszechobecne; stanowią element skła-
dowy wielu produktów spożywczych wysoko przetworzonych, a ponadto, są
obecne w bardzo popularnych wyrobach typu fast food. Niestety, dotych-
czasowe polskie opracowania tabel wartości odżywczej wybranych produk-
tów nie obejmują zawartości w nich kwasów trans, i dlatego trudno jest sys-
tematycznie kontrolować wielkość spożycia. Pomocne są badania nad
zawartością tych kwasów monitorowane w wybranych grupach produktów,
które systematycznie publikowane są w opracowaniach Instytutu Żywności
i Żywienia.
Propozycję nowych zaleceń w odniesieniu do spożycia tłuszczów propo-
nowanych przez ekspertów WHO/FAO dla populacji generalnej przedsta-
wiono w tabeli 2.
O tym, że powyższe zalecenia są możliwe do zastosowania w postaci diety
dla każdego, niech przekonają przykłady dwóch jadłospisów o zróżnicowanej
kaloryczności, w których posłużono się nowymi wytycznymi.
108
Tabela 2: Zalecenia żywieniowe dla populacji wg WHO/FAO (2002 rok)
tłuszcz całkowity
15-30% energii
SAFA – kwasy tłuszczowe nasycone < 7% energii
PUFA – kwasy wielonienasycone
6-10% energii
omega-6
5-8% energii
omega-3
1-2% energii
kwasy tłuszczowe TRANS
< 1% energii
MUFA – kwasy jednonienasycone
tłuszcz całk.
(SAFA + PUFA + TRANS)
węglowodany
55-75% energii
wolne cukry
< 10% energii
białko
10-15% energii
cholesterol
< 300 mg/dzień
chlorek sodu (sód)
< 5 g/dzień (< 2 g/dzień)
owoce i warzywa
³ 400 g/dzień
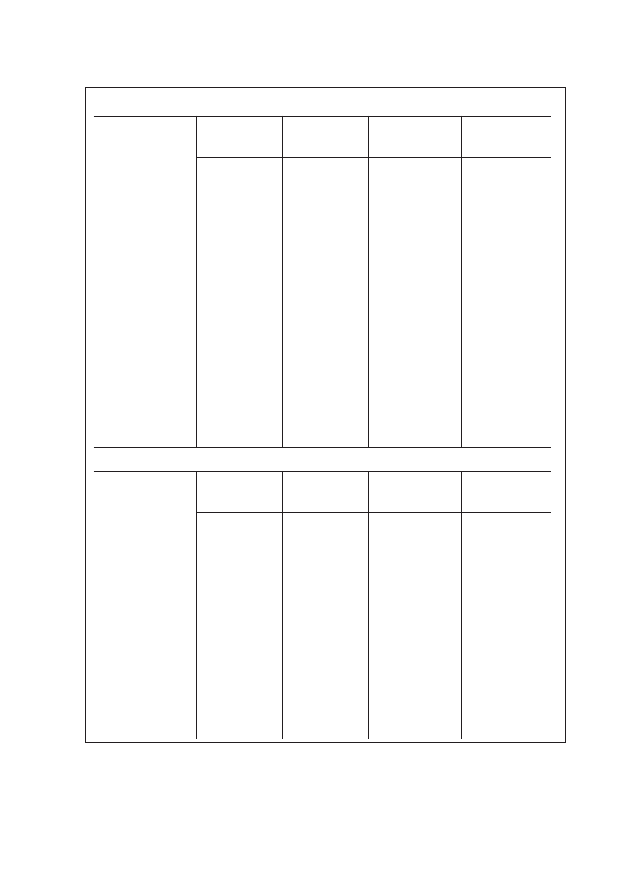
Model zwyczajowej polskiej diety dostarcza trzech głównych składników
żywieniowych prowadzących do podwyższenia poziomu cholesterolu w su-
rowicy krwi. Należą do nich: wysokie spożycie nasyconych kwasów tłuszczo-
wych, cholesterolu pokarmowego oraz brak równowagi pomiędzy spożyciem
energii, a jej wydatkowaniem.
109
Tabela 3: Przykładowe jadłospisy skonstruowane na podstawie zaleceń WHO/FAO z 2002 roku
DIETA 1800 kcal
białko 16%
tłuszcz
ogółem 24%
węglowodany
60%
błonnik 40 g
SAFA 4%
omega-6 6,28%
omega-3 1,64%
PUFA 8%
sacharoza 9%
cholesterol 91 mg
I śniadanie
575 kcal
II śniadanie
173 kcal
obiad
663 kcal
kolacja
481 kcal
mleko 0,5% 250 g
z müsli
z orzechami 30 g,
grahamka 100 g,
margaryna 10 g,
polędwica z piersi
kurczaka 20 g,
papryka 100 g.
banan 200 g.
• zupa krem
z brokułów:
– brokuły 200 g,
– włoszczyzna 60 g,
– olej 4 g,
– grzanki z bułki
40 g;
• indyk duszony
w warzywach:
– mięso z indyka
bez skóry 50 g,
– włoszczyzna 120 g,
– olej 8 g;
• kasza gryczana
40 g;
• fasolka
szparagowa 150 g;
• sok marchwiowo-
-jabłkowy 200 g.
• sałatka
z tuńczyka:
– tuńczyk z wody
50 g,
– ogórek
kwaszony 30 g,
– groszek zielony
30 g,
– pomidor 100 g;
• chleb żytni
razowy 90 g;
• margaryna 10 g;
• jabłko 140 g.
DIETA 2000 kcal
białko 14%
tłuszcz ogółem
28%
węglowodany
58%
błonnik 39,6 g
SAFA 6,54%
omega-6 6,58%
omega-3 1,60%
PUFA 8,33%
sacharoza 4,56%
cholesterol
90,1 mg
I śniadanie
632 kcal
II śniadanie
184 kcal
obiad
652 kcal
kolacja
530 kcal
mleko 0,5% 250 g
z müsli z orzecha-
mi 30 g,
grahamka 100 g,
margaryna 10 g,
szynka wiejska
30 g,
papryka 100 g.
pumpernikiel 40 g,
margaryna 5 g,
serek ziarnisty
20 g,
rzodkiewki 100 g,
mandarynki 50 g.
• zupa krupnik:
– kasza
jęczmienna 30 g,
– włoszczyzna 60 g,
– olej 4 g,
– ziemniaki 50 g;
• ryba pieczona
w folii:
– halibut 50 g,
– ziemniaki
z wody 200 g,
– brokuły z wody
200 g,
– olej 8 g;
• sok grejpfrutowy
250 g.
• sałatka grecka:
– ser Feta 50 g,
– ogórek 50 g,
– sałata 30 g,
– pomidor 100 g,
– olej 8 g;
• chleb żytni
razowy 90 g;
• margaryna 10 g;
• jabłko 140 g.
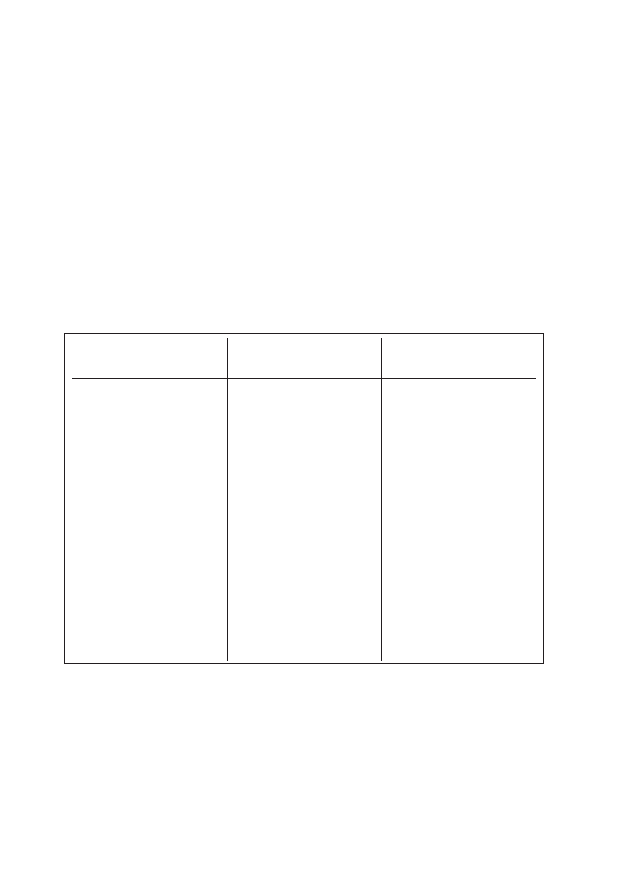
Nasycone kwasy tłuszczowe
Podstawowymi źródłami nasyconych kwasów tłuszczowych (NKT) w po-
żywieniu jest tłuszcz mleczny, mięso oraz ich przetwory. Nasycone kwasy
tłuszczowe podnoszą u większości ludzi poziom cholesterolu całkowitego
i cholesterolu frakcji LDL w surowicy krwi. Kwas mirystynowy (C: 14) i pal-
mitynowy (C: 16) w większym stopniu podwyższają poziom lipidów (chole-
sterolu całkowitego i frakcji LDL oraz HDL), niż kwas laurynowy (C: 12).
W żywności, kwas palmitynowy występuje w najszerszej gamie produktów,
co oznacza, iż jego spożycie jest najbardziej obfite w porównaniu do pozosta-
łych. Należy przy tym pamiętać, że siła hipercholesterolemicznego oddziały-
wania tych trzech kwasów zwiększa się, gdy jednocześnie w pokarmach wy-
stępuje cholesterol pokarmowy.
Kwasem nasyconym szeroko występującym w żywności, ale nie wykazują-
cym jak poprzednio opisane, niekorzystnego wpływu na poziom lipidów
w surowicy jest kwas stearynowy (C: 18), który szybko ulega w organizmie
przekształceniu w kwas oleinowy.
Ostatnie dziesięciolecia przyniosły przemysłowi spożywczemu nowe tech-
nologie, a społeczeństwom nowe mody żywieniowe. Pojawienie się na ryn-
ku żywności typu fast food, żywności typu instant i żywności wysoko prze-
110
Tabela 4: Pokarmowe źródła wybranych nasyconych kwasów tłuszczowych
Kwas mirystynowy
C: 14
Kwas palmitynowy
C: 16
Kwas stearynowy
C: 18
• masło;
• baranina;
• sery topione;
• serki Fromage;
• serki
homogenizowane;
• ser Feta;
• sery żółte;
• śmietana kremowa.
• masło;
• nabiał;
• mięso wołowe;
• mięso wieprzowe;
• wyroby
wędliniarskie;
• pasztety;
• oleje i oliwa;
• margaryny;
• chipsy;
• ciastka i herbatniki
i in.
• smalec;
• czekolady;
• ciastka Delicje;
• batony;
• wędliny drobiowe;
• majonezy.

tworzonej, stało się poważnym źródłem niekorzystnej dla zdrowia generacji
tłuszczów, jakimi są kwasy tłuszczowe typu trans. Izomery trans nienasyco-
nych kwasów tłuszczowych powstają w wyniku utwardzania olejów roślin-
nych w celach ich technologicznego użycia jako tłuszcze piekarnicze, sma-
żalnicze lub wcześniej szeroko rozpowszechnione margaryny tzw. twarde.
Oznacza to tym samym, iż w codziennym żywieniu, podstawowym źródłem
izomerów trans są wyroby przemysłowe, takie jak pieczywo cukiernicze,
chipsy, frytki, zupy i dania instant, margaryny twarde, czy inne. Niewielkie
ilości kwasów trans występują w produktach nieprzetworzonych, takich jak
tłuszcz mleczny czy mięsa wołowe lub baranie, choć w nich ilości izomerów
są dość ograniczone. Ich silne promiażdżycowe działanie wyraża się faktem,
że nie tylko wpływają na podniesienie stężenia cholesterolu frakcji LDL, ale
powodują również obniżenie stężenia cholesterolu frakcji HDL, czego nie
obserwuje się pod wpływem działania nasyconych kwasów tłuszczowych.
Stwierdzono, że w diecie bogatej w kwasy trans stosunek LDL/HDL jest zna-
miennie wyższy, niż w przypadku diety bogatej w nasycone kwasy tłuszczowe.
Ponadto udowodniono, iż wysokie spożycie izomerów trans podnosi poziom
lipoproteiny Lp (a), która jest uznanym, niezależnym czynnikiem zagroże-
nia miażdżycą. Tak więc, ograniczenie w codziennej diecie spożycia kwasów
tłuszczowych typu trans jest wyzwaniem dla przedstawicieli zdrowia publicz-
nego, technologów i producentów żywności, a zarazem jest jedną z metod
pozwalających zmniejszyć częstość występowania chorób sercowo-naczynio-
wych na tle miażdżycy.
Wielonienasycone kwasy tłuszczowe
Choć wiadome jest, iż spożycie tłuszczów ogółem, jako produktów wyso-
koenergetycznych należy ograniczać, to jednak w prawidłowo zestawionej
diecie nie może zabraknąć wielonienasyconych kwasów tłuszczowych.
W żywności występują: kwas linolowy (LA), który w wyniku desaturacji
i emulgacji przekształcony zostaje w kwasy rodziny omega-6 oraz kwas alfa-
-linolenowy (ALNA), będący prekursorem kwasów rodziny omega-3. Podsta-
wowymi kwasami rodziny omega-6 są kwasy: arachidonowy (AA) i dihomo-
gammalinolenowy (DHGLA), natomiast rodziny omega-3 kwas eikozapen-
taenowy (EPA) i dokozaheksaenowy (DHA). Eikozanoidy wywodzące się
z kwasu arachidonowego posiadają odwrotne właściwości metaboliczne niż
te, które pochodzą z kwasu dokozaheksaenowego. Dlatego, dla zachowania
zdrowia niezbędna jest równowaga podaży z żywności obu rodzajów kwasów
omega-6 i omega-3. Uważa się, że w prawidłowo zbilansowanej diecie sto-
sunek LA/ALNA powinien wynosić nie więcej niż 10. Stosunek ten sugeru-
je, że równie korzystne jest zwiększanie podaży pokarmowych źródeł kwa-
111

su
a-linolenowego, jak i zmniejszanie pokarmów dostarczających kwas lino-
lowy. Pamiętać należy, iż oba rodzaje kwasów tłuszczowych zmniejszają ryzy-
ko choroby niedokrwiennej serca.
Podstawowym źródłem pokarmowym kwasów z rodziny omega-6 są oleje:
słonecznikowy, sojowy, kukurydziany oraz margaryny z nich produkowane.
Natomiast źródłem kwasów z rodziny omega-3 są ryby, przede wszystkim
morskie oraz w mniejszym stopniu tofu, olej sojowy, rzepakowy, nasiona
i zielonolistne warzywa.
Kwasy tłuszczowe z rodziny omega-6 charakteryzują się obniżającym wpły-
wem na poziom cholesterolu frakcji LDL, średnio o 7%. Jak pokazują liczne
badania, właściwa podaż wielonienasyconych kwasów tłuszczowych na pozio-
mie od 5 do 8% udziału energii w dziennych racjach pokarmowych, sprzyja
redukcji wskaźników aterogenności, TC/HDL-C lub LDL/HDL, co z punktu
widzenia profilaktyki jest zjawiskiem niezwykle korzystnym. Ten rodzaj kwa-
sów wykazuje niewielki efekt hipotensyjny oraz charakteryzuje się brakiem
efektu na poziom trójglicerydów. Zaletą ich oddziaływania na organizm czło-
wieka jest zmniejszanie gotowości prozakrzepowej w naczyniach, do czego
dochodzi w wyniku zubażania płytek krwi w kwas arachidonowy. Wykazano,
że zastąpienie tymi kwasami w diecie 2% kwasów trans zmniejsza ryzyko cho-
roby niedokrwiennej serca i cukrzycy o ok. 40%. Pamiętać jednak należy, iż
udział wielonienasyconych kwasów tłuszczowych w diecie nie powinien prze-
kraczać 8% udziału energii. W wielu badaniach stwierdzono, iż spożywanie
kwasów tłuszczowych wielonienasyconych z rodziny omega-6 powyżej 10%
energii, wykazuje niekorzystne efekty, zwiększając podatność frakcji LDL do
oksydatywnej modyfikacji (utleniania), nasilając aterogenezę. Ponadto ich
nadmiar w diecie hamuje syntezę prostacykliny i osłabia odporność organi-
zmu. Należy jednak zaznaczyć, iż w przeciętnej diecie ich spożycie sięga
5-6% energii, czyli i tak jest zbyt małe.
Kwasy tłuszczowe omega-3 charakteryzują się szerokim działaniem w pro-
filaktyce nie tylko choroby niedokrwiennej serca i udaru mózgu, ale i w cho-
robach autoimmunologicznych, reumatoidalnym zapaleniu stawów, choro-
bie Crohna, czy niektórych chorobach nowotworowych. Jednakże najwięcej
badań poświęcono ich działaniu w prewencji miażdżycy. Stwierdzono, iż wy-
kazują zdolność hamowania wątrobowej syntezy VLDL (lipoprotein o bar-
dzo niskiej gęstości), w efekcie czego dochodzi do redukcji stężenia trójglice-
rydów w surowicy krwi. Są prekursorami prostaglandyn i leukotrienów,
będąc jednocześnie inhibitorami syntezy cytokin i mitogenów. Stymulują
śródbłonkowy tlenek azotu, dzięki czemu przeciwdziałają procesom oksyda-
cyjnym. Stąd, ich właściwa podaż w diecie zapewnia działanie antyagrega-
112
cyjne, przeciwzapalne, hipotensyjne oraz przeciwarytmiczne. Jednakże siła
ich działania w organizmie zależna jest jednak od rodzaju kwasu. Kwas do-
kozaheksaenowy pochodzący z ryb i tłuszczu rybiego oddziałuje przede
wszystkim na lipidy i lipoproteiny, ciśnienie tętnicze, częstość rytmu serca
i wartość glikemii, natomiast kwas eikozapentaenowy przede wszystkim od-
powiada za działanie antyagregacyjne. Dlatego, zalecenie spożycia kwasów
tłuszczowych omega-3 na poziomie 1-2% udziału energii w dziennych ra-
cjach pokarmowych, winno być bezwzględnie spełnione. Oznacza to, iż ry-
by powinny zostać wpisane we wszystkie jadłospisy.
Spożycie ryb morskich w naszym kraju jest dalece niewystarczające. Szacu-
je się, iż spożywanie tłustych ryb morskich przynajmniej jeden raz w tygo-
dniu zmniejsza ryzyko nagłej śmierci o ok. 52% w porównaniu do osób je-
dzących ryby rzadko. Podobnie, jak udowodniono, codzienne spożywanie
lub suplementacja 1 g kwasów tłuszczowych omega-3 zmniejsza ryzyko na-
głego zgonu u osób po przebytym zawale serca o 42%, w wyniku przeciw-
działania arytmii. Dlatego wydaje się niezwykle istotne, aby szczególnie po-
lecać regularne spożywanie ryb morskich osobom z czynnikami ryzyka
113
Tabela 5: Źródła pokarmowe wybranych kwasów tłuszczowych wielonienasyconych z rodziny omega-6
i omega-3
Kwas
linolowy
C
18: 2
Omega-6
Kwas ara-
chidonowy
C
18: 4
Omega -6
Kwas
a
a-li-
nolenowy
C
18: 3
Omega-3
Kwas
EPA
C
20: 5
Omega -3
Kwas
DHA
C
22: 6
Omega -3
• oliwa;
• oleje:
– sojowy,
– słonecz-
nikowy,
– rzepako-
wy,
– sezamo-
wy,
– arachi-
dowy,
– marga-
ryny;
• orzechy.
• mięso
i produkty
zwierzęce.
• olej:
– sojowy,
– rzepako-
wy;
• brokuły;
• szczaw;
• szpinak;
• soja;
• jarmuż;
• kapusta.
• łosoś;
• sola;
• dorsz;
• tuńczyk;
• ostrygi;
• kraby;
• sardynki.
• dorsz;
• flądra;
• halibut;
• makrela;
• łosoś;
• morsz-
czuk;
• pstrąg;
• sola;
• sardynki.

choroby niedokrwiennej serca, a zlecać jako niezbędny element terapii pa-
cjentom z rozpoznaną chorobą. Ile, komu polecać kwasów omega-3 przed-
stawiono w tabeli 6.
Jednonienasycone kwasy tłuszczowe
Jednonienasyconych kwasów tłuszczowych (właściwie kwasu oleinowego)
dostarczają nam: oliwa z oliwek, olej rzepakowy, margaryny z nich wytwo-
rzone oraz orzechy. Ich odpowiednia zawartość w diecie sprzyja redukcji po-
ziomu glukozy i trójglicerydów w surowicy krwi, szczególnie u pacjentów
z 2 typem cukrzycy. Stwierdzono, że wykazują zdolność obniżania podatno-
ści LDL na oksydatywną modyfikację. Ponadto, choć w mniejszym stopniu
niż wielonienasycone kwasy tłuszczowe omega-6, redukują cholesterol cał-
kowity i frakcję LDL. Kwasy tłuszczowe jednonienasycone są głównym tłusz-
czem diety śródziemnomorskiej (oliwa z oliwek), który – jak wykazano
w licznych badaniach epidemiologicznych – sprzyja istotnie mniejszej zapa-
dalności oraz umieralności z powodu choroby niedokrwiennej serca. Kwasy
tłuszczowe nasycone i jednonienasycone mogą być syntetyzowane w organi-
zmie człowieka i stąd w odróżnieniu od wielonienasyconych, nie są zaliczane
do kwasów niezbędnych. Z punktu widzenia praktycznego należy pamiętać,
że produkty tłuszczowe o przeważającej zawartości jednonienasyconych
kwasów tłuszczowych nadają się do obróbki kulinarnej w wysokich tempe-
raturach, czyli np. smażenia. Dlatego polecane jest smażenie tylko na oleju
rzepakowym bezerukowym, oliwie z oliwek lub margarynach specjalnie do
tego przeznaczonych.
114
Tabela 6: Ogólne wskazania do spożywania kwasów omega-3 wśród różnych grup pacjentów
pacjenci z czynnikami
ryzyka bez ChNS
dwa razy w tygodniu powinni jadać różne
tłuste ryby morskie oraz oleje i żywność
zawierającą kwas
a-linolenowy
pacjenci z chorobą
niedokrwienną serca
powinni spożywać 1 g kwasów EPA+DHA
dziennie, preferując ryby morskie, jako ich
źródło; w szczególnych wypadkach, gdy są
istotne wskazania lekarz może zalecić
suplementację farmakologiczną
pacjenci
z hipertrójglicerydemią
powinni otrzymywać 2-4 g kwasów
EPA+DHA w postaci suplementacji

Masło czy margaryna?
Od wielu lat, liczne organizacje naukowe przygotowują zalecenia żywie-
niowe dla populacji w celu zapobiegania chorobom układu krążenia na pod-
łożu miażdżycy. Zaleceniom tym towarzyszą długie listy zakazanych produk-
tów, budzące sprzeciw pacjentów, gdyż dotyczą ulubionych przez nich
składników diety. Nierzadko jest to przyczyną niepowodzeń tych kampanii,
gdyż ludzie, do których są one adresowane, nie akceptują wprowadzania da-
leko idących zmian w swoich dotychczasowych nawykach żywieniowych.
Z tego względu istotne wydaje się szukanie prostszych rozwiązań wprowa-
dzania zmian w diecie, których jednak efektywność musi zostać udokumen-
towana.
Aby sprostać takim oczekiwaniom, jedną z możliwości jest wymiana w die-
cie jednego z najczęstszych i bogatych źródeł nasyconych kwasów tłuszczo-
wych – masła, na tłuszcze nienasycone pochodzenia roślinnego (oleje lub
margaryny). O tym, że tak nieduże modyfikacje w diecie przynoszą wymier-
ne efekty terapeutyczne przekonują nas liczne badania międzynarodowe,
w tym również polskie.
Korzyści z takiej zmiany potwierdzono badaniem klinicznym, przepro-
wadzonym u zdrowych młodych mężczyzn. Po zastosowaniu wymiany do-
tychczas spożywanego masła na margarynę bogatą w wielonienasycone
kwasy tłuszczowe w zwyczajowej ilości 30 g dziennie, po czterech tygo-
dniach uzyskano redukcję cholesterolu całkowitego o blisko 7%, a chole-
sterolu frakcji LDL o 9%. Nie była to jedyna uzyskana korzyść, gdyż dzię-
ki wymianie masła na margarynę nastąpiło zmniejszenie udziału energii
z tłuszczów ogółem w diecie badanych osób aż o 3%. Należy przypuszczać,
iż zmniejszenie udziału energii z tłuszczów pod wpływem zastosowania
margaryny w stosunku do diety z masłem było korzystnym czynnikiem, ma-
jącym wpływ na redukcję stężenia cholesterolu całkowitego i frakcji LDL.
Wymiana tłuszczu do smarowania zaowocowała również obniżeniem o 4%
energii pochodzącej z nasyconych kwasów tłuszczowych, gdyż należy pa-
miętać, że margaryna zawiera o blisko 2/3 mniej tych kwasów w takiej sa-
mej ilości. Margaryna, stanowiąc dobre źródło wielonienasyconych kwa-
sów tłuszczowych, spowodowała wzrost ich zawartości w diecie o blisko
5%, wpływając w efekcie na wzrost stosunku P/S (kwasów wielonienasyco-
nych do nasyconych) z 0,30 do 0,78. Stosunek ten w prawidłowej diecie,
jak i diecie przeciwmiażdżycowej, winien być najbliższy jedności. Ponadto,
w wyniku wymiany masła na margarynę, zmniejszeniu uległa ilość spoży-
wanego cholesterolu pokarmowego, mającego również istotny wpływ na
profil lipidowy.
115

Uzyskanie poprawy profilu lipidowego pod wpływem tak małych zmian
w diecie potwierdza, iż tłuszczem jadalnym, dominującym w profilaktyce
miażdżycy powinien być tłuszcz roślinny. W omawianym badaniu potwier-
dzono, że korzystne zmiany, jakie wystąpiły pod wpływem diety z margaryną,
są bardzo szybko niwelowane po powrocie do starych nawyków, czyli masła.
Znamienny statystycznie wzrost poziomu cholesterolu całkowitego i frakcji
LDL, który nastąpił wskutek powrotu do masła, wskazuje, jak silna jest za-
leżność pomiędzy stężeniami lipidów, a ilością spożywanych kwasów tłusz-
czowych nasyconych, szczególnie mirystynowego C:14 i palmitynowego C:16,
w które bogate jest masło. Oznacza to, że stosując dietę z masłem w zwycza-
jowej ilości około 30 g dziennie spożywamy o 10 g więcej miażdżycorodnych
kwasów tłuszczowych, niż ma to miejsce przy jedzeniu tej samej ilości marga-
ryny miękkiej, bogatej w wielonienasycone kwasy tłuszczowe.
Podobne efekty przeciwmiażdżycowego oddziaływania roślinnych tłusz-
czów jadalnych (margaryn miękkich i olejów) uzyskali badacze w wielu
ośrodkach na świecie. Stosując diety z margarynami (bez kwasów trans) ob-
serwowali spadek stężenia cholesterolu LDL; odpowiednio od 5% do 12%.
Jak wspomniano wcześniej, zwiększenie udziału w diecie energii, pochodzą-
cej z wielonienasyconych kwasów tłuszczowych powyżej 8%, może powodo-
wać u części osób obniżenie stężenia cholesterolu frakcji HDL o ok. 2-3%.
Oznacza to, iż w przypadku osób z niskimi wartościami HDL (poniżej
35 mg/dL) wskazane jest kontrolowanie spożycia wielonienasyconych kwa-
sów tłuszczowych, szczególnie z rodziny omega-6. W praktyce oznacza to,
że osoby te powinny unikać nadmiernego spożycia margaryn, w których
przeważają kwasy wielonienasycone, wybierając te z przewagą jednonienasy-
conych. Podobnie jak powinni spożywać oliwę lub olej rzepakowy bezeruko-
wy, a nie sojowy czy słonecznikowy. Takie zamiany spowodują ograniczenie
spożycia kwasów omega-6.
Powyższe przykłady pokazują, iż poprawa wybranych wskaźników zdro-
wotnych może nastąpić w wyniku niewielkich modyfikacji diety. Należy rów-
nież przypuszczać, iż sugestie tak niewielkich zmian w diecie powinny być
łatwiej akceptowane przez ludzi. A o tym, że możliwe jest przygotowanie
diety niskotłuszczowej przekonać może przykład zaproponowany w tabeli 7.
Sterole i stanole roślinne
Ostatnie piętnastolecie XX wieku przyniosło zintensyfikowane badania nad
tworzeniem nowej żywności o ukierunkowanym, pożądanym oddziaływaniu na
organizm człowieka. Odpowiedzią na takie zapotrzebowanie wydają się marga-
ryny, jogurty, dresingi wzbogacone (suplementowane) sterolami roślinnymi.
116
Sterole to podstawowe składniki błon komórkowych organizmów zwierzę-
cych i roślinnych. Fitosterole, to sterole roślinne, swoją budową przypomina-
jące cholesterol, będący sterolem, charakterystycznym dla organizmów zwie-
rzęcych. Dotychczas poznanych zostało blisko 40 form steroli roślinnych,
z których jednak najbardziej poznane i najczęściej spotykane to
b-sitosterol
lub sitostanol, kampesterol lub kampestanol oraz stigmasterol i stigmasta-
nol, które swą budową są najbardziej zbliżone do pierścienia cholesterolowe-
go. Sterole roślinne to nazwa wszystkich związków, które zaliczane są do tej
grupy. W efekcie jednak, jest to dość myląca nazwa, gdyż sterolami określa-
my związki nienasycone, czyli posiadające w swym pierścieniu podwójne wią-
zania oraz stanole – ich formy nasycone, bez wiązań podwójnych. Stanole
powstają w wyniku uwodornienia steroli. Wszystkie te związki są słabo roz-
puszczalne w tłuszczach (średnio ok. 2%), będąc zarazem nierozpuszczalny-
mi w wodzie.
117
Tabela 7: Porównanie dwóch diet składających się z tej samej ilości produktów, lecz o różnej zawartości
tłuszczów
Produkty „tłuste”
Ilość
tłuszczu
[g]
Produkty „chude”
Ilość
tłuszczu
[g]
mleko 3,2% tł.
0,5 l
16
mleko 0,5%
tłuszczu
0,5 l
2,5
jogurt pełny
3,25%
150 g
4,8
jogurt niskotł.
0,18%
150 g
0,27
ser biały tłusty
100 g
9,2
ser biały chudy
100 g
1,2
salceson
50 g
14,5
szynka wołowa
50 g
2,5
boczek
100 g
47
wędlina
drobiowa
100 g
2,4
karp
150 g
10,7
dorsz
150 g
1,3
schab karkowy
150 g
35
cielęcina
150 g
3
razem
138
razem
14
138 g tłuszczu = 1242 kcal
14 g tłuszczu = 126 kcal
uwaga: 1 g tłuszczu dostarcza 9 kcal (kilokalorii) lub 37 kJ (kilodżuli)

Fitosterole (sterole i stanole) są naturalnymi składnikami olejów jadal-
nych, jednakże ich ilość w olejach jest bardzo zróżnicowana i na ogół dość
niska (z rafinacji 2500 ton olejów roślinnych można uzyskać 1 tonę steroli).
Występują również w innych produktach, jednakże z punktu widzenia żywie-
nia profilaktycznego, te ilości są znikome nawet u wegetarian, którzy spoży-
wając produkty roślinne, niekiedy tylko przekraczają 1000 mg (1 g) na dobę.
Innym źródłem (choć niezbyt bogatym) pozyskiwania steroli roślinnych są
elementy podkorowe sosen wysokopiennych. W przeciętnej, zwyczajowej
diecie, zawartość steroli jest niska. Podstawowe źródła tych składników w ży-
wieniu to oleje (zawierają od 100 do 500 mg steroli/100 g), rośliny strączko-
we (średnio ok. 220 mg/100 g) oraz niektóre nasiona – sezamu czy słoneczni-
ka (500-700 mg/100 g). Średnie spożycie steroli roślinnych w różnych krajach
jest różne, niemniej należy sądzić, iż w większości krajów europejskich,
w tym i w Polsce, wynosi średnio 200-300 mg/dzień. W Japonii, w diecie któ-
rej dominują produkty pochodzenia roślinnego, sięga ok. 400 mg/dzień.
Mechanizm hipocholesterolemicznego działania steroli i stanoli sprowa-
dza się do hamowania absorpcji cholesterolu w jelicie cienkim. Sprzyjają te-
mu również kwasy żółciowe wydzielane do dwunastnicy. Rozbite, kuliste
drobiny tłuszczu podlegają działaniu lipazy trzustkowej. Sole kwasów żół-
ciowych wytwarzają micelle, do których przenika wolny cholesterol i fosfoli-
pidy, dzięki czemu możliwa jest inkorporacja produktów lipolizy, czyli mo-
noglicerydów i kwasów tłuszczowych. Zanim jednak cholesterol pokarmowy
ulegnie wchłonięciu do wnętrza micelli, jego część (10-15%) ulega estryfika-
cji z kwasami tłuszczowymi. Dzięki działaniu trzustkowej esterazy choleste-
rolowej powstają jego formy wolne. Miejscem absorpcji produktów trawie-
nia tłuszczu jest górna część jelita czczego, przy czym monoglicerydy i kwasy
tłuszczowe są absorbowane wcześniej niż cholesterol. Cholesterol z żółci jest
lepiej absorbowany, niż pochodzący z pokarmów, gdyż w czasie wydzielania
żółci zostaje rozpuszczony w micellach, co ułatwia jego absorpcję. Precyzyj-
ny mechanizm transportu cholesterolu i lipidów do komórek jelitowych nie
jest do końca poznany. Przypuszcza się, iż decydującą rolę odgrywa gradient
pH. Mieszane micelle nie są transportowane w nienaruszonym stanie; mo-
noglicerydy, kwasy tłuszczowe i cholesterol, jako produkty rozpuszczalne
w tłuszczach, przechodzą przez warstwy lipidowe błon komórkowych rąbka
szczoteczkowego do wnętrza komórek, dzięki połączeniu z białkami oraz
w wyniku transportu biernego. W enterocycie jelitowym 70-90% choleste-
rolu poddane jest estryfikacji z kwasami tłuszczowymi, natomiast trójglicery-
dy są resyntetyzowane z monoglicerydów i kwasów tłuszczowych. Powstałe
estry cholesterolu i trójglicerydy ulegają połączeniu z apoproteiną B, two-
rząc chylomikrony, które dopiero są wydzielane do układu chłonnego, aby
118

poprzez transport do przewodu piersiowego przedostać się do krwi, gdzie
rozpoczyna się ich droga metaboliczna. Sterole, kompetytywnie zajmują
„miejsce” cholesterolu w micellach powodując jego zwiększone wydalanie
ze stolcem, gdyż hamując jego estryfikację w enterocycie, uniemożliwiają
transport zwrotny do krwi.
Korzystne oddziaływanie steroli jest możliwe dzięki temu, że hamują ab-
sorpcję cholesterolu, zarówno endogennego (wątrobowego), jak i egzogen-
nego (pokarmowego) w równym stopniu. Pula cholesterolu w jelicie cien-
kim, to blisko 70% cholesterolu z syntezy wątrobowej, wydzielanego z żółcią
oraz około 30% cholesterolu pokarmowego. Tylko 30-50% cholesterolu po-
karmowego jest absorbowane z jelita cienkiego. Na stopień tej absorpcji ma-
ją wpływ: ilość wydzielanej żółci, ruchy robaczkowe jelita, czynniki genetyczne
(np. fenotyp apoE), tłuszcz pokarmowy, wielkość cholesterolu w pokarmach
oraz podaż steroli roślinnych. Widać więc, iż ilość absorpcji cholesterolu za-
leży głównie od syntezy cholesterolu w organizmie, przybierając charakter
negatywnego sprzężenia zwrotnego; im absorpcja większa, tym produkcja
wątrobowa niższa, i odwrotnie.
Zjawisko kompensacyjnego wzrostu produkcji cholesterolu w wątrobie, na
skutek redukcji jego absorpcji w jelicie, nie jest w stanie zniwelować efektu
hipolipemicznego, wywołanego podażą steroli roślinnych. Można jednak
przypuszczać, że wzrost syntezy cholesterolu w wątrobie spowodowany jest
koniecznością wyrównania jego ubytku w żółci, do której dochodzi na skutek
inkorporacji do niej steroli, a nie cholesterolu, w trakcie absorpcji jelitowej.
Przypuszcza się, że wzrost syntezy cholesterolu po podaniu steroli wpływa
na metabolizm apolipoproteiny B. Dotychczasowe obserwacje sugerują, że
wzrost syntezy cholesterolu nie stanowi kompensacyjnego wyrównania jego
niedoboru w wątrobie, ale dzięki temu wzrasta reabsorpcja LDL z krwi do
wątroby, czemu towarzyszy wzrost receptorów dla LDL na powierzchni ko-
mórek wątrobowych. Jednocześnie zaobserwowano, iż produkcja lipoprote-
in o bardzo małej gęstości (VLDL), będących prekursorami LDL, w wyniku
stosowania steroli zostaje również zmniejszona, co w efekcie wpływa na ob-
niżenie ilości krążących we krwi LDL. Te zmiany zachodzące pod wpływem
steroli mogą tłumaczyć, dlaczego redukcja pokarmowej podaży cholesterolu
daje limitowany wpływ na poziom cholesterolu w surowicy krwi.
Dyskutowanym zagadnieniem był problem, czy sterole i stanole obniżają
stężenie cholesterolu frakcji LDL w takim samym stopniu i w taki sam spo-
sób. Jak wspomniano we wstępie, badania nad wykorzystaniem steroli ro-
ślinnych jako związków redukujących poziom cholesterolu w surowicy krwi
mają ponad pięćdziesiąt lat. Ostatnie piętnastolecie obfituje w liczne bada-
nia nad ich wykorzystaniem w profilaktyce miażdżycy, dzięki stworzeniu pro-
119

duktów spożywczych, takich jak margaryny, majonezy, dresingi czy jogurty
z ich dodatkiem, co dało możliwość szerszego i łatwiejszego zastosowania
w codziennym żywieniu. Majonez był pierwszym produktem spożywczym wy-
korzystanym jako nośnik steroli roślinnych. Jest to jednak produkt trudny
do wykorzystania w regularnym codziennym żywieniu, gdyż najczęściej uży-
wany jest jedynie jako dodatek do wybranych potraw. Nowe możliwości
otworzyły się, gdy wykorzystano margaryny, które okazały się najlepszymi
produktami do wzbogacania sterolami roślinnymi, z uwagi na odpowiednią
zawartość tłuszczu, nierzadko stanowiąc dodatkowe źródło nienasyconych
kwasów tłuszczowych. Sterole, jako związki nierozpuszczalne w wodzie, po-
trzebują tłuszczu jako nośnika, który umożliwia ich trawienie w tym samym
odcinku jelita cienkiego i w podobny sposób, jak cholesterol.
Dotychczasowe wyniki badań pokazują, iż dodatek do zwyczajowego ży-
wienia lub niskotłuszczowej diety steroli lub stanoli, powoduje spadek stę-
żenia cholesterolu całkowitego średnio o 7% i frakcji LDL o ok. 10%. Nie-
którzy autorzy sugerują, że spadek stężenia cholesterolu LDL sięga nawet
15% lub więcej, jednakże takie rezultaty osiągano w czasie jednoczesnego
stosowania diety niskotłuszczowej, suplementowanej odpowiednią podażą
frakcji rozpuszczalnych błonnika pokarmowego oraz witamin antyoksyda-
cyjnych.
Wielkość redukującego oddziaływania steroli roślinnych zależna jest od
dawki. Na podstawie dotychczasowych obserwacji można sądzić, iż optymal-
ną dawką steroli i stanoli w dziennych racjach pokarmowych wykazującą
efekt hipocholesterolemiczny jest ilość powyżej 2 g, ale nie przekraczająca
3 g. Oznacza to praktycznie, iż codziennie winno się spożywać od 4 do 6 ły-
żeczek od herbaty margaryn ze sterolami roślinnymi. Zwiększanie dawek
powyżej tej ilości nie powoduje wyższej redukcji cholesterolu całkowitego
i LDL. Powyższe obserwacje są szczególnie zachęcające do stosowania stero-
li roślinnych, gdyż jak pokazują wieloletnie doświadczenia z praktycznym
stosowaniem diety I° wg AHA, przynosi to efekt obniżenia cholesterolu
LDL średnio od 3 do 4,5%. Przy czym należy zaznaczyć, że zastosowanie ta-
kiej diety wymaga od ludzi dość gruntownej zmiany dotychczasowych zacho-
wań żywieniowych i dlatego posiada ograniczoną skuteczność.
Innym niezwykle korzystnym zjawiskiem terapeutycznego stosowania ste-
roli roślinnych w leczeniu pacjentów z hipercholesterolemią jest fakt, iż nie
wywierają one wpływu na stężenie cholesterolu frakcji HDL. Jest to czynnik
odróżniający je od oddziaływania margaryn bogatych w wielonienasycone
kwasy tłuszczowe, których stosowanie przynosi korzystne efekty hipolipe-
miczne (spadek cholesterolu całkowitego i frakcji LDL), powodując nieste-
120

ty u niektórych również spadek stężenia cholesterolu HDL, średnio o 2-4%.
Jest to w wielu wypadkach zjawisko niekorzystne, szczególnie u pacjentów
z cukrzycą, u których zaburzenia gospodarki lipidowej charakteryzują się hi-
pertrójglicerydemią i niskimi poziomami cholesterolu frakcji HDL. Pamiętać
przy tym należy, iż obniżone stężenie cholesterolu HDL (poniżej 40 mg/dL)
jest niezależnym, istotnym czynnikiem ryzyka choroby niedokrwiennej serca.
Dlatego też sterole roślinne stają się szansą na leczenie zaburzeń gospodar-
ki lipidowej wśród pacjentów z cukrzycą, otyłością typu androidalnego, pala-
czy papierosów, leczonych hormonalnie, u których często stężenie choleste-
rolu HDL jest niskie. W dotychczasowych badaniach stwierdzono, iż zmiany
w składzie lipidów zachodzące pod wpływem steroli roślinnych, prowadzą
do obniżenia wskaźników aterogennych (TC/HDL-C i LDL-C/HDL-C),
które są wyrazem korzystnego oddziaływania terapii. Dlatego też, bez wzglę-
du na podejście do oceny predykcyjnej przydatności obu tych wskaźników
w ocenie ryzyka choroby niedokrwiennej serca, należy dążyć w trakcie lecze-
nia do ich obniżania.
Sterole i stanole w żywieniu dzieci
Stosowanie margaryn w żywieniu dzieci budziło i budzi wiele, często nie-
uzasadnionych kontrowersji; odnosi się to również do margaryn ze sterola-
mi. Wyniki badania STRIP pokazują, że sterole roślinne w żywieniu 6-le-
tnich dzieci już po 3 miesiącach, przynoszą równie korzystne jak u dorosłych,
efekty hipolipemiczne. Wykazano, iż zastosowanie u zdrowych dzieci 3 g sta-
noli dziennie, powoduje spadek cholesterolu LDL o 16%, w stosunku do
wartości tej frakcji w trakcie stosowania zwyczajowej diety, natomiast poda-
nie 1,5 g stanoli redukuje o 7,5% stężenie cholesterolu LDL. Stwierdzono,
że podaż stanoli nie powoduje u dzieci żadnych ubocznych efektów, ani
zmian we wskaźnikach antropometrycznych, czy spowolnienia rozwoju psy-
chicznego. Również u dzieci młodszych (od 2 do 5 lat), po podaniu stanoli
w ilości 3 g na dobę stwierdzono już po 4 tygodniach redukcję cholesterolu
całkowitego o 12%, a cholesterolu LDL o blisko 16%. Porównywano taką
dietę do diety wysokobłonnikowej, której zastosowanie u dzieci w takim sa-
mym okresie przyniosło redukcję cholesterolu całkowitego tylko o 4%. Uzy-
skane różnice nie pozostawiają wątpliwości co do skuteczności diety ze ste-
rolami roślinnymi.
Sterole roślinne a witaminy
Mając świadomość mechanizmu działania steroli, niepokój wielu badaczy
budzi w wyniku ich stosowania – stwierdzanie obniżenia stężenia
b-karotenu
121

w surowicy krwi. Należy przy tym zaznaczyć, że stężenie witaminy A w suro-
wicy krwi nie podlega takim zmianom, podobnie jak pozostałych witamin
rozpuszczalnych w tłuszczach. Opublikowane w 2002 roku badania pokazu-
ją, iż jeśli w dziennej racji pokarmowej nie ma dostatecznej podaży owoców
i warzyw stanowiących źródło
b-karotenu, to wówczas jego stężenie w suro-
wicy krwi obniża się, niezależnie, czy podawane są w diecie sterole czy nie.
Dlatego też, zaleca się wszystkim, a szczególnie osobom stosującym sterole
roślinne, aby w ich diecie była dostateczna podaż pokarmowych źródeł karo-
tenoidów. Oznacza to, iż osoby stosujące w swoim żywieniu margaryny ze
sterolami powinny codziennie spożywać ok. 200 g warzyw i owoców poma-
rańczowo-zielonych, takich jak marchew, papryka, szpinak, sałata, szczypio-
rek lub morele, arbuzy, brzoskwinie, melony, śliwki, pomarańcze i wiele in-
nych.
Sterole roślinne a statyny
Liczne badania kliniczne i epidemiologiczne z zastosowaniem inhibitorów
reduktazy HMG-CoA sugerują, iż ich hipolipemiczna efektywność u pacjen-
tów z hipercholesterolemią waha się w granicach od 24 do 50%. Wykazano,
że jeśli pacjenci z hipercholesterolemią leczeni są (niezależnie od dawki) sta-
tynami (lowastatyna, prawastatyna, simwastatyna), to dodatek do ich diety
steroli lub stanoli powoduje dodatkowo redukcję cholesterolu całkowitego
średnio o 7% i LDL o 10%. Oznacza to, że terapia łączona – statyny i stero-
le roślinne, przynosi korzystniejsze efekty. Redukcja lipidów u osób leczo-
nych farmakologicznie nie zmienia możliwości hipolipemicznego działania
steroli, będąc podobną do wielkości redukcji, jaką obserwuje się u osób bez
farmakoterapii. Nie u wszystkich terapia statynami i sterolami zwiększa re-
dukcję cholesterolu LDL w tym samym stopniu. Przypuszcza się, iż jedną
z przyczyn może być fakt, iż osoby z wysoką absorpcją i jednocześnie niską
syntezą cholesterolu nie odpowiadają obniżeniem stężenia lipidów w czasie
stosowania steroli i być może statyn. Natomiast bardzo korzystne efekty uzy-
skuje się prowadząc terapię skojarzoną u pacjentów z wysoką syntezą i ni-
ską absorpcją cholesterolu. Jedno opublikowane badanie francuskie nad łą-
czeniem terapii margarynami wzbogaconymi sterolami z leczeniem fibratami
pacjentów z hiperlipidemią mieszaną, pokazuje korzystny efekt terapeutycz-
ny, którego wyrazem jest zwiększona o ok. 3% redukcja cholesterolu LDL.
Zagadnienie to wymaga jednak potwierdzenia w innych badaniach.
Jak wynika z przeglądu wyników wielu badań, zastosowanie steroli roślin-
nych w margarynach jest niezwykle obiecujące w prewencji chorób układu
krążenia. Należy oczekiwać, iż najbliższe lata potwierdzą opinię M. Law, iż
122

stosowanie w codziennym żywieniu tłuszczów roślinnych wzbogaconych ste-
rolami lub stanolami, poprzez obniżenie cholesterolu frakcji LDL, reduku-
je ryzyko choroby niedokrwiennej serca o 25%.
Zapamiętaj!
1. Masło jest najbogatszym źródłem aterogennych, nasyconych kwasów tłusz-
czowych w codziennym żywieniu.
2. Wielonienasycone kwasy tłuszczowe rodziny omega-3 pochodzące z ryb
morskich, wykazują działanie hipolipemiczne, antyagregacyjne, przeciwza-
palne, hipotensyjne oraz przeciwarytmiczne i dlatego ich udział w codzien-
nym żywieniu jest nieodzowny.
3. Sterole i stanole roślinne spożywane z żywnością w ilości 2-3 g/dziennie, re-
dukują stężenie cholesterolu we frakcji LDL średnio o 10-12%, zarówno
u osób z normo-, jak i hiperlipidemią.
Warto przeczytać:
W. J. Bemelmans, J. Broer, E. J. Feskens i wsp.: Effect of an increased inta-
ke of
a-linolenic acid and group nutritional education on cardiovascular risk
factors: the Mediterranean Alpha-linolenic Enriched Groningen Dietary In-
tervention (MARGARIN) study. Am. J. Clin. Nutr. 2002; 75: 221.
Diet, nutrition and prevention of chronic disease. Report of the Joint
WHO/FAO expert consultation. Geneva 2002.
J. T. Judd, D. J. Baer, B. A. Clevidence i wsp.: Effects of margarine compa-
red with those of butter on blood lipid profiles related to cardiovascular dise-
ase risk factors in normolipemic adults fed controlled diets. Am. J. Clin.
Nutr. 1998; 68: 768.
M. Kozłowska-Wojciechowska, H. Bukowska, M. Makarewicz-Wujec
i wsp.: Reduction of the plasma LDL-cholesterol level among young men as
a results of the change from butter in to margarine on the unbalanced diet.
Pol. Arch. Med. Wewn. 2001; 105: 29.
M. Law: Plant sterol and stanol margarines and health. BMJ. 2000; 320: 861.
A. H. Lichtenstein, R. J. Deckelbaum: AHA Science Advisory: Stanol/sterol
ester-containing foods and blood cholesterol levels. Circulation 2001; 103:
1177.
123

H. A. Neil, G. W. Meijer, L. S. Roe: Randomized controlled trial of use by
hypercholesterolaemic patients of a vegetable oil sterol-enriched fat spread.
Atherosclerosis 2001; 156: 329-337.
M. Noakes, P. Clifton, F. Ntanios i wsp.: An increase in dietary carotenoids
when consuming plant sterols or stanols is effective in maintaining plasma
carotenoid concentrations. Am. J. Clin. Nutr. 2002; 75: 79-86.
J. Plat, R. P. Mensink: Effects of plant sterols and stanols on lipid metabo-
lism and cardiovascular risk. Nutr. Metab. Cardiovasc. Dis. 2001; 11: 31.
E. J. Schaefer: Lipoproteins, nutrition, and heart disease. Am. J. Clin. Nutr.
2002; 75: 191.
H. Kunachowicz, I. Nadolna, B. Przygoda i wsp.: Tabele wartości odżywczej
produktów spożywczych. Prace IŻŻ, Warszawa 1998.
124

VIII. AKTYWNOŚĆ FIZYCZNA W PROFILAKTYCE
CHOROBY NIEDOKRWIENNEJ SERCA – RECEPTA
NA WYSIŁEK
Hubert Krysztofiak, Artur Mamcarz
„Aktywność fizyczna jest jedyną właściwą przeciwwagą dla braku aktywności
fizycznej. Jest znaczącym czynnikiem utrzymującym stan zdrowia i zabezpiecza-
jącym przed upośledzeniem zdrowia wynikającym z braku aktywności fizycznej.
Jeśli obywatele świata byliby wystarczająco aktywni ogromny problem, tak obec-
nie powszechnych chorób nie zakaźnych – na przykład choroby niedokrwien-
nej serca, zmniejszyłby się znacząco. W dużych populacjach o 10-20%, a cza-
sem więcej. Duża liczba starszych ludzi utrzymywałaby możliwość życia
niezależnie o wiele lat dłużej”.
(WHO, Plakat na World-Health-Day 2002)
WSTĘP
Trzy główne czynniki wpływają na stan zdrowia jednostki i na długość życia
człowieka: czynniki genetyczne, bezpośrednia działalność służby zdrowia
i czynniki środowiskowe. Trudno jeszcze dzisiaj mówić o możliwości wpływu
jednostki na pierwsze dwa czynniki. Jednak każdy może próbować unikać
czynników środowiskowych lub modyfikować ich niekorzystny wpływ. Naj-
skuteczniejszą metodą niwelowania negatywnego wpływu czynników środo-
wiskowych jest kształtowanie prawidłowych nawyków zdrowotnych. Listę
prawidłowych nawyków otwiera aktywność fizyczna.
Brak odpowiedniego poziomu aktywność fizycznej jest czynnikiem ryzyka
choroby niedokrwiennej serca, chorób metabolicznych i nowotworowych.
Dzisiaj nie ulega wątpliwości, że lekarze powinni promować aktywność fi-
zyczną wśród swoich pacjentów. Jednak, aby zachęcić pacjentów do zwięk-
szenia aktywności fizycznej nie wystarczy stwierdzić: przydałoby się, aby
Pan/Pani zwiększył/a swoją aktywność fizyczną. Konsekwencją takiego
stwierdzenia powinna być „recepta na wysiłek”, zarys programu aktywności
fizycznej, z określeniem formy, intensywności, czasu trwania i częstości po-
wtarzania sesji aktywności fizycznej, czyli program treningowy.
Celem niniejszego rozdziału jest zaprezentowanie informacji, które do-
starczą podstaw do efektywnego promowania aktywności fizycznej. W ko-
lejnych podrozdziałach omówione zostaną: mechanizmy biologiczne korzyst-
nego oddziaływania aktywności fizycznej, podstawy fizjologii wysiłku
fizycznego, fizjologiczne efekty treningu fizycznego, podstawowe informa-
125

cje dotyczące struktury i składowych treningu, zasady kwalifikacji i ustala-
nia obciążeń treningowych. Wyżej wymienione elementy omówione będą
w odniesieniu do wysiłków dynamicznych, aerobowych (tlenowych). Tego ty-
pu wysiłki bowiem są przede wszystkim rekomendowane w prewencji cho-
roby niedokrwiennej serca. Jednakże, w związku z doniesieniami sugerujący-
mi korzyści z włączania elementów treningu oporowego do programów
aktywności fizycznej, trening oporowy zostanie omówiony w oddzielnym
podrozdziale.
MECHANIZMY BIOLOGICZNE KORZYSTNEGO WPŁYWU
AKTYWNOŚCI FIZYCZNEJ
Regularna aktywność fizyczna przynosi istotne korzyści zdrowotne (tab. 1).
Specyficzne mechanizmy odpowiedzialne za wystąpienie tych korzystnych
zmian nie są jednak w pełni poznane. Trening fizyczny powoduje korzystną
modyfikację czynników ryzyka choroby niedokrwiennej serca. Redukuje ci-
śnienie i zapobiega cukrzycy, korzystnie zmienia profil lipidowy i wspomaga
kontrolę masy ciała. Korzystne efekty nie mogą być przypisane jedynie mo-
dyfikacji czynników ryzyka, ponieważ regularny wysiłek fizyczny obniża
współczynnik umieralności niezależnie od wpływu na inne czynniki ryzyka.
126
• redukcja ryzyka przedwczesnej śmierci;
• redukcja ryzyka zgonu z powodu chorób serca;
• redukcja ryzyka rozwoju cukrzycy;
• redukcja ryzyka rozwoju nadciśnienia tętniczego;
• wspomaganie redukcji ciśnienia u osób, które mają nadciśnienie
tętnicze;
• wspomaganie kontroli masy ciała;
a także:
• redukcja ryzyka rozwoju raka jelita grubego;
• redukcja rozwoju raka piersi;
• wspomaganie ograniczenia rozwoju osteoporozy;
• redukcja stresu i uczucia depresji, poprawa nastroju;
• poprawa i utrzymywanie odpowiedniego poziomu wydolności
fizycznej.
Tabela 1: Korzyści z regularnej aktywności fizycznej

Nadciśnienie tętnicze
Korzystny wpływ regularnej aktywności fizycznej na występowanie nadci-
śnienia tętniczego (NT) wykazały dwa duże badania z lat 1983-1984. Ich
efektem było stwierdzenie, że aktywność fizyczna nie tylko zapobiega roz-
wojowi nadciśnienia, ale także obniża ciśnienie tętnicze u osób z rozpozna-
ną już chorobą. U osób z łagodnym nadciśnieniem obserwuje się obniżenie
ciśnienia tętniczego przez 8 do 12 godzin po zakończeniu treningu. Średnie
ciśnienie tętnicze w dniu wysiłku jest istotnie niższe w porównaniu do dnia
bez aktywności fizycznej. Korzystny, obniżający wpływ dotyczy zarówno ci-
śnienia skurczowego, jak i rozkurczowego. Ciśnienie skurczowe obniża się
średnio o 10 mm Hg, a rozkurczowe o 8 mm Hg. Oczywiście pojawia się py-
tanie, czy włączenie do codziennego funkcjonowania odpowiedniej aktyw-
ności fizycznej może wpłynąć na dawkowanie leków przeciwnadciśnienio-
wych? Odpowiedź: opierając się na doniesieniach klinicznych można
stwierdzić, że przeciwnadciśnieniowy efekt wysiłku fizycznego utrzymuje się
po redukcji dawki leków.
Cukrzyca
Regularna aktywność fizyczna korzystnie wpływa na metabolizm glukozy
i odpowiedź komórek na insulinę. Obniża produkcję glukozy przez wątro-
bę. Powoduje większe wykorzystanie glukozy przez mięśnie, ograniczając do-
stępność dla tkanki tłuszczowej. Ważne jest także, aby pamiętać, że podczas
wysiłku transport glukozy do komórki jest – przynajmniej częściowo – nieza-
leżny od insuliny. Dodatkowym korzystnym efektem w „relacji” aktywność fi-
zyczna – cukrzyca, jest redukcja masy ciała.
Profil lipidowy
Przeprowadzono wiele badań dotyczących wpływu regularnej aktywności
fizycznej na profil lipidowy. Zmienność opisywanych wyników jest duża,
a wynika ona z różnorodności zastosowanych metod badawczych, czasu
trwania badania, badanych populacji, programów treningowych, czy wreszcie
dodatkowych interwencji farmakologicznych. Analiza większości prac po-
zwala jednak na wysunięcie następujących wniosków: regularna aktywność
fizyczna prowadzi do obniżenia poziomu cholesterolu całkowitego (TC)
(~6%), frakcji LDL (~10%) i wskaźnika TC/frakcji HDL (~13%). Jedno-
cześnie obserwuje się wzrost poziomu HDL (~5%). Co ciekawe, korzystne
zmiany poziomu HDL obserwuje się już przy aktywności fizycznej o niewiel-
kiej intensywności. W tym miejscu należy zaznaczyć, że w leczeniu zaburzeń
127

lipidowych aktywność fizyczna jest uzupełnieniem (istotnym, ale jednak uzu-
pełnieniem) prawidłowej diety i że aktywność fizyczna nie normalizuje za-
burzeń lipidowych o podłożu genetycznym.
Otyłość
W otyłości, podobnie jak w zaburzeniach lipidowych, aktywność fizyczna
wspomaga proces redukcji masy ciała i ogranicza powtórny przyrost masy
ciała. Efekt łączonej terapii – dieta i aktywność fizyczna – jest istotnie więk-
szy niż efekt samej diety (nawet o 60%). Nie jest natomiast w pełni jasne,
jaki poziom aktywności fizycznej jest optymalny w terapii otyłości. Wydaje
się, że powinien on być znacznie wyższy niż ten, który jest obecnie zalecany.
Jednak aktywność fizyczna w otyłości to nie tylko dodatkowy wydatek kalo-
ryczny, czyli korzystniejszy bilans energetyczny. Regularny wysiłek fizyczny
korzystnie modyfikuje skład ciała i dystrybucję tkanki tłuszczowej. Osoby
aktywne fizycznie, w porównaniu do osób mało aktywnych mają korzystniej-
szy wskaźnik obwodu pasa do obwodu bioder (mniej otyłości centralnej).
Dodatkowo, poprawa nastroju będąca także efektem wysiłków fizycznych,
wspomaga kształtowanie prawidłowych nawyków żywieniowych.
Efekt przeciwmiażdżycowy
Regularny trening fizyczny wpływa na zaawansowanie zmian miażdżyco-
wych. Ten korzystny wpływ aktywności fizycznej jest jednak efektem pośred-
nim, wynikającym z redukcji i redystrybucji tkanki tłuszczowej, redukcji ci-
śnienia tętniczego, modyfikacji profilu lipidowego i poprawy tolerancji
glukozy.
Badania eksperymentalne wskazują także na mechanizmy biologiczne,
które pozwalają wyjaśnić niezależny wpływ aktywności fizycznej, ogranicza-
jącej rozwój i zaawansowanie choroby niedokrwiennej serca. Najważniejsze
z tych mechanizmów to efekt przeciwzakrzepowy, poprawa funkcji śródbłon-
ka, zmiany równowagi w układzie autonomicznym i efekt przeciwniedo-
krwienny.
Efekt przeciwzakrzepowy
Aktywność fizyczna wywołuje korzystne zmiany w układzie krzepnięcia,
wyrażone w szczególności wzrostem aktywności fibrynolitycznej osocza.
Efektem systematycznego treningu fizycznego jest poprawa wskaźników ho-
meostazy – obniżeniu ulega poziom fibrynogenu, wzrasta poziom tkanko-
wego aktywatora plazminogenu, obniża się stężenie inhibitora aktywatora
128

plazminogenu. Badania wykazują natomiast nasilenie aktywacji płytkowej
u osób mało aktywnych fizycznie po krótkotrwałym wysiłku. Regularna ak-
tywność fizyczna zdecydowanie ogranicza jednak tego typu odpowiedź.
Funkcja śródbłonka
Pochodzące ze śródbłonka czynniki rozkurczające, na przykład tlenek azo-
tu (NO), uczestniczą w regulacji napięcia naczyń tętniczych i kontrolują
miejscowe procesy agregacji płytek. U pacjentów z chorobą niedokrwienną
serca, zależny od śródbłonka rozkurcz naczyń jest upośledzony. Podobnie
u osób z zaburzeniami lipidowymi, cukrzycą czy nadciśnieniem. Regularne
ćwiczenia dynamiczne poprawiają funkcję śródbłonka.
Zmiany w układzie autonomicznym
Zwiększone napięcie układu współczulnego, wyrażone podwyższeniem stę-
żenia amin katecholowych w surowicy, jest związane ze wzrostem ryzyka incy-
dentu wieńcowego, szczególnie u pacjentów z rozpoznaną chorobą serca.
Osoby aktywne fizycznie w porównaniu z osobami prowadzącymi mało ak-
tywny tryb życia, charakteryzują się większą aktywnością układu przywspół-
czulnego. Poprawę równowagi w układzie autonomicznym, czyli zmniejsze-
nie napięcia układu współczulnego pod wpływem treningu fizycznego,
obserwuje się także u pacjentów z niewydolnością serca i po zawale mięśnia
sercowego. Oceny równowagi pomiędzy układem współczulnym i przywspół-
czulnym można dokonać analizując m.in. zmienność rytmu serca.
Z korzystnymi zmianami w układzie autonomicznym u osób aktywnych fi-
zycznie wiąże się także zmniejszenie częstości występowania groźnych zabu-
rzeń rytmu serca.
Efekt przeciwniedokrwienny
Istotnym skutkiem zwiększenia wydolności fizycznej pod wpływem trenin-
gu fizycznego jest poprawa bilansu energetycznego, dotycząca także serca.
Poprawa bilansu energetycznego jest z jednej strony wynikiem względnie
mniejszego zapotrzebowania na tlen, z drugiej zaś zwiększenia możliwości
dostarczenia tlenu do pracującego mięśnia. Efektem tego jest podwyższenie
progu wystąpienia niedokrwienia mięśnia sercowego.
PODSTAWY FIZJOLOGII WYSIŁKU FIZYCZNEGO
Wysiłek fizyczny jest związany ze skurczem mięśni. W odniesieniu do izo-
lowanego mięśnia możemy mówić o:
129

Klasyfikacja wysiłków
W odniesieniu do całego ciała, klasyfikując wysiłki fizyczne w zależności
od skurczów mięśni, mówimy o wysiłkach dynamicznych, gdzie zdecydowa-
nie dominują skurcze izotoniczne (szczególnie dużych grup mięśniowych)
i o wysiłkach statycznych, gdzie zdecydowanie dominują skurcze izometrycz-
ne. Przykładem wysiłku statycznego jest hand-grip. Szczególnym typem wysił-
ku jest wysiłek oporowy, czasami opisywany jako mieszany, dynamiczno-st-
atyczny. W wysiłku oporowym pojawia się dodatkowy element – siła
przeciwdziałająca kurczącemu się mięśniowi. Przykładem ćwiczeń oporo-
wych są pompki, czy podciąganie się na drążku. Częściej natomiast ten ro-
dzaj wysiłku kojarzy się z ćwiczeniami na przyrządach i tak zwanym trenin-
giem siłowym. Powyższy podział opiera się na dominującym rodzaju skurczu
mięśni. Inny, stosowany powszechnie podział, opiera się na sposobie dostar-
czania energii do pracy mięśni. Biorąc pod uwagę sposób pozyskiwania ener-
gii do pracy mięśni mówimy o wysiłkach tlenowych (aerobowych) i beztle-
nowych (anaerobowych). Wysiłki tlenowe to takie, podczas których
większość energii do pracy uzyskiwana jest w wyniku biochemicznych pro-
cesów tlenowych. Wysiłki beztlenowe natomiast, zabezpieczane są w ener-
gię przy wykorzystaniu procesów beztlenowych.
Energetyka wysiłków fizycznych
Istotą skurczu mięśni jest przemiana energii chemicznej w energię mecha-
niczną. Bezpośrednim źródłem energii do skurczu jest adenozynotrójfosfo-
ran (ATP). Uwolnienie energii jest wynikiem rozkładu cząsteczki ATP zgod-
nie z równaniem:
ATP
® ADP + P + energia
Zapas ATP wystarcza jednak tylko na kilka skurczów maksymalnych.
Wzrost stężenia ADP i obniżenie stężenia ATP w komórce aktywizuje szereg
procesów prowadzących do odtworzenia ATP. Resynteza ATP może odby-
wać się w wyniku wewnętrznej reakcji katalizowanej przez kinazę adenylową,
zgodnie z równaniem:
130
• skurczu izotonicznym, którego efektem jest skrócenie długości
mięśnia, a co za tym idzie ruch;
oraz
• skurczu izometrycznym, którego wynikiem jest wzrost napięcia
mięśnia, ale brak jest efektu w postaci ruchu.

ADP + ADP
® ATP + AMP
Adenozynomonofosforan jest dodatkowym, silnym aktywatorem proce-
sów resyntezy ATP. Pierwszym związkiem podlegającym tej aktywacji jest
fosfokreatyna (PCr). Rozkład cząsteczki PCr przebiega pod wpływem kina-
zy kreatynowej.
PCr + ADP
® ATP + Cr
Powyższa reakcja poza dostarczaniem energii jest też wykorzystywana do
przenoszenia ATP z miejsc, w których jest on wytwarzany w dużych ilościach
(mitochondria) do miejsc, w których jest zużywany (włókienka kurczliwe).
Reakcja fosfokreatynowa jest reakcją beztlenową, charakteryzuje się wyso-
kim tempem (energia uzyskiwana jest bardzo szybko). Jest to natomiast pro-
ces o małej pojemności, zapewniający efektywne odtwarzanie ATP przez
najwyżej kilkanaście sekund. Procesem aktywowanym w dalszej kolejności
jest glikoliza.
2ATP + C6
® C3 + C3 ® pirogronian + pirogronian
pirogronian + pirogronian
® mleczan + mleczan + 4ATP
Efektem netto tej reakcji są dwie cząsteczki ATP. Glikoliza jest procesem
beztlenowym. Charakteryzuje się wysokim tempem (jednak dwa razy niż-
szym niż rozkład PCr). Mleczan (LA), powstający pod wpływem dehydro-
genazy mleczanowej z pirogronianu, podczas glikolizy dyfunduje do krwi.
Jednak w związku z tym, że proces dyfuzji jest wolniejszy niż proces wytwa-
rzania, stężenie LA w mięśniach może być dwukrotnie wyższe niż we krwi.
Wraz z wydłużaniem się czasu trwania wysiłku, zwiększa się dostępność
tlenu i substratów energetycznych. Wtedy też w pozyskiwaniu energii wzra-
sta udział procesów tlenowych. Wytwarzanie ATP sprzężone z procesami
utleniania w mitochondriach nosi nazwę fosforylacji oksydacyjnej. Dostęp-
ność tlenu determinuje utylizację produktu glikolizy, pirogronianu w proce-
sach tlenowych.
C6
® C3 + C3 ® pirogronian + pirogronian fosforylacja oksydacyjna
Ten proces, charakteryzujący się największą pojemnością jest jednocześnie
najbardziej ekonomicznym sposobem resyntezy ATP, jednak kluczowym ele-
mentem w funkcjonowaniu tego procesu jest dostępność tlenu.
Pobieranie tlenu
Za dostarczanie tlenu do wszystkich komórek organizmu odpowiedzialny
jest układ krążenia. Najważniejszym czynnikiem warunkującym odpowiedni
poziom zaopatrzenia w tlen jest objętość minutowa serca. Miarą ilości tle-
131

nu pobieranego przez organizm jest wskaźnik nazywany pobieraniem tlenu
(VO
2
). Pobieranie tlenu jest produktem objętości minutowej serca (CO)
i różnicy tętniczo-żylnej (a-vO
2
diff), która jest miarą wychwytu tlenu.
VO
2
= CO x a-vO
2
diff
Podczas wysiłku fizycznego zapotrzebowanie na tlen wzrasta proporcjo-
nalnie do intensywności wysiłku. Tak samo jak zapotrzebowanie, proporcjo-
nalnie do intensywności wysiłku, wzrasta poziom VO
2
. Przyrost poziomu
VO
2
jest konsekwencją wzrostu zarówno objętości minutowej, jak i różnicy
tętniczo-żylnej. Jednak, gdy progresywnie wzrasta intensywność wysiłku, po-
jawia się moment, kiedy zapotrzebowanie na tlen przekracza ilość pobrane-
go tlenu i mimo wzrostu obciążenia wysiłkowego brak jest przyrostu VO
2
.
Pobieranie tlenu w funkcji obciążenia osiąga wtedy stały poziom (plateau),
określany jako maksymalne pobieranie tlenu, albo pułap tlenowy (VO
2max
).
Poziom VO
2max
uznaje się za jeden z najważniejszych parametrów oceny wy-
dolności fizycznej. Plateau VO
2
w funkcji obciążenia nie zawsze udaje się
osiągnąć nawet u sportowców. Powodem takiej sytuacji jest silne zmęczenie,
ogólny dyskomfort i brak motywacji. Dlatego w wynikach testów stosowa-
nych do oceny wydolności używa się terminu szczytowe pobieranie tlenu,
czyli najwyższe osiągnięte podczas testu wykonywanego do odmowy (do cał-
kowitego zmęczenia). W warunkach klinicznych w zasadzie nie wykonuje się
takich testów.
U osób o najwyższej wydolności fizycznej obserwuje się nawet 24-krotny
wzrost pobierania tlenu w stosunku do wartości spoczynkowych (najwyższa
udokumentowana wartość VO
2max
wynosiła 94 ml O
2
/min/kg mc – norweski
biegacz narciarski, mistrz olimpijski z 1998 roku). W testach wysiłkowych
używa się czasami jednostki zwanej MET (od: metabolic equivalent): 1 MET
odpowiada spoczynkowemu pobieraniu tlenu, w przybliżeniu 3,5 ml
O
2
/min/kg mc. Zatem wynik wymienionego powyżej mistrza olimpijskiego
wyrażony w MET's wynosi ~27. Większość stosowanych obecnie urządzeń
do testów wysiłkowych ma zainstalowaną opcję wyznaczania przybliżonego
wydatku energetycznego, wyrażonego w jednostkach MET, według wzorów
opracowanych przez ACSM (American College of Sports Medicine).
Mleczan w czasie wysiłku
Gdy wraz ze wzrostem obciążenia wysiłkowego pojawia się niekorzystny
bilans pomiędzy zapotrzebowaniem, a pobieraniem tlenu, zwiększa się
udział glikolizy w procesach uzyskiwania energii. Miarą nasilenia glikolizy
jest poziom mleczanu (LA) w surowicy krwi. Podczas wysiłków o stopniowo
wzrastającej intensywności (najpowszechniej stosowanych w diagnostyce),
132

stężenie LA zmienia się w charakterystyczny sposób: przy małych i średnich
obciążeniach przyrost stężenia mleczanu w surowicy jest nieznaczny (często
oscyluje około wartości spoczynkowych), aż przy pewnym kolejnym obcią-
żeniu obserwuje się nagły, znaczący wzrost stężenia LA i akcelerację tego
przyrostu w kolejnych obciążeniach. Przebieg zmian stężenia mleczanu
w funkcji obciążenia ma zatem charakter wykładniczy. Nagły wzrost stężenia
LA w czasie wysiłku określa się mianem progu beztlenowego (progu mle-
czanowego, LAT). Próg beztlenowy jest momentem, kiedy w pozyskiwaniu
energii zaczynają dominować procesy beztlenowe. Poziom progu beztleno-
wego, wyrażony w jednostkach obciążenia, jest kolejnym, bardzo istotnym
parametrem oceny wydolności fizycznej.
Układ krążenia podczas wysiłku fizycznego
Gdy zbliża się moment rozpoczęcia wysiłku, częstość skurczów serca (HR)
wzrasta wyraźnie ponad wartości spoczynkowe. Jest to tak zwany efekt wy-
czekiwania (anticipatory response), będący skutkiem aktywacji współczulnej
i prawdopodobnie obniżenia napięcia nerwu błędnego. Układ krążenia przy-
gotowuje się do odpowiedzi na wzrost aktywności metabolicznej mięśni. Po
rozpoczęciu wysiłku, wskutek nasilonej aktywności metabolicznej, a co za
tym idzie zmiany w otaczającym środowisku, uruchamianych jest szereg lo-
kalnych czynników zwiększających przepływ krwi przez aktywne obszary.
Aby efekt był skuteczny i pełny, konsekwencją zmian lokalnych musi być
adekwatny wzrost objętości minutowej serca.
Spoczynkowa objętość minutowa serca (CO) wynosi około 5.0 l/min. Pod-
czas wysiłku CO wzrasta proporcjonalnie do obciążenia, nawet ośmiokrotnie
w stosunku do wartości spoczynkowej. Maksymalny poziom objętości minu-
towej serca może różnić się indywidualnie, w zależności od rozmiarów ciała
i poziomu wydolności fizycznej. Liniowa zależność pomiędzy CO i obciąże-
niem nie powinna dziwić, ponieważ celem przyrostu CO jest sprostanie za-
potrzebowaniu mięśni na tlen.
Wzrost objętości minutowej serca podczas wysiłku jest wynikiem wzrostu
HR i objętości wyrzutowej serca (SV).
CO = HR x SV
Udział HR i SV w kształtowaniu objętości minutowej nie jest jednak pro-
porcjonalny. Częstość skurczów serca wzrasta proporcjonalnie do intensyw-
ności wysiłku. Przebieg zmian częstości skurczów serca w funkcji obciążenia
ma przebieg w zasadzie liniowy. Zwiększenie HR podczas wysiłku fizyczne-
go jest efektem zmniejszenia napięcia nerwu błędnego lub nawet jego znie-
133

sienia w czasie wysiłków o wysokiej intensywności i wzrostu aktywności ukła-
du współczulnego. Maksymalna częstość skurczów serca (HR
max
) osiągana
w testach wykonywanych do odmowy jest uzależniona przede wszystkim od
wieku badanego. Dla określenia przybliżonej HR
max
, zazwyczaj wykorzystu-
je się uproszczony wzór:
HR
max
= 220 – wiek w latach
Objętość wyrzutowa serca jest determinowana przez cztery czynniki: po-
wrót żylny (pre-load), czynność rozkurczową, kurczliwość i opór obwodowy
(after-load). Pierwsze dwa czynniki wpływają na objętość krwi, którą mogą
przyjąć jamy serca, kolejne dwa wpływają na zdolność do ich opróżniania.
Wysiłkowy wzrost SV jest konsekwencją zarówno większego wypełnienia
jam serca przed skurczem (wzrost objętości późno-rozkurczowej, EDV), jak
i zwiększonego opróżniania jam serca (obniżenie objętości późno-skurczo-
wej, ESV). Wzrost EDV otwiera możliwość działania mechanizmu Franka-
-Starlinga. Obniżenie ESV świadczy o wzroście kurczliwości. Mechanizm
Franka-Starlinga wydaje się mieć większe znaczenie przy mniejszych inten-
sywnościach, natomiast wzrost kurczliwości jest bardziej zaznaczony przy
wyższych obciążeniach.
Większość badaczy jest zgodna, że SV wzrasta proporcjonalnie do obcią-
żenia, ale tylko do poziomu 40-60% VO
2max
. Natomiast co dzieje się z SV
powyżej tego poziomu wysiłku, nie jest w pełni jasne. Generalnie przyjmuje
się, że SV już dalej nie wzrasta, osiągając plateau pomimo dalszego wzrostu
intensywności wysiłku. Analiza badań zajmujących się SV w czasie wysiłku
wykazuje jednak pewne niezgodności, wynikające często z typu zastosowane-
go wysiłku i poziomu wydolności fizycznej badanych. Badania, które wykazu-
ją plateau przy 40-60% VO
2max
zazwyczaj wykorzystywały wysiłki na cyklo-
ergometrze i nie obejmowały osób o wysokiej wydolności. W badaniach
wyczynowych sportowców obserwowano bowiem wzrost SV nawet powyżej
poziomu 60% VO
2max
.
Efektem wzrostu objętości minutowej serca podczas wysiłku jest propor-
cjonalny do intensywności wzrost skurczowego ciśnienia tętniczego (SBP),
sięgający lub nawet przekraczający 200 mm Hg przy wysiłku maksymalnym.
Ciśnienie rozkurczowe (DBP), które jest odbiciem ciśnienia w tętnicach
w czasie, gdy serce „odpoczywa”, nie zmienia się w czasie wysiłku, wzrasta
w niewielkim stopniu lub maleje. Taka sytuacja jest skutkiem obniżonego
oporu obwodowego, w efekcie działania czynników lokalnych.
Wysiłki o tej samej intensywności wykonywane przy zaangażowaniu mięśni
górnej połowy ciała, w porównaniu do zaangażowania mięśni dolnej poło-
wy ciała, powodują większy wzrost ciśnienia tętniczego. Jest to związane
134

z mniejszą masą zaangażowanych mięśni i mniejszym unaczynieniem górnej
połowy ciała w porównaniu do dolnej. Te różnice skutkują większym całko-
witym oporem obwodowym. Różnice w ciśnieniu tętniczym pomiędzy wysił-
kami wykonywanymi przy zaangażowaniu mięśni górnej i dolnej części ciała
mają istotne znaczenie dla serca, bowiem pobieranie tlenu przez mięsień
sercowy i przepływ wieńcowy są bezpośrednio związane z iloczynem często-
ści skurczów serca i skurczowego ciśnienia tętniczego, określanego jako po-
dwójny produkt (double product, DP):
DP = HR x SBP
Podczas wysiłków o charakterze statycznym lub oporowym DP jest wyż-
szy, w porównaniu do wysiłków dynamicznych, wskazując na większe obcią-
żenie serca.
W rozważaniach o układzie krążenia w czasie wysiłku warto nadmienić kil-
ka słów o krwi, a w szczególności zawartości tlenu we krwi. W spoczynku za-
wartość tlenu we krwi tętniczej wynosi 20 ml O
2
na 100 ml krwi, a we krwi
żylnej 14 ml O
2
na 100 ml krwi. Różnica tętniczo-żylna wynosi zatem 6 ml.
Ta wartość informuje o poziomie wychwytu tlenu. W czasie wysiłku, wraz ze
wzrostem obciążenia a-VO
2
diff, stopniowo wzrasta – około trzykrotnie od
spoczynku do maksymalnego poziomu wysiłku. Wzrost jest efektem obniża-
nia się żylnej zawartości tlenu, która w pracujących mięśniach osiąga niemal
zero. Jednak po wymieszaniu krwi żylnej w prawym przedsionku wynosi 2-4 ml
tlenu na 100 ml. Tętnicza zawartość tlenu pozostaje w zasadzie niezmieniona.
Jak wspomniano powyżej, najczęściej obecnie stosowane w diagnostyce te-
sty wysiłkowe mają charakter progresywny (testy o stopniowo wzrastającej
intensywności). Cechą tych testów jest regularny wzrost obciążenia wysiłko-
wego. Czas trwania każdego poziomu intensywności jest stały – zazwyczaj 3-4
minuty, a uwarunkowane jest to osiągnięciem stabilizacji ocenianych wskaź-
ników, określanej jako stan równowagi czynnościowej (steady state). Cechą
większości omawianych powyżej wskaźników fizjologicznych jest dostosowy-
wanie poziomu do wymagań intensywności wysiłku i utrzymywanie stałego
poziomu przy stałej intensywności przez długi czas. Osiąganie stanu równo-
wagi czynnościowej jest charakterystyczne dla obciążeń submaksymalnych
i jest osobniczo powtarzalne. Ta cecha wskaźników fizjologicznych jest pod-
stawą diagnostyki wysiłkowej, programowania i kontrolowania aktywności
fizycznej.
135

FIZJOLOGICZNE EFEKTY TRENINGU FIZYCZNEGO
Celem regularnej aktywności fizycznej, treningu fizycznego jest zmniejsze-
nie kosztu fizjologicznego wysiłku. Kiedy uda się to osiągnąć, bodziec wysił-
kowy (np.: intensywność) konieczny do osiągnięcia zaplanowanego efektu
fizjologicznego (np.: wyznaczonego stanu równowagi czynnościowej) będzie
musiał mieć większą siłę. Pozytywne zmiany potreningowe dotyczą wielu
wskaźników fizjologicznych. Jednak te najważniejsze to: zwiększenie dostar-
czania tlenu do komórek mięśniowych, korzystne zmiany w układzie krąże-
nia i procesach pozyskiwania energii do wysiłku, a także zmiany zachodzące
w mięśniach.
Pułap tlenowy
Poziom VO
2max
jest determinowany genetycznie, jednak podlega zmianom
pod wpływem treningu fizycznego. Efektem dobrze zaplanowanej, regular-
nej aktywności fizycznej jest podwyższenie poziomu VO
2max
. Włączenie na-
wyku aktywności fizycznej u osób dotychczas prowadzących zdecydowanie
siedzący tryb życia, charakteryzujących się niską wydolnością, może podnieść
poziom pułapu tlenowego nawet o 20%.
Wzrost VO
2max
w efekcie treningu fizycznego jest wynikiem podwyższenia
zarówno różnicy tętniczo-żylnej, jak i maksymalnej objętości minutowej serca.
Zawartość tlenu we krwi tętniczej nie ulega zmianie pod wpływem trenin-
gu fizycznego. Podwyższenie a-vO
2
diff jest skutkiem zwiększonych zdolności
wychwytu tlenu i obniżenia zawartości tlenu we krwi żylnej. Czynnikiem li-
mitującym wzrost VO
2max
jest dostarczanie tlenu.
Adaptacja układu krążenia
Efektem treningu fizycznego jest wzrost maksymalnej objętości minuto-
wej serca. Ten efekt jest przede wszystkim wynikiem podwyższenia maksy-
malnej objętości wyrzutowej. Spoczynkowy poziom CO podczas wysiłków
submaksymalnych ulega nieznacznemu obniżeniu.
Wzrost maksymalnej objętości wyrzutowej jest efektem zwiększenia obję-
tości późnorozkurczowej, poprawy czynności rozkurczowej, jak i kurczliwo-
ści mięśnia sercowego. Poprawa kurczliwości mięśnia sercowego i czynności
rozkurczowej jest spowodowana przyrostem masy i modyfikacją właściwo-
ści elementów elastycznych mięśnia sercowego. Trening fizyczny może po-
wodować podwyższenie zarówno spoczynkowej, jak i wysiłkowej objętości
wyrzutowej nawet o 20%.
136

Istotne efekty treningu dotyczą częstości skurczów serca. Obniża się spo-
czynkowa częstość skurczów serca i HR podczas wysiłków submaksymal-
nych. Maksymalna częstość skurczów serca nie ulega zmianie, jednak popra-
wia się powysiłkowa restytucja HR (powrót do wartości wyjściowych).
Podstawowym mechanizmem odpowiedzialnym za potreningowe zmiany
HR jest korzystna modyfikacja równowagi w układzie autonomicznym.
Regularna aktywność fizyczna generalnie redukuje zarówno skurczowe,
jak i rozkurczowe spoczynkowe ciśnienie tętnicze. Trening nie ma natomiast
wpływu na wysiłkowe wartości ciśnienia tętniczego. Mimo braku redukcji
wysiłkowego SBP pod wpływem treningu fizycznego, podwójny produkt ule-
ga obniżeniu dzięki redukcji wysiłkowej częstości skurczów serca. Mamy
więc do czynienia ze zmniejszeniem obciążenia serca podczas wysiłków sub-
maksymalnych.
Próg mleczanowy
Trening fizyczny powoduje obniżenie stężenia mleczanu we krwi podczas
wysiłków submaksymalnych. Jednocześnie podwyższeniu ulega obciążenie
odpowiadające nagłemu wzrostowi stężenia mleczanu – poziom progu bez-
tlenowego (w funkcji obciążenia). Zmiany dotyczące LA są efektem zwięk-
szenia udziału procesów tlenowych w wysiłku, ale także nasilenia procesów
utylizacji mleczanu. Konsekwencją takiej sytuacji jest opóźnienie rozwoju
zmęczenia.
W tym miejscu warto zaznaczyć, że poziom progu beztlenowego to nie tyl-
ko ważny wskaźnik oceny wydolności fizycznej, ale także parametr optyma-
lizujący dobór obciążeń treningowych i umożliwiający kontrolę efektów tre-
ningu. W programowaniu aktywności fizycznej zaleca się intensywności
zbliżone do intensywności progowej, jako najbardziej efektywne z punktu
widzenia poprawy wydolności organizmu i działań prozdrowotnych.
Mięśnie szkieletowe
Zmiany zachodzące w mięśniach pod wpływem regularnej aktywności fi-
zycznej to: zwiększenie stężenia enzymów oksydacyjnych, mioglobiny i za-
pasu glikogenu oraz wzrost gęstości kapilarnej. Dalszymi efektami treningu
może być zmiana proporcji włókien mięśniowych (wzrost odsetka włókien
typu I – wolnokurczących). Sumarycznym efektem tych zmian jest wzrost
zdolności do wychwytu tlenu z krwi tętniczej.
137

STRUKTURA I SKŁADOWE TRENINGU FIZYCZNEGO
Podstawą treningu fizycznego jest regularne powtarzanie wysiłku. Jednak,
aby trening fizyczny był efektywny i bezpieczny, musi być spełnionych kilka
warunków. Należy pamiętać o prawidłowej strukturze pojedynczej sesji ak-
tywności fizycznej (jednostki treningowej) i zapewnieniu odpowiedniej ja-
kości i poziomu poszczególnych składowych treningu.
Struktura jednostki treningowej
Pojedyncza sesja aktywności fizycznej powinna składać się z trzech faz: fa-
zy rozgrzewki (warm-up), fazy treningu właściwego (training zone) i fazy
stopniowego zmniejszania obciążenia i wstępu do restytucji powysiłkowej
(cool-down). Celem rozgrzewki jest stopniowe przygotowanie organizmu do
docelowej intensywności wysiłku. Zestaw ćwiczeń stosowanych podczas roz-
grzewki obejmuje ćwiczenia dynamiczne od małych intensywności aż do in-
tensywności zbliżonej do docelowej oraz dynamiczne rozciąganie (streaching
dynamiczny). Ta faza powinna trwać przynajmniej 10 minut. Podczas fazy
treningu właściwego, przez cały czas trwania tej części treningu, wykonywa-
ne są ćwiczenia w zakresie obciążenia docelowego, optymalnego. O ile pod-
czas rozgrzewki aktywność wskaźników fizjologicznych wzrasta aż do osią-
gnięcia wyznaczonego stanu równowagi czynnościowej, o tyle celem fazy
treningu właściwego jest utrzymywanie odpowiedniego stanu równowagi
przez określony czas. Ta faza powinna trwać przynajmniej 20 minut. Faza
cool-down to stopniowe zmniejszanie obciążenia wysiłkowego i ćwiczenia
rozciągające (streaching izometryczny). Ta część treningu powinna trwać
około 10 minut.
Składowe treningu
Kiedy mówimy o programowaniu aktywności fizycznej, rozważamy cztery
elementy: formę aktywności, długość pojedynczej sesji, częstość sesji i opty-
malną intensywność.
Dobór formy, typu aktywności fizycznej jest sprawą bardzo istotną. Zapro-
ponowanie formy wymagającej technicznie (np.: jazdy na rolkach) lub w po-
czuciu osoby rozpoczynającej aktywność fizyczną – nudnej, może doprowa-
dzić do zaniechania regularnych wysiłków fizycznych. Zaproponowanie
osobie początkującej uczestnictwa w grach zespołowych, czy innych typach
aktywności związanej ze współzawodnictwem, niepotrzebnie zwiększa ryzy-
ko urazu czy incydentu sercowego. Przekraczana jest bowiem granica tole-
rancji wysiłku.
138

Proponowany typ aktywności fizycznej powinien brać pod uwagę stan wy-
dolności, zainteresowania, temperament i efekt docelowy. Osobom o małej
wydolności fizycznej, rozpoczynającym regularną aktywność fizyczną należy
polecać proste zajęcia wykonywane indywidualnie, bez presji na chwilowy
wynik. Wraz z poprawą stanu funkcjonalnego, można włączać formy bardziej
zaawansowane oraz zawierające elementy współzawodnictwa.
Optymalna długość pojedynczej sesji aktywności fizycznej jest determino-
wana efektywnym czasem potrzebnym do stymulującego zadziałania bodźca
i powinna wynosić przynajmniej 30 minut. Jednak badania epidemiologiczne
wykazują, że nawet krótsze sesje aktywności fizycznej (np.: 10 minut) wyko-
nywane wielokrotnie w ciągu dnia, przekraczające sumarycznie 30 minut
dziennie już przynoszą istotne korzyści zdrowotne. Dla osób o bardzo małej
wydolności fizycznej, rozpoczynanie aktywności od krótkich sesji wydaje się
jedynym rozwiązaniem. Wraz z rozwijaniem się korzystnych efektów trenin-
gu długość pojedynczej sesji treningowej może być zwiększana (teoretycz-
nie bez ograniczeń).
Wyniki badań w dużych populacjach potwierdzają, że najlepsze efekty re-
gularnej aktywności fizycznej osiągane są wtedy, kiedy wysiłek wykonywany
jest przynajmniej pięć dni w tygodniu, a najlepiej we wszystkie dni tygodnia.
Taka jest też docelowa częstość sesji aktywności fizycznej. Jednak podobnie
jak z czasem trwania pojedynczej jednostki treningowej, tak i tu korzystne
efekty obserwuje się już przy częstości trzy razy w tygodniu po 30 minut.
Problem doboru intensywności wysiłku w programowaniu aktywności fi-
zycznej jest rzeczą najbardziej skomplikowaną. Precyzyjne określenie opty-
malnego obciążenia wymaga zastosowania wysiłkowych testów diagnostycz-
nych, w których oceniany jest próg beztlenowy. Wyznaczenie obciążenia
progowego wyrażonego częstością skurczów serca (odpowiadających obcią-
żeniu progowemu) daje możliwość kontroli intensywności treningowej.
Metody wyznaczania intensywności treningowej, te skomplikowane i te
prostsze, zostaną omówione w dalszej części, w podrozdziale: „Ustalanie ob-
ciążeń treningowych”.
OCENA MEDYCZNA PRZED PODJĘCIEM AKTYWNOŚCI FIZYCZNEJ
Nie ulega wątpliwości, że nawet osoba z poczuciem zdrowia, rozpoczyna-
jąc program aktywności fizycznej powinna przejść podstawową ocenę me-
dyczną, ze szczególnym uwzględnieniem problemów związanych z układem
krążenia. Jeżeli badanie podmiotowe lub przedmiotowe będzie wskazywało
na istotną chorobę serca, przed rozpoczęciem treningu konieczna jest do-
139

kładna ocena kardiologiczna. Jeżeli badana osoba w badaniu podmiotowym
nie deklaruje choroby układu krążenia, ale jest obciążona czynnikami ryzy-
ka chorób serca, ma objawy lub zmiany sugerujące chorobę serca, przed roz-
poczęciem aktywności fizycznej powinna przejść test wysiłkowy i jeżeli bę-
dzie taka potrzeba – dalszą ocenę kardiologiczną. Test wysiłkowy powinien
być także wykonany u mężczyzn rozpoczynających aktywność fizyczną w wie-
ku 45 lat lub więcej i u kobiet rozpoczynających ją w wieku 55 lat lub wię-
cej. W przypadku obciążenia cukrzycą lub dwoma innymi czynnikami ryzyka
taka ocena powinna być przeprowadzona niezależnie od wieku.
Efektem badania lekarskiego powinna być ocena ryzyka związanego z wysił-
kiem i kwalifikacja badanej osoby do jednej z czterech klas (A, B, C, D), deter-
minujących zakres aktywności fizycznej, konieczność nadzoru i monitorowania
wskaźników fizjologicznych. Prezentowane tabele klasyfikacji ryzyka, związa-
nego z wysiłkiem oparte są na stanowisku American Heart Association (AHA)
i American College of Sports Medicine (ACSM) (tab. 2, 3, 4, 5).
Wnioski z badania kwalifikacyjnego
Osoby zakwalifikowane do klasy A nie wymagają nadzoru podczas aktyw-
ności fizycznej. Nie mają też ograniczeń, jeżeli chodzi o intensywność i for-
mę wysiłku. Sugeruje się jednak, aby osoby zakwalifikowane do podklas A-2
i A-3 przed podjęciem wysiłków fizycznych o dużej intensywności przeszły
diagnostyczny test wysiłkowy.
140
Tabela 2: Klasyfikacja ryzyka związanego z treningiem fizycznym; Klasa A: osoby w zasadzie zdrowe
KLASA A obejmuje:
• osoby (mężczyźni < 45 lat, kobiety < 55 lat), u których w badaniu
podmiotowym i przedmiotowym nie stwierdzono choroby serca i/lub
objawów choroby serca lub czynników ryzyka choroby niedokrwiennej
serca;
• osoby (mężczyźni
³ 45 lat, kobiety ³ 55 lat), u których w badaniu
podmiotowym i przedmiotowym nie stwierdzono choroby serca
i/lub objawów choroby serca, ale są obciążone co najwyżej jednym
czynnikiem ryzyka choroby niedokrwiennej serca;
• osoby (mężczyźni
³ 45 lat, kobiety ³ 55 lat), u których w badaniu
podmiotowym i przedmiotowym nie stwierdzono choroby serca
i/lub objawów choroby serca, ale są obciążone więcej niż jednym
czynnikiem ryzyka choroby niedokrwiennej serca.

Dla osób zakwalifikowanych do klasy B, aktywność fizyczna powinna być
zaprogramowana przez lekarza lub przez wykwalifikowaną osobę, po za-
aprobowaniu przez lekarza. Rozpoczynanie ćwiczeń powinno się odbywać
pod kontrolą medyczną. Zalecane jest, aby podczas pierwszych 6-12 sesji tre-
ningowych monitorować ciśnienie tętnicze i w miarę możliwość zapis EKG.
Po upewnieniu się, że trenująca osoba potrafi prawidłowo kontrolować po-
ziom aktywności, można dopuścić ją do ćwiczeń samodzielnych.
Dla osób zakwalifikowanych do klasy C (podobnie jak w grupie B) aktywność
fizyczna powinna być zaprogramowana przez lekarza lub przez wykwalifiko-
waną osobę po zaaprobowaniu przez lekarza. Wszystkie treningi powinny
odbywać się pod kontrolą medyczną. Podczas wszystkich sesji monitorowane
powinno być ciśnienie tętnicze i zapis EKG. Osoby zakwalifikowane do
141
Tabela 3: Klasyfikacja ryzyka związanego z treningiem fizycznym; Klasa B: osoby ze stabilną chorobą
układu krążenia, z niskim ryzykiem komplikacji podczas intensywnego wysiłku,
ale nieznacznie większym niż osoby w zasadzie zdrowe
KLASA B obejmuje osoby z jednym z poniższych rozpoznań:
• choroba niedokrwienna serca (włącznie z pacjentami po zawale mię-
śnia sercowego, pomostowaniu wieńcowym, angioplastyce i nieprawi-
dłowościami w badaniu angiograficznym);
• choroby zastawek serca, z wyłączeniem ciężkiej stenozy lub niedomy-
kalności zastawkowej;
• wrodzone choroby serca;
• kardiomiopatia: frakcja wyrzutowa
³ 30% (obejmuje stabilną niewy-
dolność serca, z wyłączeniem kardiomiopatii przerostowej lub prze-
bytego w niedalekiej przeszłości zapalenia mięśnia sercowego);
• niegroźne nieprawidłowości w badaniu wysiłkowym.
Jednak we wszystkich tych przypadkach badane osoby muszą spełniać
następujące kryteria kliniczne:
• klasa NYHA 1 lub 2;
• poziom wydolności
³ 6 METs;
• brak cech zastoinowej niewydolności serca;
• brak cech niedokrwienia mięśnia sercowego (przy wysiłku
³ 6 METs);
• prawidłowy przyrost SBP podczas wysiłku;
• brak tachykardii komorowej w spoczynku lub w czasie wysiłku;
• zdolność do samodzielnej kontroli intensywności wysiłku fizycznego.

142
Tabela 4: Klasyfikacja ryzyka związanego z treningiem fizycznym; Klasa C: osoby z średnim i wysokim
ryzykiem komplikacji kardiologicznych podczas wysiłku i/lub nie będący w stanie
samodzielnie kontrolować lub zrozumieć rekomendowanego poziomu aktywności fizycznej
KLASA C obejmuje osoby z jednym z poniższych rozpoznań:
• choroba niedokrwienna serca;
• choroby zastawek serca, z wyłączeniem ciężkiej stenozy lub
niedomykalności zastawkowej;
• wrodzone choroby serca;
• kardiomiopatia: frakcja wyrzutowa < 30% (obejmuje stabilną
niewydolność serca z wyłączeniem kardiomiopatii przerostowej lub
przebytego w niedalekiej przeszłości zapalenia mięśnia sercowego);
• źle kontrolowane, złożone komorowe zaburzenia rytmu;
Kiedy spełnione jest jedno z następujących kryteriów klinicznych:
• klasa NYHA 3 lub 4;
• wyniki testu wysiłkowego:
– poziom wydolności <6 METs,
– ból w klatce piersiowej lub niedokrwienne obniżenie odcinka ST
poniżej 6 METs,
– spadek SPB poniżej wartości spoczynkowych podczas wysiłku,
– tachykardia komorowa w czasie wysiłku;
• epizod pierwotnego zatrzymania krążenia (z wyłączeniem zatrzyma-
nia krążenia w czasie zawału lub podczas procedur diagnostycznych);
• inny istotny problem medyczny (według lekarza).
Tabela 5: Klasyfikacja ryzyka związanego z treningiem fizycznym; Klasa D: osoby z niestabilną chorobą
serca, z istotnym ograniczeniem aktywności fizycznej
KLASA D obejmuje osoby z jednym z poniższych rozpoznań:
• niestabilna choroba niedokrwienna serca;
• ciężkie stenozy lub niedomykalności zastawkowe;
• wrodzone choroby serca;
• niewyrównana niewydolność serca;
• źle kontrolowane lub niekontrolowane zaburzenia rytmu serca;
• inne problemy medyczne, które wysiłek może nasilać.

grupy C mogą po pewnym okresie treningu zostać przeklasyfikowane do
grupy B, pod warunkiem, że są w stanie w sposób nie budzący wątpliwości
kontrolować poziom intensywności treningowych.
Osobom zakwalifikowanym do klasy D nie zaleca się aktywności fizycznej,
której celem jest poprawa kondycji fizycznej.
USTALANIE OBCIĄŻEŃ TRENINGOWYCH
Przy programowaniu treningu dobór odpowiednich obciążeń jest rzeczą
najważniejszą, ale i najbardziej skomplikowaną. Wbrew ogólnemu przeko-
naniu stosowanie obciążeń maksymalnych w treningu nie jest najefektyw-
niejszą formą poprawy wydolności. Badania pokazują, że efekty treningowe
są zauważalne już przy obciążeniu na poziomie 45% VO
2max
. Jednak najlep-
sze rezultaty osiąga się ustawiając obciążenia treningowe na poziomie od-
powiadającym progowi beztlenowemu, który zazwyczaj występuje w zakresie
60-80% VO
2max
. Wyznaczenie obciążenia progowego jest najdokładniejszą
metodą ustalenia optymalnej intensywności treningowej.
Preferowaną metodą monitorowania intensywności wysiłku jest ocena czę-
stości skurczów serca. Wysiłkowa HR jest silnie skorelowana z pobieraniem
tlenu i obciążeniem. Kiedy przepisuje się intensywność treningową, ustala
się właściwy zakres częstości skurczów serca, wyznaczając dolną i górną gra-
nicę, na przykład: 140-165/min.
Wyznaczenie obciążenia treningowego (próg mleczanowy)
Treningowe obciążenia wysiłkowe, zbliżone do progu beztlenowego są
optymalne do poprawy wydolności organizmu. Podstawą określenia zakresu
intensywności dla fazy treningu właściwego jest zatem wyznaczenie progu
beztlenowego. Ponieważ poziom progu mleczanowego (LAT) w normalnych
warunkach odpowiada progowi mleczanowemu (często nazwy te używa się
zamiennie), wyznaczenie progu beztlenowego opiera się na analizie zmian
stężenia mleczanu w czasie progresywnego testu wysiłkowego. Jak wspo-
mniano powyżej przebieg zmian stężenia mleczanu w relacji do obciążenia,
w czasie wysiłku o stopniowo wzrastającej intensywności, ma charakter wy-
kładniczy. Taki przebieg można w uproszczeniu opisać dwoma prostymi. Ob-
ciążenie odpowiadające punktowi przecięcia tych prostych jest obciążeniem
progowym (ryc. 1).
143
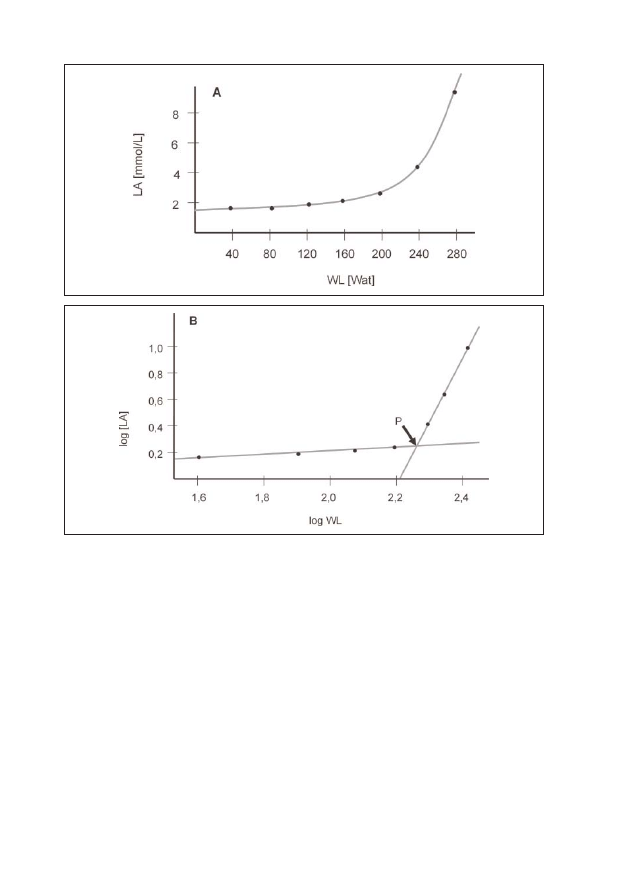
Częstość skurczów serca odpowiadającą progowi beztlenowemu wyznacza
się z liniowej relacji: [obciążenie wysiłkowe] – [HR]. Treningowy poziom czę-
stości skurczów serca (THR) mieści się w zakresie ± 5% progowej HR.
Metoda ustalania obciążeń treningowych oparta na wyznaczaniu progu
mleczanowego, z powodu obciążenia badanych osób (wielokrotne pobiera-
144
Rycina 1: Schemat wyznaczania obciążenia treningowego na postawie progu beztlenowego
(A) Przebieg zmian stężenia mleczanu we krwi (LA) w czasie wysiłku o stopniowo wzrastającej
intensywności (work load, WL) ma charakter wykładniczy. Przy lekkich i średnich obciążeniach wzrost
stężenia LA jest nieznaczny. Przy pewnym kolejnym obciążeniu następuje istotna akceleracja przyrostu
stężenia LA.
(B) Logarytmiczna metoda wyznaczania progu beztlenowego (Beavera i Wassermana).
Po zlogarytmowaniu wartości obciążenia (log WL) i stężenia mleczanu (log [LA]) ujawniają się dwa
segmenty, które można opisać za pomocą regresji liniowej. Punkt przecięcia prostych (P) naniesiony na
oś zlogarytmowanego obciążenia, po zdelogarytmowaniu określa wartość obciążenia progowego
w watach. W tym wypadku punkt przecięcia wypada przy wartości 2,26 – po zdelogarytmowaniu 180 W.

nie krwi kapilarnej) i znacznych kosztów ma ograniczone zastosowanie w re-
kreacyjnej i zdrowotnej aktywności fizycznej. Są jednak metody prostsze
i mniej inwazyjne, które w sposób wystarczająco dokładny pozwalają pro-
gramować intensywności wysiłkowe.
Wyznaczenie obciążenia treningowego na podstawie wyniku testu wysiłkowego
Podstawowych informacji pomocnych przy wyznaczeniu intensywności tre-
ningowej może dostarczyć diagnostyczny test wysiłkowy wykonywany na
bieżni ruchomej. W zasadzie wszystkie zestawy do testów wysiłkowych, jako
dodatkowy parametr prezentują przybliżony wydatek energetyczny wysiłku,
wyrażony w METs. Maksymalne obciążenie osiągnięte w teście wysiłkowym
określa się jako wydolność funkcjonalną (functional capacity, FC). Można ją
przedstawić w jednostkach METs. Ustalenie docelowej intensywności sesji
treningowej opiera się na założeniu, że minimalne efektywne obciążenie tre-
ningowe wynosi 60% FC, a optymalne jest sumą FC, wyrażoną w METs
i owych bazowych 60%. Tak więc dla osoby, która w czasie testu wysiłkowe-
go osiągnęła 6,0 METs optymalne obciążenie treningowe wynosi 60 + 6 =
66% FC, to jest 4,0 METs. Dla osoby, która w czasie testu wysiłkowego osią-
gnęła 12,0 METs optymalne obciążenie wynosi 60 + 12 = 72% FC, to jest
8,6 METs.
Podobnie jak dla opisanego powyżej progu mleczanowego częstość skur-
czów serca, odpowiadającą optymalnemu obciążeniu można wyznaczyć
z wzoru prostej, przedstawiającej relację pomiędzy obciążeniem (METs),
a częstością skurczów serca. Treningowy zakres częstości skurczów serca wy-
nosi ± 5% wyznaczonej HR (tab. 6).
Metoda Karvonena
Pomimo że podczas wysiłku HR rośnie proporcjonalnie do VO
2
, odnie-
sienie wprost zakresu 60-80% VO
2max
do HR
max
jest obciążone dużym błę-
dem, ponieważ 60 czy 80% VO
2max
nie jest równoważne z odpowiednio 60
czy 80% HR
max
. W wartościach względnych, określonemu poziomowi
VO
2max
odpowiada wyższy poziom HR
max
(na przykład: intensywności 75%
VO
2max
odpowiada 86% HR
max
), a różnica ta jest indywidualna.
Sposobem na zrównoważenie względnych wartości VO
2max
i HR
max
jest
uwzględnienie spoczynkowych wartości częstości skurczów serca. Ten spo-
sób wykorzystuje metoda Karvonena, która wprowadza pojęcie rezerwy
maksymalnej częstości skurczów serca. Rezerwa HR
max
jest różnicą pomię-
dzy maksymalną i spoczynkową częstością skurczów serca.
145
146
Tabela 6: Przykłady wyznaczania obciążenia treningowego na podstawie diagnostycznego
testu wysiłkowego
Badany: mężczyzna lat 30,
zdrowy, bez czynników ryzyka
choroby niedokrwiennej serca
Klasa ryzyka A-1
Badany: mężczyzna lat 45,
otyłość, pali papierosy (30/d),
bez nieprawidłowości w badaniu
przedmiotowym
Klasa ryzyka A-3
METs HR [/min]
METs HR [/min]
1
75
1
85
2,5
88
2.9
95
3,3
100
(B/HR
B
)
®
4,5
110
5,8
130
(C/HR
C
)
®
6,0
135
7,2
155
® (B/HR
B
)
7,4
155
8,7
175
® (C/HR
C
)
10,5
190
wyznaczenie optymalnego obciążenia treningowego
Powód przerwania testu:
– zmęczenie
Wydolność funkcjonalna:
10,5 METs, przy HR = 190/min
Obciążenie optymalne:
7,4 METs
(bo: 60 + 10,5 = 70,5% z 10,5)
Powód przerwania testu:
– wzrost ciśnienia
do 250/110 mm Hg
Wydolność funkcjonalna:
7,4 METs, przy HR = 155/min
Obciążenie optymalne:
5,0 METs
(bo: 60 + 7,4 = 67,4% z 7,4)
Wyznaczenie HR odpowiadającej
obciążeniu optymalnemu,
zgodnie ze wzorem:
HR = [ (A – B/ C – B) · (HR
C
–
HR) ] + HR
B
gdzie:
HR
A
– poszukiwane HR
A – obciążenie optymalne
(METs)
B – obciążenie poprzedzające
A (METs)
C – obciążenie następujące po
A (METs)
HR
B
– HR odpowiadające B
(METs)
HR
C
– HR odpowiadające C
HR
A
= [ (7,4 – 7,2/8,7 – 7,2) · (175
– 155) ] + 155
HR
A
= 158
Treningowy zakres HR (± 5%)
150-164 /min
HR
A
= [ (5,0 – 4,5/6,0 – 4,5) · (135
– 110) ] + 110
HR
A
= 118
Treningowy zakres HR (± 5%)
112-124 /min

Rezerwa HR
max
= HR
max
– HR
sp
W tej metodzie, treningowa częstość skurczów serca jest wyliczana jako
suma odsetka rezerwy HR
max
i spoczynkowej częstości skurczów serca. Na
przykład dla 75% VO
2max
:
THR = HR
sp
+ 0,75 (HR
max
– HR
sp
)
Oczywiście do monitorowania intensywności wysiłku przepisuje się zakres
częstości skurczów serca. Generalnie optymalny zakres to 60-80% VO
2max
.
Aby jednak bardziej precyzyjnie ustalić dolną i górną granicę HR, trzeba wy-
korzystać dane z badania podmiotowego, dotyczące dotychczasowej aktyw-
ności fizycznej, subiektywnej oceny wydolności pacjenta, czy proste informa-
cje związane z codziennym funkcjonowaniem, na przykład z pokonywaniem
schodów. Osoby początkujące, o niskiej wydolności fizycznej, powinny za-
czynać raczej od zakresu 60-70% VO
2max
. Osoby charakteryzujące się wyż-
szym poziomem wydolności fizycznej 70-80% VO
2max
(tab. 7).
Metoda Karvonena jest prostym sposobem określania treningowego za-
kresu HR, wymagającym tylko informacji o spoczynkowej i maksymalnej
147
Tabela 7: Przykład wyznaczania treningowych zakresów HR według metody Karvonena
Badany:
mężczyzna lat 32, zdrowy,
bez czynników ryzyka choroby
niedokrwiennej serca.
Sezonowo aktywny fizycznie:
narty, pływanie.
Klasa ryzyka A-1
Badany:
mężczyzna lat 48, nadwaga,
bez nieprawidłowości w badaniu
przedmiotowym, podwyższony
poziom cholesterolu (240 mg/dL).
Minimalna aktywność fizyczna.
Klasa ryzyka A-3
Rekomendowany zakres
obciążeń: 70-80% VO
2max
Rekomendowany zakres
obciążeń: 60-70% VO
2max
HR
sp
= 70
HR
max
= 188 (= 220 – 32)
THR
70
= 153
[70 + 0,70 (188 – 70)]
THR
80
= 164
[70 + 0,80 (188 – 70)]
Treningowy zakres HR: 153-164
HR
sp
= 85
HR
max
= 172 (= 220 – 48)
THR
60
= 137
[85 + 0,60 (172 – 85)]
THR
70
= 146
[85 + 0,70 (172 – 85)]
Treningowy zakres HR: 137-146
HR. Ocena spoczynkowej wartości HR jest elementem badania przedmioto-
wego. Dla dokładniejszej oceny można poprosić badanego o pomiar tętna
rano po przebudzeniu. Maksymalna częstość skurczów serca zależy od wie-
ku i do jej wyliczenia można stosować wzór podany powyżej.
Skala Borga
Odczucie ciężkości wysiłku odpowiada zazwyczaj wielkości obciążenia
względnego (%VO
2max
). Do odczucia ciężkości wysiłku stosuje się po-
wszechnie uznaną skalę Borga. Konstrukcja tej skali zakłada, że u ludzi mło-
dych, przemnożenie wartości liczbowej przez 10 odpowiada wysiłkowej czę-
stości skurczów serca.
Wykorzystanie skali Borga jest proponowane jako najprostsza forma prze-
pisywania obciążeń treningowych. Kiedy właściwie wykorzystuje się tę skalę,
obciążenia treningowe powinny mieścić się w zakresie od 12-13 (dosyć cięż-
ko) do 15-16 (ciężko) (tab. 8).
148
Tabela 8: Metoda wyznaczania intensywności na podstawie skali Borga
%VO
2max
/
%rezerwy HR
max
(wartości przybliżone)
Punkty
Ocena
ciężkości
wysiłku
6
7
wyjątkowo lekki
30
8
9
bardzo lekki
35
10
11
dosyć lekki
---60---
---12---
--------
13
dosyć ciężki
70
14
15
ciężki
-----------------80-----------------
---16---
-------
85
17
bardzo ciężki
18
19
niezwykle ciężki
20

TRENING OPOROWY
Zgodnie z zaleceniami AHA i ACSM trening oporowy (trening siłowy)
powinien być stałym elementem nowoczesnego programu aktywności fizycz-
nej, zarówno w układzie profilaktyki zdrowotnej, jak i u osób z chorobami
układu krążenia, oczywiście po ocenie ryzyka w badaniu lekarskim. Trening
siłowy ma wpływ na sprawność układu krążenia, korzystnie modyfikuje tak-
że czynniki ryzyka choroby niedokrwiennej serca. Efektem systematycznie
wykonywanych ćwiczeń oporowych jest obniżenie HR podczas wysiłków sub-
maksymalnych. Nie zmienia się natomiast spoczynkowa częstość skurczów
serca. Pod wpływem treningu siłowego zwiększa się masa mięśnia sercowego
– wzrasta grubość ścian serca. W konsekwencji rośnie kurczliwość mięśnia
sercowego i podwyższeniu ulega objętość wyrzutowa. Trening oporowy pro-
wadzi do obniżenia spoczynkowych wartości ciśnienia tętniczego u ludzi
z nadciśnieniem. Korzystne zmiany dotyczą także profilu lipidowego. Zwią-
zane są one przede wszystkim z obniżeniem stosunku poziomu cholesterolu
całkowitego do poziomu frakcji HDL oraz stosunku poziomu frakcji LDL
do HDL. Trening siłowy poprawia też tolerancję glukozy.
Ważna jest także efektywność treningu siłowego w leczeniu otyłości. Ćwi-
czenia oporowe powodują zmniejszenie ilości tkanki tłuszczowej i podwyż-
szenie beztłuszczowej masy ciała (fat free mass, FFM). Niektórzy badacze
sugerują, że wynikiem podwyższenia FFM jest wzrost spoczynkowego po-
ziomu metabolizmu, ponieważ mięśnie mają wyższy współczynnik aktywno-
ści niż tłuszcz.
Wzrost masy mięśniowej i siły w efekcie treningu oporowego poprawia in-
dywidualną zdolność do codziennego funkcjonowania, szczególnie ludzi star-
szych.
Maksymalny ciężar, jaki można podnieść jeden raz jest podstawową jed-
nostką obciążenia w programowaniu treningu siłowego i opisuje się ją jako
1-RM (one-repetition maximum). Ocenę 1-RM można wykonać podczas te-
stów siłowych wykonywanych pod nadzorem. Osoby początkujące powinny
rozpoczynać od 40-60% ciężaru opisywanego jako 1-RM i powinny być
w stanie podnieść taki ciężar 8-15 razy (powtórzenia). Jedno ćwiczenie obej-
muje wybraną grupę mięśniową. Ćwiczenia łączy się w zestawy, po 8-10
w jednym zestawie. Standardy AHA i ACSM zalecają wykonywanie 1 zesta-
wu, 8-10 ćwiczeń po 8-15 powtórzeń, 2-3 razy w tygodniu.
149

Zapamiętaj:
1. Brak odpowiedniego poziomu aktywności fizycznej jest czynnikiem ryzyka
choroby niedokrwiennej serca, chorób metabolicznych i nowotworowych,
dlatego lekarze powinni promować ideę regularnej aktywność fizycznej
wśród swoich pacjentów, ale także w swoim środowisku.
2. Idea regularnej aktywności fizycznej wymaga przełożenia praktycznego
w postaci programu treningowego. Program treningowy powinien uwzględ-
niać stan zdrowia i możliwości osoby podejmującej aktywność fizyczną.
3. Podstawą programu treningowego są odpowiednio dobrane: forma aktyw-
ności, częstość sesji treningowych, długość pojedynczej sesji aktywności fi-
zycznej i obciążenie wysiłkowe.
4. Badania potwierdzają, że najlepsze efekty zdrowotne daje powtarzanie sesji
aktywności fizycznej przez większość, jeżeli nie wszystkie dni tygodnia. Już
jednak trzy dni aktywności fizycznej w tygodniu korzystnie modyfikują czyn-
niki ryzyka choroby niedokrwiennej serca.
5. Zalecany czas trwania pojedynczej sesji treningowej wynosi 30 minut. Jed-
nak nawet kilka krótszych sesji sumujących się w 30 minut dziennie może
być efektywne z punktu widzenia zdrowotnego.
6. Optymalna intensywność treningu zdrowotnego mieści się w zakresie 60-
80% maksymalnych możliwości organizmu (VO
2max
). Badania epidemio-
logiczne wykazują jednak, że już intensywność wysiłku na poziomie 45%
VO
2max
daje wyraźne efekty zdrowotne.
Warto przeczytać:
G. F. Fletcher i wsp.: Exercise standards for testing and training. A statement
for healthcare professionals from the American Heart Association; Circula-
tion 2001; 104: 1964-1740.
M. L. Pollock i wsp.: Resistance exercise in individuals with and without car-
diovascular disease. Benefits, rationale, safety, and prescription. An advisory
from the Committee on Exercise, Rehabilitation, and Prevention on Clinical
Cardiology, American Heart Association; Circulation 2000; 101: 828-833.
J. H. Wilmore, D. L. Costill.: Physiology of sports and exercise; Human Ki-
netics 2001.
G. J. Balady i wsp.: Recommendations for cardiovascular screening, staffing, and
emergency policies at health/fitness facilities; Circulation 1998; 97: 2283-2293.
150
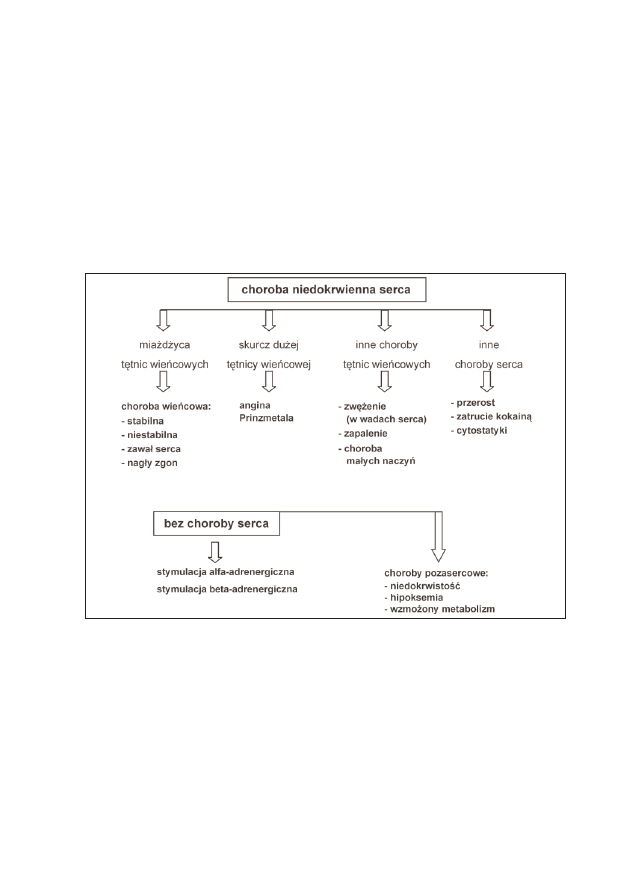
IX.
ZASADY DIAGNOSTYKI NIEINWAZYJNEJ
W CHOROBIE NIEDOKRWIENNEJ SERCA
– STANDARD POSTĘPOWANIA
Wojciech Braksator, Artur Mamcarz, Joanna Syska-Sumińska, Jarosław Król
Przyczyną niedokrwienia mięśnia sercowego jest niedostateczny dowóz tle-
nu w stosunku do zapotrzebowania. Nie każda taka dysproporcja jest wyra-
zem choroby niedokrwiennej serca. W tabeli pierwszej przedstawiono przy-
czyny niedokrwienia mięśnia sercowego. Niedokrwienie może wystąpić także
bez choroby serca (ryc. 1).
Celem współczesnej diagnostyki choroby niedokrwiennej serca (ChNS)
jest rozpoznanie przyczyn niedokrwienia mięśnia sercowego i ustalenie spo-
sobu leczenia. Cykl zdarzeń zamyka badanie naczyniowe – koronarografia,
która umożliwia wybór optymalnego sposobu terapii.
Podstawą rozpoznania ChNS jest badanie podmiotowe. Nic nie zastąpi do-
brze zebranego wywiadu, uzupełnionego badaniem przedmiotowym. W wy-
wiadzie decydującą rolę odgrywa charakter dolegliwości, obecność i nasile-
nie czynników ryzyka. Badanie przedmiotowe może pozwolić na uzupeł-
151
Rycina 1: Przyczyny niedokrwienia mięśnia sercowego
nienie zebranych danych oraz na wykrycie innych nieprawidłowości, np.
szmerów w sercu. Ważnym elementem diagnostyki są badania laboratoryj-
ne określające poziom niektórych czynników ryzyka, w tym pełen lipidogram
i poziom glikemii na czczo, a w przypadku wątpliwości krzywa obciążenia
glukozą.
Kolejnym krokiem są badania, testy nieinwazyjne, które pozwalają na
wyjaśnienie wątpliwości diagnostycznych, ocenę stopnia zaawansowania
choroby i możliwych powikłań. Standardy badań nieinwazyjnych są publi-
kowane od wielu lat. Sposób postępowania najpełniej omówiony jest w za-
leceniach Amerykańskich Towarzystw Kardiologicznych (American Heart
Association – AHA i American College of Cardiology – ACC). W Polsce po-
sługujemy się standardami Polskiego Towarzystwa Kardiologicznego
(PTK).
Idealny test diagnostyczny powinien być dodatni u wszystkich chorych,
a ujemny u wszystkich zdrowych. Nie ma takiego testu, zawsze pojawiają się
ograniczenia. Prawdopodobieństwo wystąpienia choroby oceniamy wykorzy-
stując teorię Bayesa. Teoria ta mówi, że wartość diagnostyczna danego te-
stu zależy od prawdopodobieństwa wystąpienia choroby w danej populacji.
Dlatego tak ważny jest dobrze zebrany wywiad i określenie prawdopodo-
bieństwa ChNS przed wykonaniem badania diagnostycznego. Takie praw-
dopodobieństwo wystąpienia choroby wieńcowej w zależności od płci, wieku
i objawów przedstawiono w tabeli 1 (wg zaleceń AHA w ślad za klasycznym
opracowaniem Diamonda i Forrestera z 1979 roku).
152
Tabela 1: Prawdopodobieństwo choroby wieńcowej w zależności od wieku, płci i objawów
Wiek
Płeć
Typowa
dławica
piersiowa
Nietypowa
dławica
piersiowa
Bóle
niedławicowe
Bez bólów
30-39
M
umiarkowane
umiarkowane
małe
bardzo małe
K
umiarkowane
bardzo małe
bardzo małe
bardzo małe
40-49
M
duże
umiarkowane
umiarkowane
małe
K
umiarkowane
małe
bardzo małe
bardzo małe
50-59
M
duże
umiarkowane
umiarkowane
małe
K
umiarkowane
umiarkowane
małe
bardzo małe
60-69
M
duże
umiarkowane
umiarkowane
małe
K
duże
umiarkowane
umiarkowane
małe
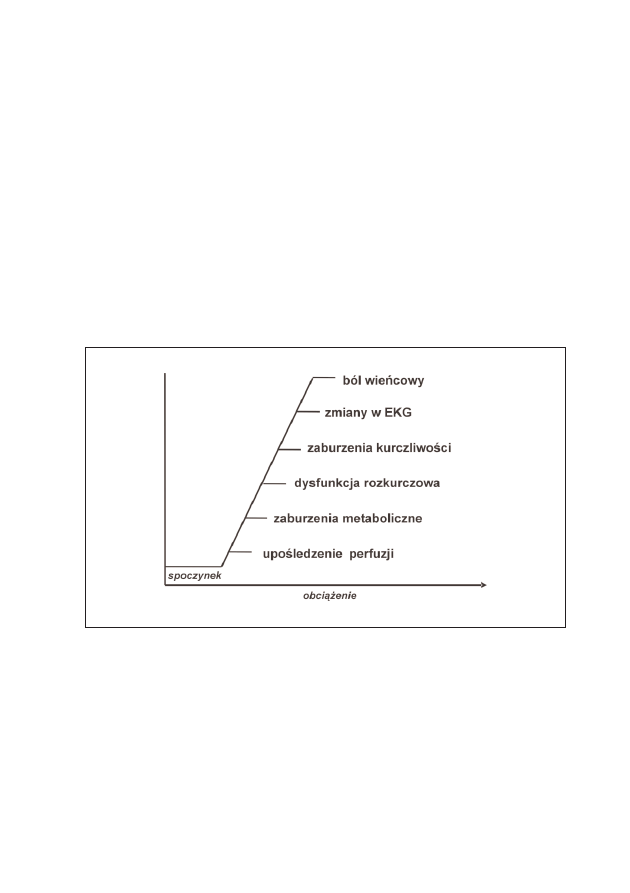
Diagnostyka nieinwazyjna największe korzyści przynosi w grupie pacjen-
tów z umiarkowanym ryzykiem ChNS (30 do 75%). Właśnie w tej grupie
chorych istnieje największa potrzeba wykonywania badań diagnostycznych
u pacjentów. W grupie pacjentów z ryzykiem do 30% prawdopodobieństwo
jest niskie, w grupie powyżej 75% wysokie i w większości przypadków nie
ma potrzeby wykonywania badań w celu postawienia rozpoznania. Rozpo-
znanie choroby lub jej wykluczenie może być ustalone bez dodatkowych pro-
cedur.
W przypadku podjęcia decyzji o wykonaniu dodatkowych testów diagno-
stycznych opieramy się na przesłankach patofizjologicznych. Zjawiska za-
chodzące w mięśniu sercowym w czasie niedokrwienia można wykryć za po-
mocą określonych procedur. Krzywa to obrazująca nazywana jest kaskadą
niedokrwienia (ryc. 2). Opisuje ona kolejność pojawiania się zmian niedo-
krwiennych.
Poszczególnym zaburzeniom odpowiadają określone procedury diagno-
styczne. Na szczycie niedokrwienia pojawia się ból, wcześniej występują
zmiany w EKG spoczynkowym, poprzedzają je zaś zaburzenia kurczliwości
wykrywane w echokardiografii obciążeniowej (stress-echo). Jeszcze wcześniej
pojawia się niedokrwienna dysfunkcja lewej komory oceniana w echokar-
diografii dopplerowskiej, zaś pierwszym zjawiskiem w kaskadzie niedokrwie-
nia jest upośledzenie przepływu w mikrokrążeniu wykrywane za pomocą
scyntygrafii perfuzyjnej.
153
Rycina 2: Kaskada niedokrwienia – kolejność pojawiania się zmian niedokrwiennych wraz ze wzrasta-
jącym obciążeniem

Standard badań nieinwazyjnych obejmuje:
Badania 1 i 2 uznane są za podstawowe, badania 3 i 4 to metody uzupeł-
niające, a 5 i 6 to procedury specjalistyczne.
Wartość spoczynkowego badania EKG w rozpoznawaniu ChNS jest niska
i nie przekracza 30%. Typowe zmiany w EKG to poziome obniżenie odcinka
ST przekraczające 1 mm, odwrócenie załamka T, uniesienie ST-T w ostrym
niedokrwieniu z możliwością świeżego zawału serca. Badanie to dokumentu-
je zmiany niedokrwienne w czasie trwania bólu lub wykrywa je w sposób
przypadkowy w badaniach przesiewowych (nieme niedokrwienie). U więk-
szości chorych z ChNS spoczynkowe badanie EKG nie wykrywa zmian nie-
dokrwiennych, bardzo często jest prawidłowe. Warto pamiętać, że zmiany
odcinka ST w EKG nie upoważniają do rozpoznania ChNS bez odpowied-
nich danych klinicznych z badania podmiotowego i przedmiotowego. Zmia-
ny ST w EKG występują bowiem w różnych sytuacjach klinicznych, np.
w blokach odnóg pęczka Hisa, zespołach preekscytacji, zaburzeniach jono-
wych, pod wpływem niektórych leków (naparstnica), a także w zespole wypa-
dania płatka zastawki mitralnej. Mogą być one także związane z pozycją cia-
ła lub płcią (wpływ żeńskich hormonów płciowych).
Wykonanie EKG u chorych z bólami w klatce piersiowej jest oczywiście
niezbędne. Można wykryć niedokrwienie, stwierdzić zaburzenia rytmu
i przewodzenia, cechy przerostu lub przeciążenia lewej komory, a także inne
nieprawidłowości. Prawidłowy zapis EKG nie może jednak uspokoić, nie wy-
klucza nawet ostrych i zaawansowanych postaci ChNS.
Podstawową metodą diagnostyczną w ChNS jest test wysiłkowy. Test wy-
siłkowy jest metodą o 70-letniej tradycji, sprawdzoną, szeroko dostępną,
tanią i bezpieczną. Jest badaniem wykorzystującym nowoczesne oprogra-
mowanie komputerowe. Metoda ta, choć podstawowa, ma wady. Główną
jest względnie niska wartość diagnostyczna, opisywana głównie przez czu-
łość, która osiąga średnio jedynie 68% i swoistość, szacowaną na 77 %.
154
1. EKG spoczynkowe;
2. test wysiłkowy EKG;
3. echokardiografię spoczynkową (ECHO serca)
4. 24-godzinne monitorowanie EKG metodą Holtera (badanie
holterowskie);
5. scyntygrafię perfuzyjną;
6. stress-echo.

Niektóre opracowania podają jeszcze niższe wartości. Mimo tych nie
w pełni zadowalających parametrów, ocena pacjenta z ChNS jest oparta
przede wszystkim na tym badaniu. Są dwa podstawowe cele badania wysił-
kowego:
Inne ważne wskazania do testu wysiłkowego EKG to:
Względne wskazania do wykonania testu wysiłkowego to:
Interpretacja testu wysiłkowego EKG opiera się na przesłankach klinicz-
nych i elektrokardiograficznych. Jednak podstawą oceny jest jakość wyko-
nania tego badania. Powinien on być wykonany według określonych reguł
(odpowiedni protokół obciążenia) zgodnie z kryteriami wieku, płci i prze-
bytej choroby serca (zawał). Główną wadą lub ograniczeniem wykonywa-
nych testów jest niemożność uzyskania wystarczającego obciążenia (przynaj-
mniej submaksymalny wysiłek fizyczny) z powodów obiektywnych lub
subiektywnych (obawa przed obciążeniem i powikłaniami). Dlatego bada-
nia powinny być wykonywane w pracowniach rekomendowanych. Najlepsze
155
• diagnostyka ChNS u dorosłych obu płci, w sytuacji, gdy
prawdopodobieństwo choroby jest umiarkowane (tab. 1);
• ocena rokowania, skuteczności leczenia i kwalifikacja do badań
inwazyjnych pacjentów, u których postawiono rozpoznanie kliniczne
ChNS.
• komorowe zaburzenia rytmu serca przy podejrzeniu o ich tło
niedokrwienne;
• stan po zawale serca w celu oceny ryzyka nowych incydentów
wieńcowych;
• ocena skuteczności zabiegów rewaskularyzacyjnych (CABG, PCI,
PTCA, stenty);
• każda istotna, negatywna zmiana stanu klinicznego pacjenta.
• chorzy z zasłabnięciami;
• osoby wykonujące szczególne zawody (piloci, kierowcy zawodowi,
operatorzy dźwigów);
• osoby planujące rekreacyjne uprawianie sportu, prowadzące
dotychczas spoczynkowy tryb życia.

wyniki testów otrzymujemy z pracowni przyklinicznych i przyszpitalnych, bo-
wiem zespół wykonujący nie jest ograniczony niepokojem możliwych, choć
rzadkich powikłań (ryzyko NZK to 1: 10 000 wykonanych badań). Klasyczna,
dodatnia interpretacja na podstawie wskaźników klinicznych to: ból wieńco-
wy, symptomatyczny spadek ciśnienia tętniczego o 20 mm Hg w stosunku do
wartości wyjściowych, a także kontrowersyjny parametr jak mała tolerancja
wysiłku i nieadekwatność chronotropowa, tzn. nieosiąganie – wraz ze wzro-
stem obciążenia – limitu tętna. Dodatni wynik pokazany w zapisie EKG to:
obniżenie ST o co najmniej 0,1 mV (1 mm), uniesienie ST w obszarze bez
patologicznego załamka Q, odwrócenie załamka T (z dodatniego na ujem-
ny) oraz groźna arytmia komorowa (od klasy III wg Lowna).
Przeciwwskazaniami do wykonania testu wysiłkowego są: pierwsze doby
ostrego zawału serca (w Polsce badanie to zwyczajowo wykonujemy od 7 doby
zawału, choć zalecenia amerykańskie mówią o możliwości wykonania testu
od 3 doby), niestabilna dusznica bolesna (do ustąpienia objawów), ciężka,
nie poddająca się leczeniu arytmia komorowa, niewyrównana, zaawansowa-
na niewydolność serca.
Wysoki odsetek fałszywie ujemnych wyników testu wysiłkowego EKG ob-
niża czułość tej próby w badanej populacji. Przyczynami tego są:
Z kolei swoistość badania obniża wysoki odsetek wyników fałszywie do-
datnich. Odpowiedzialne za to są zmiany ST-T m.in. w zespołach preekscyta-
cji, wypadaniu płatka zastawki mitralnej, zaburzeniach jonowych, zaburze-
niach ukrwienia mięśnia sercowego bez istotnych zmian w naczyniach
wieńcowych (kardiologiczny zespół X). Zmiany okresu repolaryzacji mogą
być spowodowane także przez niektóre leki, np. glikozydy naparstnicy.
Zmiany odcinka ST-T mogą także być zależne od hormonów płciowych u ko-
biet (progestageny); mimo typowych objawów klinicznych ChNS, odsetek
wyników fałszywie dodatnich w niektórych opracowaniach sięga nawet 50%.
Dotyczy to zwłaszcza odprowadzeń znad ściany dolnej i w znaczący sposób
obniża wartość diagnostyczną tego badania dla całej populacji badanej.
156
• zbyt mały wysiłek – zbyt duża ostrożność w jego wykonaniu (brak
pełnego zaplecza reanimacyjnego);
• za mało monitorowanych odprowadzeń EKG;
• zmiany w obrębie jednej tętnicy wieńcowej – trudne do wykrycia
każdą nieinwazyjną metodą badawczą;
• wpływ stosowanego leczenia, np.: beta-adrenolityki i niektóre leki
psychotropowe.
Innym badaniem elektrokardiograficznym stosowanym w diagnostyce
ChNS jest 24-godzinne monitorowanie EKG metodą Holtera (badanie hol-
terowskie). Badanie to należy do procedur uzupełniających i jest mniej war-
tościowe niż test wysiłkowy EKG w rozpoznawaniu ChNS. Wykonując to ba-
danie możemy ocenić przede wszystkim zaburzenia rytmu w przebiegu
choroby wieńcowej i jest to główny praktyczny cel jego wykonania. Badanie
holterowskie wykrywa jednak niedokrwienie w przypadku dławicy naczynio-
skurczowej (angina Printzmetala), a także zmiany niedokrwienne w określo-
nych sytuacjach, np. stresie, nadmiernym wysiłku fizycznym, nietypowej ak-
tywności seksualnej. Może być pomocne u chorych nie mogących wykonywać
wysiłków fizycznych. By rozpoznać niedokrwienie w badaniu holterowskim,
stosujemy regułę 1x1x1 (wg Deedwanii i Crbajala), tzn. obniżenie odcinka
ST o co najmniej 1 mm, trwające minimum 1 minutę, oddzielone od następ-
nego epizodu o co najmniej 1 minutę.
Innym bardzo ważnym, choć zaliczanym także do uzupełniających, jest ba-
danie echokardiograficzne przez klatkę piersiową (ECHO serca). ECHO
serca jest metodą dodatkową, ponieważ nie służy ani do rozpoznania, ani do
wykluczenia ChNS. Stabilna choroba wieńcowa, zgodnie ze standardami
PTK, przy braku dodatniego wywiadu lub cech elektrokardiograficznych
przebytego zawału serca, nie stanowi wskazania do ECHO serca w ChNS.
Wskazaniem jest w tym przypadku podejrzenie i różnicowanie innych przy-
czyn bólów w klatce piersiowej.
Po co więc wykonujemy to badanie w stabilnej chorobie niedokrwiennej?
Wykonujemy je przecież praktycznie zawsze. Cele te to ocena:
W tym ostatnim przypadku stosujemy dopplerowską analizę napływu mi-
tralnego (zaburzenia relaksacji, restrykcja). ECHO serca wykonujemy
w każdym przypadku pogorszenia stanu klinicznego pacjenta, a także w ce-
lu oceny skuteczności zabiegów na naczyniach wieńcowych, takich jak po-
mostowanie, balonowanie, stentowanie (CABG, PTCA, PCI). Dotyczy to
zarówno stanów ostrych, jak i zabiegów planowych. Ważnym celem badania
echokardiograficznego jest różnicowanie objawów sugerujących ChNS (bó-
157
• budowy serca;
• wielkości jam i grubości ścian;
• morfologii i czynności zastawek;
• funkcji skurczowej lewej komory;
• funkcji rozkurczowej.

le wieńcowe, arytmia) z innymi możliwymi przyczynami tych dolegliwości,
takimi jak kardiomiopatie, zapalenia, wady zastawkowe.
Zawał serca, zarówno w fazie ostrej, jak i przewlekłej, jest uznanym wska-
zaniem do wykonania ECHO serca. Rolę i możliwości echokardiografii w tej
jednostce chorobowej przedstawiono poniżej:
Podstawowym pytaniem klinicznym zawsze stawianym echokardiografii
jest wielkość uszkodzenia pozawałowego serca. Ocenie upośledzenia funkcji
skurczowej lewej komory służą dwa związane ze sobą parametry: frakcja wy-
rzutowa (EF%) i wskaźnik zaburzeń kurczliwości. ECHO serca jest dobrą
metodą dla oceny EF% niezależnie od sposobu jej obliczania. Dopuszczalne
jest obliczenie frakcji wyrzutowej na oko – powinien tego dokonywać jed-
nak doświadczony badacz. Zaburzenia kurczliwości oceniamy półilościowo
i półjakościowo za pomocą schematu podziału sylwetki lewej komory wg
Amerykańskich Towarzystw Kardiologicznych jak na rycinie 3.
Frakcja wyrzutowa poniżej 20% uważana jest za złą rokowniczo. Im więcej
przydzielonych punktów zaburzonej kurczliwości, tym bardziej rozległe, cięż-
kie jest uszkodzenie lewej komory, niezależnie od sposobu obliczania. Istotną
rolą echokardiografii po zawale serca jest rozpoznanie jego mechanicznych
powikłań. Najcięższym jest tętniak pozawałowy. Definicja echokardiogra-
ficzna tętniaka to: zniekształcenie zarysu światła lewej komory w skurczu
i w rozkurczu, z jakościowymi i ilościowymi zaburzeniami kurczliwości oraz
trwałym, nieodwracalnym uszkodzeniem, tj. cechami morfologicznymi
uszkodzenia (blizna) (ryc. 4).
Jeżeli metody dotychczas zastosowane nie przyniosły pełnych rozstrzy-
gnięć diagnostycznych, należy wykonać specjalistyczne badania obciążenio-
158
• pomoc w rozpoznaniu;
• lokalizacja/korelacja z unaczynieniem;
• rozległość;
• parametry hemodynamiczne (EF%);
• rozpoznanie powikłań;
• ocena mięśnia nieobjętego zawałem;
• różnicowanie obszarów uszkodzenia anatomicznego
i czynnościowego (ogłuszenie, zamrożenie);
• zawał prawej komory;
• rokowanie.
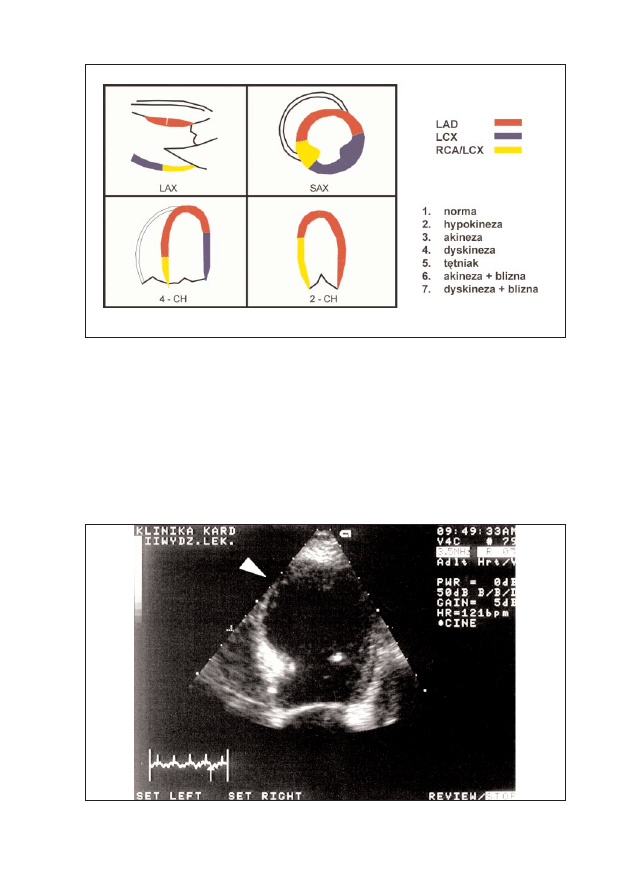
159
Rycina 3: Schemat podziału lewej komory wg Amerykańskich Towarzystw Kardiologicznych
oraz podział zaburzeń kurczliwości
LAX – projekcja przymostkowa w osi długiej lewej komory
SAX – projekcja przymostkowa w osi krótkiej lewej komory
4-CH – projekcja czterojamowa
2-CH – projekcja dwujamowa
LAD – gałąź przednia zstępująca lewej tętnicy wieńcowej
LCX – gałąź okalająca lewej tętnicy wieńcowej
RCA – prawa tętnica wieńcowa
1-7 – punkty przydzielane poszczególnym segmentom w zależności od rodzaju uszkodzenia
Rycina 4: Tętniak lewej komory serca

we w ośrodku o dużym doświadczeniu. Są to: scyntygrafia perfuzyjna i echo-
kardiografia obciążeniowa. Podstawowymi wskazaniami do nieinwazyjnych
badań obrazowych są:
Trzeba zaznaczyć, że na badania specjalistyczne kierujemy chorych po wy-
czerpaniu podstawowych możliwości diagnostycznych: EKG, ECHO, test
wysiłkowy, badanie holterowskie. Scyntygrafia wysiłkowa jest badaniem
o wysokiej czułości i stosunkowo niskiej swoistości. Jej zastosowanie w co-
dziennej praktyce nie jest duże, służy głównie do oceny kwalifikacji do proce-
dur inwazyjnych i operacji kardiochirurgicznych, w tym przeszczepów serca.
Bardziej przyjazną metodą, tańszą, szerzej dostępną, choć niełatwą do wyko-
nania jest echokardiograficzna próba wysiłkowa (stress-echo). Polecaną me-
todą jest obciążenie farmakologiczne zamiast fizycznego. Jest to badanie
możliwe do wykonania u większości pacjentów z chorobami układu serco-
wo-naczyniowego. Głównie chorzy z zarostową miażdżycą tętnic kończyn
dolnych nie są w stanie podjąć wysiłku fizycznego. Wskazania do stress-echo
przedstawiono poniżej:
160
• weryfikacja dodatniego wyniku elektrokardiograficznej próby
wysiłkowej u osoby z wyjściowo niskim prawdopodobieństwem
choroby wieńcowej;
• weryfikacja ujemnego wyniku testu wysiłkowego EKG u pacjenta
z bólami dławicowymi i wysokim prawdopodobieństwem choroby
wieńcowej;
• diagnostyka ChNS u osób z trudnym do interpretacji
elektrokardiogramem (np. blok lewej odnogi pęczka Hisa).
• diagnostyka ChNS, gdy niemożliwy jest wysiłek fizyczny;
• gdy niemożliwa jest interpretacja EKG spoczynkowego dodatniego
wysiłkowego (np.: blok lewej odnogi pęczka Hisa);
• fałszywie dodatni wynik testu wysiłkowego;
• rokowanie po zawale serca (wykrycie zamrożenia i ogłuszenia);
• kwalifikacja do rewaskularyzacji;
• ocena efektów leczenia zabiegowego i zachowawczego;
• ocena ryzyka przed rozległym zabiegiem niekardiochirurgicznym;
• ocena rezerwy skurczowej u osób ze znacznym upośledzeniem
kurczliwości lewej komory;
• pomoc w kwalifikacji operacyjnej stenozy aortalnej u chorych
z dużym upośledzeniem funkcji skurczowej lewej komory
• kardiotoksyczne działanie leków.
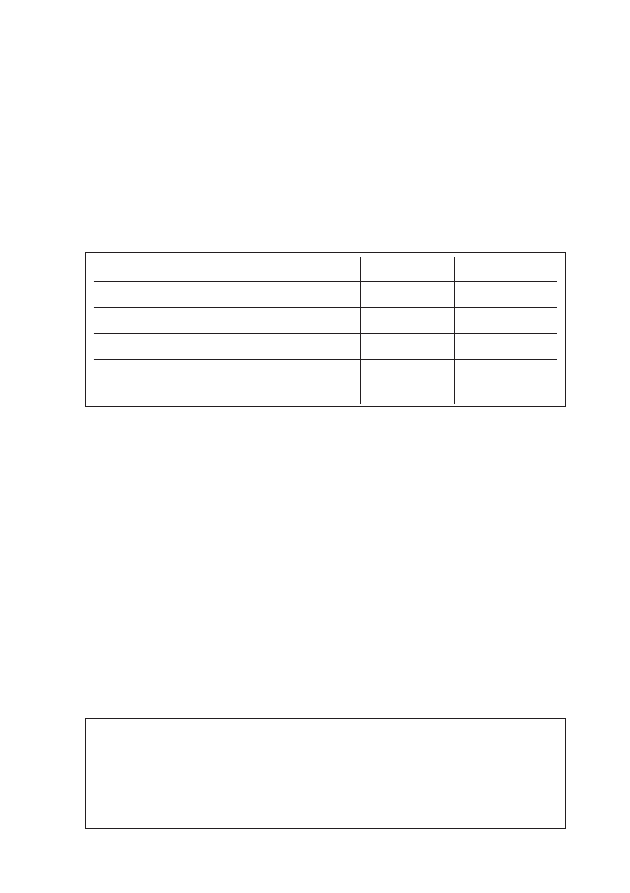
Kryterium dodatniego wyniku stress-echo jest pojawienie się nowych lub
poszerzenie dotychczas istniejących zaburzeń kurczliwości. Oceniane są także
kryteria kliniczne i elektrokardiograficzne w taki sam sposób, jak w teście
wysiłkowym EKG. Podobne są także przeciwwskazania. Możliwości inter-
pretacyjne stress-echo może limitować jakość obrazu ECHO 2D (dwuwymia-
rowego).
Porównanie wartości diagnostycznej (czułość, swoistość) nieinwazyjnych
metod diagnostycznych przedstawiono w tabeli 2.
Pozytronowa tomografia emisyjna jest dopiero od niedawna dostępna
w Polsce (2002 rok, Ośrodek w Bydgoszczy), nie sądzimy też, że jej wartość
wobec bardzo wysokich kosztów i niskiej dostępności będzie kiedykolwiek
wysoka.
Po przeprowadzeniu badań nieinwazyjnych możemy w ogromnej większo-
ści przypadków postawić lub wykluczyć rozpoznanie ChNS oraz oszacować
zaawansowanie choroby. Warto przypomnieć, że rozpoznanie ChNS stawia-
my przede wszystkim na podstawie wywiadu, oceny czynników ryzyka i praw-
dopodobieństwa choroby wieńcowej w danej populacji. Badania diagno-
styczne nie są mnożeniem zbędnych procedur i kosztów. Służą celom
opisanym powyżej. Ostatecznym badaniem jest cewnikowanie serca, koro-
narografia naczyń wieńcowych.
Podstawowy cel koronarografii to ustalenie sposobu leczenia. Jest bada-
niem dla wyboru optymalnej terapii. Główne zadania koronarografii to:
161
Tabela 2: Wartość nieinwazyjnych badań diagnostycznych w chorobie wieńcowej
BADANIE
CZUŁOŚĆ
SWOISTOŚĆ
próba wysiłkowa EKG
70-80%
60-70%
echokardiografia obciążeniowa
70-80%
80-90%
izotopowa scyntygrafia perfuzyjna
80-90%
60-70%
pozytronowa tomografia emisyjna
(PET)
90-100%
90-100%
• ustalenie wskazań oraz wybór optymalnego leczenia inwazyjnego
ChNS;
• szybka reperfuzja w ostrym zawale serca;
• potwierdzenie lub wykluczenie obecności zmian w tętnicach
wieńcowych.

Dokładne informacje dotyczące opisanych procedur Czytelnik znajdzie
w pierwszym tomie „Kardiologii Praktycznej”, poświęconym diagnostyce
kardiologicznej. Celem niniejszego opracowania jest podsumowanie najważ-
niejszych informacji i ustalenie znaczenia poszczególnych procedur w pro-
cesie diagnostycznym. Należy również z całą mocą podkreślić, że dopiero
analiza całokształtu obrazu klinicznego i logiczne, konsekwentne wykorzy-
stanie informacji płynących z badań diagnostycznych pozwoli ustalić rozpo-
znanie i wybrać optymalny sposób postępowania z chorym.
Zapamiętaj!
1. Podstawową metodą diagnostyki ChNS jest dokładnie zebrany wywiad.
2. Ocena czynników ryzyka i prawdopodobieństwa choroby wieńcowej u da-
nej osoby pozwala na rozpoznanie ChNS z wysoką trafnością.
3. Badania diagnostyczne w ChNS są najważniejsze dla grupy pacjentów
z umiarkowanym ryzykiem choroby, u chorych z ryzykiem niskim lub wyso-
kim badania dodatkowe są zwykle niepotrzebne (dla ustalenia rozpoznania).
4. Badania dodatkowe u chorych z rozpoznaną ChNS wykonujemy dla oceny
zaawansowania procesu, jego powikłań, skuteczności leczenia i celem kwa-
lifikacji do badań inwazyjnych.
5. Badania diagnostyczne dzielimy z praktycznego punktu widzenia na: pod-
stawowe (EKG, test wysiłkowy), uzupełniające (ECHO serca, badanie hol-
terowskie) i specjalistyczne (scyntygrafia i stress-echo).
6. Spoczynkowe badanie echokardiograficzne nie służy do potwierdzenia, ani
do wykluczenia ChNS.
7. Koronarografia przestaje być badaniem diagnostycznym, służy głównie do
wyboru optymalnej metody leczenia.
Warto przeczytać:
W. Braksator: Choroba niedokrwienna serca. W: Echokardiografia prak-
tyczna; pod redakcją P. Hoffmana i P. Pruszczyka, Wydawnictwo Lekar-
skie PZWL, 2001.
V. Froelicher: Podręcznik testów wysiłkowych; Bel Corp. Warszawa 2000.
Bayes de Luna: Elektrokardiografia kliniczna; Via Medica, Gdańsk 1999.
162
X.
LECZENIE CHOROBY NIEDOKRWIENNEJ SERCA
– JAK POWINIEN WYGLĄDAĆ STANDARD?
Jarosław Król, Monika Tomaszewska-Kiecana, Mirosław Dłużniewski
Z obserwacji sprzed wielu lat wiemy, że wystąpienie dolegliwości dławico-
wych związane jest z 4% ryzykiem zgonu z przyczyn sercowych w ciągu
pierwszego roku obserwacji. W 1/3 przypadków dolegliwości ustępują lub
zmniejszają się bez prób leczenia, natomiast po kilku latach trwania choro-
by – szansa na wyleczenie bez interwencji lekarza maleje do zera. Dziś nie
sposób opisać naturalnego przebiegu choroby niedokrwiennej serca, bo nie
ma pacjentów z bólami w klatce piersiowej, u których nie stosowano by le-
czenia. Standardem postępowania u chorego z dławicą piersiową jest dobór
sposobu leczenia, odpowiedni do stopnia zaawansowania choroby i ryzyka
wystąpienia jej najgroźniejszych powikłań. Czynnościowa klasyfikacja dusz-
nicy bolesnej wg Kanadyjskiego Towarzystwa Kardiologicznego (CCS), przy-
jęta także przez Polskie Towarzystwo Kardiologiczne (PTK) jest pomocna
w ustaleniu metody leczenia.
Pamiętać należy, że bóle w klatce piersiowej pojawiają się dopiero wtedy,
gdy zmiany w tętnicach wieńcowych są już zaawansowane. Ocena ryzyka tak
dramatycznych zdarzeń jak zawał serca czy nagły zgon, jest pierwszym zada-
niem stojącym przed lekarzem, do którego zgłasza się chory z objawami nie-
wydolności wieńcowej (bólami w klatce piersiowej, dusznością wysiłkową,
zaburzeniami rytmu serca). Gdy wieńcowy charakter dolegliwości nie budzi
wątpliwości, ważne jest ustalenie, czy nie ma okoliczności, które istotnie
wpływają na rokowanie (tab. 1).
163
Klasa I
– ból wieńcowy występuje tylko w trakcie długotrwałego lub
gwałtownego wysiłku. Nie ogranicza codziennej aktywno-
ści fizycznej pacjenta.
Klasa II –ból występuje przy szybkim marszu, wchodzeniu po scho-
dach powyżej I piętra, chodzeniu pod górę powyżej 200 me-
trów, podczas mrozu lub wiatru, w stresującej sytuacji, po
obfitym posiłku w pierwszych porannych godzinach.
Klasa III – ból pojawia się już przy zwykłej aktywności fizycznej, przy
wejściu na I piętro po schodach, podczas chodzenia poniżej
200 metrów, w zwykłych warunkach.
Klasa IV – występują bóle spoczynkowe i nocne, każdy wysiłek powo-
duje uczucie duszności.
Dziś, gdy możliwości farmakologicznego leczenia dusznicy bolesnej są sze-
rokie, diagnostyka inwazyjna i nieinwazyjna stają się coraz bardziej dostęp-
ne, a znajomość czynników przyspieszających rozwój miażdżycy i możliwości
ich modyfikacji rosną, rokowanie w przewlekłej niewydolności wieńcowej
powinno być coraz lepsze. Tak dzieje się w krajach, gdzie dostępność metod
diagnostycznych i leczniczych jest największa. Wzrasta też liczba chorych
z przewlekłą stabilną niewydolnością wieńcową, bo rośnie liczba chorych
skutecznie leczonych w ostrej fazie zawału serca. Poprawa rokowania wyni-
ka z zastosowania najwłaściwszego sposobu leczenia indywidualnie dobra-
nego dla konkretnego pacjenta. Dobre rokowanie, przy ograniczeniu lecze-
nia do metod zachowawczych, farmakologicznych dotyczy tych pacjentów,
którzy mają niewielkie zmiany, ograniczone do jednej lub najwyżej dwóch
tętnic wieńcowych i nie mają istotnie upośledzonej funkcji lewej komory.
Wraz ze wzrostem ryzyka wystąpienia groźnych dla życia ostrych objawów
niewydolności wieńcowej, pojawiają się wskazania do leczenia interwencyj-
nego (PCI) – np. plastyka tętnic wieńcowych lub kardiochirurgicznego – po-
mostowanie aortalno-wieńcowe (CABG).
JAK OCENIĆ RYZYKO WYSTĄPIENIA OSTRYCH ZDARZEŃ
WIEŃCOWYCH?
Ryzyko określa się jako niskie, średnie i wysokie po uwzględnieniu dwóch
najważniejszych składowych tej oceny:
164
Tabela 1: Czynniki źle wpływające na rokowanie u chorego ze stabilną dusznicą bolesną
OBRAZ KLINICZNY
BADANIA DODATKOWE
• nasilenie objawów dławicowych;
• niewydolność serca
w wywiadzie;
• podeszły wiek;
• nadciśnienie z przerostem lewej
komory;
• objawy choroby naczyń
obwodowych;
• cukrzyca;
• hiperlipidemia.
• dysfunkcja lewej komory;
• duży obszar zagrożonego
mięśnia;
• obecność substratu zaburzeń
rytmu.

Do oceny służą wyniki przeprowadzonych badań omówionych w rozdzia-
łach poświęconych diagnostyce kardiologicznej. W skrócie plan badań moż-
na przedstawić następująco:
165
• stopień uszkodzenia lewej komory;
• rozległość obszaru zagrożonego ostrym niedokrwieniem.
• wywiad i badanie przedmiotowe (towarzyszące choroby
metaboliczne w tym nadciśnienie tętnicze, palenie tytoniu, otyłość,
objawy niewydolności serca);
• podstawowe badania laboratoryjne (hemoglobina, poziom glikemii
oraz lipidogram na czczo);
• spoczynkowe badanie EKG wykonane przygodnie lub lepiej
w trakcie bólu w klatce piersiowej;
• RTG klatki piersiowej u chorych z objawami niewydolności serca
(także w przebiegu wad serca, zapalenia osierdzia czy
z podejrzeniem tętniaka aorty) oraz w celu wykluczenia płucnych
przyczyn dolegliwości;
• wysiłkowe EKG jest najistotniejsze dla potwierdzenia rozpoznania
u chorych ze średnim prawdopodobieństwem ChNS
przewidywanym na podstawie danych z wywiadów;
• EKG metodą Holtera, zwłaszcza gdy dominującym objawem są
zaburzenia rytmu serca;
• ECHO serca pozwala ocenić pochodzenie szmerów stwierdzanych
przy osłuchiwaniu serca u chorego z bólami w klatce piersiowej
(np. stenoza aortalna, kardiomiopatia), a także zaburzenia
kurczliwości lewej komory, które mogą być skutkiem niedokrwienia
lub przebytego zawału serca;
• badania obrazujące perfuzję w mięśniu sercowym (scyntygrafia,
echokardiografia obciążeniowa), gdy przeprowadzenie wysiłkowego
testu EKG nie jest celowe lub trudne do interpretacji (zespół WPW,
blok lewej odnogi pęczka Hisa, rytm ze stymulatora, badanie
niemożliwe do wykonania przez pacjenta);
• koronarografia rzadko obecnie służy do postawienia rozpoznania,
ale jest badaniem decydującym o wyborze leczenia.

LECZENIE CHOROBY NIEDOKRWIENNEJ SERCA
Cele leczenia ChNS to:
Cele te osiągnąć można na drodze leczenia farmakologicznego – prewen-
cja zawału serca i leczenie chorób stanowiących czynniki ryzyka oraz objawo-
we leczenie zmniejszające dokuczliwość choroby. Druga droga obejmująca
metody kardiologii interwencyjnej i kardiochirurgii to także leczenie obja-
wowe, zarezerwowane dla chorych ze zmianami miażdżycowymi w tętnicach
wieńcowych możliwymi do leczenia interwencyjnego. Chory po zabiegu –
plastyce tętnic wieńcowych lub operacji pomostowania aortalno-wieńcowego
– wymaga następnie leczenia farmakologicznego. Leczenie to obejmuje
przede wszystkim modyfikację czynników ryzyka rozwoju miażdżycy, bo bez
tego efekty ostrej interwencji nie mogą być trwałe.
Leczenie farmakologiczne
Standardy leczenia farmakologicznego przewidują stosowanie kwasu ace-
tylosalicylowego i innych leków działających antyagregacyjnie na płytki krwi,
a ponadto beta-adrenolityków, antagonistów kanałów wapniowych oraz azo-
tanów i coraz częściej statyn, nie tylko u chorych z zaburzeniami gospodarki
lipidowej. Standardy obejmują także leczenie nadciśnienia tętniczego i cu-
krzycy oraz farmakologiczne wspomaganie zwalczania palenia tytoniu i oty-
łości.
• Leki antyagregacyjne
Obecnie uważa się, że przyjmowanie przez wszystkich chorych z chorobą
wieńcową kwasu acetylosalicylowego w dobowej dawce 75-150 mg, u osób
bez przeciwwskazań jest standardem. Kwas acetylosalicylowy zmniejsza za-
padalność na zawał serca i częstość nagłych zgonów sercowych u chorych ze
stabilną chorobą wieńcową o 25-30%. Zmniejsza także śmiertelność oraz
częstość ponownych zawałów serca. Stosowanie preparatów kwasu acetylo-
salicylowego w prewencji pierwotnej jest celowe u chorych z czynnikami ry-
zyka jeszcze przed wystąpieniem objawów ChNS. U osób z przeciwwskaza-
166
• redukcja śmiertelności;
• prewencja pierwotna i wtórna zawału serca;
• poprawa tolerancji wysiłku;
• zapobieganie bólom dławicowym i ich doraźne leczenie.

niami do stosowania kwasu acetylosalicylowego, należy stosować leki z gru-
py tienopirydyn, takie jak tiklopidyna lub klopidogrel. Poza działaniem prze-
ciwpłytkowym leki te korzystnie wpływają na śródbłonek stymulując syntezę
tlenku azotu, prostacykliny oraz aktywują własną fibrynolizę. Standardowa
dawka tiklopidyny wynosi 500 mg na dobę (2 x 250 mg). Efekt terapeutycz-
ny występuje po 24-48 godzinach, a utrwala się po 5-6 dniach. Lek metabo-
lizowany jest przez wątrobę. Po przerwaniu stosowania tiklopidyny czynność
płytek i czas krwawienia wraca do normy po 4-10 dniach. Standardowa daw-
ka klopidogrelu wynosi 75 mg na dobę. Ma szybki początek działania, już po
przyjęciu pierwszej dawki leku. Działanie antyagregacyjne występuje po
2 godzinach, a pełny efekt leczniczy osiągany jest po 2-3 dniach leczenia.
Klopidogrel, skuteczniejszy i lepiej tolerowany przez chorych niż tiklopidy-
na, powinien być standardowo stosowany łącznie z kwasem acetylosalicylo-
wym u chorych w pierwszych tygodniach po PTCA, zwłaszcza zakończonych
wszczepieniem stentu. Ograniczeniem tego wyboru są względy ekonomicz-
ne. Należy także pamiętać o działaniach niepożądanych tej grupy leków, do
których należą: biegunka, wymioty, nudności, osutka skórna, a także najpo-
ważniejszy objaw uboczny – możliwość wystąpienia neutropenii (u 2,1% le-
czonych tiklopidyną).
Leki wieńcowe o działaniu objawowym: azotany, antagoniści kanałów
wapniowych i beta-adrenolityki. Są to leki, które w różny sposób wpływają
na metabolizm komórki mięśnia sercowego, chroniąc ją przed skutkami nie-
dokrwienia.
• Azotany
To najstarsza grupa leków stosowanych w chorobie niedokrwiennej serca.
W praktyce klinicznej wykorzystujemy trzy rodzaje azotanów: trójazotan gli-
cerolu znany jako nitrogliceryna (NTG), dwuazotan izosorbitolu (ISDN)
oraz izosorbitol-5-monoazotan (IS-5-MN). NTG i ISDN dobrze wchłaniają
się po podaniu podjęzykowym, działają szybko i krótko po podaniu, dlatego
wskazaniem do ich stosowania jest doraźne przerwanie bólu dławicowego.
Zaleca się, aby wszyscy chorzy z rozpoznaną chorobą wieńcową mieli przy
sobie jeden z preparatów do podania podjęzykowo lub w aerozolu. Sorbonit
podany przed spodziewanym dużym wysiłkiem, może zapobiec wystąpieniu
bólu dławicowego u chorych z klasy I. Monoazotany lepiej wchłaniają się po
podaniu doustnym, działają długo i zalecane są do stosowania przez chorych
jako jeden z pojedynczo stosowanych leków wieńcowych w klasie II, a także
wspólnie z innymi w klasie III i IV. Dawkowanie preparatu raz na dobę za-
bezpiecza chorego przed rozwojem tachyfilaksji. Formy preparatów stoso-
wanych w klinicznej praktyce lekarskiej:
167

Działania niepożądane azotanów to: bóle głowy (występują zwykle na po-
czątku leczenia, a jeśli utrzymują się ponad 3 doby, jest to wskazanie do
zmiany preparatu), zaczerwienienie twarzy, uczucie gorąca, hipotonia,
omdlenia, tachykardia, alergia (rzadko).
• Antagoniści kanałów wapniowych
Jest to kolejna grupa leków mająca zastosowanie w chorobie niedokrwien-
nej serca, począwszy od II klasy wg CCS. Obecnie zastosowanie mają jedy-
nie preparaty charakteryzujące się powolnym uwalnianiem i działaniem
zwalniającym rytm serca. Pochodna dihydropirydyny pierwszej generacji –
nifedipina – zwiększając zapotrzebowanie serca na tlen okazała się lekiem
niekorzystnie wpływającym na rokowanie w ChNS. Mechanizm przeciwnie-
dokrwienny AKW jest związany ze zmniejszeniem siły skurczu mięśnia ser-
cowego, zwolnieniem częstości rytmu, poprawą relaksacji lewej komory, co
w konsekwencji prowadzi do poprawy ukrwienia warstwy podwsierdziowej.
Rozszerzeniu ulegają także naczynia nasierdziowe, a poprzez obniżenie ci-
śnienia systemowego, zmniejsza się obciążenie następcze serca. Działanie
naczyniorozszerzające stanowi ważne wskazanie do stosowania AKW w wa-
riancie Prinzmetala ChNS. Inne wskazania do stosowania tej grupy leków
to współistniejące nadciśnienie tętnicze, choroby naczyń obwodowych, za-
burzenia gospodarki lipidowej i cukrzyca. W kilku badaniach klinicznych wy-
kazano podobną skuteczność AKW i leków beta-adrenolitycznych w zapo-
bieganiu ostrym epizodom wieńcowym i zgonom. Czasem stosuje się AKW
z beta-adrenolitykiem w skojarzeniu, ze względu na sumowanie się efektów
przeciwniedokrwiennych, wyższą skuteczność skojarzonego leczenia nadci-
śnienia, a także rzadsze występowanie działań niepożądanych przy zastoso-
waniu leków w mniejszych dawkach.
• Leki beta-adrenolityczne
W przeciwieństwie do dwóch poprzednich grup leków, które mają działanie
typowo objawowe i nie wpływają na śmiertelność w chorobie wieńcowej, leki
beta-adrenolityczne mają udokumentowany wpływ na redukcję śmiertelno-
168
• szybko działające tabletki i aerozole stosowane podjęzykowo oraz
na śluzówkę jamy ustnej;
• tabletki i kapsułki o średnim i długim czasie działania (doustne);
• plastry z preparatami działającymi przezskórnie;
• roztwory do stosowania parenteralnego.

ści zarówno w zawale serca, jak i niewydolności serca oraz są skuteczne w za-
pobieganiu kolejnym zawałom. Jest to jedna z największych i najbardziej
zróżnicowanych grup leków. Wskazaniami do stosowania beta-adrenolityków
są wszystkie jej postaci kliniczne, ale u chorych z wariantem Printzmetala
i chorobami naczyń obwodowych powinny być stosowane ostrożnie, gdy
wskazania do ich podawania wyraźnie przeważają nad możliwymi niekorzyst-
nymi efektami ich działania. Pacjenci po przebytym zawale serca (prewencja
wtórna), z ostrym zawałem serca, z niestabilną i stabilną dusznicą bolesną
oraz z niemym niedokrwieniem, mają wskazania do ich stosowania. Należy
także pamiętać o efekcie metabolicznym tej grupy leków, które powodują
wzrost poziomu ATP oraz fosfokreatyny, zwiększają zużycie glukozy, a po-
nadto zmniejszają stężenie wolnych kwasów tłuszczowych oraz metabolizm
beztlenowy. Wskazaniem do leczenia jest niewydolność wieńcowa powyżej
II klasy. Leki beta-adrenolityczne są bardzo skuteczne w leczeniu wysiłkowej
dusznicy bolesnej, gdyż zmniejszają częstość występowania epizodów prze-
mijającego niedokrwienia, jak również podwyższają tolerancję wysiłku. Dużą
skuteczność wykazują także w bezbólowej postaci choroby niedokrwiennej
serca (nieme niedokrwienie). Przeciwwskazaniami do stosowania leków beta-
-adrenolitycznych są hipotonia i bradykardia znacznego stopnia. Względne
przeciwwskazania (głównie dla beta-adrenolityków nieselektywnych) to: hi-
poglikemia, zaburzenia lipidowe, kurcz oskrzeli, chromanie przestankowe,
zaburzenia potencji. Do objawów niepożądanych, które mogą wystąpić lub
nasilić się w wyniku stosowania beta-adrenolityków należą: hipotonia, brady-
kardia, bloki przedsionkowo-komorowe, ostra niewydolność serca, objawy
spastyczne oskrzeli, cukrzyca ze skłonnością do hipoglikemii, alergia.
• ACE-inhibitory
Korzystne działanie kliniczne inhibitorów enzymu konwertującego w ChNS
jest związane z:
169
• poprawą hemodynamiki (zmniejszenie obciążenia wstępnego
i następczego, bez wpływu na czynność serca);
• zmniejszeniem agregacji płytek;
• poprawą bilansu tlenowego;
• lokalnym rozszerzeniem tętnic wieńcowych;
• działaniem przeciwmiażdżycowym;
• działaniem antyarytmicznym;
• zapobieganiem odkształcalności lewej komory po zawale serca.

Ostatnio potwierdzono klinicznie korzystne działanie ACE-I w ChNS.
Okazało się, że leki te zmniejszają o 20-25% ryzyko nowych incydentów
wieńcowych i konieczność powtórnej hospitalizacji z powodu niestabilnej
dusznicy bolesnej.
Warto zauważyć, że ostatnie trzy grupy leków poza działaniem „wieńco-
wym” są zalecane jako podstawowe w leczeniu nadciśnienia tętniczego, po-
wszechnie spotykanego czynnika ryzyka rozwoju miażdżycy i zawału serca.
• Statyny
Statyny to grupa leków hipolipemizujących, które poza obniżaniem pozio-
mu cholesterolu wykazują także istotne działanie stabilizujące blaszkę miaż-
dżycową. Stabilizacja blaszki miażdżycowej polega na hamowaniu odczynów
zapalnych, niszczących substancję międzykomórkową w ścianie naczyń wień-
cowych i powodujących jej pęknięcie, pobudzanych przez lipidy zgromadzo-
ne w blaszce. Statyny mają też działanie antyoksydacyjne i hamują miejsco-
wo procesy krzepnięcia. Wyniki wieloośrodkowych badań (CARE, 4S, HPS,
WOSCOPS, ASCOT) wskazują na korzystny wpływ statyn na rokowanie u cho-
rych z ChNS, zarówno w prewencji wtórnej, jak i pierwotnej, niezależnie od
wyjściowego stężenia lipidów. Należy pamiętać, że docelowe stężenia cho-
lesterolu i jego frakcji w głównej mierze zależą od stopnia zagrożenia chore-
go. Dlatego tak ważne jest oszacowanie ryzyka każdego pacjenta, oparte na
wynikach badań biochemicznych łącznie z obrazem klinicznym. Cztery pre-
paraty tej grupy (atorwastatyna, lowastatyna, simwastatyna, prawastatyna)
mają w pełni udokumentowaną skuteczność. Objawy uboczne są rzadkie
(miopatia, zaburzenia żołądkowo-jelitowe, bezsenność, bóle głowy), ich
efekt zależy od dawki. W trakcie terapii należy kontrolować poziomy trans-
aminaz ze względu na potencjalne działanie hepatotoksyczne (pierwsze
przed rozpoczęciem leczenia, kolejne po 4-6 tygodniach, następnie co 3 mie-
siące w pierwszym roku i co 6 miesięcy w roku następnym). Przy wystąpieniu
bólów mięśniowych, mogących być objawem zapalenia mięśni, konieczne
jest oznaczenie CPK – wzrost aktywności dziesięciokrotnie przewyższający
normę nakazuje zmniejszenie dawki lub przerwanie leczenia.
Leczenie niefarmakologiczne
Do niefarmakologicznych metod leczenia zaliczyć należy zmianę trybu ży-
cia pacjenta, z uwzględnieniem diety oraz stosowanie treningów fizycznych
o intensywności dobranej indywidualnie. Pacjenci bez objawów niewydolno-
ści serca mogą stosować co najmniej 30-minutowe wysiłki (pod kontrolą tęt-
na) trzy razy w tygodniu. Treningi dla chorych po zawale serca oraz z obja-
170

wami niewydolności serca muszą odbywać się w specjalnych warunkach pod
nadzorem lekarskim z możliwością monitorowania EKG. Intensywniejszy
wysiłek fizyczny w wyższych klasach niewydolności jest przeciwwskazany.
Rewaskularyzacja
Podstawowe wskazania do zabiegów kardiochirurgicznych przywracają-
cych krążenie w zwężonych tętnicach wieńcowych, stanowią zaawansowane
zmiany w tych tętnicach z objawami uszkodzenia lewej komory, niską frakcją
wyrzutową oraz rozległym obszarem zaburzeń kurczliwości po przebytym
171
LECZENIE
W KLASIE I
• kwas acetylosalicylowy 75-150 mg/d lub tiklopidyna
2 x 250 mg/d;
• NTG doraźnie;
• ISDN p. o. przed spodziewanym większym
wysiłkiem;
• określenie rezerwy wieńcowej i dostosowanie
aktywności fizycznej;
• koronarografia w trybie planowym i kwalifikacja
do plastyki, leczenia chirurgicznego lub
zachowawczego.
LECZENIE
W KLASIE II
• jak w klasie I + lek „wieńcowy” stale np.:
– monoazotan 40-60 mg/d,
– werapamil 120-360 mg/d lub diltiazem
90-360 mg/d,
– beta-adrenolityk.
LECZENIE
W KLASIE III
• ocenić czy chory jest stabilny;
• leczenie dwoma lub trzema lekami „wieńcowymi”;
• ocenić korzyść z zastosowania leku metabolicznego,
ACE-I;
• koronarografia i kwalifikacja do plastyki, leczenia
chirurgicznego lub zachowawczego.
LECZENIE
W KLASIE IV
• chory niestabilny – hospitalizacja;
• koronarografia w trybie pilnym i kwalifikacja
do plastyki, leczenia chirurgicznego lub
zachowawczego.
Tabela 2: Zalecenia terapeutyczne w zależności od klasy CCS

zawale. Korzyści wynikające ze stosowania zabiegów w tej grupie chorych są
największe, pomimo zwiększonego ryzyka operacyjnego. Chorzy z chorobą
pnia lewej tętnicy wieńcowej, ze zmianami w trzech lub dwóch tętnicach
wieńcowych, z zajęciem proksymalnego odcinka gałęzi przedniej zstępują-
cej (GPZ), z frakcją wyrzutową < 50%, mają klasyczne wskazania do zabie-
gu CABG. Natomiast wskazaniem do zabiegu plastyki tętnic wieńcowych są
zmiany w dwóch lub trzech tętnicach (w tym w GPZ) u chorych z warunka-
mi anatomicznymi umożliwiającymi zabieg, bez dużego uszkodzenia lewej
komory i bez cukrzycy oraz z wysoce nieprawidłowymi wynikami badań nie-
inwazyjnych. Inne wskazania do PTCA, to mniej zaawansowane zmiany
w tętnicach wieńcowych, u chorego po przeżytym incydencie migotania ko-
mór lub częstoskurczu komorowego, zmiany o typie restenozy po wykona-
nym wcześniej zabiegu plastyki lub restenozy w stencie, czy w przeszczepie
aortalno-wieńcowym. Także niezadowalające wyniki leczenia farmakologicz-
nego mogą być wskazaniem do zabiegu, z uwzględnieniem ryzyka z nim
związanego.
Wiele problemów poruszonych w tym rozdziale znalazło swoje rozwinięcie
w innych częściach tego podręcznika. Niniejszy tekst stanowi pewnego stop-
nia przewodnik i służy tworzeniu planu terapeutycznego.
Zapamiętaj!
1. Leczenie ChNS, poprzedzone dokładną diagnostyką, musi odpowiadać in-
dywidualnie ocenionemu klinicznemu stanowi pacjenta.
2. U chorych z wysokim ryzykiem, postępowaniem z wyboru jest leczenie inter-
wencyjne, a następnie farmakologiczne i niefarmakologiczne leczenie czyn-
ników ryzyka.
3. Uznane leki „wieńcowe” to obok azotanów, działających objawowo, beta-
-adrenolityki, antagoniści kanałów wapniowych, inhibitory enzymu kon-
wertującego i statyny oraz leki przeciwpłytkowe.
Warto przeczytać:
T. H. Lee: Management of chronic ischemic heart disease. Heart disease.
A textbook of cardiovascular medicine. 6th edition. A Harcourt Health
Sciences Company 2001.
172

Przewlekła choroba niedokrwienna serca. Część 1, 2; ACCSAP (Kardiologia
Kliniczna Dorosłych – Program Samokształcenia). ACC, AHA. Wydanie
polskie pod patronatem PTK.
Scandinavian Simvastatin Survival Study Group: Randomized trial of cho-
lesterol lowering in 4444 patients with coronary heart disease. Lancet 1994;
344: 1383-1389.
M. Accad, A. D. Michaels: Postępowanie po zawale mięśnia sercowego.
Current Treatment Options in Cardiovascular Medicine 2002, 4: 41-54.
Kardiologia po Dyplomie 2002, 1: 3: 8-21.
173

XI.
STABILNA DUSZNICA BOLESNA
Joanna Syska-Sumińska, Iwonna Grzywanowska-Łaniewska,
Mirosław Dłużniewski
Stabilna dusznica bolesna (SDB) określa stan kliniczny charakteryzujący
się występowaniem bólów dławicowych przy określonym poziomie obciąże-
nia, bez zmiany swojego natężenia, przez co najmniej kilka tygodni lub mie-
sięcy. Ból w klatce piersiowej u pacjentów ze stabilną dławicą charakteryzu-
ją: typowe umiejscowienie, zależność od wysiłku, charakter oraz czas
trwania, a także reakcja na podjęzykowe nitraty.
SDB jest klinicznym wyrazem niedokrwienia mięśnia sercowego, którego
przyczyną są najczęściej zwężenia miażdżycowe w świetle naczyń wieńco-
wych. Ta postać choroby niedokrwiennej serca jest najpowszechniejsza,
przez co stanowi poważny problem dla lecznictwa ambulatoryjnego. W Pol-
sce dotyczy około 5% mężczyzn w wieku 45-54 lata oraz ponad 20% w wie-
ku powyżej 65. roku życia. Dla kobiet proporcje te wynoszą odpowiednio
1% i blisko 15%.
Rokowanie w SDB jest stosunkowo dobre, a śmiertelność roczna waha się
w granicach 1-2%, trudno jednak przewidzieć wystąpienie groźnych incyden-
tów wieńcowych, takich jak zawał mięśnia sercowego, niestabilna dusznica
bolesna, czy nagły zgon sercowy, które stanowią bezpośrednie zagrożenie
dla życia. Jak dowodzą dane epidemiologiczne, ostre zespoły wieńcowe do-
tyczą kilkunastu procent chorych z rozpoznawaną SDB. Ostre incydenty
wieńcowe nie zależą bowiem bezpośrednio od stopnia zwężenia naczynia
wieńcowego, ale od nagłego pęknięcia stosunkowo niewielkich, niestabil-
nych blaszek miażdżycowych z następowym tworzeniem się zakrzepu na po-
wierzchni pęknięcia oraz zmniejszeniem przepływu. Sprzyjają temu pewne
czynniki, takie jak nagły wzrost ciśnienia krwi, reakcja naczyniowo-skurczo-
wa czy miejscowy odczyn zapalny.
Na chorobę niedokrwienną serca choruje w Polsce ponad 1 milion osób
i jest ona powodem około 40% zgonów mężczyzn w średnim wieku. W okre-
sie do 1991 roku według raportów Światowej Organizacji Zdrowia, Polska –
obok Węgier – wykazywała najwyższe wskaźniki zachorowalności i umieral-
ności z powodu choroby wieńcowej. Na szczęście w Polsce od 1994 roku ry-
sują się tendencje zmniejszania umieralności z powodu chorób układu krą-
żenia. Problem ten przedstawiono szerzej w innych rozdziałach.
174

PODZIAŁ CHOROBY WIEŃCOWEJ
Rozważania dotyczące trudności kwalifikacyjnych i powstawania nowych
podziałów, zwłaszcza w ostrych zespołach wieńcowych, przedstawia inny roz-
dział. Oprócz charakteryzującej się występowaniem bólów dławicowych cho-
roby wieńcowej, wyróżnia się tzw. nieme niedokrwienie. Istnieją trzy typy
niemego niedokrwienia, także ten temat przedstawiono szeroko w innym
miejscu.
Ogólnie przyjętą i zalecaną przez Polskie Towarzystwo Kardiologiczne
(PTK) klasyfikacją czynnościową choroby wieńcowej, jest podział opraco-
wany przez Kanadyjskie Towarzystwo Kardiologiczne (CCS).
175
• stabilna choroba wieńcowa (SDB);
• niestabilna choroba wieńcowa (NDB);
• zawał serca;
• nagły zgon sercowy;
• naczynioskurczowa postać choroby wieńcowej
(zespół Printzmetala – ostatnio zaliczany jest do NDB);
• zespół X.
Klasa I – zwykła aktywność fizyczna, jak spacer, wchodzenie po scho-
dach – nie wywołuje dławicy. Bóle pojawiają się przy wysiłkach
dużych, gwałtownych lub przedłużonych.
Klasa II – małe ograniczenie zwykłej aktywności. Dławica występuje
podczas szybkiego spaceru, wchodzeniu po schodach, cho-
dzeniu ponad 200 metrów pod górę, po jedzeniu, przy
wietrznej pogodzie, przy działaniu zimna, stresu emocjonal-
nego, bądź podczas paru godzin po obudzeniu.
Klasa III – znaczne ograniczenie aktywności fizycznej. Dławica występu-
je przy chodzeniu mniej niż 200 metrów, wchodzeniu na
1 piętro w zwykłych warunkach.
Klasa IV – niezdolność wykonania żadnego wysiłku fizycznego bez dyskom-
fortu; objawy dławicowe mogą występować w spoczynku.

ZASADY POSTĘPOWANIA W STABILNEJ CHOROBIE WIEŃCOWEJ
Podstawowymi celami leczenia pacjentów ze SDB są:
Na każdym etapie postępowania z chorym, niezwykle ważne jest zwalcza-
nie czynników ryzyka ChNS, promowanie właściwej aktywności fizycznej
oraz leczenie chorób współistniejących. Tylko kompleksowe działanie może
przynieść oczekiwane efekty. Wśród znanych czynników ryzyka najistotniej-
sze znaczenie mają te, które poddają się modyfikacji:
Rzucenie nałogu palenia tytoniu – jest najtańszą i przynoszącą ogromne
korzyści metodą prewencji pierwotnej i wtórnej choroby wieńcowej. Bezpo-
średnim dowodem na to jest redukcja śmiertelności o 25-50% wśród cho-
rych po zawale serca, po 5 latach od zaprzestania palenia.
Nadciśnienie tętnicze – stanowi istotny czynnik ryzyka rozwoju ChNS i za-
wału serca. Jest jedną z podstawowych przyczyn rozkurczowej niewydolności
serca oraz zaburzeń rytmu. Doprowadza do przerostu mięśnia lewej komo-
ry, uznanego za niezależny czynnik ryzyka nagłego zgonu sercowego. Lecze-
nie nadciśnienia tętniczego w sposób znamienny redukuje śmiertelność
z przyczyn sercowo-naczyniowych.
Zwalczanie zaburzeń lipidowych – znamiennie redukuje ryzyko zgonu
z przyczyn sercowych, ilość ostrych incydentów wieńcowych i udarów niedo-
krwiennych mózgu. Potwierdzają to liczne badania kliniczne.
Systematyczny wysiłek fizyczny – dostosowany indywidualnie dla każde-
go chorego przynosi wymierne korzyści. Badania kliniczne, które objęły pa-
cjentów z SDB wykazały znamienną poprawę tolerancji wysiłku, wzrost mak-
symalnego zużycia tlenu oraz poprawę jakości życia w grupie regularnie
ćwiczącej.
Należy dążyć do utrzymania pożądanej wagi ciała u każdego chorego,
szczególnie w przypadku pacjentów z cukrzycą i nadciśnieniem tętniczym.
Można wykorzystać do tego celu programy edukacji dietetycznej oraz zale-
cając odpowiednią aktywność fizyczną.
176
• zmniejszenie śmiertelności;
• pierwotna i wtórna prewencja zawału serca;
• poprawa tolerancji wysiłku;
• zapobieganie bólom dławicowym i ich doraźne leczenie.

LECZENIE FARMAKOLOGICZNE STABILNEJ CHOROBY
WIEŃCOWEJ
Leczenie farmakologiczne SDB obejmuje stosowanie leków o udowodnio-
nym wpływie na śmiertelność i obniżających ryzyko zawału oraz leków wień-
cowych o działaniu objawowym.
Ostatnie lata przyniosły zmiany w dotychczasowej koncepcji leczenia SDB.
Są one efektem zrozumienia mechanizmów patofizjologicznych leżących
u podłoża tzw. ostrych zespołów wieńcowych. Kluczowym zjawiskiem odpo-
wiedzialnym za wystąpienie powyższych zespołów klinicznych jest niestabil-
na blaszka miażdżycowa, a zasadniczym celem leczenia staje się jej stabili-
zacja.
Jednocześnie warto pamiętać o konieczności indywidualizacji terapii
u każdego chorego. Decyzja o włączeniu kolejnych leków nie zależy jedynie
od częstości występowania, czasu trwania czy natężenia bólów w klatce
w piersiowej, ale również od konieczności jednoczesnego leczenia ewentual-
nych chorób współistniejących – nadciśnienia tętniczego, zaburzeń metabo-
licznych czy niewydolności serca.
WSPÓŁCZESNE KONCEPCJE TERAPII STABILNEJ DUSZNICY
BOLESNEJ
177
• zwalczanie czynników ryzyka (modyfikacja stylu życia) u wszystkich
chorych;
• kwas acetylosalicylowy w dawce 75-150 mg, przy braku
przeciwwskazań u wszystkich chorych (tylko w sytuacji
bezwzględnych przeciwwskazań poleca się tiklopidynę lub
klopidogrel);
• beta-adrenolityki – u wszystkich chorych po przebytym zawale serca
przy braku przeciwwskazań, ewentualnie u chorych bez przebytego
zawału i przy braku przeciwwskazań;
• statyny – u wszystkich chorych z udokumentowaną bądź
podejrzewaną miażdżycą tętnic wieńcowych, jeżeli stężenie LDL
cholesterolu >130 mg/dL (docelowo 100 mg/dL);
• ewentualnie statyny – jeżeli stężenie cholesterolu LDL >100 mg/dL
lub <129 mg/dL;
• azotany podjęzykowe lub wziewne w celu szybkiego zwalczania
bólu;

CHARAKTERYSTYKA LEKÓW STOSOWANYCH W STABILNEJ
DUSZNICY BOLESNEJ
Kwas acetylosalicylowy
Metaanaliza 300 badań klinicznych potwierdziła korzyści wynikające ze
stosowania kwasu acetylosalicylowego w prewencji zawałów oraz zmniejsze-
nia śmiertelności u pacjentów ze stabilną chorobą wieńcową. Uzasadnione
jest zatem stosowanie kwasu acetylosalicylowego w dawce 75-150 mg,
u wszystkich pacjentów z rozpoznaną chorobą wieńcową. U osób z przeciw-
wskazaniami do leczenia kwasem acetylosalicylowym, należy włączyć do le-
czenia jeden z dwóch preparatów antyagregacyjnych – tiklopidynę w dawce
2 x 250 mg, bądź klopidogrel w dawce 75 mg/dobę.
Warto podkreślić, że korzystny efekt kwasu acetylosalicylowego uzyskiwa-
ny u pacjentów ze SDB, może wynikać nie tylko z jego wpływu na procesy
agregacji, ale również z działania przeciwzapalnego, którego pozbawione są
pozostałe preparaty antyagregacyjne. Kwas acetylosalicylowy redukuje stęże-
nie białka C-reaktywnego, interleukiny-6 oraz hamuje gromadzenie się ma-
krofagów w ognisku zapalnym. Poprawia funkcję śródbłonka prawdopodob-
nie poprzez blokadę cyklooksygenazo-zależnego uwalniania czynnika
naczynioskurczowego. Obecnie nie zaleca się stosowania kwasu acetylosali-
cylowego w prewencji pierwotnej ze względu na ryzyko powikłań krwotocz-
nych, natomiast można rozważyć włączenie kwasu acetylosalicylowego
w grupach wysokiego ryzyka, przy współistnieniu kilku czynników ryzyka
ChNS (np. nadciśnienie tętnicze u osób po 50. roku życia).
Leki stabilizujące blaszkę miażdżycową
• Beta-adrenolityki
Rola beta-adrenolityków w grupie chorych po przebytym zawale serca zo-
stała bardzo dobrze udokumentowana. Leki te zmniejszają śmiertelność
oraz częstość wystąpienia ponownego zawału. Udowodniono również, że re-
178
• rozważenie wprowadzenia ACE-inhibitora, szczególnie u chorych ze
współistniejącą miażdżycą tętnic wieńcowych i obwodowych oraz
cukrzycą i nadciśnieniem tętniczym;
• antagoniści kanałów wapniowych lub azotany długodziałające,
przy współistniejących przeciwwskazaniach do stosowania
beta-adrenolityków.

dukują śmiertelność w grupie chorych z niewydolnością serca. Ich rola u pa-
cjentów ze stabilną dusznicą bolesną nie została jednoznacznie potwierdzo-
na badaniami klinicznymi, nie ma jednak powodu sądzić, że efekt przeciw-
ischemiczny, antyarytmiczny oraz stabilizujący blaszkę miażdżycową
beta-adrenolityków nie przynosi wymiernych korzyści w tej grupie chorych.
Dlatego są zalecane u wszystkich pacjentów z ChNS, jeżeli nie mają prze-
ciwwskazań. Mechanizm działania leków beta-adrenolitycznych w chorobie
niedokrwiennej serca przedstawiono poniżej:
179
• zmniejszenie zapotrzebowania mięśnia sercowego na tlen;
• zwolnienie rytmu serca;
• zmniejszenie szybkości i zakresu skracania włókien mięśniowych;
• zmniejszenie ciśnienia tętniczego;
• poprawa przepływu wieńcowego;
• wydłużenie czasu rozkurczu;
• poprawa przepływu w warstwie podwsierdziowej;
• ochronne działanie na komórki mięśnia sercowego w warunkach
niedokrwienia;
• zmniejszenie ryzyka pęknięcia blaszki miażdżycowej;
• działanie antyarytmiczne.
Tabela 1: Dodatkowe efekty działania wybranych beta-adrenolityków
PREPARAT
WŁAŚCIWOŚCI
labetalol
nieselektywny beta-adrenolityk,
a
1
-adrenolityk oraz
agonista receptorów
b
2
;
karwedilol
nieselektywny beta-adrenolityk,
a
1
-adrenolityk
w mięśniach gładkich tętnic, potencjalny antagonista
kanałów wapniowych;
bucindolol
nieselektywny beta-adrenolityk, wykazujący działanie
bezpośrednio rozszerzające naczynia;
nebiwolol
wysokoselektywny
b
1
-adrenolityk, wykazujący
działanie rozszerzające naczynia, poprzez stymulację
endogennej syntezy tlenku azotu na drodze przemian
metabolicznych z L-argininy, pod wpływem działania
enzymu – syntazy tlenku azotu. Nie wolno go
zalecać pacjentom stosującym sildenafil!

Beta-adrenolityki różnią się między sobą siłą działania, kardioselektywno-
ścią, obecnością, bądź brakiem działania błonowego oraz działaniami do-
datkowymi, takimi jak efekt wazodylatacyjny. Przykłady beta-adrenolityków
posiadających dodatkowe efekty działania przedstawiono w tabeli 1.
Każdy z przedstawionych wyżej preparatów jest wskazany u chorych ze
współistniejącym nadciśnieniem tętniczym, miażdżycą tętnic obwodowych,
zastoinową niewydolnością serca. W trakcie terapii tą grupą leków, nie nale-
ży zapominać o działaniach niepożądanych:
Należy wobec tego pamiętać o przeciwwskazaniach do leczenia beta-adre-
nolitykami:
Terapii beta-adrenolitykami nie wolno przerywać nagle, może to powodo-
wać nasilenie niedokrwienia mięśnia sercowego, wywoływać objawy klinicz-
ne, a nawet ostry zespół wieńcowy. Przewlekłe leczenie powinno się odsta-
wiać powoli, poprzez zmniejszanie dawki leku przez okres 2 tygodni.
180
• efekty sercowe:
– bradykardia,
– zahamowanie zatokowe,
– bloki przedsionkowo-komorowe,
– upośledzenie kurczliwości mięśnia sercowego;
• skurcz oskrzeli;
• zmęczenie;
• hipotonia;
• depresja;
• zaburzenia erekcji;
• maskowanie objawów hipoglikemii u osób leczonych insuliną;
• objaw zimnych nóg;
• nasilenie chromania przestankowego.
• astma oskrzelowa, stany spastyczne oskrzeli;
• objawy depresji;
• zespół Raynauda;
• zaawansowana choroba naczyń obwodowych;
• istotna bradykardia oraz bloki przedsionkowo-komorowe powyżej
I stopnia, choroba węzła zatokowego.

Najczęściej stosowane u pacjentów ze SDB leki z grupy beta-adrenoli-
tyków wraz z ich dawkami przedstawiono w tabeli 2.
• Statyny
Inhibitory hydroksymetyloglutarylo-koenzymu A, obok inhibitorów kon-
wertazy angiotensyny II oraz beta-adrenolityków, uważane są za leki stabili-
zujące blaszkę miażdżycową. Działanie to jest wielokierunkowe, obejmuje
również wpływy przeciwzapalne, a udowodniono je w wielu małych i dużych
próbach klinicznych. W wielu z nich potwierdzono korzystny efekt statyn na
śmiertelność, obniżenie ryzyka ostrych incydentów wieńcowych i konieczno-
ści interwencji kardiologicznych, nie korelujący bezpośrednio z ich efektem
hipolipemizującym. Racjonalnym wytłumaczeniem tego zjawiska, jest ich
udział w procesach zachodzących w samej blaszce miażdżycowej, jak rów-
nież wpływ na poprawę funkcji śródbłonka naczyniowego.
Mechanizmy działania statyn, mogące odpowiadać za efekt stabilizacji
blaszki miażdżycowej to:
181
Tabela 2: Najczęściej stosowane beta-adrenolityki u pacjentów ze stabilną dusznicą bolesną
PREPARAT
DAWKA
ILOŚĆ DAWEK
Atenolol
25-100 mg/dobę
1-2
Metoprolol
50-150 mg/dobę
2
Metoprolol SR
50-200 mg/dobę
2
Bisoprolol
2,5-10 mg/dobę
1
• poprawa wydzielniczej funkcji śródbłonka, dzięki obniżeniu LDL;
• wzrost uwalniania tlenku azotu;
• zmniejszenie ilości lipidów w blaszce miażdżycowej;
• zmniejszenie ilości metaloproteinaz (enzymów degradujących
macierz łącznotkankową, odpowiedzialnych za efekt
niestabilności blaszki);
• zwiększenie ilości kolagenu w blaszce miażdżycowej i wzrost jego
syntezy sprzyjający stabilizacji blaszki;
• wpływ na czynniki zapalne – zmniejszenie zewnątrzpochodnych
przyczyn niestabilności blaszki.

Obecnie, zgodnie z obowiązującymi standardami, przy włączaniu statyn
opieramy się na oznaczonych poziomach cholesterolu całkowitego i frakcji
LDL.
Niewątpliwie po ogłoszeniu pod koniec 2001 roku wyników badania HPS
(Heart Protection Study) rewizji ulegną prawdopodobnie aktualnie obowiązu-
jące standardy postępowania kardiologicznego. W cytowanym badaniu, sim-
wastatyna zmniejszyła śmiertelność oraz ryzyko zawału i udaru mózgu w sze-
rokiej populacji wysokiego ryzyka. Korzyści z terapii stwierdzono również
w grupie pacjentów ze stężeniem cholesterolu w granicach lub poniżej obo-
wiązującej normy.
Potencjalnie nowe, postulowane wskazania do stosowania simwastatyny,
mogą dotyczyć osób pomiędzy 40.-80. r. ż. z wyjściowym stężeniem choleste-
rolu całkowitego >135 mg/dL oraz zdiagnozowaną co najmniej jedną z po-
niższych chorób:
Leki objawowe stosowane w chorobie niedokrwiennej serca
• Azotany
Mechanizm działania azotanów (nitratów) polega na dostarczaniu egzo-
gennego tlenku azotu do komórek śródbłonka i mięśni gładkich, co w konse-
kwencji powoduje rozszerzenie naczyń i poprawę ukrwienia. W przypadku
naczynia uszkodzonego przez proces miażdżycowy, produkcja endogenne-
go tlenku azotu jest upośledzona i niewystarczająca, przeważają wówczas
substancje naczynioskurczowe (endotelina, acetylocholina, angiotensyna II
i inne), podanie azotanów uzupełnia więc zaistniały niedobór i wywołuje roz-
kurcz naczynia.
Azotany, najdłużej stosowane leki w chorobie niedokrwiennej serca, nie
posiadają dużych badań prospektywnych, udowodniających ich wpływ na ro-
kowanie i powikłania u pacjentów z chorobą wieńcową. Obserwacje klinicz-
ne potwierdzają jednak, że azotany poprawiają jakość życia chorych ze SDB,
ograniczają objawy kliniczne i występowanie bólów dławicowych. Zapobie-
gając skurczowi naczyń wieńcowych, są skuteczne w dławicy naczynioskur-
czowej Printzmetala, a także w niemym niedokrwieniu i zespole X. Zaob-
182
• chorobą niedokrwienną serca;
• cukrzycą t. 2;
• udarem mózgowym;
• chorobą naczyń obwodowych.

serwowano korzyści ze stosowania azotanów u chorych z ChNS i niewydol-
nością serca.
Krótkodziałające azotany są lekami pierwszego rzutu w opanowywaniu
bólu wieńcowego. Choremu należy zalecić nieprzekraczanie dawki 1,2 mg
w ciągu 15 min. Dawki powinny być przyjmowane nie częściej, niż co 5 mi-
nut.
Długodziałające preparaty zgodnie z obowiązującymi standardami, zale-
cane są jako leki kolejnego wyboru, w sytuacji braku efektów stosowanej te-
rapii.
Mechanizm działania azotanów w chorobie niedokrwiennej przedstawiono
poniżej:
Ograniczeniem przewlekłej terapii azotanami jest zjawisko tolerancji, któ-
rego podłoże jest wieloczynnikowe. Do przyczyn leżących u podłoża tego
procesu zalicza się:
Jedyną stosowaną obecnie metodą mogącą zapobiec zjawisku tolerancji,
jest zachowanie w trakcie terapii co najmniej 10-12-godzinnej przerwy
w przyjmowaniu leku. Przerwa powinna zostać dostosowana do rytmu do-
bowego dolegliwości dławicowych.
183
• działanie systemowe (rozszerzenie łożyska żylnego i tętniczego);
• działania wieńcowe:
– wzrost przepływu wieńcowego,
– rozszerzenie tętnic podnasierdziowych,
– rozszerzenie kolaterali,
– znoszenie skurczu tętnic wieńcowych,
– poprawa krążenia wieńcowego w warstwie podwsierdziowej.
• działanie antyagregacyjne;
• wpływ hamujący na przebudowę mięśnia sercowego.
• niedobór grup sulfhydrylowych;
• zmniejszoną wrażliwość na cyklazę guanylową;
• wzrost aktywności fosfodiesterazy, nasilający rozpad cyklicznego
GMP;
• nadmierną degradację tlenku azotu pod wpływem anionu
nadtlenkowego.

W trakcie terapii azotanami mogą pojawić się objawy niepożądane, o któ-
rych należy pamiętać: bóle głowy, tachykardia, omdlenia, hipotonia, nudno-
ści, wymioty i niezwykle rzadko – methemoglobinemia.
Każdy mężczyzna zażywający azotany musi zostać poinformowany o cał-
kowitym zakazie stosowania sindenafilu, ze względu na ryzyko groźnych po-
wikłań ze strony układu sercowo-naczyniowego ze zgonem włącznie.
Pozostałe przeciwwskazania do stosowania azotanów to:
• Antagoniści kanałów wapniowych (AKW)
AKW stanowią szeroką i niejednorodną grupę leków. Ich podstawowy me-
chanizm działania polega na selektywnym blokowaniu kanałów wapniowych
typu L. Konsekwencją tego jest zmniejszony napływ jonów wapnia do wnętrza
kardiomiocytów i komórek mięśni gładkich naczyń, a tym samym spadek kurcz-
liwości mięśnia sercowego oraz rozkurcz naczyń obwodowych i wieńcowych.
Leki należące do II i III generacji (nitrendypina, felodypina, amlodypina, laci-
dypina) praktycznie pozbawione są depresyjnego wpływu na serce.
AKW zwiększają przepływ wieńcowy głównie poprzez rozszerzenie naczyń
podnasierdziowych – ten efekt wykorzystywany jest w terapii dusznicy na-
czynioskurczowej typu Printzmetala. Obniżenie kurczliwości mięśnia serco-
wego oraz zwolnienie czynności wywoływane przez diltiazem i werapamil
ma również swoje korzystne efekty – powoduje bowiem zmniejszenie zapo-
trzebowania mięśnia sercowego na tlen, a ma to szczególne znaczenie w wa-
runkach niedokrwienia. Rozszerzenie łożyska naczyniowego i obniżenie
oporu obwodowego skutkuje redukcją obciążenia następczego, a to z kolei
powoduje obniżenie zużycia tlenu. Wszystkie te mechanizmy wykorzystywa-
ne są w terapii pacjentów z chorobą niedokrwienną serca.
Ostatnio wprowadzono termin kardioprotekcji dla określenia ochronne-
go wpływu tej grupy leków na niedokrwiony mięsień sercowy. Przede wszyst-
kim polega ono na:
184
• kardiomiopatia przerostowa z zawężaniem drogi odpływu lewej
komory;
• tamponada serca;
• zaciskąjące zapalenie osierdzia;
• serce płucne;
• zawał prawej komory;
• istotne hemodynamicznie zwężenie lewego ujścia żylnego i tętniczego.

Jednocześnie cały czas trwają badania nad hamującym wpływem AKW na
proces tworzenia się zmian miażdżycowych w naczyniach.
AKW znajdują zastosowanie we wszystkich klasach czynnościowych dusz-
nicy bolesnej, począwszy od klasy II. Zwykle są one podawane razem z beta-
-adrenolitykami i azotanami. Korzystne są kombinacje długodziałających
pochodnych dihydropirydynowych (amlodypina, nitrendypina, lacidypina)
z lekiem z grupy beta-adrenolityków. W sytuacji przeciwwskazań do beta-
-adrenolityków są lekami pierwszego rzutu.
AKW charakteryzują się porównywalną skutecznością przeciwniedo-
krwienną z beta-adrenolitykami. Ze względu na niekorzystne efekty krótko-
działających preparatów AKW, nie należy ich stosować u pacjentów z choro-
bą niedokrwienną i po zawale mięśnia sercowego.
Według Braunwalda, terapię SDB powinno rozpoczynać się od podania
kwasu acetylosalicylowego oraz leku z grupy beta-adrenolityków. Podkreśla
on, że zawsze należy rozważyć wprowadzenie inhibitora konwertazy angio-
tensyny. Jedynie zapobiegawczo, albo w celu łagodzenia objawów bólowych,
poleca podjęzykowe stosowanie azotanów. W sytuacji, gdy bóle występują
częściej niż 2-3 razy na tydzień, zaleca włączenie leków z grupy antagonistów
kanałów wapniowych lub długodziałających azotanów, pamiętając o zjawisku
tolerancji. Jeżeli mimo takiej intensyfikacji leczenia nadal pojawiają się bóle,
sugeruje wprowadzenie trzeciego leku z grupy leków wieńcowych bądź meta-
bolicznych. Gdy tak zaprogramowana optymalna terapia nie przynosi oczeki-
wanych korzyści, choremu należy przeprowadzić diagnostykę inwazyjną.
Wskazana jest ona także u osób z grupy wysokiego ryzyka, oszacowanego na
podstawie testów nieinwazyjnych (test wysiłkowy – niedokrwienne zmiany
EKG przy obciążeniu < 7 METs, echokardiografia obciążeniowa, czy scyn-
tygrafia perfuzyjna) oraz w celu poprawy jakości życia pacjenta.
Na każdym etapie leczenia nie można zapominać o modyfikacji czynni-
ków ryzyka oraz wskazaniach do stosowania leków z grupy inhibitorów hy-
droksymetyloglutarylo-koenzymu A (statyn).
185
• poprawie przepływu wieńcowego;
• redukcji obciążenia następczego;
• redukcji arytmii wywołanej przez niedokrwienie;
• zmniejszeniu uszkodzenia poniedokrwiennego serca;
• zmniejszeniu agregacji płytek krwi;
• redukcji przerostu mięśnia lewej komory;
• poprawie relaksacji lewej komory.

Zapamiętaj!
1. Stabilna dusznica bolesna to najpowszechniejsza postać choroby wieńco-
wej.
2. Podstawą leczenia jest modyfikacja stylu życia oraz eliminacja czynników
ryzyka.
3. Do leków zalecanych w farmakoterapii SDB należą: kwas acetylosalicylo-
wy, beta-adrenolityki, ACE-inhibitory, azotany, antagoniści kanałów wap-
niowych.
4. Na każdym etapie leczenia SDB należy pamiętać o diagnostyce inwazyjnej.
Warto przeczytać:
L. Giec, Z. S. Herman (red.): Farmakoterapia chorób układu sercowo-na-
czyniowego. PZWL, Warszawa, 2000.
Standardy PTK: Standardy Postępowania w Chorobach Układu Krążenia.
Kardiologia Polska 1997; XLVI (Suplement).
ACC/AHA/ACP/ASIM guidelines for the management of patients with chro-
nic stable angina. JACC 1999; 33: 2092-2197.
J. Gersh, E. Braunwald, O. Bonow: Chronic Coronary Artery Disease.
w: E. Braunwald: Heart Disease; 6th Edition; WB Saunders Comp. 2001,
37.
186
Wyszukiwarka
Podobne podstrony:
Kardiologia praktyczna 3 Choroba niedokrwienna serca (2)
Leczenie choroby niedokrwiennej serca, Farmakologia, Kardiologiczne
Choroba niedokrwienna serca (2), Kardiologia
Choroba niedokrwienna serca, Studia - ratownictwo medyczne, 3 rok, Podstawy chorób wewnętrznych - ka
cholesterol a choroba niedokrwienna serca - ktostam - rok 4 - am bydgoszcz, IV rok Lekarski CM UMK,
Choroba niedokrwienna serca (2), Farmakologia, Kardiologiczne
Choroba niedokrwienna serca (3), Farmakologia, Kardiologiczne
CHOROBA NIEDOKRWIENNA SERCA, fizjoterapia, fizjoterapia w kardiologii i chirurgii naczyniowej
CHOROBA NIEDOKRWIENNA SERCA, KARDIOLOGIA
Choroba niedokrwienna serca
49 CHOROBA NIEDOKRWIENNA SERCA
wykład choroba niedokrwienna serca
Czynniki ryzyka choroby niedokrwiennej serca cz
Stres a rozwój choroby niedokrwiennej serca
więcej podobnych podstron