
1
Instrukcja ćwiczenia
Zastosowanie regresji liniowej do obliczania szybkości reakcji chemicznych
Celem ćwiczenia jest wykonanie obliczeń i ich wizualizacja z wykorzystaniem arkusza
kalkulacyjnego Excel. Bazą do tego ćwiczenia jest ćwiczenie przeprowadzane na pracowni
chemii ogólnej pierwszego roku pierwszego etapu studiów.
Ćwiczenie składać się będzie z dwóch głównych części:
1. badanie wpływu stężenia reagentów na szybkość reakcji;
2. badanie wpływu temperatury na szybkość reakcji i wyznaczenie energii aktywacji.
Wprowadzenie
Badanie wpływu stężenia reagentów i temperatury na przebieg reakcji:
Jeżeli reakcja chemiczna przebiega zgodnie z równaniem:
a A + b B
c C + d D
to jej szybkość opisywana jest wzorem:
v = k
[A]
a
[B]
b
gdzie k jest współczynnikiem nazywanym stałą szybkości reakcji
[ ]
[ ]
zależnym od temperatury zgodnie z równaniem:
RT
E
a
Ae
k
Po zlogarytmowaniu ostatniego równania (logarytm naturalny) otrzymujemy:
RT
E
A
ln
k
ln
a
gdzie A – stała charakterystyczna dla danej reakcji, E
a
– energia aktywacji, R – stała gazowa
równa 8.314
mol
K
J
, T – temperatura bezwzględna.
Wykonując podstawienia:
k
y
ln
A
b
ln
T
x
1
otrzymujemy typową postać równania liniowego
b
ax
y
gdzie współczynnik kierunkowy prostej jest równy
R
E
a
a
Znając wartość tego współczynnika możemy wyznaczyć energię aktywacji
Ra
E
a
Reakcja badana w laboratorium przebiega według schematu:
S
SO
O
H
O
S
H
O
S
H
2
2
3
2
2
2
3
2
2
Roztwór mętnieje na skutek wydzielania się koloidalnej siarki. Czas
jaki upływa od
zmieszania reagentów do pojawienia się zmętnienia zależy od stężeń reagujących substancji
i od temperatury. Szybkość reakcji v jest odwrotnością czasu
jej trwania.
2
Wykonanie ćwiczenia w Excelu
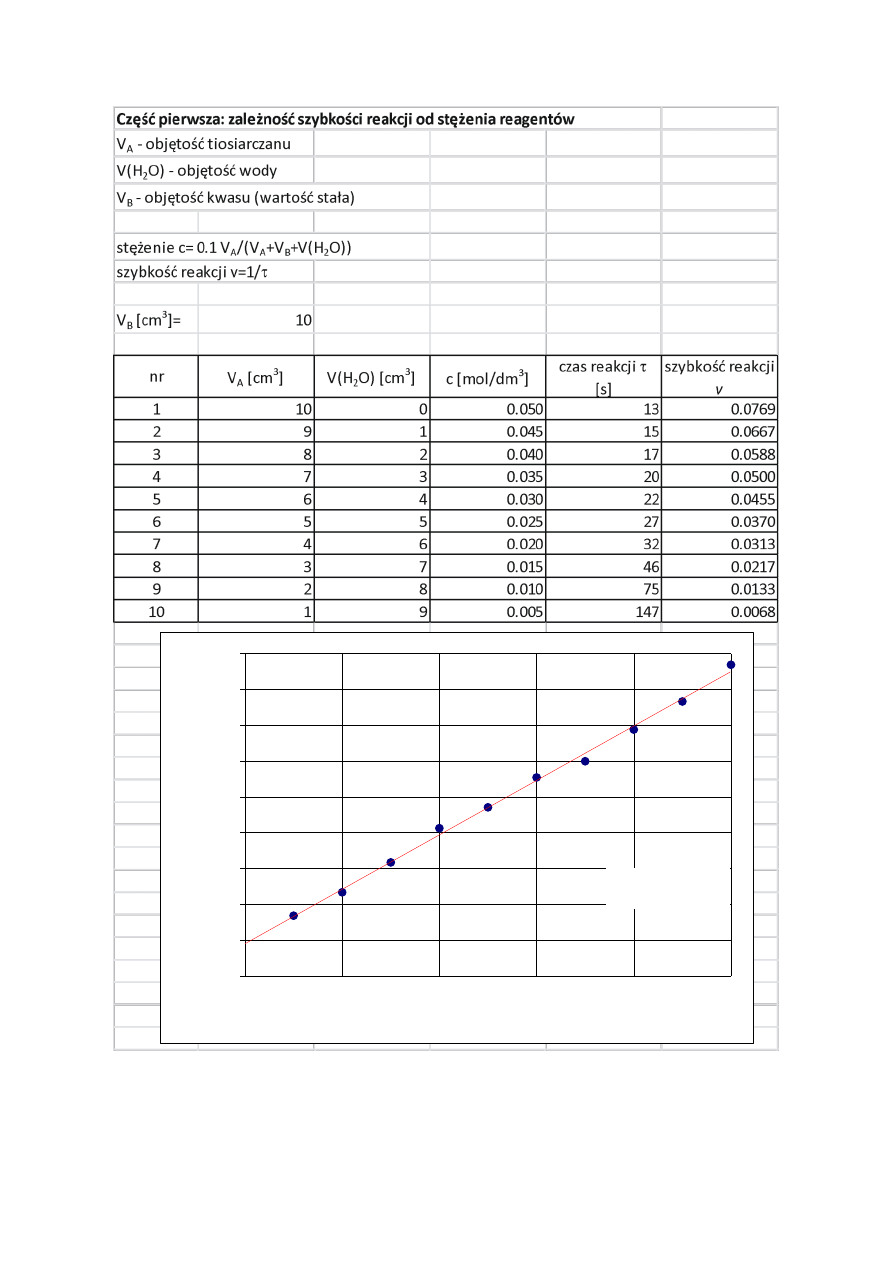
Arkusz 1. Część pierwsza: badanie wpływu stężenia reagentów na szybkość reakcji
W tej części ćwiczenia zbadano wpływ stężenia jednego z reagentów (reagent
A = Na
2
S
2
O
3
) na szybkość reakcji przy zachowaniu pozostałych parametrów, które mogą
wpływać na szybkość reakcji, w tym stężenia drugiego reagenta (reagent B = H
2
SO
4
)
(warunki pseudo-pierwszorzędowe). W tym celu przygotowano serię roztworów reagenta A
o różnych stężeniach, następnie połączono zawartość pierwszej próbówki roztworu A i
roztworu B. Po wymieszaniu obserwowano roztwór, mierząc jednocześnie czas
do
pojawienia się zmętnienia. Podobnie postąpiono z pozostałymi probówkami. Wyniki
umieszczono w tabeli.
Wypełnienia Arkusza 1
W Arkuszu 1 w komórce A1 wpisać nazwę ćwiczenia, tak jak jest to pokazane na stronie 3
instrukcji. Następnie wpisać odpowiednie teksty do kolejnych komórek, m.in. tekstową postać
wzorów do obliczeń stężenia c i szybkości reakcji v oraz V
B
[cm
3
] - objętość roztworu B. W
odpowiedniej komórce wpisać liczbę 10 jako objętość roztworu B.
W tabeli do kolumn: nr pomiaru, V
A
[cm
3
], V(H
2
O) [cm
3
] i
[s] - czas trwania reakcji -
wpisać odpowiednie liczby. Komórki w kolumnach c [mol/dm
3
] i szybkość reakcji v wypełnić
automatycznie formułami napisanymi na podstawie następujących wzorów:
- wzór do obliczenia stężenia roztworu (stężenie wyjściowe roztworu A jest równe
0.1 [mol/dm
3
]):
O
H
V
V
V
V
c
B
A
A
2
1
.
0
- wzór do obliczenia szybkości reakcji:
1
v
UWAGA: zamieszczone w tabeli liczby służą jedynie do kontroli poprawności formuł
własnych.
Po wypełnieniu tabeli wykonać wykres typu Punktowy XY przedstawiający zależność
szybkości reakcji v od stężenia tiosiarczanu c - nazwy osi X i Y takie, jakie są na wykresie
na stronie 3. Zoptymalizować wykres tzn. dobrać wielkość wykresu i obszaru kreślenia,
dobrać początek i koniec skali X i Y, umieścić siatki dla obydwu osi i sprawdzić ilość
wyświetlanych cyfr.
Na wykresie dodać linię trendu typu liniowego (regresja linowa) i w oknie Formatowanie
linii trendu
Opcje linii trendu zaznaczyć: Wyświetl równanie na wykresie i Wyświetl
wartości R-kwadrat na wykresie.
Wielkość czcionek dla wszystkich elementów na wykresie (opisy osi, równanie prostej itp.)
powinna być zawarta między 8 a 10 pkt.
Dodatkową czynnością związaną z wykresem jest przedłużenie przedstawianej zależności do
początku układu współrzędnych. W tym celu kliknąć prawym klawiszem myszy na linii
trendu wybrać polecenie Formatuj linię trendu
w oknie Formatowanie linii trendu
Opcje linii trendu, w polu Prognoza Do tyłu liczbę wpisać 0.005.
Całe opracowanie Arkusz 1 - tabela i wykres - powinny mieścić się w całości na jednej
stronie papieru formatu A4.
3
y = 1.5206x - 0.001
R² = 0.9969
-0.01
0.00
0.01
0.02
0.03
0.04
0.05
0.06
0.07
0.08
0.00
0.01
0.02
0.03
0.04
0.05
sz
ybk
o
ść
r
eak
cji
v
[1
/s
]
stężenie tiosiarczanu [mol/dm
3
]

4
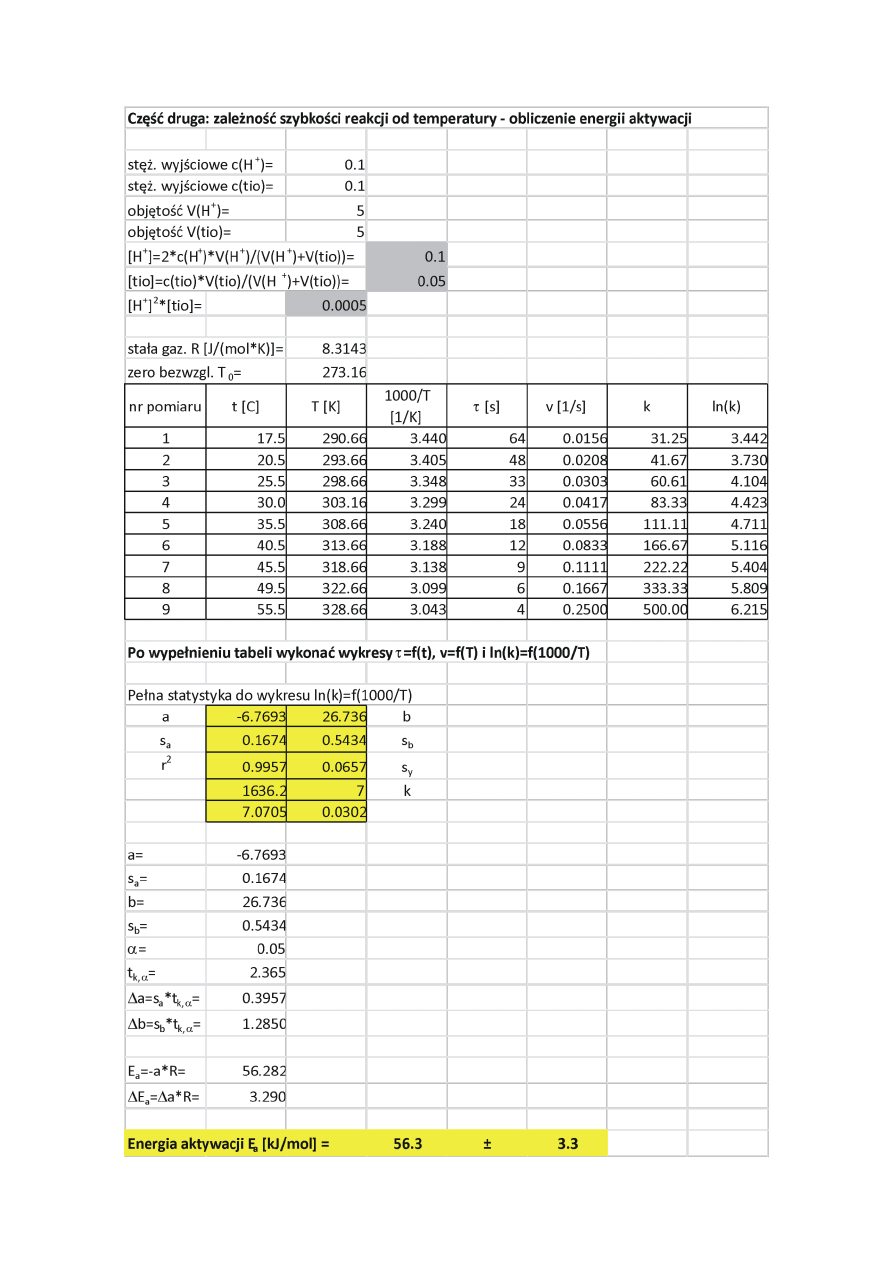
Arkusz 2. Część druga: badanie wpływu temperatury na szybkość reakcji i wyznaczenie
energii aktywacji.
W tej części ćwiczenia wyznaczana jest wartość stałej szybkości reakcji poprzez
badanie wpływu temperatury w której zachodzi badana reakcja (stężenia reagentów są stałe).
Do serii ponumerowanych probówek wlano po V = 5 ml roztworu reagenta A
o stężeniu c = 0.1 mol/dm
3
. W kolejnej serii probówek przygotowano po V = 5 ml roztworu
reagenta B o takim samym stężeniu. Wszystkie probówki z roztworami A i B umieszczono
w łaźni wodnej. Po upływie 10 minut zmierzono temperaturę, która wynosiła t
1
= 17.5
0
C.
Następnie roztwór reagenta B wlano do jednej z probówek zawierającej roztwór reagenta A.
Zmierzono czas
1
trwania reakcji (do momentu pojawienia się zmętnienia). Następnie
temperaturę podniesiono do t
2
= 20.5
0
C, w której termostatowano pozostałe probówki przez
co najmniej 10 min., po czym zmieszano zawartość dwóch kolejnych probówek z reagentami
A i B, zmierzono czas trwania reakcji
2
. Analogicznie postępowano z pozostałymi
probówkami podwyższając temperaturę za każdym razem o ok. 5
0
C i mierząc czas trwania
reakcji
. Wyniki umieszczono w tabeli.
Wypełnienia Arkusza 2
W Arkuszu 2 w komórce A1 wpisać nazwę ćwiczenia, tak jak jest to pokazane na stronie 5.
Kolejne komórki wypełnić następująco:
- wpisy kończące się znakiem "=" są tekstami;
- wpisy w komórkach bez koloru są liczbami;
- wpisy w komórkach zaznaczonych szarym kolorem są odpowiednimi formułami.
Do komórek tabeli w kolumnach: nr pomiaru, t [C] - temperatura w stopniach Celsjusza i
[s]
- czas trwania reakcji - wpisać odpowiednie liczby.
Komórki w kolumnach: T [K] - temperatura w K (T = t + T
0
), 1000/T [1/K], v [1/s] -
szybkość reakcji, k - stała szybkości reakcji i ln(k) - wypełnić automatycznie z użyciem
odpowiednich formuł. Wartości liczbowe podane w tych kolumnach na stronie 5 służą jedynie
do sprawdzenia poprawności obliczeń własnych.
UWAGA: użycie wielkości 1000/T spowoduje, że uzyskana końcowa wartość energii
aktywacji E
a
będzie wyrażona w jednostkach kJ/mol.
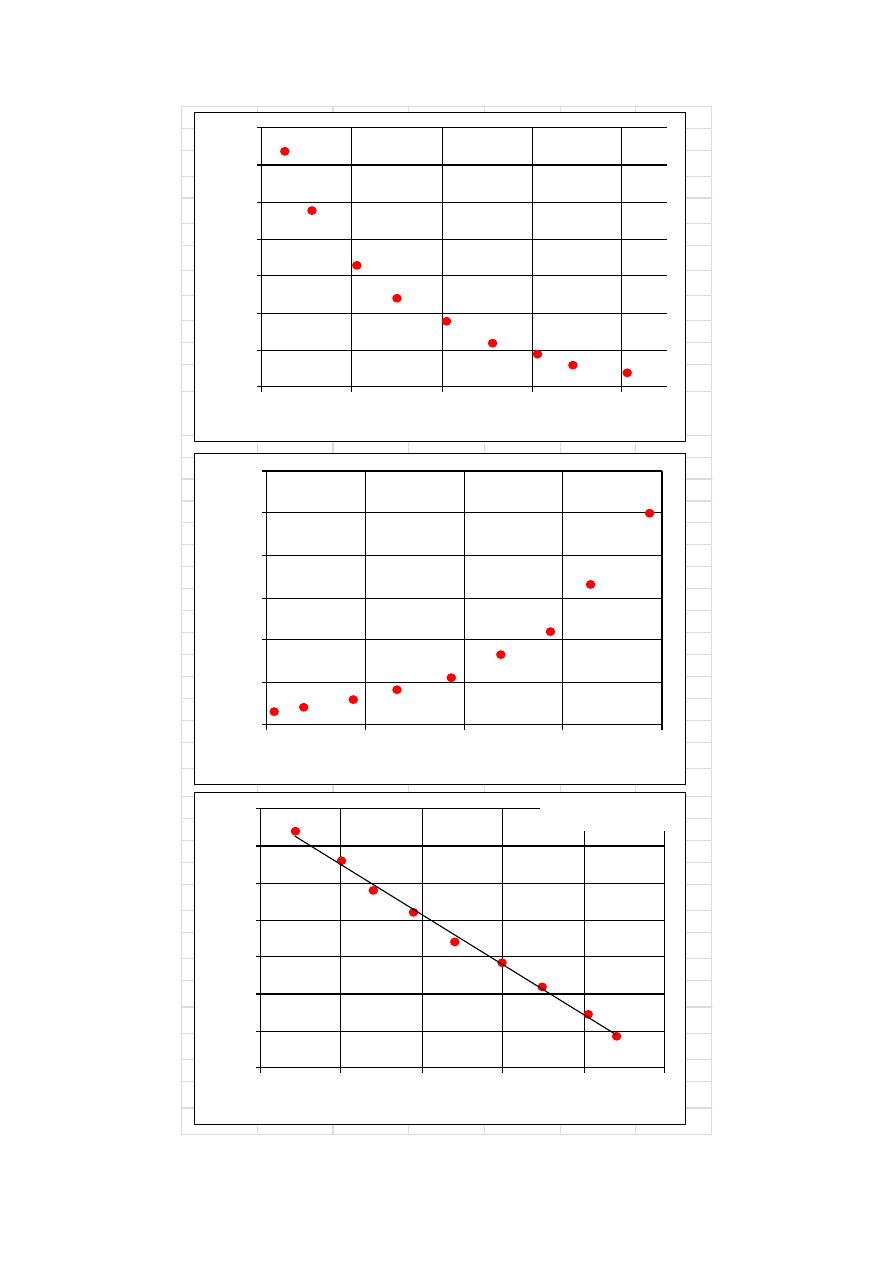
Wykonanie wykresów
Po wypełnieniu tabeli wykonać następujące wykresy typu Punktowy XY jako obiekty w
Arkuszu 2:
= f(t)
v = f(T)
ln(k) = f(1000/T)
Wykresy te pokazane są na stronie 6. Opisy osi zrobić takie, jakie są na tych wykresach.
Zoptymalizować wykresy tzn. dobrać wielkości wykresów i obszarów kreślenia, dobrać
początek i koniec skal X i Y, umieścić siatki dla obydwu osi, sprawdzić ilość wyświetlanych
cyfr, itd. Wielkości wykresów dobrać tak, żeby na stronie A4 zmieściły się całkowicie
wszystkie wykresy.
Na wykresie ln(k) = f(1000/T) dodać linię trendu typu liniowego (regresja linowa) z
równaniem prostej i kwadratem współczynnika korelacji (R-kwadrat).
Wielkość czcionek dla wszystkich elementów na wykresach (opisy osi, równanie prostej itp.)
powinna być zawarta między 8 a 10 pkt.
5
6
0
10
20
30
40
50
60
70
15
25
35
45
55
[s
]
t [C]
y = -6.7693x + 26.736
R² = 0.9957
3.0
3.5
4.0
4.5
5.0
5.5
6.0
6.5
3.0
3.1
3.2
3.3
3.4
3.5
ln
(k
)
1000/T [1/K]
0.00
0.05
0.10
0.15
0.20
0.25
0.30
290
300
310
320
330
v
[1
/s
]
T [K]
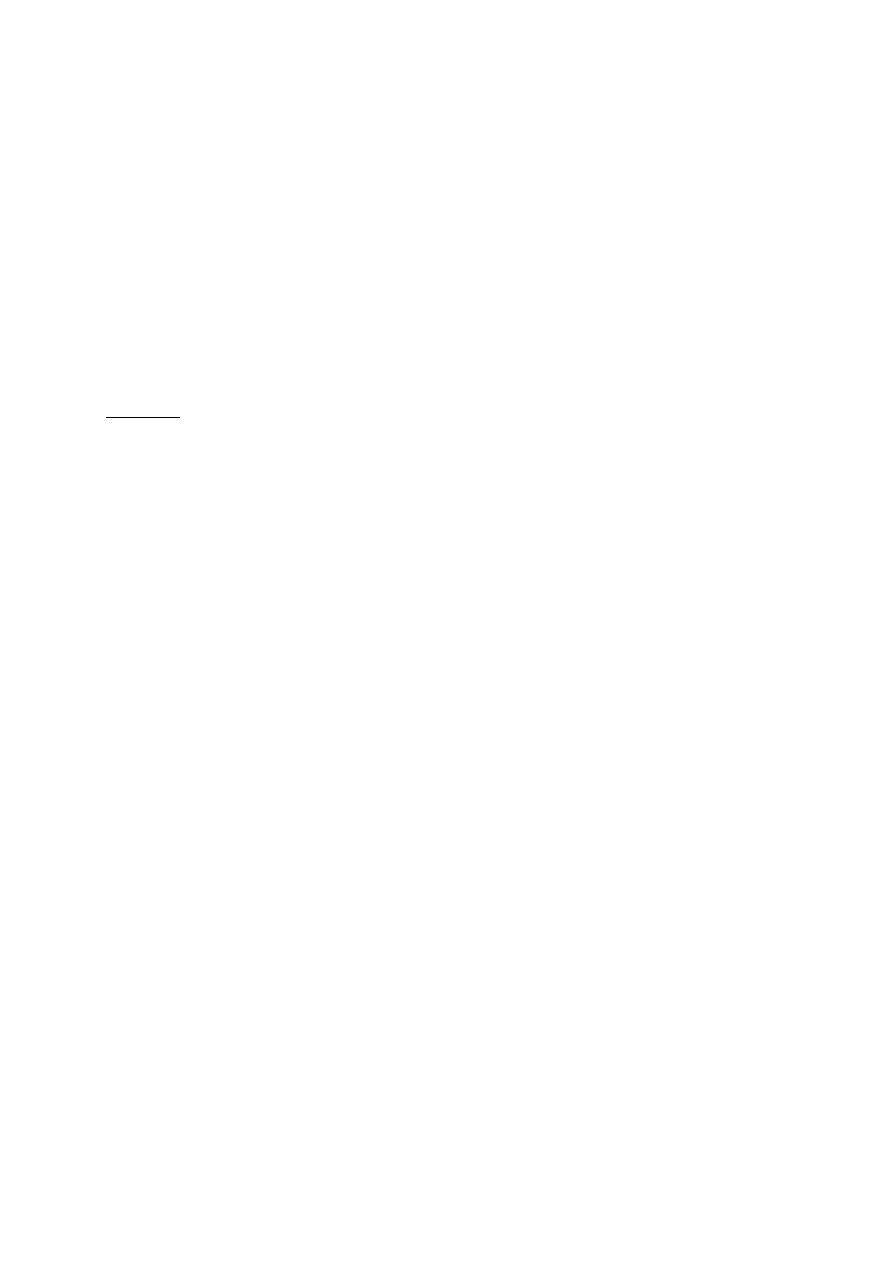
7
Obliczanie pełnej statystyki regresji do wykresu ln(k)=f(1000/T) z wykorzystaniem
funkcji statystycznej REGLINP
Wykonanie pełnej statystyki regresji opisane było w ćwiczeniu "Regresja liniowa dla danych
XY". Bazując na tamtym ćwiczeniu należy:
- w Arkuszu 2 poniżej tabeli zaznaczyć blok komórek o wymiarach 2
5;
- z karty Formuły wybrać funkcję Reglinp;
- wypełnić okno Argumenty funkcji następująco:
Znane_y: przeciągnąć myszą przez wszystkie liczby kolumny ln(k);.
Znane_x: przeciągnąć myszą przez wszystkie liczby kolumny 1000/T;
Stała: wpisać wartość logiczną PRAWDA lub 1;
Statystyka: wpisać wartość PRAWDA lub 1.
Następnie wcisnąć OK.
W pasku formuły wyświetli się formuła w postaci: =REGLINP(H14:H22;D14:D22;1;1).
UWAGA: zakres adresów argumentów X i Y będzie zależny od wykonującego ćwiczenie.
Ustawić kursor myszy w pasku formuły (w dowolnym miejscu formuły) i nacisnąć
klawisze: Ctrl+Shift+Enter.
Wyświetlone wartości liczbowe są wartościami statystyki metody najmniejszych kwadratów.
Opis poszczególnych komórek tabeli podany jest na stronie 5 instrukcji. Komórki nieopisane
związane są z rozkładem F - nie są w tym opracowaniu wykorzystywane.
Obliczenia końcowe - obliczenie energii aktywacji E
a
Do wykonania obliczeń końcowych wpisać zawartość komórek tak, jak to jest przedstawione
na stronie 5. Część wartości liczbowych uzyskana jest przez wpisanie prostej formuły
kopiującej zawartość odpowiedniej komórki (=Adres_komórki), część - przez wpisanie
odpowiedniej, bardziej złożonej formuły.
W celu obliczenia przedziałów ufności
a i
b dla współczynników a i b prostej należy
zastosować rozkład Studenta (patrz ćwiczenie "Regresja liniowa dla danych XY")
Wykonać obliczenia do końca tak, jak przedstawione jest to na stronie 5. Wynik końcowy
podać zgodnie z zasadami obowiązującymi przy formatowaniu wynik ± niepewność.
Wykresy jako nowe Arkusze
Dla każdego wykresu wykonać następujące czynności: skopiować wykres i zmienić jego
lokalizację: karta kontekstowa Narzędzia wykresów
karta Projektowanie
grupa
Lokalizacja
Przenieś wykres
otwiera się okno Przenoszenie wykresu - zaznaczyć
Nowy arkusz. Nazwy Arkuszy powinny mieć postać: Wykres 1, Wykres 2 i Wykres 3.
Wszystkie elementy na nowych arkuszach Wykres 1, 2 i 3 powinny mieć opisy czcionkami z
zakresu od 12 do 14 pkt. Sprawdzić skalowanie osi X i Y, i wykonać ewentualne poprawki.
Wyszukiwarka
Podobne podstrony:
,fizyka L, regresja liniowa id Nieznany (2)
2 Regresja liniowa dla danych Nieznany (2)
zadanie 2- regresja liniowa, Statyst. zadania
06.regresja liniowa, STATYSTYKA
08 Zastosowanie programow kompu Nieznany (2)
L4 regresja liniowa klucz (2)
1 Zastosowanie parametru predko Nieznany (2)
Wycena nieruchomości ćwiczenie 2 Budowa modelu wartości nieruchomości przy zastosowaniu regresji wie
3 Istotność parametrów modelu regresji liniowej
3-Estymacja parametrów modelu regresji liniowej, # Studia #, Ekonometria
11 regresja liniowa bis, Wariancja empirycznych współczynników a i b regresji liniowej
Estymacja parametrów modelu regresji liniowej 2
14 Zastosowanie przepisow prawa Nieznany (2)
statystyka, Korelacja i regresja liniowa, Korelacja i regresja liniowa
Regresja prosta, Przykłady Regresja prosta, Regresja liniowa prosta na przykładzie danych zawartych
więcej podobnych podstron