
HALOGENOWANIE - CHLOROWANIE
2
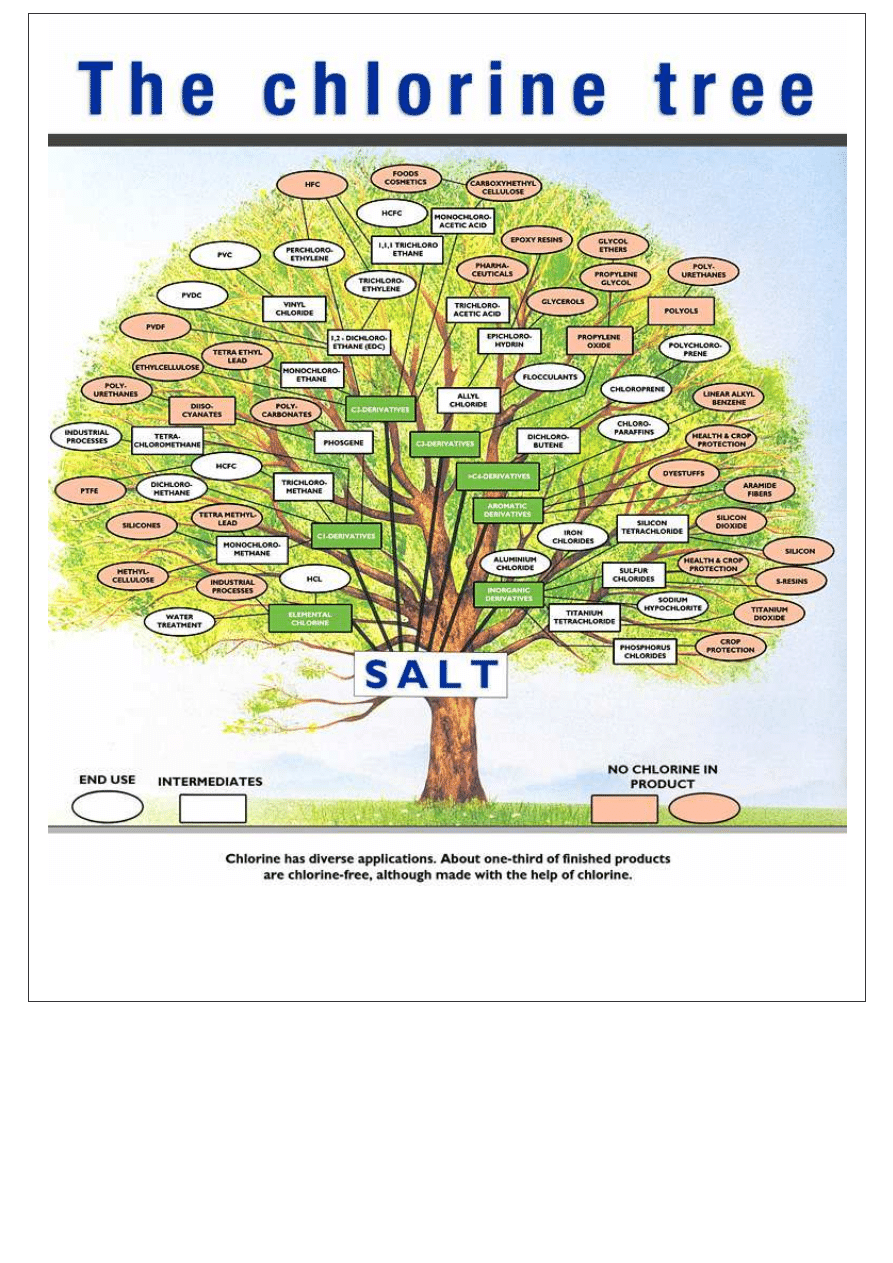

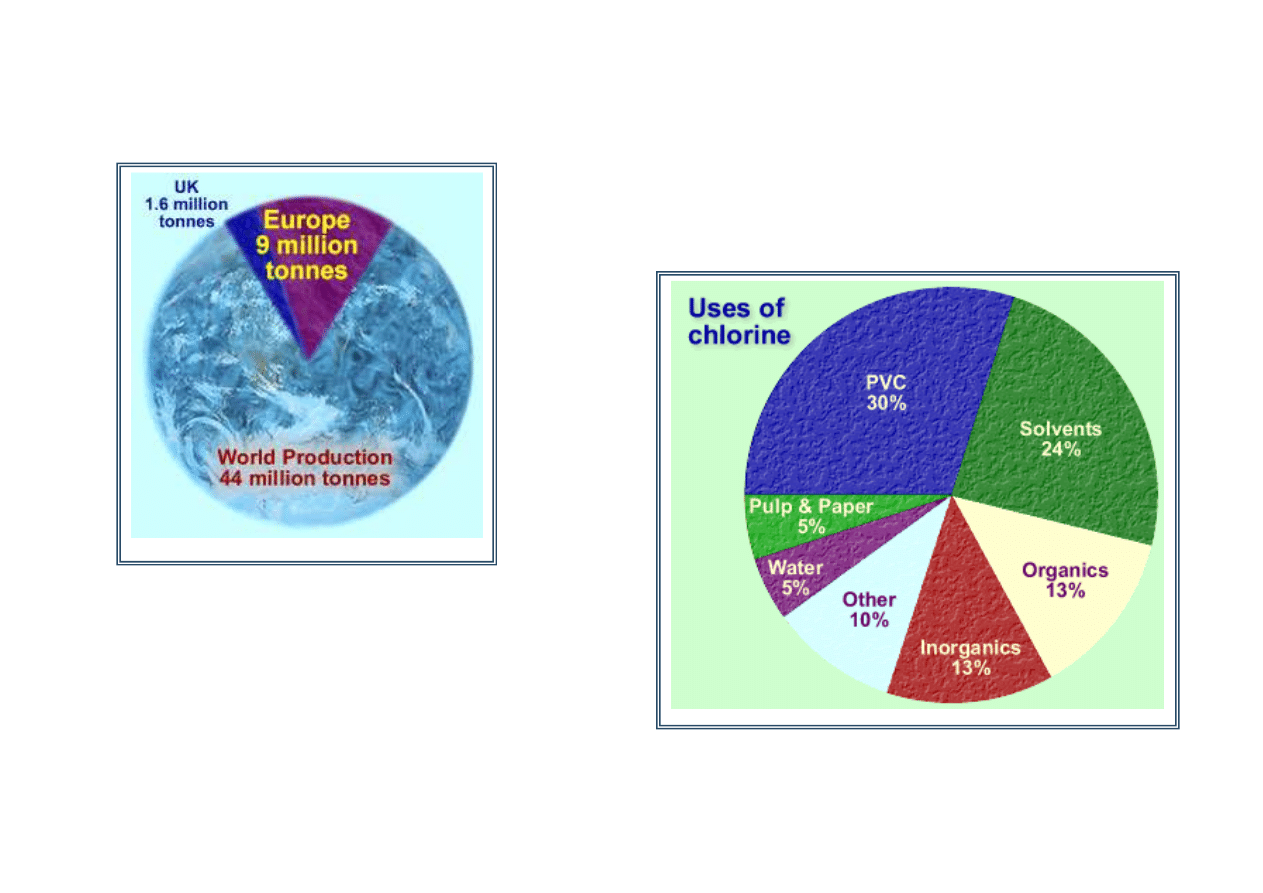
Pierwsza synteza chloru – (Schecle 1774 r.)
4 HCl + MnO
2
Cl
2
+ MnCl
2
+ 2 H
2
O
Obecnie głównym ródłem chloru jest elektroliza solanki.
braunsztyn
Wa niejsze procesy chlorowcowania realizowane w przemy le
Substrat
Czynnik
chloruj cy
Warunki reakcji
Produkt
Metan
Etan
Propan
Propan+propyle
n
Pentany
Parafina
Cl
2
Cl
2
Cl
2
nadmiar Cl
2
Cl
2
Cl
2
400-500
o
C
350-400
o
C
300-350
o
C
450-550
o
C
(chloroliza)
250-300
o
C
60-90
o
C
chlorek metylu, chlorek metylenu,
chloroform, tetrachlorek w gla
chlorek etylu,
1-, 2-chloropropan,
tetrachlorek w gla, perchloroetylen
monochloropentany
monochloroparafina (15% Cl) lub
wielochloropochodne o zawarto ci do 75%
chloru
Etylen
Etylen
Etylen
Etylen
Propylen
Propylen
Propylen
Propylen
n-Buteny
Chlorek allilu
Cl
2
HCl+O
2
HCl
HOCl
HOCl
Cl
2
HCl
Cl
2
HOCl
HOCl
FeCl
3
, 40-70
o
C
CuCl
2
, 220-240
o
C
AlCl
3
, 30-90
o
C
20-40
o
C
25-35
o
C
450-500
o
C
FeCl
3
, 120
o
C
FeCl
3
, 50
o
C
30-40
o
C
30-50
o
C
1,2-dichloroetan
1,2-dichloroetan
chlorek etylu
wodny r-r chlorohydryny etylenowej
wodny r-r chlorohydryny propylenowej
chlorek allilu
2-chloropropan
1,2-dichloropropan
wodny r-r chlorohydryn butylenowych
wodny r-r dichlorohydryn gliceryny
6
Alkohol allilowy
Acetylen
Acetylen
Acetylen
Winyloacetylen
HOCl
HCl
Cl
2
Cl
2
HCl
20-30
o
C
HgCl
2
, 110-210
o
C
FeCl
3
,
80
o
C
40
o
C
CuCl
2
, 60
o
C
wodny r-r monochlorohydryn gliceryny
chlorek winylu
tetrachloroetan
1,2-dichloroetylen
chloropren
Benzen
Benzen
Toluen
Toluen
Fenol
Fenol
Fenol
Fenol
Difenyl
Naftalen
Naftalen
Cl
2
Cl
2
Cl
2
Cl
2
NaOCl
Cl
2
SO
2
Cl
2
Cl
2
Cl
2
Cl
2
Cl
2
FeCl
3
,
80
o
C
UV, 20-40
o
C
UV, 100
o
C
FeCl
3
, 100
o
C
20-40
o
C
150-180
o
C
25
o
C
AlCl
3
, 60-180
o
C
FeCl
3
, 60-220
o
C
FeCl
3
, 100
o
C
AlCl
3
, 100-200
o
C
chlorobenzen, wielochlorobenzeny
heksachlorocykloheksan
chlorek benzylu,
60% o-chlorotoluen, 40% p-chlorotoluen
mieszanina o- i p-chlorofenolu
o-chlorofenol
p-chlorofenol
pentachlorofenol
wielochloropochodne o zawarto ci do 65%
wag. Cl
2
1-chloronaftalen
wielochloropochodne o zawarto ci do 60%
wag. Cl
2
Metanol
Etanol
Etanol
Propanol
Alkohol
izopropylowy
HCl
HCl
Cl
2
HCl
HCl
ZnCl
2
, 100
o
C
ZnCl
2
, 100
o
C
60-90
o
C
ZnCl
2
, 100
o
C
ZnCl
2
, 100
o
C
chlorek metylu
chlorek etylu
wodzian chloralu
chlorek n-propylu
chlorek izopropylu
7
Alkohole
amylowe
Kwas octowy
Aceton
Kwas
benzoesowy
p-tolueno-
sulfonamid
HCl
PCl
3
Cl
2
PCl
3
NaOCl
ZnCl
2
, 100
o
C
100
o
C
60
o
C
70
o
C
20-40
o
C
chlorki amylowe
chlorek acetylu
chloroaceton
chlorek benzoilu
chloramina T

Ogólna charakterystyka halogenowania
Pod poj ciem halogenowania rozumie si wszystkie reakcje polegaj ce na
wprowadzeniu atomów chlorowca (chloru, fluoru, bromu i jodu) do cz steczek
w glowodorów lub innych zwi zków organicznych.
Najbardziej rozpowszechnione s procesy chlorowania.
Fluorowanie i bromowanie ma zdecydowanie mniejsze znaczenie przemysłowe, a
jodowanie znaczenie marginalne.

9
Czynniki chloruj ce:
1. Chlor i bezwodne chlorowodory - s one rozpuszczalne w cieczach organicznych
(Br
2
>Cl
2
>F
2
i HBr>HCl>HF), co umo liwia przeprowadzenie procesów w fazie
ciekłej.
2. Mieszanina chlorowodoru i tlenu lub powietrza w obecno ci katalizatora mie-
dziowego - tzw. proces oksychlorowania.
3. Zwi zki chloru – PCl
3
, PCl
5
, POCl
3
, SOCl
2
(chlorek tionylu), SO
2
Cl
2
(chlorek
sulfurylu), COCl
2
- stosowane s bardzo rzadko w procesach przemysłowych.
4. Kwas chlorowy(I) (HClO) i jego sole - NaOCl, Ca(OCl)Cl.

10
Chlorowanie alkanów
CnH
2
n
+2
+ Cl
2
CnH
2
n
+1
Cl + HCl
W zale no ci od warunków procesu, obok mono- tworz si równie
polichloropochodne CnH2nCl2, CnH2n-1Cl3,..., a do CnCl2n+2.
Chlorowanie alkanów mo na prowadzi w sposób:
1. termiczny,
2. fotochemiczny,
3. w obecno ci katalizatorów.
W skali przemysłowej chlorowanie alkanów najcz ciej prowadzi si metod
termiczn .
11
Chlorowanie termiczne
Mechanizm rodnikowy
Cl
2
Cl + Cl
R + HCl
RH + Cl
R + Cl
2
RCl + Cl
RH + Cl
R + HCl

12
Warunki:
•
Chlorowaniu metanu - w temp. ok. 425-500
o
C
•
Chlorowanie homologów metanu
o
etanu w temp. 375-450
o
C,
o
frakcji naftowej w ok. 100
o
C.
W temperaturach ni szych od optymalnych, reakcje chlorowania nie zachodz , za w
wy szych nast puje odszczepienie wodoru z utworzeniem chlorowodoru, smoły i
koksu,
CH
4
+ 2 Cl
2
C + 4 HCl

13
Chlorowanie fotochemiczne
Chlorowanie w glowodorów gazowych przeprowadza si w obecno ci
rozpuszczalników nie ulegaj cych chlorowaniu, np. CCl
4
, do którego przy
na wietlaniu wprowadza si równocze nie chlor i w glowodór poddawany reakcji
chlorowania.
Chlorowanie fotochemiczne przebiega w niskich temperaturach (ok. 20
o
C),

14
Chlorowanie katalityczne
Prowadzi si za pomoc chloru w obecno ci
miedzi, antymonu, cyny, jodu, siarki i
innych, naniesionych na porowate no niki, jak w giel aktywny, pumeks. Szczególnie
aktywnym katalizatorem jest chlorek miedziowy, osadzony na porowatym no niku.
Katalizatorami homogenicznymi mog by zwi zki tworz ce rodniki, jak np.
diazometan, tetraetyloołów, heksafenyloetan, które powoduj dysocjacj cz steczek
chloru na atomy inicjuj ce reakcj ła cuchow .

15
In
ne metody chlorowania alkanów
Chlorkiem sulfurylu SO
2
Cl
2
, fosgenem COCl
2
, chlorkiem miedzi(II) CuCl
2
, czy PCl
5
.
Przykład
Gazowe alkany mo na chlorowa w temp. 400
o
C CuCl
2
, znajduj cym si w stanie
suspensji w gazie.
RH + 2 CuCl
2
RCl + 2 CuCl + HCl
Chlorek miedzi(I) utlenia si powietrzem w temp. 325-400
o
C i poddaje działaniu
chlorowodoru.
2 CuCl + 0,5 O
2
+ 2 HCl
2 CuCl
2
+ H
2
O
Zregenerowany chlorek miedzi(II) u ywa si ponownie w procesie chlorowania.
16
Chlorometan
CH
3
Cl
rozpuszczalnik specjalny (np. do polimeryzacji kauczuku
butylowego, do produkcji dentek)
czynnik metyluj cy
etery, półprodukty,
pestycydy
dimetylochlorosilan
silikony
+ Si
tetrametyloołów
dodatek do paliw
metyloceluloza
rodek zag szczaj cy farby
drukarskie
merkaptan metylowy
DMSO
siarczek dimetylu
rodek chłodz cy
+ stop
Pb-Na
+alkaliceluloza
+ NaHS
+ Na
2
S
17
Chlorek metylenu
CH
2
Cl
2
chlorobromometan
rozpuszczalnik tworzyw sztucznych, tłuszczów, olejów
+ Br
2
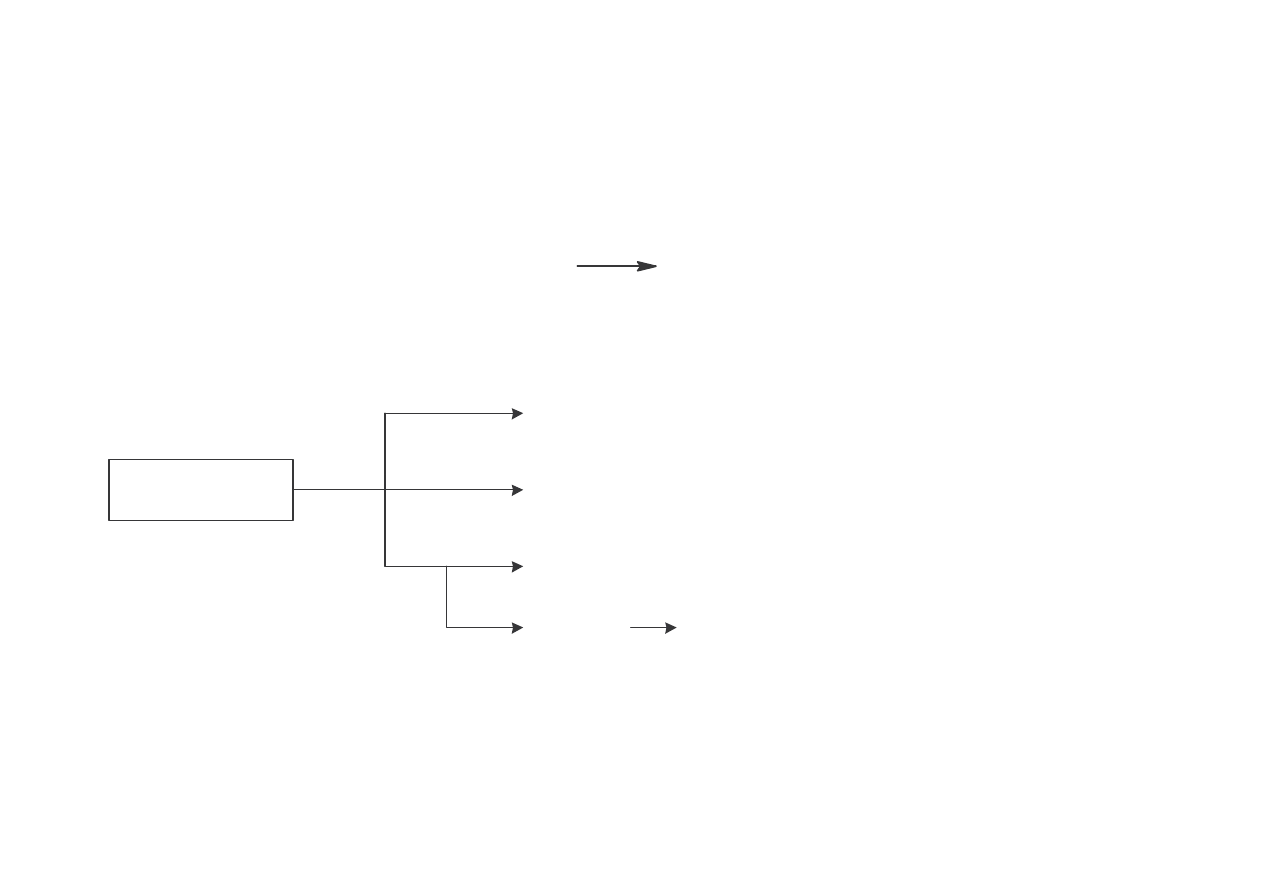
18
Chloroform
Przechowuje si go w butelkach ze szkła ciemnego, gdy pod wpływem wiatła i
tlenu atmosferycznego rozkłada si z wydzieleniem silnie truj cego fosgenu.
CHCl
3
+ 0,5 O
2
COCl
2
+ HCl
CHCl
3
rozpuszczalnik alkoholi, tłuszczów, olejów, ywic, kalafoni i kauczuku
do oczyszczania penicyliny i inych antybiotyków
freon R21
teflon
+ HF
freon R22

19
Tetrachlorometan
CCl
4
freony
rozpuszczalnik ywic, PCW, tłuszczów, olejów
odtłuszczacz metali
rodek ga niczy (dawniej)
czyszczenie odzie y na sucho (dawniej)
rozpuszczalnik do reakcji chlorowania w fazie ciekłej
zwalczanie szkodników
20
Metody otrzymywania chlorometanów
chlorowanie metanu
CH
4
CH
3
Cl
CH
2
Cl
2
CHCl
3
+Cl
2
-HCl
+Cl
2
+Cl
2
-HCl
-HCl
CCl
4
+Cl
2
-HCl
Proces chlorowania metanu mo na prowadzi metod :
jednostopniow – chlorowanie termiczne,
dwustopniow – chlorowanie termiczne i fotochemiczne, które przebiega w
niskiej temperaturze w fazie ciekłej.

21
Działanie chlorowodorem na metanol z otrzymaniem chlorku metylu,
CH
3
OH + HCl
CH
3
Cl + H
2
O
Oksychlorowanie metanu
CH
4
+ HCl + O
2
CH
3
Cl + H
2
O
Jest to tzw. proces Transcat.
22
Chlorowanie termiczne
Warunki procesu:
Aparatura odporna na chlor,
Surowce pozbawione wilgoci,
Temperatura – ok. 500
o
C,
Reaktor adiabatyczny,
Proces egzotermiczny - ciepło odprowadzane wraz z kilkakrotnym nadmiarem
CH
4
,
Selektywno przereagowania CH
4
na chlorometany 85-90%.
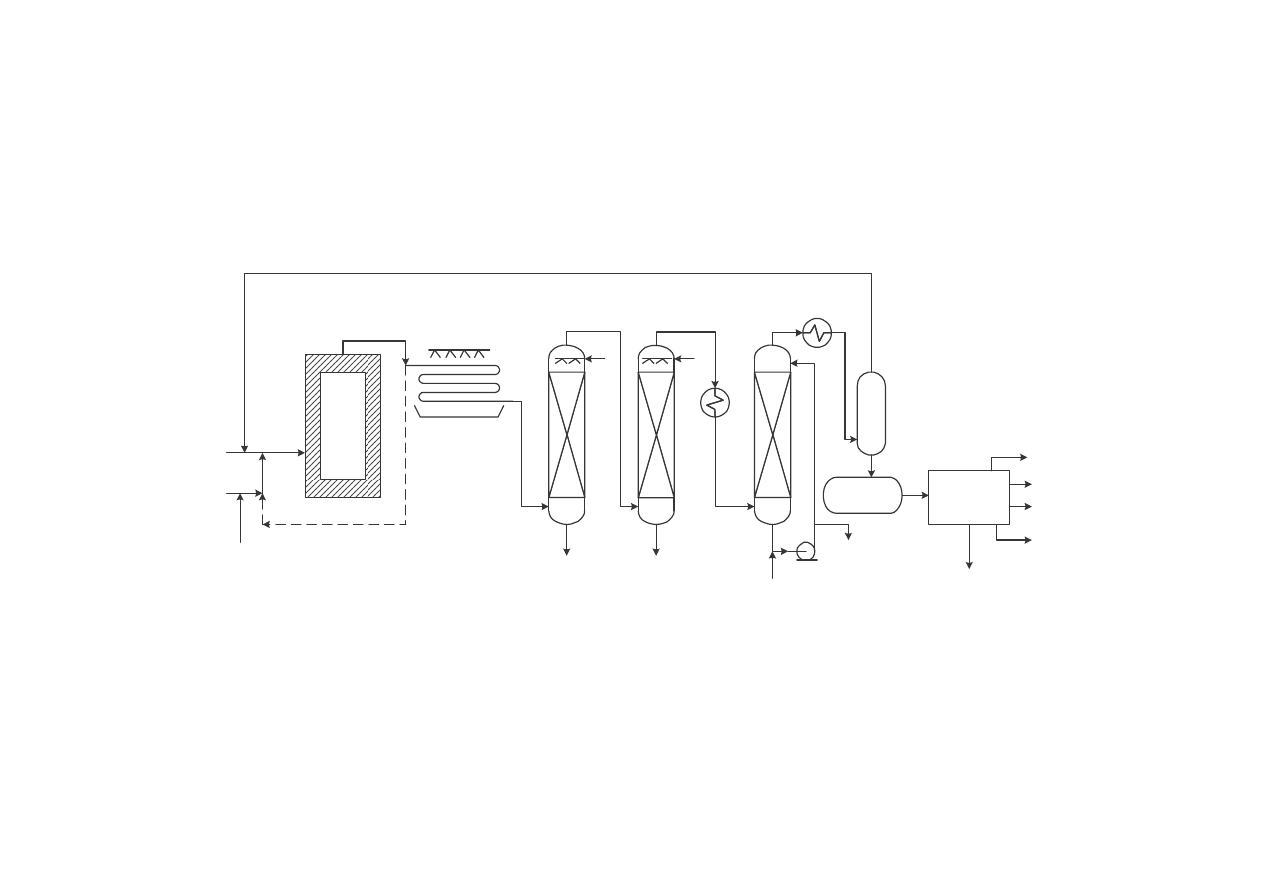
23
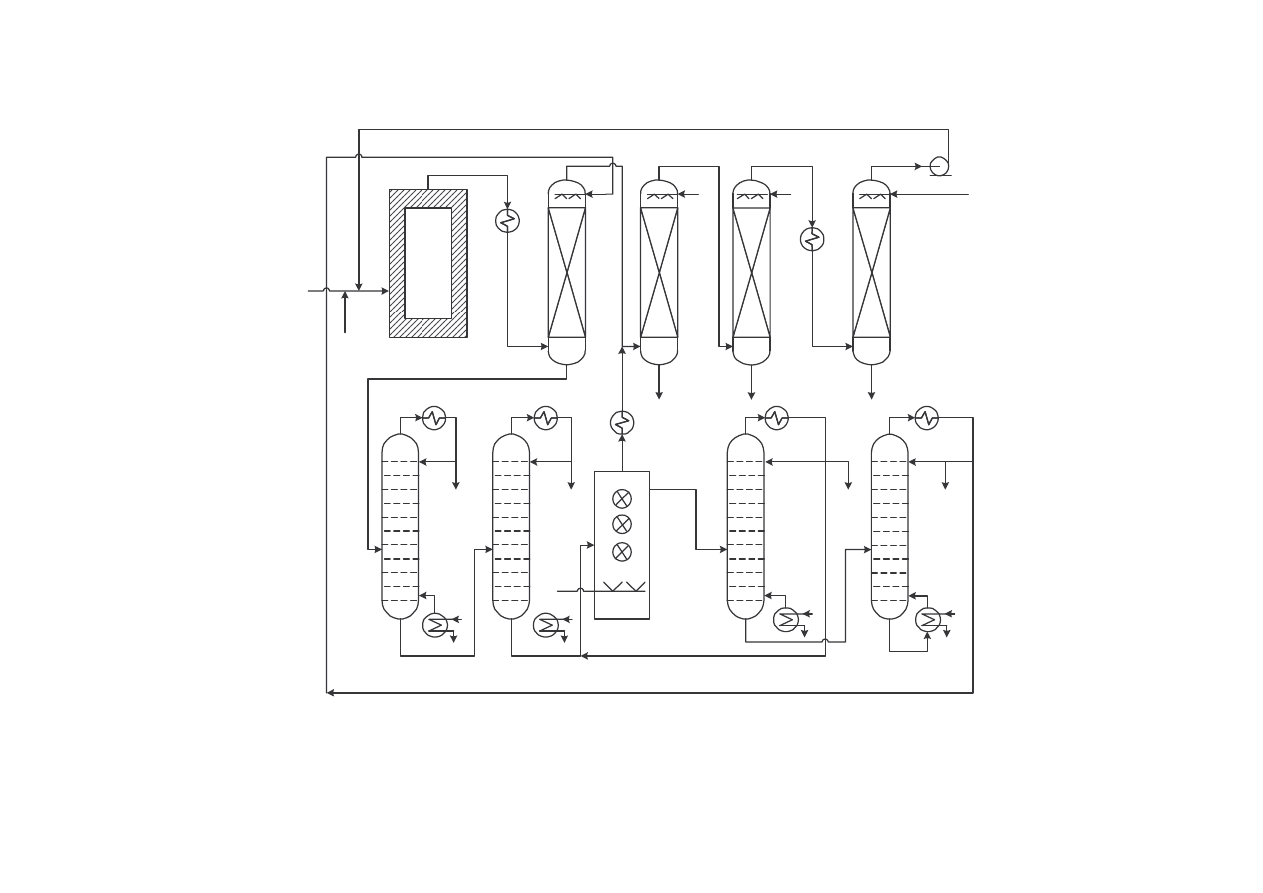
Schemat instalacji chlorowania metanu metod jednostopniow
Układ 4 kolumn
rektyfikacyjnych
odpady chloroorganiczne
powietrze
Cl
2
CH
4
1
2
3
4
H
2
O
NaOH
32% HCl
stê¿ony H
2
SO
4
5
6
5
7
8
9
CH
3
Cl
CH
2
Cl
2
CHCl
3
CCl
4
1 – reaktor (chlorator termiczny), 2 – chłodnica ociekowa, 3 – absorber HCl, 4 – absorber
alkaliczny (do absorpcji resztek HCl), 5 – chłodnice wodne, 6 – wie a susz ca, 7 – pompa, 8 –
zbiornik
24
Cl
2
CH
4
1
2
3
4
H
2
O
NaOH
32% HCl
st ony H
2
SO
4
2
5
CH
3
Cl
CH
2
Cl
2
CHCl
3
CCl
4
6
7
CH
4
recyrkulowany (+ CH
3
Cl)
r-r chlorowcopochodnych w CCl
4
8
9
10
Cl
2
CCl
4
obiegowy
11
12
2
1 – chlorator termiczny, 2 – chłodnice wodne, 3 - 3 – absorber HCl, 4 – absorber alkaliczny (do absorpcji resztek HCl), 5 –
chłodnice wodne, 6 – wie a susz ca, 7 – pompa, 8, 9, 11, 12 – kolumny rektyfikacyjne, 10 – chlorator fotochemiczny

Inne chloroalkany
Chlorowanie etanu metod termiczn
C
2
H
6
+ Cl
2
C
2
H
5
Cl + HCl
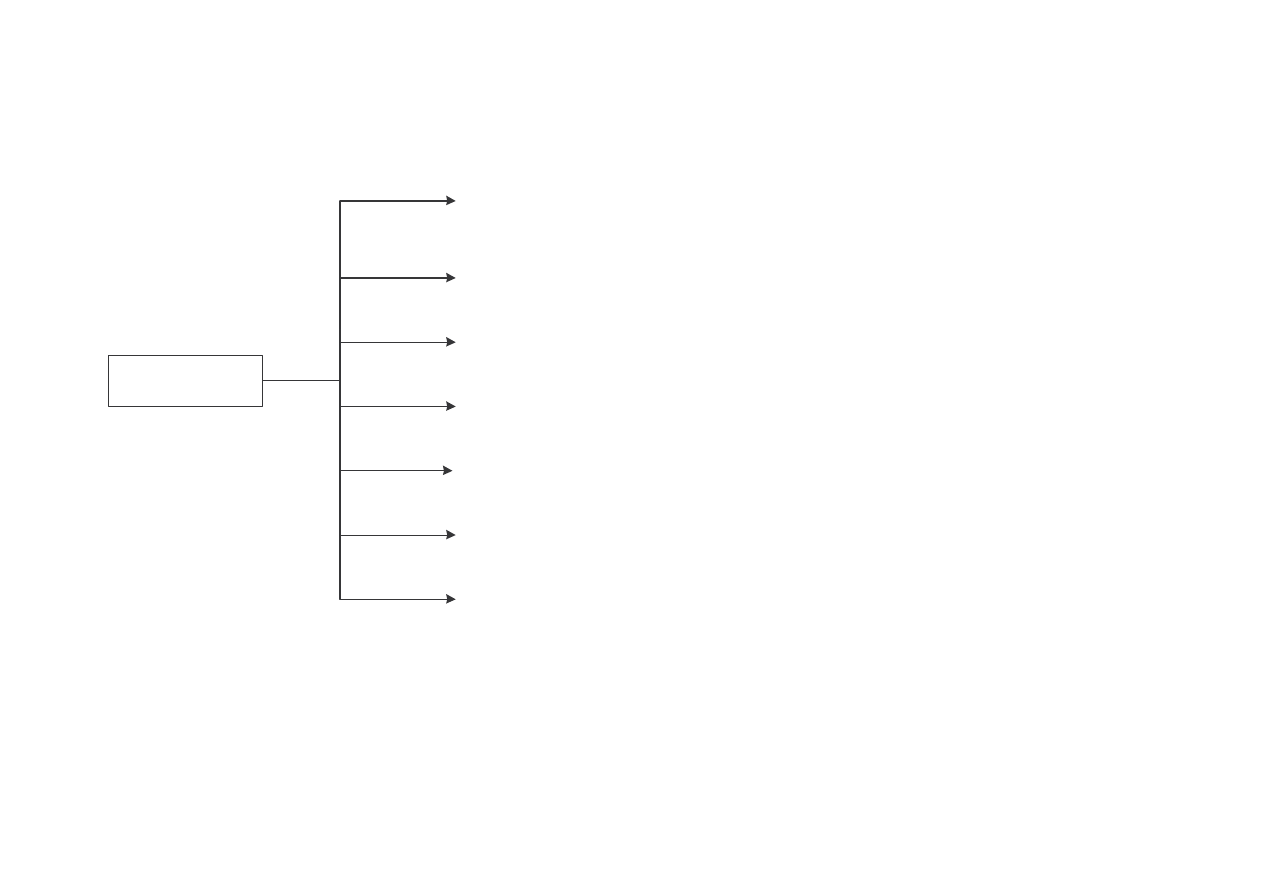
26
Zastosowanie chlorku etylu
C
2
H
5
Cl
etyloceluloza
merkaptan etylowy (do nawanniania gazu)
etyloaminy
tetraetyloołów (dodatek do paliw)
jako czynnik etyluj cy
w medycynie
czynnik chłodz cy w zakresie +5 - -5
o
C
celuloza
NaHS
NR
3
Pb Na stop
Etyloceluloza wykorzystywana jest do otrzymywania powłok antykorozyjnych, na
cz ci maszyn oraz izolacji kabli i przewodów. Surowiec lakierniczy do produkcji
lakierów nanoszonych na metale i drewno.

27
Chlorowanie pentanów
Chlorowania frakcji pentanowej z destylacji benzyny (mieszanina n-pentanu i
izomerów) prowadzi do mieszaniny chloropentanów (w tym monochloropentanów).
C
5
H
12
+ Cl
2
C
5
H
11
Cl + HCl
Hydroliza chlorków 10% wodnym r-rem NaOH, w temp. 180-200
o
C, pod ci nieniem 1
MPa prowadzi do mieszaniny alkoholi pentylowych
C
5
H
11
Cl + NaOH
C
5
H
11
OH + NaCl
Pentanole wykorzystuje si do otrzymywania technicznego octanu pentylu - wchodzi
w skład rozpuszczalnika stosowanego w przemy le lakierniczym do lakierów opartych
na estrach celulozy.

28
Chloroparafiny
Chloroparafinami nazywa si produkty chlorowania ciekłych i stałych mieszanin
(frakcji) w glowodorów n-parafinowych.
Chloroparafiny s nietoksyczne, nie rozpuszczalne w wodzie, natomiast dobrze
rozpuszczalne w olejach naftowych i wielu rozpuszczalnikach aromatycznych.

29
Chlorowanie frakcji w glowodorów n-parafinowych wydzielonych z nafty
prowadzone jest najcz ciej w celu otrzymania tzw.
chloroparafiny-13, zawieraj cej
12-15% wag. chloru.
Chloroparafiny-13 jest ona
czynnikiem alkiluj cym benzen w produkcji tzw.
kerylobenzenu (kerylobenzeny – produkty alkilowania benzenu alifatycznymi
w glowodorami naftowymi o długo ci ła cuchów od C
10
-C
14
) – półproduktu w
syntezie rodków powierzchniowo-czynnych typu alkiloarylosylfonianów.

30
Chloroparafiny ciekle, zawieraj od 40-49% Cl
2
i u ywa si jako dodatki
modyfikuj ce własno ci farb i lakierów oraz olejów smarowych, oraz do produkcji
plastyfikatorów (szczególnie poli(chlorku winylu).
Stałe chloroparafiny, zawieraj 70-72% Cl
2
i wykorzystuje si jako dodatki do mas
plastycznych i kauczuków w celu „uodpornienia” ich na działanie ognia, czyli
ognioodporne masy plastyczne.
Przykładowe warunki chlorowania
Chlorowanie ciekłych n-parafin (np. C
10
-C
18
) prowadzi si w sposób ci gły w
reaktorach kolumnowych, wprowadzaj c od dołu gazowy chlor (przeciwpr d).
Utrzymuje si temperatur ok. 100
o
C dzi ki cyrkulowaniu cz ci produktu.
31
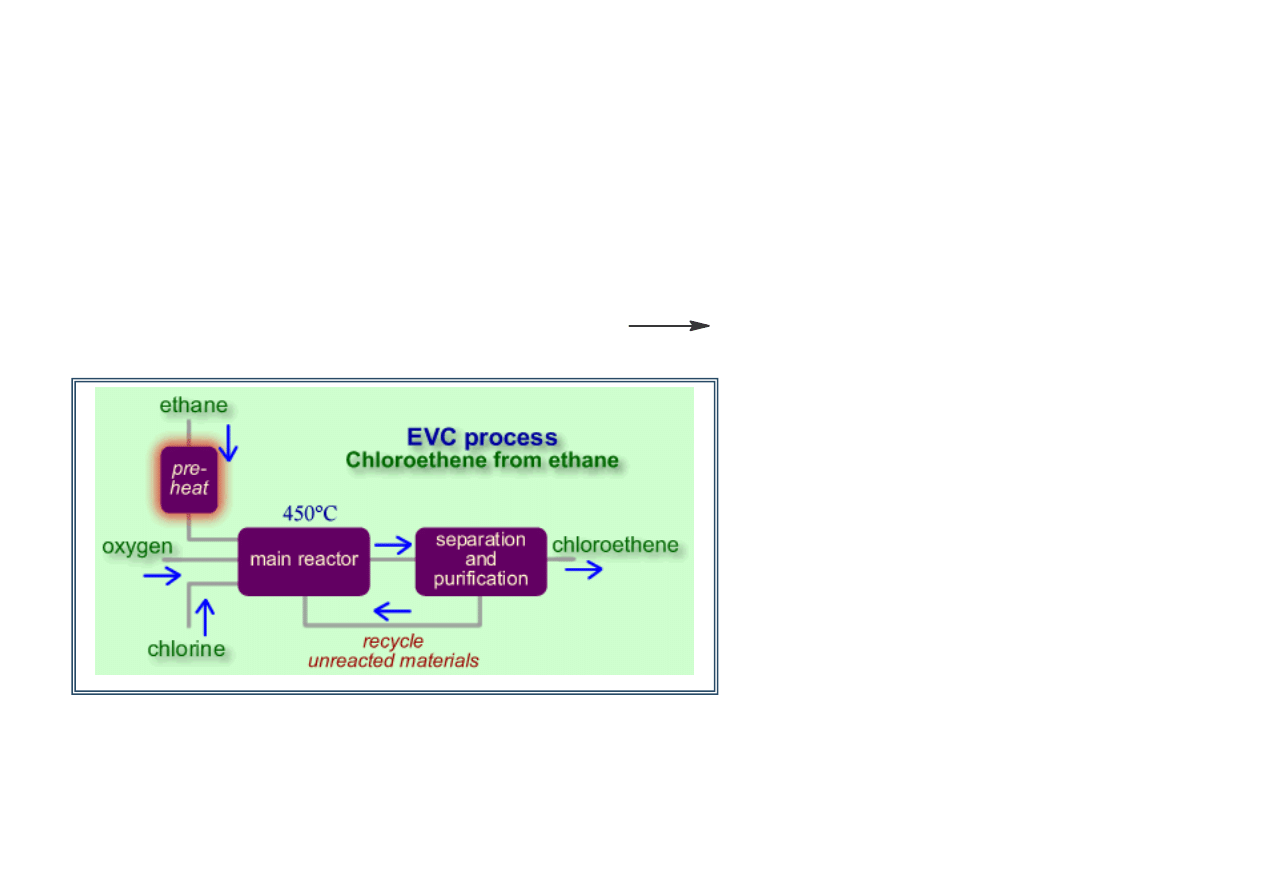
Oksychlorowanie etanu
Najnowszy proces otrzymywania chlorku winylu – EVC (European Winyls
Corporation) – uruchomiony w Wilhelmshaven w Niemczech
2 CH
3
-CH
3
+ Cl
2
+ 1.5 O
2
2 CH
2
=CHCl + H
2
O
Zalety procesu:
1.
Proces jest ok. 20% ta szy ni
tradycyjne oksychlorowanie
etylenu
2.
Unika si tworzenia
kancerogennych produktów
po rednich
3.
Mniejsze zu ycie energii

32
Instalacja chlorku winylu w Wilhelmshaven w Niemczech

33
C
HLOROWANIE OLEFIN
Chlorowanie etylenu do 1,2-dichloroetanu
1,2-Dichloroetan (EDC) jest bezbarwn , trudno paln ciecz o temperaturze
wrzenia 84
o
C. Dobrze rozpuszcza oleje, tłuszcze, asfalty, ywice, bitumy i
kauczuki.
Warianty chlorowania etylenu:
•
reakcja z chlorem (starsza metoda),
•
oksychlorowanie (nowsza metoda).
34
Addycja chloru do etylenu
CH
2
=CH
2
+ Cl
2
CH
2
Cl-CH
2
Cl
∆H<0 (-180 kJ/mol)
Aktywacja chloru katalizatorem Lewis’a
kat
+ Cl Cl
:
:
..
..
..
..
:
:
..
..
..
..
Cl
Cl
kat

35
Warunki reakcji:
faza ciekła,
reaktor barbota owy,
katalizator -
FeCl
3
, ZnCl
2
lub SbCl
3
,
temperatura - 40-70
o
C, ci nienie - 0,4-0,5 MPa (wariant niskotemperaturowy),
lub 120-130
o
C (wariant wysokotemperaturowy),
Selektywno tworzenia 1,2-dichloroetanu - 98% w przeliczeniu na etylen i 99%
w przeliczeniu na chlor .
Chlorowanie etylenu mo na przeprowadza równie w fazie gazowej w temperaturze
90-130
o
C. Wówczas tworzenie EDC ma charakter rodnikowy;
36
Oksychlorowanie etylenu
CH
2
=CH
2
+ 2 HCl + 0.5 O
2
ClCH
2
-CH
2
Cl + H
2
O
∆H<0 (-234 kJ/mol)
Etap reakcji
CH
2
=CH
2
+ 2 CuCl
2
ClCH
2
-CH
2
Cl + Cu
2
Cl
2
Etap regeneracji
Cu
2
Cl
2
+ 0.5 O
2
CuO
.
CuCl
2
CuO
.
CuCl
2
+ 2 HCl
2 CuCl
2
+ H
2
O

37
Warunki procesu:
faza gazowa,
temperatura - 220-240
o
C,
ci nienie - 0,2-0,4 MPa,
reaktor z fluidalnym zło em katalizatora,
ciepło odbierane za pomoc w ownic "zanurzonych" w warstwie fluidalnej,
przy 94-97% konwersji etylenu i 95-97% konwersji HCl, selektywno tworzenia
1,2-dichloroetanu dochodzi do 97%. (Na stacjonarnym katalizatorze 93-97%
konwersja etylenu i 94-95% HCl, selektywno tworzenia EDC 94%).
Produkty uboczne - chlorek winylu, chlorek etylu, 1,1-dichloroetan, chlorek
winylidenu, cis- i trans-1,2-dichloroetyleny, trichloroetylen, chloral i wysokowrz ce
składniki.
Do firm, które jako pierwsze przeprowadziły technicznie proces oksychlorowania
nale ały Gododrich, Dow i Monsanto (w USA w 1964 r.).

38
Dehydrochlorowanie 1,2-dichloroetanu do chlorku winylu
Alkaliczne:
CH
2
Cl-CH
2
Cl + NaOH
CH
2
=CHCl + NaCl + H
2
O
Nie ma adnego znaczenia przemysłowego!
Termiczne:
∆H>0 (71 kJ/mol)
CH
2
Cl-CH
2
Cl
CH
2
=CHCl + HCl
∆
Dow Chemical, Ethyl, B.F. Goodrich, Hoechst, ICI, Mitsui Toatsu, Monsanto, Stauffer.
39
Mechanizm reakcji:
CH
2
Cl-CH
2
Cl
CH
2
Cl-CH
2
+ Cl
.
.
CH
2
Cl-CH
2
Cl + Cl
.
.
CH
2
Cl-CHCl + HCl
CH
2
=CHCl + Cl
.
.
CH
2
Cl-CHCl
CH
2
=CHCl + HCl
.
.
CH
2
Cl-CH
2
+ Cl

40
Warunki dehydrochlorowania:
reaktor rurowy
Temperatura - 400-600
o
C (preferowana 500-550
o
C),
Ci nienie - 0,1-4 MPa.
redni czas przebywania reagentów w reaktorze - 10-20 s.
Konwersja EDC - 50-60%; 98% selektywno ci.
41
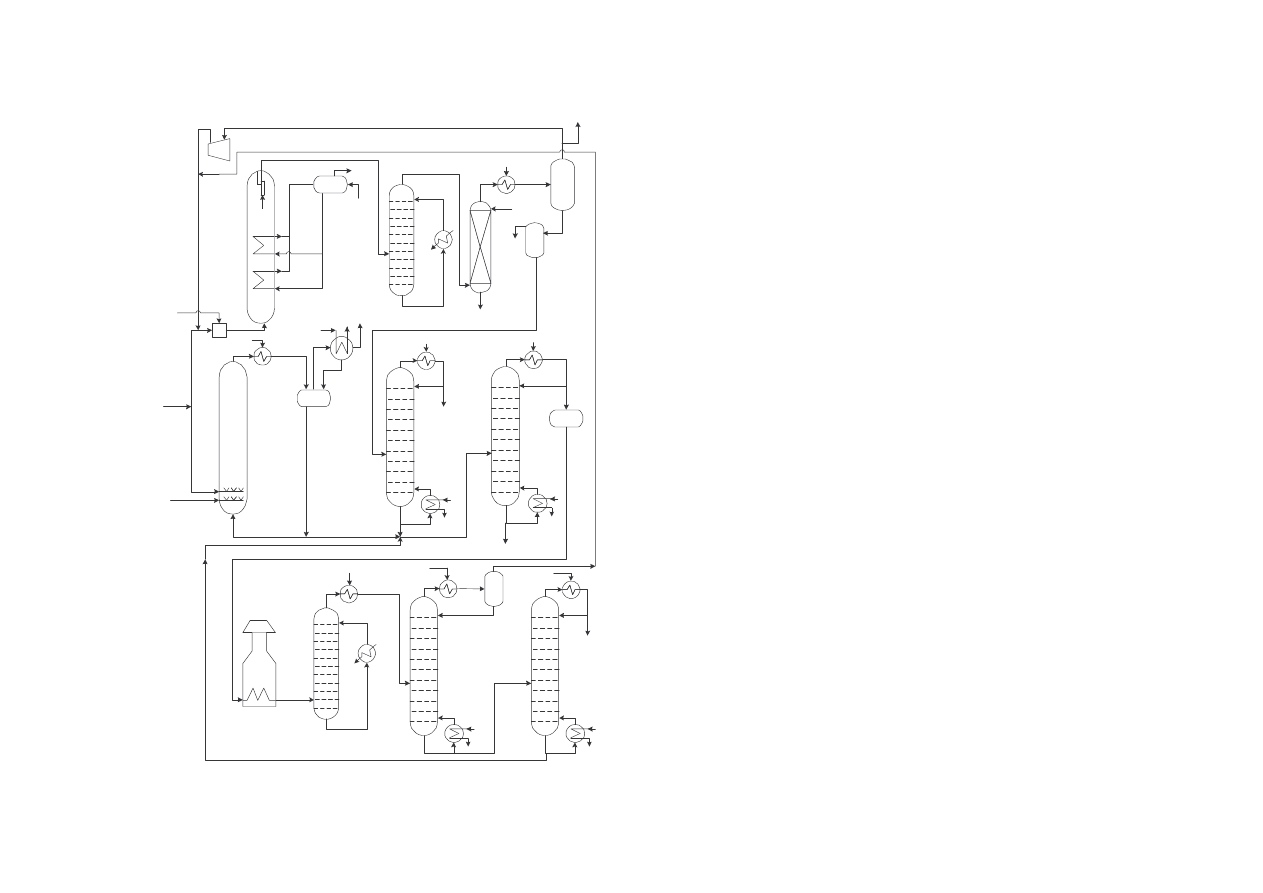
Zbilansowane chlorowanie i oksychlorowanie etylenu do chlorku winylu
CH
2
=CH
2
+ Cl
2
CH
2
Cl-CH
2
Cl
2 CH
2
Cl-CH
2
Cl
2 CH
2
=CHCl + 2 HCl
∆
CH
2
=CH
2
+ 2 HCl + 0.5 O
2
ClCH
2
-CH
2
Cl + H
2
O
Sumarycznie:
2 CH
2
=CH
2
+ Cl
2
+ 0.5 O
2
2 CH
2
=CHCl + H
2
O
42
1
2
3
4
5
6
7
10
8
gazy odlotowe
H
2
O
H
2
O
NaOH
Para
HCl
H
2
O
9
Tlen
7
13
H
2
O
Solanka
H
2
O
H
2
O
7
7
Etylen
Chlor
11
12
14
A
16
Para
Para
B
EDC + woda
15
EDC
17
18
19
21 chlorek winylu
H
2
O
7
7
7
H
2
O
20
5
Para
Para
EDC
EDC
C
2
H
4
+ O
2
H
2
O
22
22
22
22
1 - mieszalnik, 2 - reaktor
oksychlorowania etylenu, 3 - zbiornik
para-kondensat, 4, 18 - chłodnice
kolumnowe, 5 - wymienniki ciepła, 6 -
absorber, 7 - skraplacze, 8, 13, 20 -
separatory, 9 - spr arka, 10 -
oddzielacz, 11 - reaktor chlorowania
etylenu, 12 - chłodnica solankowa, 14,
15, 19, 21 - kolumny rektyfikacyjne, 16
- zbiornik EDC, 17 - piec rurowy, 22 -
kotły parowe.
A - niskowrz ce produkty uboczne
(chloroform,
tetrachlorometan,
chlorobutadien, 1,1-dichloroetan i inne)
oraz woda, B - wysokowrz ce produkty
uboczne - pozostało chloroorganiczna
(ok. 35% 1,1,2-trichloroetanu, ok. 15%
cis- i trans-1,3-dichlorobutylenów, ok.
15% 1,1,2,2-tetrachloroetanu i in.).
43
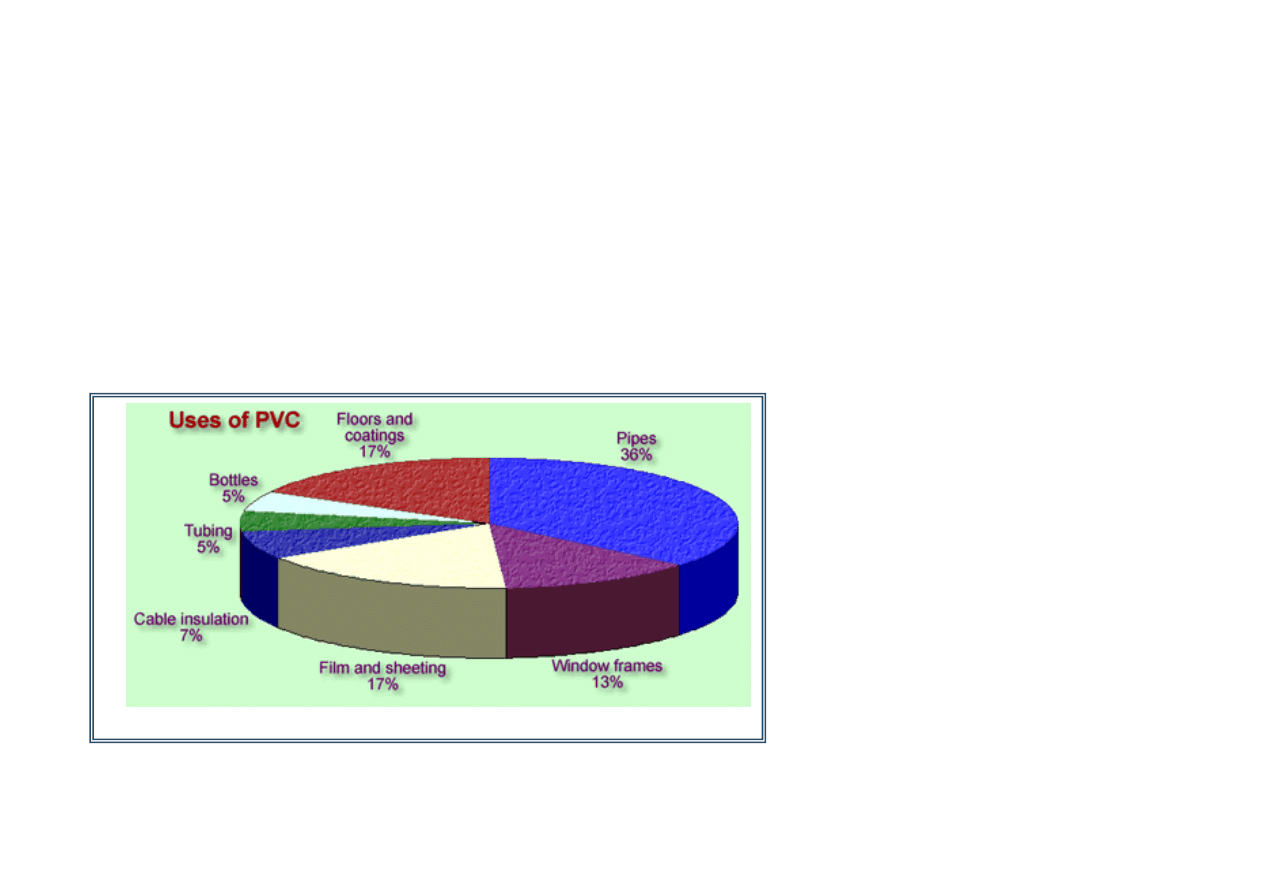
Zastosowanie chlorku winylu
wiatowa produkcja chlorku winylu w 1996 r. wynosiła 22 mln t.
Najwi kszymi producentami w Ameryce Płn. s firmy Dow Chemical i Geon, w
Europie Zachodniej – EVC International i Solvay; za w Japonii – firmy Tosoh i
Kaneka.
Chlorek winylu jest wyko-
rzystywany (99% produkcji)
jako monomer lub komonomer
do polimeryzacji. Najwa niej-
sze znaczenie techniczne znaj-
duje polimeryzacja chlorku wi-
nylu do poli(chlorku winylu).

44

45
Chlorowanie propylenu – chlorek allilu
Chlorek allilu jest bezbarwn , łatwopaln ciecz o charakterystycznym, ostrym
zapachu, o temperaturze wrzenia 45
o
C. Jest wchłaniany do organizmu przez
skór , układ oddechowy i pokarmowy. Wykazuje działanie narkotyczne.
Powoduje podra nienia luzówek, skóry. Przez skór wchłania si szybko,
powoduj c poparzenia.
46
Otrzymywanie chlorku allilu
CH
3
CH=CH
2
+ Cl
2
CH
2
=CHCH
2
Cl + HCl
Reakcja uboczna:
CH
3
CH=CH
2
+ Cl
2
CH
3
CH-CH
2
Cl
Cl
47
Mechanizm reakcji:
Cl
2
2 Cl
.
Cl
.
+ CH
3
CH=CH
2
.
CH
2
CH=CH + HCl
Cl
.
+ ClCH
2
CH=CH
2
Cl
2
+
.
CH
2
CH=CH
2
Warunki reakcji:
Temperatura - > 350
o
C (ok. 500
o
C)
Surowiec - 95% propylen, dobrze oczyszczony od propanu i innych
w glowodorów,
5-6 moli cz steczek propylenu na 1 mol cz steczek chloru,
Wydajno chlorku allilu - 80%.
Produkty uboczne - 1,2-dichloropropan, 2-chloropropen, i 1,3-dichloropropen.
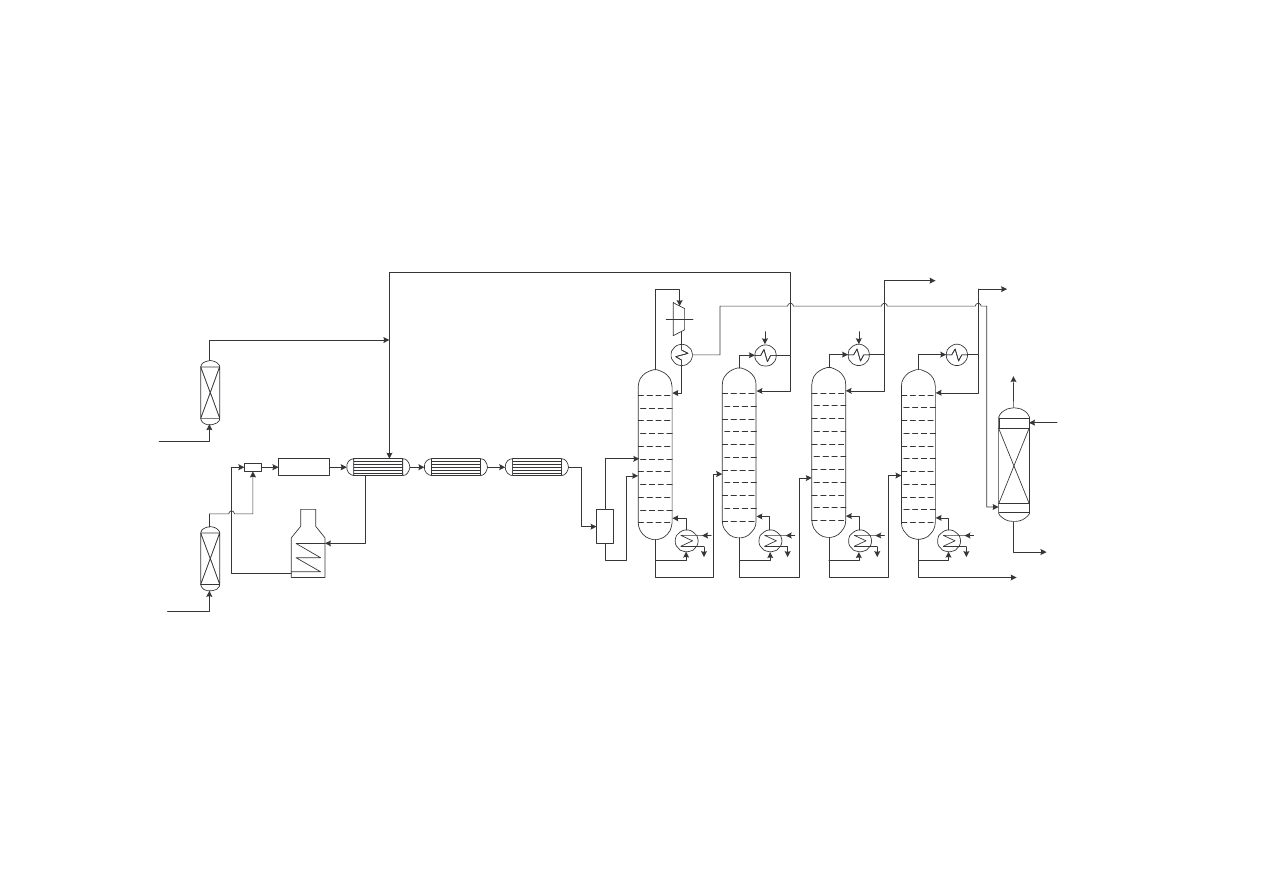
48
Uproszczony schemat instalacji produkuj cej chlorek allilu według technologii
opracowanej w Zakładach Chemicznych „Organika-Zachem” w Bydgoszczy
H
2
O
1
1
2
3
4
4
4
propylen
chlor
5
6
7
8
9
10
H
2
O
11
12
woda
chlorek allilu
frakcja lekka
frakcja ci ka
1 - adsorbery, 2 - mieszalnik, 3 - chlorator, 4 - przeponowe wymienniki ciepła, 5 - piec
rurowy, 6 - zbiornik, 7 - spr arka, 8-11 - kolumny rektyfikacyjne, 12 – absorber

49
Zastosowanie Chlorku Allilu
do produkcji epichlorohydryny,
alkoholu allilowego.
Innymi wa nymi pochodnymi chlorku allilu s : skrobia allilowa, ftalan diallilu,
tiozynoamina, silikony allilowe i alletryna (allilopiretyna), a tak e izotiocyjanianu
allilu (sztuczny olej gorczyczny).
Chlorek allilu polimeryzuje w obecno ci katalizatorów typu Friedla-Craftsa, tworz c
polimery wykorzystywane do impregnacji papieru i drewna oraz jako kleje, smary i
lakiery.

50
Produkcja chlorku allilu w Polsce
Chlorek allilu produkowany jest przez Zakłady Chemiczne „Zachem” w Bydgoszczy,
jako produkt po redni w syntezie epichlorohydryny.
Wyszukiwarka
Podobne podstrony:
05 Majid 5744 Nieznany (2)
cw PAiTS 05 id 122324 Nieznany
2015 04 09 08 25 05 01id 28644 Nieznany (2)
NAI2006 05 id 313056 Nieznany
05 Spoinyid 5835 Nieznany
matma dyskretna 05 id 287941 Nieznany
cwiczenie 05 id 125057 Nieznany
05 Wykonywanie, odczytywanie i Nieznany
05 Occhid 5768 Nieznany (2)
714[01] Z1 05 Malowanie farba e Nieznany
05 TSid 5852 Nieznany (2)
05 Wodaid 5865 Nieznany (2)
pp test odp zima 05 air boratyn Nieznany
lab pwsp 05 id 258618 Nieznany
Zestaw 05 id 587909 Nieznany
05 5id 5463 Nieznany (2)
2009 10 05 praid 26669 Nieznany
26429 05 id 31506 Nieznany
05 procesyid 5808 Nieznany (2)
więcej podobnych podstron