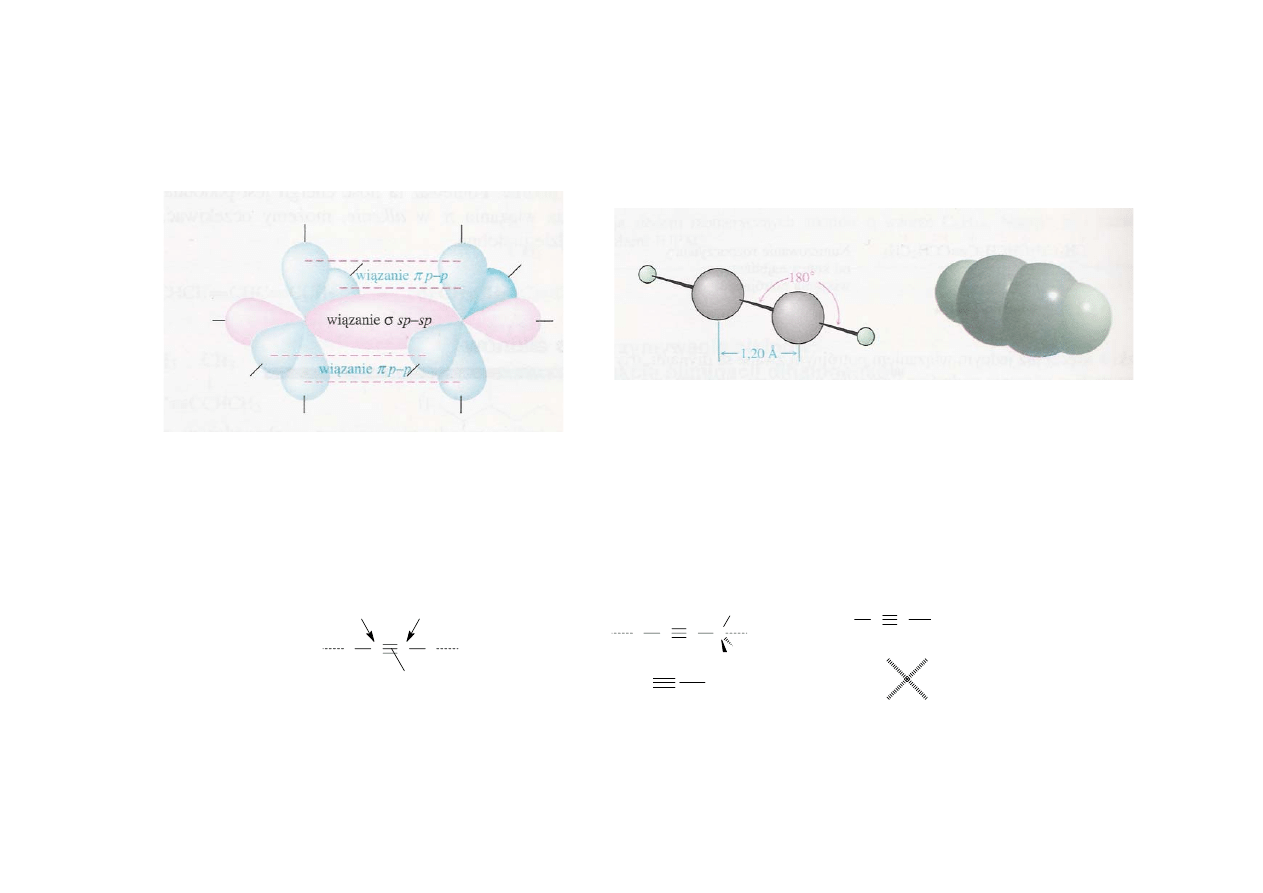
Alkiny
Budowa najprostszych alkinów
π
π
σ
C
C
H
H
sp
sp
wszystkie atomy
w jednej linii
systematycznie: etyn
zwyczajowo: acetylen (t. wrz. -82
o
C)
a)
b)
C
C
C
H
H
H H
propyn (t. wrz. -23
o
C)
c)
C
C
H
grupa etynylowa
nie: acetylenowa
.
.
czyli:
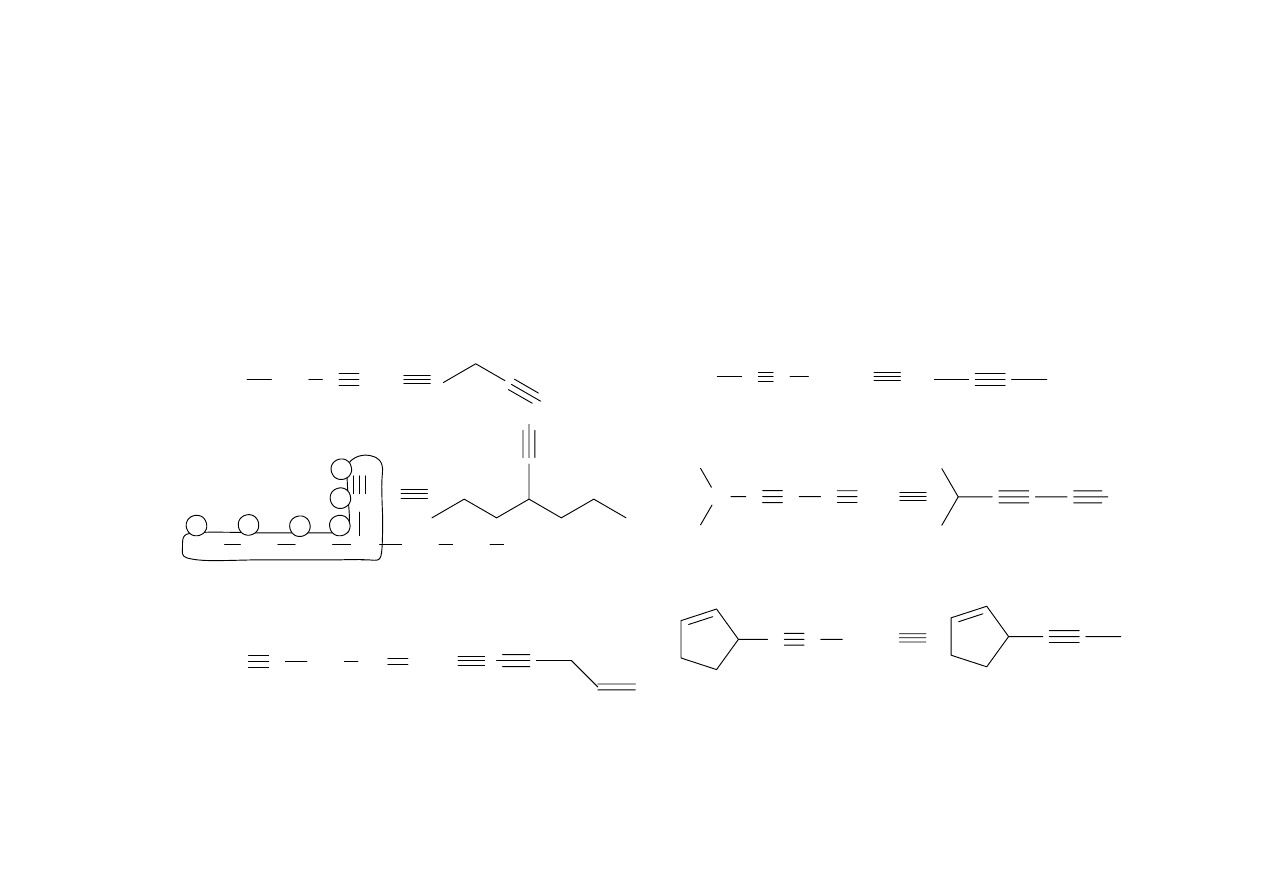
Nazewnictwo alkinów
Końcówką charakterystyczną nazw alkenów, sygnalizującą obecność
w związku wiązania podwójnego, jest "-yn" lub, po spółgłoskach:
g
, k, l, "-in".
a) CH
3
CH
2
C
CH
.
1
2
3
4
but-1-yn
b)
CH
3
CH
2
CH
2
CH
C
CH
2
CH
2
CH
3
CH
.
1
2
3
4
6
5
c)
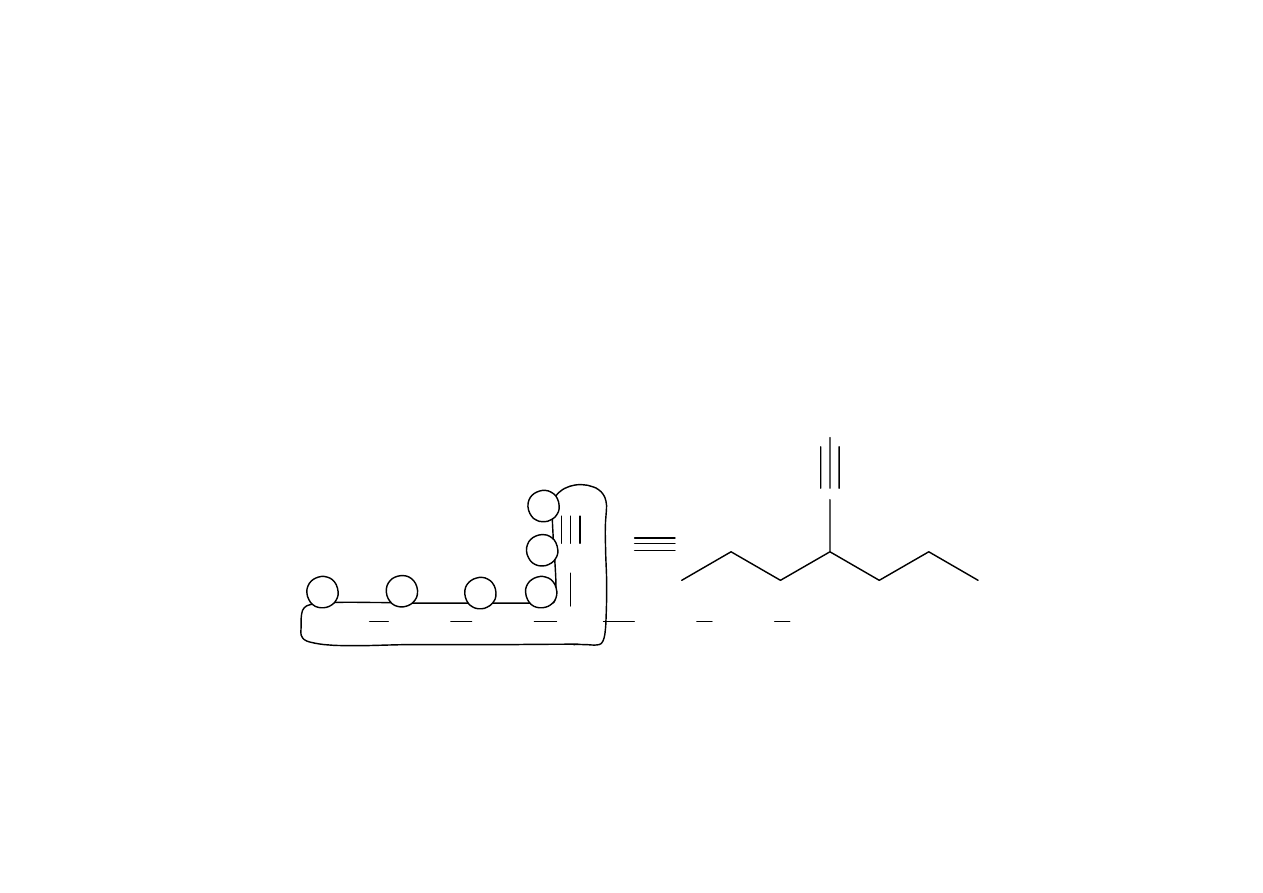
3-propyloheks-1-yn
CH C
Cl
Cl
C
C
CH
4
3
2
1
5
Cl
.
.
.
Cl
5,5-dichloropenta-1,3-diyn
d)
CH
C
CH
2
CH
CH
2
.
pent-1-en-4-yn
5
1
2
3
4
e)
C
C
CH
3
.
.
3-(prop-1-ynylo)cyklopenten
but-2-yn
4
3
2
1
CH
3
C C CH
3
f)
.
.
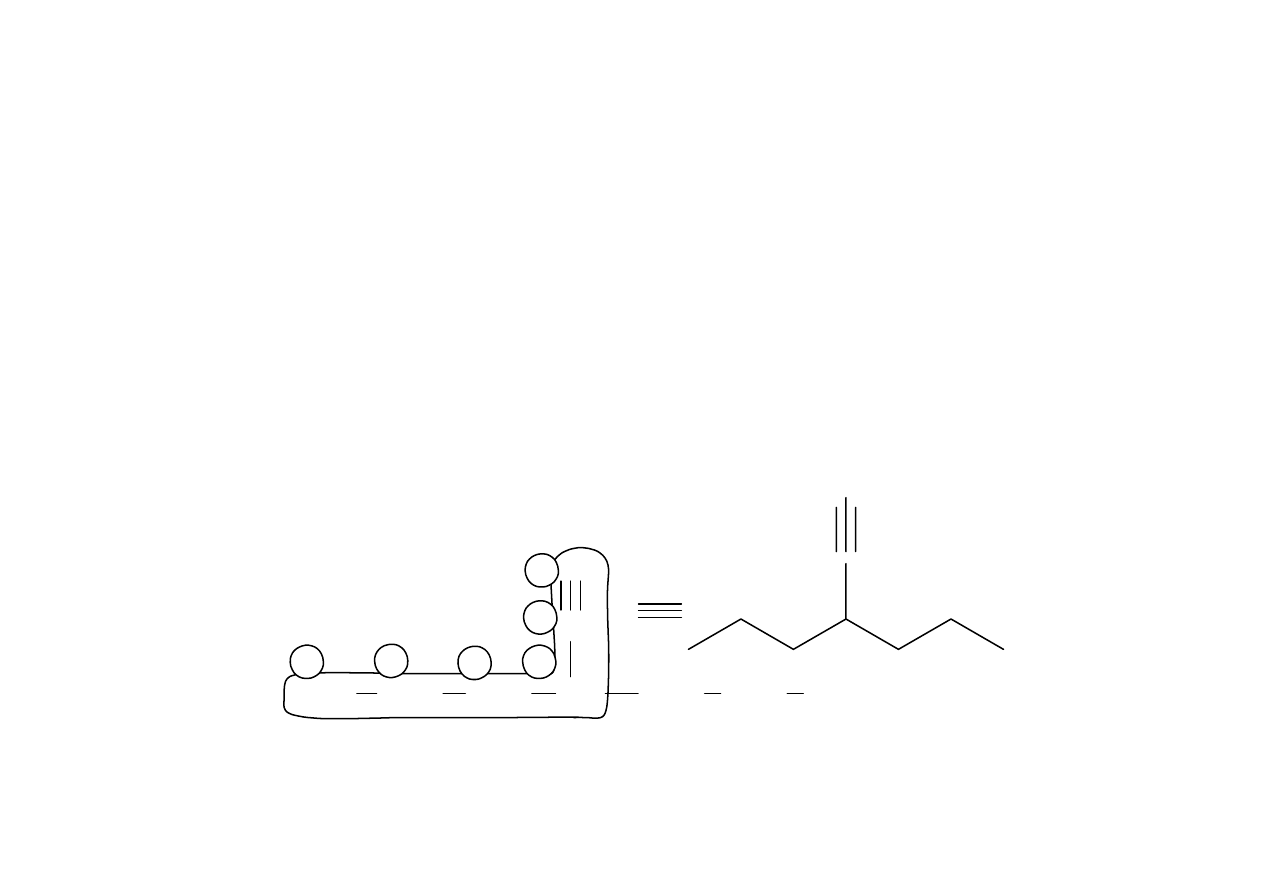
Nazewnictwo alkinów
Utworzenie nazwy łańcuchowego alkinu o jednym wiązaniu wielokrotnym
(potrójnym) obejmuje kolejno:
1) Wybór łańcucha głównego, czyli najdłuższego łańcucha zawierający wiązanie
potrójne. Głównym łańcuchem w związku jest zatem sześciowęglowy
łańcuch z wiązaniem podwójnym, a nie łańcuch nasycony o siedmiu
atomach węgla.
CH
3
CH
2
CH
2
CH
C
CH
2
CH
2
CH
3
CH
.
1
2
3
4
6
5
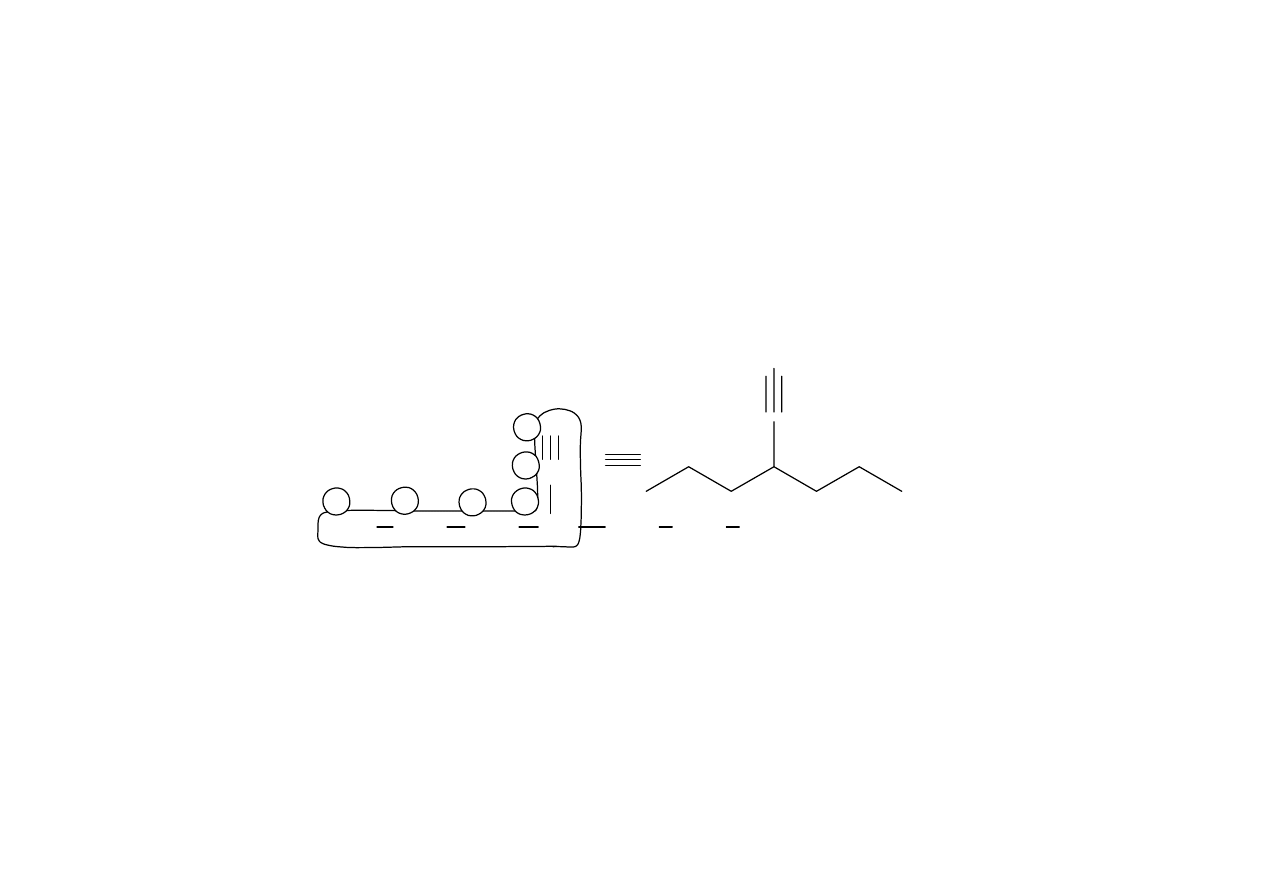
Nazewnictwo alkinów
2) Ponumerowanie atomów węgla w łańcuchu głównym numeruje
zaczynając od końca łańcucha bliższego wiązania potrójnego. Gdy
wiązanie znajduje się w równej odległości od obu końców, należy
wybrać taką numerację, aby podstawniki miały jak najniższe lokanty.
3) Określenie położenia wiązania potrójnego przez podanie numeru atomu
węgla przy którym "rozpoczyna" się wiązanie potrójne. Numer ten
podaje się jako liczbę (lokant) pomiędzy rdzeniem (określającym liczbę
atomów głównym łańcuchu, np. prop-, but-, heks-) a końcówką -yn (lub
-in) i oddziela poziomymi kreskami od reszty nazwy Związki a i b to
odpowiednio but-1-yn i but-2-yn, a związek d należy nazwać jako
pochodną heks-1-ynu.
CH
3
CH
2
CH
2
CH
C
CH
2
CH
2
CH
3
CH
.
1
2
3
4
6
5
Nazewnictwo alkinów
4) Uporządkowanie w kolejności alfabetycznej nazw wszystkich grup
znajdujących się przy głównym łańcuchu. Nazwy poprzedza się
lokantami i, ewentualnie, przedrostkami zwielokrotniającymi w
przypadku dwóch lub więcej identycznych grup, podobnie jak miało to
miejsce przy nazywaniu alkanów i alkenów.
CH
3
CH
2
CH
2
CH
C
CH
2
CH
2
CH
3
CH
.
1
2
3
4
6
5
3-propyloheks-1-yn
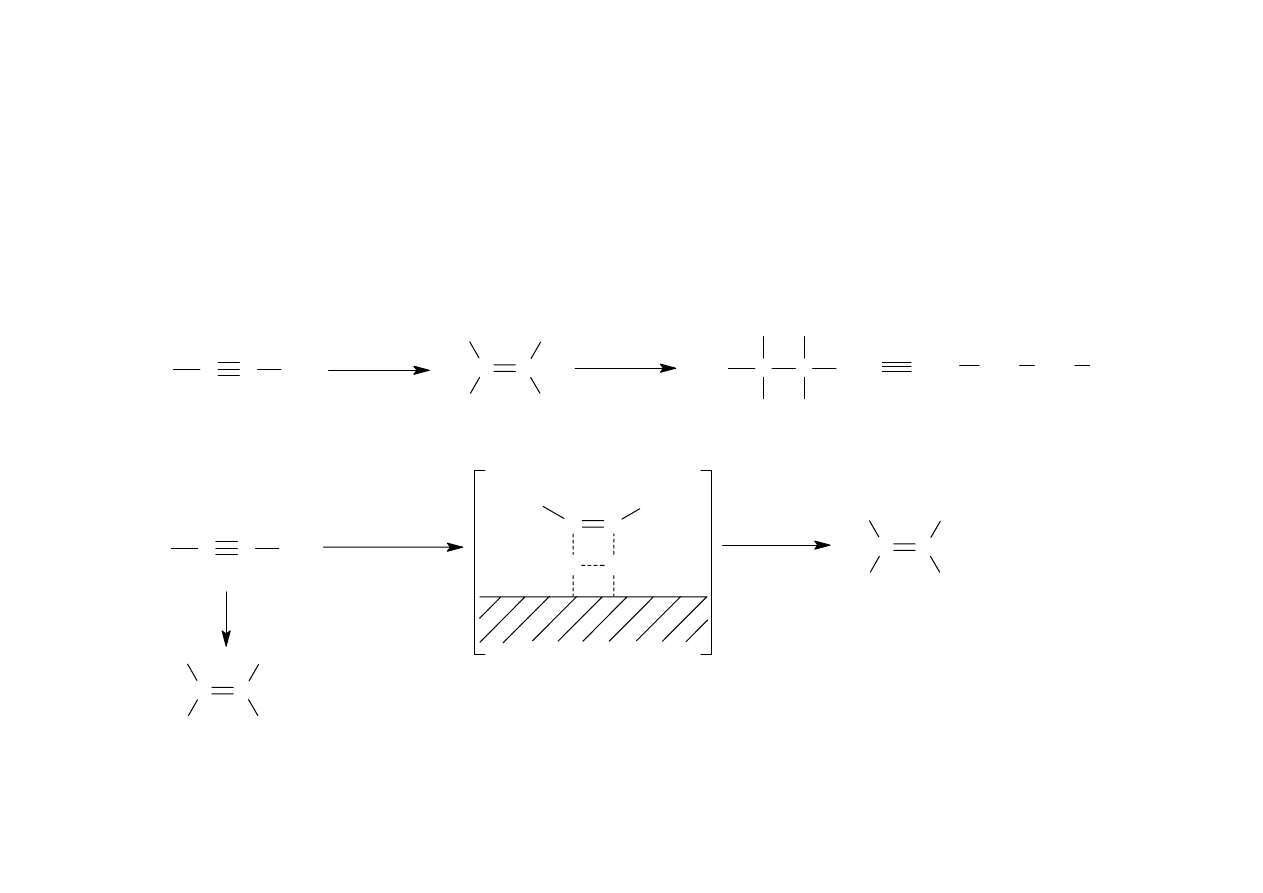
Reakcje alkinów
Uwodornienie katalityczne
C
C
CH
3
CH
3
H
2
/ Pt
C
C
CH
3
H
CH
3
H
H
2
/ Pt
C
C
CH
3
H
H
CH
3
H
H
CH
3
CH
2
CH
2
CH
3
but-2-yn
(Z)-but-2-en
butan
całkowite uwodornienie
C
C
CH
3
CH
3
katalizator
C
C
CH
3
CH
3
H
H
H
2
katalizator
Lindlara
C
C
CH
3
H
CH
3
H
(Z)-but-2-en
TYLKO IZOMER Z !
a)
b)
C
C
H
CH
3
CH
3
H
Li / NH
3
(E)-but-2-en
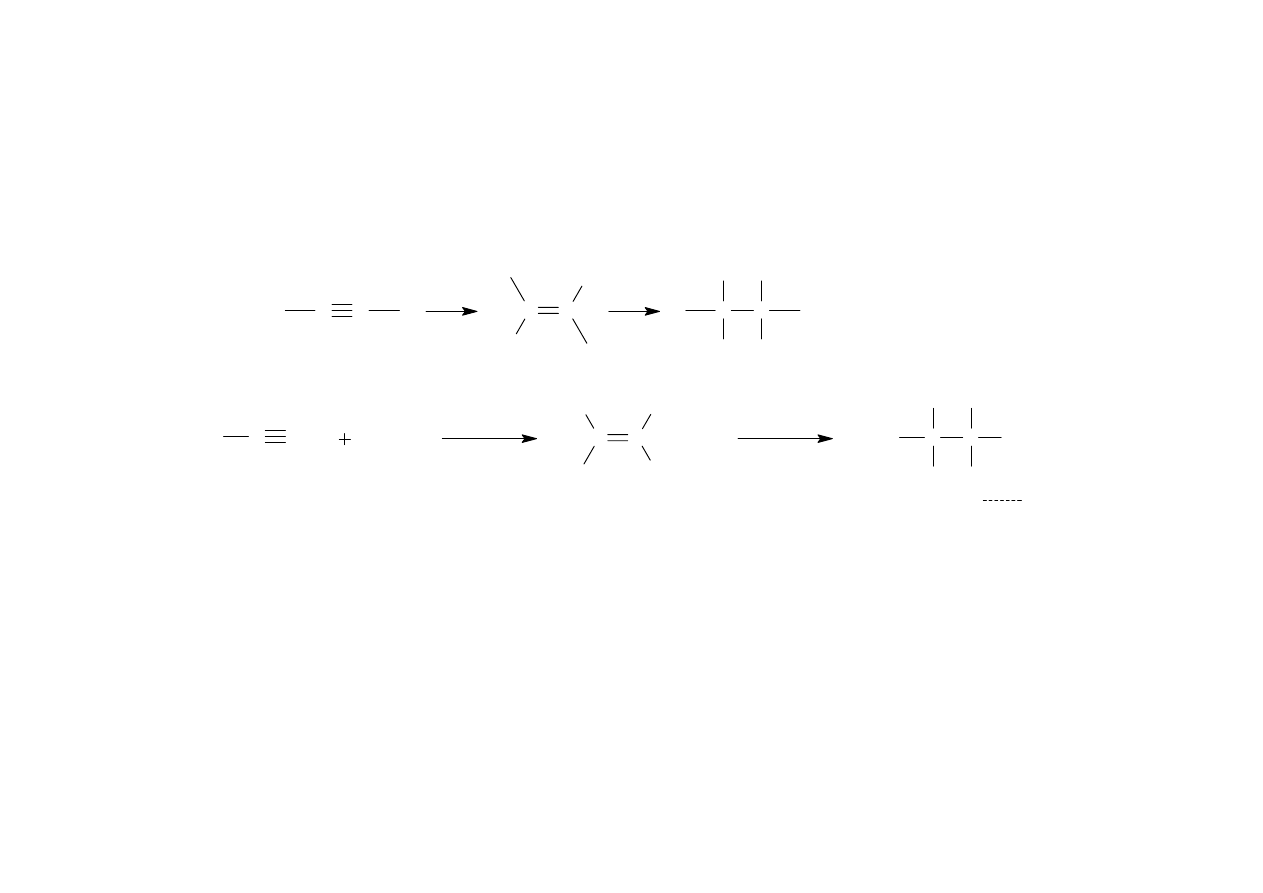
Reakcje alkinów
Addycja halogenów
Alkiny łatwo reagują z chlorem i bromem dając odpowiednie produkty
addycji. W trakcie reakcji ulega rozerwaniu najpierw jedno z wiązań
π i
do sąsiednich atomów węgla przyłączają się atomy halogenu.
Ponieważ addycja chloru i bromu zachodzi w sposób anti, powstaje
alken, podstawiony atomami halogenu po przeciwnych stronach
wiązania podwójnego - zazwyczaj jest to izomer E. Addycja kolejnej
cząsteczki halogenu do wiązania podwójnego prowadzi do
odpowiedniego tetrabromo- lub tetrachloroalkanu
propyn
np.
C
CH
CH
3
Br
2
(E)-1,2-dibromopropen
1,1,2,2-tetrabromopropan
C
C
CH
3
Br
Br
H
Br
Br
X = Cl, Br
C
C
X
2
C
C
X
X
C
C
X
X
X
X
X
2
C
C
Br
H
CH
3
Br
Br
2

Reakcje alkinów
Addycja halogenowodorów
1) Proces addycji przebiega podobnie jak w przypadku alkenów, z orientacją zgodną z
regułą Markownikowa: atom wodoru łączy się z tym atomem węgla, który w
cząsteczce alkinu posiadał więcej atomów atomów wodoru.
2) Reakcja addycji halogenowodorów nie jest procesem stereoselektywnym - powstaje
mieszanina halogeneków winylu o konfiguracji Z oraz E. Na wzorach strukturalnych
fakt ten odnotowuje się rysując dwa wiązania przy winylowym atomie węgla przy
pomocy linii falistych.
3) Orientacja addycji drugiej cząsteczki H-X jest analogiczna jak pierwszej - atom
halogenu łączy się z tym atomem węgla, który w cząsteczce halogenku winylu był już
podstawiony chlorem, bromem lub jodem. W konsekwencji produktem addycji jest
związek, który posiada dwa atomy halogenu przy jednym atomie węgla, czyli tak
zwany dihalogenek geminalny.
4) Alkiny reagują z halogenowodorami wolniej niż alkeny.
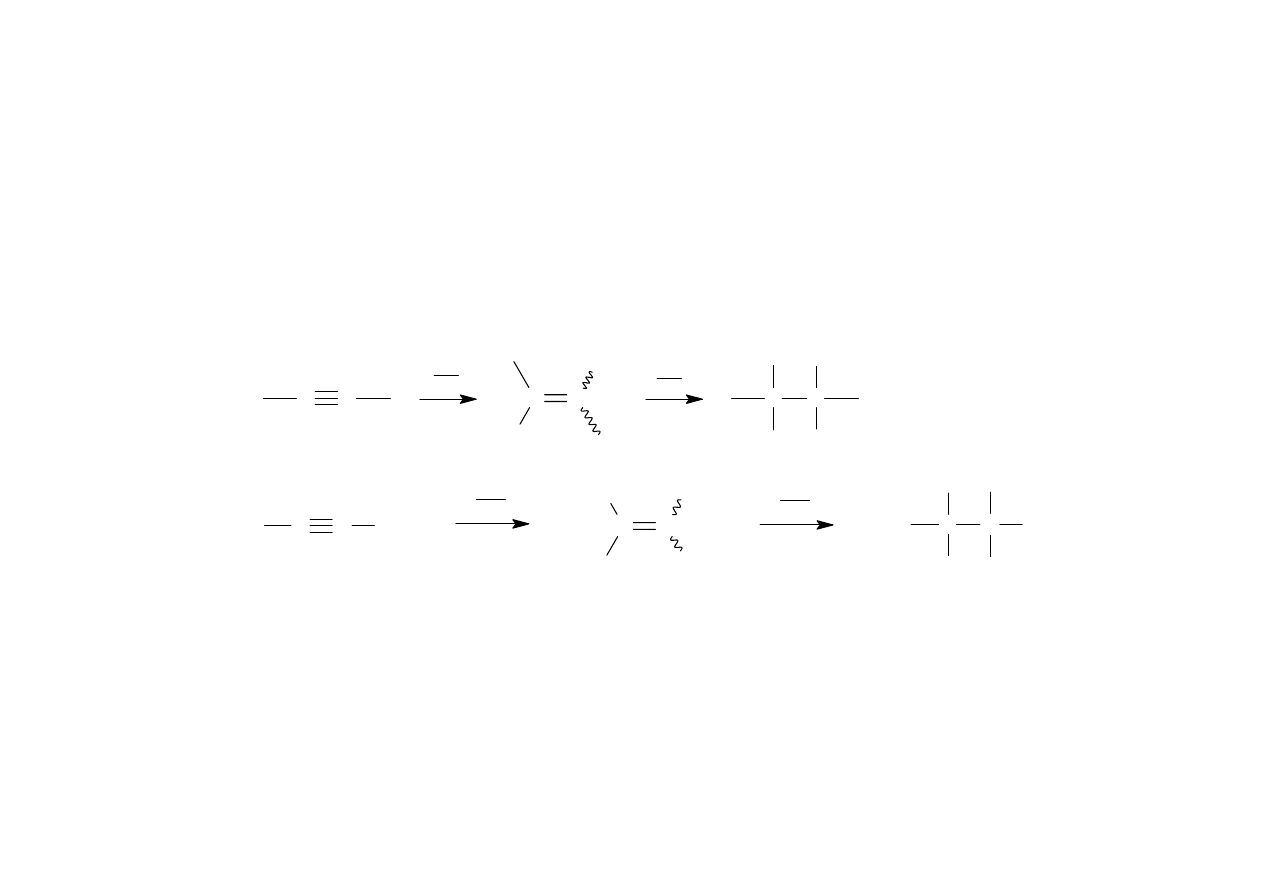
Reakcje alkinów
Addycja halogenowodorów do alkinów
C
C
CH
3
I
I
H
H
CH
3
C
C
CH
3
CH
3
H
I
C
C
X
X
H
H
C
C
H
X
C
C
X = Cl, Br, I
H
X
H
X
H
I
C
C
CH
3
I
CH
3
H
but-2-yn
2-jodobut-2-en
(mieszanina izomerów Z i E)
2,2-dijodobutan
Reakcje alkinów
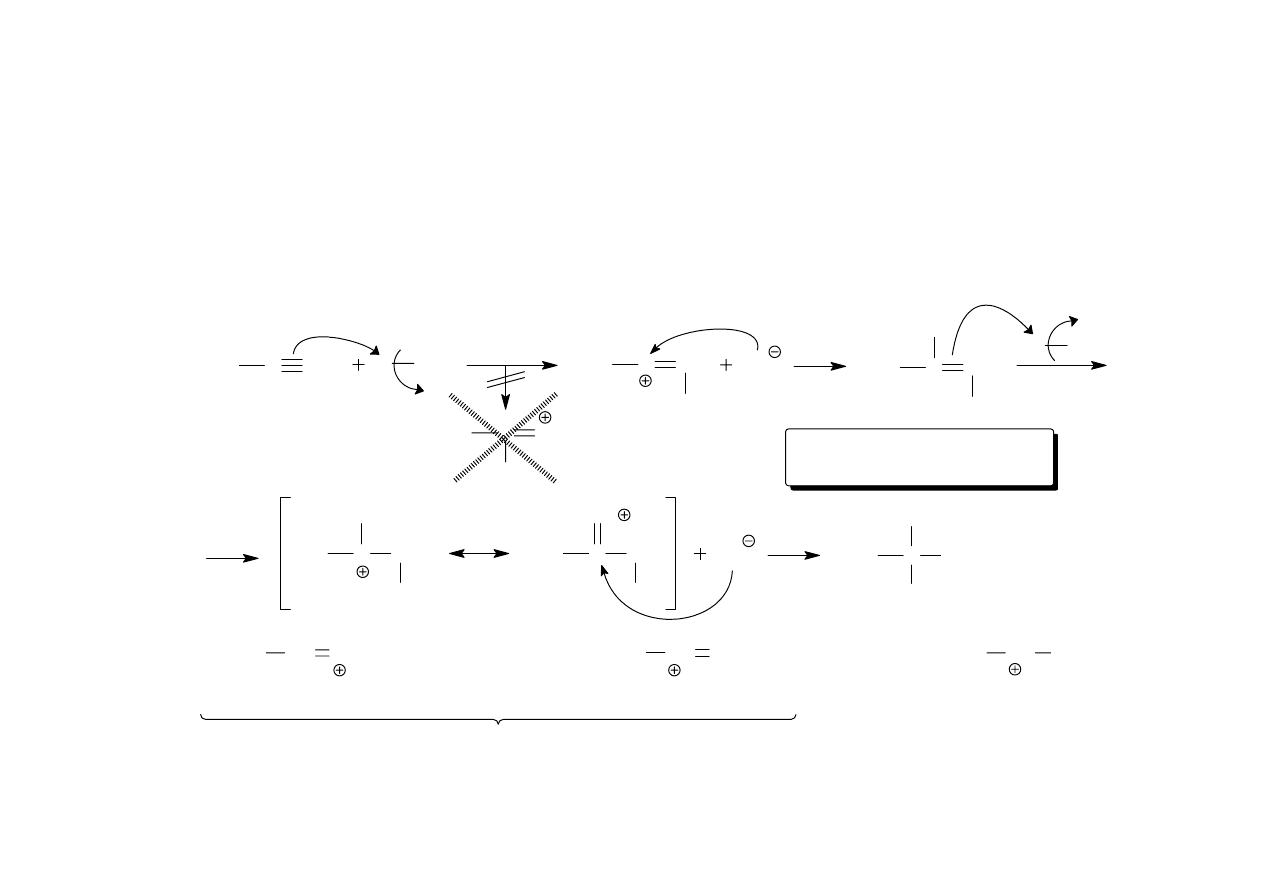
Addycja halogenowodorów do alkinów
c)
CH CH
CH
3
mniej trwały niż
mniej trwały niż
CH CH
2
CH
3
CH CH
3
CH
3
ładunek na atomie 2
o
kationy winylowe - bardzo nietrwałe , powstają powoli!
C
CH
2
CH
3
H
Cl
l l
l
ładunek na atomie 1
o
l
l
C
CH
2
CH
3
H
Cl
Cl
l ll
l
C
CH
3
CH
3
Cl
Cl
2,2-dichloropropan
I
II
orientacja addycji zgodna
z regułą Markownikowa !
mechanizm przykładowej addycji:
C
CH
CH
3
H
C
CH
CH
3
propyn
l
ll
H
Cl
l
l l
lCl
C
CH
CH
3
H
nie powstaje!
2-chloropropen
H
Clll
l
C
CH
CH
3
H
Cl
l l
l
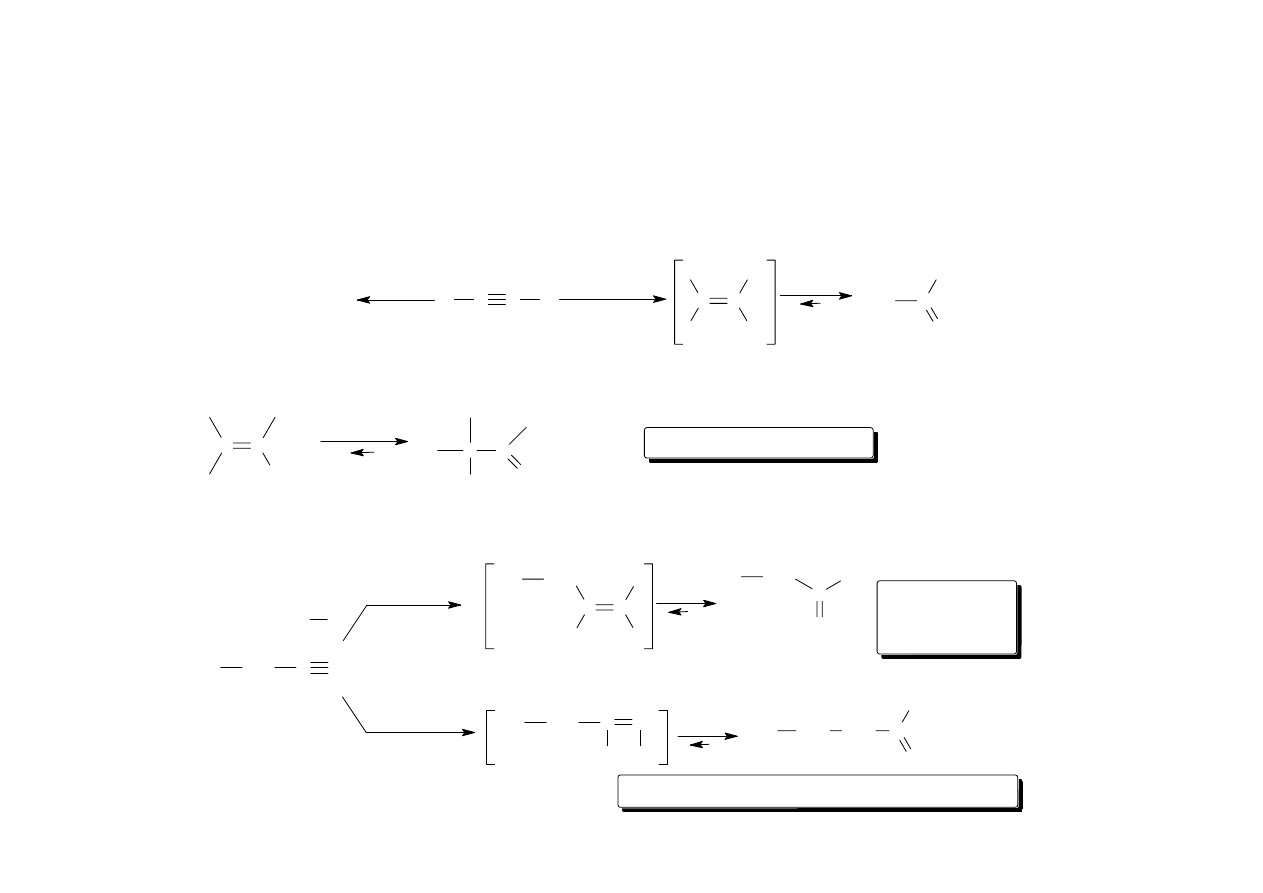
Reakcje alkinów
Addycja wody - tautomeria keto-enolowa
a)
reakcja nie zachodzi
bez obecności
katalizatora rtęciowego
C
C
H
H
H
2
O, H
+
H
2
O
kat. H
2
SO
4
,
HgSO
4
C
C
H
H
H
OH
alkohol winylowy,
nietrwały !
CH
3
C
H
O
aldehyd octowy
(etanal)
b)
C
C
OH
C
H
C
O
forma enolowa
forma ketonowa
(lub aldehydowa)
położenie stanu równowagi całkowicie
przesunięte w prawo (w stronę ketonu lub aldehydu)
c)
C
CH
CH
2
CH
3
H
+ HO
kat. H
+
, Hg
++
C
C
CH
2
HO
H
H
CH
3
CH
2
C
CH
3
O
CH
3
produkt addycji
zgodnej z regułą
Markownikowa
enol
keton
butan-2-on
tautomeria keto-enolowa
1. (BH
3
)
2
2. H
2
O
2
, OH
-
C
CH
CH
2
CH
3
OH
H
enol
CH
2
C
CH
2
CH
3
H
O
aldehyd: butanal
produkt addycji niezgodnej z regułą Markownikowa
Reakcje alkinów
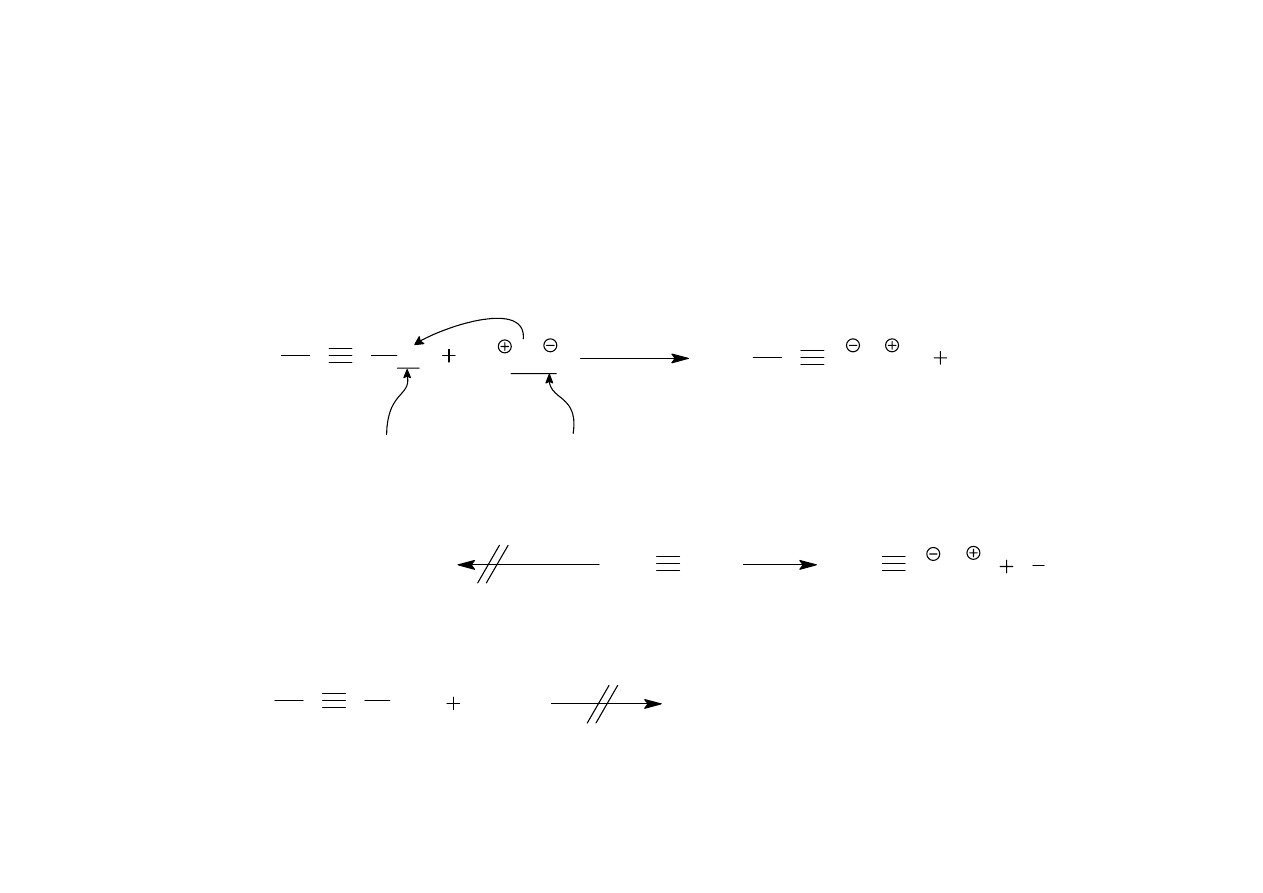
Alkiny jako słabe kwasy
HC
C Na
C
C Na
CH
3
a)
C
C
H
CH
3
alkin terminalny: bardzo słaby kwas
Na NH
2
ll
kwasowy
atom wodoru
bardzo mocna
zasada
NH
3
propynid sodu
(sól sodowa propynu)
propyn
amidek
sodu
b)
HC
CH
etyn
(acetylen)
NaOH
Na
reakcja nie zachodzi
(za słaba zasada)
1
2
H
2
etynid sodu
(acetylenek sodu)
c)
C
C
CH
3
CH
3
NaNH
2
reakcja nie zachodzi, w alkinie
brak kwasowych atomów wodoru
but-2-yn
l
l
l
pK
a
= ok. 25
pK
a
= ok. 34
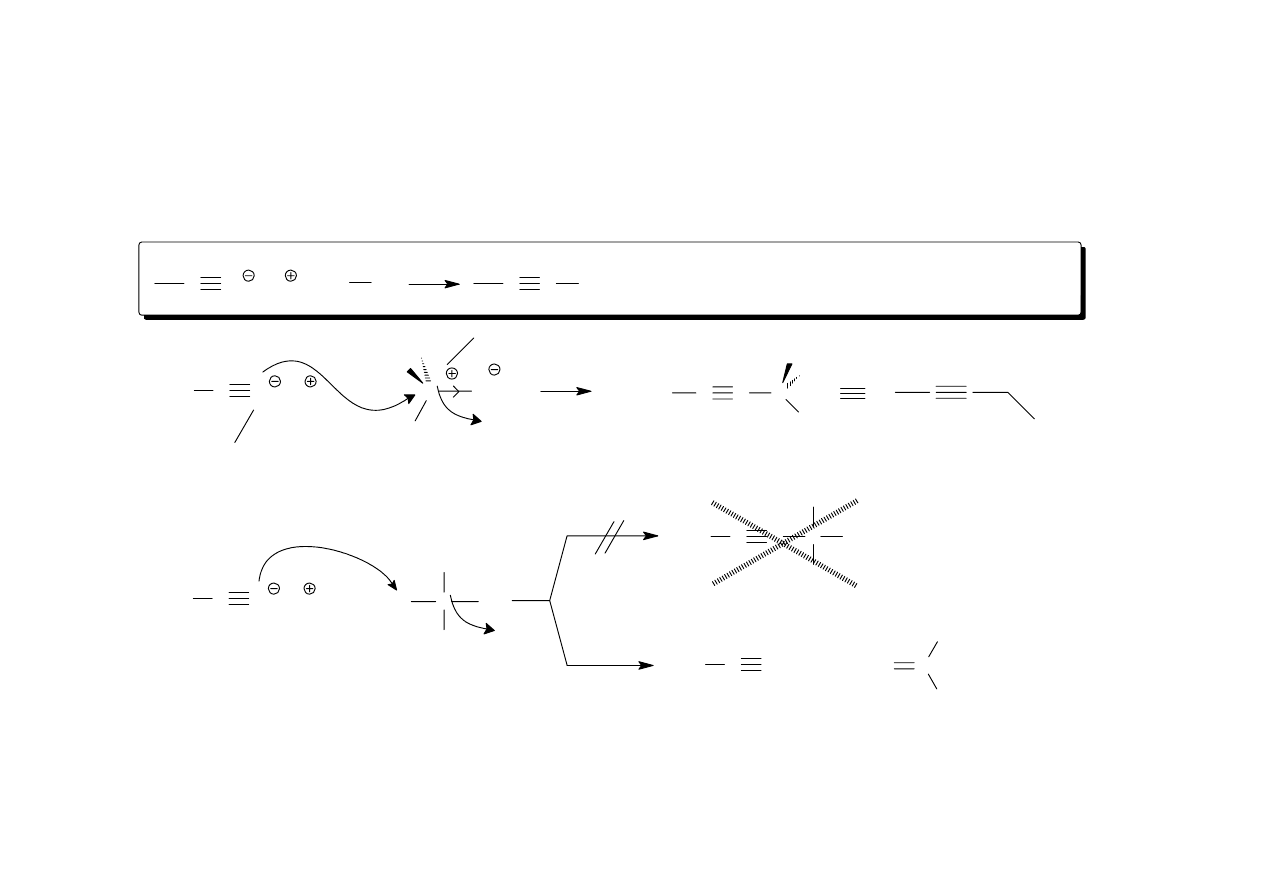
Reakcje alkinów
Wydłużanie łańcucha węglowego alkinów
a)
C
C
R
R
X
+
C
C
l
Na
+ NaX
X = Cl, Br, I
R - grupa alkilowa, musi być 1
o
lub CH
3
!
C
C Na
CH
3
l
+
C
Br
CH
3
H
H
δ
δ
atom nukleofilowy
atom elektrofilowy
C
C
CH
3
C
CH
3
H
H
.
.
- NaBr
pent-2-yn
l
C
C Na
CH
3
b)
+
CH
3
C
CH
3
CH
3
I
C
C
CH
3
C
CH
3
CH
3
CH
3
4,4-dimetylopent-2-yn
C
CH
CH
3
+
C
H
2
C
CH
3
CH
3
+ NaI
2-metylopropen
(produkt eliminacji jodowodoru z jodku tert-butylu)
propyn
2-jodo-2-metylopropan
(jodek tert-butylu)
sól sodowa propynu
(propynid sodu)
np.
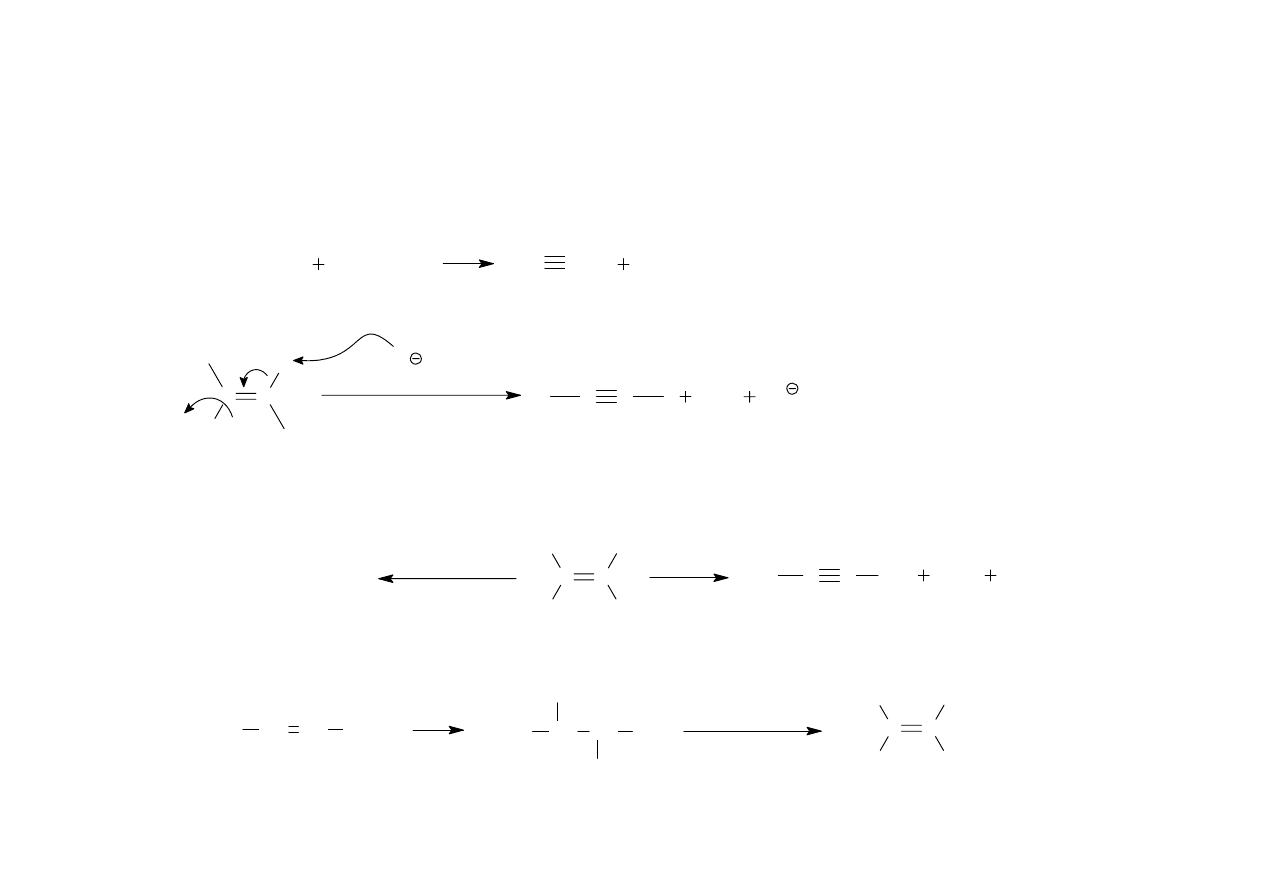
Reakcje alkinów
Laboratoryjne metody otrzymywanie alkinów
a)
CaC
2
2 H
2
O
HC
CH
Ca(OH)
2
węglik wapnia
(karbid)
b)
C
C
X
H
bardzo mocna zasada
Z
halogenek winylu - niereaktywny
C
C
HZ
X
np. :
C
C
CH
3
H
Br
CH
3
NaNH
2
KOH / etanol
C
C
CH
3
CH
3
NH
3
NaBr
reakcja nie zachodzi!
KOH jest za słabą
zasadą, by oderwać
HBr od atomów C
sp
2
l
X = Cl, Br, I
acetylen
(etyn)
2-bromobut-2-en
but-2-yn
2-bromobut-2-en
C
C
CH
3
H
Br
CH
3
c)
CH CH
CH
3
CH
3
Br
2
CH CH
CH
3
CH
3
Br
Br
KOH / etanol
-KBr, - H
2
O
but-2-en
2,3-dibromobutan
Document Outline
- Alkiny
- Nazewnictwo alkinów
- Nazewnictwo alkinów
- Nazewnictwo alkinów
- Nazewnictwo alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
- Reakcje alkinów
Wyszukiwarka
Podobne podstrony:
Wyk 02 Pneumatyczne elementy
02 OperowanieDanymiid 3913 ppt
02 Boża radość Ne MSZA ŚWIĘTAid 3583 ppt
OC 02
PD W1 Wprowadzenie do PD(2010 10 02) 1 1
02 Pojęcie i podziały prawaid 3482 ppt
WYKŁAD 02 SterowCyfrowe
02 filtracja
02 poniedziałek
21 02 2014 Wykład 1 Sala
Genetyka 2[1] 02
02 czujniki, systematyka, zastosowania
auksologia 13 02 2010
02 MAKROEKONOMIA(2)id 3669 ppt
więcej podobnych podstron