
Obróbka
cieplno-chemiczna

Obróbka cieplno-chemiczna
Obróbka cieplno-chemiczna jest dziedzina obróbki
cieplnej obejmującą zespół operacji umożliwiających zmianę
składu chemicznego i struktury warstwy powierzchniowej
stopów w wyniku zmian temperatury i chemicznego
oddziaływania środowiska.
Obróbka cieplno-chemiczna polega na zamierzonej
dyfuzyjnej
zmianie
składu
chemicznego
warstwy
powierzchniowej elementów metalowych w celu uzyskania
odpowiednich właściwości użytkowych.
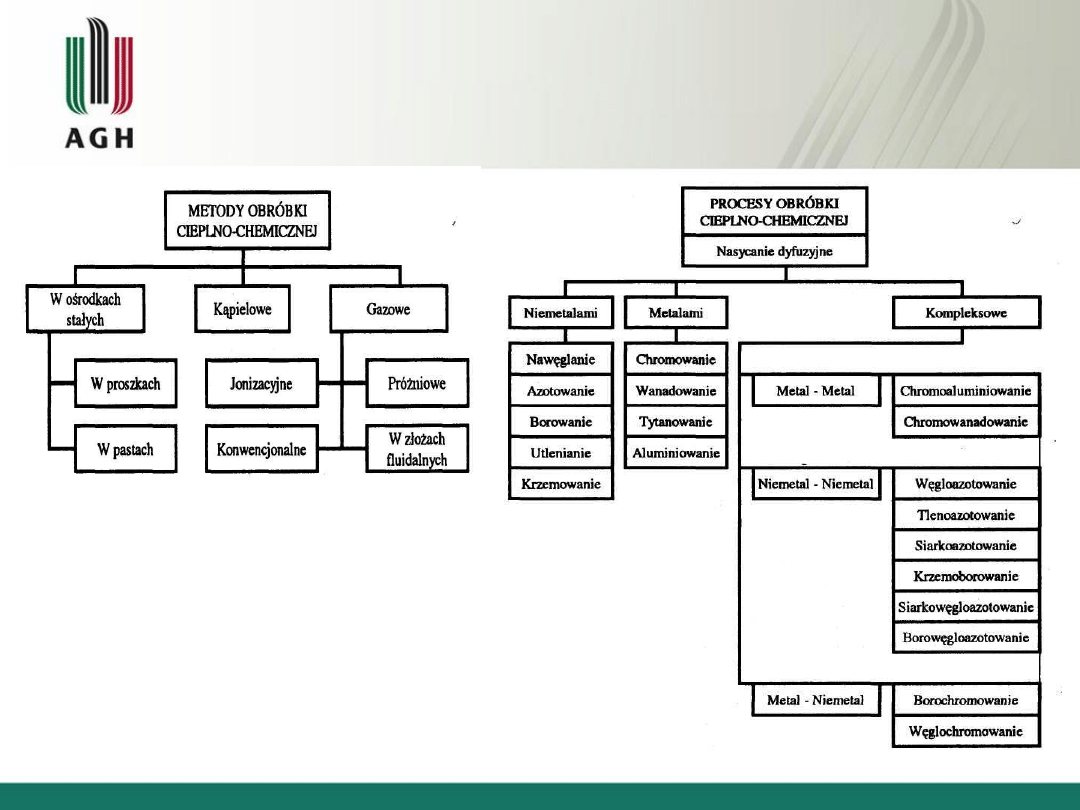
Rodzaje obróbki cieplno-chemicznej
Rodzaje obróbki cieplno-chemicznej ze
względu na stan ośrodka nasycającego
Klasyfikacja metod obróbki cieplno-chemicznej ze względu na
rodzaj dyfundującego pierwiastka
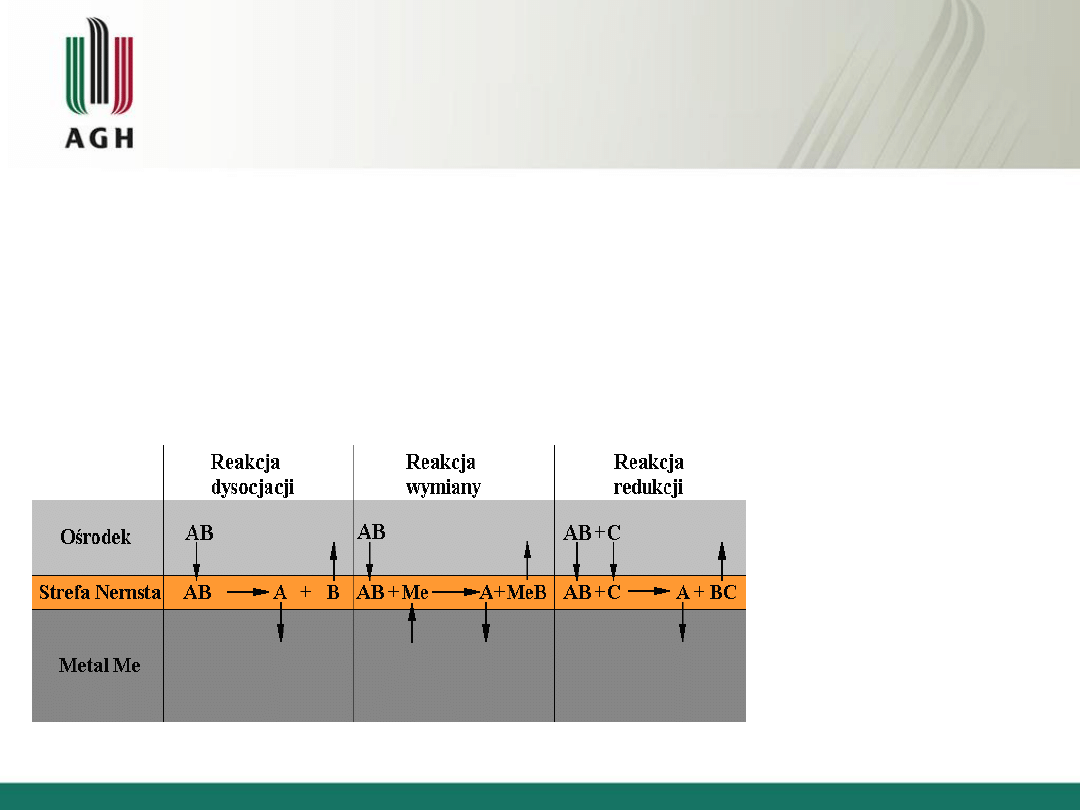
Dyfuzyjne procesy obróbki
cieplno-chemicznej zachodzą gdy:
1. Pierwiastek dyfundujący występuje w postaci „
in stastu nascendi
”
czyli wolnych atomów, które w chwili tworzenia się wykazują większą
aktywność.
W zależności od rodzaju aktywnego ośrodka i temperatury procesu mogą
występować trzy typy reakcji prowadzące do wytwarzania aktywnych atomów
pierwiastka nasycającego
Schemat reakcji wydzielania pierwiastka dyfundującego
Dysocjacja
polega na
rozkładzie cząsteczek
związku i utworzeniu
aktywnych atomów
pierwiastka dyfundującego,
np.:
2 CO
CO
2
+
C
NH
3
3H +
N

2.
Dyfuzyjne procesy obróbki
cieplno-chemicznej zachodzą gdy:
Pierwiastek dyfundujący ulega
adsorpcji na powierzchni metalu
,
(nagromadzenie wolnych atomów na powierzchni metalu).
Adsorpcja
— polegająca na wchłanianiu (rozpuszczaniu) wolnych
atomów przez powierzchnię metalu (zachodzi tylko wtedy, gdy
pierwiastek wprowadzany rozpuszcza się w obrabianym metalu).

3. Zachodzi przemieszczenie się zaadsorbowanych atomów w głąb
metalu -
dyfuzja
.
Dyfuzja
-
aktywowany cieplnie proces zachodzący wskutek ruchu
atomów w sieci przestrzennej metalu w kierunku wyrównania
stężenia składników. Warunkiem przebiegu dyfuzji jest
rozpuszczalność w stanie stałym pierwiastka nasycającego w osnowie
metalicznej obrabianego materiału.
Dyfuzyjne procesy obróbki
cieplno-chemicznej zachodzą gdy:
Schematyczna reprezentacja procesu mieszania
dwóch substancji na drodze dyfuzji

Mechanizmy dyfuzji
Polega na wymianie atomu z wakancją.
Warunkiem zajścia takiego podstawowego aktu
dyfuzji jest, że muszą znajdować się w sieci
wakancje oraz musi zostać pokonana bariera
potencjału otaczająca atomy, co także wymaga
odpowiedniej energii.
•
wakansowy
w roztworach różnowęzłowych
•
międzywęzłowy
w roztworach międzywęzłowych,
charakterystyczny dla dyfuzji węgla i azotu w stalach
Polega na kolejnym przeskakiwaniu atomów
międzywęzłowych, tzn. o małych średnicach w
porównaniu z atomami osnowy, z jednej luki
międzyatomowej do drugiej - sąsiedniej.

Prawa opisujące dyfuzję -
Prawa Ficka
Są to dwa prawa dotyczące zjawiska
dyfuzji, których sformułowanie przypisuje
się
niemieckiemu
fizykowi
i
matematykowi Adolfowi Fickowi. Są one
współcześnie stosowane w modelowaniu
procesów dyfuzji w tkankach, neuronach,
biopolimerach czy farmakologii.
Adolf Fick
ur. 3 września 1829
zm. 21 sierpnia 1901

I Prawo Ficka
Stosowane w opisie procesów dyfuzji kiedy
stężenie strumienia
dyfuzji objętościowej nie zmienia się z czasem
. Opisuje ono
strumień dyfuzji J (strumień atomów, tj. ilość atomów składnika
nasycającego na jednostkę powierzchni i czasu [1/cm
2
s].
D - współczynnik dyfuzji [cm
2
/s] [m
2
/s],
c- stężenie [1/cm
3
],
x – odległość [cm],
dc/dx – gradient stężenia pierwiastka dyfundującego.
Współczynnik dyfuzji zależy od:
- temperatury
- rodzaju roztworu (międzywęzłowy, różnowęzłowy)
- rodzaju sieci rozpuszczalnika.

Równanie Arrheniusa
D = D
o
· exp(-Q/RT)
Wpływ temperatury na D opisuje równanie Arrheniusa:
D – współczynnik dyfuzji [cm
2
/s] [m
2
/s]
D
0
- stała zależna od struktury krystalicznej rozpuszczalnika,
osnowy i rodzaju roztworu oraz temperatury,(cm
2
/s)
Q – energia aktywacji dyfuzji [J/mol]
T – temperatura [K]
R - stała gazowa 8,314 [J/mol*K]
D – współczynnik dyfuzji [cm
2
/s] [m
2
/s]
Średnia droga dyfuzji:

Jest stosowane, gdy strumień dyfuzji zmienia się
lokalnie w czasie. Opisuje zależność stężenia
dyfundującego pierwiastka od czasu i miejsca.
II Prawo Ficka
Porównanie współczynników dyfuzji węgla w żelazie i samodyfuzji żelaza
[cm
2
/s]
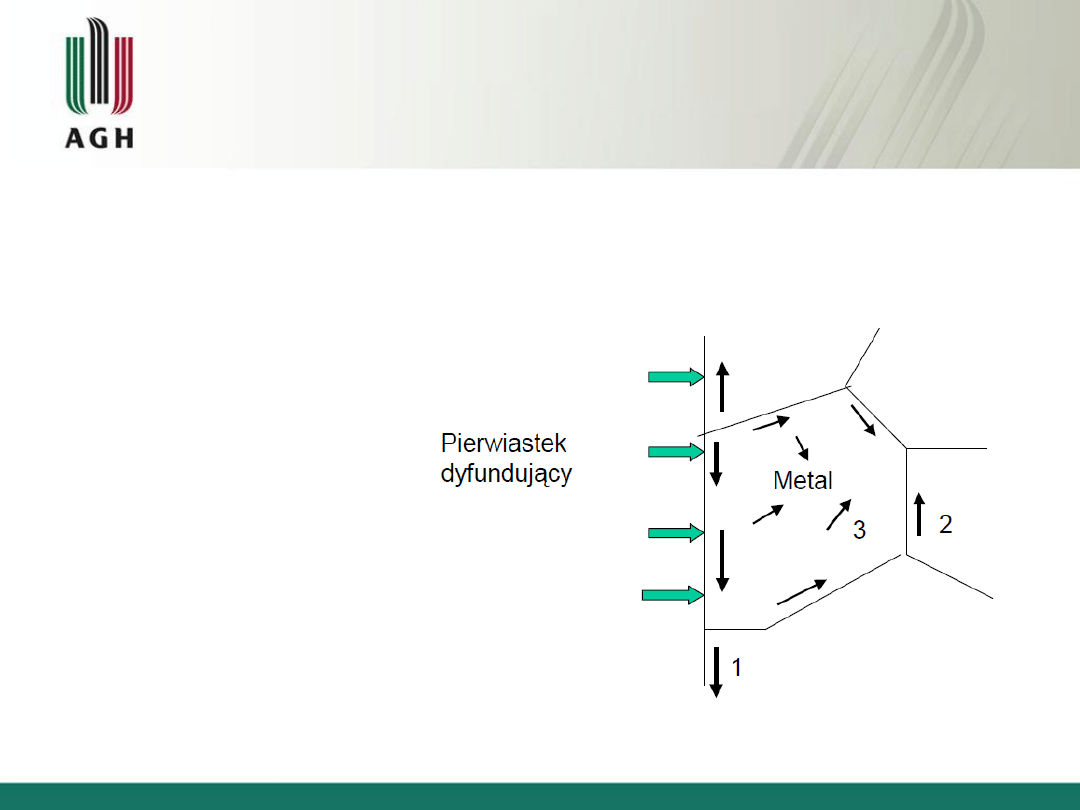
Drogi dyfuzji
1. Wzdłuż ziaren — najłatwiej
2. Wzdłuż granic ziaren — trudniej
3. Wewnątrz ziaren — najtrudniej

Nawęglanie
Polega na
dyfuzyjnym nasyceniu warstwy wierzchniej stali węglem
podczas wygrzewania obrabianego przedmiotu w ciągu określonego czasu
w ośrodku, w którym powstaje węgiel atomowy.
Cel nawęglania: podwyższenie twardości i odporności na ścieranie
powierzchni stalowego elementu przy zachowaniu dobrej ciągliwości
(udarności) rdzenia.
Stale do nawęglania o zawartości węgla od 0,1 do 0,25% lub
stopowe z głównymi dodatkami stopowymi poprawiającymi hartowność:
Cr, Ni, Mn, Mo, Ti, W. Wprowadzone są one do stali w celu
podwyższenia hartowności oraz zwiększenia plastyczności rdzenia.
Temperatura i czas nawęglania:
Temperatura nawęglania–powyżej Ac
3
(zakres istnienia austenitu), 850-
950
C, czas 2-8 h.

Nawęglanie
W zależności od warunków nawęglania w
warstwie powstają równe strefy:
Strefa
nadeutektoidalna
(0,85-1,0%C),
zawierającą perlit i węgliki żelaza, które tworzą
niekorzystną siatkę cementytu po granicach ziarn,
Strefa eutektoidalna
(0,7-0,85 %C) zawierającą
wyłącznie perlit,
Strefa podeutektoidalną
, zawierającą ferryt i perlit,
przy czym ilość ferrytu zwiększa się w kierunku
rdzenia.
Twardość stali niskowęglowej po nawęglaniu może osiągać
60
do
65
HRC.
Grubość warstwy nawęglonej nie przekracza zazwyczaj
0,5-2mm
.
Typowe części, dla których stosuje się nawęglanie:
• koła zębate silnie obciążone i poddawane zmiennym obciążeniom
• wałki rozrządu i krzywki sterujące
• sworznie tłokowe
• pierścienie i wałki łożysk wielogabarytowych
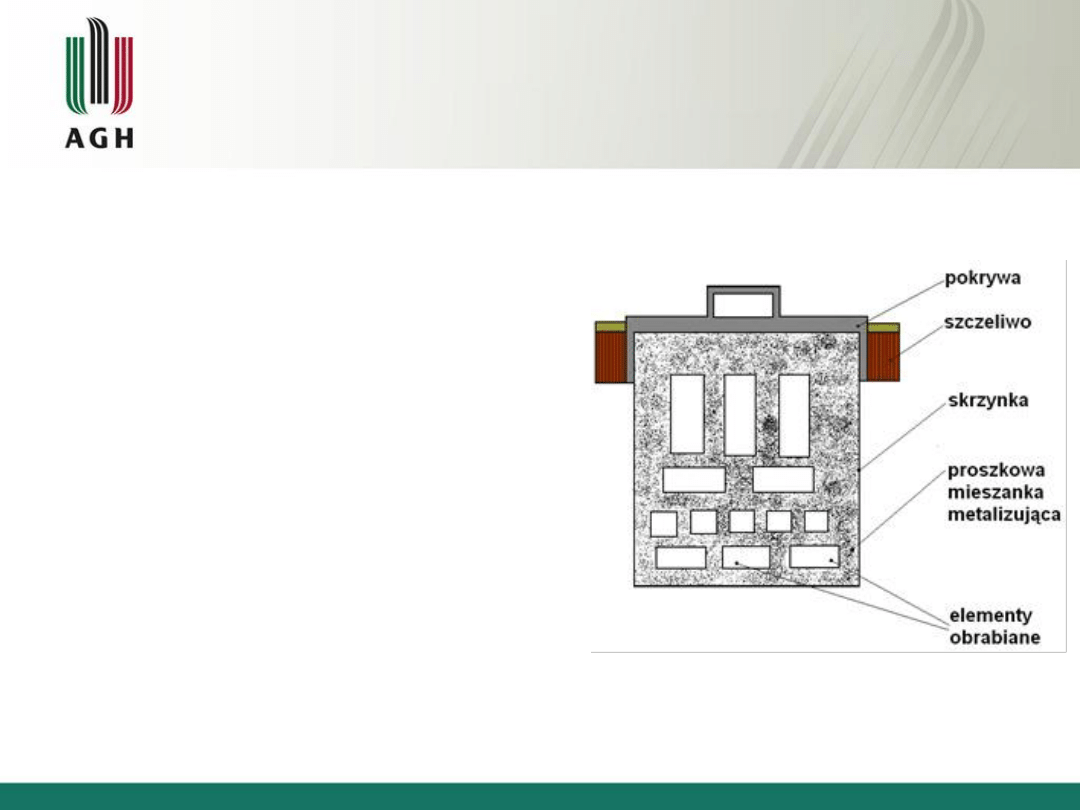
Nawęglanie w karboryzatorach stałych
(proszkach)
Wygrzewanie przedmiotów w temp. 880-950
C w ośrodku składającym się z
mieszaniny granulowanego węgla drzewnego (85-95%) z i węglany BaCO
3
, Na
2
CO
3
lub CaCO
3
(5-15%).
Reakcje:
2C + O
2
2CO,
BaCO
3
BaO + CO
2
,
CO
2
+C
2CO
2CO
C
at
+ CO
2
Zalety:
- niski stopień trudności procesu,
- łatwa obsługa i powtarzalność wyników nawęglania,
Wady:
- trudność otrzymania cienkich warstw,
- brak możliwości regulacji węgla w warstwie,
- brak możliwości automatyzacji procesu.

Nawęglanie gazowe
Nagrzanie i wygrzanie części stalowych w atmosferze nawęglającej,
przepływającej przez szczelną komorę pieca o temp. 880- 950
o
C.
Atmosfery nawęglające:
- atmosfery generatorowe, powstałe z gazu ziemnego lub propanu,
- atmosfery bezgeneratorowe, utworzone z surowych gazów lub węglowodorów
ciekłych.
Ośrodkami nawęglającymi są mieszaniny gazów: CO-CO
2
-CH
4
-H
2
-H
2
O lub
jeszcze dodatkowo z N
2
.
Reakcje:
2CO→ C+CO
2
CH
4
→ C+2H
2
CO+H
2
→ C+H
2
O
Zalety:
- duża ekonomiczność procesu dzięki skróceniu czasu procesu,
- możliwość łatwego regulowania zawartości węgla w warstwie nawęglanej,
- możliwość bezpośredniego hartowania po nawęglaniu,
- wysoki stopień mechanizacji procesu,
- wysoka wydajność pieców.
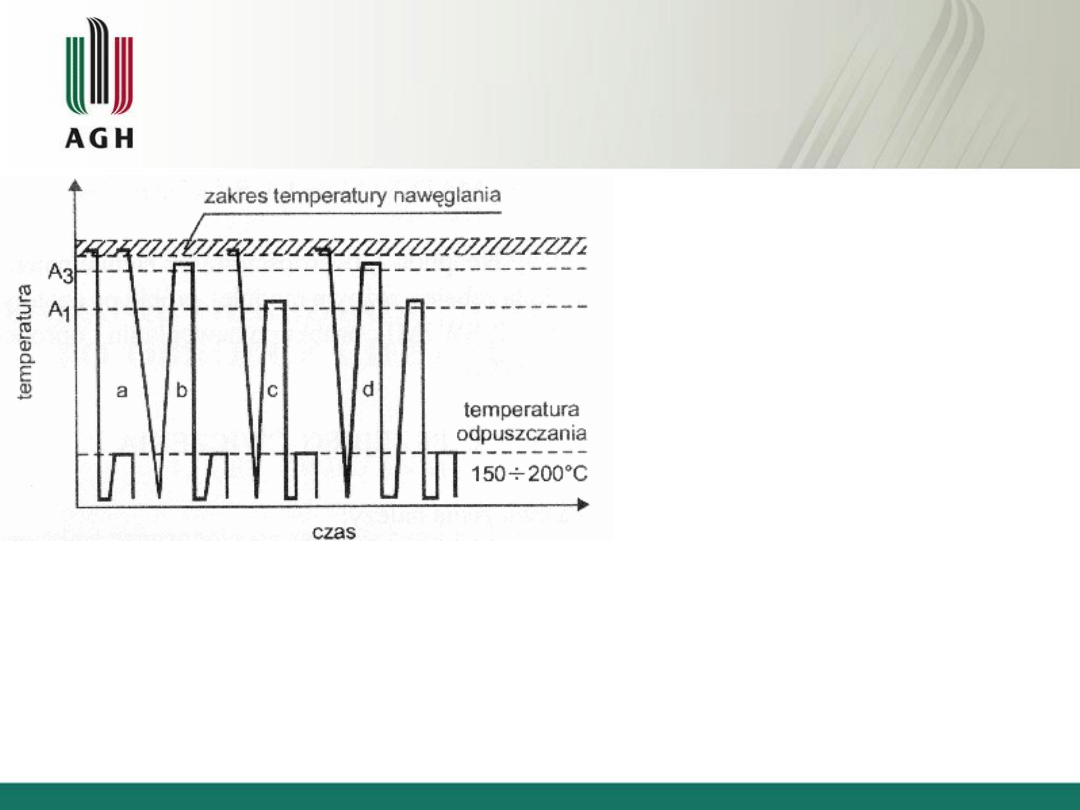
Obróbka cieplna po nawęglaniu
a
– hartowanie bezpośrednie z
temperatury nawęglania i niskie
odpuszczanie
b
– jednokrotne hartowanie z
temperatury właściwej do rdzenia i
niskie odpuszczanie
c
– jednokrotne hartowanie z
temperatury właściwej dla warstwy
wierzchniej i niskie odpuszczanie
d
– dwukrotne hartowanie z niskim
odpuszczaniem
Struktura i twardość powierzchni stali po hartowaniu i odpuszczaniu:
martenzyt (sam lub z małym udziałem Fe
3
C) o twardości ~60 HRC.
Sposoby zabezpieczenia powierzchni nie podlegających nawęglaniu:
- pokrywanie pastami ochronnymi,
- miedziowanie elektrolityczne,
-
pozostawienie naddatku materiału o grubości większej niż głębokość warstwy
nawęglonej.

Azotowanie
Nasycanie azotem powierzchni przedmiotów stalowych (stale konstrukcyjne o
zawartości węgla 0,3-0,4%) lub stale średniowęglowe zawierające dodatki
Al, Ti, V, Mo, Cr wykazujące wysokie powinowactwo chemiczne do azotu.
Celem
azotowania
jest
nadanie
przedmiotom
wysokiej
twardości
powierzchniowej, odporności na ścieranie, wysokiej odporności zmęczeniowej oraz
odporności na korozję.
Temperatura i czas azotowania: zakres temperatur 480-800
C, czasy
azotowania do 100 godz.
Azotowanie utwardzające (sposób konwencjonalny lub jonowy) - uzyskanie
bardzo trwałej i odpornej na zużycie ścierne warstwy wierzchniej elementów
obrabianych przy zachowaniu wysokich własności mechanicznych rdzenia.
Azotowanie antykorozyjne (sposób konwencjonalny) poprawienia odporności
stali i żeliw na działanie środowiska korozyjnego.
Ponieważ azotowanie przeprowadza się w niezbyt wysokiej
temperaturze, stal uprzednio poddaje się
ulepszaniu cieplnemu!
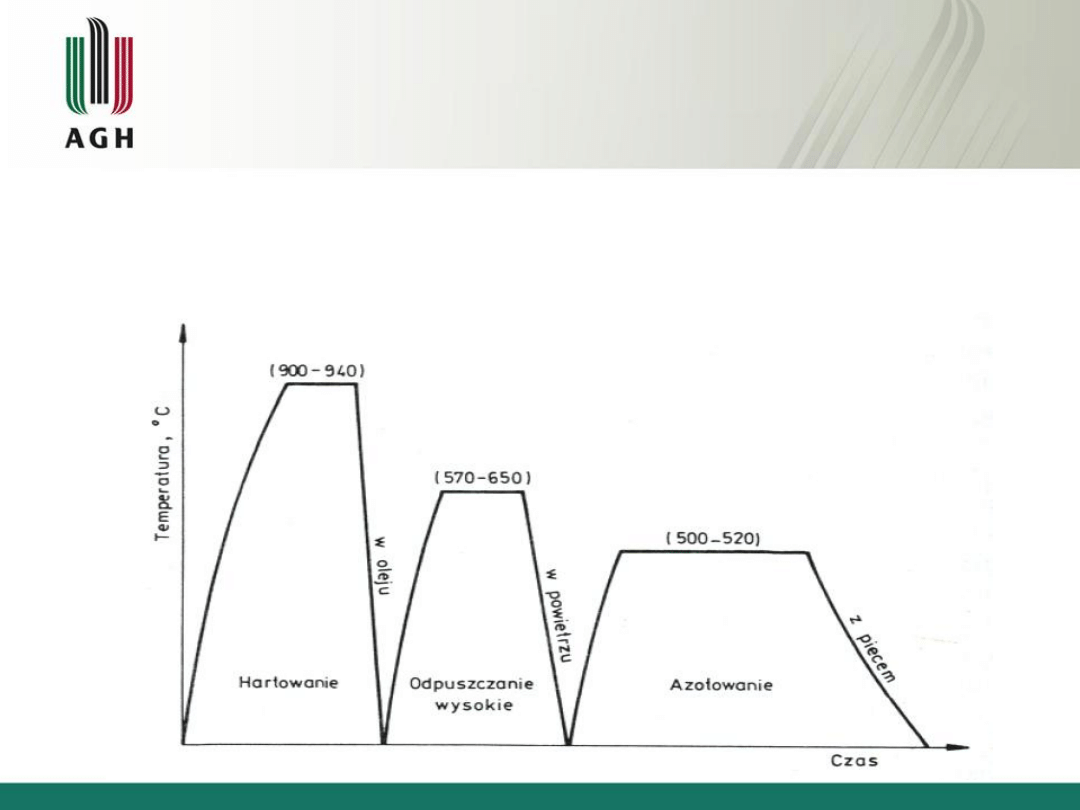
Obróbka cieplna przed azotowaniem
Ulepszanie cieplne
(hartowanie + odpuszczanie wysokie) w celu
uzyskania optymalnych właściwości mechanicznych w rdzeniu
elementu.

Właściwości warstw azotowanych:
- dużą twardość (do 1200 HV),
- dobra wytrzymałość zmęczeniowa,
- wyższa odporność w podwyższonej
temperaturze (do temperatury azotowania),
- dobra odporność na zacieranie i zużycie o
charakterze adhezyjnym,
- małe odkształcenia w procesie
technologicznym.
Azotowanie
Fazami tworzącymi się w warstwie w
procesie azotowania są:
faza
- ferryt azotowy (nitroferryt) (roztwór
stały azotu w żelazie
)
faza
- austenit (nitroaustenit) azotowy
(roztwór stały azotu w żelazie
)
faza
’
–azotek żelaza (Fe
4
N)
faza
- azotek żelaza (Fe
2
N)

Azotowanie utwardzające
Ośrodek: amoniak, temperatura: 480-560°C, czas: kilkanaście- kilkadziesiąt
godzin.
Reakcja dysocjacji:
2NH
3
2N+3H
2
Przedmioty do azotowania muszą być oczyszczone i odtłuszczone;
powierzchnie, które nie podlegają azotowaniu, zabezpieczone pastami lub
powłokami.
Grubość warstwy: od 0,2-0,8 mm
Twardość po azotowaniu: stale niestopowe ~ 1100 HV (wiąże się z
wytworzeniem na powierzchni fazy γ’ (Fe
4
N)); stale stopowe ~ 1500 HV.
Zastosowanie:
Elementy konstrukcyjne i narzędziowe narażone podczas pracy na zużycie ścierne i
korozję, np. elementy silników i pomp w przemyśle okrętowym, lotniczym i
motoryzacyjnym, narzędzia do obróbki plastycznej i skrawania, elementy
wytłaczarek i wtryskarek

Azotowanie antykorozyjne
Ośrodek: amoniak, temperatura: 600-800°C, czas: 1-6 godzin
Grubość warstwy: 0,005-0,03 mm (stale, żeliwa niestopowe)
Struktura warstwy wierzchniej po azotowaniu: azotek typu ε = Fe
2
N o dużej
odporności korozyjnej i roztwór N w Fe
.
Po azotowaniu antykorozyjnym można prowadzić obróbkę cieplną!
Zastosowanie:
Elementy wykonane ze stali niestopowych i niskostopowych oraz żeliw np. palniki
spawalnicze, zawory, okucia budowlane, części hamulców kolejowych, części
rowerów, części armatury wodociągowej i instalacji pary wodnej.

Węgloazotowanie i azotonawęglanie stali
Polega na nasyceniu powierzchni przedmiotów stalowych jednocześnie węglem i
azotem w temperaturze 750-950°C (węgloazotowanie) i azotonawęglanie
(450-650 °C).
Cel: wytworzenie na powierzchni przedmiotów stalowych warstwy o wysokiej
twardości i odporności na ścieranie w znacznie większym stopniu niż dla warstw
nawęglanych.
WĘGLOAZOTOWANIE KĄPIELOWE
Składniki kąpieli: cyjanki i cyjaniany Na i K. Ponadto kąpiele zawierają węglany
tych pierwiastków. Podczas procesu zachodzą reakcje umożliwiające tworzenie się
cyjanianów i wydzielanie C i N.
NaCN+O
2
2NaCNO
4NaCNO+2O
2
2K
2
CO
3
+CO
2
+C+4N
Wysoka toksyczność procesu i trudności w utrzymaniu stałego składu
kąpieli.
Węgloazotowanie kąpielowe w niskich temperaturach
Węgloazotowanie kąpielowe w wysokich temperaturach

WĘGLOAZOTOWANIE GAZOWE
- w atmosferach zawierających amoniak i gaz nawęglający lub ciekłe węglowodory.
- temperatura: 560-580
o
C,
- czas: 2-5h
- zalety: wyeliminowanie trujących soli, możliwość regulacji procesu przez zmianę
ilości gazów nawęglających i amoniaku.
Węgloazotowanie i azotonawęglanie stali

• Siarkowanie
• Borowanie
• Aluminiowanie
• Chromowanie
• Cynkowanie
• Cynowanie
• Kadmowanie
• Miedziowanie
• Niklowanie
• Ołowiowanie
• Srebrzenie
• Złocenie
Inne rodzaje metalizacji dyfuzyjnej…

Cel ćwiczenia
„Wyznaczenie współczynnika dyfuzji węgla w
warstwie nawęglonej ”

Wyniki pomiarów
Lp. T [
o
C] T[K]
x
[mm]
D
[cm
2
/s]
ln D
1/T
[K
-1
]
t [s]
1.
2.
3.
T – temperatura w skali bezwzględnej [K]
x – grubość warstwy nawęglonej [mm]
D – współczynnik dyfuzji [cm
2
/s]
t – czas nawęglania [s]

Obliczenia
Dt
x
2
1.
Ze wzoru na średnią drogę dyfuzji obliczamy współczynnik dyfuzji D:
2. Naszkicować wykres zależności współczynnika dyfuzji D od
temperatury.
3. Naszkicować wykres zależności ln(D) od odwrotności temperatury.
W tym celu obliczono:
ln (D)
,
bezwymiarowa
i
1/T
[K
-1
]
Obliczamy wartość D dla poszczególnych próbek

Obliczenia
4. Wyznaczyć prostą regresji:
y=-ax +b
Znając współczynnik kierunkowy „a” tej prostej oraz wartość stałej
gazowej R możemy korzystając z zależności :
tg
= a= -Q/R
Q – energia aktywacji dyfuzji [J/mol]
R–stała gazowa 8,314 [J/molK]
Wyznaczamy energię aktywacji
:
a = -Q/R Q = -aR
5. Na podstawie wyznaczonej energii aktywacji obliczamy D
o
, korzystając
ze wzoru:
D = D
o
· exp(-Q/RT)

Obliczenia
Tabela 2 Zestawienie wyników
WNIOSKI KOŃCOWE
Lp. T [K]
Q
[J/mol]
R
[J/mol*
K]
D
[cm
2
/s]
Do
1.
2.
3.
Wyszukiwarka
Podobne podstrony:
obróbka cieplno chemiczna (8)
Obróbka cieplno - chemiczna, azotowanie, Azotowanie
OBRÓBKA CIEPLNO CHEMICZNA2, nauka, zdrowie, materiałoznawstwo, Obróbka cieplna
obrobka cieplno chemiczna
obróbka cieplno chemiczna stali
Sprawozdanie z Materiałoznawstwa--obróbka cieplno-chemiczna, Materialoznawstwo
obrobka cieplno-chemiczna, Techniki wytwarzania
Obróbka cieplno-chemiczna3, BHP
Obrobka cieplno chemiczna stali Nieznany
Obrobka cieplno-chemiczna, POLITECHNIKA (Łódzka), Nauka o Materiałach, 1 semestr
obróbka cieplno chemiczna stali
Obrobka cieplno chemiczna 3
Obróbka cieplno-chemiczna, Materiałoznawstwo I i II
OBRÓBKA CIEPLNO-CHEMICZNA CZĘŚCI MASZYN - Lab 6, Studia, Materiałoznastwo, Metaloznastwo i Podstawy
obróbka cieplno-chemiczna i metalurgia, BHP
obróbka cieplno-chemiczna, BHP
Ćw. 8 - Obróbka cieplno - chemiczna - azotowanie, Studia, ROK I, 2 semestr, Obróbka na gorąco, spraw
więcej podobnych podstron