
Technologie wytwarzania metali
• Odlewanie
• Metalurgia proszków
• Otrzymywanie monokryształów
• Otrzymywanie materiałów superczystych
• Techniki próżniowe
KRYSTALIZACJA METALI I STOPÓW
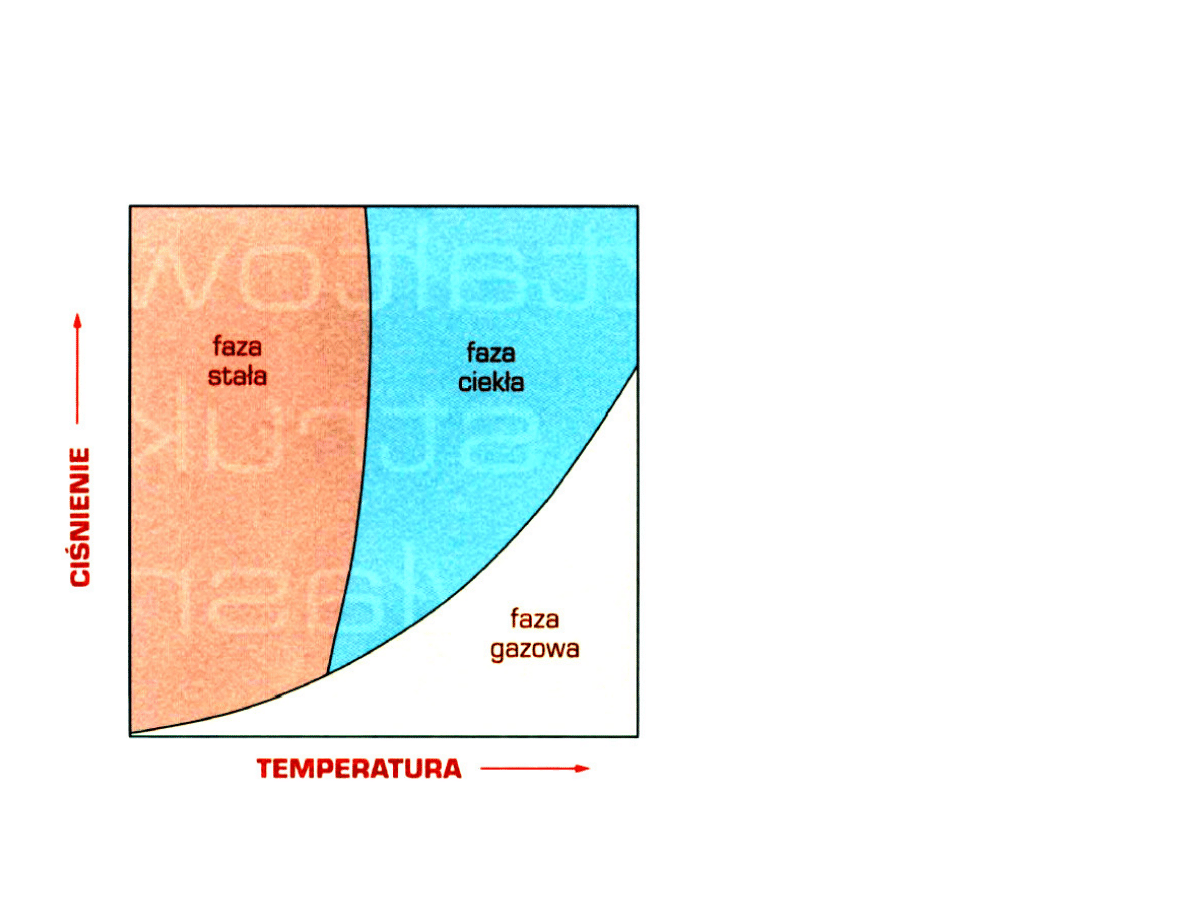
Równowaga faz w układzie jednoskładnikowym
Krzepnięcie - przemiana
fazy ciekłej w fazę stałą
Krystalizacja – przemiana
fazy ciekłej w fazę stałą o
budowie krystalicznej. Ma
podstawowe znaczenie w
procesie kształtowania
wyrobów metalowych na
drodze odlewania
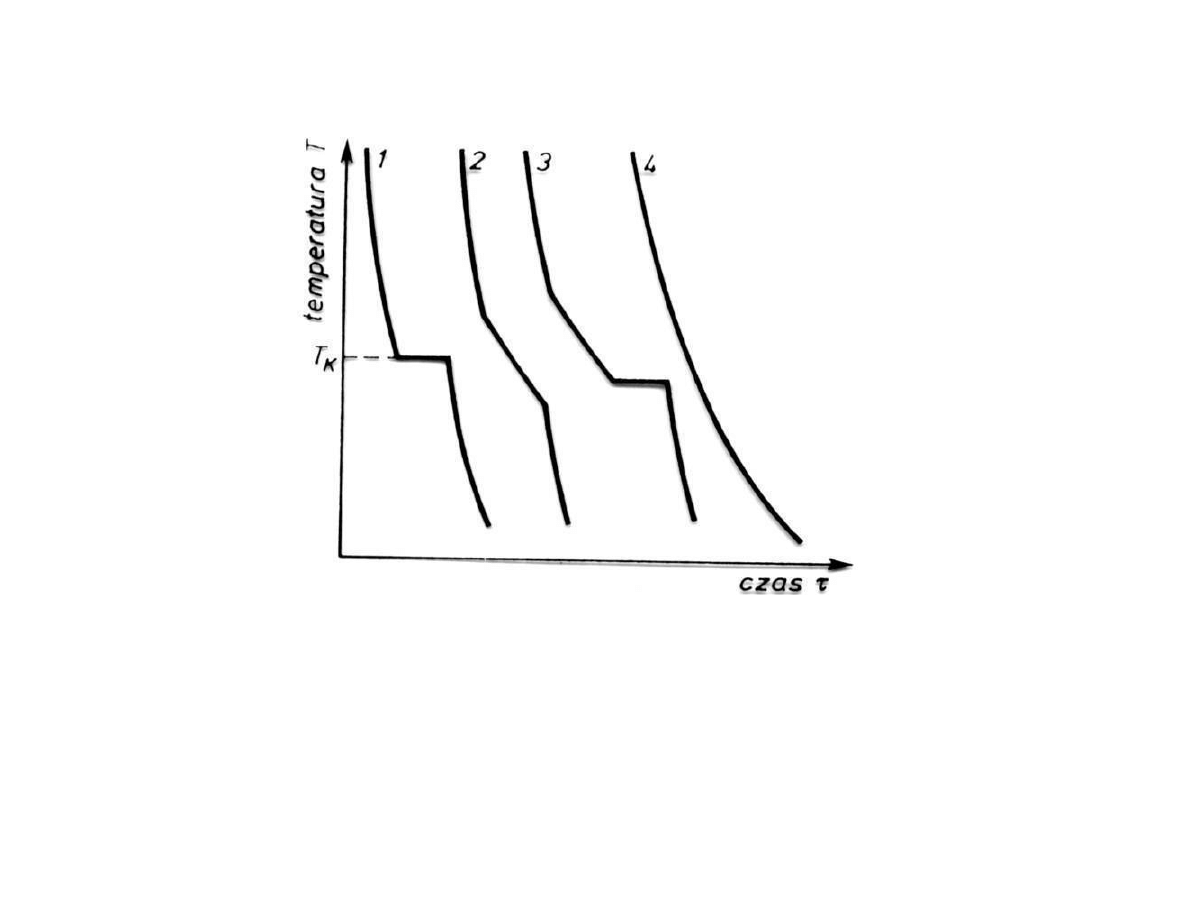
Zmiany temperatury w funkcji czasu chłodzenia od stanu
ciekłego: 1-3 materiały krystaliczne, 4 materiał amorficzny

•
Krystalizacja przebiega przez zarodkowanie i wzrost
zarodków krystalizacji:
1. zarodkowanie - powstawanie zarodków krystalizacji,
czyli miejsc, od których kryształy zaczynają powstawać
-
zarodki krystalizacji
– zespoły bliskiego
uporządkowania w fazie ciekłej o wielkości większej od
krytycznej (kilkuatomowe skupiska fazy stałej o typowej
dla niej strukturze krystalicznej), które rozrastając się
powodują stopniowe przechodzenie fazy ciekłej w stałą.
2. swobodny wzrost pojedynczych kryształów zwany
propagacją krystalizacji
3. reorganizacja warstwy powierzchniowej i powstawanie
tzw. mikrostruktury krystalicznej,
4. zlepianie się pojedynczych kryształów w większe
struktury.

•Szybkość krystalizacji zależy od:
–szybkości zarodkowania, tj. liczby zarodków
krystalizacji tworzących się w ciągu jednostki
czasu w jednostce objętości cieczy,
–liniowej szybkości krystalizacji, tj. szybkości
przesuwania się frontu krystalizacji, mierzonej
w jednostkach długości na jednostkę czasu.
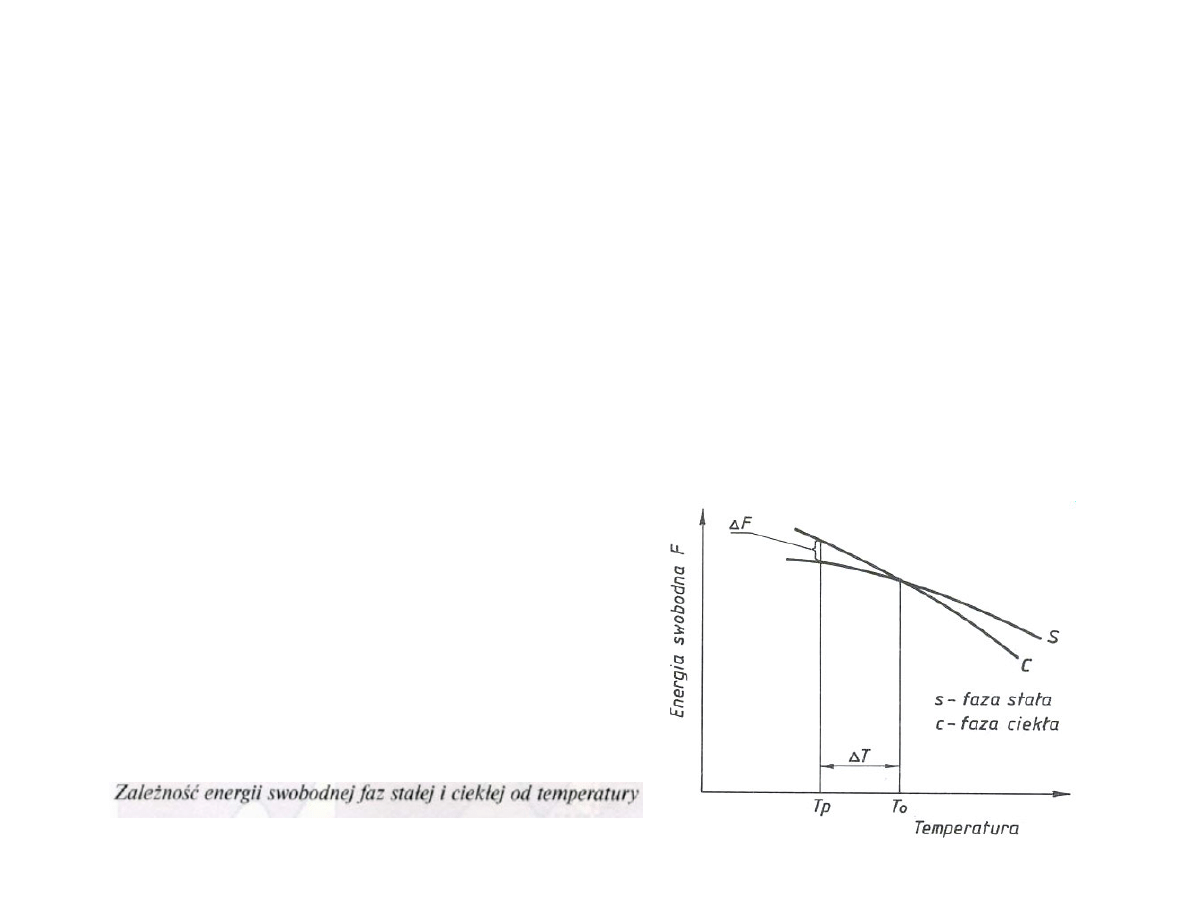
•Aby krystalizacja mogła się rozpocząć, procesowi temu musi
towarzyszyć
zmniejszenie się energii swobodnej układu
.
•Jest to możliwe wówczas, gdy temperatura ciekłego metali spadnie
nieco poniżej temperatury krystalizacji (Ts) tj. temperatury
równowagi faz; ciekłej i stałej.
•Temperaturę, w której praktycznie zaczyna się krystalizacja,
nazywamy rzeczywistą temperaturą krystalizacji (Tp). Natomiast
różnicę między teoretyczną a rzeczywistą temperaturą krystalizacji
nazywamy
stopniem przechłodzenia (
∆T)
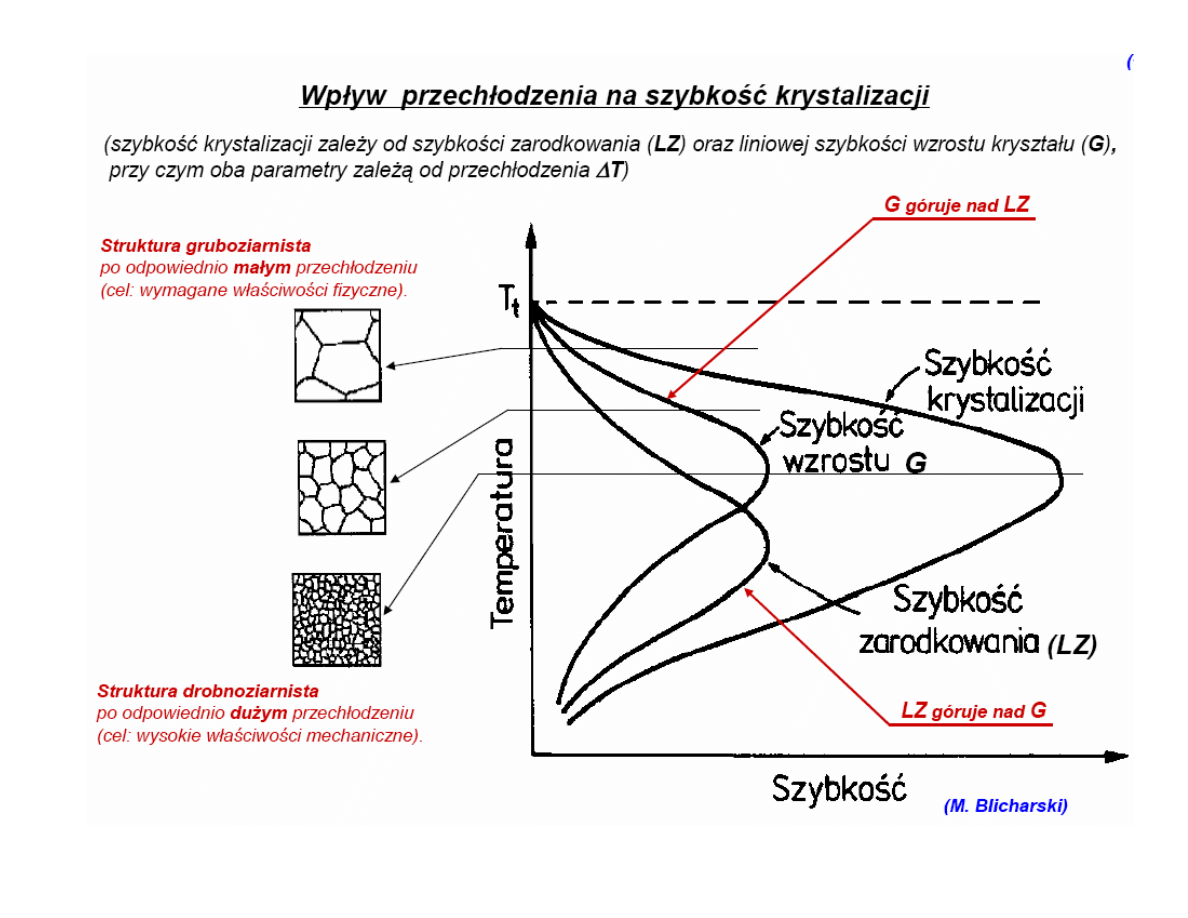

• Przy nieznacznym przechłodzeniu (małej szybkości
chłodzenia) metal ma strukturę gruboziarnistą
• Ze zwiększeniem szybkości przechłodzenia liniowa
szybkość krystalizacji wzrasta
wolniej
od szybkości
zarodkowania, metal ma strukturę drobnoziarnistą
• Maksimum szybkości zarodkowania odpowiada większemu
przechłodzeniu niż maksimum liniowej szybkości
krystalizacji, metal osiąga w tym zakresie najmniejszą
wielkość ziarna
• Przy bardzo dużych szybkościach chłodzenia szybkość
zarodkowania i liniowa szybkość krystalizacji są równe zeru,
metal posiada amorficzną strukturę szkła.

Zarodkowanie
może być:
•
homogeniczne, gdy prawdopodobieństwo
powstania zarodka jest jednakowe w dowolnym
miejscu układu.
•
heterogeniczne, gdy funkcje zarodków przejmują
obce, nierozpuszczone w cieczy cząstki faz
stałych
,
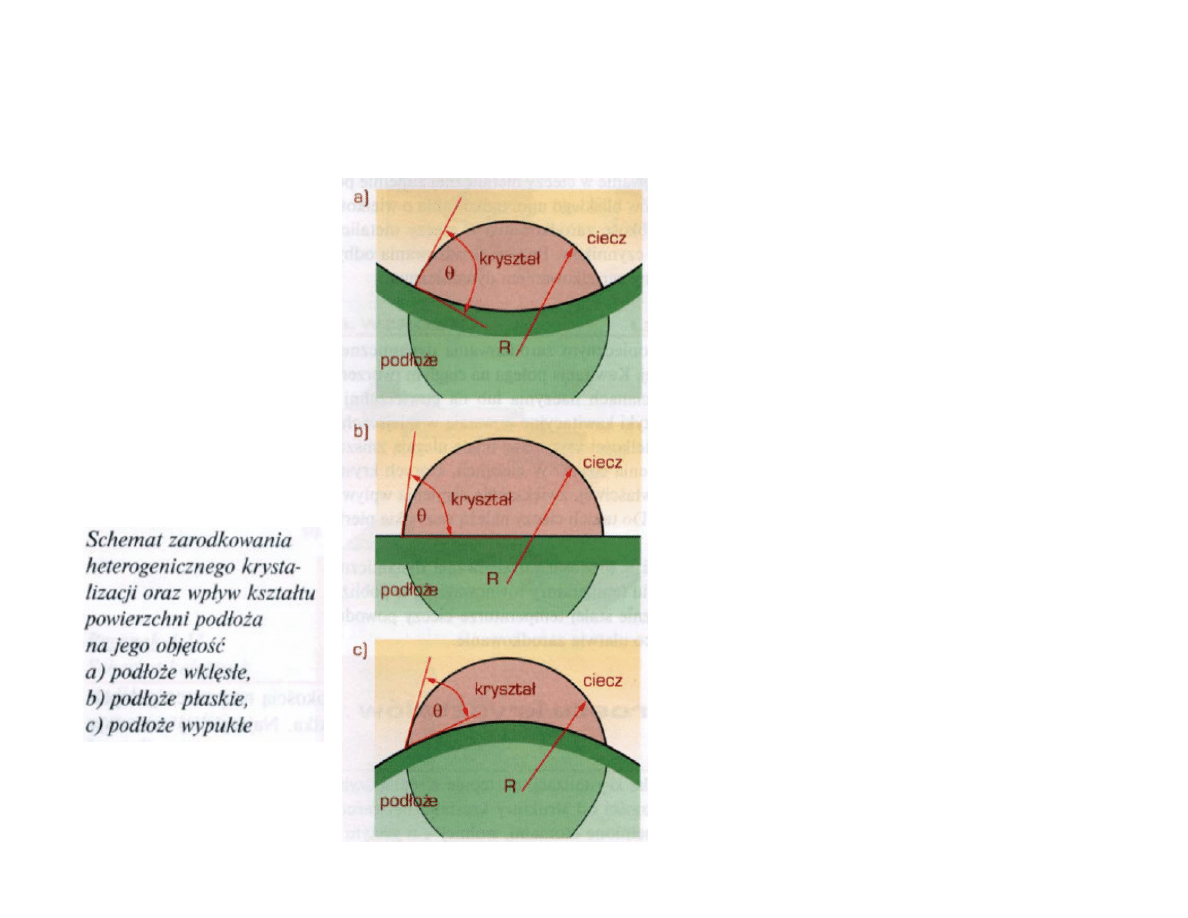
Zarodki na obcym ciele
stałym np.: ściany formy
odlewniczej, cząstki
zanieczyszczeń stałych w
cieczy itp..
Zarodkowanie heterogeniczne
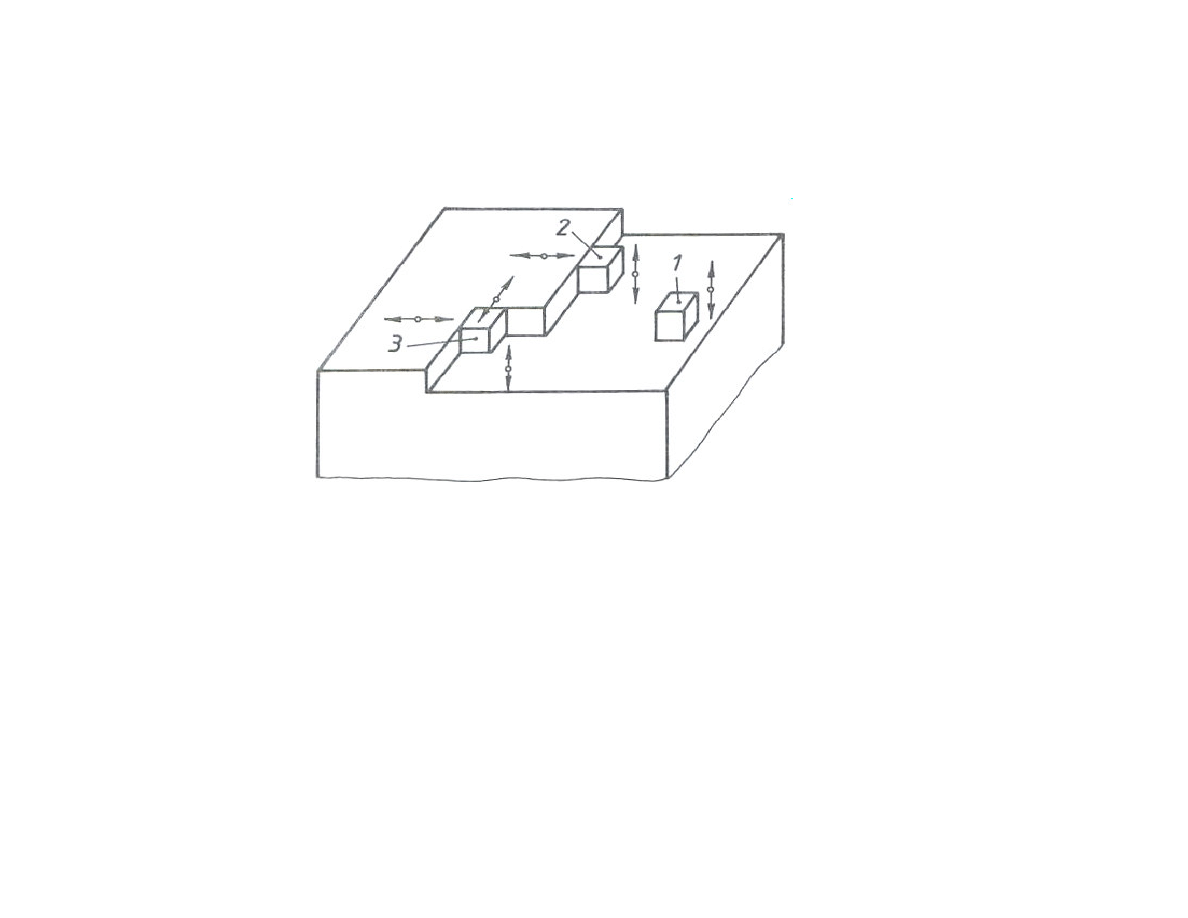
Wzrost zarodków – osadzanie na jego powierzchni atomów z cieczy w
pozycjach odpowiadających położeniom w sieci przestrzennej.
•Prawdopodobieństwo (teoretyczne) przyłączenia atomu do zarodka
wzrasta w kolejności położeń: ściana –1, krawędź – 2, naroże – 3 (1,2,3-
kierunkowe działanie wiązań).
•Najkorzystniejsze rzeczywiste warunki: stopnie na powierzchni w wyniku
wyjścia na powierzchnię dyslokacji śrubowej.
•Warunek postępu krystalizacji: odprowadzanie ciepła krzepnięcia, które
zmniejsza przechłodzenie.
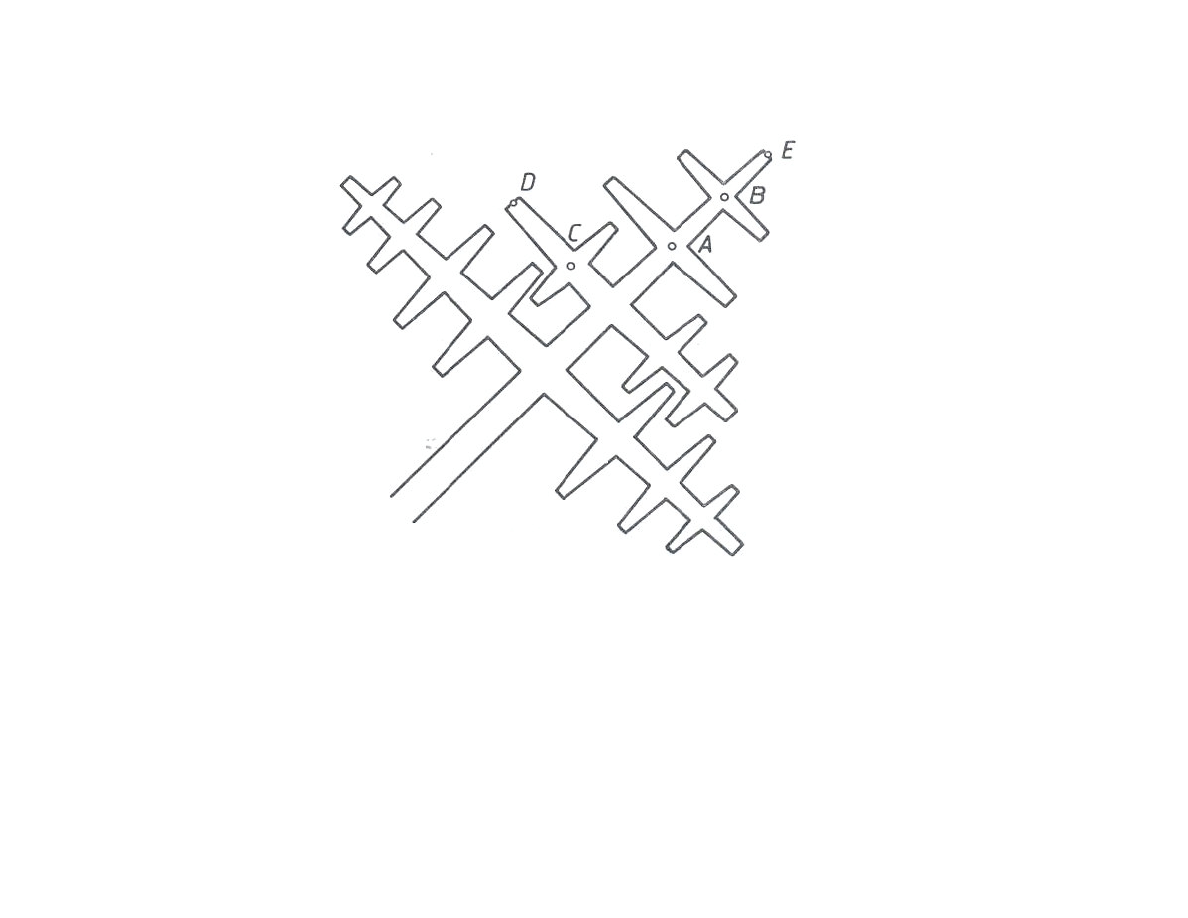
Krystalizacja czystych metali - wzrost dendrytyczny
Schemat wzrostu dendrytu (kryształu o kształcie drzewa): gdy w
wyniku wydzielania ciepła krzepnięcia i zaniku przechłodzenia
zostanie zahamowany szybki wzrost kryształu od A do B, kryształ
zaczyna wzrastać w innym kierunku w miejscu dostatecznego
przechłodzenia, np. od C do D.

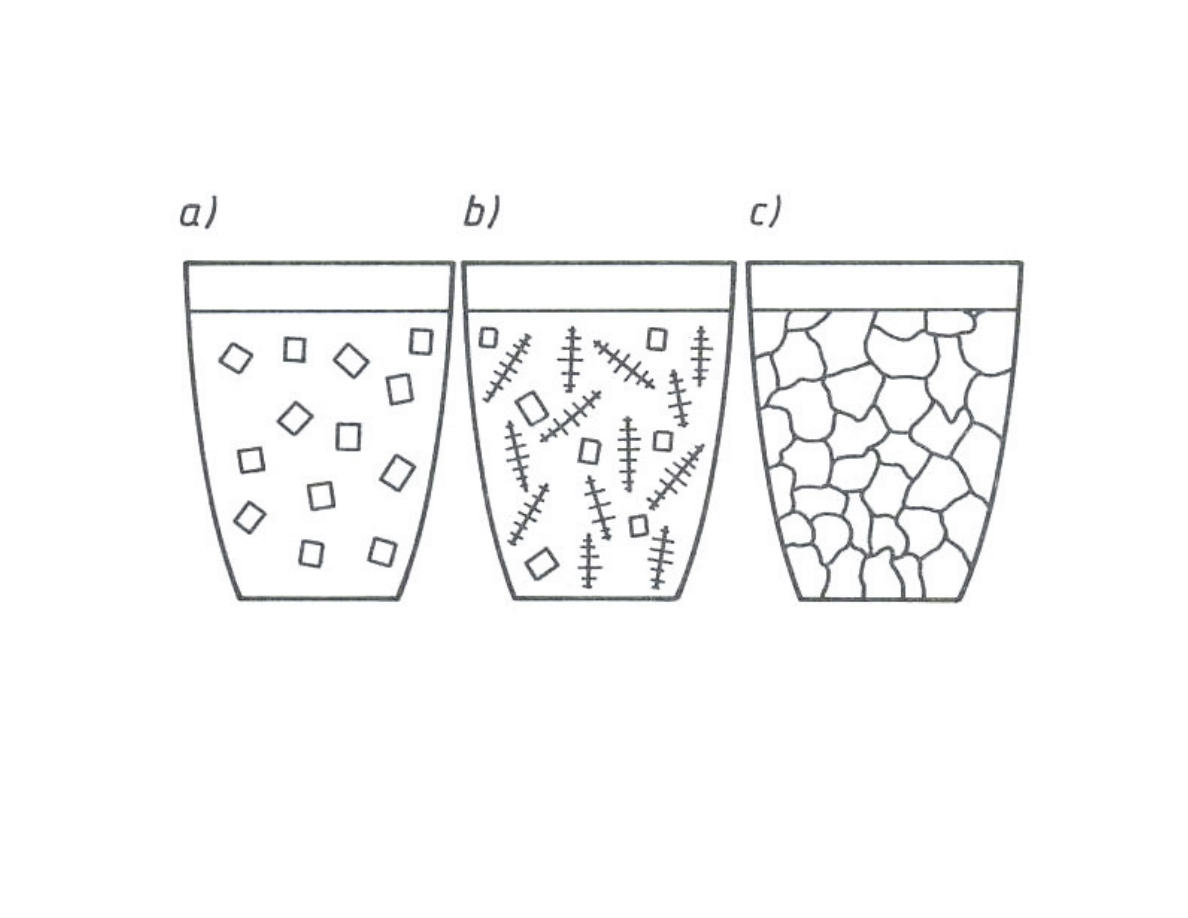
Kolejne etapy krystalizacji: a) zarodki, b) dendryty, c) ziarna
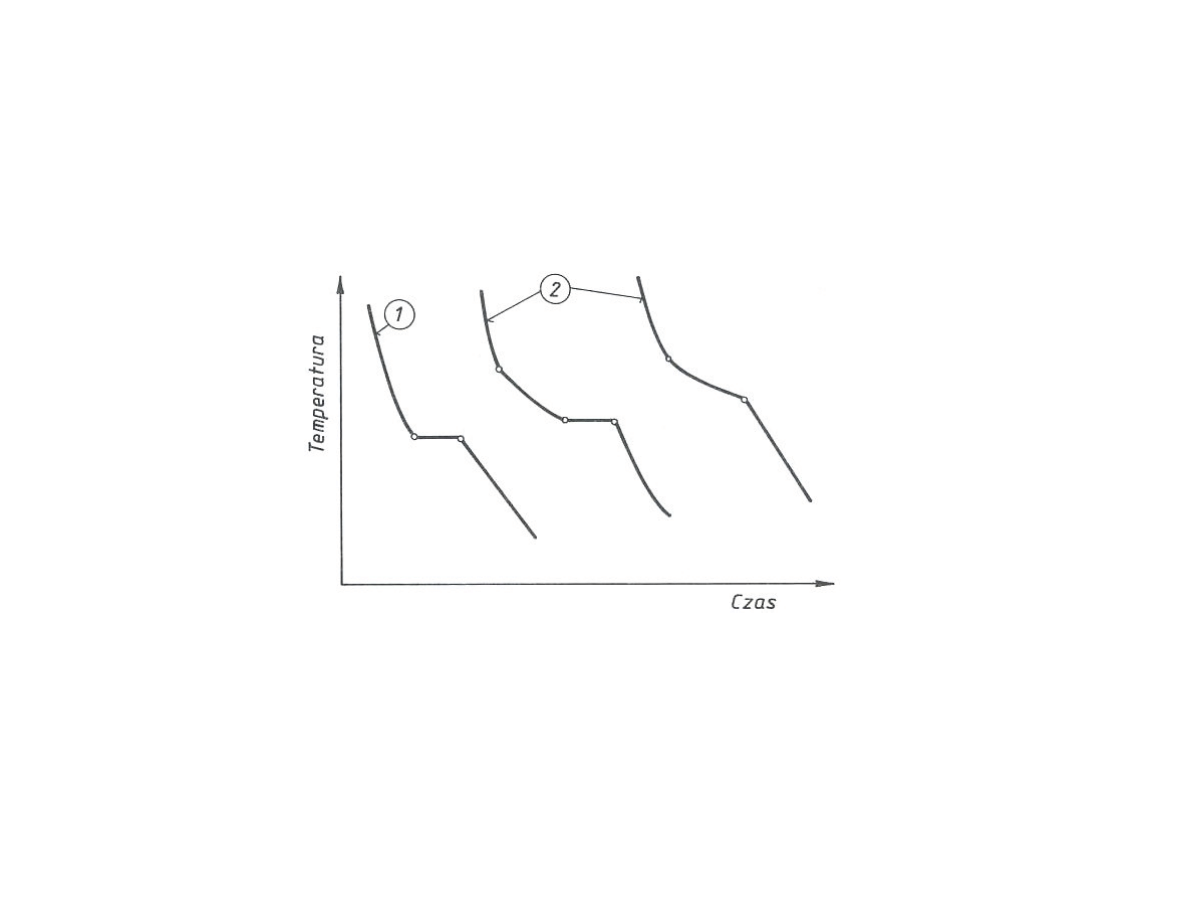
Krystalizacja stopów – cechy charakterystyczne
• skład fazy ciekłej i stałej zmieniają się w trakcie krystalizacji
• krystalizacja przebiega zwykle w zakresie temperatur (likwidus – solidus)
Zmiany temperatury metalu (1) i stopów metali (2) w trakcie krystalizacji
Faza – część układu o makroskopowo jednakowych właściwościach
termodynamicznych (skład, budowa, właściwości), oddzielona od pozostałej części
powierzchnią rozdziału – granicą faz
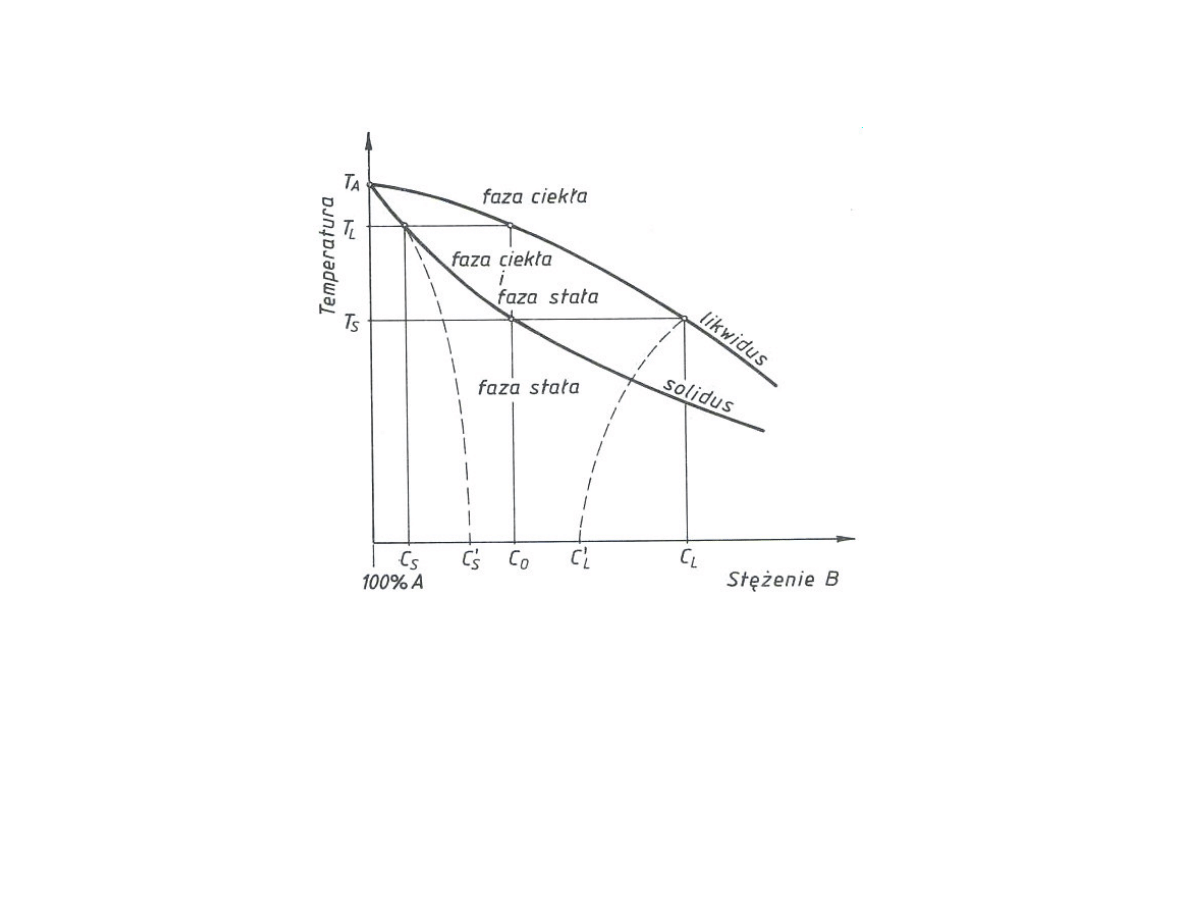
Segregacja dendrytyczna - zróżnicowanie składu chemicznego w
obrębie dendrytu lub ziarna fazy stałej, będące wynikiem krystalizacji w
zakresie temperatur likwidus – solidus
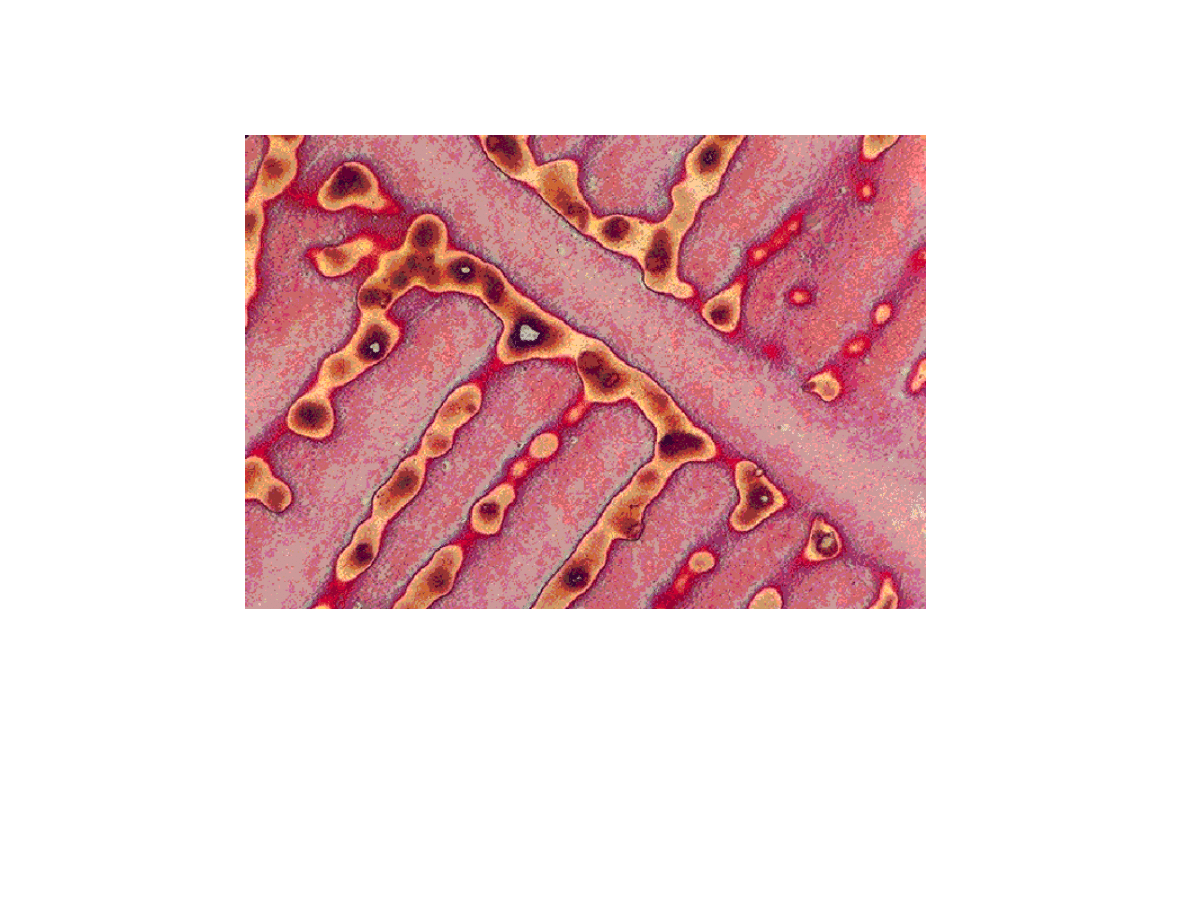
Różne zabarwienie odpowiada różnemu stężeniu składników stopu
- segregacja dendrytyczna
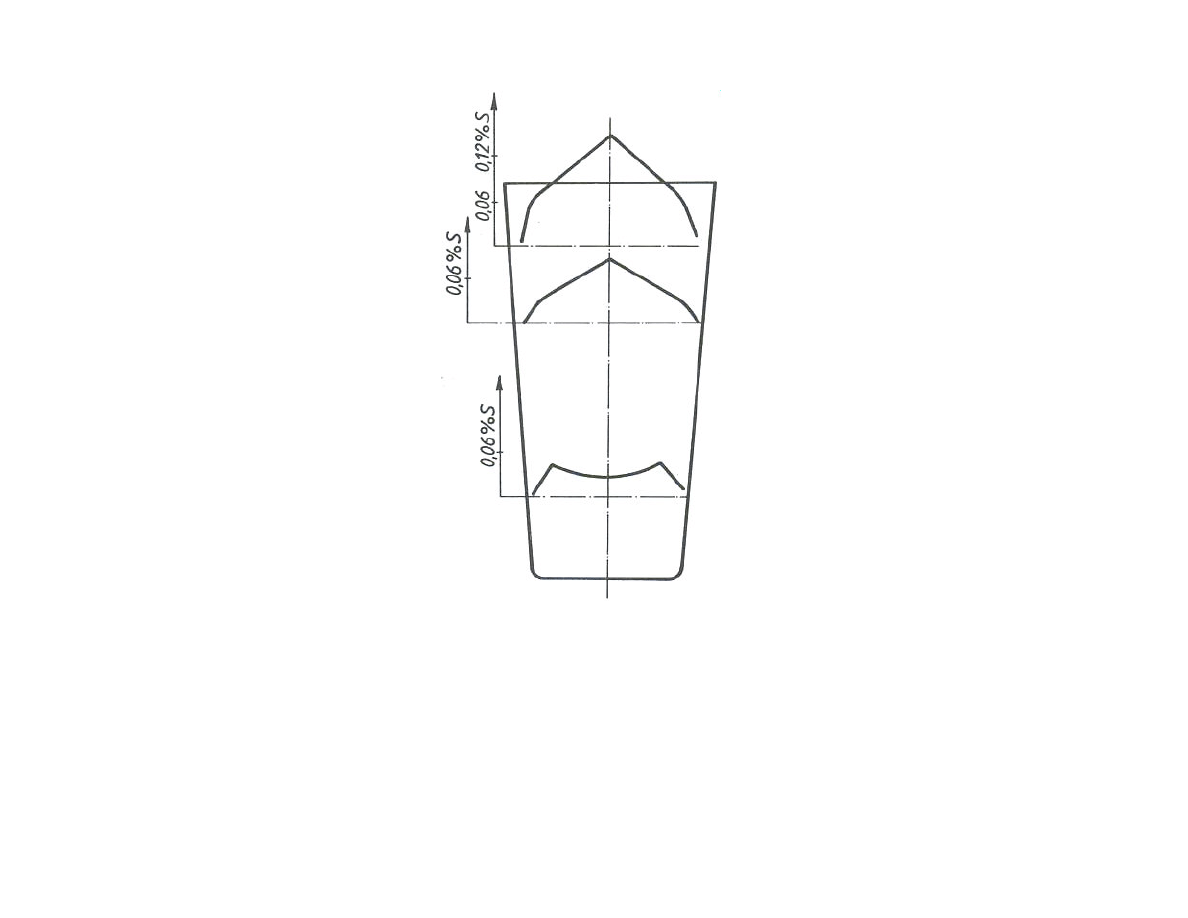
Segregacja w skali makroskopowej - zróżnicowanie składu
chemicznego w objętości odlanego elementu, będące wynikiem
stopniowego krzepnięcia elementu oraz obecności cząstek
niemetalicznych (siarczki, tlenki)
Struktura pierwotna – struktura utworzona podczas krystalizacji.
Charakter struktury zależy głównie od:
• szybkości chłodzenia
• obecności obcych wtrąceń, będących zarodkami krystalizacji
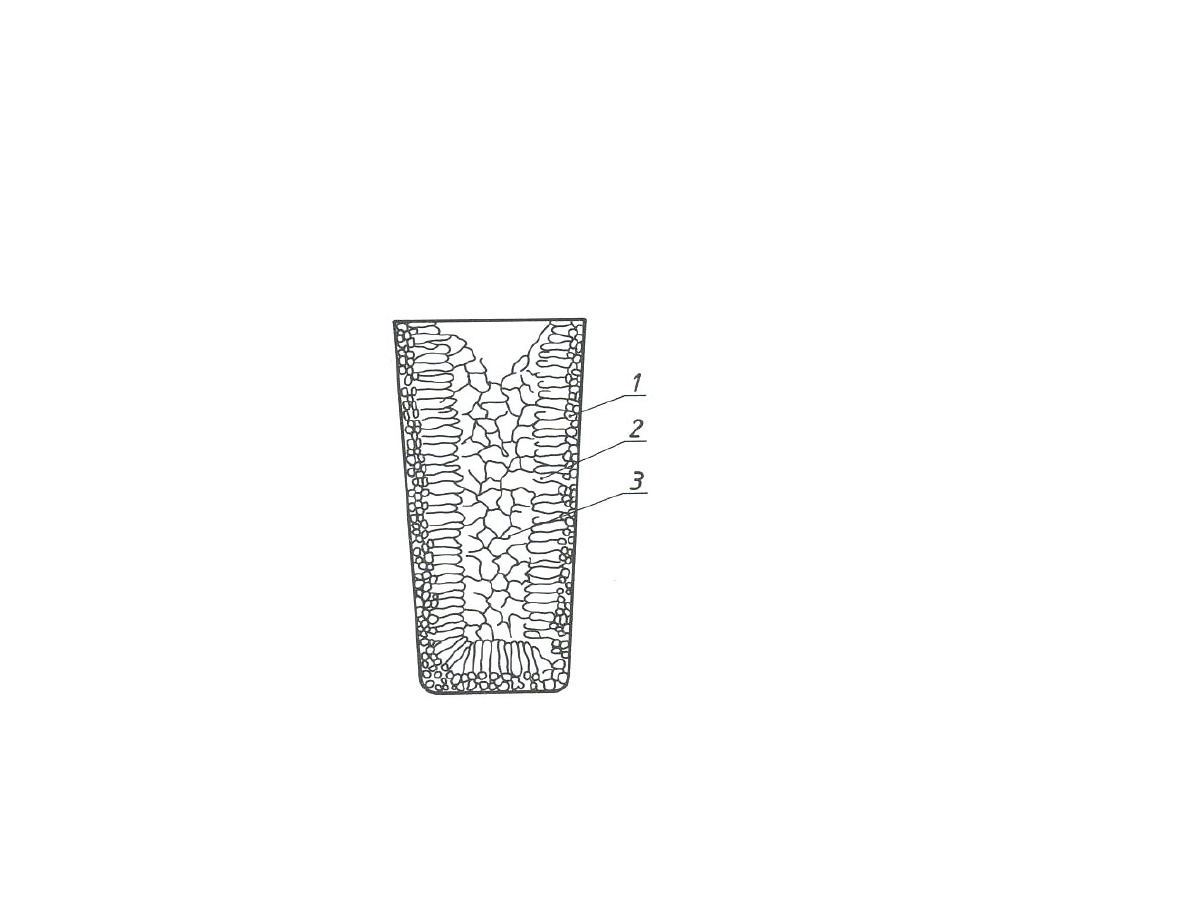
Struktura pierwotna wlewka. Ziarna metalu o różnym kształcie i
wielkości: 1- kryształy zamrożone, 2 – kryształy słupkowe, 3 –
kryształy wolne (równoosiowe)
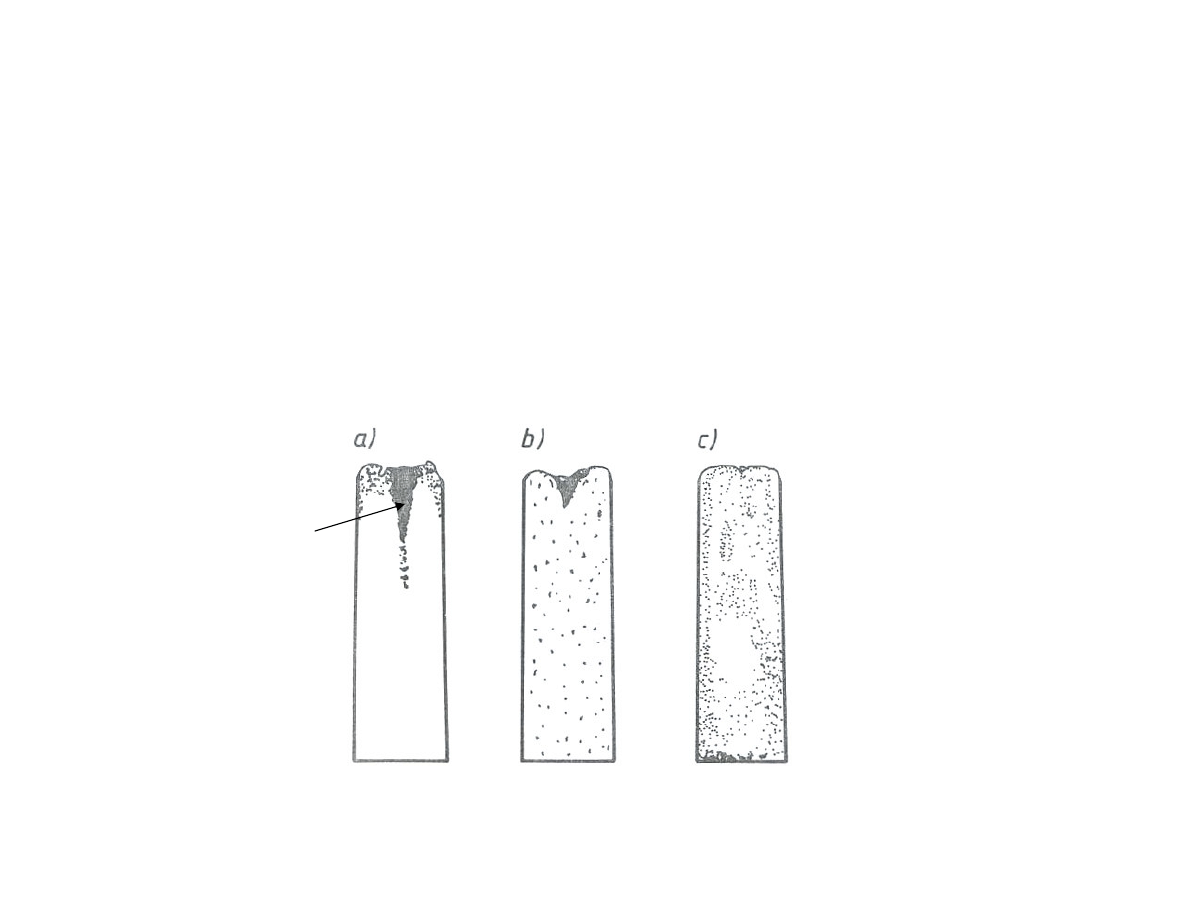
Struktura pierwotna wlewka stali: a) uspokojonej, b) półuspokojonej,
c) nieuspokojonej
Porowatość powstała podczas krystalizacji – np. w wyniku wydzielania
się ze ciekłej stali dwutlenku węgla : FeO + C = CO
2
↑+ Fe, czemu
można zapobiec dodając odtleniacze.
a) Stal uspokojona – odtleniona dostateczną ilością Si, Mn, Al
b) Stal półuspokojona – częściowo odtleniona
c) Stal nieuspokojona – odtleniona w niewielkim stopniu Mn
Jama usadowa
Wyszukiwarka
Podobne podstrony:
Otrzymywanie metali z rud
Otrzymywanie metali metodami elektrochemicznymi
Otrzymywanie metali
Metalurgia sciaga, Metalurgia - to nauka zajmująca się otrzymywaniem metali z rud, Ruda- utwory skal
Metalurgia i odlewnictwo pytania odp, Metalurgia sciaga, Metalurgia - to nauka zajmująca się otrzymy
Przykłady metod hutniczych otrzymywania metali
Otrzymywanie produktów krystalicznych w reaktorze o działaniu ciągłym
Otrzymywanie metali(1)
hoffmann, Technologia chemiczna – surowce i procesy przemysłu nieorganicznego L,OTRZYMYWANIE PRODUKT
Otrzymywanie metali
3struktura krystaliczna metali
Krystaliczna skruktura metali, Księgozbiór, Studia, Materiałoznastwo
wykład+nr+3+ +Krystalizacja+metali +Fazy+stopów
Otrzymywanie proszków metali metodami elektrochemicznymi
W5 Krystalizacja metali
Krystaliczna struktura metali - laborka, Automatyka i Robotyka, Semestr 3, Obróbka cieplna i powier
więcej podobnych podstron