ROZDZIA 1. TERMODYNAMIKA
Mariusz Mroczek
Ad e) Na pocz¡tek obliczymy liczb¦ moli gazu, pomno»on¡ przez staª¡ gazow¡, poniewa» wiel-
ko±¢ nR b¦dzie wyst¦powaªa w kolejnych wzorach. Do tego celu mo»na skorzysta¢ z równania
stanu, np. dla stanu A:
p
A
V
A
= nRT
A
,
nR =
p
A
V
A
T
A
=
2 · 10
5
· 10 · 10
−3
400
= 5
J/K.
Warto sprawdzi¢, »e wynik jest taki sam dla stanu B oraz C.
Dla izochorycznej przemiany A → B mamy:
Q
AB
= nc
V
∆T
AB
= n
3
2
R ∆T
AB
=
3
2
· 5 · (1000 − 400) = 4 500
J;
∆U
AB
= Q
AB
(z wªasno±ci przemiany), ∆U
AB
= 4 500
J;
W
AB
= 0.
Dla izobarycznej przemiany C → A mamy:
Q
CA
= nc
p
∆T
CA
= n
5
2
R ∆T
CA
=
5
2
· 5 · (400 − 1000) = −7 500
J;
∆U
CA
= nc
V
∆T
CA
= n
3
2
R ∆T
CA
=
3
2
· 5 · (400 − 1000) = −4 500
J;
∆U
CA
= Q
CA
+ W
CA
,
−4 500
J = −7 500 J + W
CA
,
W
CA
= 3 000
J.
Zwró¢my uwag¦ na znaki obliczonych wielko±ci.
Przykªad 1.8.6 (Cykl przemian, sprawno±¢ cyklu)
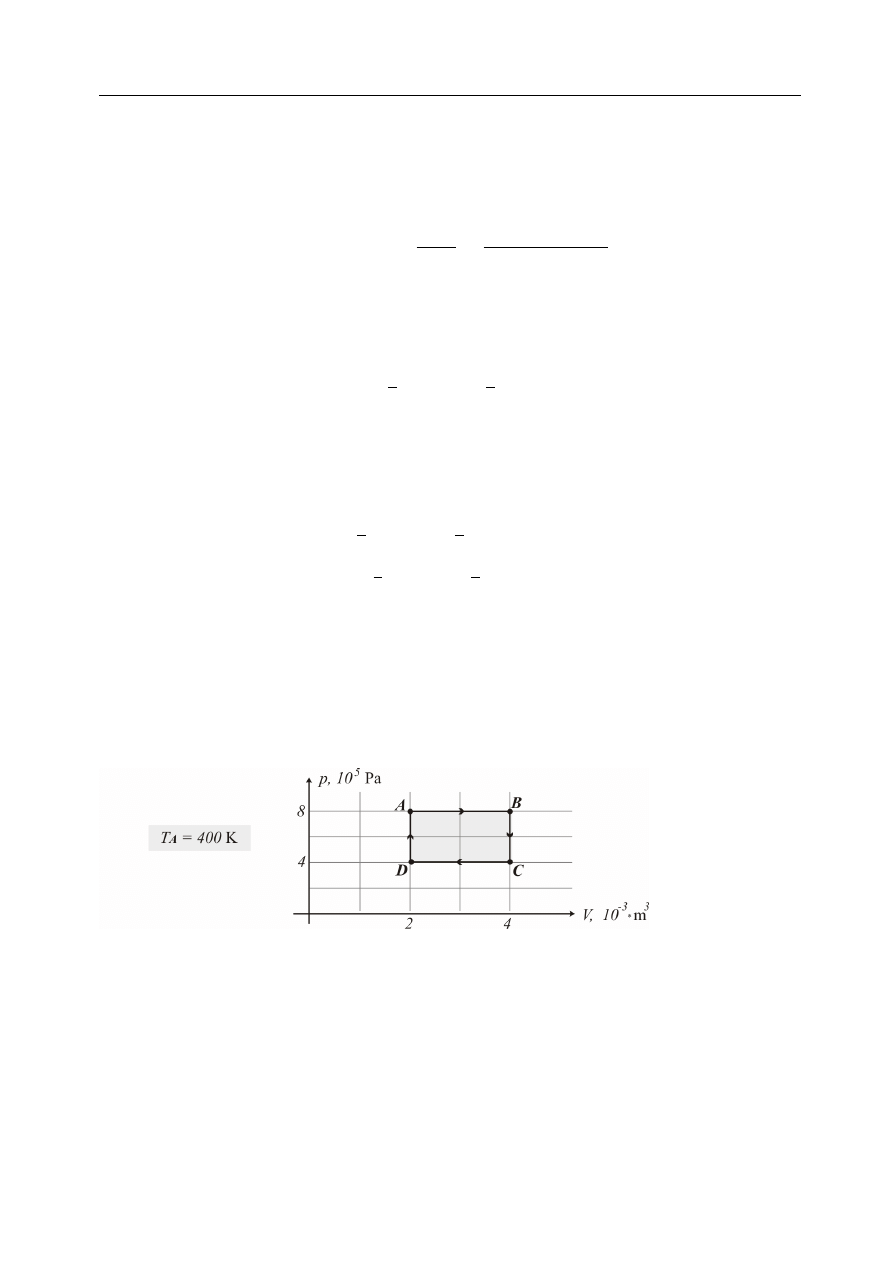
Na zamieszczonym wykresie, w pªaszczy¹nie parametrów stanu (V, p), przedstawiony jest pe-
wien cykl przemian gazu doskonaªego. Temperatura gazu w stanie A wynosi T
A
= 400 K
.
a) Doko«cz zdania:
Przemiany A → B oraz C → D s¡ przemianami ...............................
Przemiany B → C oraz D → A s¡ przemianami ...............................
b) Oblicz |W
u
|
- warto±¢ bezwzgl¦dn¡ pracy u»ytecznej otrzymanej w efekcie cyklu przemian
A → B → C → D → A
.
c) Oblicz temperatury gazu: T
B
, T
C
, T
D
, gdy znajdowaª si¦ on odpowiednio w stanach: B,
C
, D.
32
EDUKARIS
1.8. PRZYKADY Z ROZWIZANIAMI
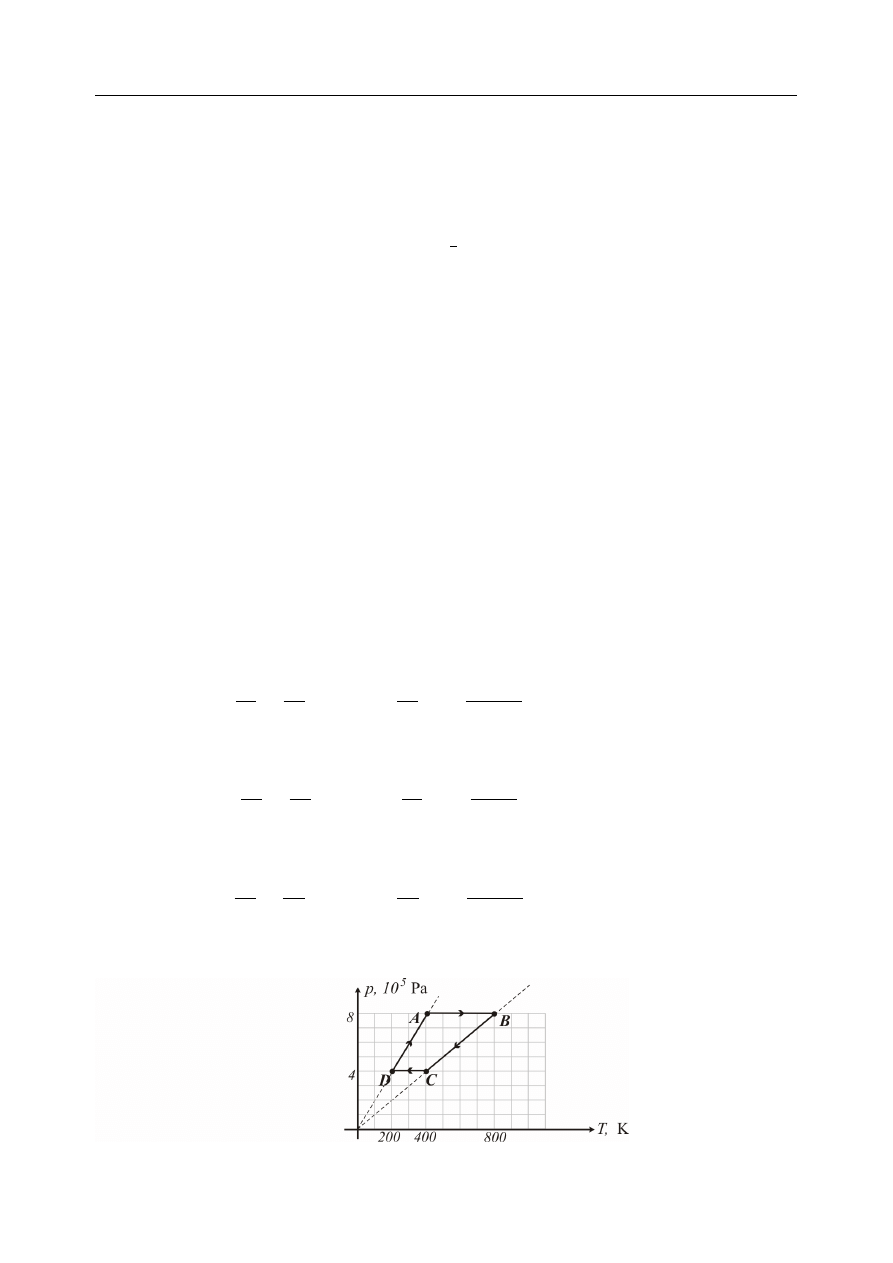
d) Korzystaj¡c z rozwi¡zania podpunktu b), narysuj wykres przemian w cyklu A → B →
C → D → A
w pªaszczy¹nie (T, p).
e) Na których etapach cyklu gaz pobiera ciepªo a na których oddaje ciepªo?
f) Oblicz ilo±¢ ciepªa wymienionego z otoczeniem na poszczególnych etapach cyklu. Ile wy-
nosi ich suma? Przyjmij, dla tego gazu C
V
=
3
2
R
.
g) Oblicz sprawno±¢ tego cyklu.
Rozwi¡zanie
Oznaczenia oraz dane przyjmujemy jak w tre±ci zadania oraz jak na rysunku.
Ad a)
Przemiany A → B oraz C → D s¡ przemianami izobarycznymi.
Przemiany B → C oraz D → A s¡ przemianami izochorycznymi.
Ad b) Warto±¢ bezwzgl¦dna pracy u»ytecznej otrzymanej w efekcie cyklu przemian A → B →
C → D → A
jest równa liczbowo polu ograniczonemu gur¡ ABCD. W tym wypadku mo»na
ªatwo obliczy¢ pole:
|W
u
| =
pole gury ABCD = 4 · 10
5
· 2 · 10
−3
J = 800 J.
Ad c) Temperatury w odpowiednich stanach obliczamy z wªasno±ci przemian. Poniewa»
przemiana A → B jest izobaryczna, to dla takiej zachodzi:
V
A
T
A
=
V
B
T
B
,
T
B
=
V
B
V
A
T
A
=
4 · 10
−3
2 · 10
−3
· 400
K = 800 K.
Dla izochorycznej przemiany B → C mamy:
p
B
T
B
=
p
C
T
C
,
T
C
=
p
C
p
B
T
B
=
4 · 10
5
8 · 10
5
· 800
K = 400 K.
Nast¦pna przemiana, C → D, jest izobaryczna:
V
C
T
C
=
V
D
T
D
,
T
D
=
V
D
V
C
T
C
=
2 · 10
−3
4 · 10
−3
· 400
K = 200 K.
Ad d) Wykres cyklu w pªaszczy¹nie (T, p) prezentuje zamieszczony ni»ej rysunek.
33

ROZDZIA 1. TERMODYNAMIKA
Mariusz Mroczek
Ad e) W przemianie A → B gaz pobiera ciepªo (rozpr¦»anie izobaryczne, wzrost tempera-
tury).
W przemianie B → C gaz oddaje ciepªo (izochoryczne chªodzenie, spadek temperatury).
W przemianie C → D gaz oddaje ciepªo (spr¦»anie izobaryczne, spadek temperatury).
W przemianie D → A gaz pobiera ciepªo (izochoryczne ogrzewanie, wzrost temperatury).
Ad f) Na pocz¡tek obliczymy liczb¦ moli gazu, pomno»on¡ przez staª¡ gazow¡, poniewa» wiel-
ko±¢ nR b¦dzie wyst¦powaªa w dalszych wzorach. Do tego celu mo»na skorzysta¢ z równania
stanu, np. dla stanu A:
p
A
V
A
= nRT
A
,
nR =
p
A
V
A
T
A
=
8 · 10
5
· 2 · 10
−3
400
= 4
J/K.
Obliczamy ciepªo pobrane przez gaz w przemianie izobarycznej A → B:
Q
AB
= nc
p
∆T
AB
;
Q
AB
= n
5
2
R ∆T
AB
=
5
2
· 4 · (800 − 400) = 4 000
J.
Obliczamy ciepªo oddane przez gaz w przemianie izochorycznej B → C:
Q
BC
= nc
V
∆T
BC
;
Q
BC
= n
3
2
R ∆T
BC
=
3
2
· 4 · (400 − 800) = −2 400
J.
Obliczamy ciepªo oddane przez gaz w przemianie izobarycznej C → D:
Q
CD
= nc
p
∆T
CD
;
Q
CD
= n
5
2
R ∆T
CD
=
5
2
· 4 · (200 − 400) = −2 000
J.
Obliczamy ciepªo pobrane przez gaz w przemianie izochorycznej D → A:
Q
DA
= nc
V
∆T
DA
;
Q
DA
= n
3
2
R ∆T
DA
=
3
2
· 4 · (400 − 200) = 1 200
J.
Zauwa»my, »e ilo±¢ ciepªa wymienionego z otoczeniem wynosi:
Q
pobrane
+ Q
oddane
= 4 000
J + 1 200 J − 2 400 J − 2 000 J = 800 J,
tyle, co praca u»yteczna uzyskana w cyklu. Odpowiedz dlaczego tak jest?
Ad g) Obliczamy sprawno±¢ naszego cyklu:
η =
|W
u
|
Q
pobrane
,
η =
800
4 000 + 1 200
≈ 0, 15.
34
Wyszukiwarka
Podobne podstrony:
A32 Ziyang J Cat 2001 id 49773 Nieznany (2)
podreczny sprzet gasniczy id 36 Nieznany
cat 6AD en id 108772 Nieznany
Podrecznik SystemInformation id Nieznany
podreczniki 2 id 365831 Nieznany
Cheshire Cat C50 id 113534 Nieznany
podrecznik do komunikacji id 36 Nieznany
A32 Ziyang J Cat 2001 id 49773 Nieznany (2)
Abolicja podatkowa id 50334 Nieznany (2)
4 LIDER MENEDZER id 37733 Nieznany (2)
katechezy MB id 233498 Nieznany
metro sciaga id 296943 Nieznany
perf id 354744 Nieznany
interbase id 92028 Nieznany
Mbaku id 289860 Nieznany
Probiotyki antybiotyki id 66316 Nieznany
miedziowanie cz 2 id 113259 Nieznany
LTC1729 id 273494 Nieznany
więcej podobnych podstron