
Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
1. Pielęgniarstwo anestezjologiczne — rys historyczny
1.1.
Znieczulenie
1.2. Aparaty do znieczulenia
1.3. Historia resuscytacji
2. Ocena stanu zdrowia i życia w miejscu wypadku
3. Reanimacja krążeniowo-oddechowa — CPR
3.1. Etapy postępowania resuscytacyjnego
4. Elektroterapia — rola pielęgniarki
5. Farmakoterapia — drogi podawania leków
Bibliografia
Literatura podstawowa
Literatura dodatkowa
1

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
1. Pielęgniarstwo anestezjologiczne — rys historyczny
W podawaniu znieczuleń i w opiece nad chorym znieczulonym osoby pełniące funkcje
pielęgniarskie wyprzedziły lekarzy.
Podawaniem pierwszych znieczuleń i opieką nad pacjentem w sali operacyjnej do lat
1940–1950 powszechnie zajmowały się siostry zakonne i pielęgniarze.
Całe rzesze sióstr zakonnych przez wiele lat podawały samodzielnie „narkozę” używając
do tego celu chloroformu, eteru, chlorku etylu, a nawet dożylnie — przy użyciu
pierwszych barbituranów. Anestezjologia w Polsce — jako niezależna medyczna
specjalność — powstała w 1952 roku (obchodziła więc swoje pięćdziesięciolecie w 2002
roku). Jej rozwój wymagał od pielęgniarek poszerzenia wiedzy na temat tej specjalności.
W latach 70. zmieniło się oblicze pielęgniarstwa wobec wzmacniania się pozycji
anestezjologii, co spowodowało wzrost naboru pielęgniarek do pracy w tych oddziałach
oraz intensywne podnoszenie kwalifikacji przez organizowanie kursów.
Kształcenie podyplomowe pielęgniarek w tej dziedzinie to kurs kwalifikacyjny. Warto tu
wspomnieć, że pierwsze takie kursy odbywały się wspólnie dla lekarzy i pielęgniarek,
a więc od pierwszej chwili rozwoju anestezjologii i intensywnej terapii lekarz
i pielęgniarka uczyli się razem intensywnego leczenia, pielęgnowania, rehabilitowania,
całodziennej najlepszej opieki.
12 grudnia 1981 roku weszło Rozporządzenie MZiOS w sprawie szkolenia
specjalizacyjnego pielęgniarek i położnych (DzU MZiOS Nr 1 z 1982 roku), zaś
zarządzenie Ministra Zdrowia i Opieki Społecznej z dnia 27 lutego 1998 roku DzU Nr 37
jest podstawą prawną anestezjologii i intensywnej terapii, określa miejsce i zadania
pielęgniarki anestezjologicznej (anestezjolog znieczula w asyście pielęgniarki).
Ważnym wydarzeniem w dziedzinie rozwoju pielęgniarstwa anestezjologicznego miało być
wyodrębnienie 18 kwietnia 1980 roku, na posiedzeniu Towarzystwa Anestezjologii
i Intensywnej Terapii w Poznaniu, Sekcji Pielęgniarstwa przy Zarządzie Głównym
Polskiego Towarzystwa Anestezjologii i Intensywnej Terapii. Warto zaznaczyć, że od lat
80. powstawały pierwsze prace magisterskie na wydziałach pielęgniarskich w Akademiach
Medycznych z dziedziny anestezjologii lub pielęgniarstwa anestezjologicznego
i intensywnej opieki.
2

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Pielęgniarki w anestezjologii i intensywnej terapii stanowią istotny trzon zespołu
medycznego, prowadzą wysokospecjalistyczną opiekę. Dostateczna liczba dobrze
przygotowanych pielęgniarek w stosunku do liczby leczonych pacjentów stanowi
o rzeczywistej jakości opieki. Od pielęgniarki anestezjologicznej wymaga się znajomości
i umiejętności stabilizacji funkcji życiowych, znajomości sprzętu i aparatury
specjalistycznej, znajomości leków, umiejętności ścisłej obserwacji chorego i jej
interpretacji. Od pielęgniarek wymaga się opanowania, cierpliwości, współczucia
i zrozumienia. W pracy obciążonej tak dużym wysiłkiem i wysoką odpowiedzialnością
ścisła współpraca lekarsko-pielęgniarska jest bardzo ważnym elementem szeroko
pojętego bezpieczeństwa pacjenta i personelu.
1.1. Znieczulenie
Pokonanie bólu podczas zabiegów operacyjnych radykalnie wpłynęło na postęp chirurgii.
Stało się to możliwe dzięki wprowadzeniu do lecznictwa anestetyków. W roku 1844 próby
zastosowania podtlenku azotu do zabiegów stomatologicznych podjął amerykański
dentysta Horace Wells. Publiczny pokaz nie przyniósł sukcesu, przeciwnie — został on
wyśmiany przez zebranych lekarzy i studentów.
Polski lekarz pracujący w Petersburgu — Stanisław Klikowicz — w 1880 roku
opublikował doniesienia o zastosowaniu podtlenku przy porodzie — w tym celu i nie tylko
— podawany jest do dzisiejszego dnia. Równocześnie w laboratoriach chemicznych
przeprowadzano pierwsze badania nad działaniem eteru. Zabiegu operacyjnego z tym
środkiem dokonano 16 października, była to operacja wycięcia guza szyi. W Polsce po raz
pierwszy eter do narkozy zastosował w klinice krakowskiej 7 lutego 1847 roku Ludwik
Bierkowski.
Wciąż trwały poszukiwania nowych środków. Wśród nich znalazły się chlorek etylu oraz
wodzian chloralu. Jednocześnie wysuwano pierwsze wątpliwości co do pełnego
bezpieczeństwa narkozy. Rozpiętość między skuteczną dawką znieczulającą a śmiertelną
okazała się tak mała, że łatwo było ją przekroczyć nawet przy zachowaniu środków
ostrożności. James Young Simpson (1811–1870) po przeprowadzeniu 50 prób
zsyntetyzowanym chloroformem uznał, że ten środek jest lepszy od eteru
i w 1847 roku dla Edynburskiego Towarzystwa Lekarskiego przeprowadził swoje
doświadczenia. Chloroform wzbudził wielką sensację — zwłaszcza, że działał pewniej
i szybciej od stosowanych dotychczas podtlenku azotu i eteru. Warto wspomnieć, że
3

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
chloroform zastosowano podczas porodu u królowej Wiktorii, a odkrywca tej metody —
Simpson —
otrzymał z jej rąk tytuł lorda.
Jednak po narkozie chloroformowej miało miejsce kilka zejść śmiertelnych. Zaczęto więc
podejmować próby zmniejszania niebezpieczeństwa, mieszając chloroform z eterem
i z alkoholem. Przy odpowiednim stosowaniu środków ostrożności chloroform używany
był do narkozy przez około 100 lat.
Udanym początkiem anestezji dożylnej było wprowadzenie w 1933 roku przez
farmakologa Helmutha Weesa preparatu Evipan-Natrium. Po wprowadzeniu innych
środków narkoza dożylna ograniczała narkozę wziewną. Obecnie możemy połączyć te
metody.
1.2. Aparaty do znieczulenia
Z narkozą wiąże się wprowadzenie masek i aparatów umożliwiające stopniowe
dawkowanie środka anestetycznego. Pierwsze oryginalne aparaty do znieczulenia
pochodzą z lat 40. XIX wieku — były to kawałki materiału trzymane przed twarzą
pacjenta. Wells, który jest odkrywcą N
2
O, jest też twórcą pierwszego aparatu do
znieczulenia. Była to maska twarzowa z pojemnikiem zawierającym podtlenek azotu.
W 1846 roku, w uwieńczonej sukcesem demonstracji znieczulenia eterowego, Wiliam
Morton (1819–1868) zastosował szklany parownik. Lekarze praktykujący dostosowywali
części aparatury, która mogła być użyta do inhalacji leków — wtedy to wiele szklanych,
a nawet i mosiężnych urządzeń stało się aparatami do znieczulenia.
Najprostsze maski to maski Kurta Schimmelbuscha (1860–1895), które — obłożone gazą
— umożliwiały kroplowe podawanie eteru na ich powierzchnię, a pacjent wdychał
wydobywające się opary. Maska ta pojawiła się w 1890 r. i szybko stała się najbardziej
popularna wśród tego typu przyrządów.
Thomas Clover stworzył trzy podstawowe aparaty do znieczulenia. Pierwszy to pojemnik
na opary chloroformu. Drugi to aparat szeregowy, który umożliwiał wprowadzenie
podtlenku azotu, poprzedzając znieczulenie eterowe. Trzeci natomiast to przenośny
parownik do inhalacji eterowej, który stał się popularny na całym świecie.
4

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Na początku XX wieku budową aparatów do znieczulenia zajęli się fizycy i inżynierowie.
Udoskonalone aparaty skonstruował Dräger — miały one obieg zamknięty i wentylatory.
W latach 50. XX wieku wprowadzono do praktyki anestezjologicznej sztuczne
wentylatory, a więc aparat do znieczulenia został na stałe połączony z respiratorem. Na
salach operacyjnych pojawiła się olbrzymia ilość sprzętu medycznego, aparaty do
pomiaru ciśnienia krwi, aparaty do EKG. Rozwój elektroniki szybko postępuje, wraz z nim
nowe aparaty i monitory. Dziś są to już aparaty do znieczuleń z wbudowanymi
monitorami i wbudowanym układem ssącym.
1.3. Historia resuscytacji
Pierwsza skuteczna reanimacja została opisana w Biblii, w Księdze Królewskiej — wtedy
to prorok Eliasz pozornie ożywiał zmarłe dziecko.
W starożytnym Egipcie i starożytnej Japonii podejmowano resuscytację, stosując
powieszenie głową w dół, rolując na beczce, przewożąc na wole lub koniu.
W Ameryce Południowej Indianie zastosowali w resuscytacji niekonwencjonalne metody,
np. wpuszczali dym z fajki do odbytnicy. Początki bardziej naukowego podejścia do tego
problemu datuje się na rok 1543 — wtedy Versalius wdmuchiwał zwierzęciu powietrze
poprzez trzcinę umieszczoną w tchawicy. Szczegóły intubacji tchawicy i wentylowania
płuc opisali Cullen i lord Cathcart w 1776 roku. Stwierdzono wówczas, że jeżeli oddech
usta–usta lub usta–nos jest niewystarczający, należy wprowadzić do głośni lub do
tchawicy rurkę i przez nią podawać powietrze. Zaobserwowano wtedy również, że jeżeli
wentylujemy płuca psa zaintubowanego, serce podejmuje czynność, przy zaprzestaniu
wentylacji — serce ponownie się zatrzymuje. Postęp resuscytacji wynika również
z zastosowania defibrylacji, która przywraca spontaniczną akcję serca.
W wieku XIX wentylację płuc wdmuchiwanym powietrzem zastąpiono wykonywaniem
biernych ruchów klatki piersiowej. W XX wieku natomiast opracowano szereg innych
metod usprawniających, takich jak np. unoszenie kończyn, by zwiększyć objętość
wdechu. Rozwój podstawowych metod resuscytacji opartych na rzetelnych
eksperymentach naukowych nastąpił w latach 50., spopularyzowano wtedy wentylację
powietrzem wydechowym ratownika, a także udowodniono, że można uzyskać
wystarczającą wymianę gazową u pacjentów zwiotczonych.
5

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Badania Petera Safara (1924–2003) — twórcy nowoczesnej reanimacji — wykazały, że
drożność dróg oddechowych można skutecznie uzyskać przez odchylenie głowy do tyłu
i wysunięcie żuchwy ku przodowi, co zapobiega niedrożności spowodowanej przez tkanki
miękkie.
Rozwój nowoczesnych technik resuscytacji krążeniowo-oddechowej CPR datuje się na lata
60. ubiegłego stulecia. Sukces i siła tych metod wynika z możliwości ich zastosowania
w każdym miejscu, również przez osoby, które nie są fachowcami w tej dziedzinie.
Postęp na polu resuscytacji to opracowanie zasad resuscytacji i dobrych programów
edukacji. Europejska Rada ds. Resuscytacji (European Resuscitation Council — ERC)
założona została w 1989 roku jako Rada Interdyscyplinarna ds. Resuscytacji i Medycyny
Ratunkowej.
W 1992 roku ERC zaprezentowała na I Kongresie Naukowym ERC w Brighton (Wielka
Brytania) zasady:
⎯ podstawowych metod podtrzymywania życia (Basic Life Suport — BLS),
⎯ zaawansowanych metod podtrzymywania życia (Advanced Life Suport — ALS).
W 1994 roku zostały zaprezentowane zalecenia dla podtrzymywania życia w pediatrii
(Pediatric Life Support — PLS) i zalecenia dotyczące postępowania w zaburzeniach rytmu
serca przed zatrzymaniem krążenia na drugim Kongresie w Moguncji (Niemcy).
Zadaniem ERC jest ochrona życia poprzez ulepszenie standardów prowadzenia
resuscytacji w Europie i koordynowanie aktywności innych europejskich organizacji, które
zajmują się głównie resuscytacją krążeniowo-oddechową (Cardiopulmonary Resuscitation
— CPR).
ERC realizuje swoje zadania przez:
⎯ tworzenie zaleceń i wskazań, właściwych dla Europy, w celu ćwiczenia resuscytacji
krążeniowo-oddechowej i mózgowej,
⎯ uaktualnianie tych zleceń w świetle krytycznego przeglądu ćwiczeń CPR,
⎯ promowanie kontroli ćwiczeń resuscytacyjnych zawierających standaryzację zapisu
prób resuscytacji,
6

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
⎯ projektowanie standaryzowanych programów nauczania przeznaczonych dla
wszystkich ćwiczących w Europie, o zasięgu obejmującym społeczeństwo
i kwalifikowanych lekarzy,
⎯ promowanie i koordynowanie odpowiednich badań,
⎯ organizowanie stosownych kongresów i innych spotkań naukowych w Europie,
⎯ promowanie politycznej i społecznej świadomości wymogów i ćwiczeń resuscytacji
w Europie.
7

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
2. Ocena stanu zdrowia i życia w miejscu wypadku
Wypadki stanowią nadal najczęstszą przyczynę zgonów wśród dzieci i dorosłych do
45 roku życia. Ta ogólna zła sytuacja wymaga, aby urazom poświęcić więcej uwagi
i środków w celu skuteczniejszego zapobiegania im i leczenia ich następstw. W tym
module zwrócono uwagę zarówno na rozpoznanie stanu zagrożenia życia, podjęcie
czynności ratowniczych, jak i na bezpieczeństwo zespołu ratowniczego. Istnieje
określenie, że medycyna jest zajęciem stworzonym dla osób o usposobieniu obsesyjno-
kompulsywnym. Dotyczy to zwłaszcza osób pracujących w ratownictwie, ponieważ wiele
zależy od tego, w jaki sposób zespół zatroszczy się o szczegóły. Zespół ratunkowy musi:
⎯ dbać o swoją karetkę, by była gotowa do wyjazdu,
⎯ znać najszybszą drogę dojazdu do miejsca wezwania,
⎯ wiedzieć, jak ocenić miejsce pod kątem obecności dodatkowych zagrożeń,
⎯ wiedzieć, kiedy miejsce wypadku jest bezpieczne, a jeśli nie jest, to co należy zrobić,
⎯ wiedzieć, kiedy należy wezwać pomoc,
⎯ znać sprzęt i utrzymać go w gotowości,
⎯ wybrać szpital najwłaściwszy dla poszkodowanego i najlepszą drogę dojazdu.
Ocena miejsca zdarzenia, miejsca urazu zaczyna się od czynności, które są wykonane
przed podejściem do chorego. Ocena miejsca zdarzenia obejmuje:
⎯ bezpieczeństwo własne,
⎯ bezpieczeństwo na miejscu zdarzenia,
⎯ wstępną segregację poszkodowanych i ogólną liczbę chorych,
⎯ niezbędny sprzęt oraz potrzebę dodatkowych środków,
⎯ mechanizm urazu.
Bezpieczeństwo własne
Ratownik najbardziej narażony jest na zakażenie przez płyny ustrojowe, jak również
poprzez wentylację zastępczą. Rękawiczki są obowiązkowe, ochraniacz na oczy i maska
powinny się znaleźć u ratownika odpowiedzialnego za drożność dróg oddechowych.
Należy pamiętać o ochronie samych chorych przez zmianę rękawiczek przed udzielaniem
pomocy kolejnemu poszkodowanemu.
W czasie reanimacji pomiędzy pacjentem a ratownikiem istnieje możliwość przeniesienia
zakażenia. Mimo że ze śliny osoby zakażonej można wyizolować drobnoustroje
chorobotwórcze, przekazywanie przez ślinę wirusów obecnych we krwi należy do
8

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
rzadkości. Dotąd opisano zaledwie 15 udokumentowanych przypadków zakażenia
związanego z BLS, w większości tych przypadków chodzi o bakterie. Nie opisano
zakażenia wirusem zapalenia wątroby typu B ani typu C. Opisano trzy przypadki
zakażenia HIV nabytego w trakcie resuscytacji zakażonych pacjentów, w dwóch spośród
tych przypadków doszło do głębokiego zakłucia igłą, zaś w trzecim doszło do zabrudzenia
rąk z otarciem naskórka. Duże zaniepokojenie budzi narastanie liczby świeżych zakażeń
gruźlicą. Dane te pochodzą z 2003 roku. Opracowane zostały przez Polską Radę
Resuscytacji, która została założona w 2001 roku.
Podczas resuscytacji ratownik powinien korzystać z rękawic i okularów ochronnych. Maski
twarzowe z zastawkami bezzwrotnymi zapobiegają przenoszeniu bakterii, skuteczność
masek bez zastawki nie jest dotychczas potwierdzona. Szczególnie uważnie trzeba się
obchodzić z ostrymi przedmiotami, które bezpośrednio po użyciu należy wyrzucać do
odpowiedniego pojemnika.
Bezpieczeństwo na miejscu zdarzenia
Bezpieczeństwo na miejscu zdarzenia wymaga uwzględnienia pewnych sytuacji:
⎯ kontaktu z ogniem lub substancjami toksycznymi,
⎯ niebezpieczeństwa porażenia prądem,
⎯ podejścia do poszkodowanego po lodzie, wodzie lub zboczu albo w pobliżu budynków
zagrożonych zawaleniem.
Nie należy wchodzić na teren obszarów, w których istnieje możliwość zmniejszonego
stężenia tlenu czy toksycznego stężenia substancji chemicznych bez odpowiedniego
zabezpieczenia.
Nigdy nie powinno się wchodzić na teren obszaru zagrożonego bez partnera i linii
zabezpieczającej. W przypadku wyżej wymienionej sytuacji poszkodowany powinien być
natychmiast wyniesiony z miejsca zdarzenia, nie oznacza to jednak, że ratownik powinien
narażać własne życie. W tym celu należy wezwać służby posiadające odpowiedni sprzęt,
np. straż pożarną, pogotowie energetyczne.
Segregacja poszkodowanych
Jeśli całkowita liczba poszkodowanych przewyższa możliwość udzielenia pomocy, należy
wezwać dodatkowe jednostki. Zwykle potrzebna jest jedna karetka na jednego
poszkodowanego. Ważne, by zespół ratowniczy sprawdził, czy liczba poszkodowanych
odpowiada scenie (sytuacji) zdarzenia. Jeśli chorzy są nieprzytomni i nie ma świadków
9

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
zdarzenia, należy zwrócić uwagę, czy nie ma poszlak wskazujących na obecność innych
poszkodowanych (np. plecaki, dokumenty, lista pasażerów autobusu).
Niezbędny sprzęt
Jeśli jest to możliwe, należy zabrać ze sobą na miejsce wypadku cały ratowniczy sprzęt —
w ten sposób zaoszczędzamy czas na ewentualny powrót do karetki.
Mechanizm urazu
Mechanizm urazu zazwyczaj jest oczywisty po obejrzeniu miejsca zdarzenia, ale sytuacja
może też wymagać zebrania wywiadu od poszkodowanego lub świadków wypadku.
Pewne obrażenia można przewidzieć, gdyż energia wyzwalana podczas wypadku podlega
prawom fizyki. Wobec tego poszkodowani w wypadku o dużej energii są szczególnie
narażeni na ciężkie obrażenia. Chociaż przy wstępnym badaniu nie stwierdza się u nich
objawów urazów zagrażających życiu, to powtórne badanie ukazuje nam ciężkie
obrażenia. Tak więc udzielając pomocy ofiarom wypadku, należy przyjąć, że doznali oni
ciężkich obrażeń — aż do momentu ich wykluczenia.
Na mechanizm urazu wpływają następujące czynniki:
⎯ prędkość uderzenia,
⎯ kinetyka i rozmiar ciała poszkodowanego,
⎯ mechanizm uwalniania energii, czyli rozległe zniszczenie pojazdu.
Wiedza na temat mechanizmu urazu pozwala trafnie przewidywać obrażenia wewnętrzne.
Urazy związane z ruchem to:
⎯ urazy tępe — powstałe w wyniku zderzenia, upadku, uderzenia tępym przedmiotem,
⎯ urazy przenikające — powstające na skutek upadku na umocowane obiekty, zakłucia
nożem.
Zadaniem jednostki ratownictwa jest segregacja chorych i identyfikacja stanów
bezpośredniego zagrożenia życia.
Ocena wstępna, która nie powinna trwać dłużej niż 2 minuty, została podzielona na
etapy:
1. Ogólne wrażenie, czyli ustalenie liczby poszkodowanych, w razie konieczności
wdrożenie protokołów postępowania w wypadku masowym, zaobserwowanie pozycji
10

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
poszkodowanego względem otaczających go przedmiotów, zachowania się chorego,
widoczne rany, krwawienia.
2. Obserwacja drożności dróg oddechowych (chrapanie, stridor).
3. Obserwacja krążenia — w czasie wyszukiwania tętna należy zwrócić uwagę na kolor
skóry, jej temperaturę, nawrót kapilarny u niemowląt i małych dzieci. W przypadku
krwawień opaski uciskowe należy stosować w wyjątkowych sytuacjach, w żadnym
wypadku nie wolno używać narzędzi do zatrzymania krwawienia, by nie uszkodzić
innych struktur biegnących w okolicy naczyń (nerwy).
Wstępna ocena pozwala na wyselekcjonowanie chorych priorytetowych:
⎯ ofiar urazów o niebezpiecznym mechanizmie,
⎯ chorych, u których stwierdzono:
• utratę przytomności,
• trudności w oddychaniu,
• zaburzenia perfuzji,
• występowanie silnego bólu,
⎯ chorych sprawiających ogólne złe wrażenie.
Takich chorych należy zakwalifikować do kategorii „ładuj i jedź”.
Przeżycie chorego z ciężkim urazem zależy od czasu. Związek pomiędzy czasem
chirurgicznego leczenia a przeżyciem chorych został opisany przez dr. Adamsa Cowley’a
z Oddziału Wstrząsu Urazowego w Baltimore w stanie Maryland w USA. Zauważył on, że
największą szansę przeżycia po urazie (ok. 85%) mieli chorzy, którzy trafili na salę
operacyjną w ciągu godziny od urazu, czas ten został nazwany „złotą godziną”
W warunkach przedszpitalnych mówi się o „platynowych dziesięciu minutach”, w ciągu
których należy zidentyfikować chorych, podjąć decyzje terapeutyczne i rozpocząć
transport poszkodowanych do odpowiednich oddziałów.
Interwencje, które przyczyniają się do pomyślnego wyniku końcowego po nagłym
zatrzymaniu krążenia tworzą „łańcuch przeżycia”. Tworzą go 4 ogniwa:
⎯ dostęp do służb pomocy doraźnej i zespołu resuscytacyjnego,
⎯ wczesne podjęcie podstawowych zabiegów resuscytacyjnych,
⎯ wczesne wykonanie defibrylacji,
⎯ wczesne podjęcie zaawansowanych zabiegów resuscytacyjnych.
11

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
3. Reanimacja krążeniowo-oddechowa — CPR
3.1. Etapy postępowania resuscytacyjnego
I etap — utrzymanie podstawowych czynności życiowych
(BLS — Basic Life Support):
⎯ A — (Airway) — zapewnienie drożności dróg oddechowych,
⎯ B — (Breathing) — prowadzenie wentylacji mechanicznej płuc,
⎯ C — (Circulation) — prowadzenie pośredniego masażu serca.
II etap — metody zaawansowane utrzymania czynności życiowych
(ALS — Advanced Life Support):
⎯ D — (Drugs) — farmakoterapia,
⎯ E — (Electrocardiography) — monitorowanie czynności bioelektrycznej serca (EKG),
⎯ F — (Fibrillation treatment) — leczenie migotania komór — defibrylacja, szerzej
elektroterapia.
III etap — postępowanie poresuscytacyjne:
⎯ G — (Gauging) — ocena skuteczności postępowania resuscytacyjnego,
⎯ H — (Human mentation) — metody terapii w celu powrotu lub utrzymania
prawidłowej czynności mózgu (protekcja OUN),
⎯ I — (Intensive care) — intensywna terapia zachowawcza, mająca na celu wyrównanie
wszelkich zaburzeń po resuscytacji, np.: wentylacja mechaniczna, podtrzymanie
układu krążenia, wyrównanie zaburzeń metabolicznych.
Resuscytacja bezprzyrządowa (BLS):
⎯ A — drożność,
⎯ B — oddech,
⎯ C — krążenie.
Resuscytacja — zespół czynności ratunkowych (oddech zastępczy, masaż serca,
elektroterapia oraz farmakoterapia), mających na celu utrzymanie lub przywrócenie
transportu tlenu do tkanek, w wyniku których u poszkodowanego powróciła spontaniczna
czynność serca i spontaniczna (lub wspomagana) czynność oddechowa.
12

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Reanimacja — zespół czynności ratunkowych (oddech zastępczy, masaż serca,
elektroterapia i farmakoterapia), mających na celu utrzymanie lub przywrócenie
transportu tlenu do tkanek, w wyniku których u poszkodowanego powróciła spontaniczna
czynność serca, spontaniczna (lub wspomagana) czynność oddechowa, czynność
ośrodkowego układu nerwowego (mózgu) — powrót świadomości.
Dlatego też obecnie stosuje się określenia: resuscytacja krążeniowo-oddechowa (Cardio-
Pulmonary Resuscitation — CPR) oraz resuscytacja krążeniowo-oddechowo-mózgowa
(Cardio-Pulmo-Cerebro Resuscitation — CPCR).
Rozpoznanie zatrzymania krążenia:
⎯ utrata przytomności (ok. 6–10 s po ustaniu krążenia mózgowego),
⎯ brak oddechu lub oddech „łapiący”; płytkie, nieregularne oddechy — 10–15 s po
zatrzymaniu krążenia,
⎯ brak tętna na dużych tętnicach (tętnice szyjne i udowe),
⎯ bladość lub sinica powłok skórnych,
⎯ szerokie, niereagujące na światło źrenice (porażenie mięśnia rzęskowego — 60–90 s
po ustaniu krążenia).
MOŻLIWOŚCI I GRANICE RESUSCYTACJI
Zabiegi resuscytacyjne podejmuje się w oparciu o stwierdzenie:
⎯ braku oddechu,
⎯ braku tętna na dużych tętnicach (szyjne, udowe, ramienne).
Ocena znamion, takich jak: sinica, szerokość źrenic i ich reakcje na światło, oziębienie
dystalnych części ciała, obecność lub brak odruchu rzęsowego lub rogówkowego
jest o p ó ź n i a n i e m w d r o ż e n i a c z y n n o ś c i r e s u s c y t a c y j n y c h .
Ułożenie pacjenta w przypadku resuscytacji:
⎯ płasko na twardym podłożu,
⎯ nogi uniesione powyżej poziomu głowy (zwiększenie oporu obwodowego).
Postępowanie w NZK:
1. Wezwać zespół reanimacyjny — podstawowe znaczenie dla ratownika ma jak
najwcześniejsze uzyskanie pomocy.
2. Udrożnić górne drogi oddechowe.
13

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
3. Usunąć ciała obce z jamy ustnej, które mogą utrudnić oddychanie, np. protezy
zębowe.
4. Rozpocząć oddech zastępczy metodą:
⎯ usta–usta,
⎯ usta–nos,
⎯ usta–usta i nos,
⎯ workiem samorozprężalnym.
Technika wentylacji workiem samorozprężalnym polega na szczelnym przyłożeniu maski
twarzowej do twarzy pacjenta i uciskaniu drugą ręką worka samorozprężalnego
z częstością normalnie oddychającego człowieka. Należy zwrócić uwagę na unoszenie się
i opadanie klatki piersiowej oraz na zmianę zabarwienia skóry.
Maskę przy twarzy poszkodowanego utrzymuje się chwytem „C”. Kciuk i palec
wskazujący lewej ręki (u praworęcznych) obejmuje maskę, pozostałe trzy palce zbliżają
do maski twarzowej żuchwę. Aby zwiększyć dostarczanie tlenu do płuc ratowanego, na
zastawkę wdechową zakładamy worek rezerwuarowy, do którego dostarcza się tlen
w objętości 15 l/min.
Niebezpieczeństwem prowadzenia wentylacji workiem samorozprężalnym jest możliwość
przedostania się gazów wdechowych do żołądka ratowanego. Przedostanie się gazów
wdechowych do żołądka powoduje wzrost ciśnienia w żołądku i może stać się przyczyną
ulania treści pokarmowej i jej aspiracji do dróg oddechowych.
Można temu zapobiec przez:
⎯ prawidłowe odgięcie głowy,
⎯ uniesienie żuchwy,
⎯ wprowadzenie rurki ustno-gardłowej,
⎯ wykonanie wolnych wdechów (niskie ciśnienie wdechu),
⎯ czekanie na wydech,
⎯ wykonanie tzw. manewru Sellicka — manewr Sellicka polega na uciśnięciu chrząstki
pierścieniowatej (poniżej chrząstki tarczowatej — jabłka Adama), co powoduje, że
zamyka ona przełyk. Zabieg ten należy wykonywać przez cały czas prowadzenia
wentylacji zastępczej. Objętość oddechowa powinna wynosić 10 ml/kg m.c.
⎯ kontynuować oddech, sprawdzając tętno na dużych tętnicach,
⎯ brak tętna — rozpocznij uciskanie klatki piersiowej (pośredni masaż serca).
14

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Na wysokości 1/3 dolnej części mostka umieść poduszkę dłoniową swojej pierwszej ręki
na górnej powierzchni drugiej ręki, spleć palce obu rąk tak, aby być pewnym, że nie
wywierają ucisku na żebra. Pochylając się nad pacjentem z wyprostowanymi ramionami,
naciskaj pionowo w dół na mostek tak, by obniżył się na głębokość 3,5–5,0 cm (dorośli),
zwolnij ucisk, następnie połącz wentylację z uciskiem klatki piersiowej (15:2).
CPR prowadzone przez jednego ratownika:
⎯ początek wentylacji (dwa wolne wdmuchnięcia trwające po 1–1,5 s. Po każdym
wdechu oczekiwanie na wydech),
⎯ pośredni masaż serca — sztuczne oddychanie (15:2),
⎯ sztuczne oddychanie wykonuje się w czasie przerwy między uciśnięciami mostka.
CPR prowadzone przez dwóch ratowników:
⎯ początek wentylacji (dwa wolne wdmuchnięcia trwające po 1–1,5 s; po każdym
wdechu oczekiwanie na wydech),
⎯ pośredni masaż serca — sztuczne oddychanie (15:2),
⎯ sztuczne oddychanie wykonuje się w czasie przerwy między uciśnięciami mostka.
U pacjenta zaintubowanego masaż serca i oddech mogą być prowadzone niezależnie od
siebie.
Częstość ucisku — ok. 80–90/min (dorośli).
Zapewnij dostęp do żyły.
Resuscytację należy kontynuować do czasu:
⎯ nadejścia wykwalifikowanej pomocy i przejęcia przez nią resuscytacji,
⎯ powrotu spontanicznego oddechu/krążenia,
⎯ fizycznego wyczerpania ratownika.
Czynności resuscytacyjnych nie podejmuje się w przypadku stwierdzenia pewnych
znamion śmierci:
⎯ plam opadowych,
⎯ stężenia pośmiertnego.
Najczęstszym powikłaniem pośredniego masażu serca jest:
⎯ złamanie żeber,
⎯ pęknięcie mostka,
⎯ oderwanie żeber od mostka.
15

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Wentylacja bezprzyrządowa
1. Usta–usta:
⎯ udrożnić drogi oddechowe i utrzymać ich drożność,
⎯ zacisnąć otwory nosowe kciukiem i palcem wskazującym jednej ręki,
⎯ ustami dokładnie objąć i uszczelnić usta ratowanego,
⎯ wdmuchiwać powietrze około 2 sekund, obserwując unoszenie się klatki piersiowej
jako potwierdzenie skuteczności działań,
⎯ oddalić usta od ust ratowanego, pozwalając na wydech ratowanego.
2. Usta–nos (pierwsza metoda z wyboru, zapewniająca lepsze uszczelnienie między
ustami ratownika a nosem ratowanego, zmniejsza ciśnienie w czasie wentylacji,
zapobiega rozdęciu żołądka i wymiotom):
⎯ udrożnić drogi oddechowe, unosząc żuchwę i przyciskając ją do szczęki,
⎯ kciukiem docisnąć wargę dolną do górnej w celu uszczelnienia zaciśniętej szpary
ust ratowanego,
⎯ swoimi ustami objąć nozdrza zewnętrzne ratowanego,
⎯ po wdmuchnięciu powietrza otworzyć usta ratowanego tak, aby mógł on dokonać
wydechu.
3. Usta–usta i nos (metoda z wyboru u noworodków, niemowląt i małych dzieci):
⎯ po udrożnieniu dróg oddechowych szczelnie objąć ustami usta i nos dziecka,
⎯ powietrze wdmuchiwać ostrożnie, pamiętając o odpowiednio małej objętości
oddechowej dziecka,
⎯ obserwować ruchy klatki piersiowej jako potwierdzenie skuteczności działania.
Tabela 1. Częstość wentylacji
Częstość oddechu (oddechy na minutę)
Dorosły
: 10–12
Dziecko powyżej 2 r.ż. :
12–20
Niemowlę od 6 miesiąca życia, dziecko do 2 r.ż. :
20
Noworodek i niemowlę do 6 m.ż. :
30
16

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Podstawy wentylacji bezprzyrządowej:
1. Zastępuje się jedną fazę oddechu — wdech za pomocą wtłaczania powietrza pod
ciśnieniem do dróg oddechowych.
2. Wydech jest spowodowany siłami sprężystości klatki piersiowej.
3. Powietrze wydychane — wdmuchiwane ratowanemu — ma wystarczające stężenie
tlenu dla wykonania skutecznego BLS.
Błędy i niebezpieczeństwa związane z wentylacją zastępczą niezaintubowanego pacjenta:
⎯ rozdęcie żołądka przez stosowanie zbyt wysokich ciśnień, grożące regurgitacją
i aspiracją treści pokarmowej do dróg oddechowych,
⎯ niewłaściwe trzymanie maski, powodujące nieszczelność,
⎯ niewystarczająco odgięta głowa,
⎯ niewłaściwe trzymanie worka oddechowego.
Wentylacja przyrządowa
⎯ rurka ustno-gardłowa,
⎯ rurka Sussex,
⎯ worek samorozprężalny,
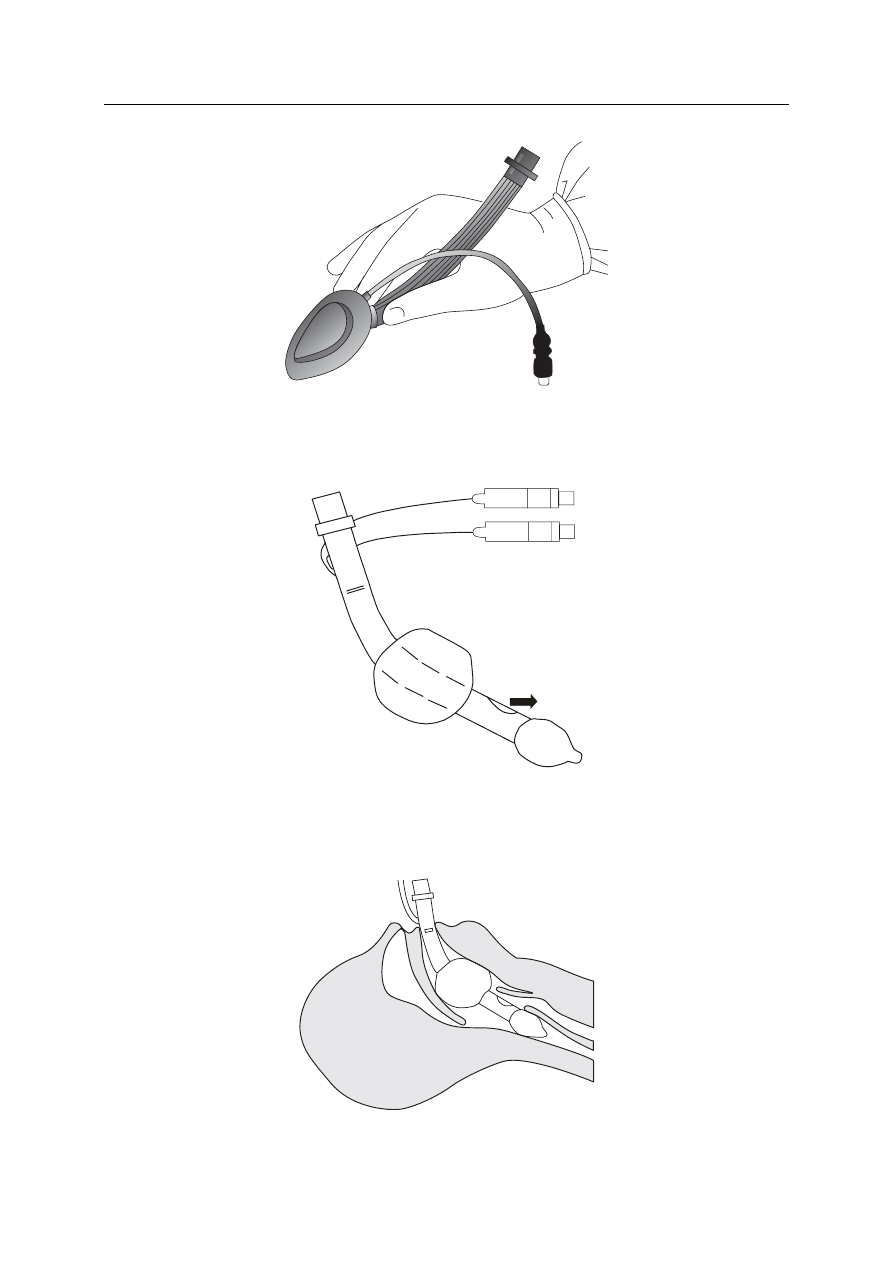
⎯ maska krtaniowa (rysunek 1),
⎯ rurka krtaniowa (rysunek 2 i 3),
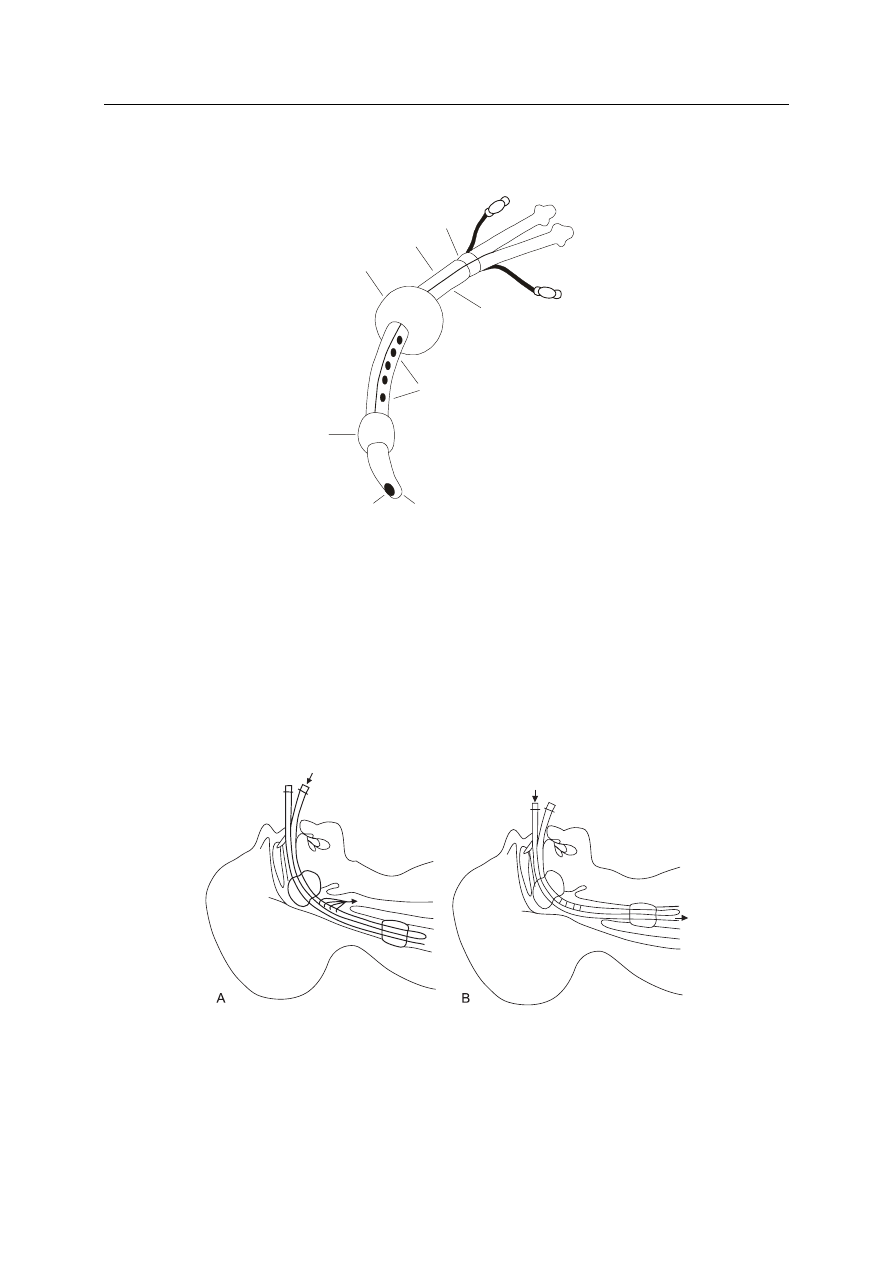
⎯ rurka Combitube (rysunek 4 i 5),
⎯ intubacja:
• ustno-tchawicza,
• nosowo-tchawicza,
⎯ konikotomia (konikopunkcja),
⎯ tracheotomia (tracheopunkcja),
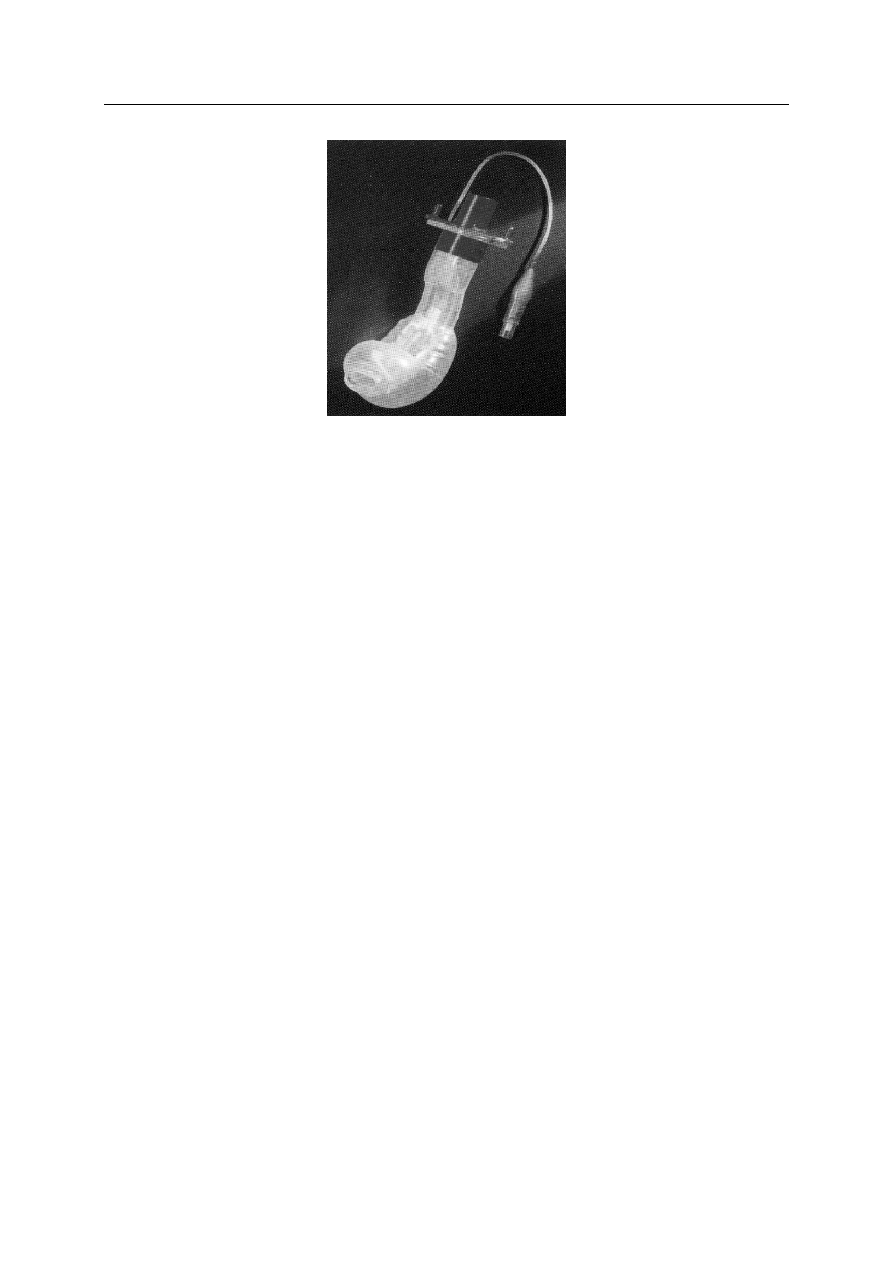
⎯ rurka COPA (rysunek 6).
17
Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Rysunek 1. Maska krtaniowa
mankiet
dalszy dystalny
- blokuje wejście
do przełyku
mankiet
bliższy proksymalny
- stabilizuje rurkę
otwór
wentylacyjny
Rysunek 2. Rurka krtaniowa — budowa
Rysunek 3. Sposób wentylacji rurką krtaniową
18
Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
1
5
6
7
2
8
4
3
1 — rurka „przełykowa”
2 — rurka „tchawicza”
3 — perforacja rurki „przełykowej”
4 — zaślepiony koniec rurki „przełykowej”
5 — otwór rurki „tchawiczej”
6 — mankiet przełykowy (10–15 ml)
7 — mankiet gardłowy(100 ml)
8 — marker
Rysunek 4. Rurka Combitube — budowa
11
Rysunek 5. Sposoby wentylacji rurką Combitube
A — rurka Combitube w przewodzie pokarmowym, B — rurka Combitube w tchawicy
19
Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Rysunek 6. Rurka COPA
Czas tolerancji narządów na niedotlenienie:
⎯ kora mózgowa — ok. 3–4 min,
⎯ rdzeń przedłużony — ok. 10–30 min,
⎯ serce — ok. 45 min,
⎯ wątroba, nerki — ok. 60 min.
20

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
4. Elektroterapia — rola pielęgniarki
Defibrylację po raz pierwszy opisali Prevost i Batelli w 1899 r., przerywając migotanie
komór u psa, natomiast po raz pierwszy u człowieka wykonał Beck w 1948 r.
Mięsień sercowy pobudzany jest do skurczu przez układ bodźcowo-przewodzący serca.
Układ ten wytwarza prąd elektryczny i rozprowadza go do każdego włókna mięśniowego.
W ten sposób wszystkie włókna mięśniowe kurczą się jednocześnie, co zapewnia wyrzut
krwi z komór.
Defibrylacją nazywamy przepuszczenie prądu elektrycznego (stałego) przez klatkę
piersiową w celu przerwania migotania komór. W momencie przepływu przez serce
silnego impulsu elektrycznego prądu stałego, błony komórkowe wszystkich komórek
mięśni poprzecznie prążkowanych serca zostaną rozładowane i następnie zaczną
gromadzić potencjał jednakowo. Dojdzie do wygaszenia nieprawidłowych ognisk
pobudzenia, a sterowanie mięśniem przejmie układ bodźco-przewodzący serca.
Defibrylacja jest metodą skuteczną i bezpieczną.
Wczesna defibrylacja:
⎯ migotanie komór jest najczęstszym mechanizmem nagłego zatrzymania krwi
u dorosłych,
⎯ defibrylacja elektryczna jest najskuteczniejszym sposobem leczenia migotania komór,
⎯ prawdopodobieństwo skuteczności defibrylacji elektrycznej maleje w miarę upływu
czasu,
⎯ świadek zdarzenia może utrzymać dzięki CPR serce w migotaniu przez 10–15 minut,
⎯ szanse powodzenia defibrylacji zmniejszają się gwałtownie z upływem czasu o około
7–10% w ciągu każdej minuty.
Miejsce przyłożenia elektrod
Najczęściej jedną elektrodę przykłada się na lewo od brodawki sutkowej (środek
elektrody powinien leżeć w linii pachowej środkowej), a drugą na prawo od górnej części
mostka, poniżej obojczyka. Jedną elektrodę umieszczamy z przodu, w okolicy
przedsercowej, a drugą z tyłu za sercem, w lewej okolicy podłopatkowej (jeśli są to
elektrody przylepne).
21

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Defibrylator:
⎯ monitoruje czynność elektryczną serca,
⎯ przygotowuje określoną wielkość prądu stałego,
⎯ bezpiecznie wyzwala taki prąd przez elektrody,
⎯ dokumentuje przeprowadzony zabieg defibrylacji.
Części składowe defibrylatora:
⎯ zasilacz i konwerter prądu stałego o określonym napięciu,
⎯ kondensator stanowiący pojemność dla prądu stałego o regulowanej mocy,
⎯ przełącznik pozwalający skierować zgromadzony prąd poprzez elektrody,
⎯ system prezentacji elektrokardiogramu, alarmy i zabezpieczenia,
⎯ rejestrator,
⎯ pulpit pozwalający na ustawienia określonych parametrów defibrylacji i kontroli,
⎯ źródła zasilania bateryjnego (akumulatory).
Kardiowersja (defibrylacja synchronizowana)
Polega na przepływie prądu stałego o energii 25–360 J przez klatkę piersiową chorego,
trwającym 1,5–4 ms, w odstępie 40 ms po załamku R w zapisie EKG. Powoduje
rozładowanie elektryczne serca i umożliwia powrót rytmu zatokowego.
Powikłania kardiowersji i defibrylacji
Przepływ prądu może spowodować uszkodzenie mięśnia sercowego, a nawet martwicę,
szczególnie po wielu szybko powtarzanych wyładowaniach energii. Mogą również
wystąpić zaburzenia krążenia mózgowego i zatory tętnicze. Sporadycznie rytm
konwertowany zmienia się w bardziej niebezpieczny — częstoskurcz komorowy,
migotanie komór albo pojawia się asystolia.
Stymulacja elektryczna ma na celu podtrzymanie rytmu pracy serca, gdy fizjologiczne
ośrodki bodźcotwórcze nie są w stanie pobudzić serca do wydolnej hemodynamicznie
pracy i utrzymania wystarczającego ciśnienia tętniczego krwi.
Rodzaje stymulacji:
1. Stymulacja endokawitarna — wprowadzenie elektrody drogą dożylną do prawego
przedsionka lub prawej komory.
2. Stymulacja przezprzełykowa — lewego przedsionka lub lewej komory przy użyciu
elektrody wprowadzonej do przełyku. Wymaga ona nieco większej energii bodźców niż
22

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
stymulacja wewnątrzsercowa. Czas wprowadzania elektrody jest bardzo krótki, co ma
znaczenie w sytuacjach naglących.
3. Stymulacja przezskórna — jest metodą najszybszą i najmniej inwazyjną. Elektrody
stymulatora umieszcza się na skórze przedniej i tylnej ściany klatki piersiowej.
4. Stałe stymulatory — zwykle wszczepiane choremu, są wygodne i bezpieczne, a ich
główną zaletą jest natychmiastowe działanie.
Ustawienia stymulatora
Ustawienia stymulatora zależą od wskazań klinicznych. Ogólnie można przyjąć, że na
początku należy ustawić maksymalną moc pobudzeń, a następnie ją zmniejszać pod
kontrolą uzyskanego rytmu. Częstotliwość powinna być ustawiona na 80–100
impulsów/min. W razie stymulacji ze wskazań nagłych, po zatrzymaniu krążenia, należy
stosować asynchroniczny tryb pracy stymulatora.
23

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
5. Farmakoterapia — drogi podawania leków
Podawanie leków w CPR jest postępowaniem drugoplanowym i ma na celu:
⎯ poprawę perfuzji narządowej podczas CPR,
⎯ ułatwienie defibrylacji elektrycznej,
⎯ zapobieganie nawrotom złośliwych niemiarowości komorowych,
⎯ ochronę mózgu i — w mniejszym stopniu — serca przed wpływem niedokrwienia
i niedotlenienia,
⎯ normalizację zaburzeń metabolicznych.
Drogi podawania leków w CPR:
⎯ dostęp dożylny,
⎯ dostęp dotchawiczy,
⎯ dostęp doszpikowy.
Optymalnym sposobem podawania leków podczas resuscytacji krążeniowo-oddechowej
jest droga dożylna. Często pielęgniarka podejmuje samodzielnie te czynności:
⎯ kaniulacja żyły centralnej:
• szyjna zewnętrzna,
• szyjna wewnętrzna,
• szyjna podobojczykowa (niebezpieczeństwo odmy);
⎯ kaniulacja żyły obwodowej:
• żyła odłokciowa (możliwość omyłkowej kaniulacji tętnicy),
• żyły przedramienia,
• żyły grzebietowe rąk i stóp z powodu krańcowej centralizacji krążenia słabo nadają
się do podawania leków podczas zatrzymania akcji serca;
⎯ droga dotchawicza (podawanie leków przez rurkę intubacyjną i tracheostomijną).
Według najnowszych doniesień drogą tą można podać jedynie Adrenalinę, Lidokainę,
Atropinę.
Obecnie zaleca się dawki 2–3 razy większe niż podawane dożylnie rozpuszczone w 10 ml
wody do iniekcji lub NaCl 0,9%. Po podaniu leku należy wykonać 5 sztucznych oddechów
w celu zwiększenia rozproszenia leków do dalszych części dróg oddechowych, dzięki
czemu zwiększa się ich wchłanianie.
24

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Ważne: Nie wolno podawać do dróg oddechowych NaHCO
3
wodorowęglanu sodu,
ponieważ uszkadza tkanki. Ważne jest, by dożylnie adrenaliny nie podawać w jednej linii
z wodorowęglanem sodu.
25

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Bibliografia
1. Brzeziński T., 2000: Historia medycyny, PWN, Warszawa.
2. Choroby wewnętrzne, 1996: (red.) F. Kokot, PZWL, Warszawa.
3. Kruszyński Z., 1999: Podstawy anestezjologii i intensywnej terapii, Wydawnictwa
Uczelniane Akademii Medycznej im. Karola Marcinkowskiego, Poznań.
4. Larsen H., 2003: Anestezjologia, Wydawnictwo Medyczne Urban & Partner, Wrocław.
5. Marino P. L., 2001: intensywna terapia, Medyczne Urban & Partner, Wrocław.
6. Saint-Maurice C., Miller A., Meynadier J., 1998: Ból, diagnostyka, leczenie
i prewencja, Warszawa.
7. Zembała M., 1989: Kardiologia interwencyjna, Lech Poloński, Zabrze.
26

Pielęgniarstwo anestezjologiczne — rys historyczny.
Postępowanie w stanach zagrożenia życia
Literatura podstawowa
1. Kruszyński Z., 1999: Podstawy anestezjologii i intensywnej terapii, Wydawnictwa
Uczelniane Akademii Medycznej im. Karola Marcinkowskiego, Poznań.
Literatura dodatkowa
1. Choroby wewnętrzne, 1996: (red.) F. Kokot, PZWL, Warszawa.
2. Zembała M., 1989: Kardiologia interwencyjna, Lech Poloński, Zabrze.
27
Document Outline
- Pielęgniarstwo anestezjologiczne — rys historyczny. Postępowanie w stanach zagrożenia życia
Wyszukiwarka
Podobne podstrony:
Modul 3 id 305625 Nieznany
3 modul id 33860 Nieznany (2)
Modul 1 4 id 305609 Nieznany
5 modul id 40284 Nieznany (2)
modul 1 5 id 305610 Nieznany
4 modul 2 id 37767 Nieznany
3 modul 3 id 33862 Nieznany (2)
3 modul 4 id 33863 Nieznany (2)
modul 2 5 id 305624 Nieznany
Modul 3 3 id 305627 Nieznany
3 modul 2 id 33861 Nieznany (2)
6 modul id 43783 Nieznany (2)
Modul 1 2 id 305607 Nieznany
bibliografia modul 8 id 85025 Nieznany (2)
Modul III 2 id 305653 Nieznany
więcej podobnych podstron