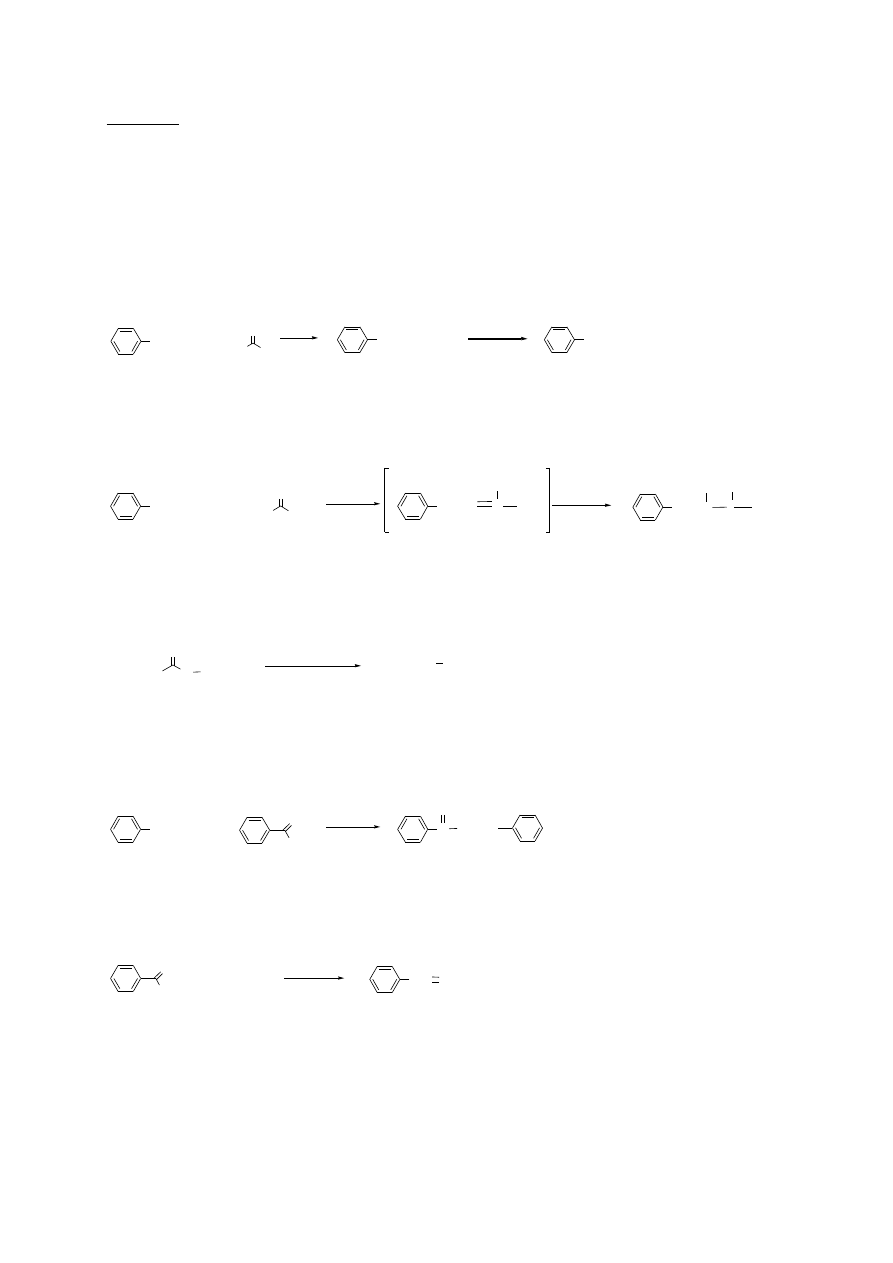
Zestaw A
termin „1”; 01.02.2008
Egzamin z Chemii Organicznej 2007/2008, Wydział Inżynierii Chemicznej i Procesowej
Zad. 1. (34p) Przedstaw schematy poniższych reakcji (za pomocą wzorów strukturalnych)
oraz podaj nazwy produktów (oprócz podpunktu 10):
1.(3p) bromek fenylomagnezu + (1) aldehyd mrówkowy, (2) HCl
(aq) →
(addycja zw. Grignarda do związków karbonylowych)
alkohol benzylowy
2.(4p) benzyloamina + (1) aceton wobec H
+
, (2) LiAlH
4
→
(aminowanie redukcyjne aldehydów i ketonów)
benzylo-izopropyloamina
3.(5p) propanian etylu + (1) LiAlH
4
, (2) HCl aq
→
(redukcja estrów)
propan-1-ol etanol
4.(3p) alkohol benzylowy + chlorek benzoilu →
(estryfikacja alkoholi)
benzoesan benzylu
5.(3p) benzaldehyd + NH
2
OH (kat. H
+
) →
(addycja amoniaku i jedo pochodnych do aldehydów i ketonów)
oksym benzaldehydu
1
MgBr
H H
O
CH
2
OMgBr
CH
2
OH
+
HCl aq
CH
2
OH
O
Cl
C
O
OCH
2
+
CH
2
NH
2
H
3
C CH
3
O
H
+
CH
2
N C
CH
3
CH
3
LiAlH
4
CH
2
N C
H
CH
3
CH
3
H
+
O
H
NH
2
OH
H
+
CH N-OH
+
CH
3
CH
2
O CH
2
CH
3
O
(1) LiAlH
4
CH
3
CH
2
CH
2
OH
CH
2
CH
3
OH
+
(2) HCl aq
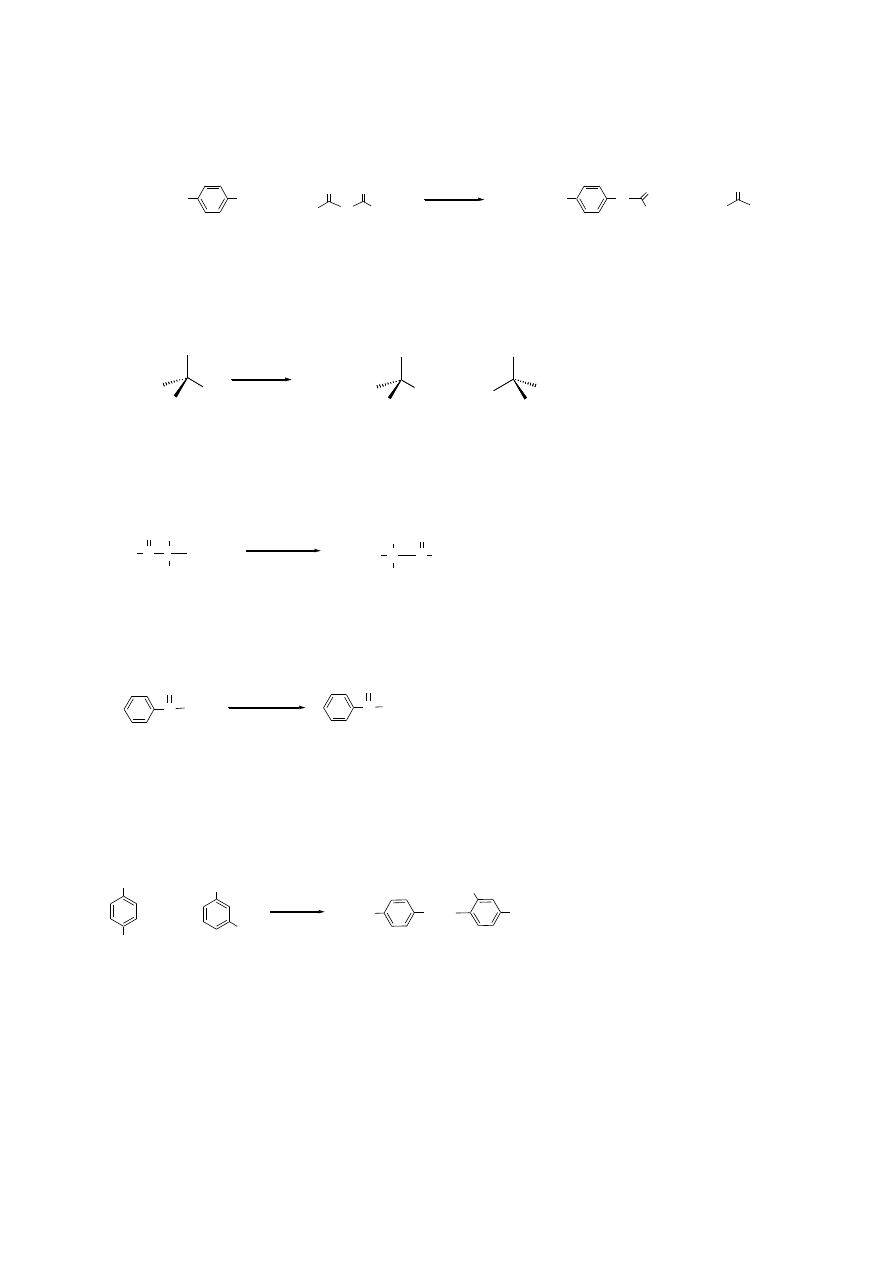
6.(3p) p-izopropylofenol + bezwodnik octowy →
(estryfikacja fenoli)
octan p-izopropylofenolu kwas octowy
7.(5p) (R)-2-chloro-2-fenylobutan + H
2
O (nadmiar) →
(substytucja nukleofilowa halogenków alkilowych, solwoliza, S
N
1)
(R)-2-fenylobutan-2-ol
(S)-2-fenylobutan-2-ol
8.(3p) 3,3-dimetylo-2-butanon + 3 mole I
2
+ NaOH (nadmiar) →
[reakcja haloformowa (jodoformowa)]
2,2-dimetylopropionian sodu jodoform
9.(3p) benzamid + NaOH
(aq) (nadmiar, ∆t) →
(hydroliza amidów kwasowych)
benzoesan sodu
10.(2p) chlorek p-nitrobenzenodiazoniowy + m-krezol, pH 9 →
(sprzęganie soli diazoniowych)
2
OH
(CH
3
)
2
CH
CH
3
O
CH
3
O
O
O
(CH
3
)
2
CH
O
CH
3
CH
3
O
OH
+
+
Ph
(R)
Cl
CH
3
CH
3
CH
2
H
2
O
Ph
(R)
OH
CH
3
CH
3
CH
2
Ph
(S)
OH
CH
3
CH
2
CH
3
+
nadmiar
C
O
NH
2
C
O
ONa
NaOH
nadmiar
+ NH
3
CH
3
C
O
C
CH
3
CH
3
CH
3
ONa
C
O
C
CH
3
CH
3
CH
3
I
2
/NaOH
+ CHI
3
N
2
+
Cl
−
NO
2
CH
3
OH
N=N
O
2
N
H
3
C
OH
+
pH 9
Ph
(R)
Cl
CH
3
CH
3
CH
2
H
2
O
Ph
(R)
OH
CH
3
CH
3
CH
2
Ph
(S)
OH
CH
3
CH
2
CH
3
+
nadmiar

Zad. 2. (6p) Wykonaj następujące polecenia:
a. podaj nazwę związku A z uwzględnieniem jego konfiguracji absolutnej oraz określ
konfigurację absolutną związków B i C,
b. narysuj wzór przestrzenny stereoizomeru związku B,
c. narysuj wzór krzyżowy Fischera związku C.
A
B
C
kwas (S)-2-bromo-2,3-
dimetylobutanowy
3
CH
2
OCH
3
(S)
CH
3
NC
H
C
6
H
5
(S)
H
3
C
CH
2
CH
3
Br
COOH
(S)
H
3
C
CH(CH
3
)
2
Br
CH
2
OCH
3
(R)
H
3
C
CN
H
CH
3
CH
2
C
6
H
5
(S)
Br
CH
3
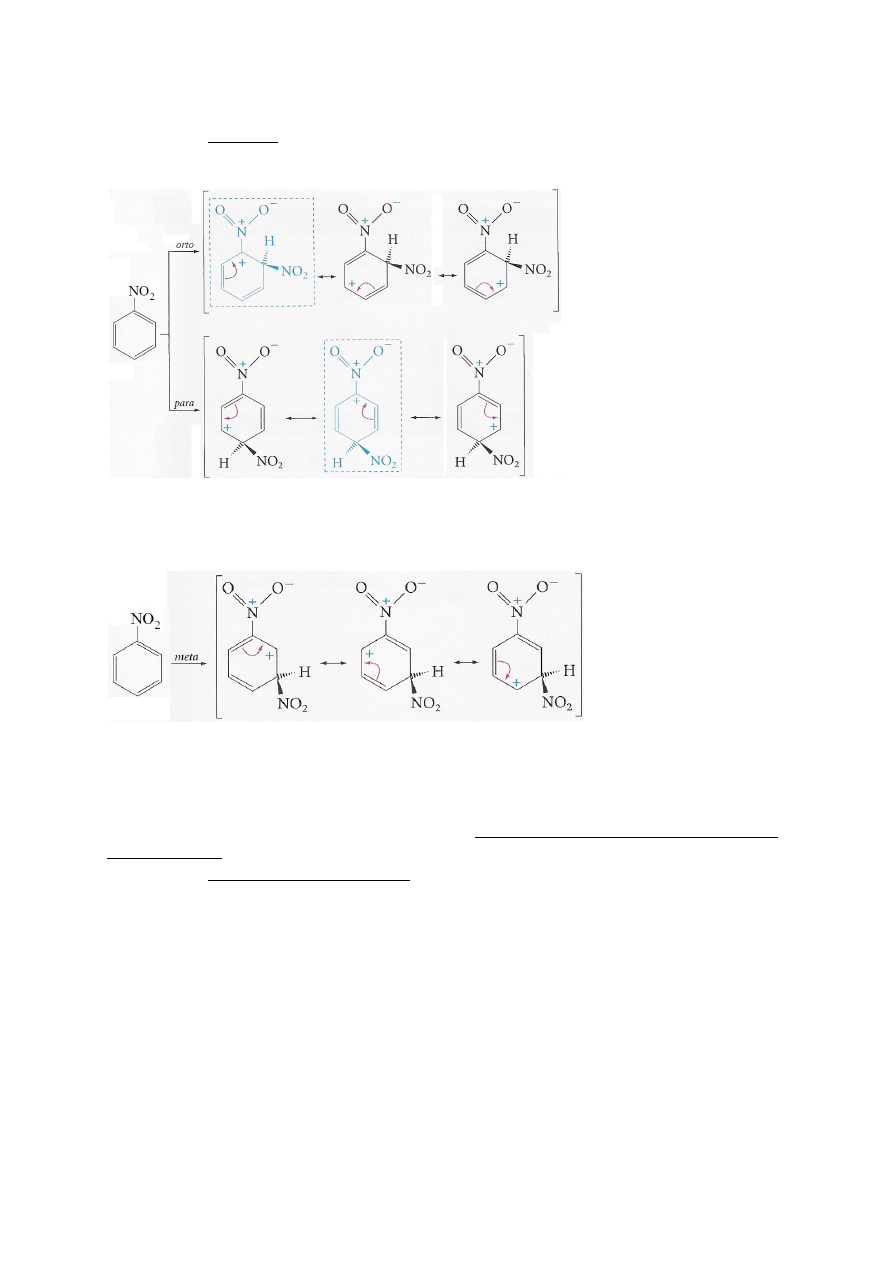
Zad. 3. (12p) Wyjaśnij regioselektywność reakcji nitrowania nitrobenzenu na podstawie
porównania budowy odpowiednich kompleksów sigma (narysuj struktury mezomeryczne tych
kompleksów).
Struktury A i E - szczególnie nietrwałe; ładunek dodatni zlokalizowany na atomie węgla
związanym z podstawnikiem posiadającym cząstkowy ładunek dodatni.
W żadnej ze struktur ładunek dodatni nie jest zlokalizowany na atomie węgla związanym z
podstawnikiem posiadającym cząstkowy ładunek dodatni.
W reakcjach S
E
z udziałem pochodnych benzenu z podstawnikami posiadającymi cząstkowy
ładunek dodatni na atomie związanym z atomem węgla z pierścienia aromatycznego
otrzymuje się meta-
podstawione produkty
, ponieważ tylko wtedy w kompleksie
σ
(sigma)
ładunek dodatni nie jest zlokalizowany na atomie węgla związanym z podstawnikiem
posiadającym cząstkowy ładunek dodatni.
4
A
B
C
D
E
F
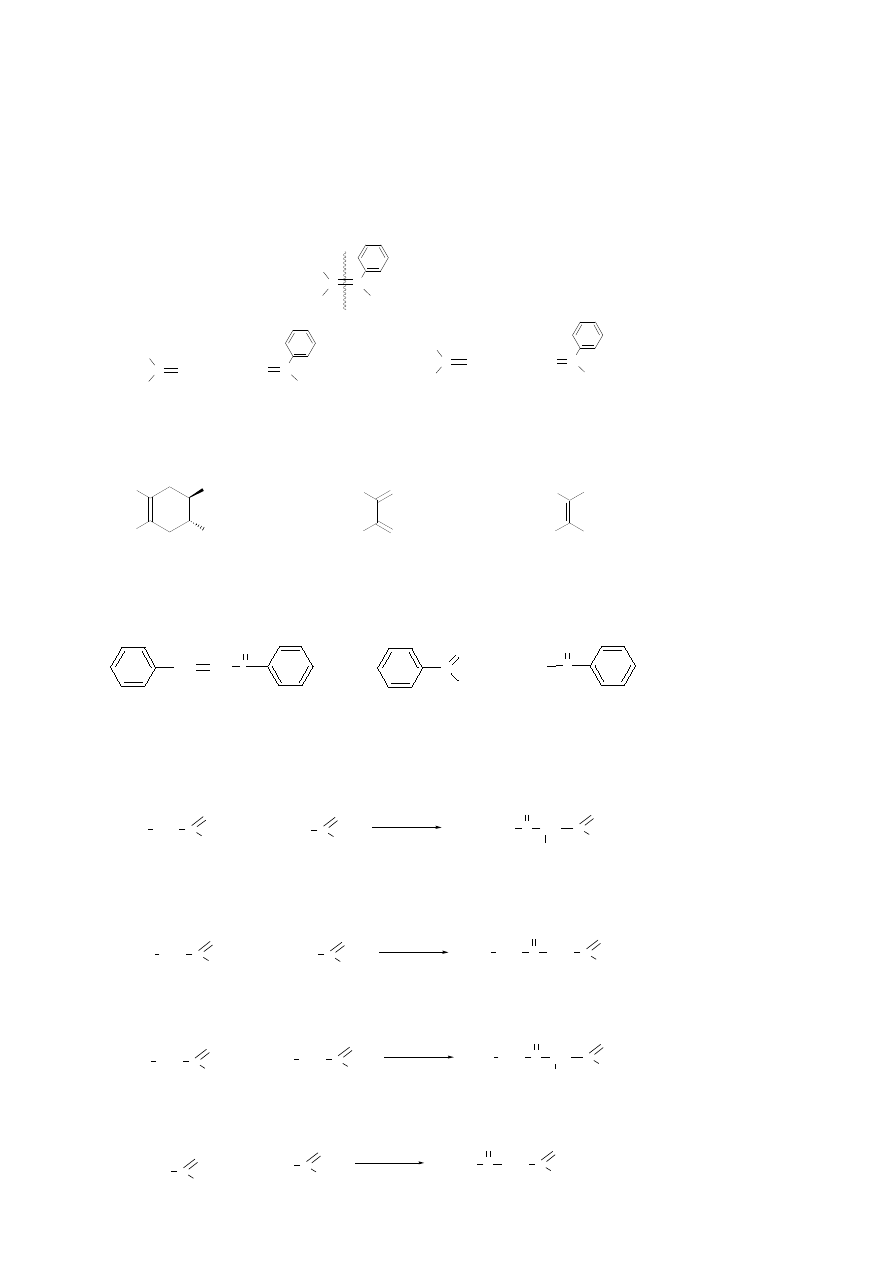
Zad. 4. (16p) Podaj wzory strukturalne oraz nazwy substratów organicznych, z których
można otrzymać poniższe związki we wskazanych reakcjach:
a. (6p) 1-fenylo-2-metylopropen (w reakcji Wittiga)
aceton
benzaldehyd
b. (6p) trans-1,2,4,5-tetrametylocykloheksen (w reakcji Dielsa-Aldera)
2,3-dimetylobuta-1,3-dien
(E)-but-2-en
c. (4p) 1,3-difenylo-1-oksoprop-2-en [C
6
H
5
-C(O)-CH=CH-C
6
H
5
, w reakcji kondensacji
aldolowej]
benzaldehyd
acetofenon
Zad. 5. (10p) Podaj budowę i nazwy wszystkich produktów, jakie powstaną w reakcji
kondensacji Claisena octanu etylu i propionianu etylu oraz napisz schematy zachodzących
reakcji.
5
C
C
H
3
C
H
3
C
H
O
C
H
3
C
H
3
C
C
Ph
3
P
H
PPh
3
C
H
3
C
H
3
C
C
O
H
i
lub
i
CH
3
CH
3
H
3
C
H
3
C
CH
2
CH
2
H
3
C
H
3
C
H
3
C
H
CH
3
H
i
i
C
CH
CH
O
O
C
H
C
H
3
C
O
CH
3
CH
2
C
O
OC
2
H
5
CH
3
CH
2
C
O
OC
2
H
5
CH
3
C
O
OC
2
H
5
CH
3
C
O
OC
2
H
5
C
2
H
5
ONa
C
2
H
5
ONa
CH
3
CH
2
C
O
OC
2
H
5
CH
3
CH
2
C
O
OC
2
H
5
C
2
H
5
ONa
CH
3
C
O
OC
2
H
5
C
2
H
5
ONa
CH
3
C
O
OC
2
H
5
CH
3
C
O
CH
2
C
O
OC
2
H
5
CH
3
CH
2
C
O
CH
2
C
O
OC
2
H
5
CH
3
CH
2
C
O
CH C
O
OC
2
H
5
CH
3
CH
3
C
O
CH C
O
OC
2
H
5
CH
3
+
+
+
3-oksopentanian etylu
2-metylo-3-oksopentanian etylu
3-oksobutanian etylu
propionian etylu
octan etylu
+
2-metylo-3-oksobutanian etylu
propionian etylu
octan etylu
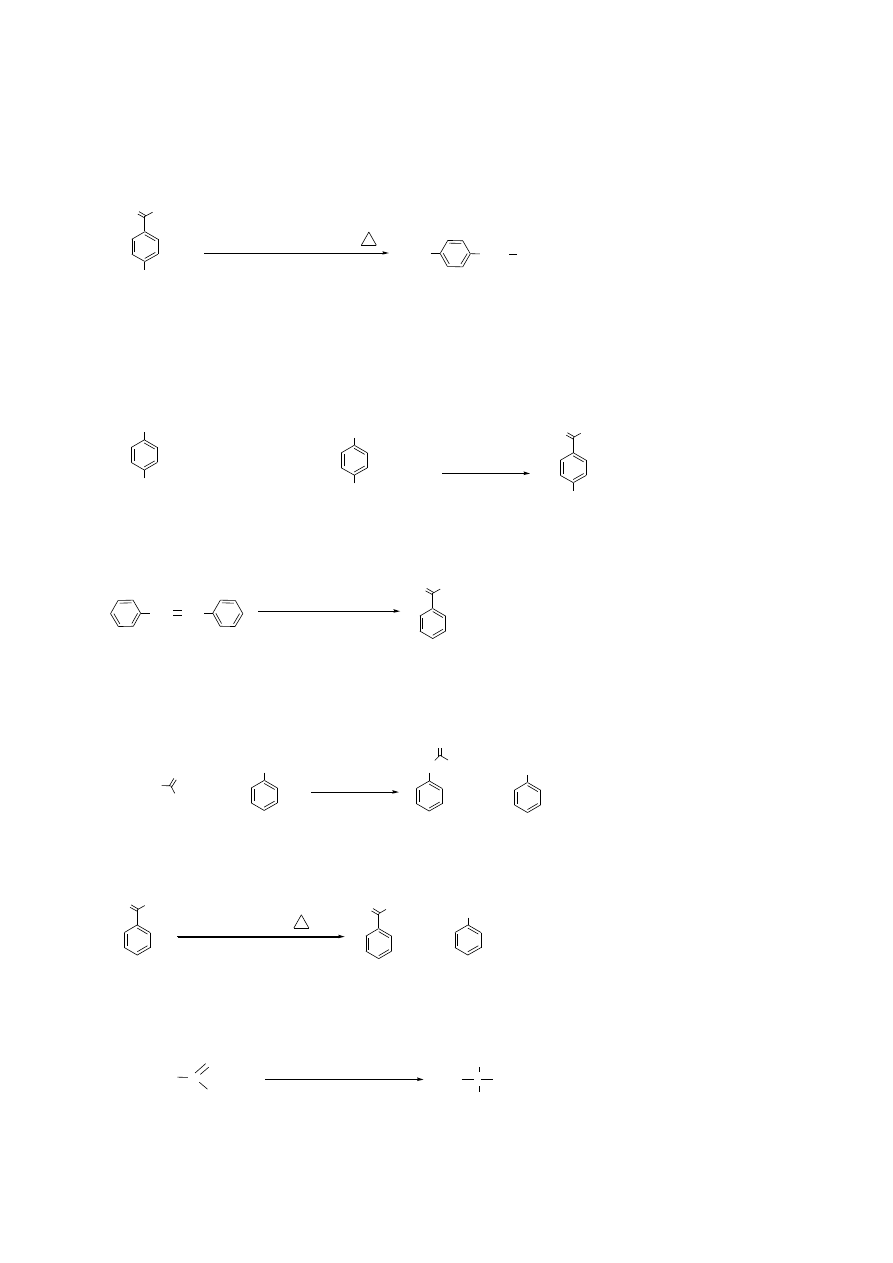
Zad. 6. (30p) Przedstaw schematy poniższych reakcji (za pomocą wzorów strukturalnych)
oraz podaj nazwy związków oznaczonych literami:
1.A + (1) NH
2
NH
2
, (2) KOH, ∆t → p-nitropropylobenzen (redukcja Wolfa-Kiżnera)
2.B + K
2
Cr
2
O
7
/H
+
→ kwas p-nitrobenzoesowy (utlenianie alkoholi lub utlenianie
łańcuchów bocznych w alkilobenzenach)
3.C + (1) O
3
, (2) Zn/H
2
O → aldehyd benzoesowy (ozonoliza alkenów)
4.D + anilina (2 mole) → N-fenyloacetamid (acetanilid) + chlorek aniliniowy (otrzymywanie
amidów kwasowych)
5.E + NaOH (50%, ∆t) → benzoesan sodu + alkohol benzylowy (reakcja Cannizzaro)
6.F + (1) jodek metylomagnezu (2 mole), (2) HCl (aq) → alkohol tert-butylowy (addycja zw.
Grignarda do estrów – otrzymywanie alkoholi trzeciorzędowych)
6
NO
2
O C
2
H
5
O
2
N
CH
2
C
2
H
5
(1) NH
2
NH
2
, (2) KOH,
t
p-nitropropiofenon
O H
CH CH
(1) O
3
, (2) Zn/H
2
O
1,2-difenyloetan
H
3
C
Cl
O
NH
2
HN CH
3
O
NH
3
+
Cl
−
+
+
chlorek acetylu
O H
O ONa
CH
2
OH
NaOH (50%, t)
+
benzaldehyd
C
CH
3
OC
2
H
5
O
C
CH
3
H
3
C
CH
3
OH
(1) CH
3
MgI, (2) HCl aq
octan etylu
NO
2
CH
2
OH
NO
2
O OH
K
2
Cr
2
O
7
/ H
+
alkohol p-nitrobenzylowy
NO
2
CH
3
lub
p-nitrotoluen
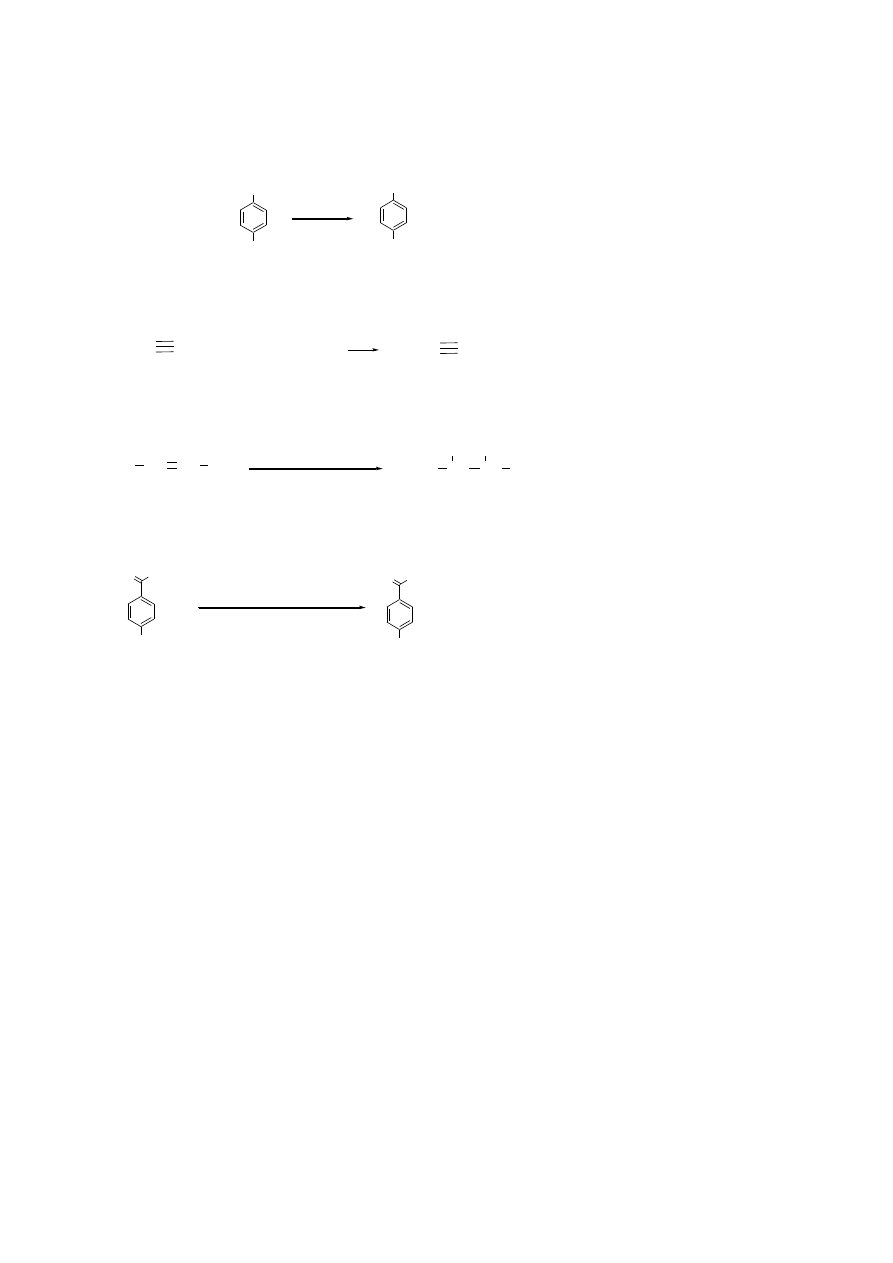
7.G + jodek metylu → 4-bromoanizol (eter 4-bromofenylowo-metylowy) + NaI (reakcja
Williamsona)
8.H + 1-bromobutan → hept-2-yn + NaBr (alkilowanie alkinów terminalnych)
9.I + KMnO
4
(aq), 0
°
C → butano-2,3-diol (utlenianie alkenów)
10.J + NaOH (aq) (nadmiar) → p-metylobenzoesan sodu + etanol (hydroliza estrów)
7
ONa
Br
CH
3
I
OCH
3
Br
4-bromofenolan sodu
O OC
2
H
5
CH
3
O ONa
CH
3
NaOH (aq, nadmiar)
+ C
2
H
5
OH
p-metylobenzoesan etylu
CH CH
H
3
C
CH
3
OH OH
CH CH
H
3
C
CH
3
KMnO
4
(aq), 0°C
but-2-en
CH
3
-C
C-Na
C
3
H
7
CH
2
Br
CH
3
-C
C-CH
2
C
3
H
7
+
propynylosód
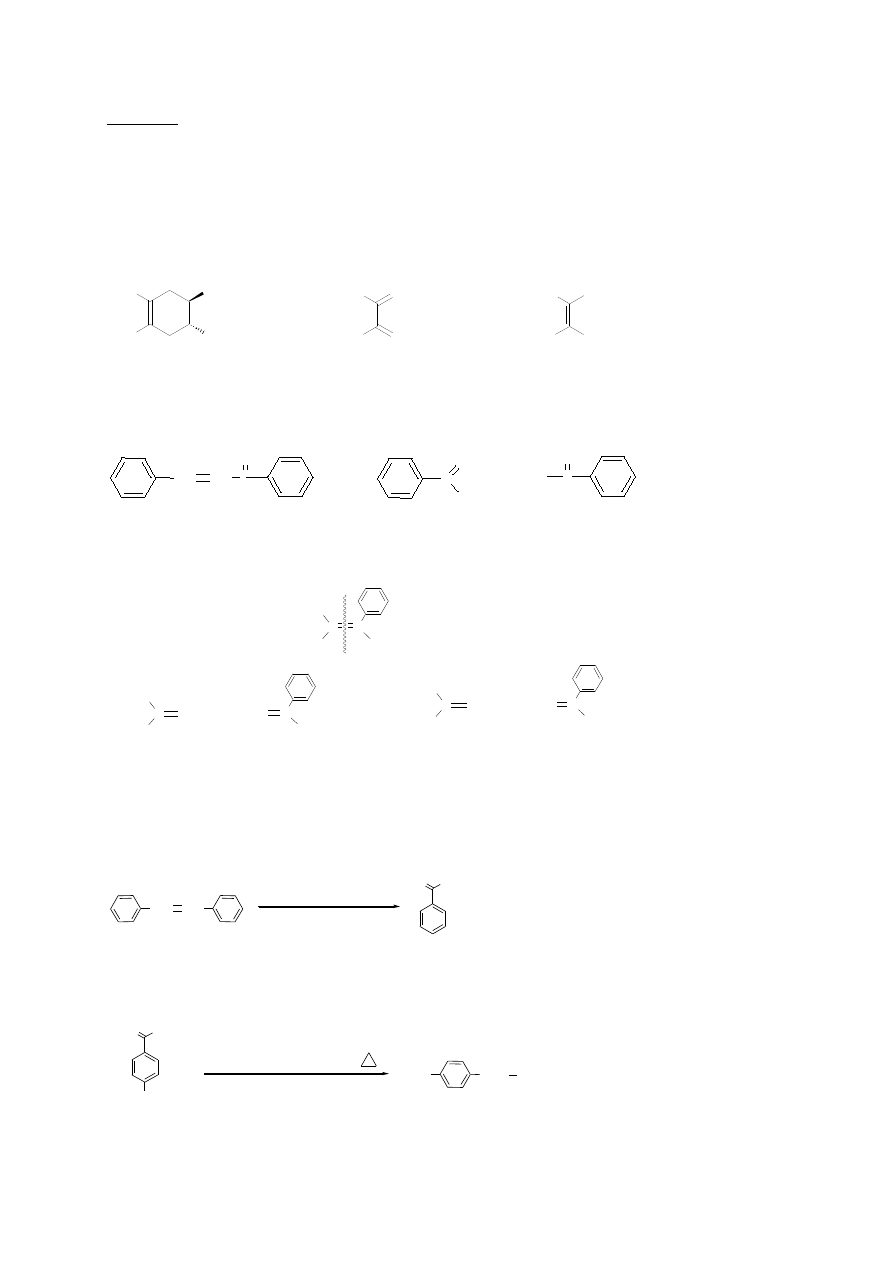
Zestaw B
termin
„1”;
01.02.2008
Egzamin z Chemii Organicznej 2007/2008, Wydział Inżynierii Chemicznej i Procesowej
Zad. 1. (16p) Podaj wzory strukturalne oraz nazwy substratów organicznych, z których
można otrzymać poniższe związki we wskazanych reakcjach:
a. (6p) trans-1,2,4,5-tetrametylocykloheksen (w reakcji Dielsa-Aldera)
2,3-dimetylobuta-1,3-dien
(E)-but-2-en
b. (4p) 1,3-difenylo-1-oksoprop-2-en [C
6
H
5
-C(O)-CH=CH-C
6
H
5
, w reakcji kondensacji
aldolowej]
benzaldehyd
acetofenon
c. (6p) 1-fenylo-2-metylopropen (w reakcji Wittiga)
aceton
benzaldehyd
Zad. 2. (30p) Przedstaw schematy poniższych reakcji (za pomocą wzorów strukturalnych)
oraz podaj nazwy związków oznaczonych literami:
1.A + (1) O
3
, (2) Zn/H
2
O → aldehyd benzoesowy (ozonoliza alkenów)
2.B + (1) NH
2
NH
2
, (2) KOH, ∆t → p-nitropropylobenzen (redukcja Wolfa-Kiżnera)
8
C
C
H
3
C
H
3
C
H
O
C
H
3
C
H
3
C
C
Ph
3
P
H
PPh
3
C
H
3
C
H
3
C
C
O
H
i
lub
i
CH
3
CH
3
H
3
C
H
3
C
CH
2
CH
2
H
3
C
H
3
C
H
3
C
H
CH
3
H
i
i
C
CH
CH
O
O
C
H
C
H
3
C
O
NO
2
O C
2
H
5
O
2
N
CH
2
C
2
H
5
(1) NH
2
NH
2
, (2) KOH,
t
p-nitropropiofenon
O H
CH CH
(1) O
3
, (2) Zn/H
2
O
1,2-difenyloetan
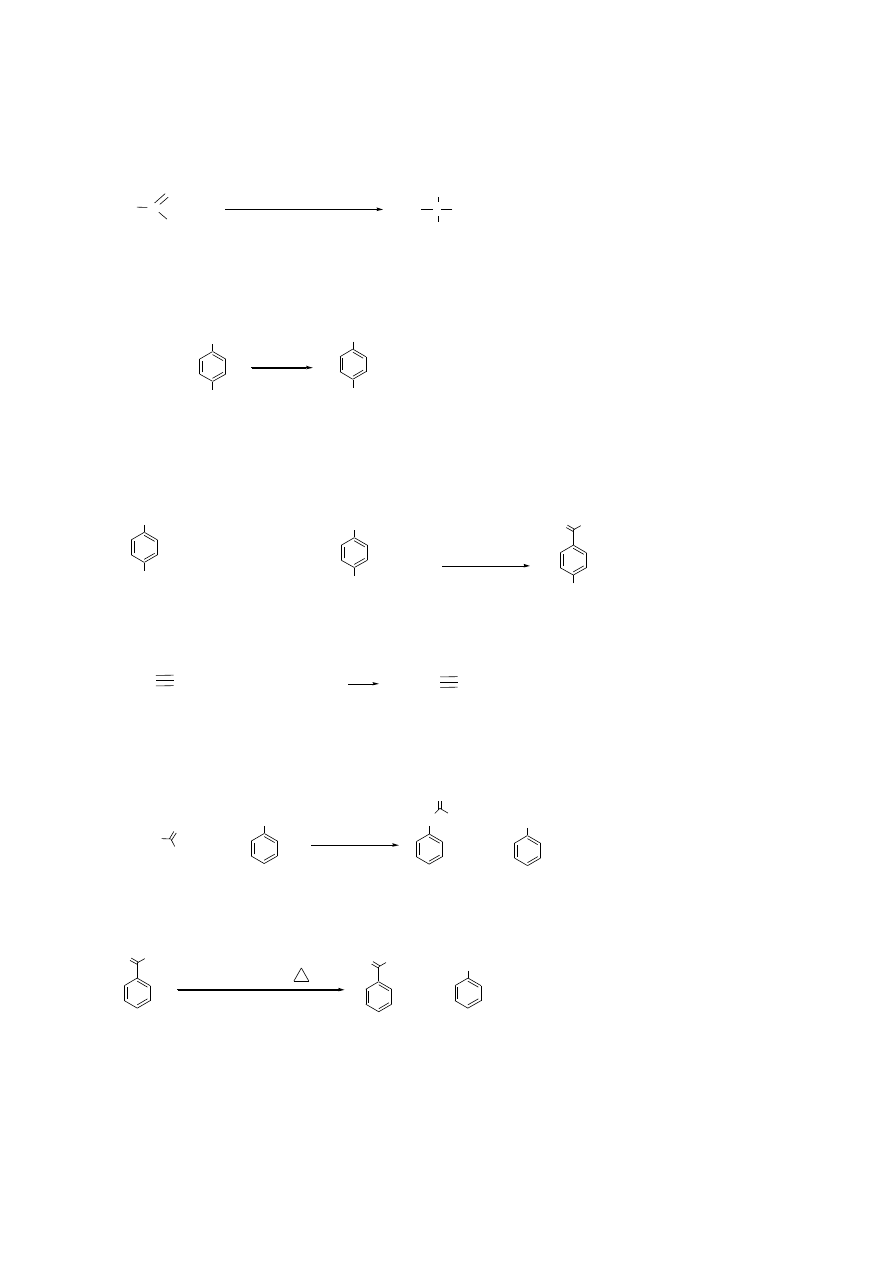
3.C + (1) jodek metylomagnezu (2 mole), (2) HCl (aq) → alkohol tert-butylowy (addycja
zw. Grignarda do estrów – otrzymywanie alkoholi trzeciorzędowych)
4.D + jodek metylu → 4-bromoanizol (eter 4-bromofenylowo-metylowy) + NaI (reakcja
Williamsona)
5.E + K
2
Cr
2
O
7
/H
+
→ kwas p-nitrobenzoesowy (utlenianie alkoholi lub utlenianie
łańcuchów bocznych w alkilobenzenach)
6.F + 1-bromobutan → hept-2-yn + NaBr (alkilowanie alkinów terminalnych)
7.G + anilina (2 mole) → N-fenyloacetamid (acetanilid) + chlorek aniliniowy (otrzymywanie
amidów kwasowych)
8.H + NaOH (50%, ∆t) → benzoesan sodu + alkohol benzylowy (reakcja Cannizzaro)
9
H
3
C
Cl
O
NH
2
HN CH
3
O
NH
3
+
Cl
−
+
+
chlorek acetylu
O H
O ONa
CH
2
OH
NaOH (50%, t)
+
benzaldehyd
C
CH
3
OC
2
H
5
O
C
CH
3
H
3
C
CH
3
OH
(1) CH
3
MgI, (2) HCl aq
octan etylu
ONa
Br
CH
3
I
OCH
3
Br
4-bromofenolan sodu
NO
2
CH
2
OH
NO
2
O OH
K
2
Cr
2
O
7
/ H
+
alkohol p-nitrobenzylowy
NO
2
CH
3
lub
p-nitrotoluen
CH
3
-C
C-Na
C
3
H
7
CH
2
Br
CH
3
-C
C-CH
2
C
3
H
7
+
propynylosód

9.I + NaOH (aq) (nadmiar) → p-chlorobenzoesan sodu + etanol (hydroliza estrów)
10.J + KMnO
4
(aq), 0
°
C → butano-2,3-diol (utlenianie alkenów)
Zad. 3. (6p) Wykonaj następujące polecenia:
a. podaj nazwę związku C z uwzględnieniem jego konfiguracji absolutnej oraz określ
konfigurację absolutną związków A, B,
b. narysuj wzór krzyżowy Fischera związku B,
c. narysuj wzór przestrzenny stereoizomeru związku A.
A
B
C
(S)-2-bromo-2-fenylobutan
10
C
6
H
5
(S)
H
3
C
CH
2
CH
3
Br
CH
2
OCH
3
(S)
CH
3
NC
H
COOH
(S)
H
3
C
CH(CH
3
)
2
Br
COOH
(R)
CH
3
(H
3
C)
2
HC
Br
H
CH
2
OCH
3
CN
CH
3
O OC
2
H
5
Cl
O ONa
CH
3
NaOH (aq, nadmiar)
+ C
2
H
5
OH
p-chlorobenzoesan etylu
CH CH
H
3
C
CH
3
OH OH
CH CH
H
3
C
CH
3
KMnO
4
(aq), 0°C
but-2-en
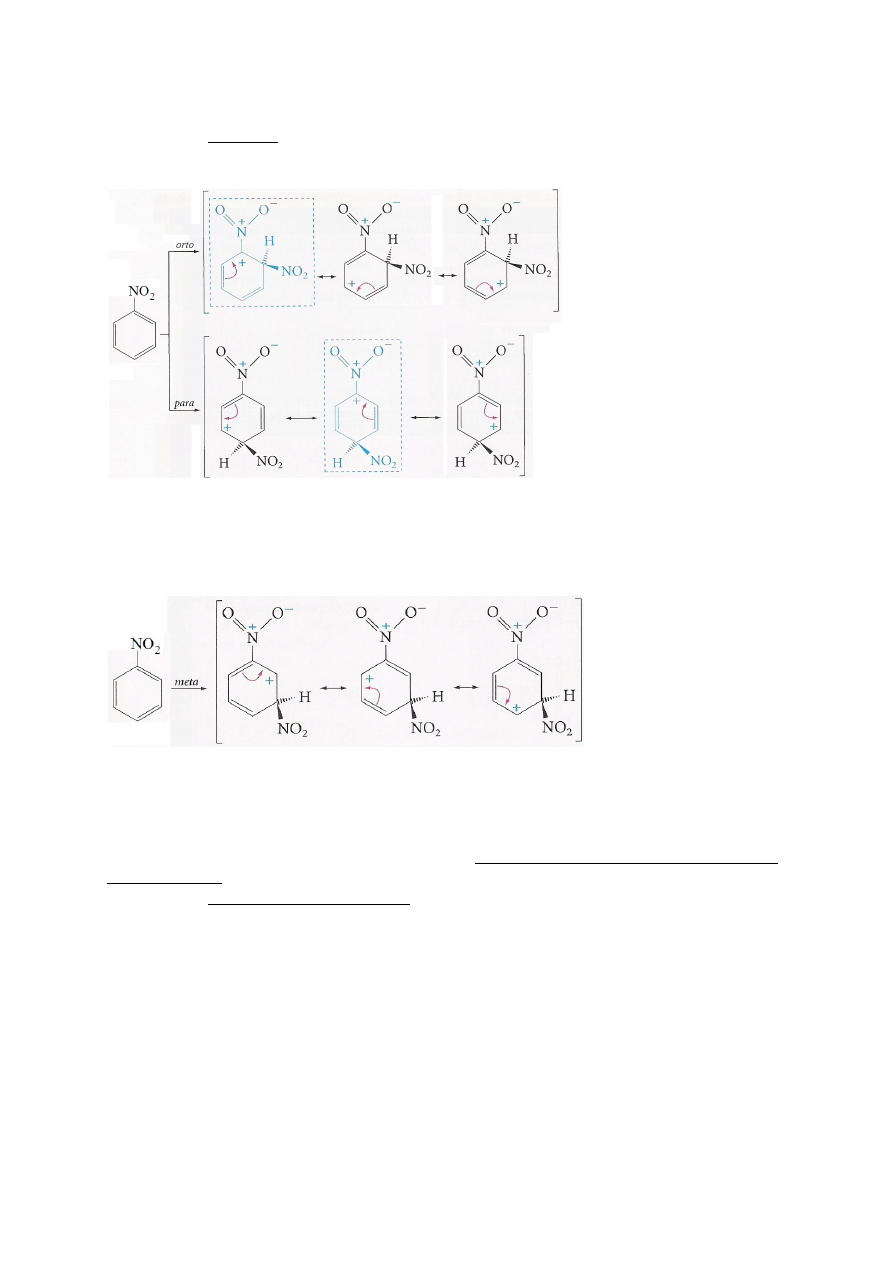
Zad. 4. (12p) Wyjaśnij regioselektywność reakcji nitrowania nitrobenzenu na podstawie
porównania budowy odpowiednich kompleksów sigma (narysuj struktury mezomeryczne tych
kompleksów).
Struktury A i E - szczególnie nietrwałe; ładunek dodatni zlokalizowany na atomie węgla
związanym z podstawnikiem posiadającym cząstkowy ładunek dodatni.
W żadnej ze struktur ładunek dodatni nie jest zlokalizowany na atomie węgla związanym z
podstawnikiem posiadającym cząstkowy ładunek dodatni.
W reakcjach S
E
z udziałem pochodnych benzenu z podstawnikami posiadającymi cząstkowy
ładunek dodatni na atomie związanym z atomem węgla z pierścienia aromatycznego
otrzymuje się meta-
podstawione produkty
, ponieważ tylko wtedy ładunek dodatni nie jest
zlokalizowany na atomie węgla związanym z podstawnikiem posiadającym cząstkowy
ładunek dodatni.
11
A
B
C
D
E
F
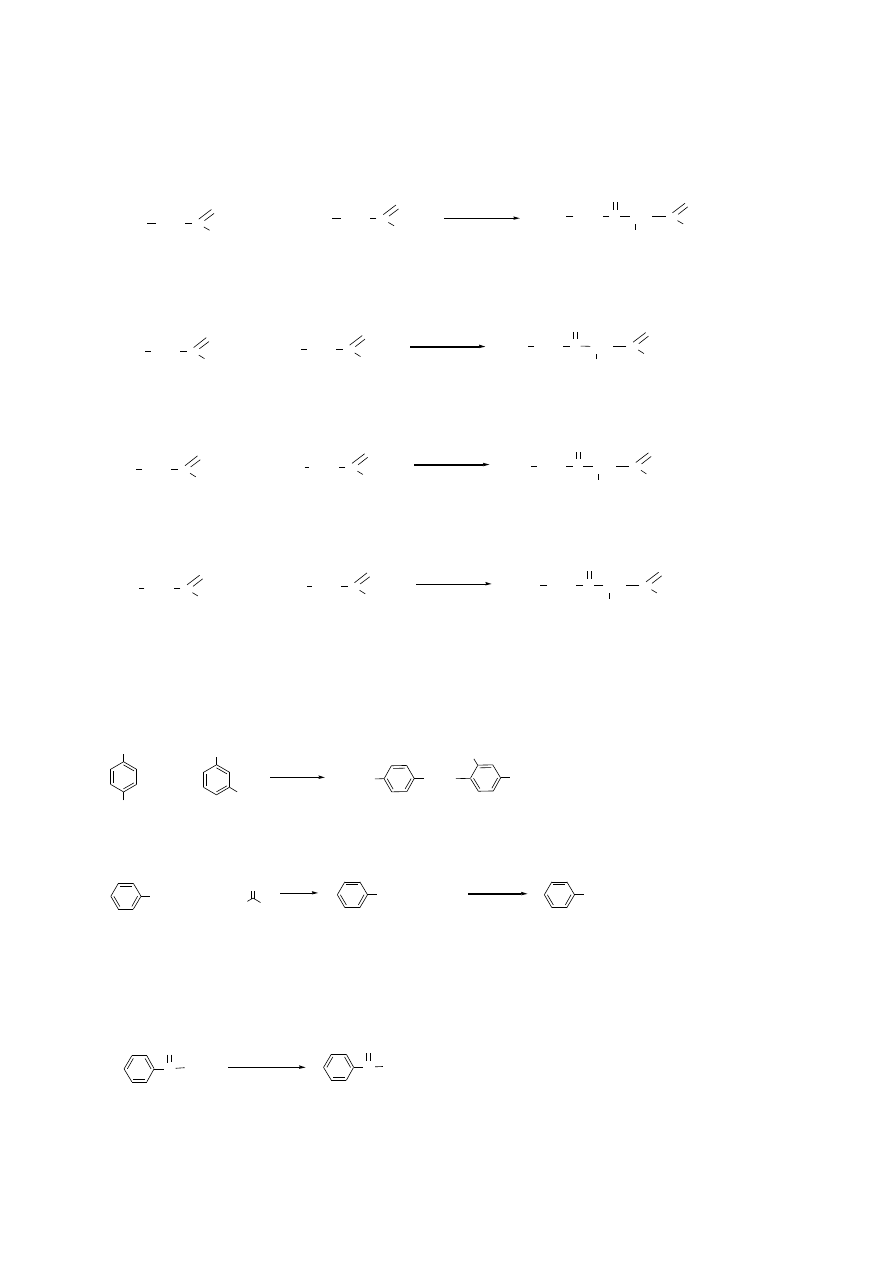
Zad. 5. (10p) Podaj budowę i nazwy wszystkich produktów, jakie powstaną w reakcji
kondensacji Claisena butanianu etylu i propionianu etylu oraz napisz schematy zachodzących
reakcji.
Zad. 6. (34p) Przedstaw schematy poniższych reakcji (za pomocą wzorów strukturalnych)
oraz podaj nazwy produktów (oprócz podpunktu 10):
1.(2p) chlorek p-nitrobenzenodiazoniowy + m-krezol, pH 9 →
(sprzęganie soli diazoniowych)
2.(3p) bromek fenylomagnezowu + (1) aldehyd mrówkowy, (2) HCl
(aq) →
(addycja zw. Grignarda do związków karbonylowych)
alkohol benzylowy
3. (3p) benzamid + NaOH
(aq) (nadmiar, ∆t) →
(hydroliza amidów kwasowych)
benzoesan sodu
12
N
2
+
Cl
−
NO
2
CH
3
OH
N=N
O
2
N
H
3
C
OH
+
pH 9
MgBr
H H
O
CH
2
OMgBr
CH
2
OH
+
HCl aq
C
O
NH
2
C
O
ONa
NaOH
nadmiar
+ NH
3
C
O
OC
2
H
5
CH
3
CH
2
CH
3
CH
2
C
O
OC
2
H
5
C
2
H
5
CH
2
C
O
OC
2
H
5
OC
2
H
5
C
2
H
5
CH
2
C
O
CH
3
CH
2
C
O
OC
2
H
5
C
2
H
5
CH
2
C
O
OC
2
H
5
C
2
H
5
ONa
C
2
H
5
ONa
C
2
H
5
ONa
C
O
OC
2
H
5
CH
3
CH
2
OC
2
H
5
C
2
H
5
CH
2
C
O
C
2
H
5
ONa
CH
3
CH
2
C
O
CH C
O
OC
2
H
5
CH
3
CH
3
CH
2
C
O
CH C
O
OC
2
H
5
C
2
H
5
C
2
H
5
CH
2
C
O
CH C
O
OC
2
H
5
CH
3
C
2
H
5
CH
2
C
O
CH C
O
OC
2
H
5
C
2
H
5
+
+
+
2-metylo-3-oksopentanian etylu
2-etylo-3-oksoheksanian etylu
2-etylo-3-oksopentanian etylu
butanian etylu
propionian etylu
+
2-metylo-3-oksoheksanian etylu
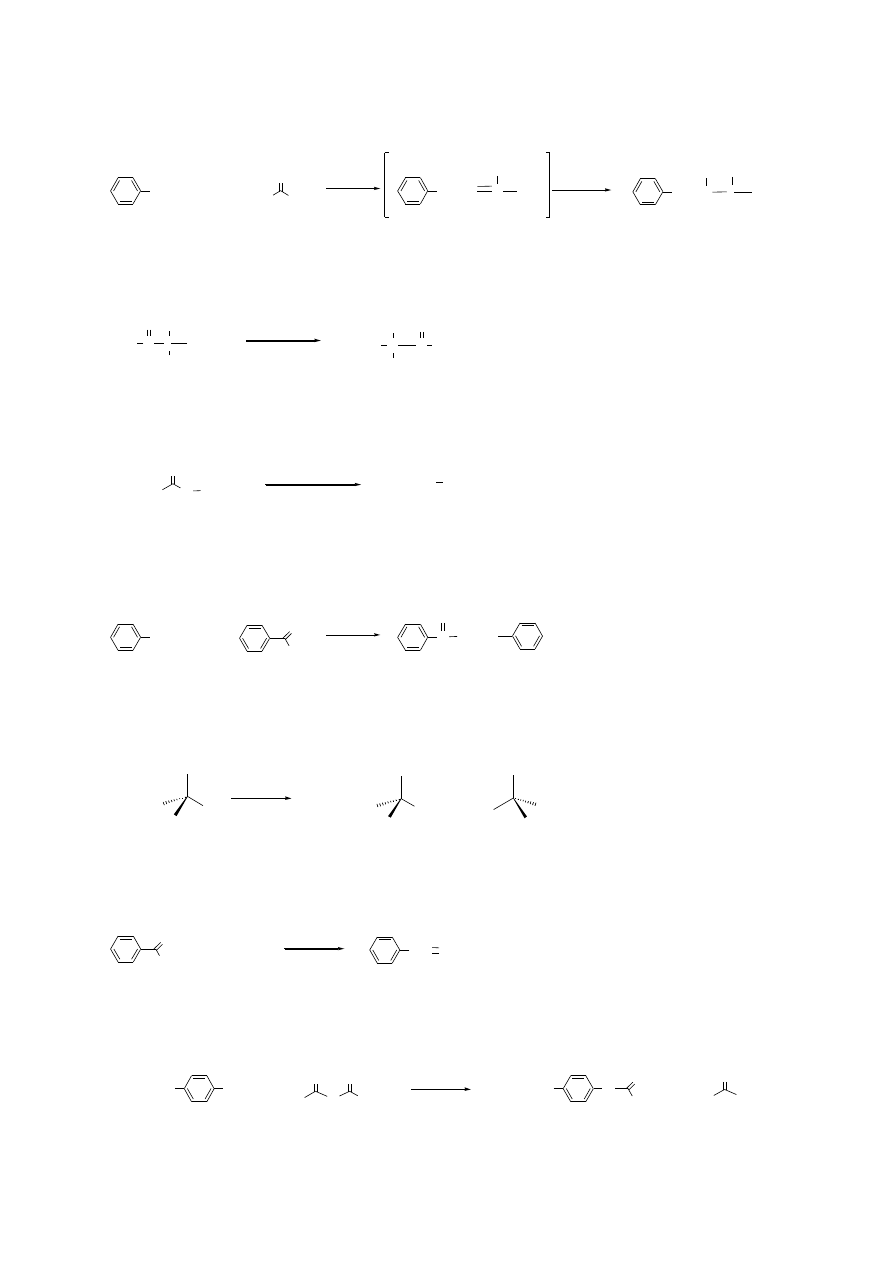
4.(4p) benzyloamina + (1) aceton wobec H
+
, (2) LiAlH
4
→
(aminowanie redukcyjne aldehydów i ketonów)
benzylo-izopropyloamina
5.(3p) 3,3-dimetylo-2-butanon + 3 mole I
2
+ NaOH (nadmiar) →
[reakcja haloformowa (jodoformowa)]
2,2-dimetylopropionian sodu jodoform
6.(5p) propanian etylu + (1) LiAlH
4
, (2) HCl aq
→
(redukcja estrów)
propan-1-ol etanol
7. (3p) alkohol benzylowy + chlorek benzoilu →
(estryfikacja alkoholi)
benzoesan benzylu
8.(5p) (R)-2-chloro-2-fenylobutan + H
2
O (nadmiar) →
(substytucja nukleofilowa halogenków alkilowych, solwoliza, S
N
1)
(R)-2-fenylobutan-2-ol
(S)-2-fenylobutan-2-ol
9.(3p) benzaldehyd + NH
2
OH (kat. H
+
) →
(addycja amoniaku i jedo pochodnych do aldehydów i ketonów)
oksym benzaldehydu
10.(3p) p-izopropylofenol + bezwodnik octowy →
(estryfikacja fenoli)
octan p-izopropylofenolu kwas octowy
13
OH
(CH
3
)
2
CH
CH
3
O
CH
3
O
O
O
(CH
3
)
2
CH
O
CH
3
CH
3
O
OH
+
+
CH
2
NH
2
H
3
C CH
3
O
H
+
CH
2
N C
CH
3
CH
3
LiAlH
4
CH
2
N C
H
CH
3
CH
3
H
+
CH
2
OH
O
Cl
C
O
OCH
2
+
Ph
(R)
Cl
CH
3
CH
3
CH
2
H
2
O
Ph
(R)
OH
CH
3
CH
3
CH
2
Ph
(S)
OH
CH
3
CH
2
CH
3
+
nadmiar
CH
3
C
O
C
CH
3
CH
3
CH
3
ONa
C
O
C
CH
3
CH
3
CH
3
I
2
/NaOH
+ CHI
3
O
H
NH
2
OH
H
+
CH N-OH
+
CH
3
CH
2
O CH
2
CH
3
O
(1) LiAlH
4
CH
3
CH
2
CH
2
OH
CH
2
CH
3
OH
+
(2) HCl aq
Document Outline
- Egzamin z Chemii Organicznej 2007/2008, Wydział Inżynierii Chemicznej i Procesowej
- A
- B
- C
- kwas (S)-2-bromo-2,3-dimetylobutanowy
- Egzamin z Chemii Organicznej 2007/2008, Wydział Inżynierii Chemicznej i Procesowej
- A
- B
- C
- (S)-2-bromo-2-fenylobutan
Wyszukiwarka
Podobne podstrony:
chemia fizyczna lab id 112228 Nieznany
Chemia kliniczna kontrola id 11 Nieznany
chemia okiem niechemika id 1126 Nieznany
chemia fizyczna egzamin id 1122 Nieznany
chemia maj 2005 id 112453 Nieznany
chemia przykladowe zad id 11281 Nieznany
Chemia Organiczna Cz1 id 112665 Nieznany
chemia tematy 1kolos id 112928 Nieznany
Chemia polimerow II id 113148 Nieznany
ORG PLAN id 339220 Nieznany
Chemia zadania 13 id 113043 Nieznany
chemia 1b druk id 111785 Nieznany
Chemia egzamin III id 112134 Nieznany
Chemia Organiczna Cz4 id 112695 Nieznany
Chemia zadania 12 id 113042 Nieznany
Chemia zadania 10 id 113041 Nieznany
Chemia matura odp id 112466 Nieznany
Chemia analityczna skrypt id 11 Nieznany
więcej podobnych podstron