
Ruchy Brown’a i dyfuzja
Krzysztof Dołowy

Proces rozpuszczania cukru w wodzie ma
charakter jednokierunkowy.
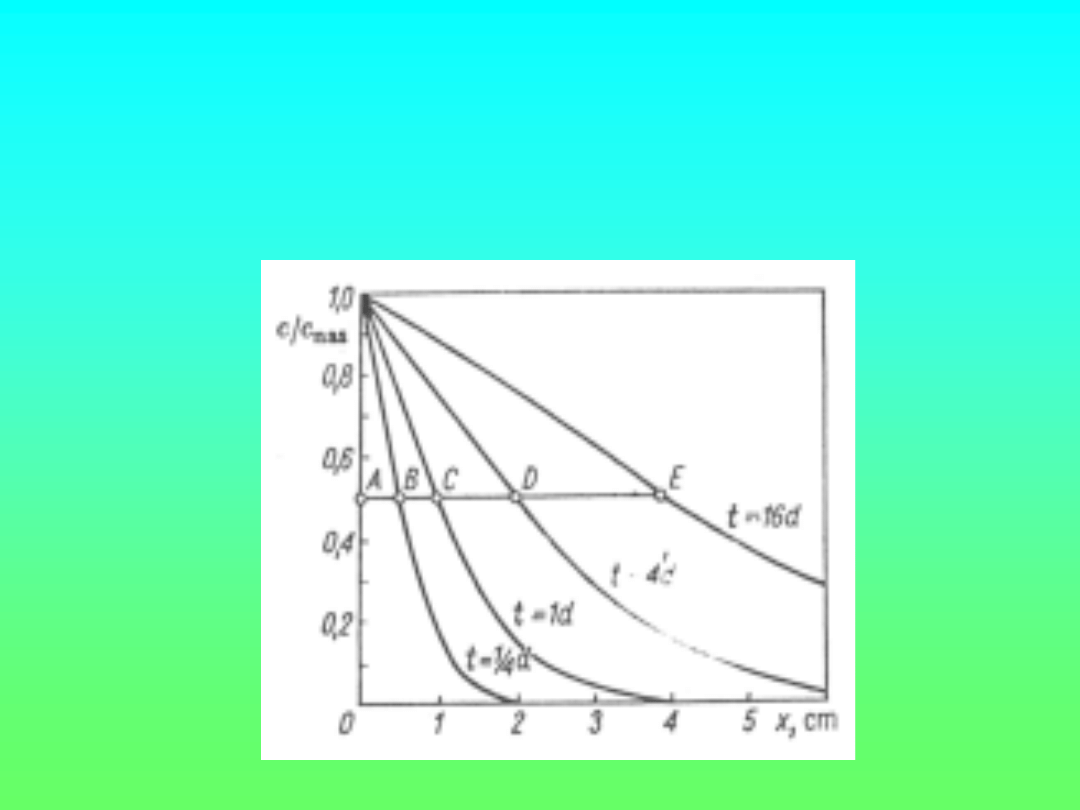
Makroskopowa szybkość dyfuzji jest niewielka.
Potrzeba tygodni, aby stężenie osiągnęło połowę
maksymalnej wielkości w odległości 10 cm od
roztworu stężonego.
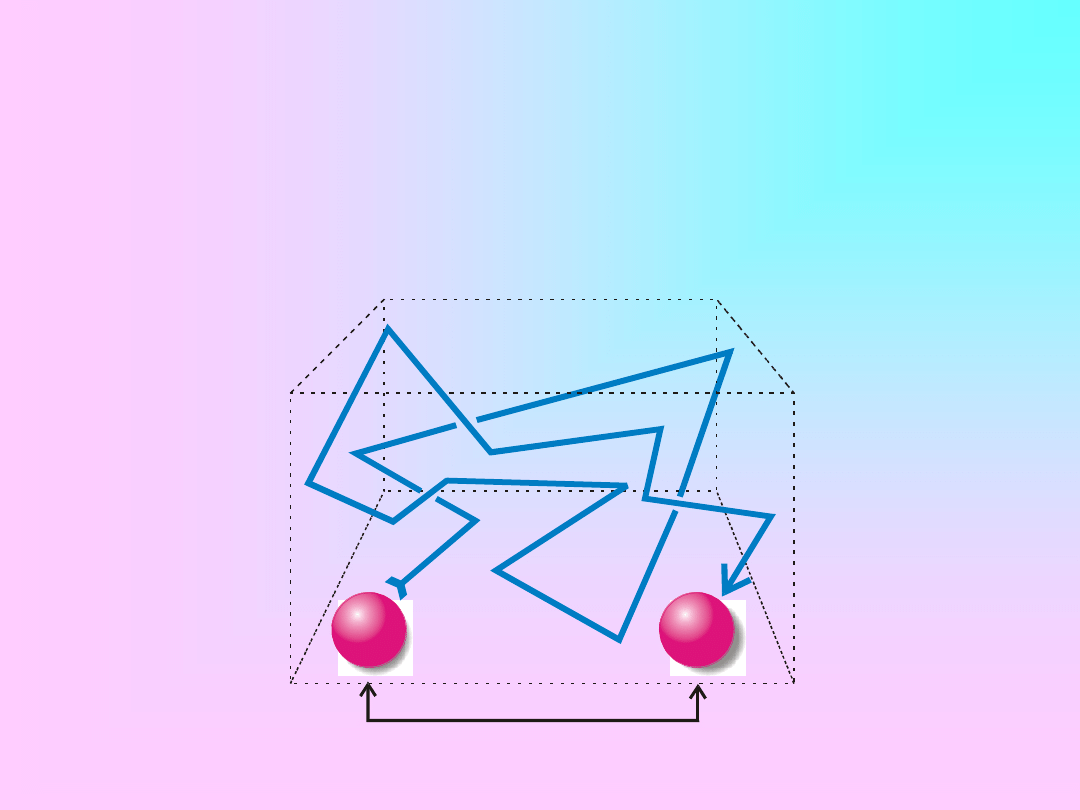
pokonana odległość
Cząstki w roztworze poruszają się ruchem, którego
kierunek jest chaotycznie zmienny – ruchy
Brown’a.
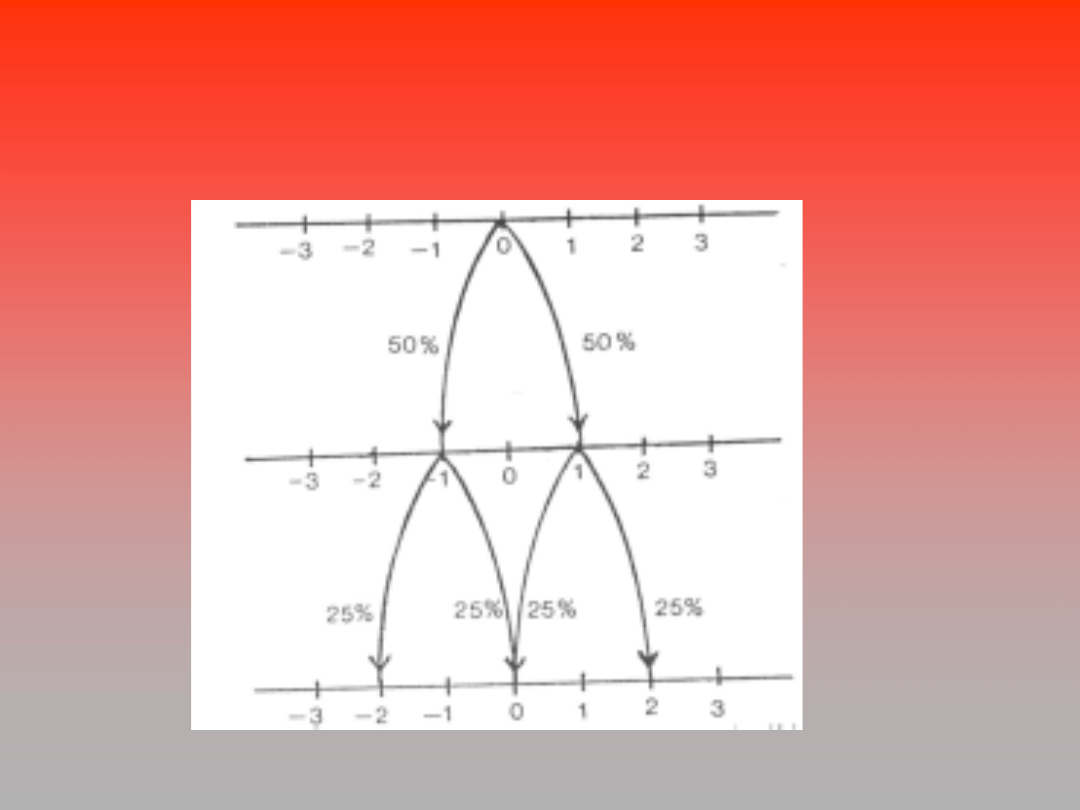
Położenie pijanego marynarza po
wykonaniu 2 kroków
0
0,05
0,1
0,15
0,2
0,25
0,3
-9
-7
-5
-3
-1
1
3
5
7
9
Oddalenie
P
ra
w
do
po
do
bi
e
ńs
tw
o
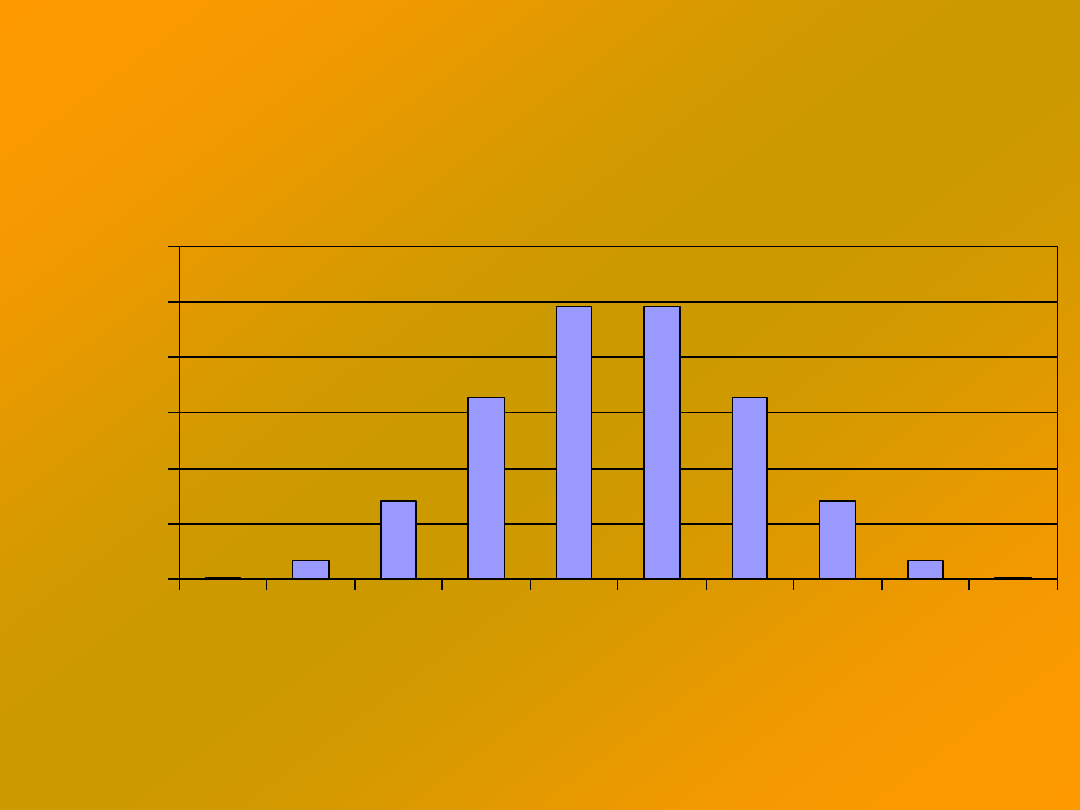
Położenie marynarza po wykonaniu 9 kroków

1
1
x
1
1
x
1
2
2
1
2
1
2
1
x
x
x
?
2
N
x
Średnie przesunięcie kwadratowe miara ruchu
chaotycznego
Ile wynosi przesunięcie po
wykonaniu N kroków?

1
1
N
N
x
x
1
1
N
N
x
x
1
2
2
1
2
2
2
N
N
N
N
x
x
x
x
N
x
N
2
Przesunięcie po wykonaniu N kroków jest
proporcjonalne do ilości kroków.
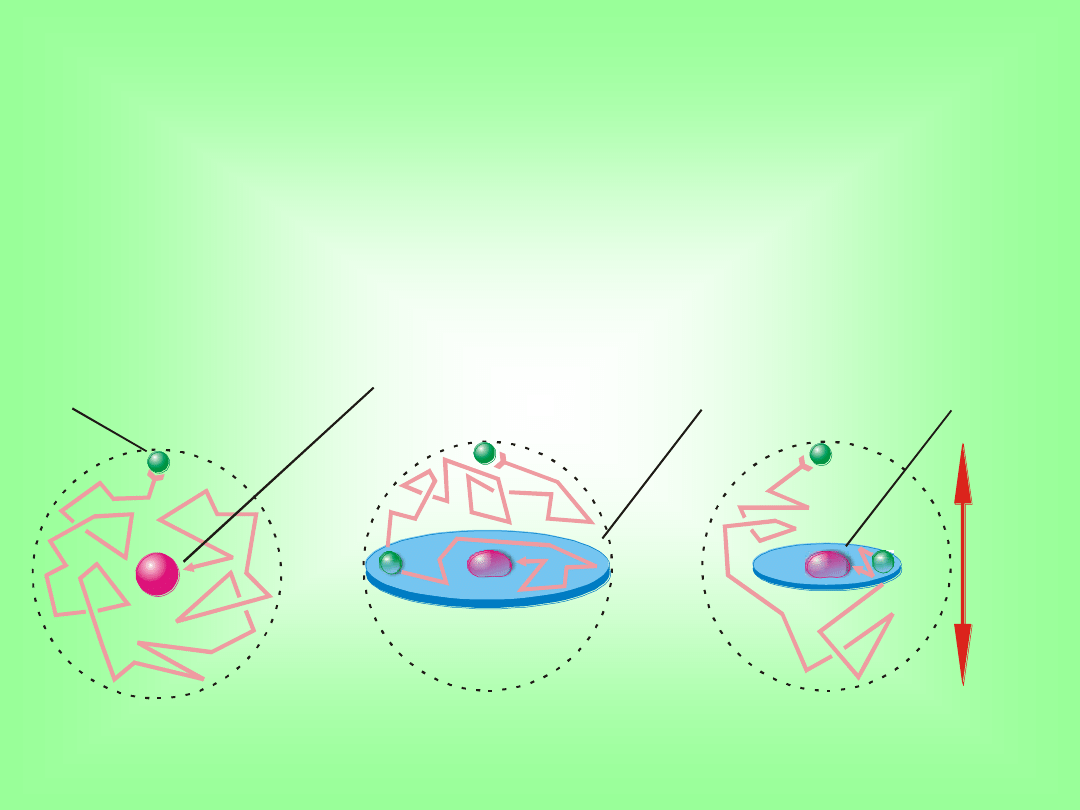
cel o średnicy 5A
o
cząsteczka
metabolitu
duża błona
mała błona
10 m
30 minut do celu
2 minuty do celu
20 sekund do celu
Istnienie błon i zamiana ruchu chaotycznego w
trzech wymiarach na ruch w dwóch wymiarach
znacznie przyśpiesza trafianie molekuły do celu.
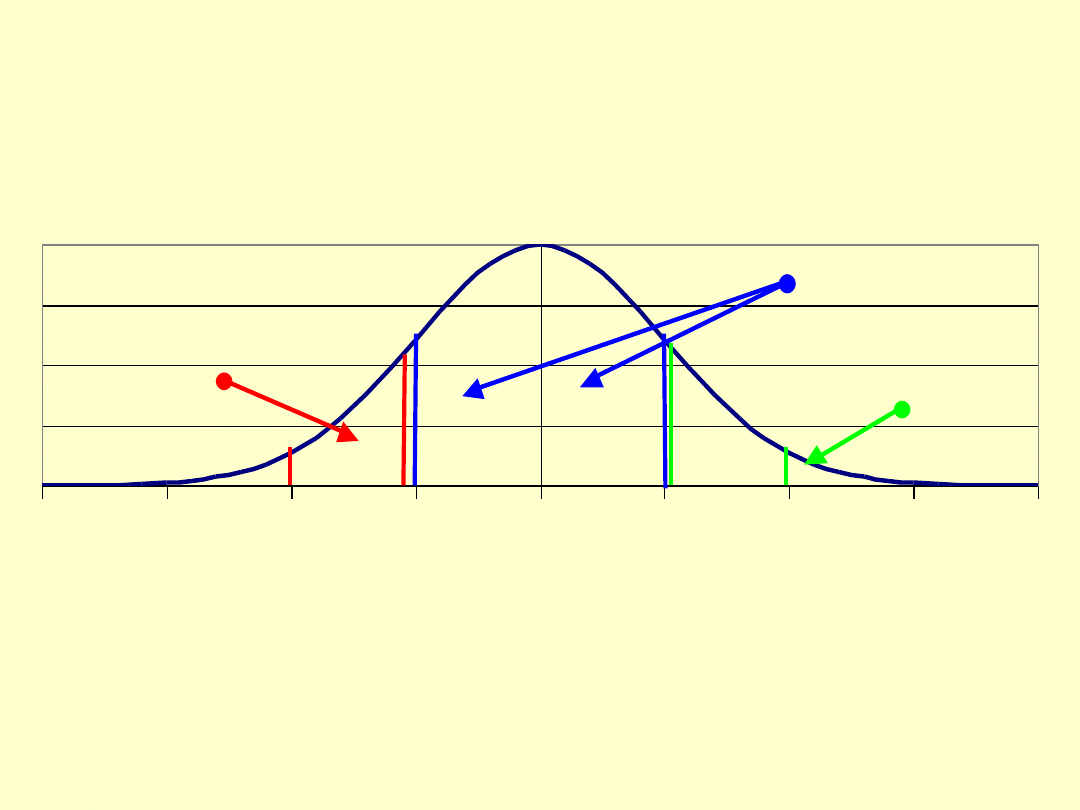
Rozkład normalny
0
0,1
0,2
0,3
0,4
-4
-3
-2
-1
0
1
2
3
4
68%
13,5%
2,5%
Na osi x odchylenie standardowe od wielkości
średniej. Na osi y ułamek wszystkich przypadków.

Wszystkie molekuły znajdują się
w ciągłym ruchu i zderzają się ze
sobą.
Prędkości poszczególnych
molekuł różnią się.

Energia kinetyczna molekuły zależy od
temperatury (czasem nazywana jest wobec
tego energią ruchów termicznych).
Wygodną jednostką energii pojedynczej
molekuły jest
kT
czyli iloczyn stałej
Boltzmann’a i temperatury bezwzględnej.
Średnia energia ruchów molekuł wzdłuż
jednej osi układu współrzędnych (np.
rozrywająca wiązanie chemiczne) wynosi
1kT.
E
kin
%
E
kin
X/1
>0,5kT
61%
>7kT
9,1·10
-4
>1,0kT
37%
>10kT
4,5·10
-5
>1,5kT
22%
>15kT
3·10
-7
>2,0kT
14%
>20kT
2·10
-11
>3,0kT
5%
>30kT
9·10
-16
>5,0kT
0,67%
>40kT
4·10
-20
Energia ruchów termicznych molekuł wzdłuż jednej
osi w stanach skondensowanych, w jednostkach kT
W każdej chwili w jednym ml wody znajduje się 1320
molekuł mających energię większą niż 40kT.
6
2
2
24
!
2
4
!
2
!
4
2
4
4
2
2
1
2
1
2
1
2
2
0
2
2
2
1
!
0
n
n
...
3
2
1
!
1
!
1
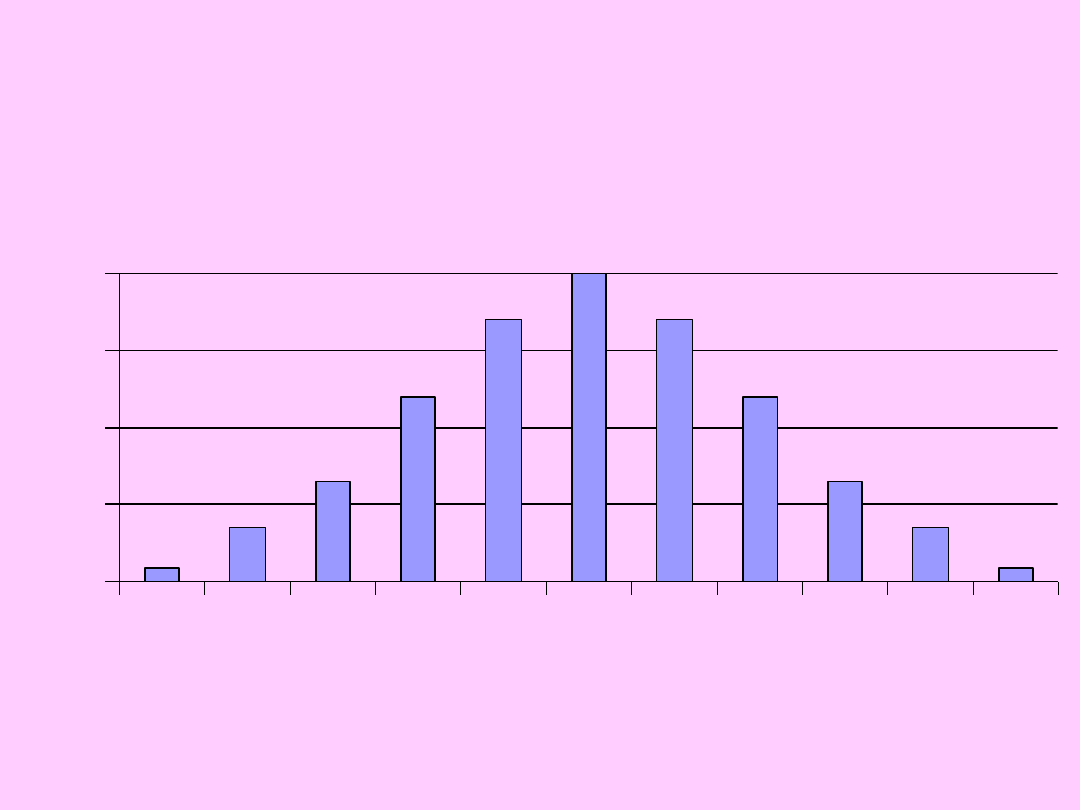
0%
5%
10%
15%
20%
11 12 13 14 15 16 17 18 19 20 21
Ilość molekuł po lewej stronie
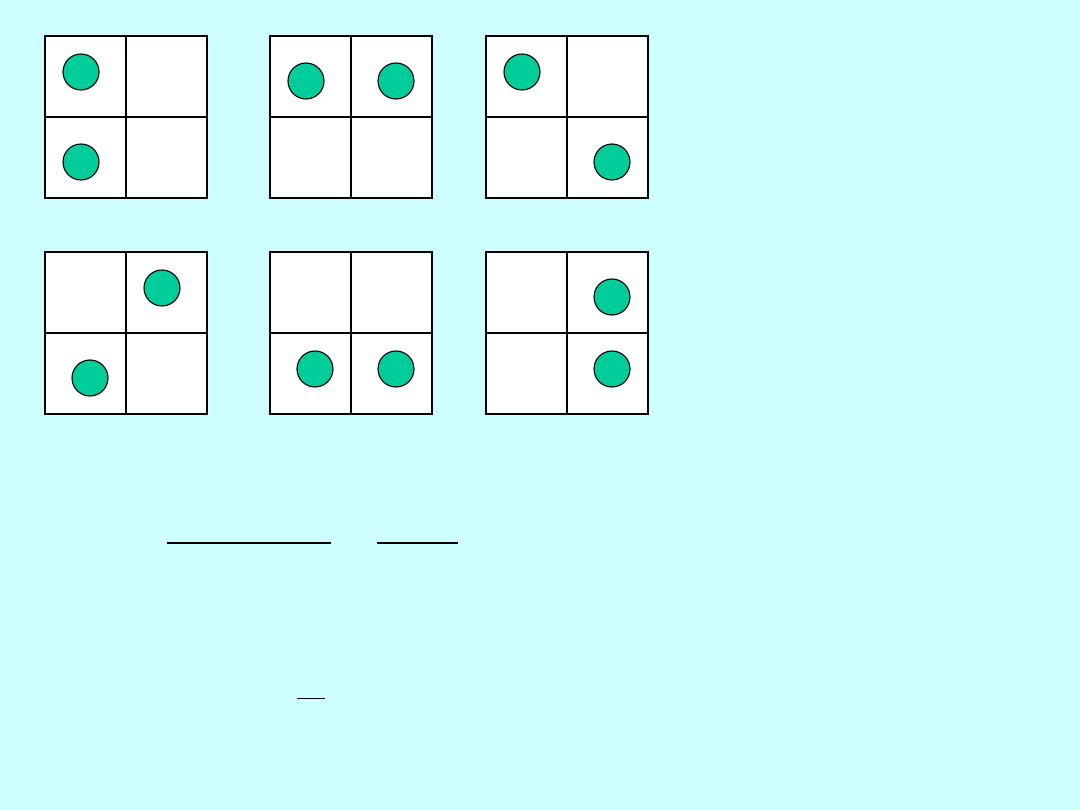
Na 64 miejscach znajdują się 32 molekuły.
Jakie jest prawdopodobieństwo, że po jednej stronie
znajdzie się N molekuł?
kT
kT
S
T
12
,
0
10
2
,
3
10
6
,
3
ln
17
17
16
,
16
15
,
17
kT
kT
S
T
40
1
10
6
,
3
ln
17
16
,
16
0
,
32

Jaka jest przyczyna dyfuzji?
Co jest siłą popychającą molekuły?
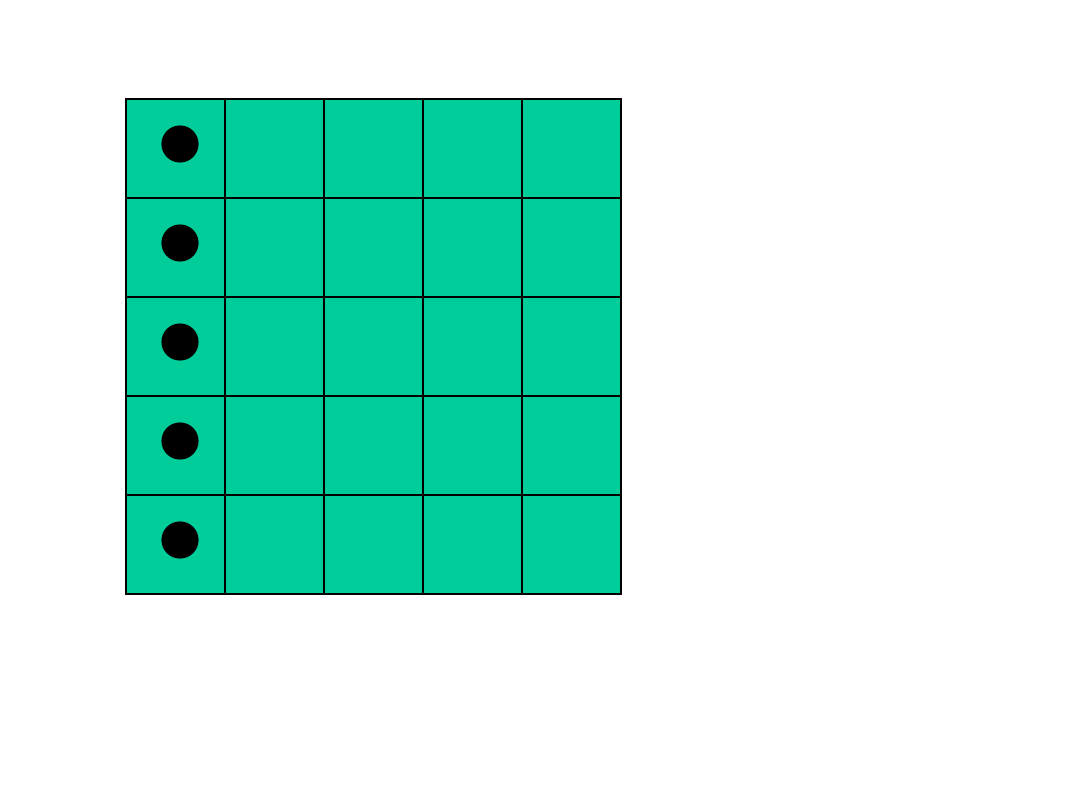
1
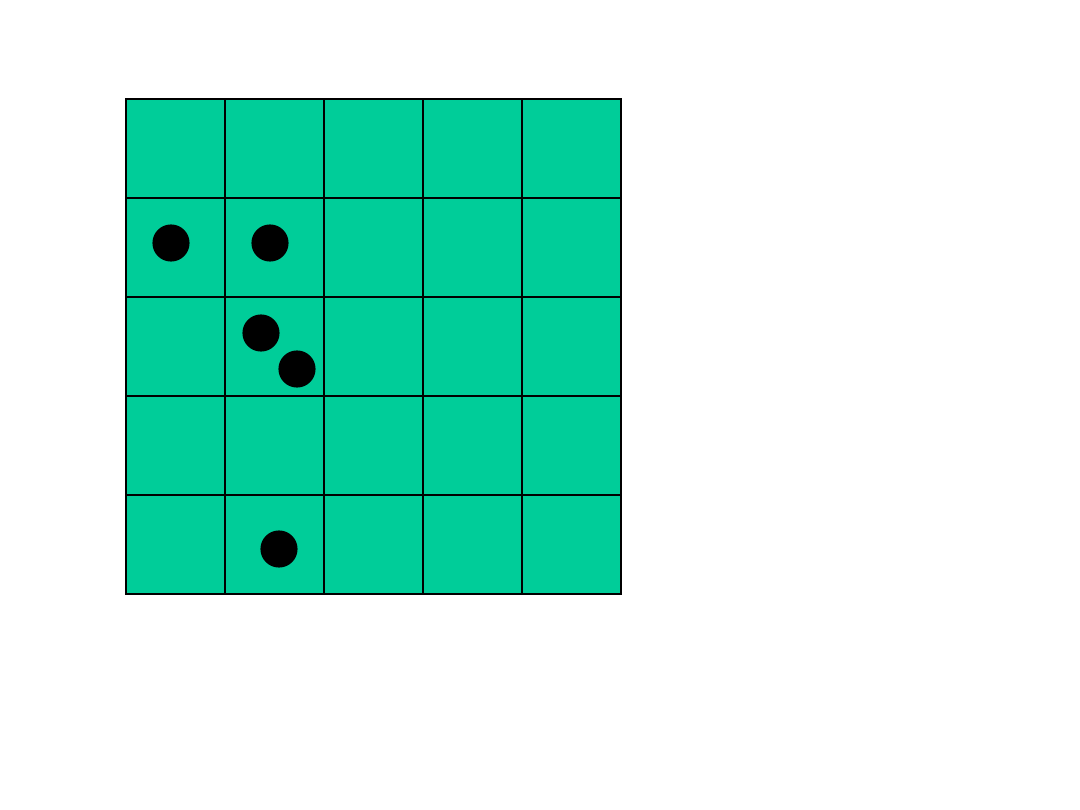
2
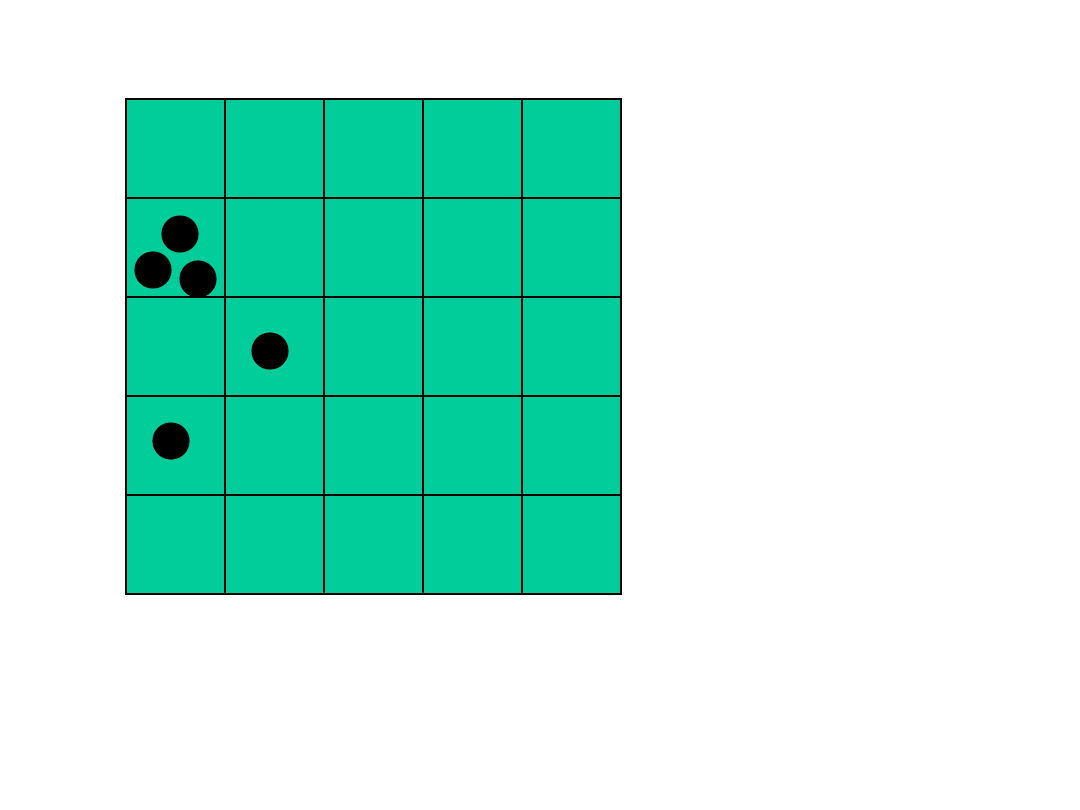
3
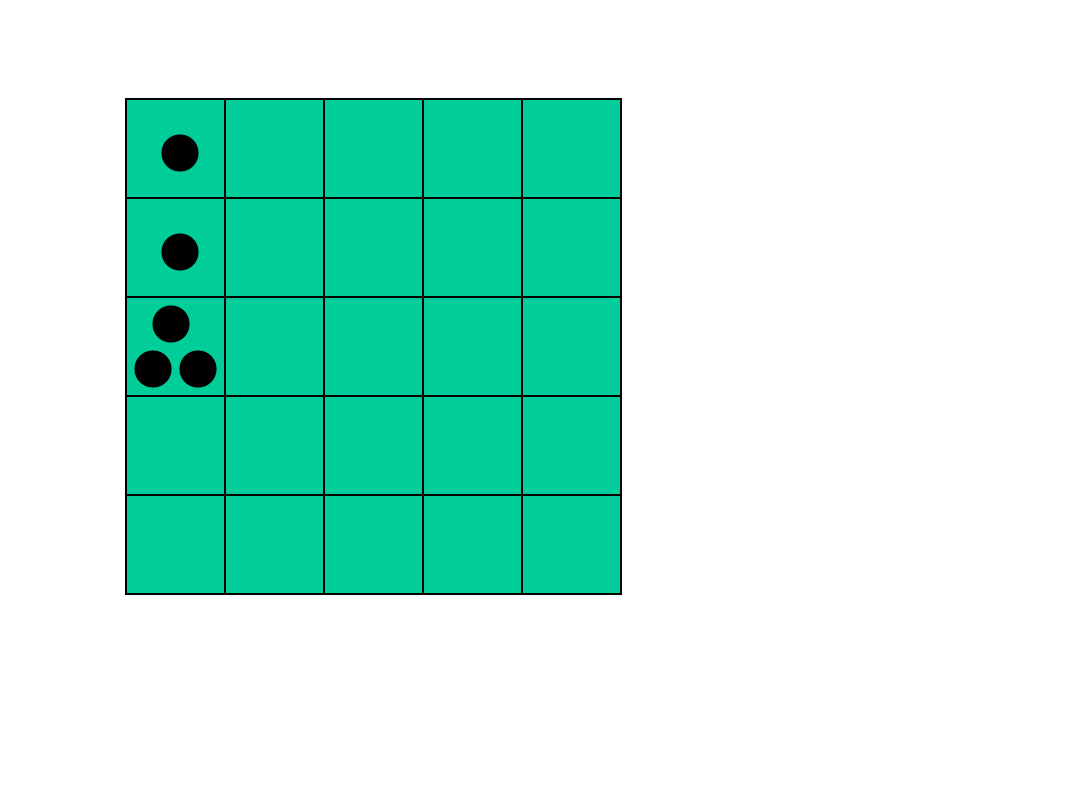
4
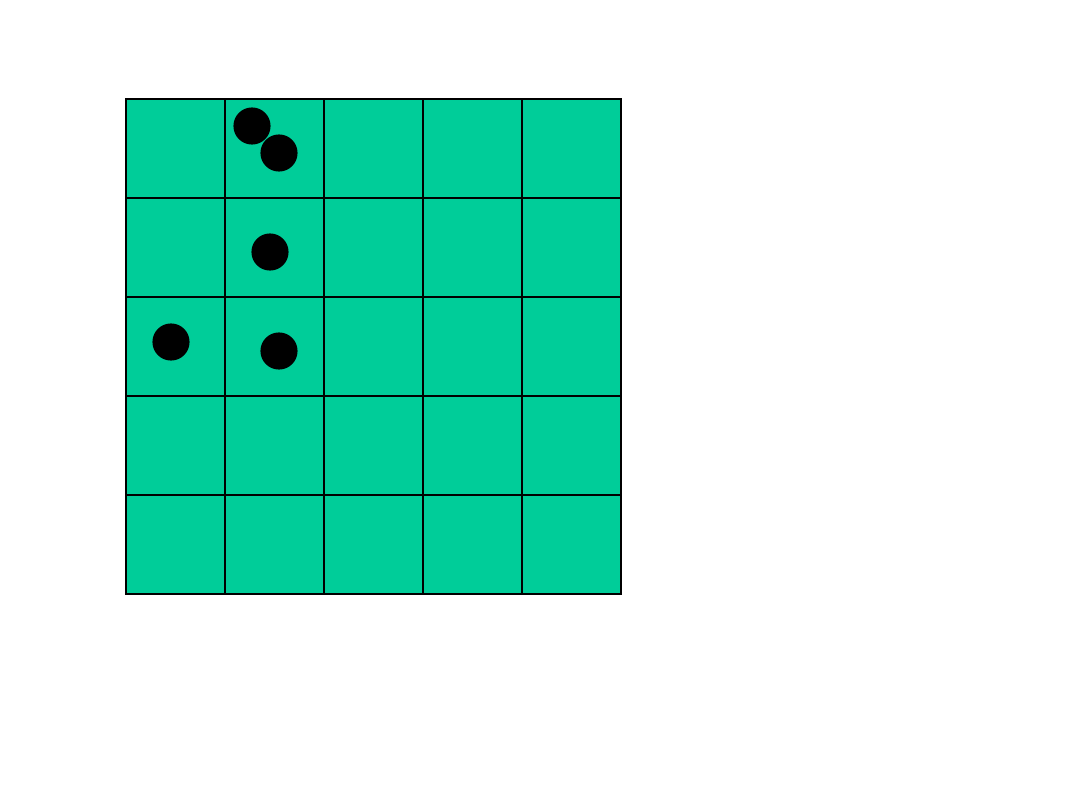
5
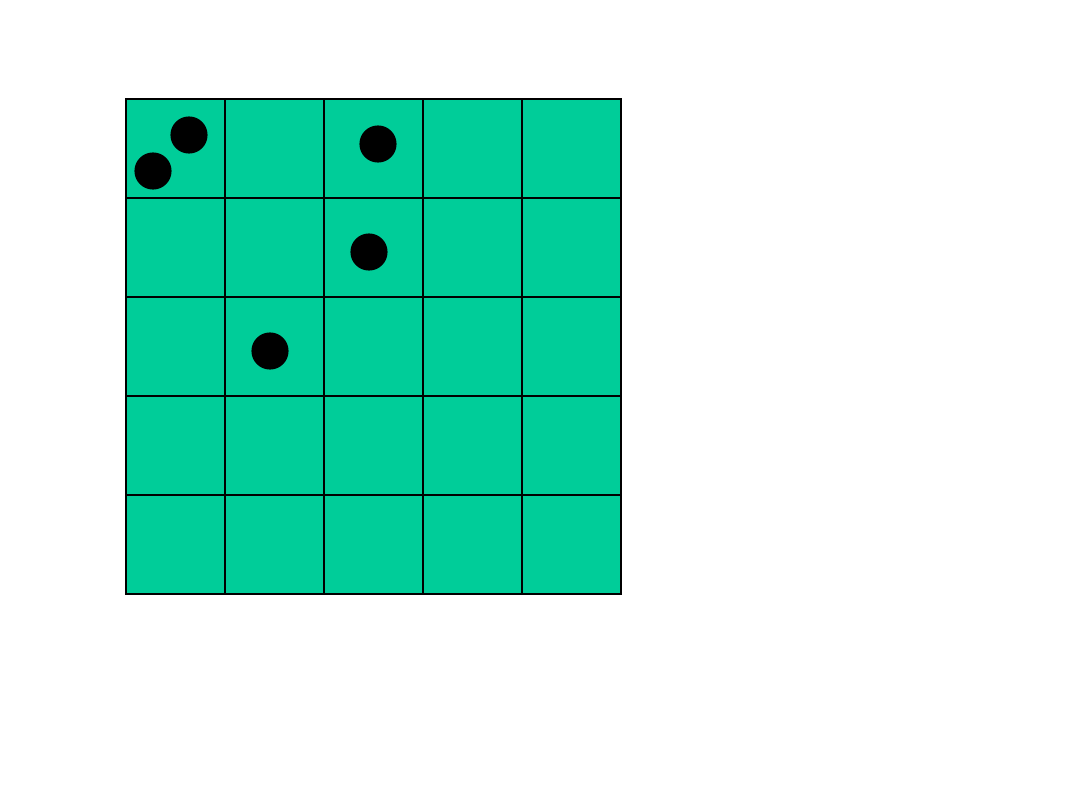
6
7
8
9
10
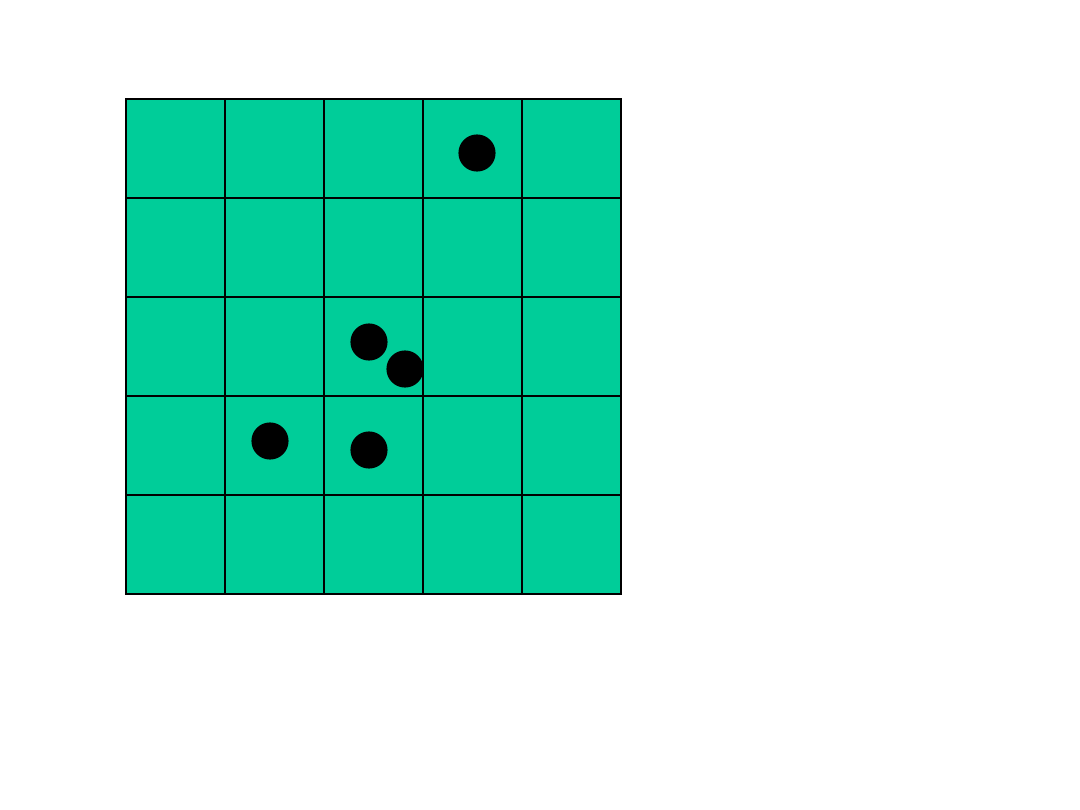
11
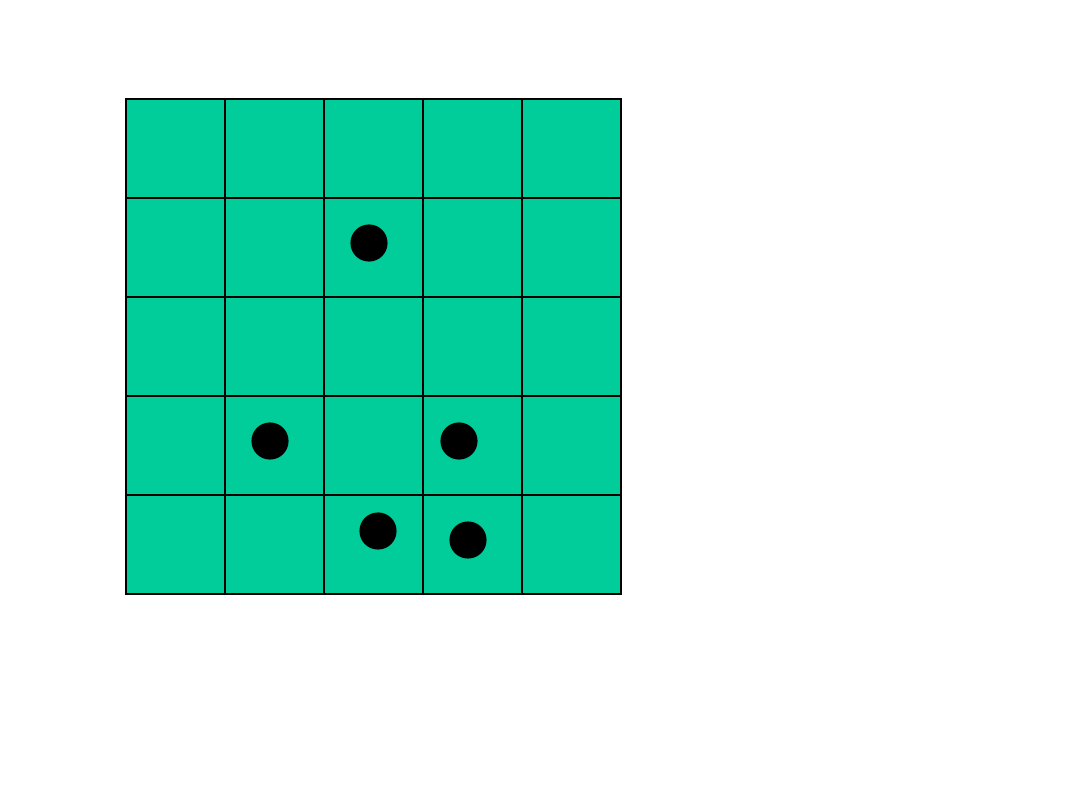
12
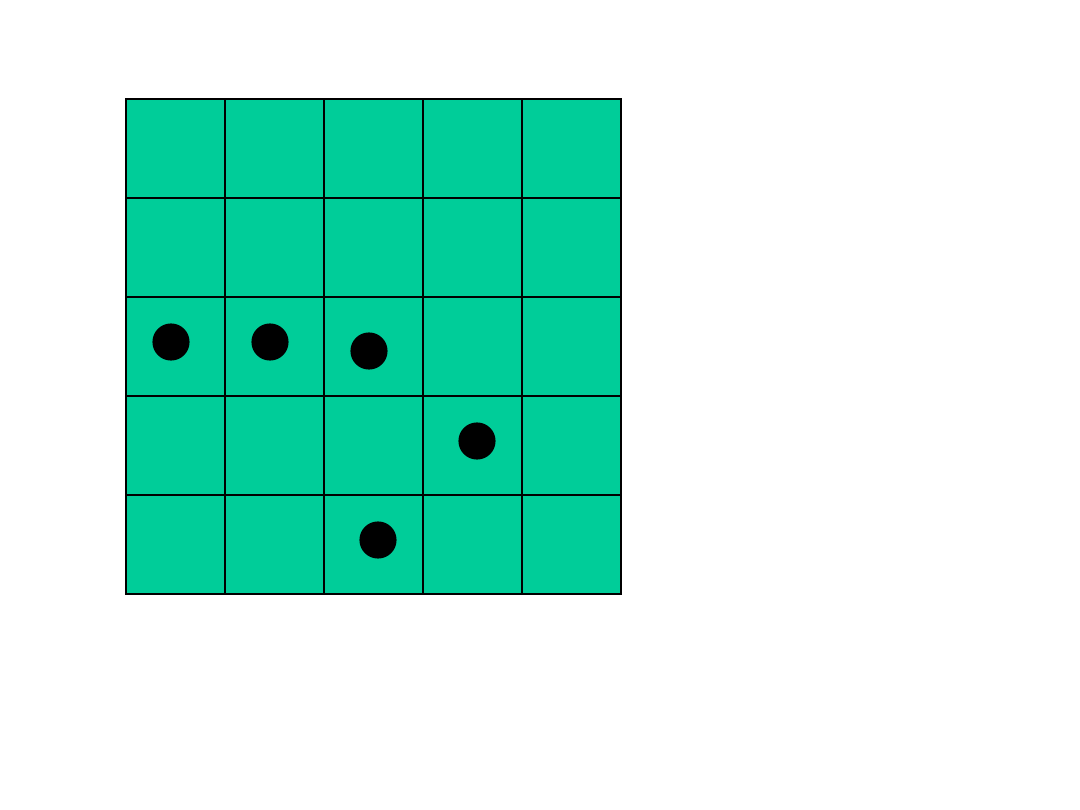
13
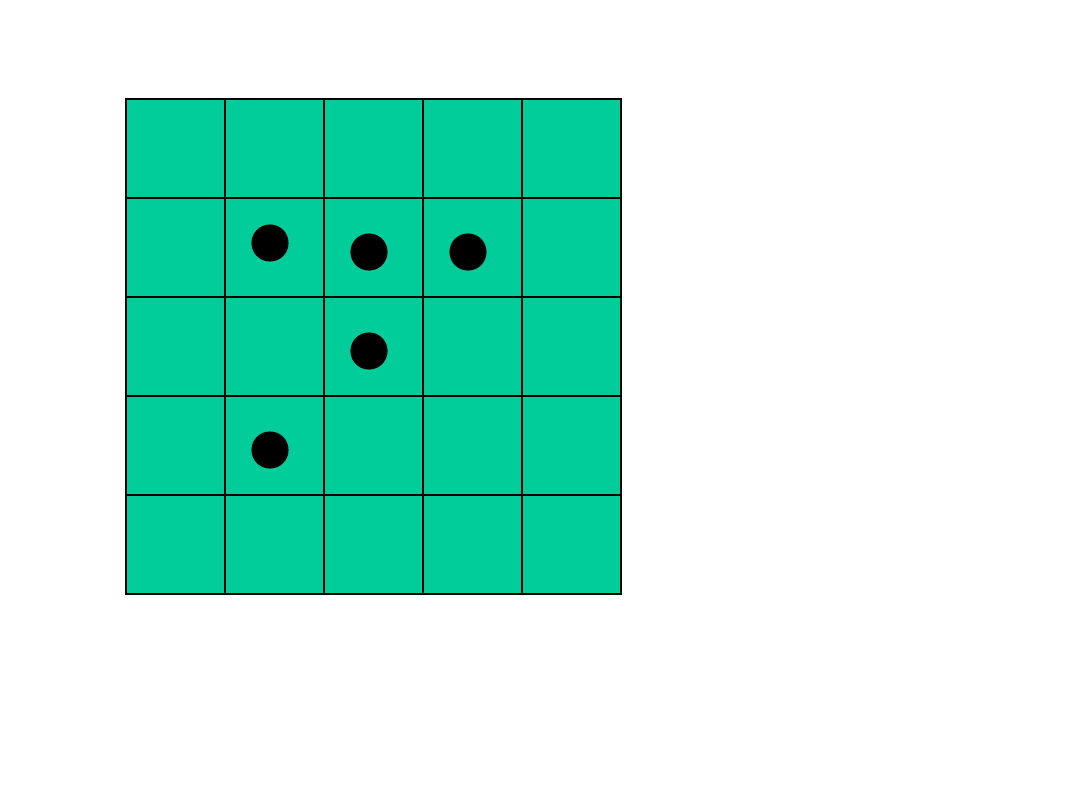
14
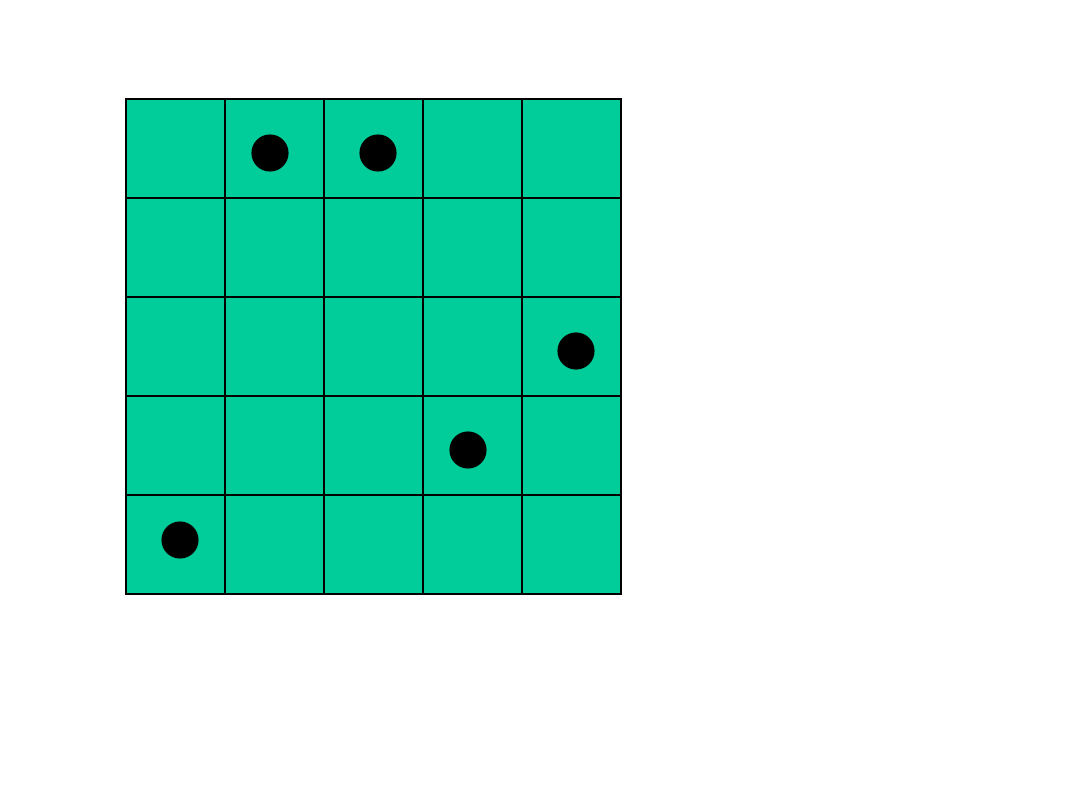
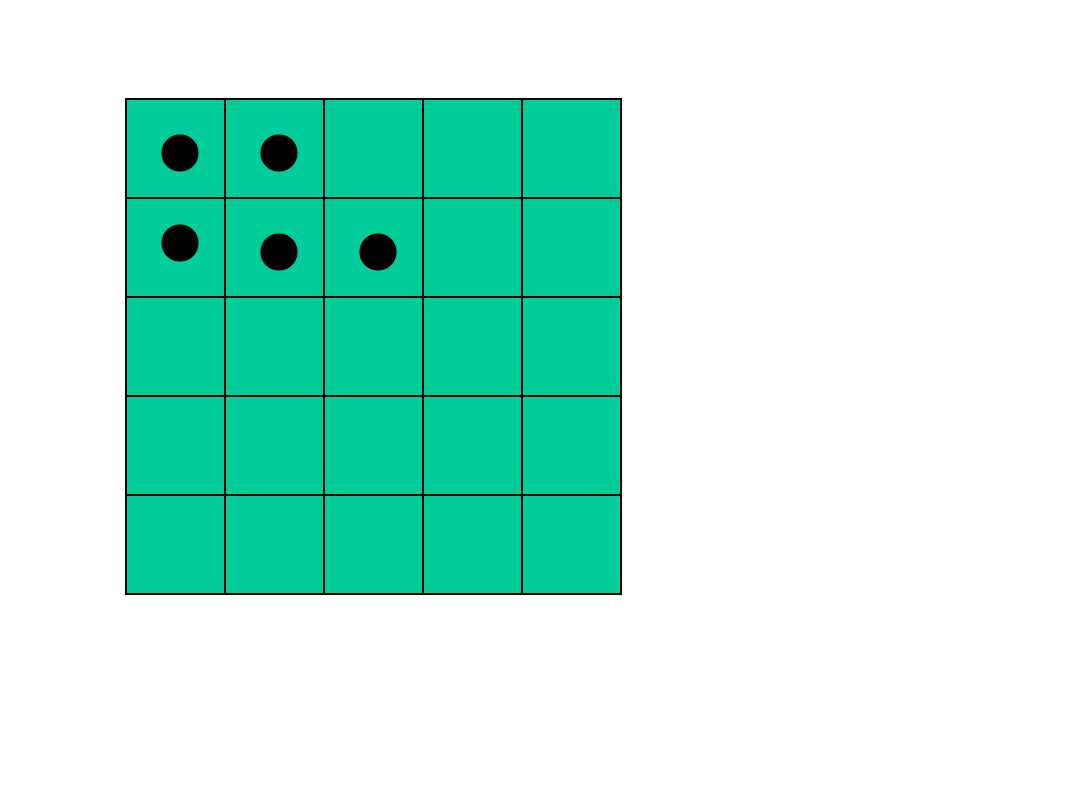
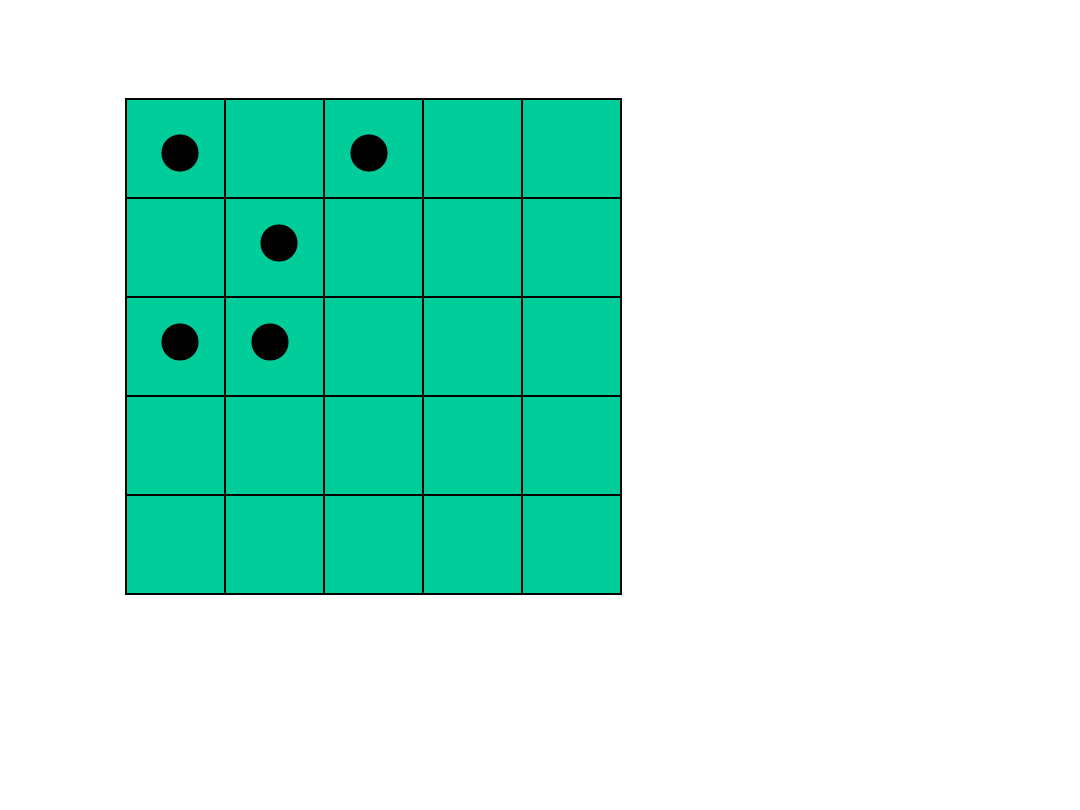
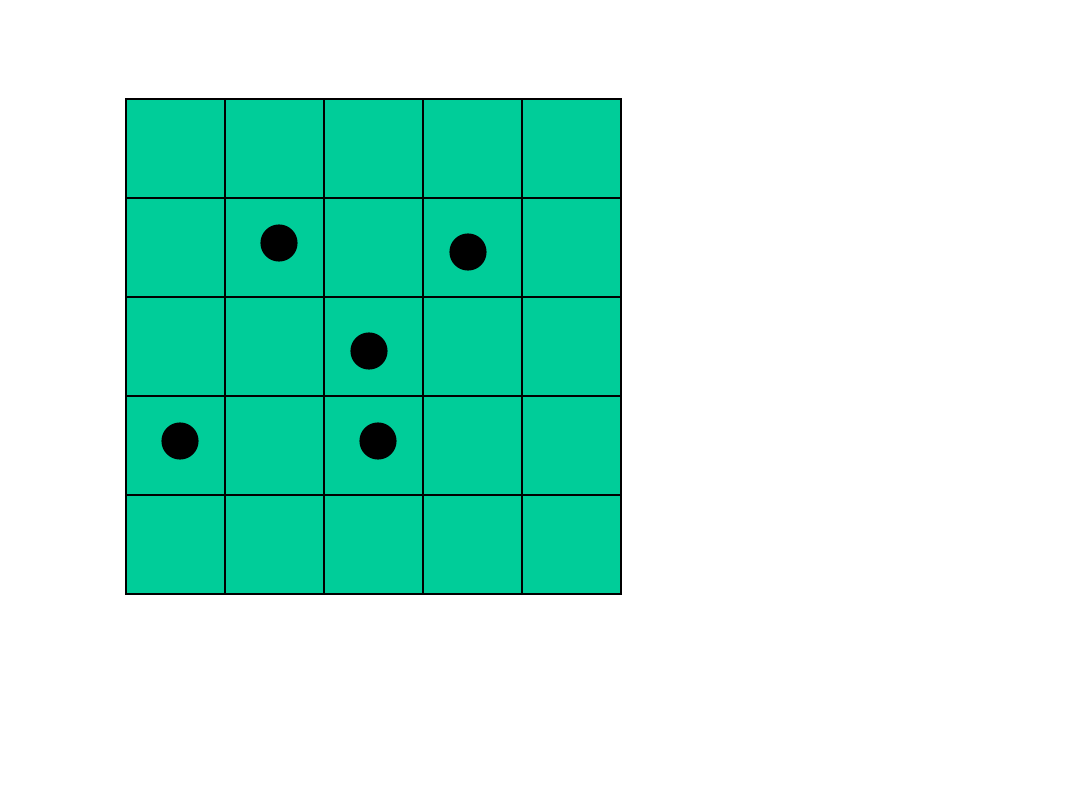
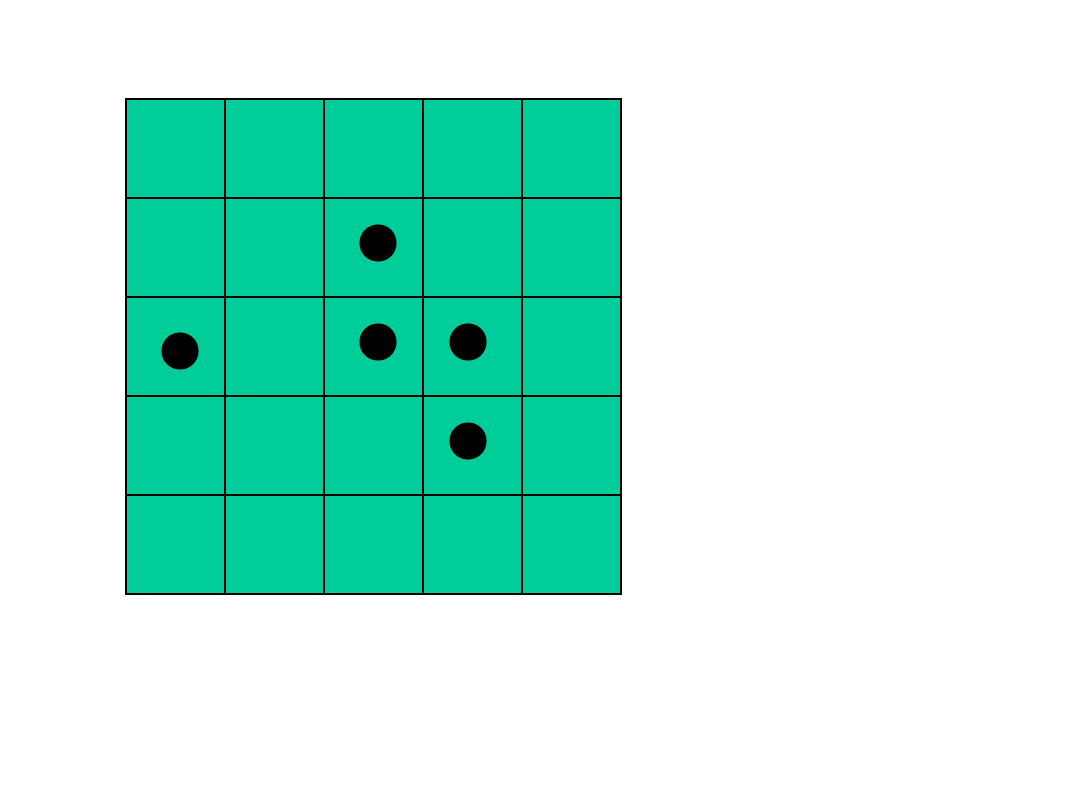
15

Powrót układu do stanu początkowego w przypadku
tablicy 5x5 i 5 molekułach zdarza się raz na 81.000
przypadków.
W przypadku tablicy 7x7 i 7 molekułach raz na
125 milionów przypadków itd.
Przyczyną dyfuzji jest wzrost prawdopodobieństwa
układu o przypadkowym rozmieszczeniu molekuł –
czyli wzrost entropii.

Tasowanie nowej talii kart powiększa ich stan
nieuporządkowania

Wyszukiwarka
Podobne podstrony:
społeczne ruchy miejskie Castells
Ruchy wody morskiej i wody podziemne
Wyklad 5a Dyfuzja
Ustalony ruch przez dyfuzje gazow wg Maxwella
IM 5 dyfuzja wyklad 03
14 Offe, Nowe ruchy społeczne Przekraczanie granic polityki instytucjonalnej
dyfuzja innowacji
Aromaterapia Brown
cw 1 dyfuzja
brown frideric mózg 367LPATEJ24XUTOFEUDK4YDOQF5N3E5YOWWIDMY
(25) Nie odpowiadający za swoje ruchy, w drodze, pos
Ruchy głowy i szyi, WSZ
Grawitacyjne ruchy masowe
współczynnik dyfuzji
Ruchy górotwórcze
Dyfuzja Wzajemnanaszehehe
Solidus, Dyfuzja, Wyżarzanie jako przesycanie, Przesycanie, Starzenie, Kawitacja
Ruch socjalistyczny, Prywatne, CA K. Leszczyńska Wpółczesne ruchy politgyczne
Dżihad 3, US, II semestr, Współczesne ruchy społeczne
więcej podobnych podstron