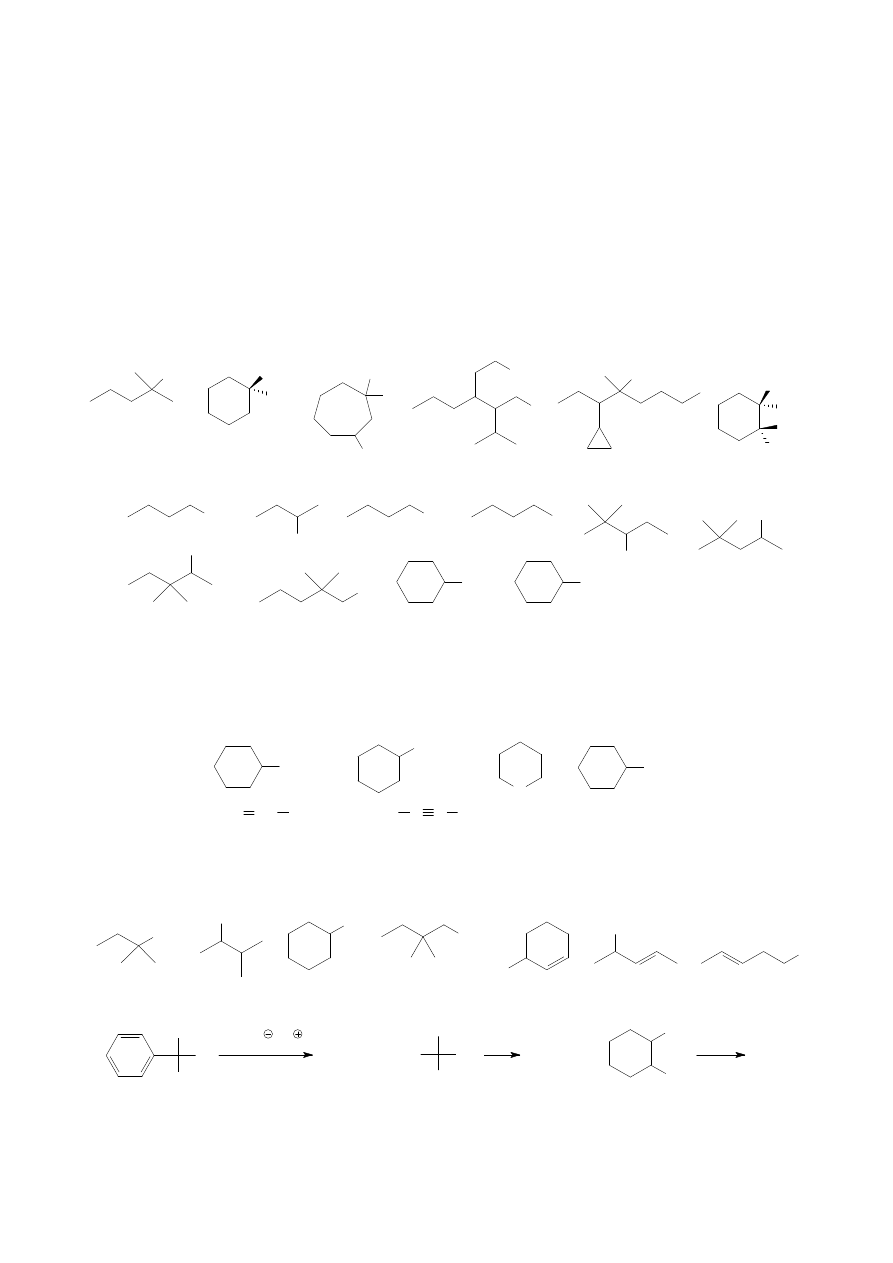
9. Halogenki alkilowe. Substytucja nukleofilowa (S
N
1, S
N
2) i eliminacja (E1, E2).
(konwersatorium, gr. B3 – Chemia, I rok, 2010/2011L)
Zagadnienia
a) Nazewnictwo i rzędowość halogenków alkilowych.
b) Trwałość i przegrupowania karbokationów.
c) Warunki i mechanizmy reakcji substytucji nukleofilowej (S
N
1, S
N
2) oraz eliminacji (E1, E2). Określanie
stereochemii reakcji – inwersja konfiguracji, racemizacja. Reguła Zajcewa.
d) Konkurencyjność reakcji substytucji nukleofilowej oraz eliminacji – przewidywania głównego produktu
reakcji halogenku i nukleofila na podstawie struktury substratu, właściwości nukleofila, zasadowości grupy
opuszczającej i rozpuszczalnika.
Zadania
1. Podaj nazwy systematyczne następujących halogenków alkilowych.
Br
a)
b)
Cl
CH
3
c)
Cl
Cl
F
d)
F
Br
e)
Cl
Cl
I
f)
Cl
Cl
CH
3
H
2. Określ, dla którego z każdej pary halogenków reakcja S
N
2 będzie zachodziła szybciej.
Cl lub
Cl
a)
b)
Cl lub
I c)
Cl
d)
lub
Cl
Br
lub
Br
e)
Cl
CH
2
Cl
lub
3. Próby syntezy eteru tert-butylowo-metylowego, (CH
3
)
3
C-O-CH
3
, z chlorku tert-butylu oraz metanolanu
sodu (CH
3
O
-
Na
+
, mocna zasada) zakończyły się całkowitym niepowodzeniem. Przedstaw strukturę
otrzymanego związku i zaproponuj skuteczną metodę syntezy wspomnianego eteru.
4. Z jakiego halogenku alkilowego i nukleofila można w wyniku reakcji S
N
2 otrzymać następujące
połączenia?
a)
CH
2
OH b)
SCH
2
CH
3
c)
O
d)
CH
2
NH
2
e) H
2
C
CH CH
2
CN
f)
C
C
H
CH
2
CH
2
CH
3
5. Podaj spodziewane produkty solwolizy zachodzącej wg mechanizmu S
N
1, powstające w wyniku
ogrzewania poniższych halogenków alkilowych w etanolu. Tam gdzie to możliwe, narysuj struktury
rezonansowe pośrednich karbokationów.
Br
a)
b)
Br
c)
Cl
d)
Br e)
Br
f)
Br
g)
Br
6. Podaj przewidywane produkty poniższych reakcji:
a)
CH
3
CH
2
CH
3
Cl
CH
3
O Na
...................
b)
CH
3
H
CH
2
CH
3
Cl
KI
...................
c)
CH
3
Br
H
2
O
..................
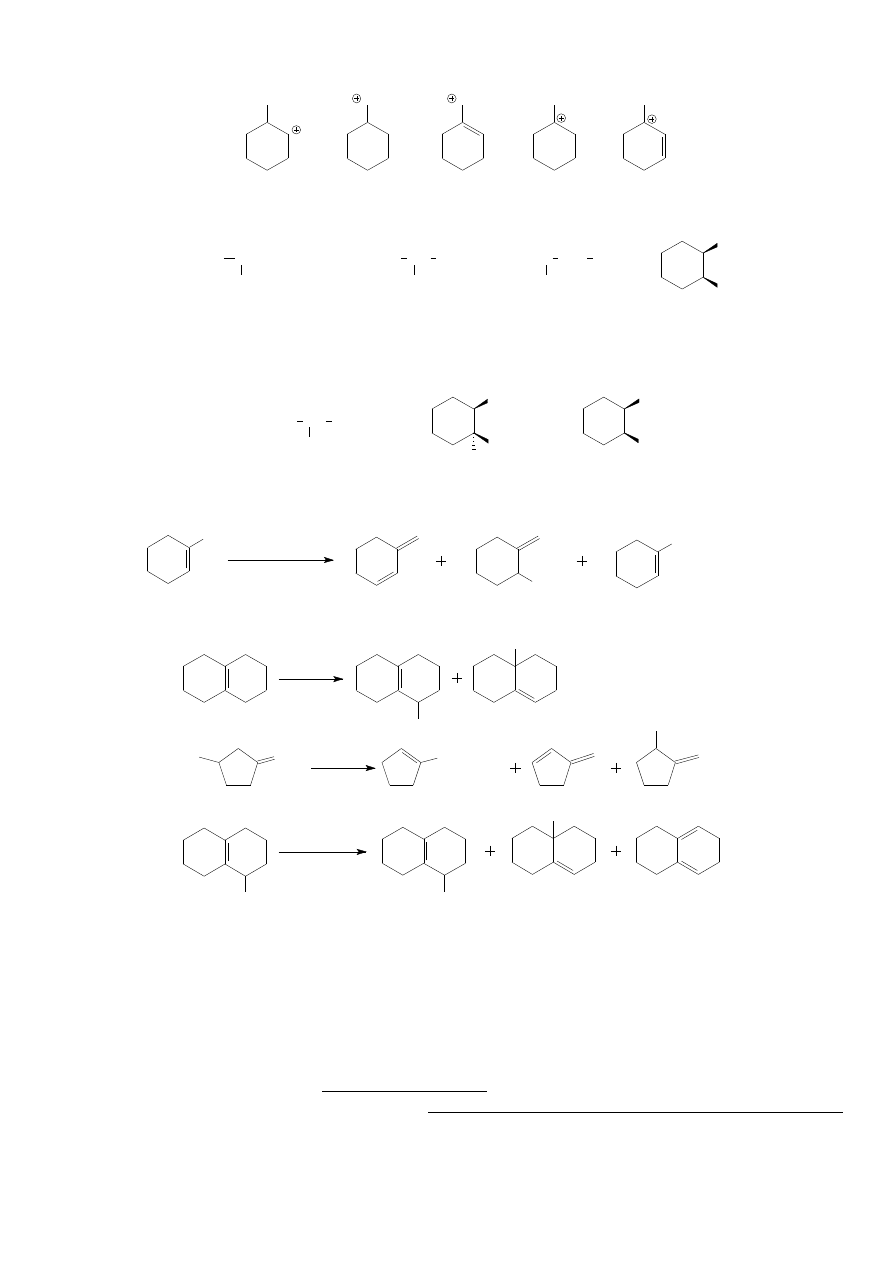
7. Uszereguj poniższe karbokationy według malejącej trwałości. Dwa spośród nich mogą ulegać
przegrupowaniu – wskaż je i narysuj struktury przegrupowanych karbokationów.
CH
3
CH
2
CH
3
CH
3
a)
b)
d)
e)
c)
CH
2
8. Przedstaw możliwe produkty dehydrohalogenacji poniższych związków, zachodzącej wg mechanizmu E2.
Wskaż produkty główne.
(CH
3
)
2
CH C(CH
3
)
2
Br
a)
b) (CH
3
)
2
CH CH CH
3
Br
c) (CH
3
)
2
C CH
2
CH
3
Br
d)
CH
3
Cl
9. Jaki będzie główny produkt dehydrohalogenacji (E2) trans-1-chloro-2-metylocykloheksanu? Uzasadnij
w oparciu o zaproponowany mechanizm.
10. Przedstaw możliwe produkty eliminacji E1 poniższych związków. Wskaż produkty główne.
(CH
3
)
3
C CH CH
3
Br
a)
b)
CH
3
Br
CH
3
c)
CH
3
Br
11. Solwoliza 1-bromometylocykloheksenu w etanolu prowadzi do trzech głównych produktów. Podaj
mechanizmy tłumaczące powstawanie tych związków.
CH
2
Br
etanol
ogrzewanie
OC
2
H
5
CH
2
OC
2
H
5
12. Zaproponuj mechanizmy tłumaczące powstawanie następujących produktów reakcji.
Br
Br
NBS
hν
a)
Br
CH
2
CH
2
OCH
3
OCH
3
CH
3
OH
ogrzew.
b)
Br
ogrzew.
CH
3
CH
2
OH
OC
2
H
5
OC
2
H
5
c)
13. Zestaw związki według malejącej reaktywności w podanych przemianach:
a) reakcja E1:
I. jodek tert-butylu II. chlorek tert-butylu
III. chlorek sec-butylu
b) reakcja S
N
2: I. 1-bromobutan
II. 1-jodobutan
III. 2-jodo-2-metylopentan
c) reakcja S
N
2: I. 1-chloropentan
II. 2-chloropentan
III. 2-chloro-2-metylopentan
d) reakcja S
N
1 I. jodek tert-butylu II. chlorek tert-butylu
III. chlorek sec-butylu
14. (2S,3S)-2-Bromo-3-metylopentan pod wpływem jonów hydroksylowych (lub wody) może ulegać,
w zależności od warunków, reakcjom substytucji i eliminacji, zarówno według mechanizmu jedno- jak
i dwucząsteczkowego. Przedstaw dokładne mechanizmy każdego z procesów (S
N
1, S
N
2, E1 i E2) oraz
wskaż w każdym z przypadków główny produkt, pamiętając o uwzględnieniu aspektów stereochemicznych.
15.
*)
W jaki sposób (S)-2-bromobutan można enancjoselektywnie przekształcić w (S)-butan-2-ol?
Wyszukiwarka
Podobne podstrony:
09 Halogenki alkilowe substytucja eliminacja materialy dodatkowe
AEGON pytania 30 od 26 05 2011 h, AEGON777 id 52 (2)
psychologia społeczna i wychowawcza wykł. 26.05.2011, Egzamin podzielony na grupy ćwiczeniowe godz
26 05 2011 id 31262 Nieznany (2)
AEGON pytania 100 od 26 05 2011 h, AEGON777 id 52 (2)
Korale dla mamy - 26.05.2011 ost, Scenariusze - przedszkole
Halogenki alkilowe – substytucja nukleofilowa – grupa opuszczająca – kwasy i zasady
Zadania z reakcji substytucji nukleofilowej i eliminacji w halogenkach alkilowych
09 05 2011
09 Czek, Weksel 26[1] 05 08
Łódź konsultacje w sprawie Pl Niepodległości (09 05 2011)
Historia sztuki nowożytnej polskiej, 09 05 2011
halogenki alkilowe
19 05 2011 CAid 18227
FIZJOLOGIA CZŁOWIEKA (X WYKŁAD 5 05 2011 r )
więcej podobnych podstron