
Korozja - niszczenie metali , będące wynikiem ich oddziaływania ze środowiskiem.
Czasami określenie korozja stosuje się w odniesieniu do niszczenia tworzyw sztucznych, betonu lub
drewna, chociaż przyjmuje się że w tym przypadku lepszym określeniem jest degradacja.
Korozja jest zjawiskiem naturalnym
Całkowite jej zahamowanie jest bardzo trudne i nie zawsze celowe
Są duże problemy z tworzywami sztucznymi wolno korodującymi
Procesy korozyjne są często pożyteczne – trawienie metali, baterie, warstwy pasywne
Czynniki wpływające na korozję
Wewnętrzne
•
Rodzaj metalu
•
Skład chemiczny
•
Struktura
•
Stan powierzchni
•
Obróbka cieplna
•
Obróbka mechaniczna
•
Naprężenia własne
Zewnętrzne
•
Rodzaj środowiska
•
Skład środowiska
•
Temperatura
•
Prędkość przepływu
•
Ciśnienie atmosferyczne
•
Polaryzacja zewnętrzna
Rodzaje korozji
Zależnie od mechanizmu
elektrochemiczna i chemiczna
Zależnie od środowiska
korozja wodna
korozja atmosferyczna
korozja wysokotemperaturowa
Mechanizm korozji elektrochemicznej
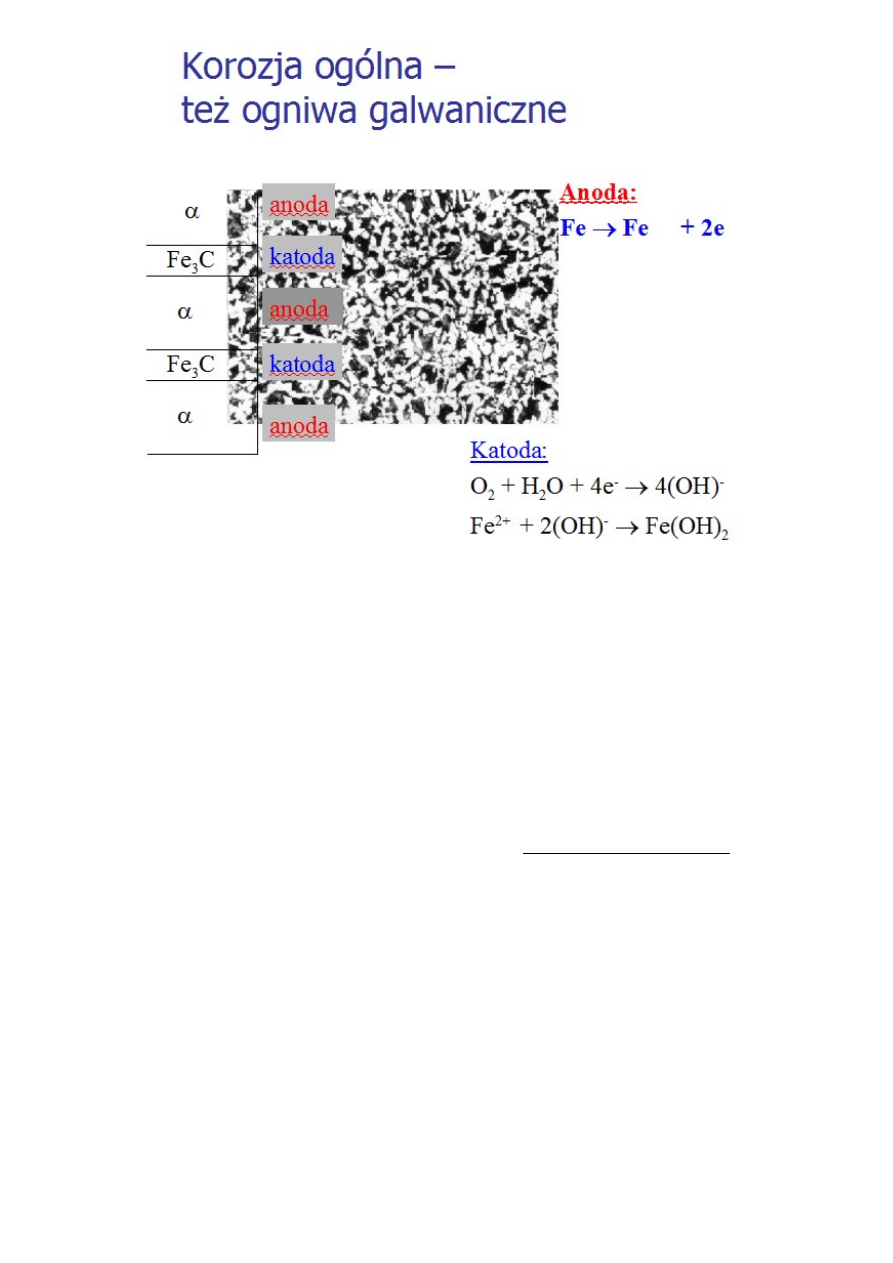
Na powierzchni metalu można zlokalizować miejsca mające charakter anod i katod
Na anodach zachodzi proces utleniania:
Fe Fe+2 + 2e
Na katodach zachodzi proces redukcji:
1/2 O2 + H2O + 2e = 2 OH -
2H+ + 2e = H2
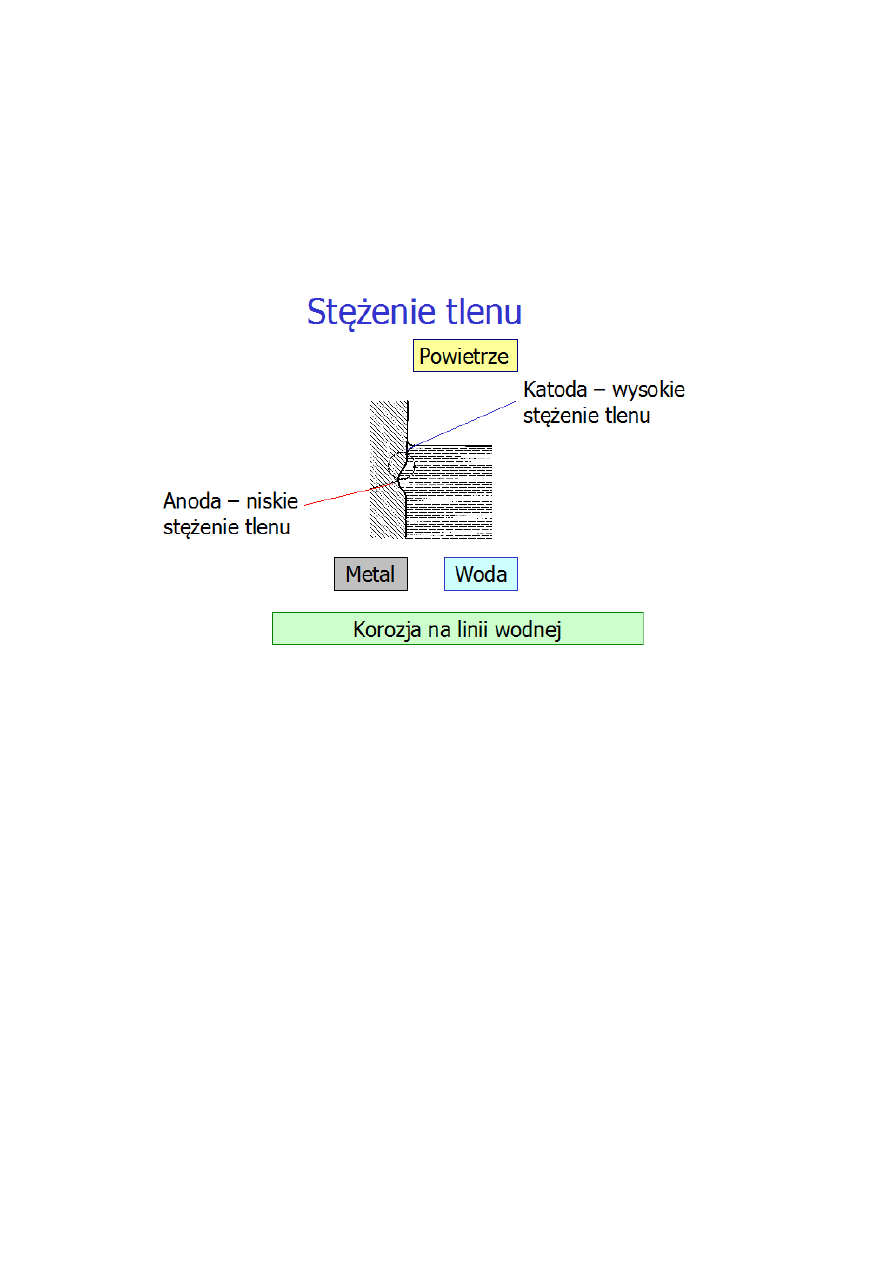
Rodzaje ogniw korozyjnych
Różne materiały
Różne stężenia
Różne napowietrzenie
Zróżnicowane naprężenia
Materiał skorodowany – materiał nieskorodowany
Zróżnicowane temperatury
Osiem postaci korozji
•
Korozja ogólna
•
Korozja galwaniczna
•
Korozja wżerowa
•
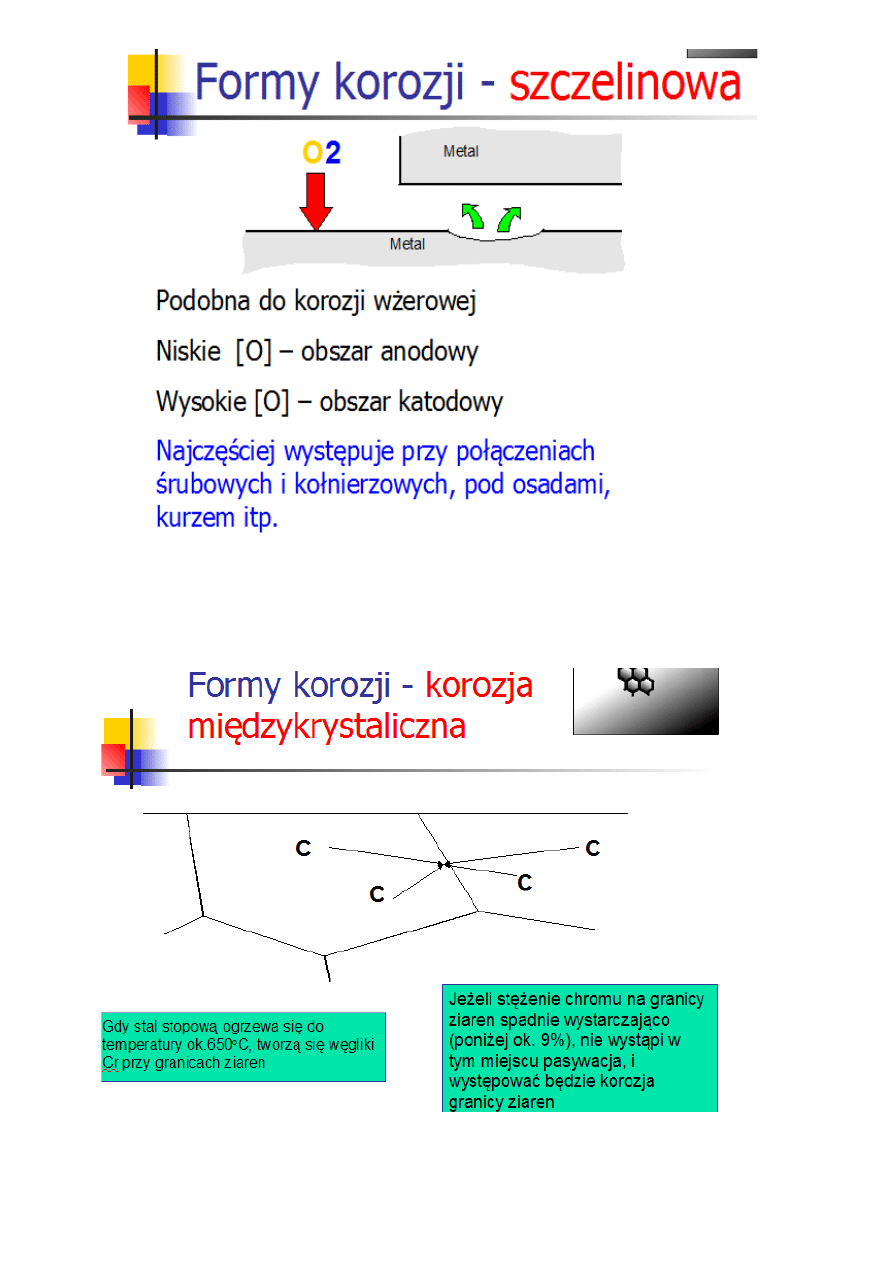
Korozja szczelinowa
•
Korozja międzykrystaliczna
•
Korozja selektywna
•
Erozja – korozja
•
Korozja naprężeniowa
Formy korozji - galwaniczna
Szereg napięciowy metaliUszeregowanie metali w zależności od wartości ich potencjałów
korozyjnych względem elektrody wodorowej (NEW)
Wskazuje na tendencję do korozji
Metale o potencjałach wyższych od NEW – metale szlachetne
Metale o potencjałach niższych od NEW – metale nieszlachetne
Korozja wżerowa
Korozja wżerowa jest jedną z postaci korozji lokalnej. Charakteryzuje się tym, że atak zlokalizowany
jest na niewielkich, dyskretnych miejscach na powierzchni metalu. Korozja wżerowa ma miejsce
głównie w obojętnych i kwaśnych roztworach zawierających chlorki lub inne halogenki. Miejscami
inicjacji korozji wżerowej mogą być wtrącenia niemetaliczne, mikroszczeliny powstające podczas
obróbki mechanicznej.
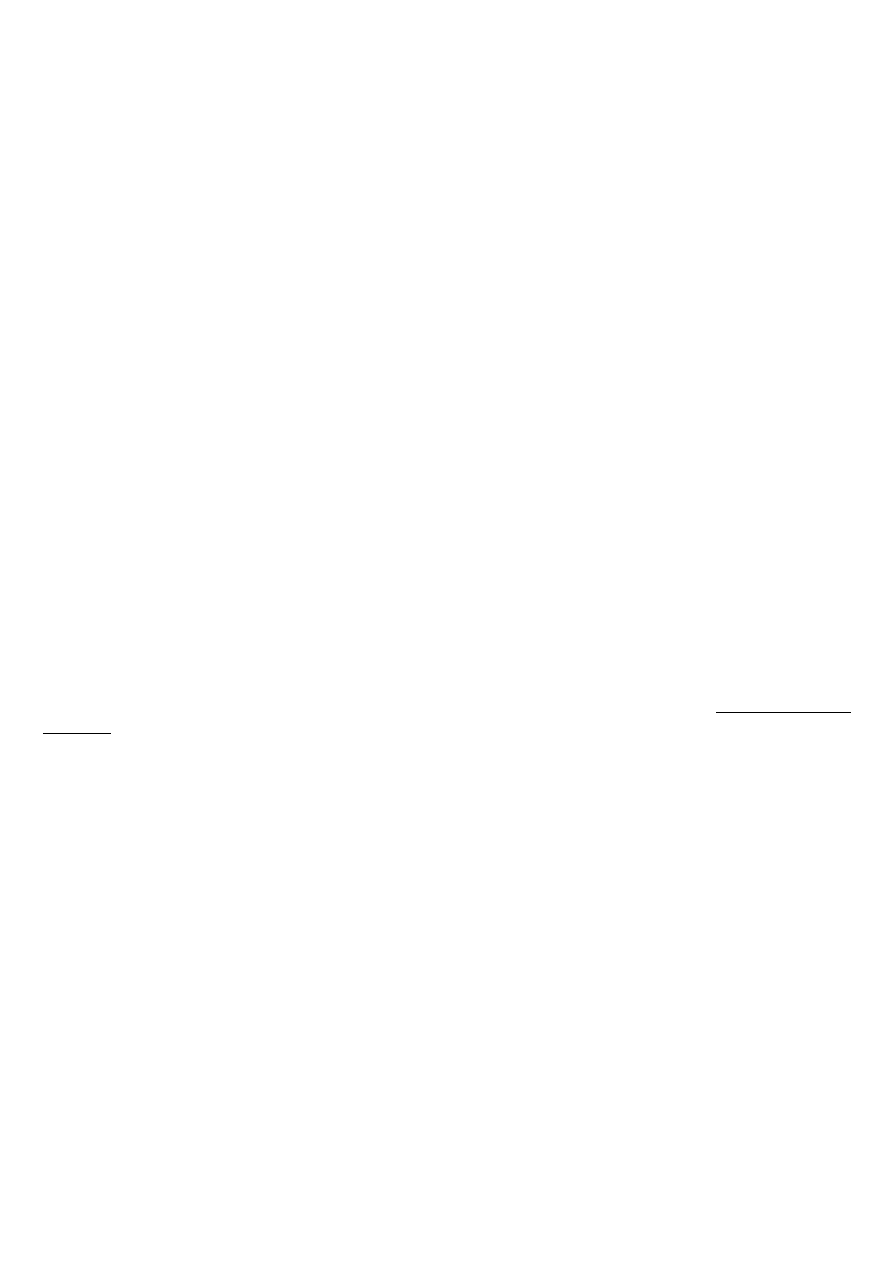
Używanie stali stopowych o niskiej zawartości węgla
Używanie stali stabilizowanych, zawierających pierwiastki łatwo tworzące węgliki (Nb lub Ti) w celu
związania węgla
Dla istniejących konstrukcji, które uległy uczuleniu obróbka cieplna w celu wyrównania stężenia
chromu w masie stali (proces trudny z punktu widzenia praktycznego)
Formy korozji - selektywna
Stopy zawierające jeden składnik bardziej szlachetny i drugi (stanowiący podstawowy składnik stopu)
bardziej aktywny (np. brąz, Cu + Zn)
Podstawowy składnik stopu może ulegać rozpuszczeniu pozostawiając matrycę ze stopu bardziej
szlachetnego
Odcynkowanie brązów(mosiądzów)
Grafityzacja żeliwa szarego
Powoduje utratę wytrzymałości mechanicznej bez oczywistej zmiany kształtu.
Formy korozji – erozja korozja
Przepływ może powodować:
Zwiększenie szybkości transportu tlenu do powierzchni metalu ( + pomaga pasywacji, - zwiększa
szybkość korozji)
Zwiększa szybkość rozpuszczania się warstw produktów korozji
Mechanicznie usuwa warstwy tlenkowe
Korozja naprężeniowa
Specyficzne współdziałanie środowiska korozyjnego i naprężeń (własnych lub zewnętrznych).
Cl-, OH- - stale stopowe;
amoniak – stopy miedzi;
Podstawowym celem ochrony przed korozją jest zmniejszenie szybkości korozji do akceptowalnego
poziomu
Znaczenie ochrony przed korozją
Straty do 3 tys. $ na mieszkańca
ok. 30% strat – brak wiedzy
Środki zainwestowane w badania i szkolenie są bardzo opłacalne
Ochrona ma duże znaczenie proekologiczne pozwala unikać skażeń i chroni instalacje ochrony
środowiska (IOS, oczyszczalnie)
Metody ochrony przed korozją
Ochrona powłokowa (uniwersalna, powszechna – 80% zabezpieczeń)
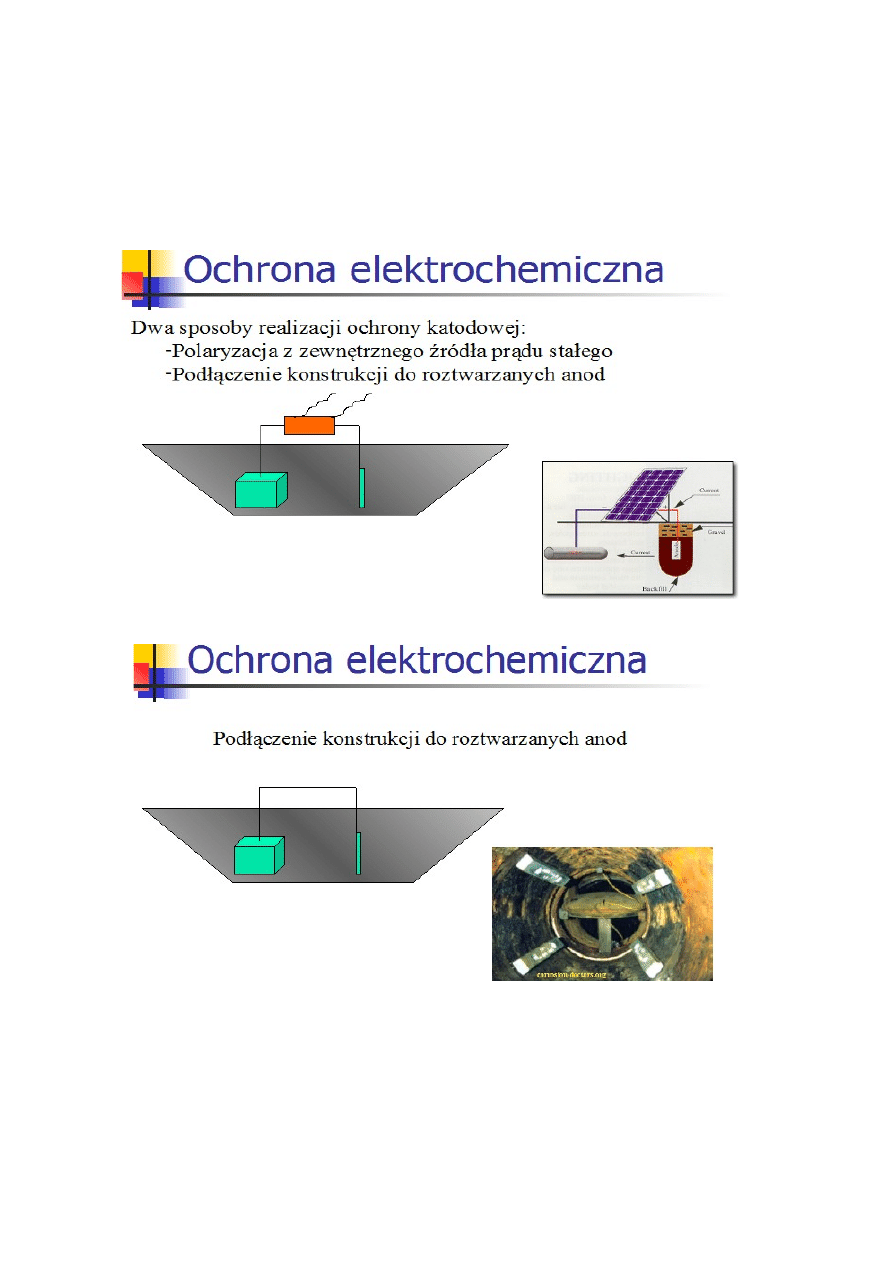
Ochrona elektrochemiczna (w zanurzeniu, zwykle uzupełnienie powłokowej)
Ochrona katodowa (protektory, zewnętrzne źródła prądu stałego,
Ochrona anodowa.
Modyfikacja środowiska (inhibitory, odtlenianie, klimatyzacja, osuszanie)
Dobór materiałów
Stopy metali
Kompozyty
Nanowarstwy
Odpowiednie projektowanie konstrukcji
Projekt konstrukcji powinien ułatwiać przygotowanie powierzchni, malowanie, nadzór i renowację.
Ochrona powłokowa
Zadaniem tego typu ochrony jest oddzielenie środowiska korozyjnego od materiału podlegającego
ochronie.
Modyfikacja środowiska
Ograniczanie wilgotności atmosfery
Zmniejszenie zawartości tlenu
Dodatek inhibitorów korozji
Korekcja pH (głównie alkalizacja)
Zmiana temperatury

Dodatek biocydów
Dobór materiałów
W literaturze dostępne są ogromne ilości danych dotyczących szybkości korozji większości metali o
znaczeniu technologicznym w różnych środowiskach korozyjnych.
Monitorowanie korozji
W celu kontroli procesów korozyjnych monitorujemy dwa główne parametry
Czynniki powodujące korozję – pH, chlorki, wilgotność, zanieczyszczenia atmosfery, itp.
Aktualne wartości parametrów związanych z procesem korozyjnym – czyli np. prąd korozyjny.
Pomiary korozyjne
Metody wyznaczania szybkości korozji
Metody wyznaczania szybkości korozji
Metody grawimetryczne - wagowe
Metody analityczne
Metody wolumetryczne
Metody elektrochemiczne
Metody grawimetryczne
Szybkość korozji jest bardzo często wyznaczana na podstawie zmiany masy wzorca wykonanego z
interesującego nas materiału w środowisku korozyjnym.
Pokazujemy w takim przypadku absolutną miarę zniszczeń materiału.
Warunkiem koniecznym miarodajności wyniku jest równomierność badanego zjawiska korozji.
Co z korozją lokalną ???
Grawimetryczne wyznaczanie szybkości korozji jest w tym przypadku błędem ponieważ nie
jesteśmy w stanie jednocześnie określić powierzchni na jakiej proces korozji ma miejsce.
Grawimetria znajduje zastosowanie w ocenie intensywności korozji lokalnej – ale o tym później .
Co z tymi zmianami masy ???
Wyznaczamy zazwyczaj ubytek masy próbki, której szybkość korozji chcemy poznać, ale możemy
również wyznaczyć przyrost jej masy.
Co wyznaczać łatwiej ???
Ubytek masy
Wystarczające jest usunięcie produktów korozji zbierających się na powierzchni badanej próbki.
Znając masę próbki przed wprowadzeniem do środowiska korozyjnego i po usunięciu produktów
korozji zabieramy się do obliczania
Ubytek masy a szybkość korozji
Ubytek masy czyli weight loss:
W = (mpocz – mkońc) * S
Szybkość korozji – czyli wprowadzamy czas – corrosion rate:
Vkor = W * t
A więc wyznaczamy Vkor
Zardzewiałą próbkę, której masę początkową powinniśmy znać musimy pozbawić produktów korozji
tak aby nie naruszyć zdrowego metalu.
Szlifowanie, polerowanie
A więc pozostaje znaleźć sposób aby rozpuścić tylko produkty korozji.
Rozpuszczamy produkty korozji

Metody chemiczne
20% NaOH + 200 g/dm3 Zn (5 min.)
roztwór wrzący
HCl (stęż.) + 50 g/dm3 SnCl2 + 20 g/dm3 SbCl3
temperatura otoczenia
Metody elektrochemiczne
A: Węgiel lub ołów
K: Próbka stalowa z produktami korozji
Roztwór: 50 g/dm3 H2SO4 + 2 cm3 inh.
Gęstość prądu: 20 A/cm2
Temperatura: 74°C
Czas oczyszczania: 3 minuty
Metoda wolumetryczna
Fe Fe2+ + 2e-
2H+ + 2e- H2
Fe + 2H+ Fe2+ + H2
Metody analityczne
Oznaczenie jonów korodującego metalu w środowisku, np. żelaza, chromu, niklu, miedzi,
aluminium.
Pomiary korozyjne
Inżynieria materiałowa
Potencjał
Potencjał punktu w przestrzeni jest definiowany jako praca przeniesienia jednostkowego ładunku
do tego punktu z nieskończoności.
Jednostką potencjału jest , V ( =J/C)
Pomiary potencjału
Potencjał elektrodowy
Potencjał elektrody definiuje się jako siłę elektromotoryczną ogniwa złożonego z danej elektrody i
odpowiedniej elektrody porównawczej.
Pomiary potencjału elektrodowego
Umowna standardowa elektroda odniesienia jest oparta na reakcji:
Standardowa elektroda wodorowa ( SEW )
2
2
2
H
e
H
+
−
+
=
Jony wodorowe w roztworze
o jednostkowej aktywności
Elektrony w metalu
Gazowy
wodór
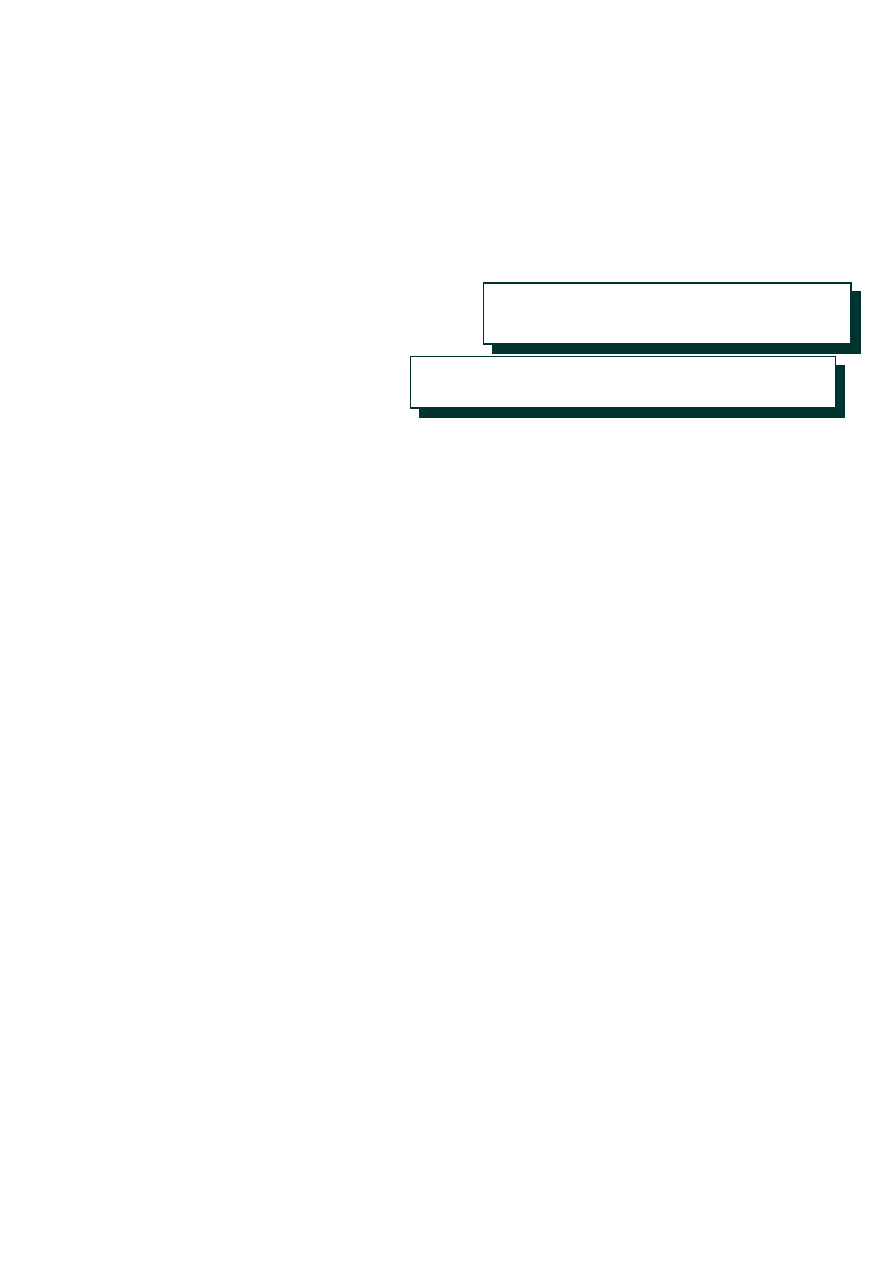
Wtórne elektrody odniesienia
Elektrody odniesienia pierwszego rodzaju – metal w równowadze z rozpuszczalna solą:
Cu <=> Cu
2+
+ 2e
-
Potencjał kontrolowany przez stężenie jonów Cu2+
Wtórne elektrody odniesienia
Elektrody odniesienia drugiego rodzaju , metal w równowadze z trudno rozpuszczalna solą i
roztworem zawierającym anion wchodzący w skład soli:
Electrod a Ag/AgCl
Potencjały popularnych elektrod odniesienia
Praktyczne pomiary potencjału
Pomiary potencjału Wymagania –Rezystancja wejściowa
Wysoka rezystancja wejściowa zmniejsza błędy związane z rezystancją układu mierzonego
W przypadku większości pomiarów korozyjnych wystarczająca jest wartość 107 , ale dla
układów o wysokich rezystancjach (farby, warstwy pasywne, itp.) 109 lub więcej jest
wymagane.
Pomiary potencjału Wymagania – – Odpowiedź częstotliwościowa
Odpowiedź częstotliwościowa ( zdolność do wykrywania niewielkich zmian Często mało istotna
przy pomiarach korozyjnych .
Pomiary przy 1 Hz są bardzo łatwe
Pomiary powyżej 1kHz są bardziej skomplikowane
Pomiary przy 50 Hz są trudne ( z powodu nakładania się częstotliwości źródła zasilania ).
Pomiary potencjału Wymagania - Rozdzielczość
Rozdzielczość jest to zdolność do wykrywania małych zmian potencjału przy pomiarach dużych
wartości.
Pomiary potencjału Wymagania - Rozdzielczość
Rozdzielczość jest to zdolność do wykrywania małych zmian potencjału przy pomiarach dużych
wartości.
dla większości pomiarów korozyjnych rozdzielczość 1 mV jest wystarczająca
Pomiary potencjału Wymagania - Rozdzielczość
Rozdzielczość jest to zdolność do wykrywania małych zmian potencjału przy pomiarach dużych
wartości.
dla większości pomiarów korozyjnych rozdzielczość 1 mV jest wystarczająca
w pomiarach szumu elektrochemicznego i badaniach pokrewnych może być konieczne
zastosowanie przyrządów o rozdzielczości 1V
Pomiary potencjału Wymagania - Czułość
Pomiary potencjału Wymagania - Precyzja
Rozdzielczość jest zdolnością do detekcji małych zmian potencjału przy pomiarach dużych wartości
Czułość jest to zdolność do pomiaru małych wartości
Ag
Ag
e
AgCl
Ag
Cl
⇔
+
⇔
+
+
−
+
−
Stężenie jonówAg
+
utrzymuje potencjał
równowagowy
Stężenie jonów chlorkowych reguluje stężenie jonów Ag
+
[Ag
+
][Cl
-
] = const

Precyzja lub dokładność jest zdolnością do uzyskiwania ‘ prawdziwych ’ wartości
Metody pomiaru potencjału
Miernik analogowy ( magnetoelektryczny )
Niska impedancja (typically 20 k /V)
Słaba odpowiedź częstotliwościowa (~1 Hz)
Niska czułość (~1 mV)
Niska rozdzielczość (~1%)
Słaba precyzja (~3%)
Metody pomiaru potencjału
Miernik analogowy (e lektroniczny )
Wysoka impedancja ( zwykle 10 M )
Słaba odpowiedź częstotliwościowa (~1 Hz)
Możliwa wysoka czułość (~1 V)
Niska rozdzielczość (~1%)
Słaba precyzja (~3%)
Metody pomiaru potencjału
Miernik cyfrowy
Wysoka impedancja ( zwykle od 10 M )
Słaba odpowiedź częstotliwościowa ( ok. 3 Hz)
Wysoka czułość (10 V d o 100 nV)
Wysoka rozdzielczość (0.1% d o 0.0001%)
Wysoka precyzja (0.1% d o 0.0001%)
Metody pomiaru potencjału
Electrometr ( cyfrowy )
Bardzo wysoka impedancja (~1014 )
Słaba odpowiedź częstotliwościowa (<1 Hz)
Wysoka czułość (1 V d o 100 nV)
Wysoka rozdzielczość (0.1% d o 0.001%)
Wysoka precyzja (0.1% d o 0.001%)
Metody pomiaru potencjału
Rejestratory
Impedancja zależna od typu urządzenia ( od 103 do 107 )
Średnia odpowiedź częstotliwościowa (~10 Hz)
Średnia czułość (~10 V)
Średnia rozdzielczość (~0.1%)
Średnia precyzja (~0.1%)
Metody pomiaru potencjału
Oscyloskop
Wysoka impedancja (106 to 107 )
Wysoka odpowiedź częstotliwościowa ( od 10 MHz)
Średnia czułość (~100 V)
Słaba rozdzielczość (~1%)
Słaba precyzja (~1%)
Metody pomiaru potencjału
Komputerowy zapis danych
Wysoka impedancja (~107 )
Zmienna odpowiedź częstotliwościowa (10 Hz d o 1 MHz lub więcej )
moderate to good sensitivity (~10 V)
moderate to good resolution (0.5 d o 0.01%)
moderate to good precision (0.5 d o 0.01%)
facilitates subsequent plotting and analysis
Szereg napięciowy metali
Wykresy Pourbaix
Wykresu P. podają informacje o możliwości istnienia w stanie równowagi metalu, jego jonów lub
związków.
Dane do sporządzania wykresów są uzyskiwane poprzez obliczenia na podstawie wartości funkcji
termodynamicznych
Rozpatrywany jest układ metal-woda w warunkach standardowych
Diagram Pourbaix
Linia czerwona: 2H2O = O2 + 4H+ + 4e-
E = 1.229 – 0.059 pH
Linia niebieska: 2H+ + 2e- = H2
E = 0.00 – 0.059 pH
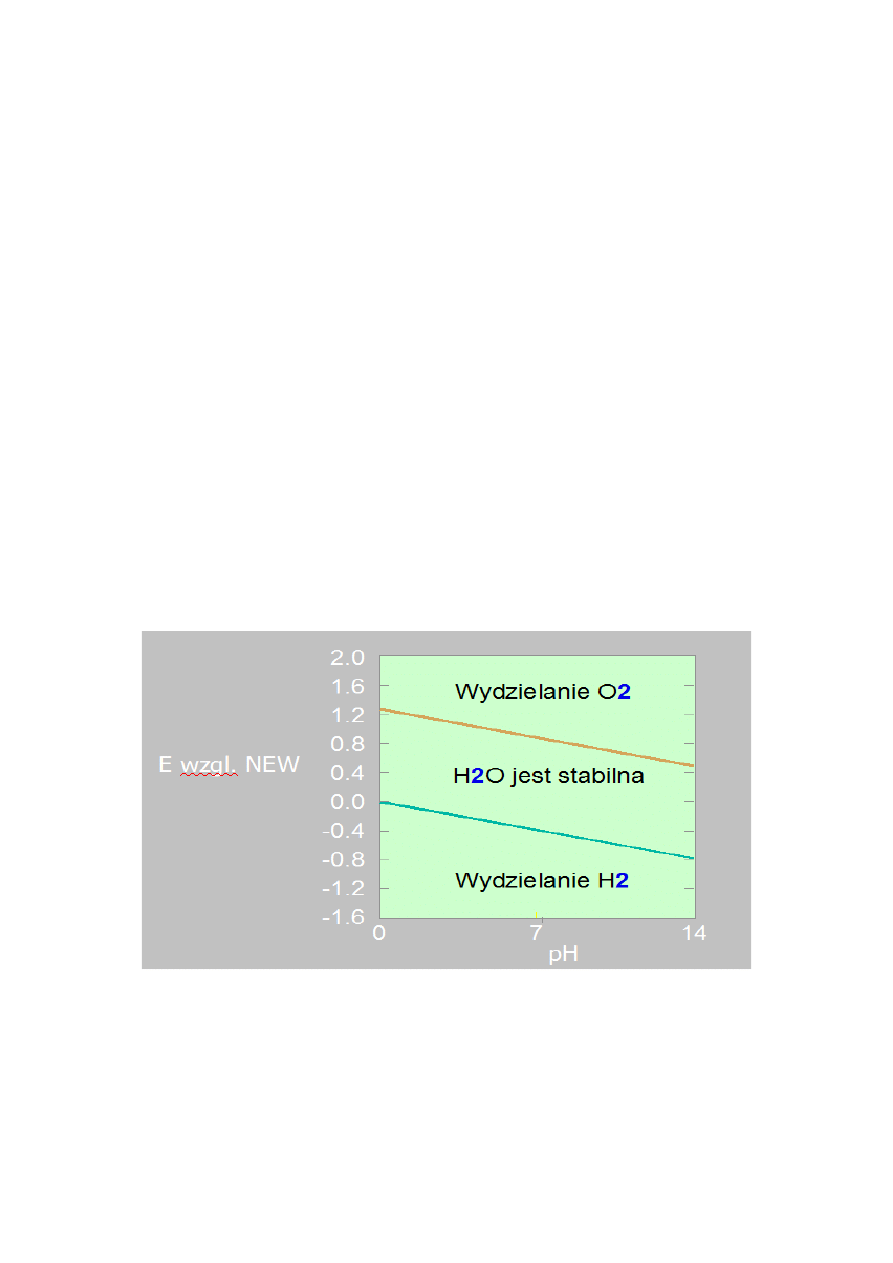
Diagram Pourbaix dla żelaza
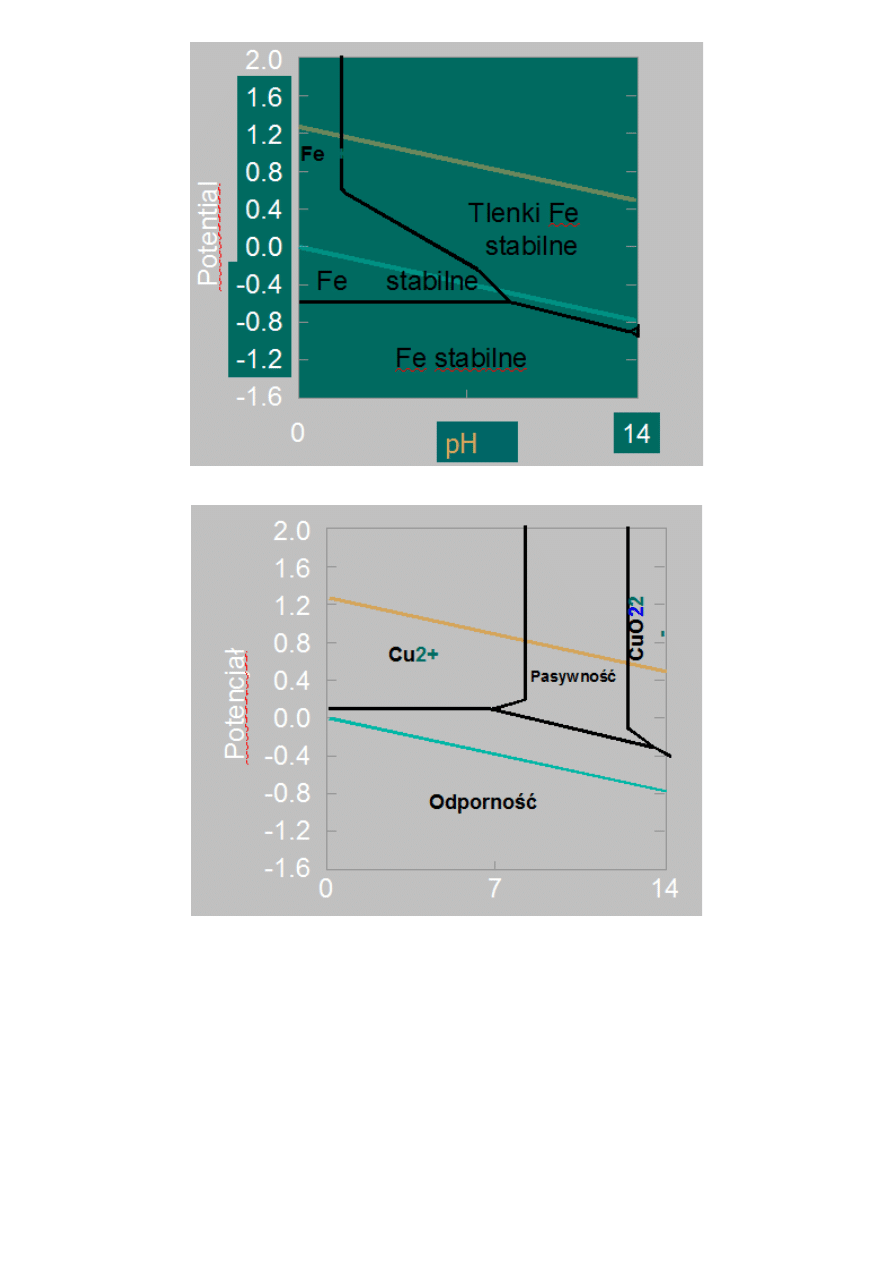
Diagram Pourbaix dla Cu
Diagram Pourbaix dla Zn
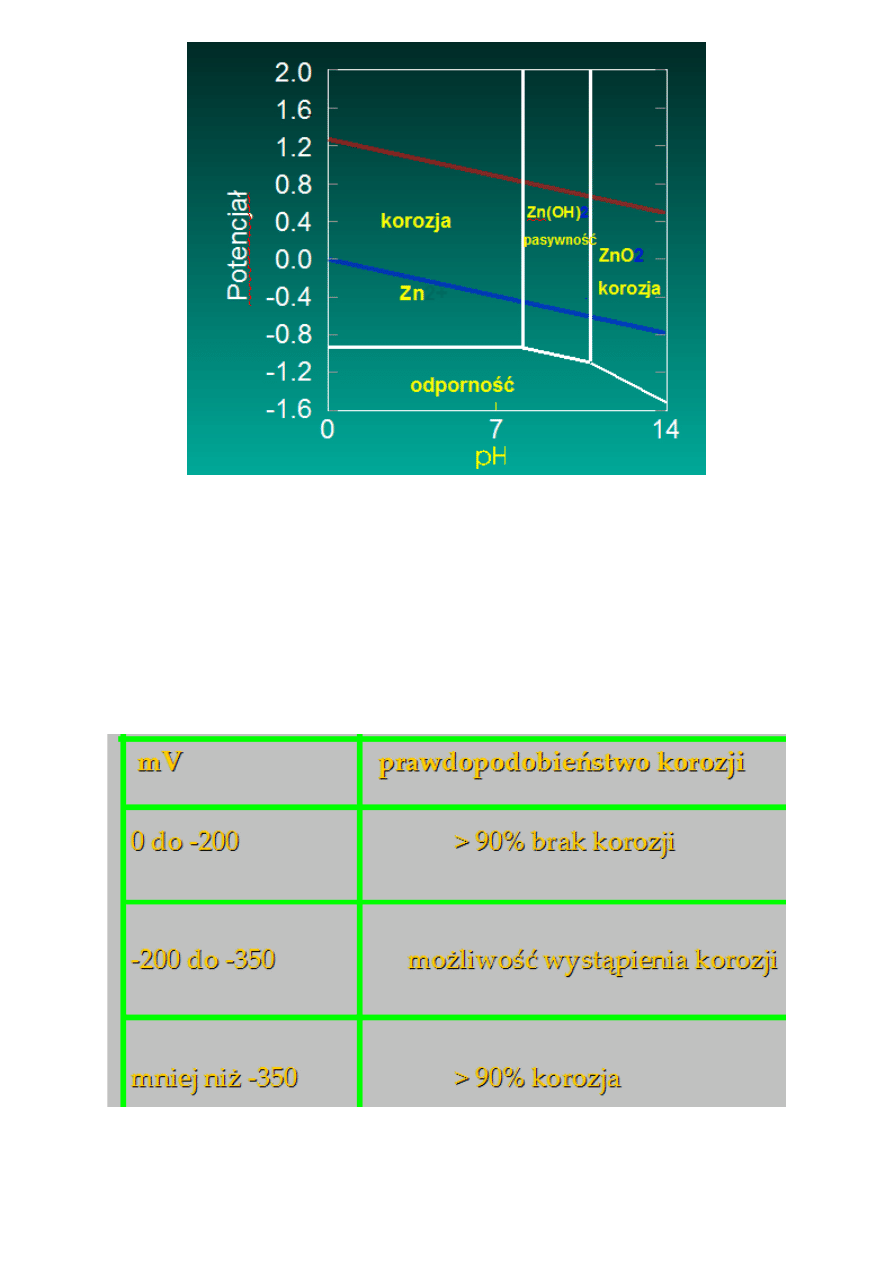
Metale odporne termodynamicznie, np.: Ag, Au, Pt
Metale nieodporne termodynamicznie i znajdujące się w stanie pasywnym, np.: Cr, Al., Ti
Metale nieodporne termodynamicznie i znajdujące się w stanie aktywnym, np.: Fe, Zn, Cd.
Pomiary potencjału w korozji
Wartości potencjału korozyjnego
Określanie możliwości zajścia procesu korozji na podstawie pomiaru potencjału wzgl. elektrody
siarczano-miedziowej

Badania powłok
Aby badanie mogło być uznane za wiarygodne, sposób jego przeprowadzenia oraz
zastosowane przyrządy powinny znajdować oparcie we właściwej normie (ISO, PN, DIN,
ASTM, BS). Wybór odpowiedniej normy powinien być uzgodniony z wykonawcą i
inwestorem przed rozpoczęciem prac.
Wybrana do prowadzenia badań norma powinna w jednoznaczny sposób podawać:
Warunki i sposób prowadzenia badania;
Rodzaje przyrządów i zasadę ich działania;
Sposoby interpretacji wyników.
Do najczęściej badanych parametrów powłok należą:
Grubość warstwy mokrej;
Grubość warstwy suchej;
Twardość;
Szczelność;
Przyczepność.
Pomiary warunków klimatycznych
Warunki klimatyczne panujące w strefie prowadzenia zabezpieczeń powłokowych
determinują możliwość wykonywania prac. Podczas nakładania powłoki ochronnej
obecność wilgotności na zabezpieczanej powierzchni lub w najbliższym otoczeniu, jest
przyczyną złych wyników prac.
Metody pomiaru grubości i twardości wykładzin
Badania grubości powłok można podzielić na:
Metody badania powłok mokrych;
Metody badania powłok suchych.
Pomiar grubości powłoki mokrej
Pomiar przybliżony,
Stosowany w celu sprawdzenia grubości w procesie aplikacji
Badanie grubości powłok mokrych
TS - grubość warstwy suchej, m
Tm - grubość warstwy mokrej, m
×
×
−
=
r
w
m
S
d
d
p
T
T
100
1

p - zawartość części lotnych w wyrobie, %
dw - gęstość wyrobu, g/cm3
dr - gęstość rozpuszczalnika
Pomiar grubości powłoki suchej
Można przeprowadzić różnymi sposobami;
Wybór zależy od wymaganej dokładności pomiaru;
Metody pomiaru powłok suchych
za pomocą mierników mechanicznych;
za pomocą mierników elektronicznych;
za pomocą mierników ultradźwiękowych;
za pomocą mierników ingerencyjnych;
Pomiar za pomocą mierników mechanicznych
Stosowany do podłoży stalowych;
Grubość powłoki wywiera wpływ na zmianę przyciągania magnetycznego;
Wartość odczytuje się jako miejsce zatrzymania wskazówki, po oderwaniu stałego magnesu od
powłoki.
Szeroki zakres pomiarowy;
Duży błąd pomiaru oraz brak możliwości kalibracji.
Pomiar za pomocą mierników elektronicznych – podłoża ferromagnetyczne
Działają na zasadzie indukcji magnetycznej
Ocena grubości powłok niemagnetycznych na podłożach magnetycznych (lakiery, farby, tworzywa
sztuczne, emalie, gumy, ceramika, powłoki galwaniczne)
Kształt próbek dowolny,
Szeroki zakres pomiarowy.
Pomiar za pomocą mierników elektronicznych – podłoża nieferromagnetyczne
Działają na zasadzie prądów wirowych,
Ocena grubości powłok niemagnetycznych na podłożach niemagnetycznych (lakiery, farby,
tworzywa sztuczne, emalie, gumy, ceramika, powłoki galwaniczne)
Kształt próbek dowolny,
Szeroki zakres pomiarowy.
Zalety mierników elektronicznych
Pomiar powłoki;
Przechowywanie danych;
Ocena statystyczna;
Prowadzenie dokumentacji pomiarowej (wydruki, historiogramy)
Pomiar za pomocą mierników ultradźwiękowych
Nieniszczący pomiar grubości powłok z farb, lakierów, plastików i innych pokryć izolacyjnych.
Możliwość oceny grubości całkowitej powłoki wielowarstwowej, jak i grubości poszczególnych

warstw.
Współpraca z komputerami i drukarkami wyników.
Pomiar za pomocą mierników ingerencyjnych
Praktyczne zastosowanie ma metoda nacięć klinowych;
Grubości powłok na metalu, drewnie, plastikach;
Można wyznaczyć grubość całkowita powłoki jak i poszczególnych warstw.
Zasada pomiaru
Przyrządem tnącym wykonać nacięcia powłoki pod kątem ostrym do podłoża.
Ocena wyników badań
Pomiar twardości powłoki
Metody wahadłowe – tylko w laboratorium;
Metody ołówkowe;
Metoda badania śladu odcisku;

Metoda zadrapań;
Metody ołówkowe
Ołówki (od 6B do 9H) – w laboratorium
Urządzenia pozwalające uzyskać stały i niezmienny nacisk na powłokę - teren
Badanie twardości powłok. Informacje ogólne.
Norma DIN 55 945 definiuje twardość, jako: „odporność powłoki na mechaniczne oddziaływania
takie jak nacisk, zadrapanie lub zarysowanie”.
PN-79 / C-81530 - Oznaczanie twardości powłok
Norma została wprowadzona zamiast normy PN-73/C-81530.
Wprowadzono nową metodę oznaczania twardości powłok lakierowych za pomocą aparatu
Buchholza.
Możliwość badań w laboratorium jak i w warunkach produkcyjnych.
Przedmiot normy
Przedmiotem normy są metody oznaczania twardości powłok lakierowych
Rodzaje metod
A - oznaczanie względnej twardości powłok wahadłem Persoza i wahadłem Königa
B - oznaczanie twardości powłok przyrządem Buchholza
Twardość powłoki wg metody A - twardość określana czasem wyrażonym w sekundach, w którym
następuje zanikanie wahań wahadła opartego na powłoce.
Wartości względne odnoszone do czasu zanikania wahań wahadła opartego na płytce szklanej
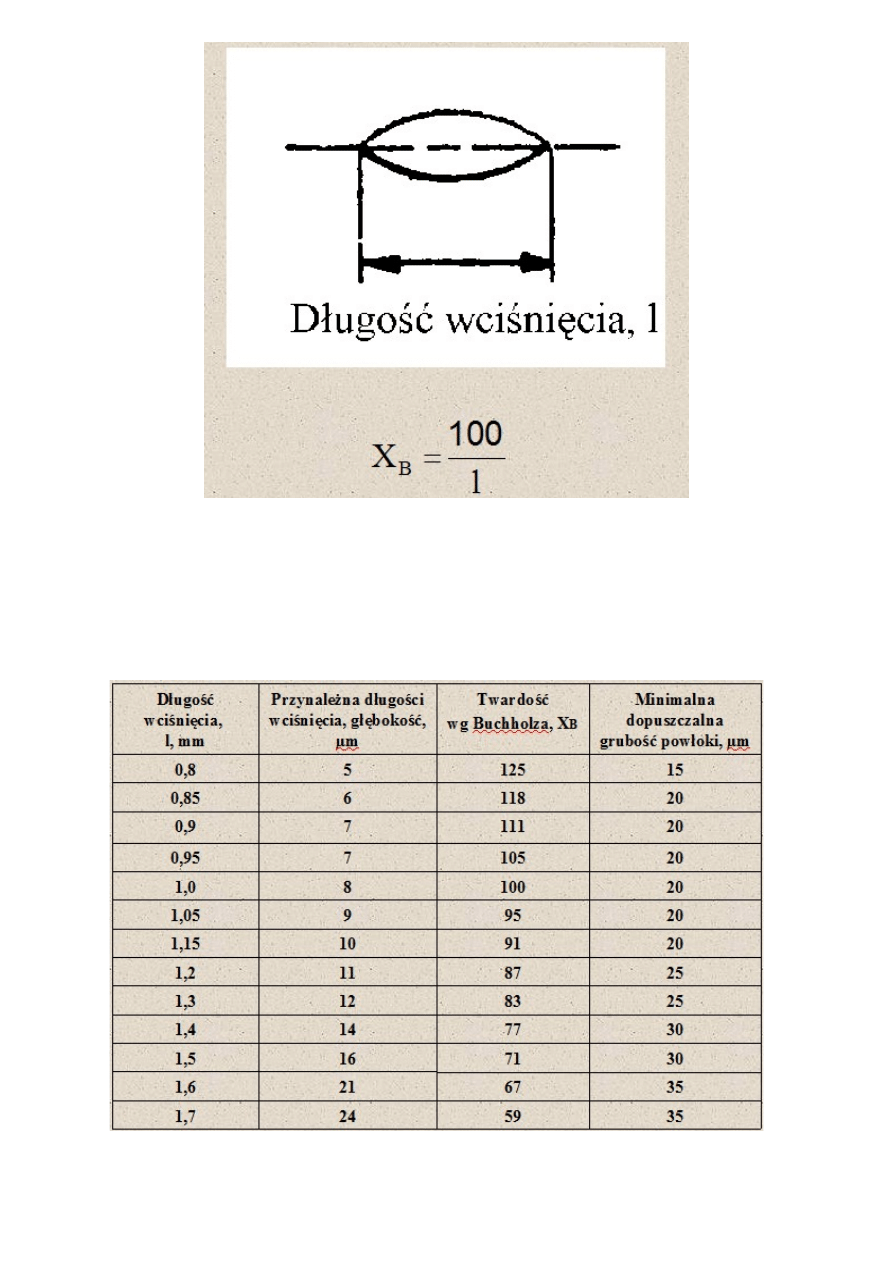
Twardość powłoki wg metody B - twardość określona odwrotnością długości wciśnięcia
pozostawionego na powłoce przez element wciskający. .
Wahadło Köeniga - metoda laboratoryjna
Twardość względna > 0,5
Kulki ze stali stopowejtwardość HRC 63 ± 3, d = 5 ± 0.05 mm
Okres wahań 1,4 ± 0,02s
Stała szklana 250 ± 10 s
Masa 200 ± 0,2g
Wahadło Persoza - metoda laboratoryjna
Twardość względna < 0,5
Kulki ze stali stopowejtwardość HRC 59 ± 1, d = 8 ± 0.05 mm
Okres wahań 1,0 ± 0,01s
Stała szklana 420 s
Masa 500 ± 0,1g

Warunki prowadzenia oznaczeń
Płytki do badań powinny być gładkie i równe.
Powłoka na płytkach powinna być gładka, wolna od nierówności, np.wtrąceń pigmentów,
kurzu, zacieków itp.
Grubość powłoki powinna wynosić 30 ±5 m
Badania twardości powłok należy przeprowadzić w temperaturze 20 ± 2°C i przy wilgotności
względnej 65 ± 5%.
Dodatkowe wyposażenie
Statyw
Skala umożliwiająca odczytanie zmiany kąta wychylenia w granicach 6 do 3 ° w przypadku
wahadła Koniga oraz 12 do 4° w przypadku wahadła Persoza.
Licznik do zliczania wychyleń wahadła
Płytka szklana do wyznaczenia stałej szklanej.
Obliczanie wyniku oznaczenia
Twardość względną powłoki (X) oblicza się ze wzoru:
X = a/b
gdzie:
a - czas zanikania wahań wahadła na powłoce badanej, s
b- stała szklana, s
Badanie twardości powłok lakierowych
Aparat Buchholz’a
Zasada pomiaru polega na badaniu zagłębienia narzędzia w materiał. Długość śladu pozosta-
wionego przez ciężarek o określonych normą kształcie i wadze.
Parametry przyrządu
Częścią zasadniczą przyrządu jest element wciskający w kształcie podwójnego stożka
ściętego.
Twardość elementu wciskającego – co najmniej 61 HRC
Materiał – stal nierdzewna
Siła działająca na powłokę – 4,90 ± 0,05 N
Wyposażenie dodatkowe
Lupa o powiększeniu 20-krotnym z podziałką o działce elementarnej 0,1 mm wyposażona we
własne źródło światła (kąt padania 60°).
Sekundomierz.

Wynik końcowy oznaczenia
Za wynik należy przyjąć średnią arytmetyczną co najmniej trzech oznaczeń,
których wyniki nie różnią się więcej od wyniku średniego niż 5%
Raport z badań powinien zawierać
Odniesienie do odpowiedniej normy;
Rodzaj i symbol handlowy badanego wyrobu;
Technologię przygotowania powłoki;
Rodzaj podłoża;
Wynik testu jako twardość powłoki wg Buchholtza, XB;
Datę wykonania badania.
Badanie twardości powłok lakierowych
Metoda ołówkowa (BN-78 / 6111-03)
Metodą stosuje się do badania powłok i pokryć lakierowych z wyjątkiem powłok
matowych oraz powłok z wyrobów zawierających pigment w postaci łusek.
Twardość powłoki oznaczana metoda ołówkową jest własnością charakteryzującą odporność
powłoki lakierowej na wtłaczanie ostrza określonego ołówka powierzchnię powłoki.
Zasada metody
Polega na rysowaniu badanej powłoki ołówkiem o stopniowanej twardości i
wybraniu ze zbioru ołówków dwóch kolejno po sobie następujących, z których
bardziej miękki daje ślad grafitu a twardszy pozostawia na powłoce widoczne
wgłębienie.
Przyrządy i materiały
Zestaw ołówków składający się z 17 ołówków o następujących twardościach:
6B, 5B, 4B, 3B, 2B, B, HB, F, H, 2H, 3H, 3H, 4H, 5H, 6H, 7H, 8H, 9H
Waga uchylna o maksymalnym obciążeniu 2kg
Papier ścierny o ziarnistości 400
Wykonanie oznaczenia

Płytkę umieszcza się na szalce wagi;
Przesuwać ołówek po powierzchni powłoki na odcinku ok. 10 cm (przez 1 s) w kierunku do siebie;
Obciążenie wagi powinno wynosić podczas przesuwania 750 g;
Badanie rozpoczynać od ołówków miękkich
Interpretacja wyników
Twardość ołówkową powłoki określa się przez podanie numerów dwóch kolejno po sobie
następujących ołówków zestawu.
Na przykład zapis 2H-3H oznacza, że ołówek 2H pozostawia ślad grafitu na powłoce, podczas
gdy 3H wgłębia się w nią.
Wynik oznaczenia
Badania należy przeprowadzić na co najmniej 3 próbkach, z których 2 powinny wykazywać te
sama twardość ołówkową.
Protokół z badań powinien zawierać:
nazwę i symbol handlowy wyrobu technologie przygotowania powłoki rodzaj podłoża
wynik badania datę wykonania oznaczenia
SZYBKOŚĆ KOROZJI PRZYKŁADOWE ZADANIA
ZAD1
Pręt stalowy o przekroju kwadratowym ( bok - 4 mm) i długości 10 cm wrzucono do roztworu kwasu
chlorowodorowego (solnego). Po dwóch godzinach, okazało się, że w wyniku reakcji korozyjnej
wydzieliło się 0.0448 dm3 gazu. Obliczyć szybkość korozji pręta stalowego w badanym środowisku,
dFe = 7800 kg/m3. Przyjmując zasadę, że szybkość korozji poniżej 0,135 mm/rok kwalifikuje materiał
do zastosowania w danych warunkach pracy wskazać, czy badana stal jest w środowisku kwasu
siarkowego materiałem odpornym ??
ZAD2
Blaszkę o masie 12,4569 g dokładnie wyszlifowano i odtłuszczono. Po ponownym zważeniu jej masa
wynosiła 12,1009 g. Tak przygotowany wzorzec eksponowano przez 60 dni w solance o pH = 5. Po
tym czasie próbkę wytrawiono w kwasie solnym z dodatkiem inhibitora korozji. Masa próbki po
wypłukaniu i wysuszeniu wynosiła 10,6009 g. Wyznaczyć szybkość korozji stali w mm/rok. Wymiary
próbki – 20
×
50 mm. DFe = 7500 kg/m3. Przyjmując zasadę, że szybkość korozji poniżej 0,135
mm/rok kwalifikuje materiał do zastosowania w danych warunkach pracy wskazać , czy badana stal
jest w środowisku solanki materiałem odpornym.
Wyszukiwarka
Podobne podstrony:
Pomiary korozyjne 5
ściąga pomiary 3, semestr 5, pomiary korozyjne
Pomiary korozyjne 1
Pomiary korozyjne 4 pomiar potencjalu
Pomiary korozyjne 2
download Zarządzanie Produkcja Archiwum w 09 pomiar pracy [ www potrzebujegotowki pl ]
2 1 Podstawowe czynności pomiarowe w geodezji
BYT 2005 Pomiar funkcjonalnosci oprogramowania
6 PKB 2 Pomiar aktywności gospodarczej rozwin wersja
Praktyczna interpretacja pomiarów cisnienia
wyklad 13nowy Wyznaczanie wielkości fizykochemicznych z pomiarów SEM
13a Pomiary jakosci
NIEPEWNOŚĆ POMIARU
Strategia pomiarów środowiska pracy
PEM (10) Nieoewność pomiaru
2 8 Błedy pomiarów
Pomiar odpylaczy kotłowych
więcej podobnych podstron