
SPEKTROSKOPIA
Spektroskopia
to dziedzina nauki, która obejmuje
metody badania materii przy użyciu
promieniowania
elektromagnetycznego
, które może być w danym układzie
wytworzone (emisja) lub może z tym układem oddziaływać
(adsorbcja).
Definicje wybranych terminów:
Zakres nadfioletu
, UV (ang. Ultraviolet) –zakres widma
elektromagnetycznego od 10 do 380nm, zwykle 200-380nm.
Zakres widzialny
, VIS (ang. Visible) –zakres widma
elektromagnetycznego widzialny dla oka 380 do 780nm.
Absorpcja
–przekształcenie energii promienistej w inne
formy energii wskutek oddziaływania z materią.
Przepuszczanie
–przejście promieniowania przez dane
środowisko bez zmiany częstości monochromatycznych
składowych promieniowania.
Wiązka promieniowania
–promieniowanie rozchodzące się
w przestrzeni w określonym kącie bryłowym.
Promieniowanie
monochromatyczne
–wiązka
promieniowania widma elektromagnetycznego o jednakowych
kwantach energii.
Natężenie, I
0
–natężenie promieniowania padajacego.
Natężenie, I
S
–natężenie wiązki pomiarowej, po przejściu
przez kuwetę zawierającą próbkę badaną.
Natężenie, I
r
–natężenie wiązki odniesienia, po przejściu
przez roztwór odniesienia (ślepą próbę).
Kuweta
–naczyńko optyczne stosowane do pomiarów.

Ślepa próba
–roztwór przygotowany w ten sposób aby
kompensował absorbancję pochodzącą od odczynników lub
też składników próbki różnych od oznaczanego.
Tło
–absorbcja wszystkich nieznanych, lub znanych ale nie
oznaczanych, składników próbki.
Grubość warstwy absorbującej, b
–w przypadku cieczy i
gazów odległość między wewnętrznymi powierzchniami ścian
naczyńka zawierającego ośrodek absorbujacy.
Transmitancja,
T
–stosunek
natężenia
wiązki
promieniowania przepuszczanego przez próbkę do natężenia
wiązki padającej T = I/I
0
w praktyce T = I
S
/I
r
.
Absorbancja
A
–logarytm
dziesiętny
odwrotności
transmitancji; A = log(1/T).
Współczynnik absorbcji właściwej, a
S
–stosunek absorbancji
(A) do grubości warstwy absorbującej (b) i stężenia substancji
absorbującej (c); a
S
= A/bc; b [cm], c [gdm
-3
].
Współczynnik absorbcji molowy,
ε
–wsp. dla którego
stężenie substancji absorbującej (c) jest wyrażone [mol
⋅
dm
-3
].
Widmo
–uporządkowana
zależność
między
moca
promieniowania absorbowanego lub emitowanego i jego
liczbą falową, długością promieniowania bądź częstością.
Widmo absorbcji
–widmo, które powstaje w wyniku
przejścia promieniowania przez ośrodek absorbujący.
Krzywa wzorcowa
–wykres zależności pomiędzy mierzona
wielkością (absorbcją, transmitancją) a stężeniem oznaczanej
substancji.

SPEKTROMETRIA
Spektrometria
zajmuje się rejestracją i pomiarami
efektów wytwarzania bądź oddziaływania promieniowania
elektromagnetycznego z badaną materią.
Za podstawę podziału spektroskopii przyjmuje się
następujące trzy kryteria:
1.forma wymiany energii miedzy promieniowaniem i
materią,
• zwiększenie energii układu w wyniku pochłaniania
promieniowania -
spektroskopia absorpcyjna
• oddanie części energii przez układ drogą emisji
promieniowania -
spektroskopia emisyjna
2. właściwości składników materii, dotyczą istoty badanych
przemian zachodzących w składnikach materii,
•
spektroskopię jądrową,
•
spektroskopię atomową,
•
spektroskopię cząsteczkową,
3. podstawę podziału wg. zakresu promieniowania stanowi
wielkość fotonu, który jest pochłaniany lub emitowany, a
tym samym obszar w którym jest zawarte badane widmo:
•
spektroskopię rentgenowską
,
•
spektroskopię optyczną,
•
radiospektroskopię: mikro, krótko i długofalową,

PRAWA ABSORPCJI
Prawo Lamberta-Beera:
Dla równoległej ściśle monochromatycznej wiązki
promieniowania elektromagnetycznego, w przypadku
nieabsorbującego
rozpuszczalnika,
kiedy
brak
jest
jakichkolwiek
oddziaływań
między
cząsteczkami
substancji absorbujacej czy też między cząsteczkami tej
substancji i rozpuszczalnika:
absorbancja
A
jest proporcjonalna do stężenia roztworu
c
i grubości warstwy absorbującej
b
m
bc
abc
I
I
A
ε
=
=
=
0
log
Prawo addytywności absorbancji
dotyczy roztworów i
mieszanin wieloskładnikowych. Wyraża ono absorbancje
całkowitą środowiska, A, jako sume niezależnych absorbancji
poszczególnych składników (A
1
, A
2
, .....A
n
)
∑
=
=
+
+
+
=
n
i
i
n
A
A
A
A
A
1
2
1
....
Odstępstwa od praw absorpcji:
1.
związane z próbką
, zależą od charakteru środowiska;
• zmiana współczynnika załamania promieniowania,
• zbyt wysokie stężenie (oddziaływanie składników
roztworu; hydroliza, solwatacja, polimeryzacja),
• nakładanie się przekrojów czynnych cząstek
2.
instrumentalne
;
• brak monochromatyzacji wiązki promieniowania,
• niska klasa przyrządu

APARATURA SPEKTROFOTOMETRYCZNA NA
ZAKRES UV/VIS
Spektrofotometr
jest przyrządem pomiarowym, którego
zasadniczym przeznaczeniem jest pomiar transmitancji i/lub
absorbancji ciał stałych, ciekłych i gazowych.
Do
najważniejszych
części
składowych
spektrofotometrów należą:
1.
źródło promieniowania
–powinno się charakteryzować
ciągłym widmem emisji, o równomiernym rozkładzie
energetycznym
w
całym
zakresie
stosowania
i
odpowiednio dużej mocy,
2.
monochromator
–jego zadaniem jest rozszczepienie
promieniowania
polichromatycznego,
emitowanego
przez
źródło
promieniowania,
i
wyodrębnienie
z
otrzymanego
widma
fragmentu
zawierającego
promieniowanie o żądanej długości fali
λ
,
3.
komora próbki -
z kuwetami pomiarowymi w których
umieszcza się próbki ciekle i gazowe, stanowią w
procesie pomiarowym integralna część spektrofotometru,
4.
detektor promieniowania
–pełnią funkcję
przetwarzania
energii promienistej na energię elektryczną, powinny
wykazywać wysoką czułość, niski poziom szumów i
liniowość przetwarzania sygnałów,
5.
układ pomiarowy
–wychyleniowe i kompensacyjne
Typy metod spektrofotometrycznych:
1. metoda krzywej wzorcowej,
2. metoda dodatku wzorca,
3. metoda porównania z wzorcem,
4. metoda spektrofotometrii różnicowej

Zalety metod spektrofotometrycznych:
1.
dostępna, prosta w obsłudze i stosunkowo tania
aparatura,
2. wysoka czułość pomiaru,
3.
duża
dokładność
[1-5%]
[0.2-0.5%
dla
metod
różnicowych] i precyzja pomiaru dla stężeń >10
-4
%
[<10%] dla śladów >10
-7
[<30%] ,
4.uniwersalność, absorbancja powinna się mieścić w
zakresie od 0.1 do 1.0
Układy barwne stosowane spektroskopii UV/VIS
Zabarwienie substancji pochodzi stąd, że z całego
zakresu długości fal światła białego tylko pewna część jest
pochłaniana przez substancję i światło wychodzące ma barwę
dopełniającą.
Pochłanianie światła jest uwarunkowane przejściami
elektronów walencyjnych z poziomu podstawowego na
poziom wzbudzony w pewnych grupach funkcyjnych w
molekule –stąd nazwa widma elektronowe.
Większość układów barwnych powstaje w wyniku
reakcji tworzenia się kompleksów zarówno z odczynnikami
nieorganicznymi jak i organicznymi:
1.
Rodanki
[NH
4
SCN, KSCN lub NaSCN] tworzą barwne
kompleksy z Fe, Co, Ni, Cu, Ti, V, W. Rozpuszczalne w
wodzie i rozpuszczalnikach organicznych.
2.
Nadtlenek wodoru
z Ti, V, Mo, W;
chlorki, bromki
i
jodki
z Bi Sb, Pd, Fe, Cu, Ag;
molibdenian
z Si, As, P.
3.
Własne zabarwienie:
Cu
2+
, MnO
4
-
, Cr
2
O
7-
4.
Odczynniki organiczne jak np.:
Ditizon [
Pb, Zn, Cd,
Bi, Ag ,Cu
], barwniki azowe [
Mn, Zn, Cd, Ni, Co, In, U,
Fe
], Na-DDTK [
Cu, Bi, Mn, Mo, Co
].
SPEKTROSKOPIA ATOMOWA
Stan podstawowy
–stan atomu charakteryzujący się
najmniejszą energią dla podstawowej konfiguracji elektronów,
Stan wzbudzony
–dostarczenie do atomu odpowiedniej
charakterystycznej dla niego energii powoduje przeniesienie
elektronu walencyjnego do poziomu o wyższej energii.
Metody analityczne oparte na spektroskopii atomowej
obejmują trzy różne techniki analityczne:
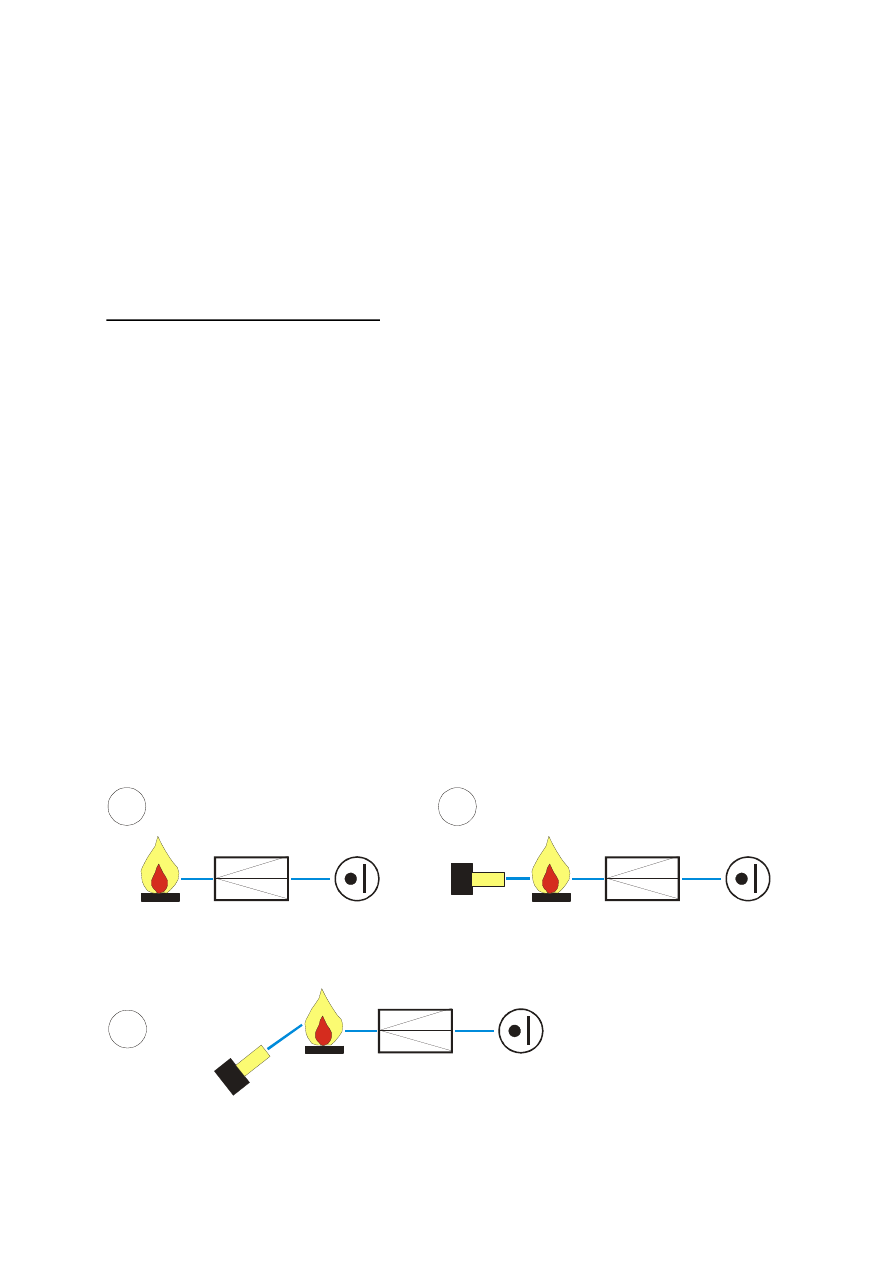
1.
emisję
atomową
–wzbudzenie
atomów
poprzez
dostarczenie im energii termicznej (płomień, łuk
elektryczny, plazma) -
pomiar emisji (długości i
intensywności) promieniowania
,
2.
absorpcję
atomową
–atomy
będące
w
stanie
podstawowym są wzbudzane wiązką promieniowania
o odpowiadającej im energii -
pomiar (zmiany
intensywności wiązki I
0
) absorpcji
,
3.
fluoroscencję atomową
–wzbudzenie jak w absorpcji
atomowej, pomiar sygnału jak emisji atomowej,
lampa
lampa
atomizer
atomizer
atomizer
detektor
detektor
detektor
monochromator
monochromator
monochromator
1
2
3

OGÓLNA BUDOWA SPEKTROMETRU ABSORPCJI
ATOMOWEJ
1.
Źródło promieniowania
, lampy emitujące wąskie linie
atomowe oznaczanego pierwiastka
•
lampy
z
katoda
wnękową
jedno
i
wielopierwiastkowe
• bezelektrodowe lampy wyładowcze z generatorem
częstości radiowej
2.
Modulator
, pozwala wyeliminować promieniowanie
emitowane przez atomizer
3.
Atomizer,
wytworzenie odpowiedniej ilości atomów w
stanie podstawowym poprzez dostarczenie im energii
termicznej
•
atomizery
płomieniowe
,
rozpylacz,
komora
mieszania, głowica palnika
•
atomizery
bezpłomieniowe,
piece
grafitowe
ogrzewane prądem elektrycznym
4.
Monochromator
–służy do wyodrębnienia wybranego
pasma o odpowiedniej długości fali z wiązki
promieniowania emitowanego przez lampę i atomizer
5.
Detektor,
urządzenie (zwykle fotopowielacz) służące do
zamiany energii elektromagnetycznej (promieniowania)
na energię elektryczną (prąd) proporcjonalną do
intensywności promieniowania
6.
Inne jak
: soczewki, zwierciadła, układy elektroniczne,
zliczające, uśredniające i rejestrujące
Układy optyczne:
• układy jednowiązkowe,
• układy dwuwiązkowe
PROCESY ZACHODZACE W ATOMIZERZE

M
+
+
A
−
(roztwór)
1. rozpylenie
M
+
+
A
−
(aerozol)
2. desolwatacja
MA
(ciało stałe)
3. topnienie
MA
(ciecz)
4. parowanie
MA
(gaz)
5.
atomizacja
M
0
+
A
0
(gaz)
6.
wzbudzenie
M
*
(gaz)
7. jonizacja
M
+
+
e
−
(gaz)
INTERFERENCJE
Konsekwencją prowadzenia pomiarów bez korekcji
lub/i kompensacji interferencji są błędne wyniki pomiarów
zawartości analitu w próbce.
•
interferencje spektralne
–absorpcja promieniowania
przez obecne w próbce składniki inne niż oznaczany
pierwiastek
•
interferencje spektralne
–związane z nieodtwarzalnymi
procesami tworzenia wolnych atomów analitu w stanie
podstawowym (zbyt niska lub zbyt wysoka temperatura
atomizacji, jonizacja, powstawanie trudnodysocjujących
związków chemicznych, itp.)
•
interferencje
fizyczne,
-wywołane
różnymi
właściwościami próbki (lepkość, gęstość, obecność sp-a)

MIARECZKOWANIE POTENCJOMETRYCZNE

Polega na
pomiarze różnicy potencjałów
pomiędzy
elektrodą wskaźnikową i elektrodą odniesienia po dodaniu
każdej porcji odczynnika miareczkującego.
Jest możliwe do wykonania wówczas gdy dobierze się
elektrodę wskaźnikowa, która będzie reagowała bezpośrednio
na zmiany składnika oznaczanego lub miareczkującego
zachodzące podczas miareczkowania.
Krzywa miareczkowania potencjometrycznego
jest
analogiczna do klasycznej krzywej miareczkowania z tym, że
w
PR
obserwujemy gwałtowny skok potencjału.
Instrumentalne
a
nie
wizualne
określenie
PK
miareczkowania
jest
ścisłe,
obiektywne,
dokładne
i
precyzyjne.
Typy miareczkowań potencjometrycznych:
•
miareczkowanie
alkacymetryczne
–wykonywane
wobec elektrod wskaźnikowych czułych na zmiany
stężenia jonów wodorowych, np. elektroda szklana
•
miareczkowanie redoks
–wykonywane wobec elektrody
platynowej, przyjmuje się, że potencjał tej elektrody jest
proporcjonalny do logarytmu stosunku stężeń postaci
utlenionej do zredukowanej danego układu utl-red,
•
miareczkowanie kompleksometryczne
–wykonywane
wobec elektrod jonoselektywnych. Stosowane do
oznaczania metali i badania reakcji tworzenia i rozpadu
kompleksów. Stężenie kationu nie związanego w
kompleks (np. wolnego jonu metalu) maleje początkowo
stopniowo a w pobliżu PR w sposób gwałtowny,
•
miareczkowanie
strąceniowe
–badanie
reakcji
polegających
na
strącaniu
osadów
–iloczyn
rozpuszczalności osadu musi mieć dużą wartość. Np.

strącanie jonów srebra za pomocą jonów chlorkowych
wobec elektrody srebrowej (I rodzaju).
Sposoby wyznaczania punktu końcowego PK
•
metoda graficzna
•
metoda pierwszej pochodnej,
-wyznaczenie stosunku
przyrostu potencjału do przyrostu objetości w funkcji
objetości
( )
V
f
dV
dE
=
•
metoda drugiej pochodnej,
-druga pochodna
∆
2
E/
∆
V
2
ma inny znak przed PK (
dodatni
) niż po przekroczeniu
PK (
ujemny
).
Wyszukiwarka
Podobne podstrony:
przewodnik biofizyka id 407075 Nieznany
BIOFIZYKA 2 id 86951 Nieznany (2)
biofizyka 2 id 86907 Nieznany
przewodnik biofizyka id 407075 Nieznany
biofizyka materialy id 87015 Nieznany
biofizyka egzamin plonka id 869 Nieznany
Biofiza pogrupowane id 86891 Nieznany (2)
BIOFIZYKA WYMAGANIA id 87047 Nieznany (2)
Abolicja podatkowa id 50334 Nieznany (2)
4 LIDER MENEDZER id 37733 Nieznany (2)
katechezy MB id 233498 Nieznany
metro sciaga id 296943 Nieznany
perf id 354744 Nieznany
interbase id 92028 Nieznany
Mbaku id 289860 Nieznany
Probiotyki antybiotyki id 66316 Nieznany
miedziowanie cz 2 id 113259 Nieznany
LTC1729 id 273494 Nieznany
D11B7AOver0400 id 130434 Nieznany
więcej podobnych podstron