
1
Ćwiczenie 2. Ocena efektywności oczyszczania ścieków w modelowym
systemie „osadu czynnego”
1. Wprowadzenie
Azot i fosfor są substancjami biogennymi (biogenami), tzn. umożliwiają i intensyfikują
procesy wzrostu zarówno komórek roślinnych, jak i bakteryjnych. Znajdując się w wodach w
większych ilościach, powodują zaburzenie naturalnej równowagi w zbiorniku. Przyjmuje się,
iż nadmierny rozwój glonów w odbiorniku, mogą powodować stężenia azotu powyżej 0,3
mg/dm
3
i stężenia fosforu większe od 0,1 mg/dm
3
. Zjawisko przejawiające się poprzez
zwiększanie żyzności (trofii) tj. wzrost stężenia związków biogennych (fosforu P i azotu N) w
środowisku wodnym nosi nazwę eutrofizacjii. Proces eutrofizacji jest jak najbardziej
naturalny, lecz uległ nasileniu na skutek zintensyfikowania rozwoju gospodarki, nawożenia
pół uprawnych i degradacji obszarów lesistych. Jednakże głównym źródłem przedostawania
się związków biogennych do rzek i jezior są ścieki miejskie.
Z tej przyczyny niezbędne stało się wprowadzenie aktów prawnych ograniczających ilości
azotu, fosforu jak również związków organicznych zrzucanych do odbiornika [1], a co za tym
idzie, poprawę skuteczności oczyszczania. Technologia ”osadu czynnego” jest
najpowszechniej stosowaną metodą usuwania biogenów ze ścieków bytowo-gospodarczych
na biologicznych oczyszczalniach ścieków.
Oczyszczanie ścieków metodą osadu czynnego jest wzorowane na tlenowych procesach
samooczyszczania zachodzących w wodach powierzchniowych i polega na mineralizacji
zanieczyszczeń organicznych znajdujących się w ściekach przez drobnoustroje osadu
czynnego w instalacjach technicznych. W wyniku tego procesu mikroorganizmy uzyskują
energię niezbędną do życia, powstają mineralne formy węgla, azotu, fosforu i siarki oraz
następuje przyrost biomasy. Nadmiar organizmów wynikający z rozkładu związków
organicznych, tzw. osad nadmierny, jest usuwany z systemu
Intensyfikacja procesu, w porównaniu z naturalnym samooczyszczaniem, polega na
sztucznym natlenieniu środowiska wodnego, oraz na zwiększeniu ilości drobnoustrojów
biorących udział w procesie, co pozwala na doprowadzenie większej ilości zanieczyszczeń.
Powietrze doprowadzane do komór napowietrzania spełnia podwójną funkcję:
i) utrzymuje cieki i osad stałym ruchu, uniemożliwiając opadanie osadu na dno zbiornika
ii) tlen zawarty rozpuszczony w ściekach służy jako substrat w reakcjach
biochemicznego utleniania zanieczyszczeń zawartych w ściekach.
Osad czynny jest kłaczkowatą zawiesiną złożoną głównie z bakterii (z rodzaju
Pseudomonas, Acinetebacterium, Zooglea, Enterobacteriae, Aeromonas, Flavobacterium,
Achromobacter, Micrococcus), a także pierwotniaków - orzęsków (z rodzaju Paramecium,
Vorticella, Aspidisca, Suctoria) i wiciowców (z rodzaju Tetramitus, Trigonomonas, Bodo),
oraz wrotków i niektórych grzybów. Kłaczki osadu czynnego powstają na skutek
wydzielania przez komórki bakteryjne otoczek śluzowych, w wyniku czego powstają
regularne formy zooglenalne („skupiska zooglenalne”).
2
2. Cel
Celem niniejszych zajęć laboratoryjnych jest ocena efektywności biologicznego
oczyszczania ścieków (usuwania N,P i zw. organicznych) w modelowym reaktorze osadu
czynnym.
3.Zabiegi wstępne
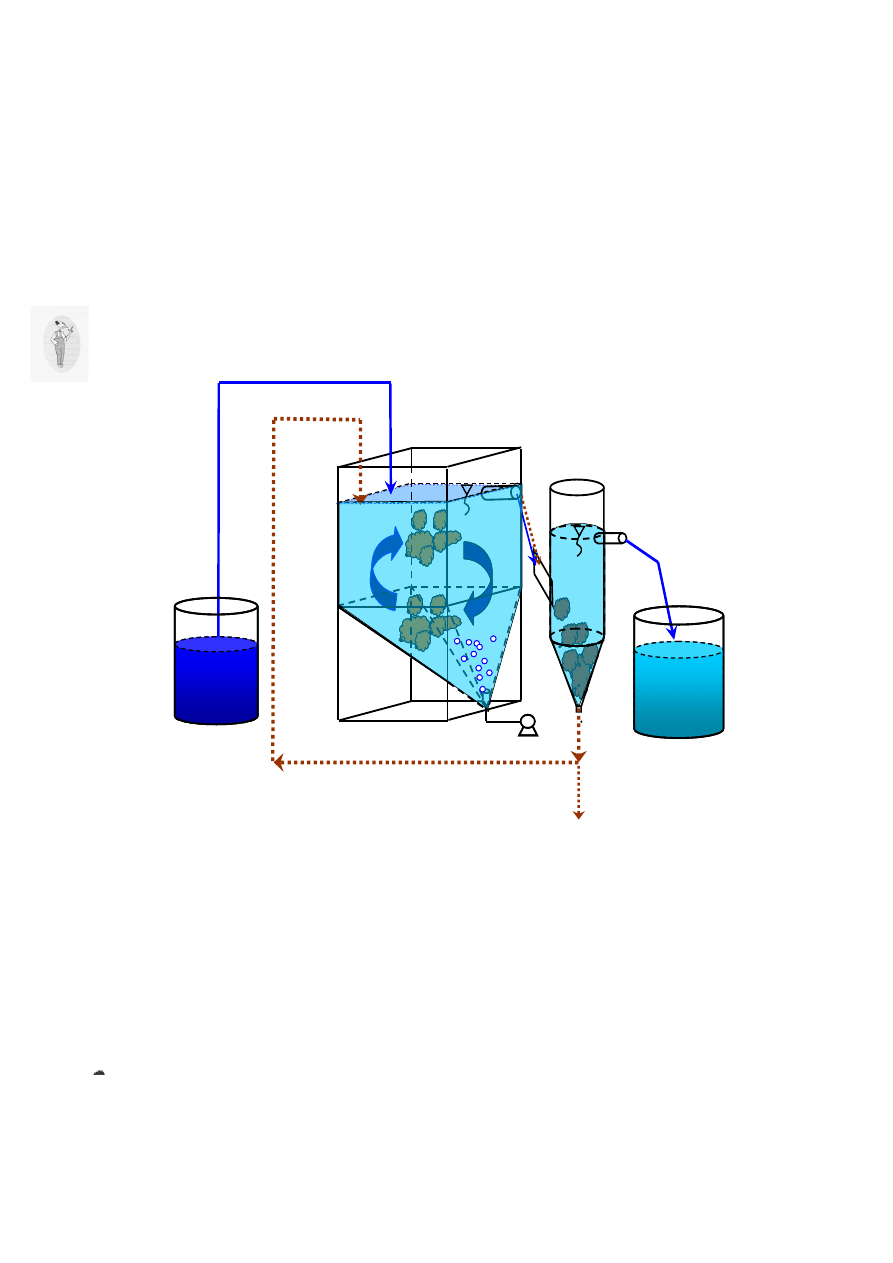
Zapoznać się z budową modelowego systemu osadu czynnego.
Scieki
Oczyszczone
Osadnik
Recyrkulacja osadu
Scieki
Surowe
Komora
napowietrzania
Osad nadmierny
Rys.1 Schemat systemu osadu czynnego
Grupa studencka dzieli się na zespoły, z których każdy będzie wykonywał dane oznaczenia
zanieczyszczeń w ściekach dopływających jak również odpływających z układu.
3
Tabela 1.Zakres i metody oznaczeń
Oznaczenie
Metoda oznaczenia
ChZT
standardowa metoda dwuchromianowa
Azot amonowy
metoda kolorymetryczna (z wersenianem sodowym i odczynnikiem
Nesslera) SPEKOL 11 firmy Carl Zeiss Jena
Azot azotynowy
metoda kolorymetryczna (z kwasem sulfanilowym i alfanaftyloaminą)
SPEKOL 11 firmy Carl Zeiss Jena
Azot azotanowy
metoda kolorymetryczna (z 2,6 dimetylofenolem), SPEKOL 11 firmy
Carl Zeiss Jena
Fosforany
metoda kolorymetryczna (z kwasem askorbinowym i odczynnikiem
mieszanym) SPEKOL 11 firmy Carl Zeiss Jena
4.Wykonanie ćwiczenia
Badania należy rozpocząć od pobrania próbek ścieków surowych (dopływ) oraz
ścieków oczyszczony (odpływ) w ilości ok. 300 ml. Pobrane próbki przefiltrować na filtrze
twardym w celu usunięcia zawiesin. W filtracie należy oznaczyć zanieczyszczenia wg
metodyki podanej w Tabeli 1.
UWAGI!
Do każdego oznaczenia należy przygotować próbkę referencyjną tzw. „ślepą” na wodzie
destylowanej.
Przed oznaczeniem należy przygotować odpowiednie rozcieńczenie umożliwiające
detekcję. Wykorzystywana metoda pozwala na oznaczenie stężenia w granicach 0,1- 2,5 mg/l.
Przykładowo stężenie w ściekach N - NH
4
+
= 50 mg/l., stąd proponowane rozcieńczenie 1:25
(tj. 25 razy).
Oznaczone stężenia fosforanów należy przeliczyć na stężenie fosforu (mg PO
4
3-
mg P).
Wyniki analiz zespołów studenckich należy zebrać w tabeli 2.
Tabela 2
Oznaczenia
Jednostki
Ścieki
surowe
Ścieki
oczyszczone
Stopień
usunięcia [%]
Norma
ChZT
[mgO
2
/dm
3
]
Azot amonowy
[mgN-NH
4
+
/dm
3
]
Azot azotynowy
[mgN-NO
2
-
/dm
3
]
-
Azot azotanowy
[mgN-NO
3
-
/dm
3
]
-
Fosfor
[mg P/dm
3
]
*BZT
5
[mgO
2
/dm
3
]
*Biochemiczne Zapotrzebowanie na Tlen (frakcja zw. organicznych rozkładalna biologicznie) dla ścieków
surowych przyjąć BZT
5
= 0.7 ChZT, dla ścieków oczyszczonych przyjąć BZT
5
= 0.1 ChZT

4
5.Opracowanie wyników
Na podstawie zebranych wyników analiz (Tabela 2) sekcje 4-5 osobowe opracowują wyniki.
5.1. Uzupełnij tabelę 3 i dokonaj oceny efektywności biologicznego oczyszczania ścieków
(usuwania zanieczyszczeń organicznych ChZT, BZT
5
oraz N i P) w reaktorze osadu czynnego
w oparciu o dane literaturowe [1].
5.2. Przeprowadź dyskusję wyników zmian zanieczyszczeń w reaktorze ze zwróceniem uwagi
na procesy biologiczne tam zachodzące (nitryfikacja, usuwanie związków organicznych).
6. Literatura
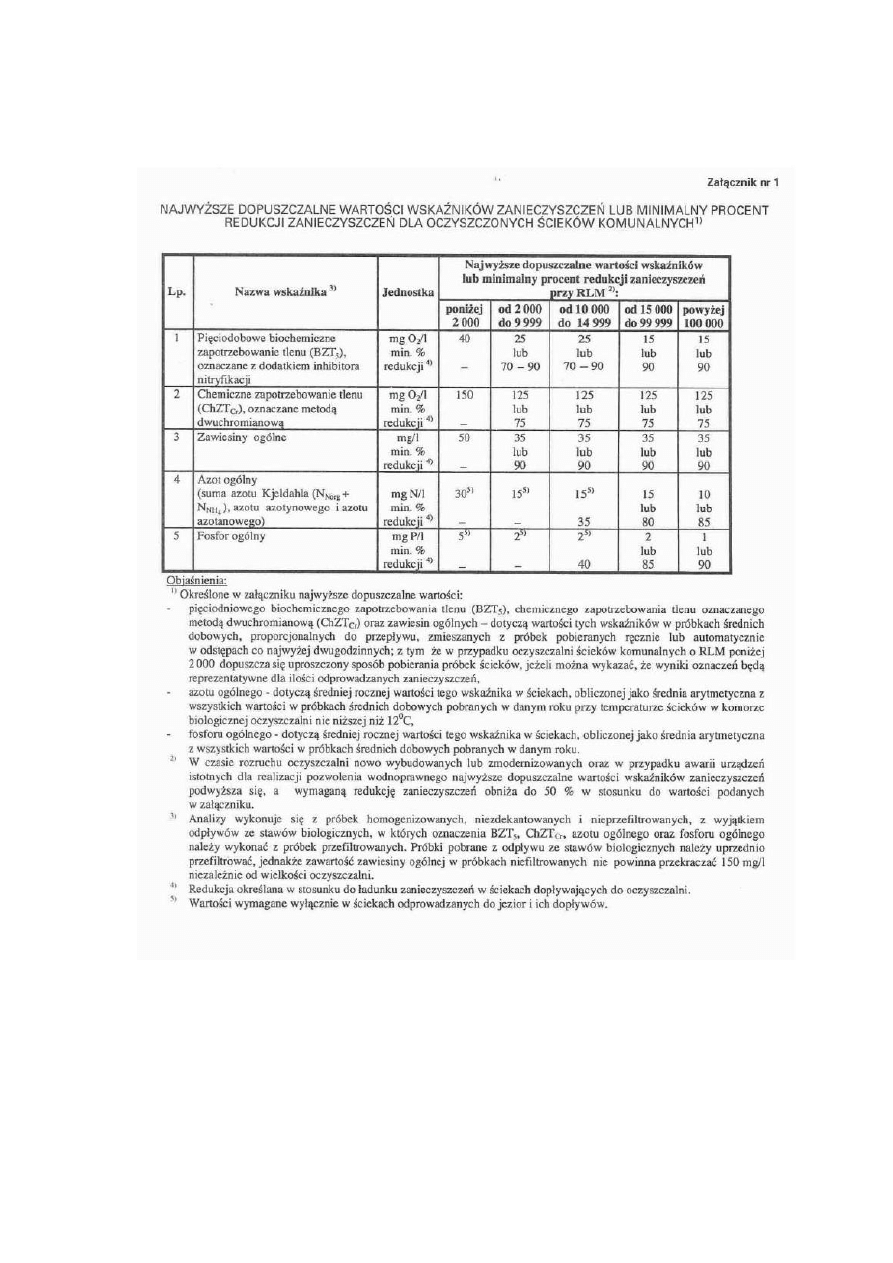
1. Rozporządzenie Ministra Środowiska z dnia 24 lipca 2006 (Dz.U.06.137.984.) (
zmiana z dnia 28 stycznia 2009 r. DZ U 2009 R. NR 27 POZ. 169) w sprawie
warunków, jakie należy spełnić przy wprowadzaniu ścieków do wód lub do ziemi oraz
w sprawie substancji szczególnie szkodliwych dla środowiska wodnego
2. „Biotechnologia ścieków” - praca zbiorowa pod redakcją Korneliusza Mikscha;
wydawnictwo Politechniki Śląskiej; Gliwice 2000 r.
3. „Poradnik eksploatatora oczyszczalni ścieków” – praca zbiorowa pod redakcją Z.
Dymaczewskiego, J. Oleszkiewicza, M Sozańskiego ; Poznań 1997 r.
4. „Biotechnologia w ochronie środowiska” Klimiuk Ewa, Łebkowska Maria, ISBN 83-01-
14067-4, Wydawnictwo Naukowe PWN SA, Warszawa 2005.
7. Pytania kontrolne:
1. Co to jest osad czynny?
2. Na czym polega proces nitryfikacji?
3. Wyjaśnij, na czym polega oczyszczanie ścieków metodą osadu czynnego (na podstawie
schematu na rys. 1)?
4. Jaką grupę zanieczyszczeń charakteryzuje parametr ChZT?
5. Co to jest odbiornik ścieków?
6. Jakie związki określamy mianem substancji biogennych?
7. Co to jest „osad nadmierny”?
8. Co to są ścieki?
9. Co to jest eutrofizacja i jak wpływa na odbiornik ścieków?
10. Jaką rolę pełni napowietrzanie w komorze napowietrzania?
8. Uwagi dodatkowe
Zaliczenie ćwiczenia:
- Sekcje 3-4 osobowe przygotowują 1 sprawozdanie (instrukcja punkt
5)
UWAGA!
Termin oddania: 2 tygodnie od daty wykonanego ćwiczenia!!!
5
Załącznik 1
Wyszukiwarka
Podobne podstrony:
Instrukcja cw 3 Metody biotechnologii
Instrukcja cw 2 Metody biotechnologii
Cw 3 Metody biotechnologii
Instrukcja cw 4 Metody biotechnologii
Cw 5 6 Metody biotechnologii
Instrukcja cw 5 Metody biotechnologii
Cw 4 Metody biotechnologii
Instrukcja cw 3 Metody biotechnologii
ćw. 5- barwniki-metodyka, Biotechnologia UKW I ST, Biotechnologia żywności UKW
ćw 6 - metodyka konserwanty NOWA, Biotechnologia UKW I ST, Biotechnologia żywności UKW
1 ĆW. kwas mlekowy - METODYKA, Biotechnologia UKW I ST, Biotechnologia żywności UKW
4 ĆW. Liczby tłuszczowe -metodyka, Biotechnologia UKW I ST, Biotechnologia żywności UKW
więcej podobnych podstron