
I. Wstęp teoretyczny.
Kryterium Rayleigha.
Kryterium pozwalające ocenić, czy dwie linie widmowe są rozdzielone. Warunkiem rozróżnialności
obrazów dyfrakcyjnych dwóch równoległych linii widmowych jest spełnienie kryterium:
maksimum jednego obrazu dyfrakcyjne musi być położone w miejscu minimum drugiego obrazu.
Kryterium jest stosowane do określania zdolności rozdzielczej elementów i układów optycznych.
Nie jest ono ścisłym prawem. Dla obrazów dyfrakcyjnych powstałych po przejściu światła przez
otwór kołowy warunek Rayleigha można zapisać wzorem:
sin(φ)=1,22 λ
d
φ - minimalny kąt między promieniami, których obrazy mają być rozróżnialne, czyli inaczej – ich
odległość kątowa;
λ – długość fali światła
d – średnica otworu
Ponieważ kąt φ jest bardzo mały, można zapisać w przybliżeniu:
φ≈
1,22 λ
d
Oddziaływanie van der Waalsa.
Oddziaływania między trwałym dipolem i indukowanym (wzbudzonym) dipolem. W cząsteczkach,
które nie posiadają trwałego momentu dipolowego, może on być wzbudzany przez cząsteczki
z trwałym momentem; następnie taki wzbudzony dipol i trwały dipol oddziałują na siebie podobnie
jak dwa trwałe dipole, tyle że znacznie słabiej; w cząsteczkach bez trwałego momentu dipolowego
występują natomiast stochastyczne fluktuacje ich chmur elektronowych, powodujące powstawanie
chwilowych momentów dipolowych; cząsteczka posiadająca chwilowy moment dipolowy może go
wzbudzić w cząsteczce sąsiadującej, wskutek czego obie cząsteczki mogą się nawzajem chwilowo
przyciągać lub odpychać.
Uśrednienie sił odpychających i przyciągających daje w wyniku oddziaływanie przyciągające
proporcjonalne do 1/r6; oddziaływania van der Waalsa wynikają m.in. z korelacji ruchów
elektronów pomiędzy oddziałującymi atomami – dlatego w metodach obliczeniowych
nieuwzględniających korelacji elektronowej sił tych praktycznie nie ma.
Potencjał Lenarda-Jonesa.
Matematyczny model przybliżający oddziaływania pary neutralnych atomów lub cząsteczek.
Najczęściej stosowanymi postaciami tego potencjału są następujące wyrażenia:

Gdzie ε – to głębokość studni potencjału, σ jest skończoną odległością, w której potencjał wynosi
zero. Symbol r oznacza odległość między cząstkami, a r
m
jest odległością dla której energia
potencjalna osiąga minimum; dla tej odległości potencjał ma wartość (- ε).
Czynnik z r
-12
odpowiada za siły odpychające, które rosną w miarę zbliżania się cząstek na skutek
nakładania się orbitali atomowych. Z kolei czynnik r
-6
odpowiada dalekozasięgowym siłom
przyciągającym (omówione oddziaływania Van der Waalsa).
Adsorpcja.
Jest to proces wiązania się cząsteczek, jonów lub atomów na powierzchni lub granicy faz
fizycznych, powodujący lokalne zmiany stężenia. Adsorpcja może mieć charakter fizyczny
(adsorpcja fizyczna, fizysorpcja) lub chemiczny (chemisorpcja). Adsorpcja ma charakter
powierzchniowy, co odróżnia ją od innego zjawiska – absorpcji, która polega na pochłanianiu
w całej objętości. Zdolność adsorpcyjna to masa adsorbatu, która może być zaadsorbowana przez
jednostkę masy adsorbentu. Jest ona zależna od wielu zmiennych i wyznaczana doświadczalnie dla
danego płynu i warunków ( ciśnienie, temperatura, rodzaj i czas zetknięcia).
Adsorpcja fizyczna, to zjawisko adsorpcji na skutek działania sił oddziaływania
międzycząsteczkowego – siła van der Waalsa (z wyłączeniem wiązań chemicznych – wówczas
mówimy o chemisorpcji) pomiędzy cząsteczką adsorbatu a powierzchnią adsorbentu. Energia
związana z procesem adsorpcji fizycznej jest z reguły rzędu kilki kJ/mol. Wielkość adsorpcji
fizycznej silnie zależy od temperatury, ciśnienia lub stężenia adsorbatu. Siły van der Waalsa zależą
od rodzaju powierzchni absorbentu i adsorbatu, jednak mają charakter w dużym stopniu
niespecyficzny, gdyż wynikają przede wszystkim z powszechnego istnienia sił dyspersyjnych
(Londona) związanych z budową materii.
Chemisorpcja polega na tworzeniu silnych wiązań chemicznych między adsorbentem i adsorbatem.
Jest ona adsorpcją jednowarstwową – na powierzchni adsorbentu może zaadsorbować jedynie jedna
warstwa (monowarstwa).Chemisorpcji towarzyszy zawsze adsorpcja fizyczna w obrębie
monowarstwy oraz adsorpcja wielowarstwowa – na istniejącej chemisorbowanej monowarstwie.

Adsorpcja fizyczna stanowi ważny etap pośredni pomiędzy adsorbatem gazowym
i chemisorbowanym. Oddziaływania związane z chemisorpcją są oddziaływaniami specyficznymi.
Związane są z efektem orientacyjnym (
a w przypadku adsorpcji jonów także z oddziaływaniami elektrostatycznymi.
Fizysorpcja
•
brak bariery energetycznej (nie wymaga
aktywacji),
•
szybki proces,
•
oddziaływania słabe (<0,4 [eV]),
•
zawsze atomowa lub cząsteczkowa,
•
proces odwracalny,
•
może powstać wielowarstwa.
Chemisorpcja
•
może występować bariera energetyczna
(wymaga energii aktywacji),
•
różnorodna kinetyka procesu,
•
powstanie wiązań kowalencyjnych, jonowych,
metalicznych (sile wiązania >0,4 [eV]),
•
może być dysocjatywna,
•
często nieodwracalna,
•
ograniczona do monowarswy
Zjawisko piezoelektryczne.
Prostym zjawiskiem piezoelektrycznym nazywamy zjawisko powstawania indukcji elektrycznej
w ciele stałym pod wpływem naprężeń. Zjawisko to powstaje tylko w pewnych ciałach stałych,
mających uporządkowaną budowę atomową i wykazujących właściwą budowę materii. Odwrotnym
zjawiskiem piezoelektrycznym nazywamy zjawisko powstawania odkształceń kryształu pod
wpływem pola elektrycznego.
Zjawisko piezoelektryczne jest zjawiskiem nieparzystym i liniowym, ze względu na
proporcjonalność między polem elektrycznym a naprężeniem mechanicznym.
Piezoelektryk lub materiał piezoelektryczny to kryształ, w którym obserwowane jest zjawisko
piezoelektryczne. Piezoelektrykami mogą być zarówno monokryształy (np. kwarc), jak i
polikryształy, których komórki elementarne nie mają środka symetrii. Istnieją również ceramiki i
substancje organiczne o właściwościach piezoelektrycznych, takie jak polimery, DNA, białka i
kości. Niektóre piezoelektryki są również piroelektrykami i ferroelektrykami.
Mikroskopy SPM. Mikroskop sił atomowych – AFM (ang. atomic force microscope).
Mikroskopy SPM (ang. Scanning Probe Microscope, Mikroskop ze skanującą sondą), to grupa
instrumentów służących do badań powierzchniowych właściwości materiałów. Badania te mogą
być przeprowadzane w skali ułamków nanometrów, aż do poziomu mikrometrów. Wszystkie
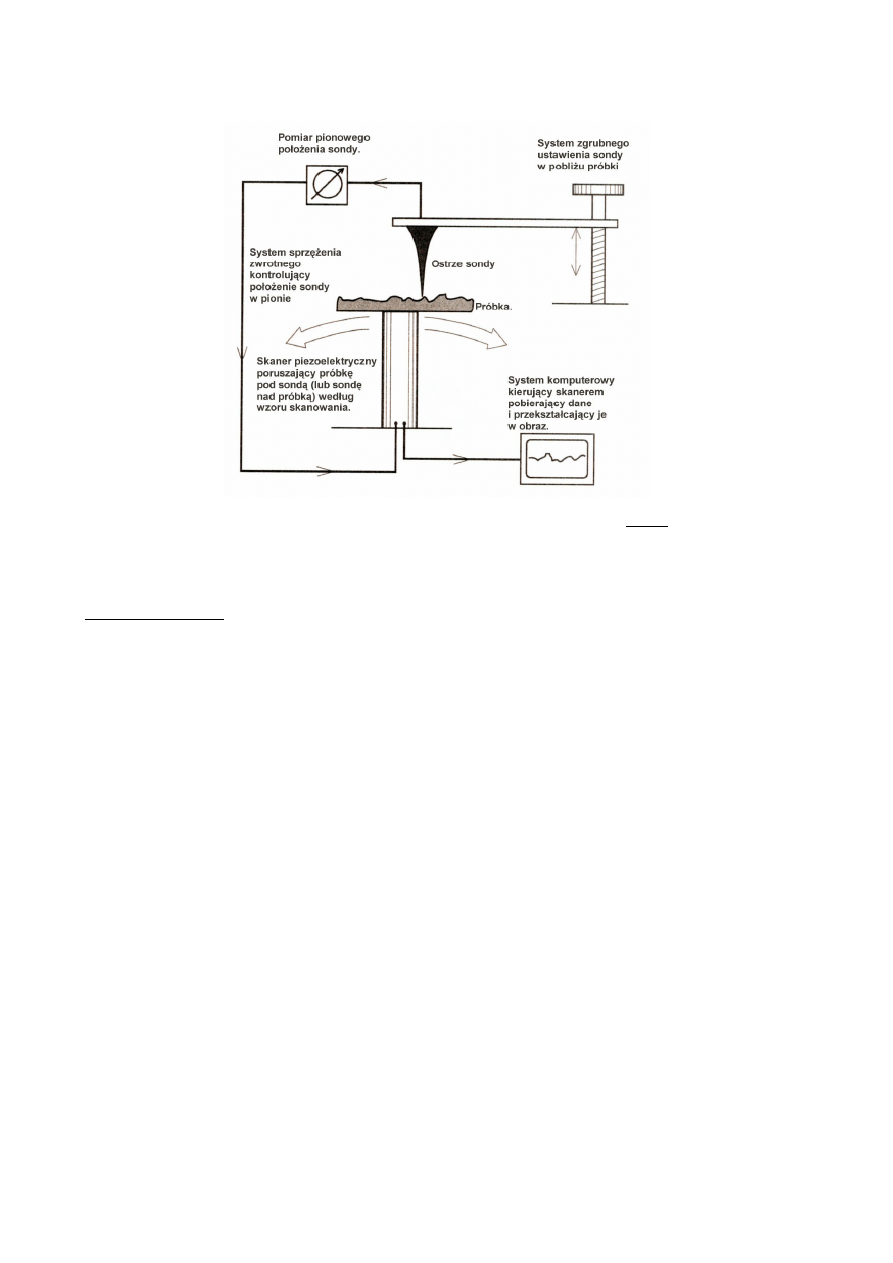
mikroskopy SPM zawierają elementy pokazane na rysunku poniżej:
Mikroskop sił atomowych (AFM) bada powierzchnię próbki zaostrzoną sondą – o długości rzędu
kilku milimetrów, średnica jej jest mniejsza od 10nm. Sonda umieszczona jest na końcu dźwigienki
w odległości 100-200um. Siła występująca pomiędzy powierzchnią próbki a igłą sondy powoduje
ugięcie
dźwigienki
, podczas przemieszczania się sondy nad powierzchnią próbki, lub próbki pod
sondą. Siła działająca na sondę jest miarą odległości pomiędzy nimi. Czułość odczytu ugięcia
dźwigni sięga dziesiątych części angstrema. Mikrosondy stosowane w AFM produkuje się
zazwyczaj z krzemu i azotku krzemu.
Pomiar ugięcia dźwigni mierzony jest metodami optycznymi, pozwala na utworzenie przez
komputer topograficznej mapy powierzchni próbki. Metoda zapewnia pomiar dużej rozdzielczości,
względem trzech osi x, y, z. W przeciwieństwie do mikroskopu elektronowego próbka nie podlega
kontrastowaniu, mrożeniu – znajduje się w naturalnym środowisku, co przy dodatkowej możliwości
pracy w cieczy stanowi bazę do obrazowania elementów biologicznych.
•
MFM (Magnetic Force Microscope), mikroskop sił magnetycznych – obrazowanie różnic sił
magnetycznych działających na sondę w badanych punktach danego materiału. Skanująca sonda pokryta
jest cienką warstewką ferromagnetyka. Mikroskop pracuje w trybie bezkontaktowym. Wykorzystywany
do obrazowania struktury domen magnetycznych, ale także do topografii próbki.
•
EFM (Electrostatic Force Microscope) , mikroskop sił elektrostatycznych. W mikroskopie tym
wytwarza się różnicę potencjałów pomiędzy sondą a próbką, nad którą przesuwa się dźwigienka z
ostrzem nie dotykającym próbki. Kiedy sonda znajdzie się nad powierzchnią o różnym ładunku
statycznym następuje ugięcie dźwigienki proporcjonalne do wielkości ładunku w dół lub górę, w
zależności od znaku ładunku. EFM sporządza mapę lokalnego rozmieszczenia ładunku elektrycznego
(domen elektrycznych). Wykorzystywany jest do tworzenia obrazu pola elektrostatycznego ponad
badanym układem elektronicznym, który jest włączony lub wyłączony (tzw. próbkowanie napięcia).
Wyszukiwarka
Podobne podstrony:
Material teoretyczny id 284375 Nieznany
obieg teoretyczny id 327051 Nieznany
AFM wstęp teoretyczny
gk 01 wstep id 191745 Nieznany
aue wstep id 72298 Nieznany
cwiczenia5 wstep id 124970 Nieznany
AWP wyklad wstep D id 74559 Nieznany
Antologia wstep by AG id 18051 Nieznany (2)
cwiczenie AFM id 101087 Nieznany
NoM wstep id 320698 Nieznany
Zloza 2014 wstep id 566869 Nieznany
pdxp wstep id 353063 Nieznany
Mury wstep id 310556 Nieznany
Komunikaty Wstep 8 id 243824 Nieznany
Komunikaty Wstep 9 id 243825 Nieznany
biewuc wstep id 85633 Nieznany (2)
Fiz wstep id 173360 Nieznany
JPPO Wstep do wykladu id 228827 Nieznany
więcej podobnych podstron