Termodynamika
Równanie stanu gazu dla 1 kg masy czynnika
RT
v
p
=
⋅
gdzie: p - bezwzględne ciśnienie statyczne czynnika
T
R
p
v
⋅
=
⇒
=
ρ
ρ
1
v– objętość właściwa czynnika (dla 1 kg!!!)
R- indywidualna stała gazowa
T- bezwzględna temperatura czynnika T=(273,15 + t )[K]
Równanie stanu gazu dla całej masy czynnika
mRT
pV
V
m
v
mRT
m
v
p
=
⇒
=
⋅
⇒
=
⋅
⋅
RT
pv
RT
v
p
µ
µ
µ
=
⇒
=
⋅
/
ponieważ
m
V
v
=
⋅
µ
i
B
R
=
⋅
µ
otrzymujemy równanie
BT
V
p
m
=
⋅
µ
- masa cząsteczkowa czynnika
V
m
– objętość molowa
kmol
m
3
=
=
⇒
=
3
2
96
,
1
42
,
22
44
.
m
kg
np
V
CO
m
m
m
ρ
µ
ρ
inny wzór na gęstość w warunkach umownych:
u
u
m
u
m
u
T
R
P
stąt
T
R
p
T
R
v
p
⋅
−
⇒
⋅
=
⋅
⇒
⋅
=
⋅
ρ
ρ
,
1
stałą R liczymy ze wzoru
m
B
R
µ
=
B- 8314,3
⋅
K
kmol
J
, do obliczeń ciepła właściwego podstawiamy B=8,3143
⋅
K
kmol
kJ
W warunkach umownych
p
u
=101325 [Pa] czyli około 760[mmHg]
T
u
=273,15 [K]
Dla umownych warunków temperatury i ciśnienia V
m
dla różnych gazów przyjmuje taką samą wartość
V
m
=22,42
kmol
m
3
T
B
V
p
m
⋅
=
⋅
→
µ
⋅
=
n
m
gdzie: n- liczba kmoli cząsteczek gazu
T
R
n
V
p
m
⋅
⋅
⋅
=
⋅
µ
→
B
R
=
⋅
µ
T
B
n
V
p
m
⋅
⋅
=
⋅
Mieszaniny gazów
Równania stanu gazu przed zmieszaniem
T
R
m
V
p
1
1
1
=
⋅
i
T
R
m
V
p
2
2
2
=
⋅
Wartości które należy
pamiętać:
p
u
=101325 [Pa]
T
u
=273,15 [K]
V
m
=22,42
kmol
m
3
B- 8314,3
⋅
K
kmol
J
lub
B=8,3143
⋅
K
kmol
kJ
ps
µ
-masa cząst. powietrza
suchego = 28,87
kmol
kg
p, T
m
1
, V
1
, R
1
p, T
m
2
, V
2
, R
2

Po otwarciu zaworu
T
mR
V
p
m
=
⋅
a)
2
1
m
m
m
+
=
b)
2
1
V
V
V
+
=
c)
2
1
n
n
n
+
=
(bilans molowy)
Określanie udziałów masowych
2
2
1
1
2
1
0
,
1
g
m
m
g
m
m
m
m
m
m
=
∩
=
⇒
=
+
Udziały objętościowe
2
2
1
1
2
1
0
,
1
r
V
V
r
V
V
V
V
V
V
=
∩
=
⇒
=
+
Udziały molowe
2
2
1
1
2
1
0
,
1
z
n
n
z
n
n
n
n
n
n
=
∩
=
⇒
=
+
Przeliczanie udziałów
przeliczenie objętościowych na masowe
i
m
i
i
R
R
r
g
⋅
=
lub
m
i
i
i
r
g
µ
µ
⋅
=
przeliczenie masowych na objętościowe
m
i
i
i
R
R
g
r
⋅
=
lub
i
m
i
i
g
r
µ
µ
⋅
=
i
i
r
z
=
∑
⋅
=
i
i
m
r
µ
µ
m
m
R
B
=
µ
∑
⋅
=
i
i
m
R
g
R
m
m
B
R
µ
=
∑
⋅
=
i
i
m
r
ρ
ρ
m
i
i
V
µ
ρ
=
Cieśnienie cząstkowe
p
r
p
i
i
⋅
=
Obliczanie bilansów ciepła, mocy cieplnej układów, strumienia przekazywanego ciepła
1.)
t
c
m
Q
∆
⋅
⋅
=
lub inaczej
)
(
1
2
t
t
c
m
Q
Vm
−
⋅
⋅
=
gdzie m- masa
[ ]
kg
lub strumień masy
s
kg
czynnika, c-masowe ciepło właściwe
⋅
K
kg
kJ
2.)
t
C
V
Q
∆
⋅
⋅
=
lub inaczej
)
(
1
2
t
t
C
V
Q
Vm
−
⋅
⋅
=
gdzie V- objętość
[ ]
3
m
lub strumień obj.
s
m
3
czynnika, C-objętościowe ciepło właściwe
⋅
K
m
kJ
3
,
przy czym C musi być określone w tych samych warunkach p i T co V, najlepiej w war. umownych.
3.)
t
n
Q
c
∆
⋅
⋅
=
µ
lub inaczej
)
(
1
2
t
t
n
Q
CVm
−
⋅
⋅
=
µ
gdzie n- liczba kmoli czynnika,
c
µ
-molowe ciepło właściwe
⋅
K
kmol
kJ
,
Energia wewnętrzna molowa
kmol
kJ
U
µ
⋅
⋅
=
⇒
=
⋅
⇒
⋅
⋅
⋅
=
kmol
kJ
T
i
B
U
B
N
k
kmol
kJ
T
i
N
k
U
2
1
2
1
µ
µ
gdzie: k-stała Boltzmana, N-liczba Awogadra, i-liczba stopni swobody, T-temp. bezwzględna
⋅
=
kmol
kJ
u
U
µ
µ
gdzie u-energia wewnętrzna właściwa,
µ
-masa cząsteczkowa
T
i
B
u
⋅
⋅
=
⋅
2
1
µ
Molowe ciepło właściwe przy stałej objętości
⋅
⋅
=
K
kmol
kJ
i
B
c
v
2
1
µ
Molowe ciepło właściwe przy stałym ciśnieniu
)
2
(
2
1
+
⋅
=
⇒
⋅
+
=
i
B
c
K
kmol
kJ
c
B
c
p
v
p
µ
µ
µ
Określenie [i] dla gazów
Rodzaj gazu
liczba st. swobody
przykład gazu
gaz jednoatomowy
3
gaz 2- atomowy
5
O
2
, N
2
gaz 3-atomowy
CO
2
– 6
pozostałe 7
CO
2
H
2
0, CH
4
Obliczanie ciepła właściwego przy V= const
masowe
⋅
⋅
=
=
K
kg
kJ
i
B
c
c
v
v
µ
µ
µ
2
1
objętościowe
⋅
⋅
=
=
K
m
kJ
i
B
V
c
C
m
v
v
3
42
,
22
2
1
µ
Obliczanie ciepła właściwego przy p= const
masowe
⋅
+
⋅
=
=
K
kg
kJ
i
B
c
c
p
p
µ
µ
µ
)
2
(
2
1
objętościowe
⋅
+
⋅
=
=
K
m
kJ
i
B
V
c
C
m
p
vp
3
42
,
22
)
2
(
2
1
µ
Obliczanie ciepła właściwego mieszanin gazowych
∑
⋅
⋅
=
K
kg
kJ
c
g
c
i
i
m
∑
⋅
⋅
=
K
m
kJ
C
r
C
i
i
m
3
∑
⋅
=
3
m
kg
r
i
i
m
ρ
ρ
∑
⋅
=
i
i
m
V
g
V
∑
⋅
=
i
i
m
R
g
R
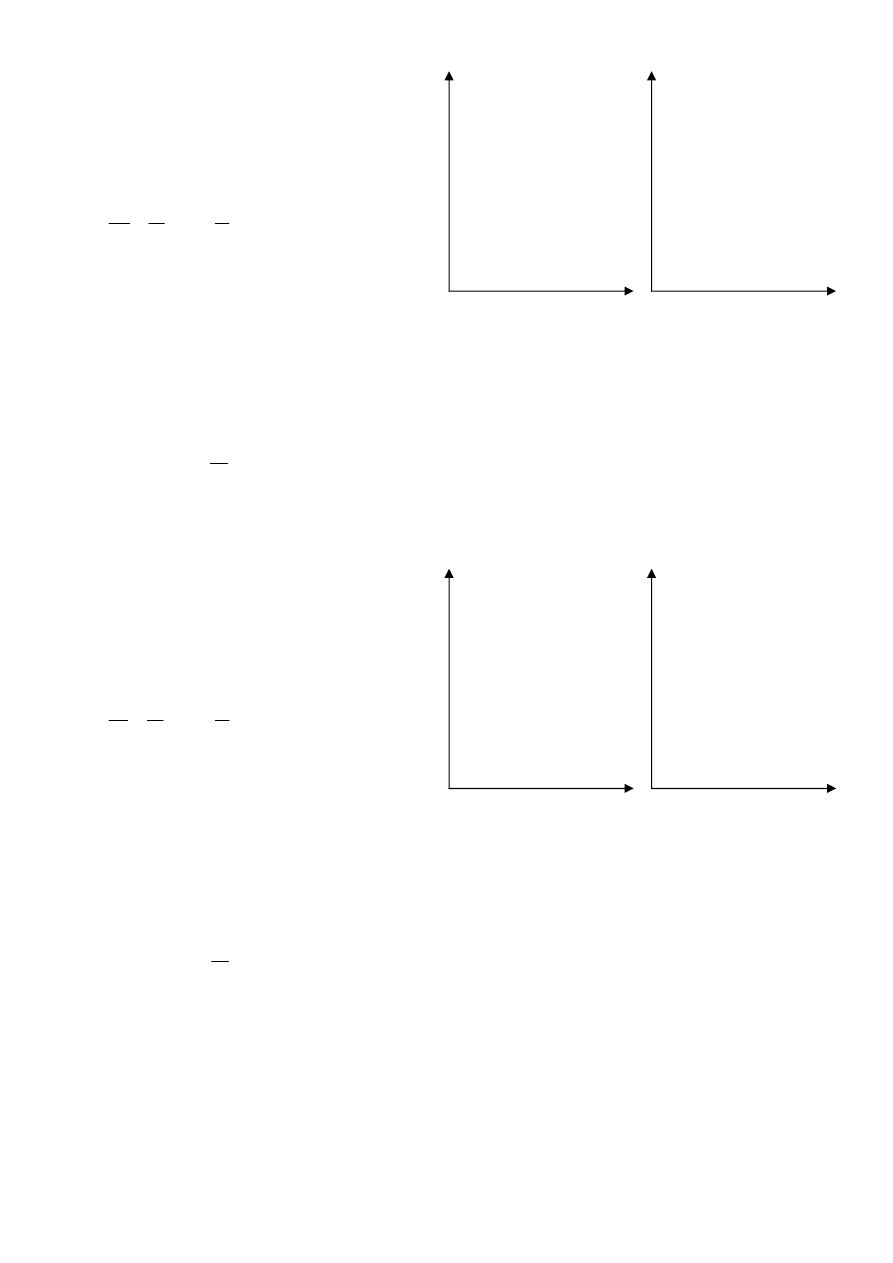
Przemiana izochoryczna
v=const
dv=0
1
1
RT
v
p
=
⋅
2
2
RT
v
p
=
⋅
1
1
2
1
T
T
p
p
=
const
T
p
=
Zmiana energii wewnętrznej
)
(
1
2
2
1
1
2
T
T
c
dT
c
u
u
v
v
−
⋅
=
⋅
=
−
∫
Zmiana entalpii właściwej
Praca rzeczywista
)
(
1
2
2
1
1
2
T
T
c
dT
c
h
h
p
p
−
⋅
=
⋅
=
−
∫
0
0
2
1
=
→
=
⇒
⋅
=
−
dv
bo
l
dv
p
dl
Zmiana entropii
Praca techniczna
1
2
1
2
ln
T
T
c
s
s
v
⋅
=
−
)
(
)
(
2
1
1
2
2
1
p
p
V
p
p
V
dl
T
−
⋅
=
−
⋅
−
=
−
Ciepło wymienione między układem a otoczeniem w czasie przemiany
1
2
2
1
u
u
q
dT
c
pdv
dT
c
dq
dl
du
dq
v
v
−
=
⇔
⋅
=
+
⋅
=
⇒
+
=
−
Przemiana izobaryczna
p=const
dp=0
1
1
RT
V
p
=
⋅
2
2
RT
V
p
=
⋅
1
1
2
1
T
T
V
V
=
const
T
V
=
Zmiana energii wewnętrznej
)
(
1
2
2
1
1
2
T
T
c
dT
c
u
u
v
v
−
⋅
=
⋅
=
−
∫
Zmiana entalpii właściwej
Praca rzeczywista
)
(
1
2
2
1
1
2
T
T
c
dT
c
h
h
p
p
−
⋅
=
⋅
=
−
∫
)
(
1
2
V
V
p
dv
p
dl
−
=
⋅
=
Zmiana entropii
Praca techniczna
1
2
1
2
ln
T
T
c
s
s
p
⋅
=
−
0
2
1
2
1
=
⇒
=
⇒
⋅
=
−
−
T
T
dl
O
dp
dp
V
dl
Ciepło wymienione między układem a otoczeniem w czasie przemiany
)
(
1
2
2
1
T
T
c
q
dh
dq
dl
dh
dq
p
T
−
=
⇔
=
⇒
+
=
−
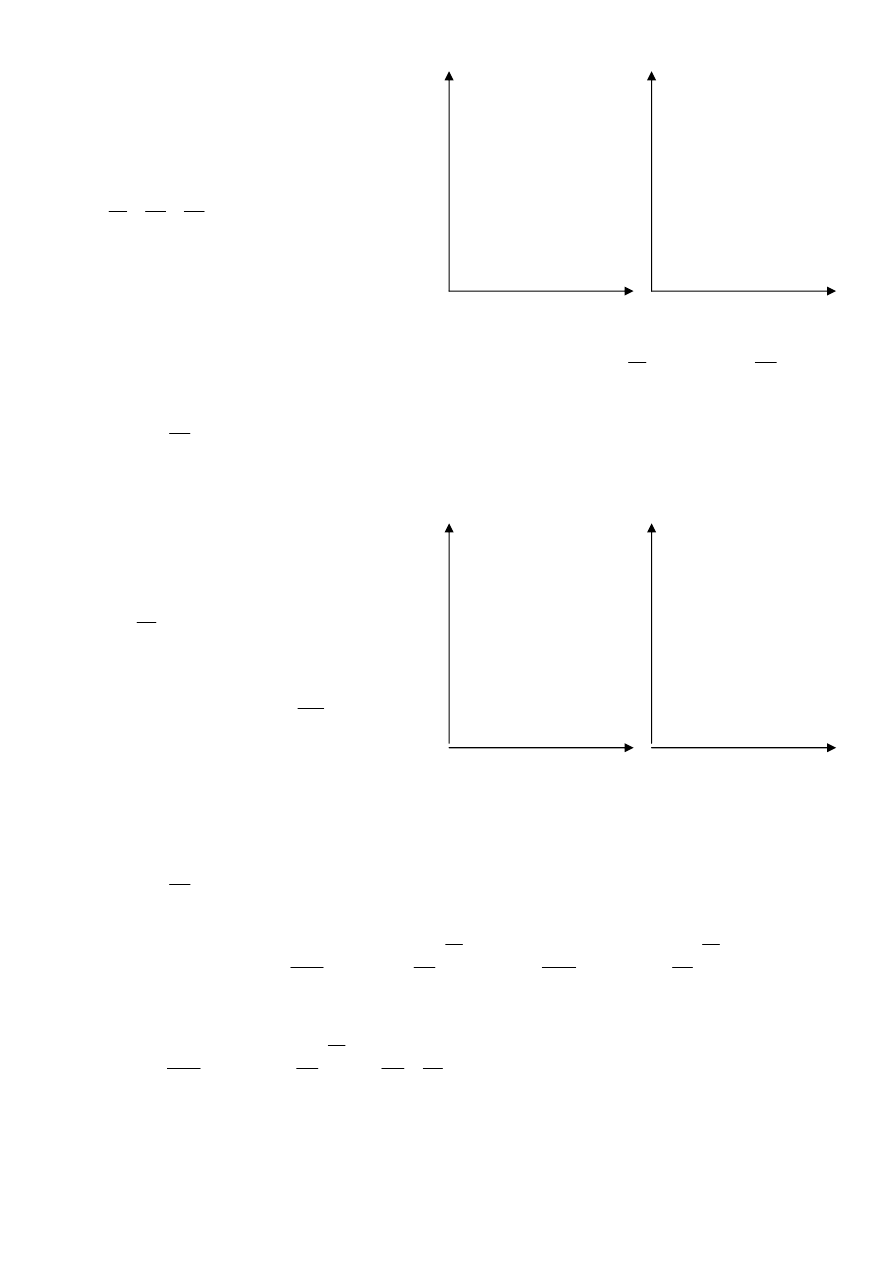
Przemiana izotermiczna
T=const
dT=0
RT
V
p
=
⋅
1
1
RT
V
p
=
⋅
2
2
2
1
2
1
2
1
ρ
ρ
=
=
p
p
V
V
const
v
p
=
⋅
Zmiana energii wewnętrznej
⇒
=
⋅
=
−
∫
0
2
1
1
2
dT
c
u
u
v
nie ma zmiany energii
Zmiana entalpii właściwej
Praca rzeczywista
⇒
=
⋅
=
−
∫
0
2
1
1
2
dT
c
h
h
p
nie ma zmiany entalpii
1
2
ln
V
V
T
R
dv
p
dl
⋅
⋅
=
⋅
=
i
2
1
ln
p
p
T
R
dl
⋅
⋅
=
Zmiana entropii
Praca techniczna
)
(
1
2
2
1
1
2
s
s
T
q
ds
T
dq
T
dq
s
s
−
⋅
=
⇒
⋅
=
⇒
=
−
−
dl
dl
T
=
−
2
1
Ciepło wymienione między układem a otoczeniem w czasie przemiany
T
dl
dl
dq
=
=
Przemiana adiabatyczna
const
V
p
k
=
⋅
v
p
c
c
k
=
k
k
V
p
V
p
2
2
1
1
⋅
=
⋅
const
pV
k
=
const
p
RT
p
k
=
⋅
const
T
p
k
k
=
⋅
−
1
Zmiana energii wewnętrznej
Zmiana entalpii właściwej
)
(
1
2
2
1
1
2
T
T
c
dT
c
u
u
v
v
−
⋅
=
⋅
=
−
∫
Zmiana entropii
Ciepło wymienione między układem a otoczeniem w czasie przemiany
0
1
2
=
=
−
T
dq
s
s
0
=
dq
Praca rzeczywista
−
⋅
⋅
⋅
−
=
−
⋅
=
−
=
−
k
k
v
p
p
T
R
k
T
T
c
du
dl
1
1
2
1
2
1
1
1
1
)
(
lub
−
⋅
⋅
⋅
−
=
−
k
k
p
p
V
p
k
dl
1
1
2
1
1
1
1
1
Praca Techniczna
dl
k
dl
k
c
c
dl
dl
p
p
V
p
k
k
dl
T
v
p
t
k
k
T
⋅
=
⇒
=
=
⇒
−
⋅
⋅
⋅
−
=
−
−
−
2
1
1
1
2
1
1
2
1
1
1

Przemiana politropowa
const
V
p
n
=
⋅
v
p
c
C
c
C
n
−
−
=
n
n
V
p
V
p
2
2
1
1
⋅
=
⋅
const
pV
n
=
const
p
RT
p
n
=
⋅
const
T
p
k
k
=
⋅
−
1
n
n
p
p
T
T
1
1
2
1
2
−
=
Zmiana energii wewnętrznej
Zmiana entalpii właściwej
)
(
1
2
2
1
1
2
T
T
c
dT
c
u
u
v
v
−
⋅
=
⋅
=
−
∫
Zmiana entropii
Ciepło wymienione między układem a otoczeniem w czasie przemiany
1
2
1
2
ln
T
T
c
T
dT
c
s
s
⋅
=
⋅
=
−
0
=
dq
Praca rzeczywista
−
⋅
⋅
⋅
−
=
−
⋅
=
−
=
−
n
n
v
p
p
T
R
n
T
T
c
du
dl
1
1
2
1
2
1
1
1
1
)
(
lub
−
⋅
⋅
⋅
−
=
−
n
n
p
p
V
p
n
dl
1
1
2
1
1
1
1
1
Praca Techniczna
−
⋅
⋅
⋅
−
=
−
−
n
n
T
p
p
V
p
n
n
dl
1
1
2
1
1
2
1
1
1
Moc teoretyczna dla każdej z przemian
2
1
−
⋅
=
T
t
l
m
N
gdzie m-strumień masy
s
kg
Obieg Carnota
Sprawność cieplna
q
q
q
i
0
−
=
η
q-il. ciepła dopr. ze źródła górnego
q
0
-il. ciepła odpr. z układu do źr. dolnego
T
T
T
s
s
T
s
s
T
s
s
T
q
q
q
s
s
s
s
s
s
T
s
s
T
s
s
T
q
s
s
T
q
i
0
1
2
1
2
0
1
2
0
1
4
2
3
1
2
0
4
3
0
3
4
0
0
1
2
)
(
)
(
)
(
)
(
)
(
)
(
)
(
−
=
−
⋅
−
⋅
−
−
⋅
=
−
=
=
∩
=
−
=
−
=
−
−
=
−
=
η

Procesy spalania paliw w kotłach
Każde paliwo musi być znane pod względem składu chemicznego, czyli udziałów:
c-węgla, h-wodoru pierwiastkowego, s-siarki, n-azotu (rzadko występuje),o-tlenu, w-wody związanej,
A-części niepalne.
∑ musi się równać 1kg.
−
r
i
Q
wartość opałowa, il. ciepła z 1kg masy, B - strumień paliwa doprowadzonego
s
kg
h
kg
lub
−
p
V
strumień objętości powietrza doprowadzonego do komory spalania
( )
−
t
v
L
objętościowe teoretyczne zapotrzebowanie powietrza,
λ
λ
λ
λ- współczynnik nadmiaru powietrza
Zapotrzebowanie tlenu do spalania
Na 1 kg C przypada
3
8
12
32
=
kg O
2
Na 1 kg H
2
przypada
8
4
32
=
kg O
2
Na 1 kg S przypada 1 kg O
2
Teoretyczne zapotrzebowanie na tlen
Teoretyczne objętościowe zapotrzebowanie na tlen
( )
−
+
+
=
kgpal
kgO
o
s
h
c
O
t
m
2
8
3
8
( )
( )
( )
( )
⋅
=
⋅
=
⋅
=
kgpal
O
m
O
O
V
O
V
O
t
m
t
m
O
m
t
m
O
t
V
2
3
32
4
,
22
2
2
µ
Ponieważ źródłem tlenu jest powietrze zatem teoretyczne obj. zapotrzebowanie powietrza wynosi
( ) ( )
( )
⋅
⋅
=
=
kgpal
pow
m
O
O
L
t
m
t
v
t
v
.
32
21
,
0
4
,
22
21
,
0
3
Rzeczywistą ilość powietrza do spalania określa współczynnik nadmiaru powietrza
( )
( )
t
v
rz
v
L
L
=
λ
Określa się go ze wzorów
1.) Przy zupełnym spalaniu paliwa w spalinach nie ma CO
n
o
79
21
21
−
=
λ
przy zupełnym spalaniu skład spalin jest następujący b+o+n=100%
2.) Przy niezupełnym spalaniu – w spalinach jest CO
n
t
o
5
,
0
79
21
21
−
−
=
λ
przy czym skład spalin jest następujący b+t+o+n=100%
b - udział obj. CO
2
i SO
2
w spalinach suchych lub wartość w %
t – udział obj. CO w spalinach suchych lub wartość w %
o– udział obj. O
2
w spalinach suchych lub wartość w %
n– udział obj. azotu w spalinach suchych lub wartość w %
Przy niezupełnym spalaniu skład spalin mokrych będzie wynosił
%
100
2
=
+
+
+
+
O
H
r
n
o
t
b
O
H
r
2
-udział pary wodnej w spalinach w %
Rzeczywiste obj. zapotrzebowanie powietrza
( )
( )
t
v
rz
v
L
L
⋅
=
λ
Strumień objętości pow. doprowadzonego do komory paleniskowej
( )
( )
rz
v
t
v
p
L
B
s
pow
m
L
B
V
⋅
=
⋅
⋅
=
•
3
λ
Strumień objętości spalin
[
]
2
3
12
42
,
22
2
CO
CO
um
c
V
CO
∩
⋅
=
,
[
]
SO
um
s
V
SO
3
32
42
,
22
⋅
=
,
[
]
x
NO
NO
um
n
V
x
3
28
42
,
22
⋅
=
[
]
O
H
um
w
h
V
O
H
2
3
)
9
(
18
42
,
22
2
+
⋅
=

Spalanie przy λ=1
( )
+
+
⋅
+
⋅
+
⋅
+
⋅
=
.
.
.
.
79
,
0
)
9
(
18
42
,
22
28
42
,
22
32
42
,
22
12
42
,
22
3
pal
kg
sp
um
L
w
h
n
s
c
Vs
t
v
Spalanie przy λ>1 (nadmiar powietrza)
( )
(
) ( )
⋅
−
⋅
+
⋅
⋅
+
+
⋅
+
⋅
+
⋅
+
⋅
=
.
.
.
.
1
21
,
0
79
,
0
)
9
(
18
42
,
22
28
42
,
22
32
42
,
22
12
42
,
22
3
pal
kg
sp
um
L
L
w
h
n
s
c
Vs
t
v
t
v
λ
λ
Strumień objętości spalin wypływających z kotła
⋅
=
•
h
sp
um
V
B
V
s
sp
.
3
gdzie: B – strumień paliwa doprowadzonego do kotła
(
)
(
)
u
r
k
w
w
w
w
u
r
w
w
w
w
k
H
t
t
c
m
B
H
B
t
t
c
m
⋅
−
⋅
⋅
=
⇒
⋅
−
⋅
⋅
=
η
η
2
1
2
1
gdzie:
k
η
- sprawność kotła,
u
r
H
- wartość
opałowa w warunkach roboczych,
=
kgK
kJ
c
w
19
,
4
- średnie ciepło właściwe wody,
w
m
-ilość
podgrzewanej wody (strumień),
2
1
w
w
t
t
∩
- parametry wody podgrzewanej przez kocioł.
+
⋅
⋅
−
=
kg
kJ
w
h
r
H
H
o
r
u
r
)
9
(
gdzie: r- ciepło parowania z tablic 2500
kg
kJ
,
o
r
H
-ciepło spalania w warunkach roboczych.
Bilans cieplny kotłów opalanych paliwem stałym:
∑
+
=
.
str
u
p
Q
Q
Q
gdzie:
p
Q
-moc dostarczona z paliwem,
u
Q
-użyteczna moc cieplna,
str
Q
-ciepło strat mocy cieplnej
[ ]
kW
H
B
Q
r
u
p
⋅
=
u
Q
- dla kotłów wodnych
(
)
[ ]
kW
t
t
c
m
Q
w
w
w
w
u
2
1
−
⋅
⋅
=
⇒
u
Q
- dla kotłów parowych
(
)
[ ]
kW
t
c
i
D
Q
w
w
p
u
2
⋅
−
⋅
=
⇒
gdzie: D- strumień masy pary wypływ. z kotła,
p
i
- entalpia pary,
2
w
w
t
c
⋅
- entalpia wody przed kotłem
Sprawność cieplna kotła:
p
u
k
Q
Q
=
η
, spr. kotłów wodnych:
(
)
r
u
w
w
w
w
k
H
B
t
t
c
m
⋅
−
⋅
⋅
=
2
1
η
, spr. kotłów parowych
(
)
r
u
w
w
p
k
H
B
t
c
i
D
⋅
⋅
−
⋅
=
2
η
Obliczanie wysokości komina:
(
)
[ ]
(
)
[ ]
m
g
p
h
Pa
g
h
p
rz
s
rz
p
s
rz
s
rz
p
s
ρ
ρ
ρ
ρ
−
⋅
∆
=
⇒
−
⋅
⋅
=
∆
gdzie: h- wysokość komina (od śr. komory paleniskowej), g- przyspieszenie ziemskie 9,81 [m/s
2
]
rz
p
ρ
- gęst. powietrza w war. rzecz.,
rz
s
ρ
- gęst. spalin w war. rzecz., ∆p
s
– podciśnienie spalin [Pa]
=
=
=
3
29
,
1
42
,
22
87
,
28
m
kg
V
m
p
u
p
µ
ρ
przeliczenie na war. rzeczywiste
rz
rz
rz
u
u
u
T
p
T
p
ρ
ρ
⋅
=
⋅
ponieważ:
ρ
1
=
V
s
O
H
O
H
s
O
O
s
N
N
s
SO
So
s
CO
co
i
i
u
s
V
V
r
V
V
r
V
V
r
V
V
r
V
V
r
r
2
2
2
2
2
2
2
2
2
2
,
,
,
,
=
=
=
=
=
⇒
⋅
=
∑
ρ
ρ
m
O
H
O
H
m
CO
CO
m
O
O
m
N
N
m
SO
SO
m
CO
CO
u
s
V
r
V
r
V
r
V
r
V
r
V
r
2
2
2
2
2
2
2
2
2
2
2
2
µ
µ
µ
µ
µ
µ
ρ
⋅
+
⋅
+
⋅
+
⋅
+
⋅
+
⋅
=
Wyszukiwarka
Podobne podstrony:
Egzamin, TC Termodynamika wzory
Tresc zadan z egzaminu z cwiczen z Termodynamiki
egzamin z TC 2, elektro, 1, Podstawy Techniki Mikroprocesorowej
termodynamika Wzory do teorii z przeplywow plynow scisliwych, Wzory z przepływów płynów ściśliwych
grk egzamin notatki sciaga wzory
termodynamika Wzory do teorii z wymiany ciepla dla USM, Wzory do teorii z podstaw termodynamiki
Egzamin teoretyczny z termodynamiki
Fizyka Termodynamika Wzory ciesiolek
WZORY SiEwFiR EGZAMIN
wzory egzamin
wzory egzamin FINANSE PRZEDSI c4 98BIORSTW
matematyka wzory na 1 egzamin
wzory egzamin
Termodynamika egzamin [1]
Wzory do teorii z podstaw termodynamiki
termaiii, Termodynamika III. Egzamin - zadania. 08.02.2006, Termodynamika III
więcej podobnych podstron