3. Swoista odpowiedź immunologiczna cz.1
Antygen: pełnowartościowy, hapten; autologiczny, izogeniczny (syngeniczny), allogeniczny,
ksenogeniczny; antygeny MHC (HLA), antygeny reagujące krzyżowo (heterofilne); alergen,
tolerogen. Determinanty antygenowe (epitopy), immunogenność (antygenowość), swoistość,
immunogenność a budowa chemiczna antygenu i wielkość cząsteczki; antygeny T-zależne i T-
niezależne, superantygeny.
Główne etapy swoistej odpowiedzi immunologicznej: faza indukcyjna (rozpoznanie antygenu), faza
centralna (aktywacja, proliferacja - selekcja klonalna i różnicowanie zaangażowanych komórek w
limfocyty efektorowe), faza efektorowa (eliminacja antygenu przy współdziałaniu różnych
mechanizmów i komórek). Pamięć i tolerancja immunologiczna.
Limfocyty: subpopulacje: B (B1, B2), T (Th1, Th2, Ts, Tc), NK, NS, antygeny różnicowania (CD) i
inne receptory (B – Ig, T – TCR), krążenie limfocytów
Prezentacja antygenu: komórki prezentujące antygen (APC), przetworzenie antygenu.
Swoista odpowiedź komórkowa: typu cytotoksycznego - rozpoznanie antygenu (T CD8 – restrykcja
MHC kl. I), mechanizmy cytotoksyczności; typu późnego – rozpoznanie antygenu (Th – MHC kl.
II), faza efektorowa (aktywowany makrofag). Udział cytokin (interleukiny, IFN- ).
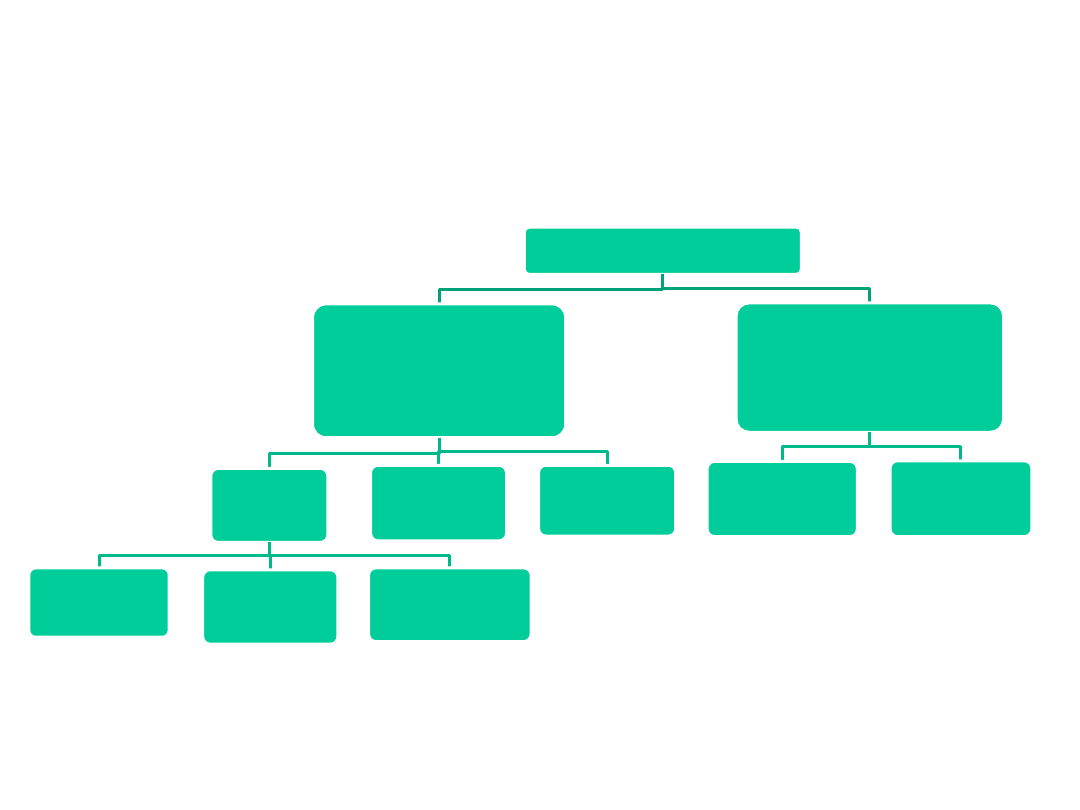
IMMUNE SYSTEM
Innate
(Nonspecific)
1 line of defense
Anatomical
barriers
mechanical
factors
Chemical
factors
Biological
factors
Cellular
components
Humoral
components
Adaptive
(Specific)
2 line of defense
Protects / re-exposure
Cellular
components
Humoral
components
Układ odpornościowy

Wrodzona - nabyta odporność
wrodzona (nieswoista)
od urodzenia
nabyta (swoista)
powstaje latami
reakcja natychmiastowa
wymaga czasu pomiędzy ekspozycją
a odpowiedzią
nieswoista antygenowo
nieswoista, jednakowa reakcja dla różnych
patogenów i obcych
antygenowo swoista
odpowiedź wysoce swoista
pamięć nie powstaje
powstaje pamięć dla antygenu
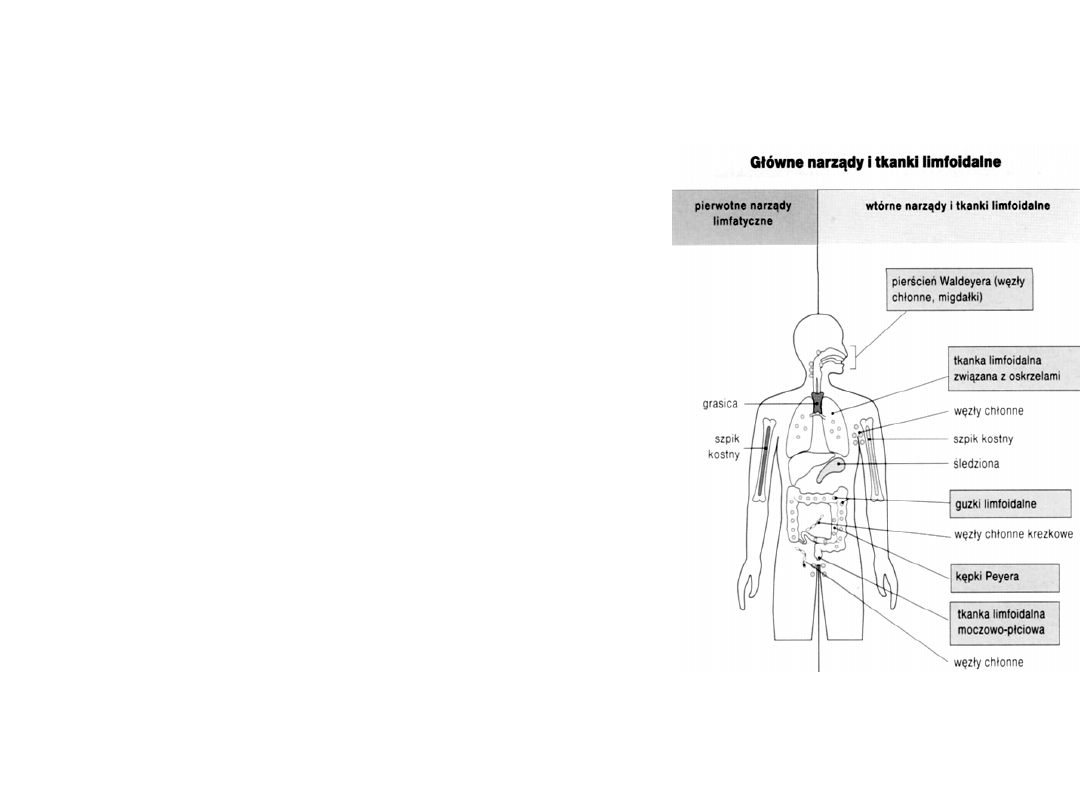
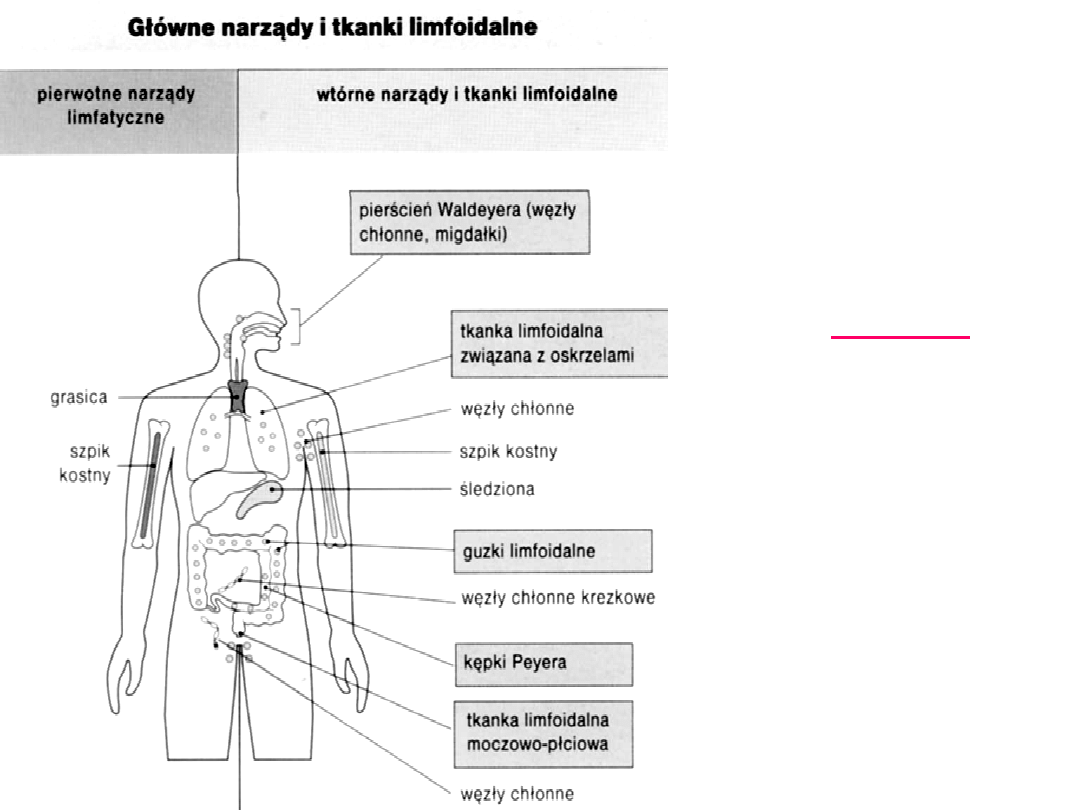
Budowa układu limfatycznego
(1-2% masy ciała)
• narządy pierwotne (centralne):
* grasica
–
rozwój i dojrzewanie limfocytów T,
selekcja limfocytów pod względem tolerancji na
autoantygeny
* szpik kostny
–
rozwój i dojrzewanie limfocytów B
• narządy wtórne (obwodowe)
:
zasiedlanie przez dojrzałe T i B, kooperacja T i B z
antygenem, współdziałanie z fagocytami i komórkami
pomocniczymi
* śledziona
–
rozpoznanie antygenów
krwiopochodnych
* węzły chłonne
–
antygeny krążące w chłonce
absorbowane przez skórę, trzewia
* tkanki „śluzówkowe”-
MALT (GALT, BALT),
SALT, kępki Peyera.. – antygeny, które przekroczyły
bariery powierzchniowe
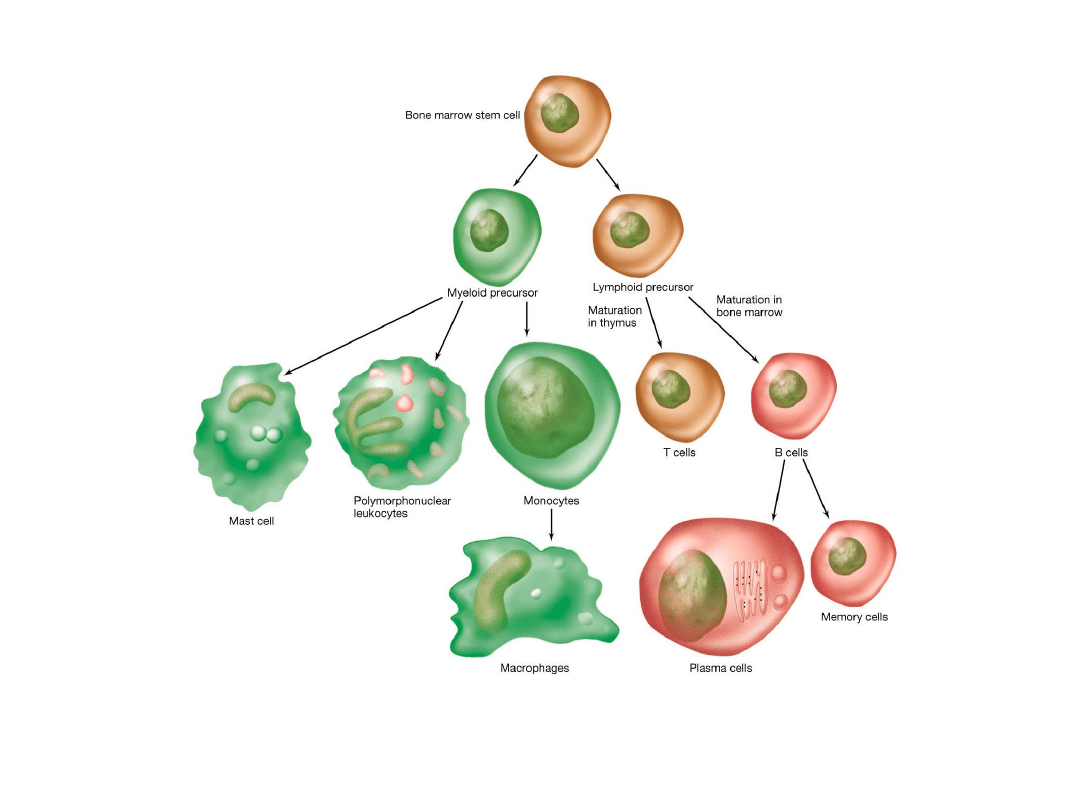
Podstawowe komórki –
limfocyty:
pochodzą z komórek macierzystych
narządów pierwotnych,
krążą we wtórnych,
specyficznie rozpoznają antygeny
poprzez odpowiednie receptory
limfocyty nie posiadają stałej
lokalizacji – stale krążą
krążenie limfocytów między
narządami wtórnymi poprzez
krew i chłonkę umożliwia kontakt
antygenu z dużą liczbą limfocytów

Antygen
–
każda cząsteczka
rozpoznawana przez limfocyty T lub
B: bakteria, wirus, pasożyt..., komórka nowotworowa,
przeszczepu, pyłek, związek chemiczny
Epitop
– pojedyncza determinanta antygenu, łączy się z paratopem przeciwciała,
na jednej cząsteczce antygenu może znajdować się wiele epitopów
Cechy antygenu
:
• Immunogenność
– zdolność wywołania odpowiedzi komórkowej
lub humoralnej
• Swoistość
– zdolność przeciwciał lub uczulonych limfocytów do
selektywnego reagowania z epitopem antygenu, który wywołał
odpowiedź
Hapten
–
może łączyć się z przeciwciałem, ale nie może go wytworzyć, o ile
nie połączy się z białkiem (nośnik immunogenności) – kwasy nukleinowe,
lipidy, chrom, nikiel, leki (penicylina
)

Antygeny
Antygen T (grasiczo) - zależny
–
wymaga rozpoznania przez limfocyty B i T celem
wytworzenia przeciwciał – większość antygenów, głównie białkowe
w efekcie powstaje odpowiedź humoralna i komórkowa
Antygen T-niezależny
–
wystarczy rozpoznanie przez limfocyty B, głównie
polisacharydy, np. otoczka S.pneumoniae, H.influenzae, N.miningitidis
powstają tylko przeciwciała, nie ma odpowiedzi komórkowej
Antygen heterofilny
–
wspólne epitopy występują w różnych cząsteczkach, np. w
krwince i bakterii,
powstają reakcje krzyżowe
Antygen: homologiczny – heterologiczny
Antygen: autologiczny, syngeniczny, allogeniczny, ksenogeniczny –
przy przeszczepie

Limfocyty
- różne morfologicznie
• T
-
posiadają receptor TCR wiążący antygen
Th 1, Th 2 – pomocnicze (CD4 – koreceptor dla MHC-II), 95% małe limfocyty
Tc – cytotoksyczne (CD8 - MHC-I) – 50% małe limfocyty
Treg – regulatorowe (CD4 ale i CD8, CD25) Ts – supresorowe
• NK
- ok. 70% dużych ziarnistych (CD16, CD56, CD57)
• B
-
receptory immunoglobulinowe
IgM, IgD,
MHC-I,II
, CD19 CD20
CD21.. nieliczne wykazują ekspresję IgG,IgA, IgE
*
posiadają charakterystyczne markery tzw. antygeny różnicowania CD
–cluster of
differentiation > 200
*
warunkują one fenotyp i pełnienie określonej funkcji biologicznej
T – CD2-wiąże krwinki barana CD3- przenosi sygnał
•
wydzielają cytokiny
•
posiadają receptory:
dla cytokin, MHC, Fc (CD16, CD64), C, o cechach integryny
(CD2 - LFA), selektyny (CD62 - E, L, P)
aktywacja T lub B wyzwala dodatkową ekspresję niektórych cząsteczek powierzchniowych
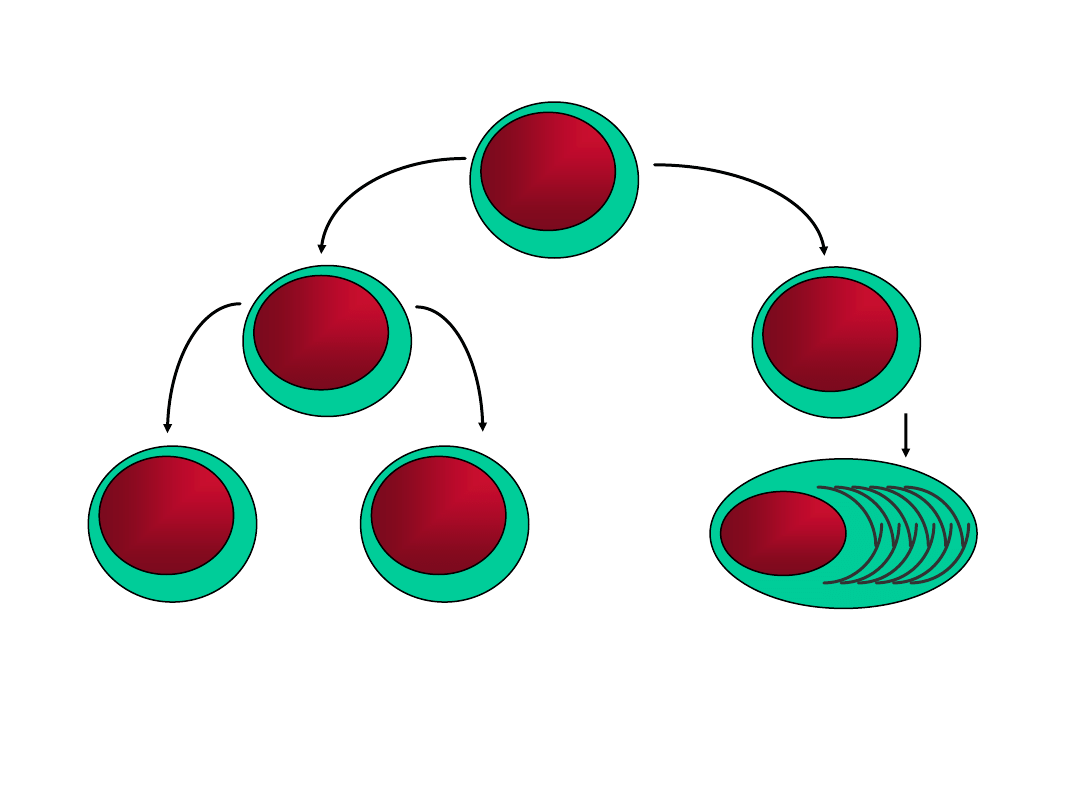
Limfocyty
30-40% populacji leukocytów w krążeniu, różne morfologicznie
i czynnościowo
pomocnicze-helper,
aktywacja B, makrofagów
Th1
Th2
cytotoksyczne: wirus,
n
owotwór, przeszczep
Tc
plazmocyty
– produkcja
przeciwciał
PC
T
B
T 60-70%
B 10-20%
LP
Treg (s)
–
hamują autoreaktywne T i B, aktywację
Th, tolerancja pokarmowa, na przeszczepy
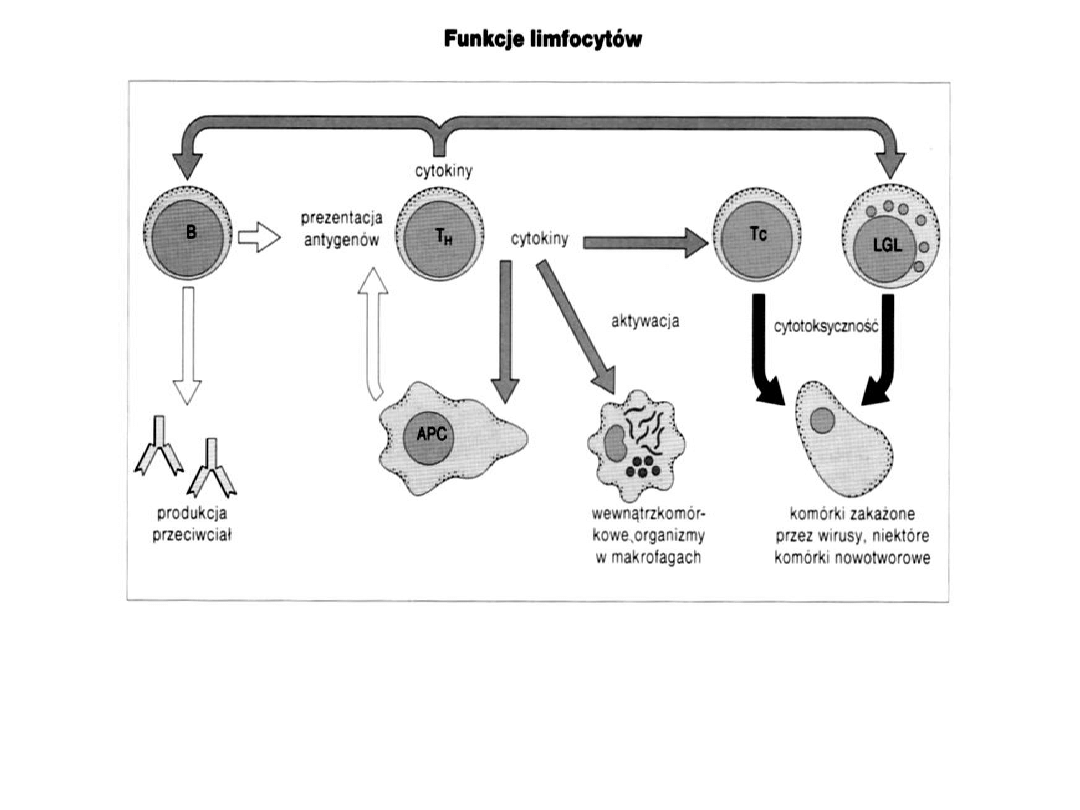
Limfocyty - odpowiedzialne za swoistą odpowiedź immunologiczną – nabytą
*
humoralna – limfocyty B, wytworzenie swoistych przeciwciał
* komórkowa – limfocyty T
,
powstanie „uczulonych” limfocytów
o różnych funkcjach
efektorowych, wytwarzanie cytokin – przenoszą sygnały między komórkami (interferony
- IFN, interleukiny - IL, czynniki stymulujące kolonie - CSF, czynniki martwicy
nowotworu - TNF
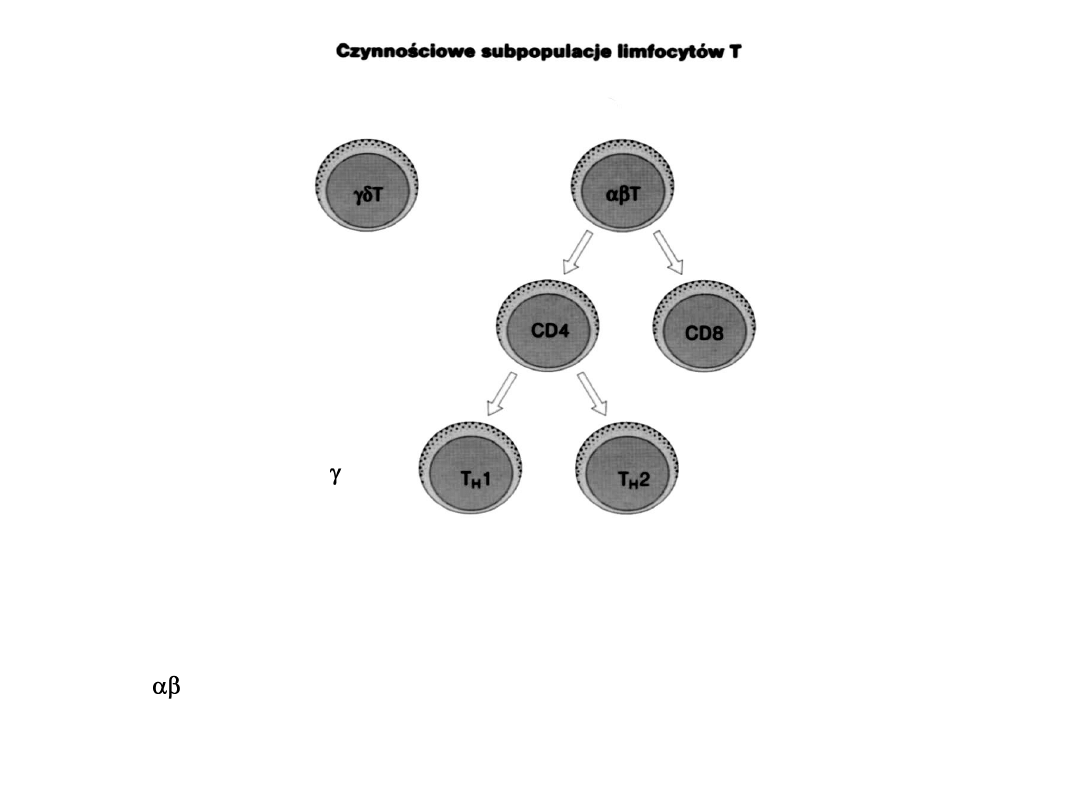
TCR2
90-95%
CD4/8
TCR1
5-10%
większość CD8
Receptor TCR jest rozstrzygającym markerem T
T CD4 rozpoznają antygen z MHC kl.II
T CD8 rozpoznają antygen z MHC kl.I
Stosunek CD4/CD8 – 1,5 – 2,5
T
- do rozpoznania antygenu wymagają sygnału kostymulującego CD28
wiążącego się z ligandem B7-1 (CD80) i B7-2 (CD45) na APC
Il-2,
IL-12,
IFN
,TNFβ
bardziej ↑ komórkową
Il-2, Il-4, Il-5, Il-6, Il-9 Il-10,
Il-13
bardziej
↑
humoralną
MHC kl. II
MHC kl. I
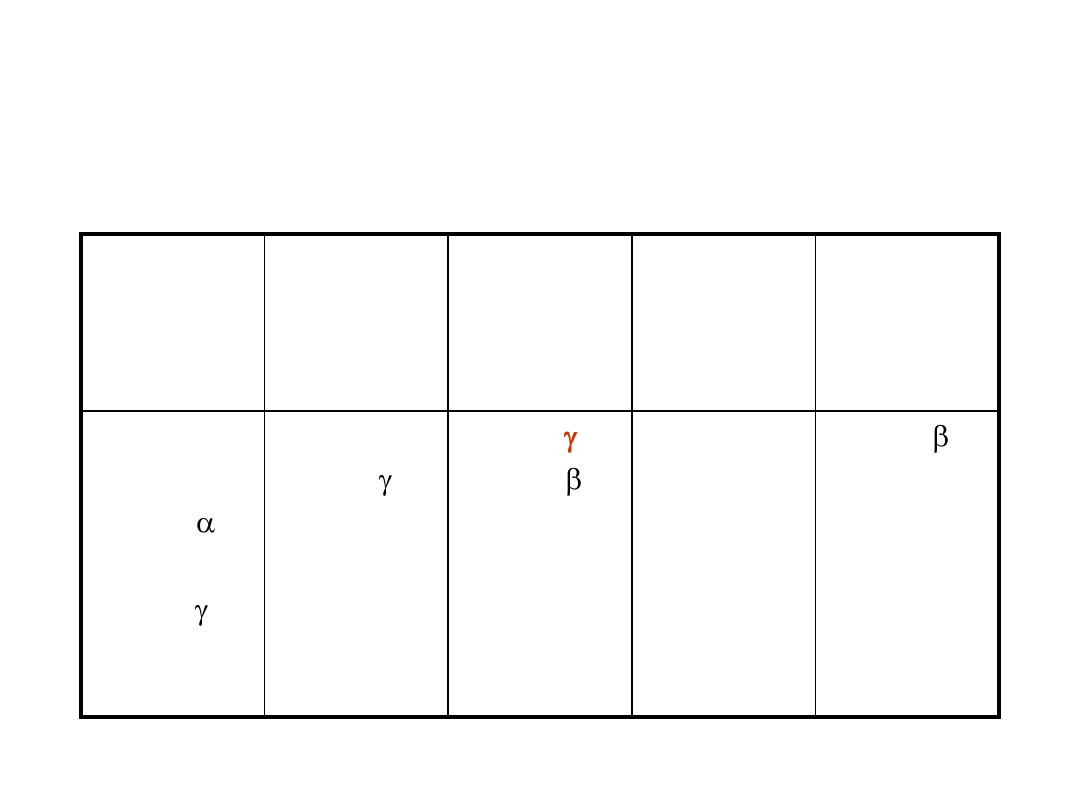
Profil cytokinowy limfocytów T CD4
Thp
prekursorowe,
dziewicze,
różnicują w Th1
lub Th2
Th0
hipotetyczna?
cytokiny Th1 i
Th2
Th1
średnie stężenia
antygenu
Th2
wysokie lub
niskie stężenia
antygenu
Th3
regulatorowe
IL-2
Il-4
TNF-
IL-13
INF-
IL-4
INF-
INF-
TNF-
IL-2
IL-12
IL-2
IL-4
IL-5
IL-6
IL-9
IL-10
IL-13
TGF-

Fazy odpowiedzi immunologicznej:
• indukcyjna
-
rozpoznanie antygenu
przez limfocyt, proliferacja klonu
limfocytów T lub B, T i B swoiście rozpoznających antygen, a właściwie pojedynczy
epitop - tzw.
selekcja klonalna
• efektorowa
–
eliminacja antygenu, patogenu – różne możliwości:
*
neutralizacja
przez swoiste przeciwciała - wirusy, toksyny bakteryjne, enzymy
*
fagocytoza immunologiczna
– opsonizacja bakterii zewnątrzkomórkowych przez
przeciwciała – kooperacja odpowiedzi swoistej z nieswoistą
*
aktywacja makrofagów
przez cytokiny (IFN ) – niszczenie bakterii
wewnątrzkomórkowych, np. prątki gruźlicy
*
reakcje cytotoksyczne
– skierowane przeciwko całym komórkom, zbyt dużym do
sfagocytowania, np. komórki zakażone wirusem, nowotworowe, przeszczepu..
biorą w nich udział TcCD8, aktywowane NK, mechanizm ADCC
*
apoptoza
– komórki cytotoksyczne przekazują sygnał komórce docelowej do
samozniszczenia
• pamięć immunologiczna
–
długo żyjące T i B, posiadające tą samą
swoistość w wiązaniu antygenu

rozpoznanie „nieswoiste” - odporność wrodzona
uniwersalny, selektywny mechanizm reagowania organizmu przed infekcją
•
receptory PRR (pattern recognition receptors) na komórkach rozpoznają
stałe
struktury drobnoustrojów - PAMP (pathogen associated molecular patterns).
•
PRR =
receptory TLR (Toll-podobne)
wykryte w latach 90-tych u muszki
owocowej Drosophila, łączą reakcje nieswoiste ze swoistymi
* na kom. immunologicznie kompetentmych (makrofagi, komórki dendrytyczne,
komórki tuczne, eozynofile, neutrofile, limfocyty B), komórki nabłonkowe jelit,
dróg oddechowych, komórki śródbłonka, fibroblasty, keratynocyty, kardiomiocyty
i adipocyty.
•
pobudzenie receptorów TLR przez produkty drobnoustrojów → sygnał
aktywujący mechanizmy odporności immunologicznej nieswoistej:
* wzmożona synteza czynników przeciwbakteryjnych
* cytokin prozapalnych (TNF-a, IL-1, -6, -8, -12), chemokin, tlenku azotu (NO)
* dojrzewanie komórek dendrytycznych - tracą właściwości pinocytarne,
nabywają cech prezentacji antygenu
* aktywacja APC: wzrost syntezy cytokin prozapalnych, wzrost ekspresji molekuł
adhezyjnych oraz molekuł kostymulujących (CD40, CD80, CD86)
•
indukcja odpowiedzi immunologicznej swoistej (limfocyty T i B)
•
TLR uczestniczą w regulacji odpowiedzi immunologicznej, wpływają bezpośrednio
lub pośrednio na funkcję Treg CD4+CD25+, prowadzą do ich indukcji i
hamowania odpowiedzi immunologicznej lub do zniesienia ich aktywności
supresyjnej (kontrasupresji).

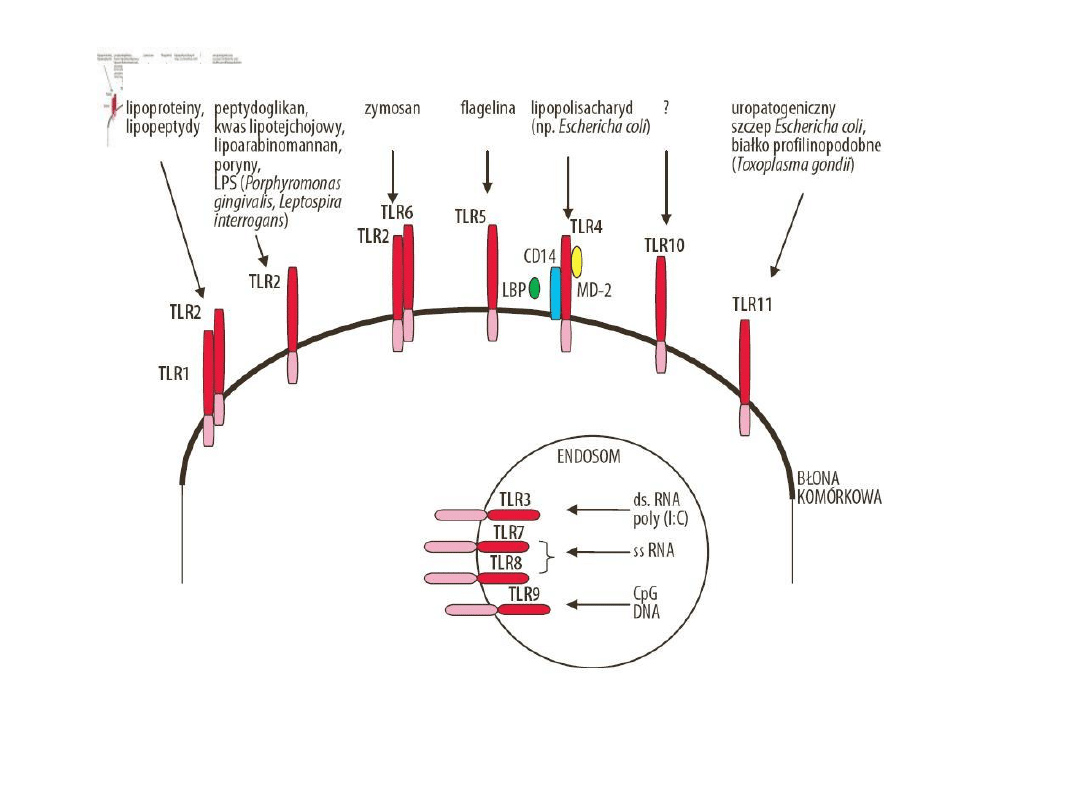
rozpoznają materiał genetyczny
drobnoustrojów, które wcześniej
uległy częściowej
degradacji w lizosomach.
CD14 - monocyty, makrofagi, granulocyty, limofcyty B
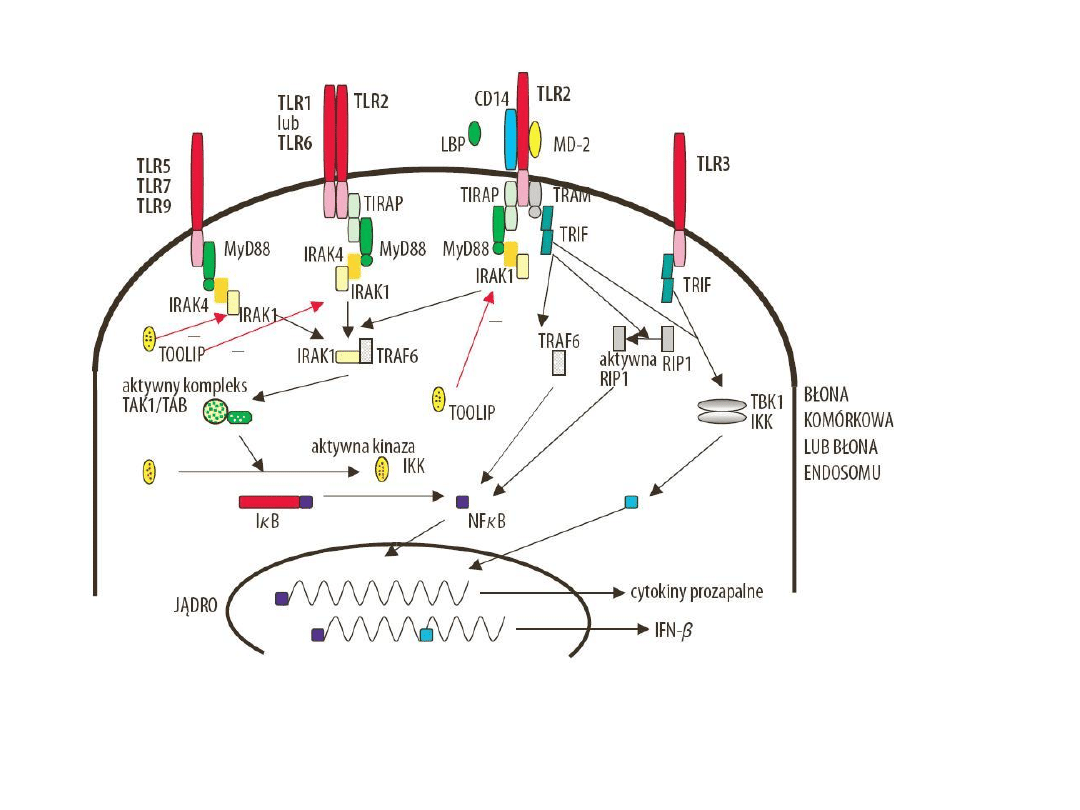

Komórki APC – prezentujące antygen
Antigen Presenting Cells
populacja heterogenna:
w skórze, węzłach chłonnych, śledzionie, grasicy, w
obrębie nabłonka błon śluzowych; linia mieloidalna – CD11c, limfoidalna – CD123;
posiadają różne markery CD (S-100, CD11c, CD50 – niedojrzałe; CD1a, CD80 -
dojrzałe), Fc R i
MHC-II
•
k
omórki Langerhansa –
skóra, prezentują pw. Th1
• komórki splatające się –
grasica
• komórki dendrytyczne grudek –
węzły, śledziona, śluzówka, brak MHC–II
• limfocyty B
– prezentują gł. Th2
• makrofagi –
jako jedyne silnie fagocytują
ale cytokiny typu IFN i TNF mogą indukować ekspresję MHC-II na keratynocytach,
nabłonkach tarczycy,śródbłonkach i tym komórkom umożliwiać prezentację antygenu
choroby autoimmunozacyjne, przedłużony stan zapalny..
rola APC:
wewnątrzkomórkowe przetworzenie antygenu, związanie z antygenami
MHC-II i ekspozycja kompleksu na błonie komórkowej, prezentacja T CD4
prezentacja T CD8 odbywa się przez każdą komórkę – wszystkie posiadają MHC-I
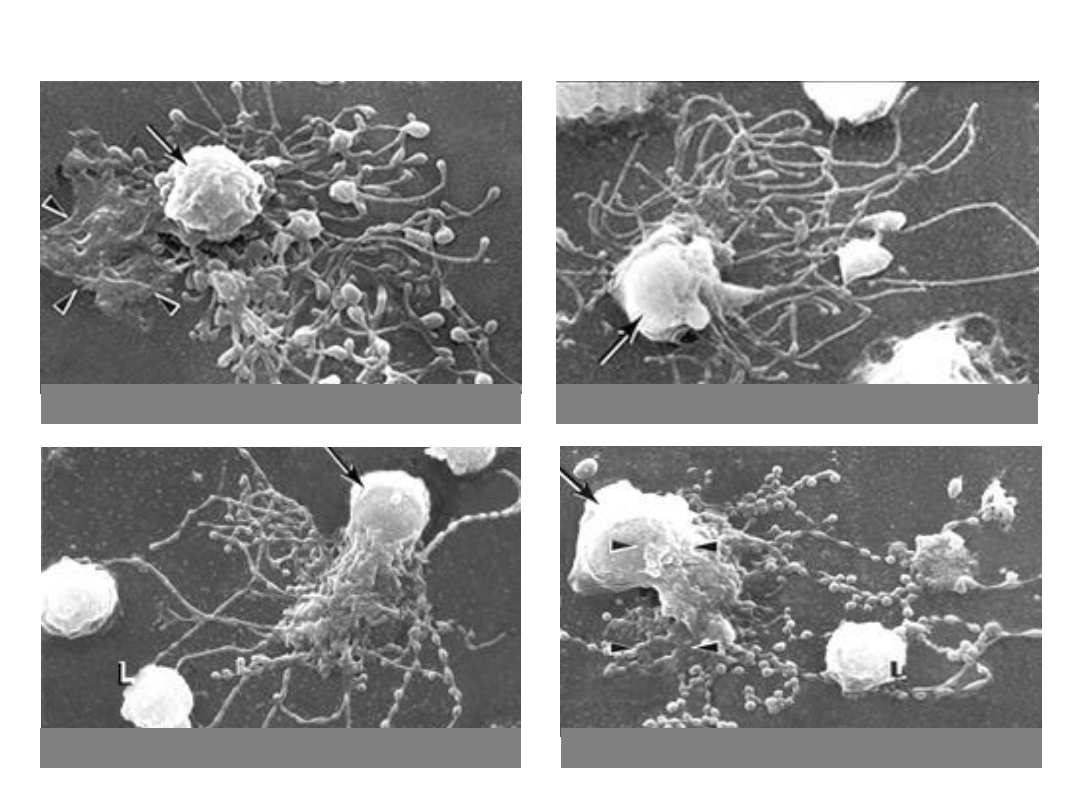
Maturation of Follicular Dendritic cells
Club-shaped tips of developing dendrites
Filiform dendrites
Bead formation on dendrites
Bead formation on dendrites
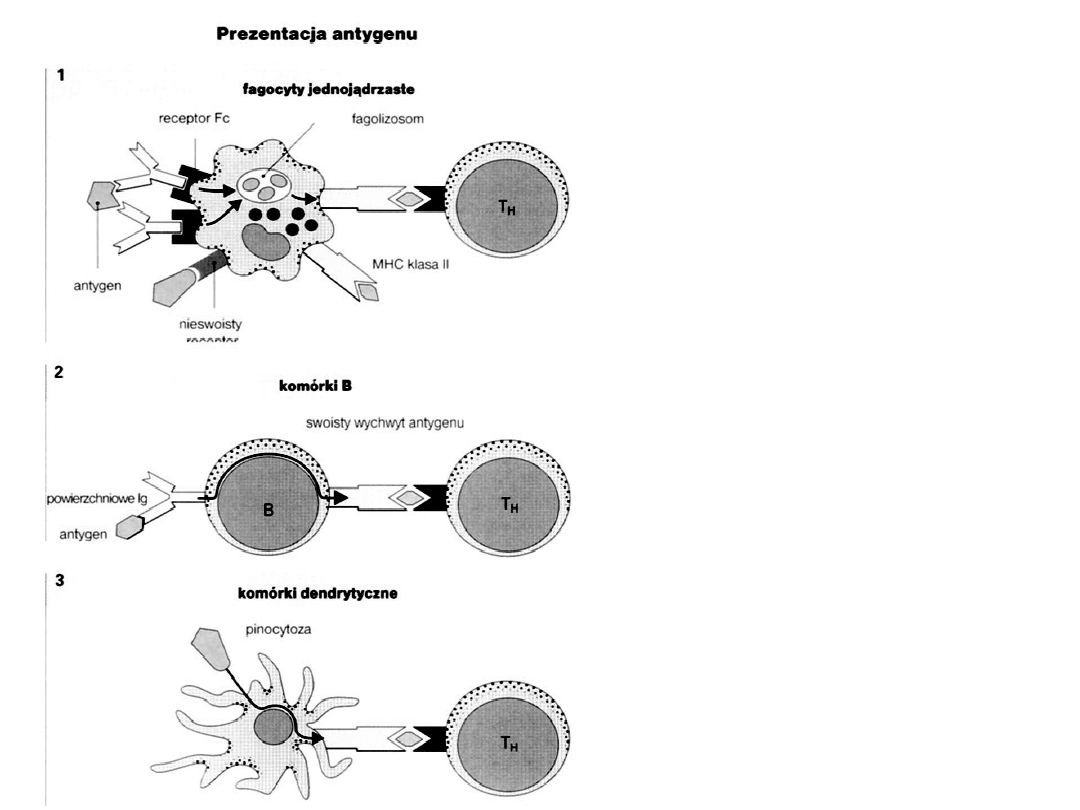
Prezentacja antygenu odbywa się tylko
Th związanym z MHC kl. II
Makrofagi wychwytują antygen
poprzez nieswoiste receptory lub
jako kompleksy immunologiczne
Aktywowane B poprzez Ig powierzchniowe
i prezentują Th
Pobierają antygen drogą pinocytozy
stale mają ekspresję MHC II na
powierzchni
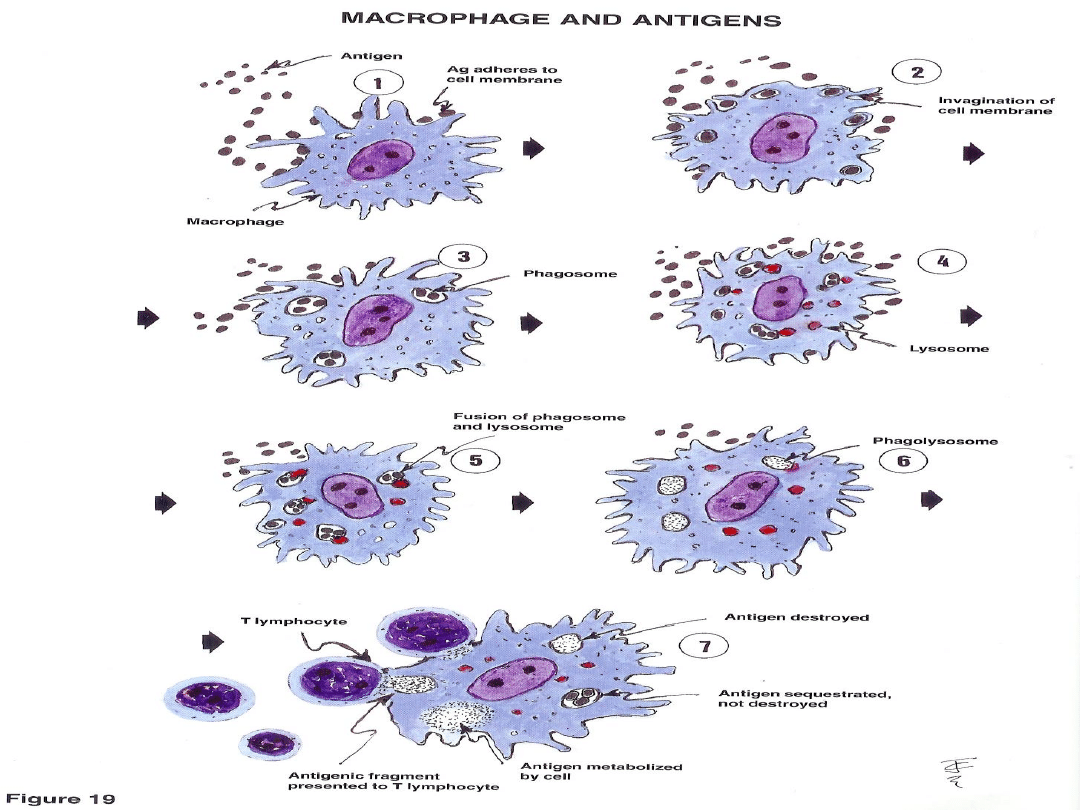

peptydy związane
z powierzchnią
Antygen musi b
yć odpowiednio przetworzony
aby był rozpoznany przez T
Y
T
T cell
odpowiedź
brak
brak
brak
odpowiedzi
brak
rozpuszczalny
natywny Ag
związany z
powierzchnią Ag
rozpuszczalne
peptydy Ag
prezentacja peptydu Ag
przez komórkę z
ekspresją MHC
przetworzenie
antygenu
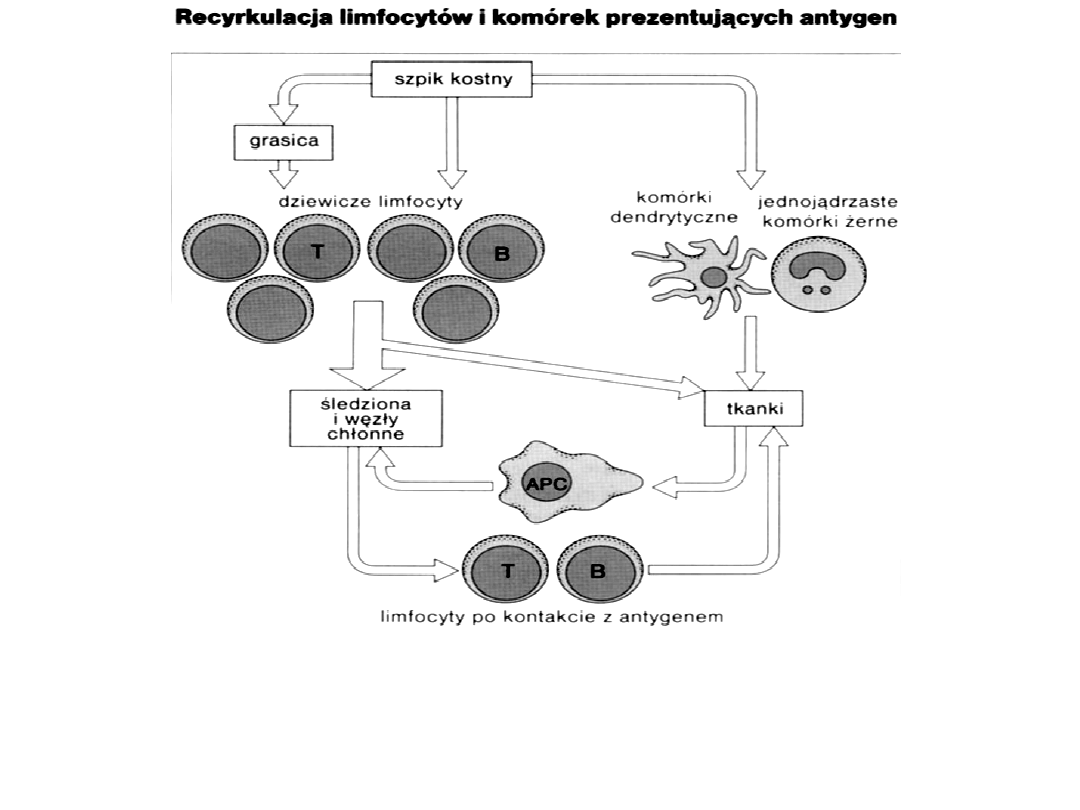
Dziewicze limfocyty z centralnych tkanek limfoidalnych migrują do obwodowych (śledziona,
węzły chłonne). APC pochodzące również z komórki macierzystej szpiku wnikają w tkanki,
Wychwytują antygen i przenoszą do komórek limfoidalnych, gdzie prezentują antygen limfocytom
T i B. Po kontakcie a antygenem limfocyty migrują z tkanek limfoidalnych do miejsca zakażenia
lub zapalenia
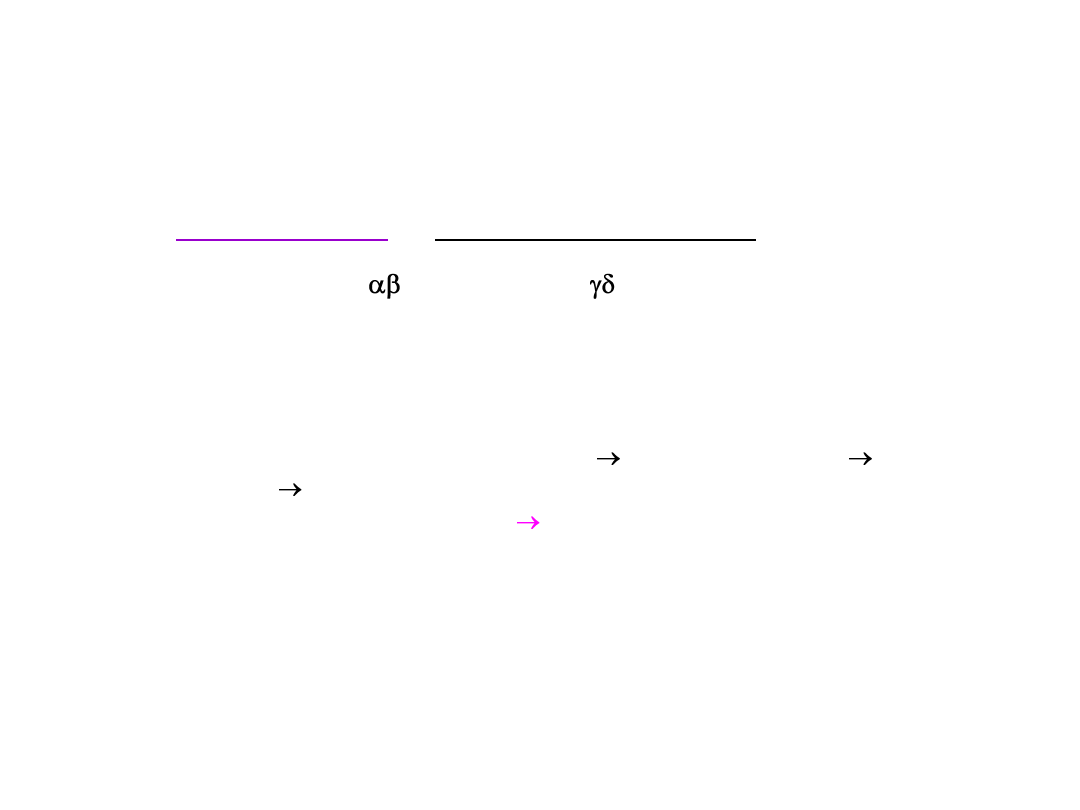
Rozpoznanie antygenu
• limfocyty T
–
rozpoznają małe fragmenty peptydów prezentowane na
powierzchni
komórek
APC
poprzez receptor
TCR
łącznie z cząsteczkami
MHC
tzw.
restrykcja MHC
lub
rozpoznanie asocjatywne
*
receptor TCR
: TCR
- 90-95%, TCR
- 5-10%
Th CD4 – MHC kl. II
Tc CD8 – MHC kl. I
w wieku starszym spadek ekspresji MHC – słabsza odpowiedź na antygen
• limfocyty B
–
rozpoznają antygeny T-niezależne (bardziej oporne na
degradację przez APC) poprzez
receptory Ig
klonalna aktywacja B
komórki
plazmatyczne
wytwarzanie przeciwciał
w wieku starszym spadek limfocytów B
osłabienie odpowiedzi pierwotnej na
antygen
• antygeny T-zależne –
wytwarzanie przeciwciał powstaje w kooperacji
B i głównie Th2
Th2 – wzmagają produkcję przeciwciał, pw. IgE, stany alergiczne, autoimmunizacja
Th1 - biorą udział w reakcjach zapalnych komórkowych – aktywacja makrofaga
(DTH), cytotoksyczność
ale cytokiny Th1 znoszą funkcje Th2 i odwrotnie
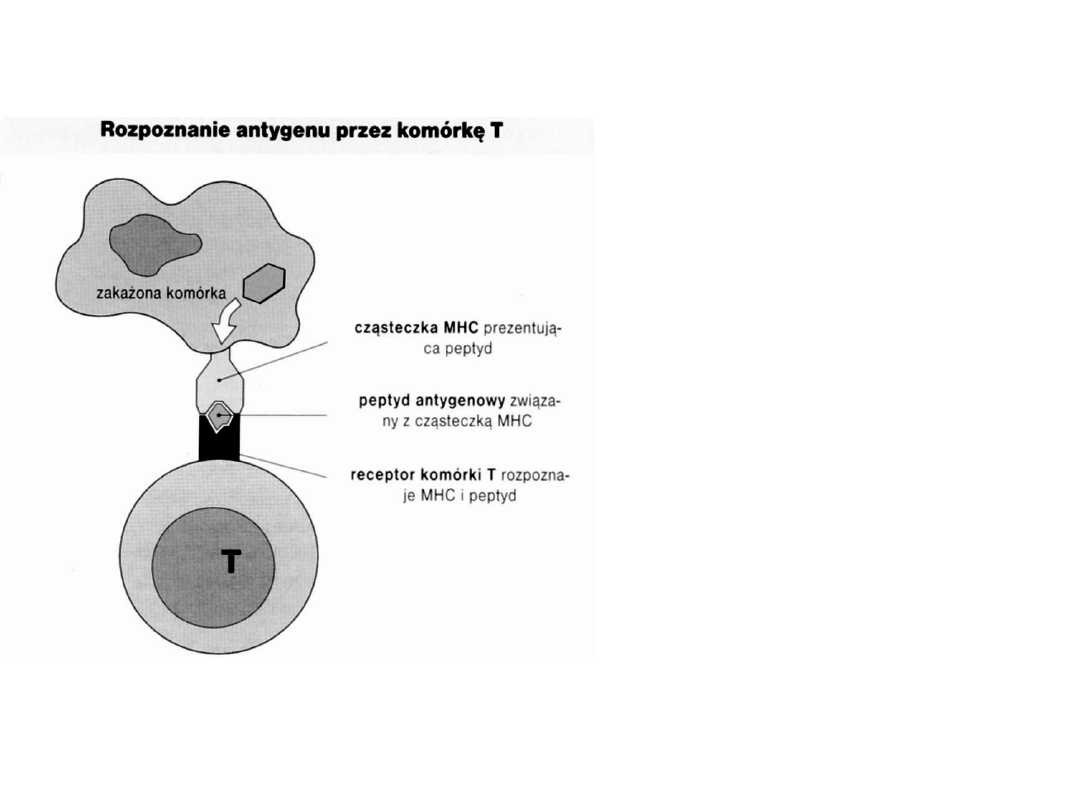
T rozpoznają antygeny pochodzące z innych
komórek jako peptydy łącznie z MHC
T CD4 – MHC kl. II
T CD8 – MHC kl. I
poprzez receptor TCR
B rozpoznaje część antygenu – epitop
przez receptor immunoglobulinowy
Antygen wybiera i generuje swoisty klon
wiążących go komórek T lub B
Stymulowane limfocyty proliferują,
wytwarzają cytokiny, ujawniają nowe
receptory, odpowiadają na inne cytokiny
Część komórek zachowuje
pamięć dla danego
antygenu,
co zapewnia trwałą odporność
na patogen
APC
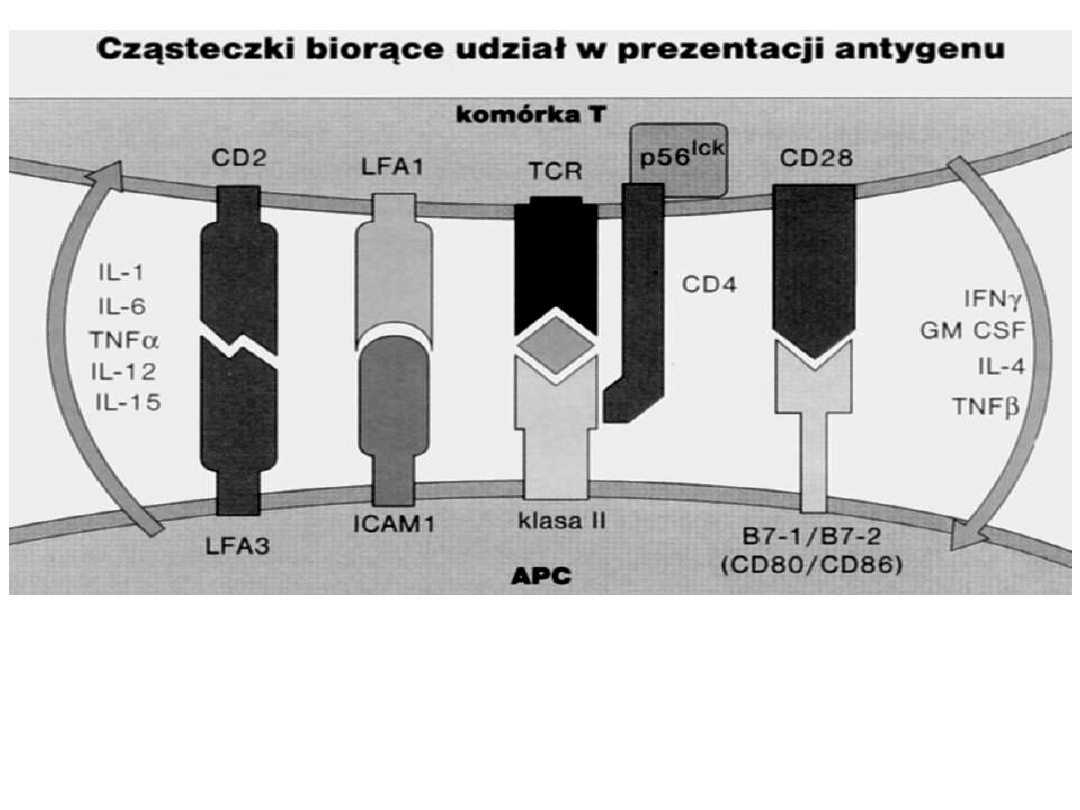
W prezentacji antygenu Th bierze udział TCR + CD4 oraz MHC kl. II na APC.
Istotne są także inne cząsteczki na powierzchni komórek a także cytokiny – wytwarzane przez Th i APC
Aktywowane Th wytwarzają cytokiny, które zwiększają zdolność prezentacji antygenu przez APC.
Aktywacja T prowadzi do proliferacji komórkowej i różnicowania się w komórki efektorowe
Niektóre komórki mogą przetrwać długo jako komórki pamięci
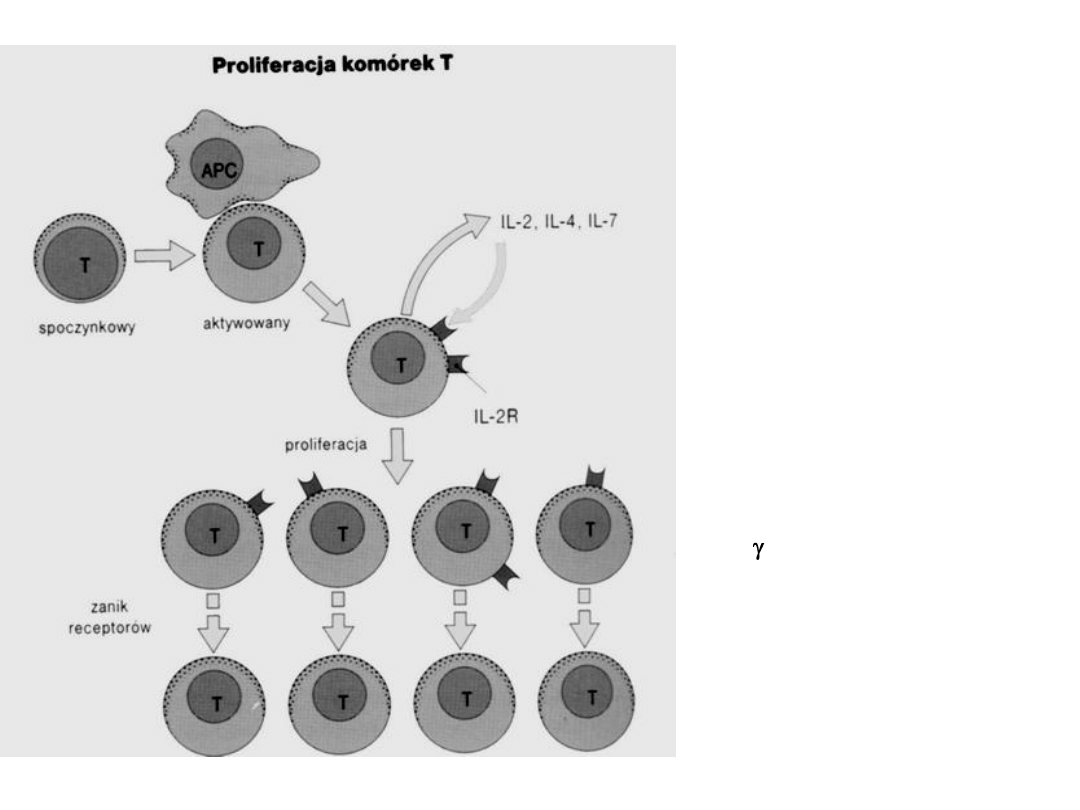
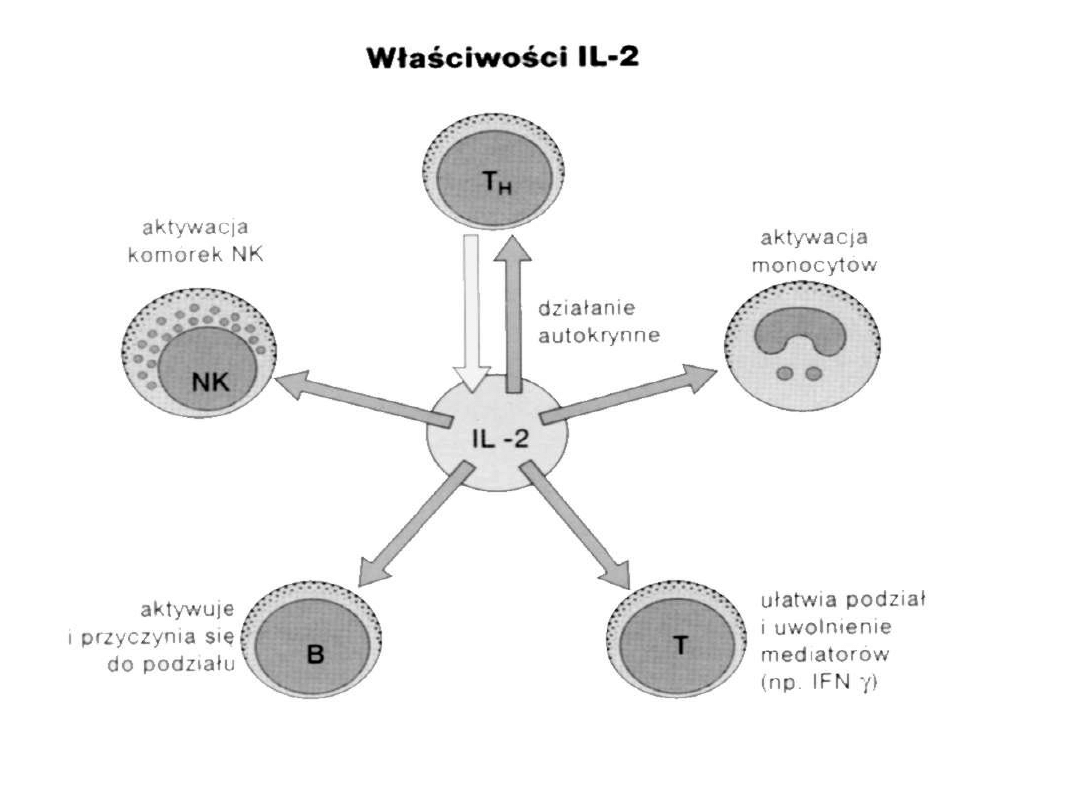
T spoczynkowe nie produkują
cytokiny Il-2.
Aktywacja pod
wpływem antygenu - ekspresja
receptora dla Il-2 i produkcja Il-2.
(działanie autokrynne – na tą samą
komórkę i pakrynne - na sąsiednią)
Indukuje to proliferację.
Dalsza stymulacja antygenowa
zmniejsza receptory dla Il-2.
Il-2 – główny czynnik wzrostu i
aktywacji wszystkich T, zwłaszcza
cytotoksycznych
- aktywacja monocytów
- NK – komórki LAK
- ułatwia podział i uwolnienie
INF
- może być produkowana przez CD8
i LGL
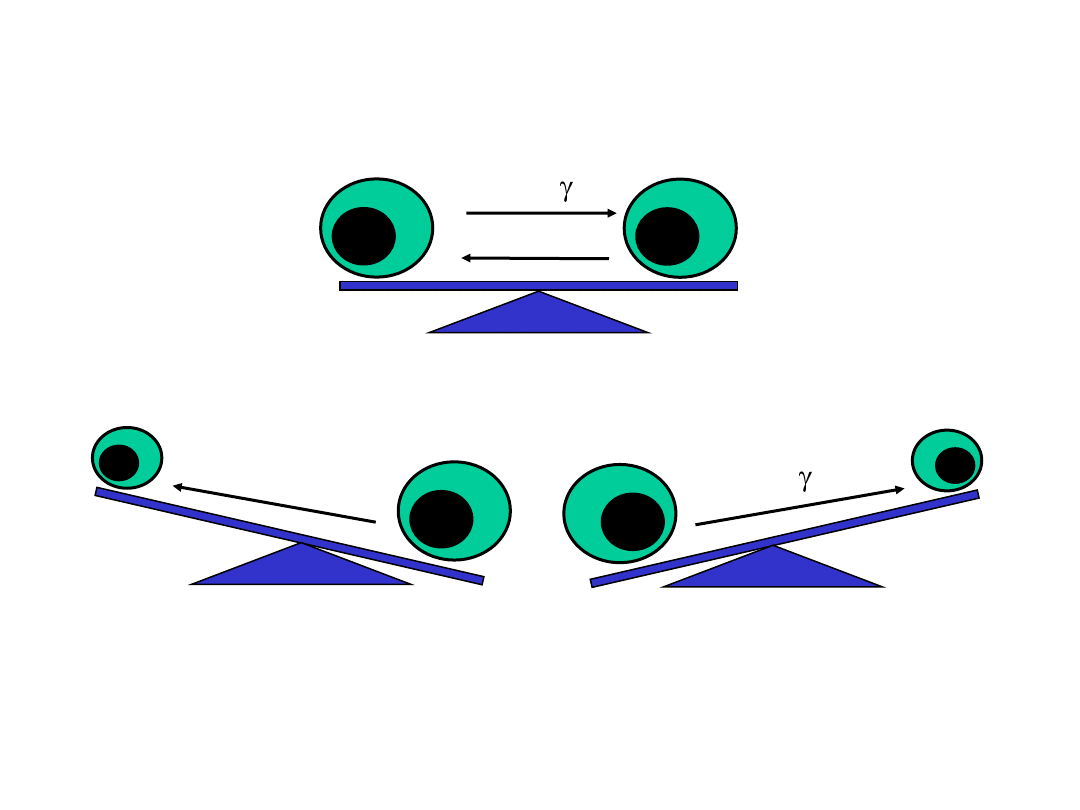
Th1 może znosić funkcje Th2 i odwrotnie
Th2
IFN-
IL-10
-
-
Th1
Th2 dominuje
Th1
IL-10
Th2
-
Th1 dominuje
Th2
Th1
IFN-
-
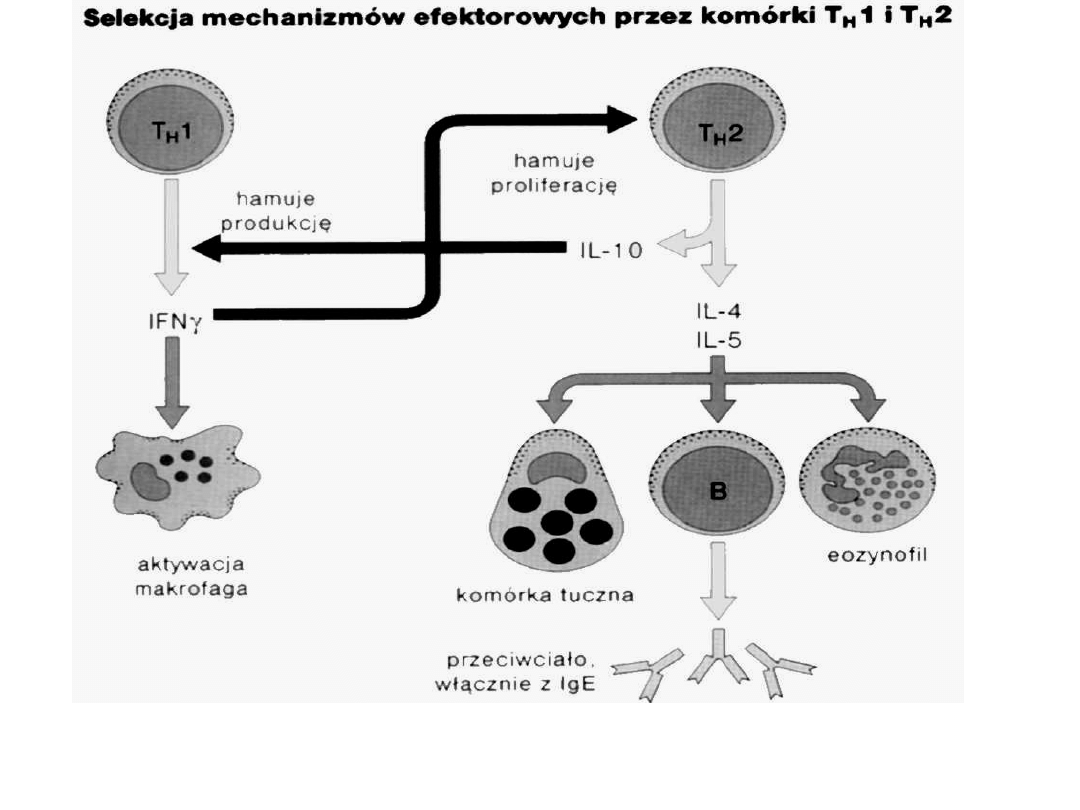
Produkcja cytokin przez Th1 i Th2 kieruje różnymi drogami efektorowymi
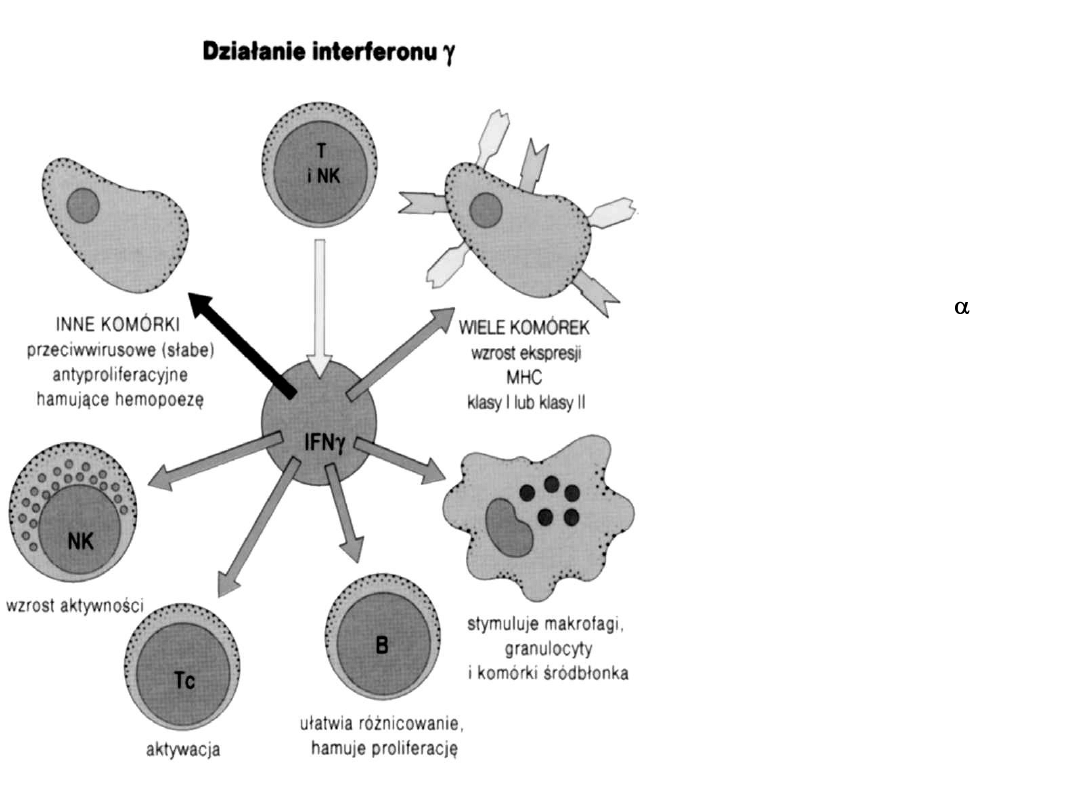
Wytwarzany przez aktywowane T i NK
Najbardziej aktywnie stymuluje
makrofagi
Zwiększa funkcję prezentacji antygenu
przez różne typy komórek
Słabiej działa na NK niż IFN
Hamuje proliferację Th2
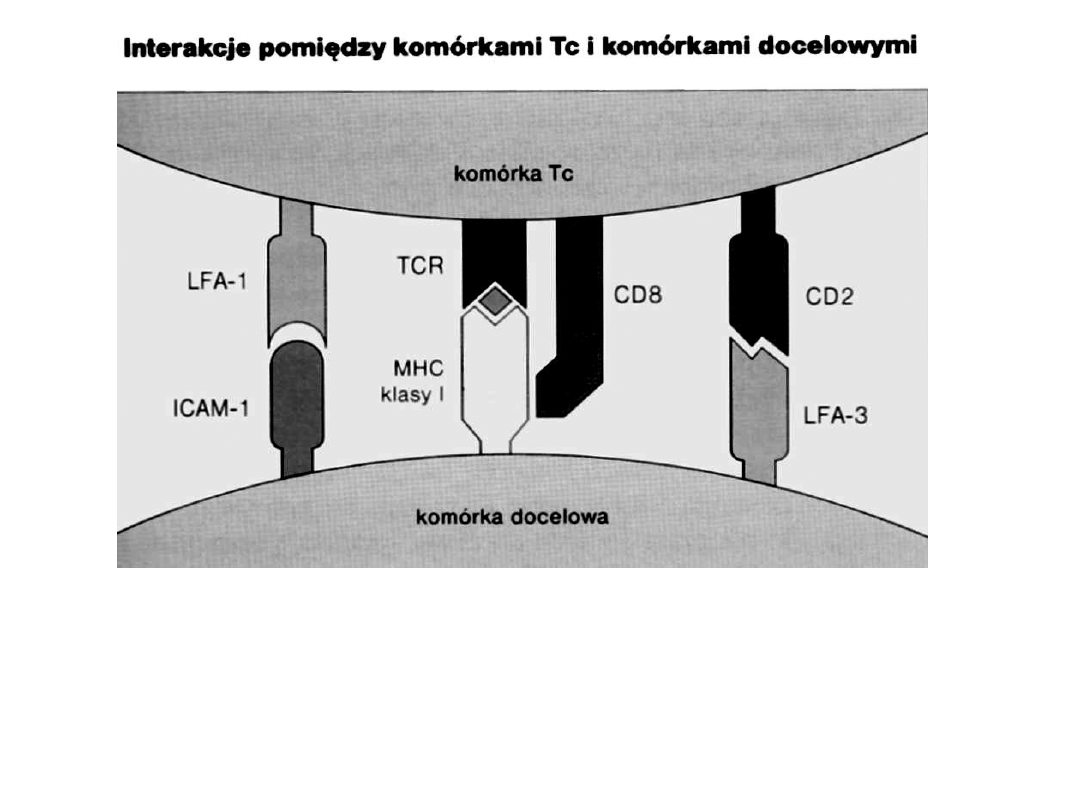
Cytotoksyczność komórek Tc i Nk jest obroną przeciw
patogenom wewnątrzkomórkowym,
komórkom nowotworowym, komórkom przeszczepu.
Tc rozpoznają komórki zainfekowane przez TCR i CD8 i MHC kl.I oraz inne ligandy
Wtedy uruchamiany jest sygnał do uruchomienia mechanizmu cytotoksyczności
Istnieje kilka mechanizmów zabijania
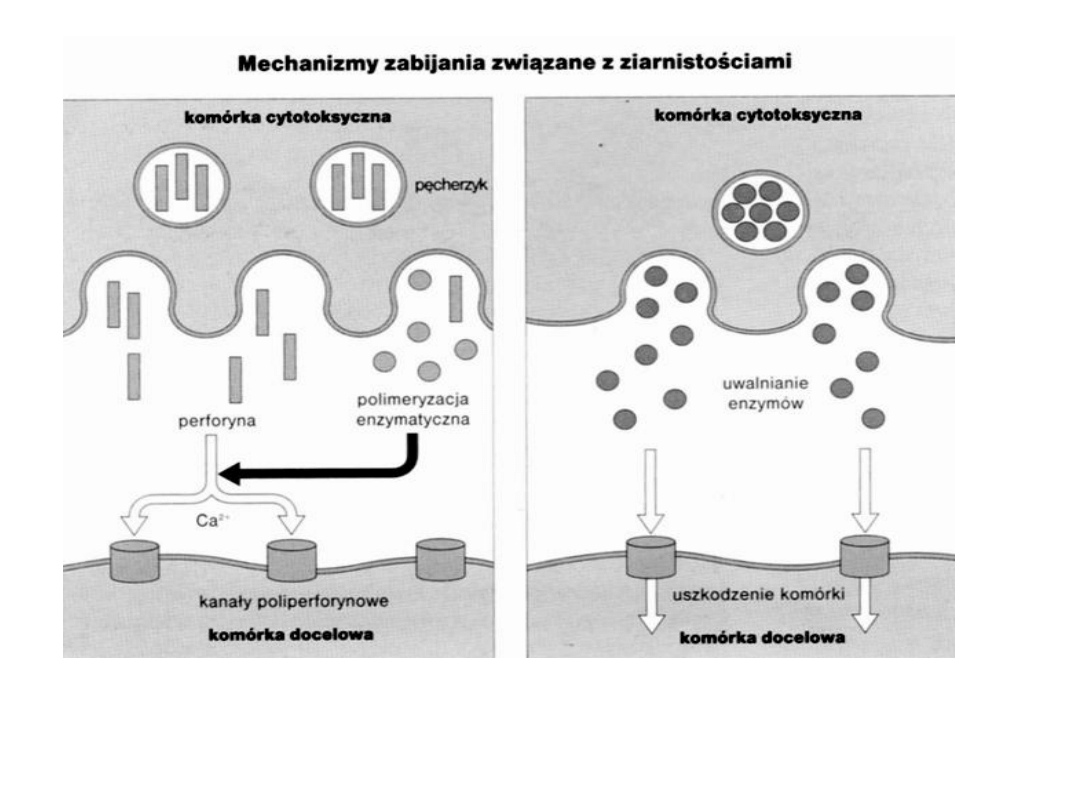
Cytotoksyczna komórka ulega degranulacji
:
uwalnia
perforyny
, w obecności Ca uwalnia
granzymy
– enzymy z ziarnistości
tworzą się kanały – śmierć komórki przechodzą przez kanały do komórki
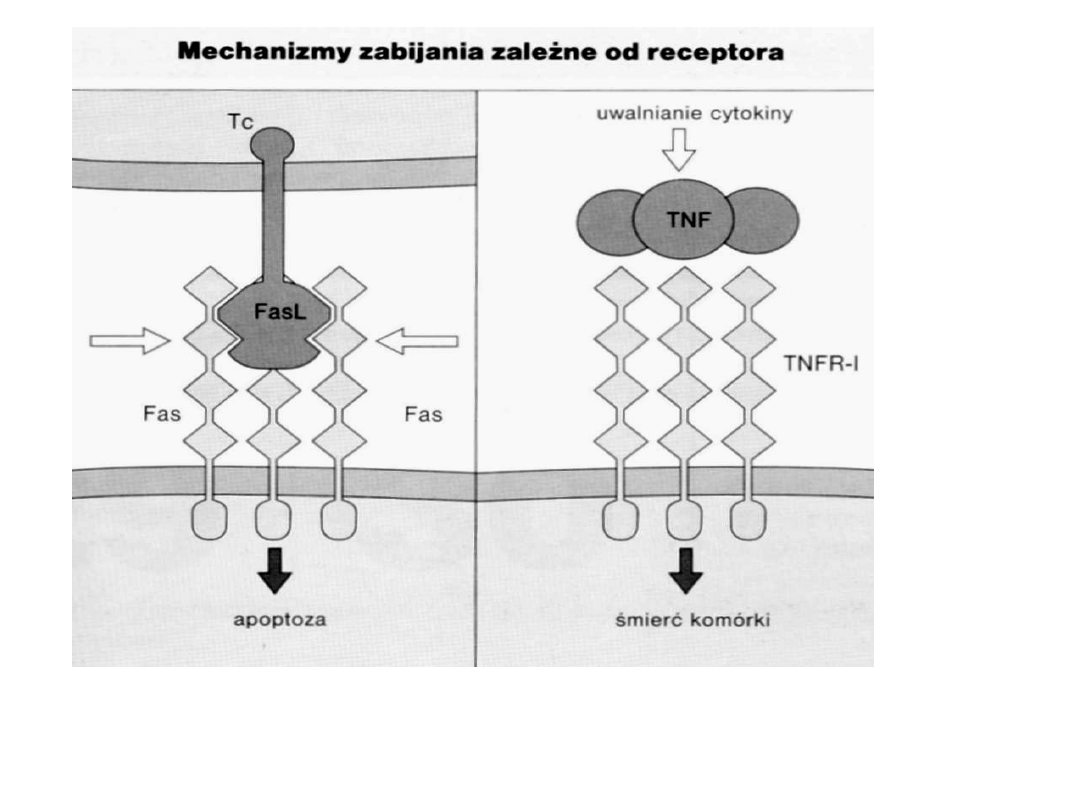
Fas ligand na Tc + Fas na komórce docelowej
, podobny mechanizm, dłużej trwa
połączenie z wewnątrzplazmatyczną proteiną
MORT-1 – prowadzi do
apoptozy
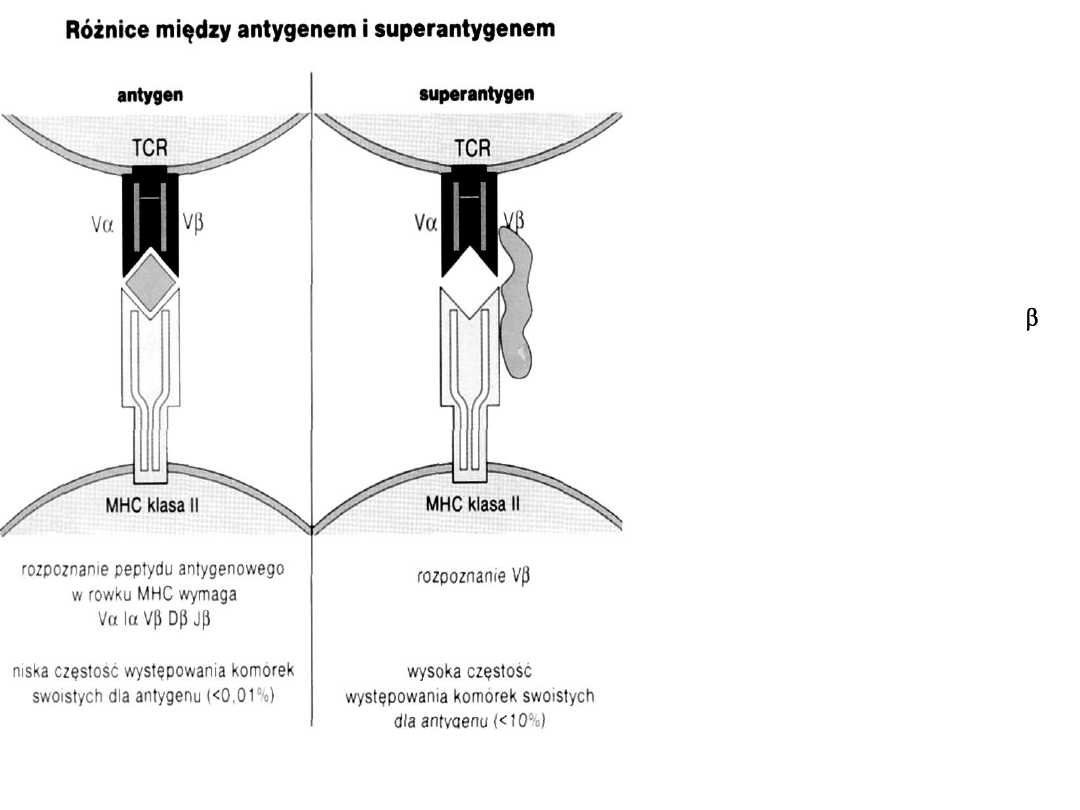
Antygen musi ulec „obróbce”
przez APC do peptydu, który jest
rozpoznawany w rowku MHC.
Superantygen
, np. enterotoksyny
gronkowcowe, toksyny wstrząsu
toksycznego, niektóre wirusy
wiążą się bezpośrednio
z MHC kl.II i odcinkiem V łańcucha
W zależności od warunków może być
odpowiedź immunologiczna lub
anergia klonalna
Nieswoista stymulacja T i B
może zachodzić poprzez mitogeny
np. PHA – fitohemaglutynina – z ziaren
fasoli
ConA – konkanawalina – z rycyny
Wiążą się z TCR i CD2

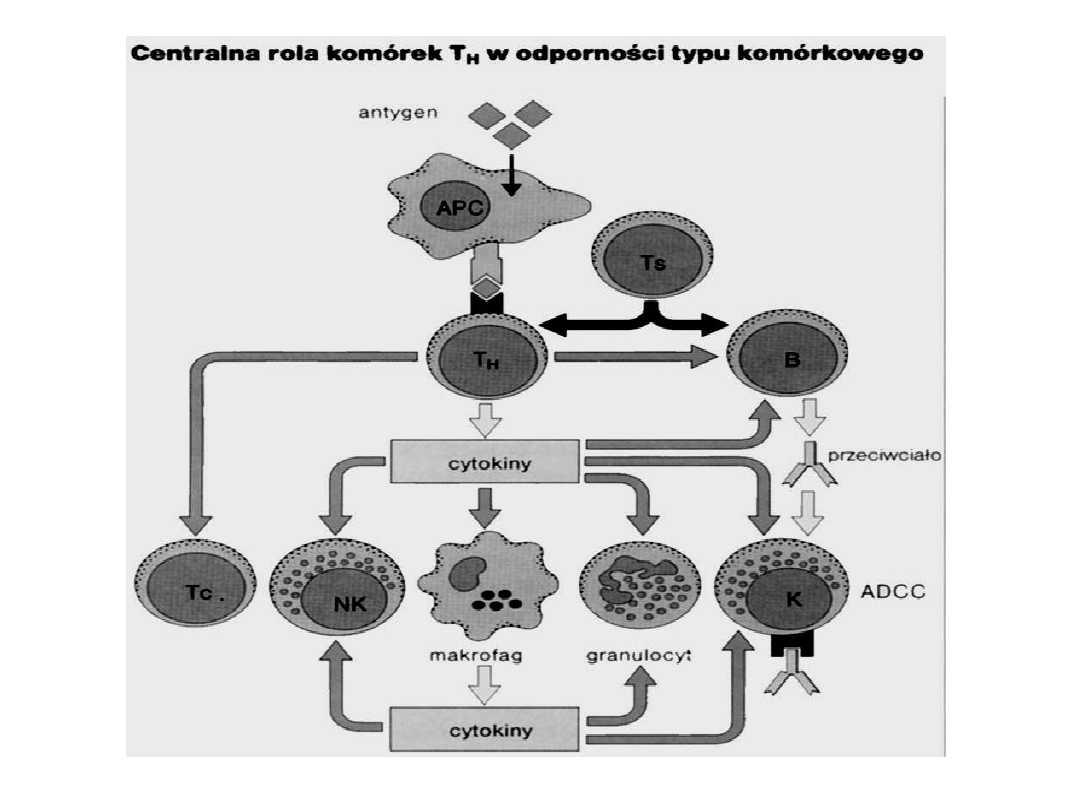
Typy odpowiedzi komórkowej
centralną rolę pełni limfocyt T CD4
– wytwarzane cytokiny
regulują różne typy współdziałania komórkowego
Mechanizmy efektorowe
– zależą od charakteru antygenu
•
aktywacja makrofagów (Th1 - IFN )
- powstaje naciek typu ziarniny,
zabijanie pasożytów wewnątrzkomórkowych: prątki, brucelle, listerie
•
nadwrażliwość typu późnego DTH
– np. na tuberkulinę, alergia
kontaktowa, komórką efektorową jest T CD4, potem może być napływ
makrofagów
•
cytotoksyczność T CD8
(Th - Il-2 + APC - Il-12) – cytoliza komórek
zakażonych wirusem, odrzucanie przeszczepu – różne formy zabijania:
perforyny, granzymy, mechanizmy zależne od receptora Fas ligand
•
cytotoksyczność zależna od przeciwciał (ADCC)
– komórki K, mają
receptor Fc (CD16), wiążą się z przeciwciałem przyłączonym do antygenu
na komórce
•
LAK
– limfocyty aktywowane Il-2, NK ? – wykazują większą
cytotoksyczność, próbuje się w leczeniu raka
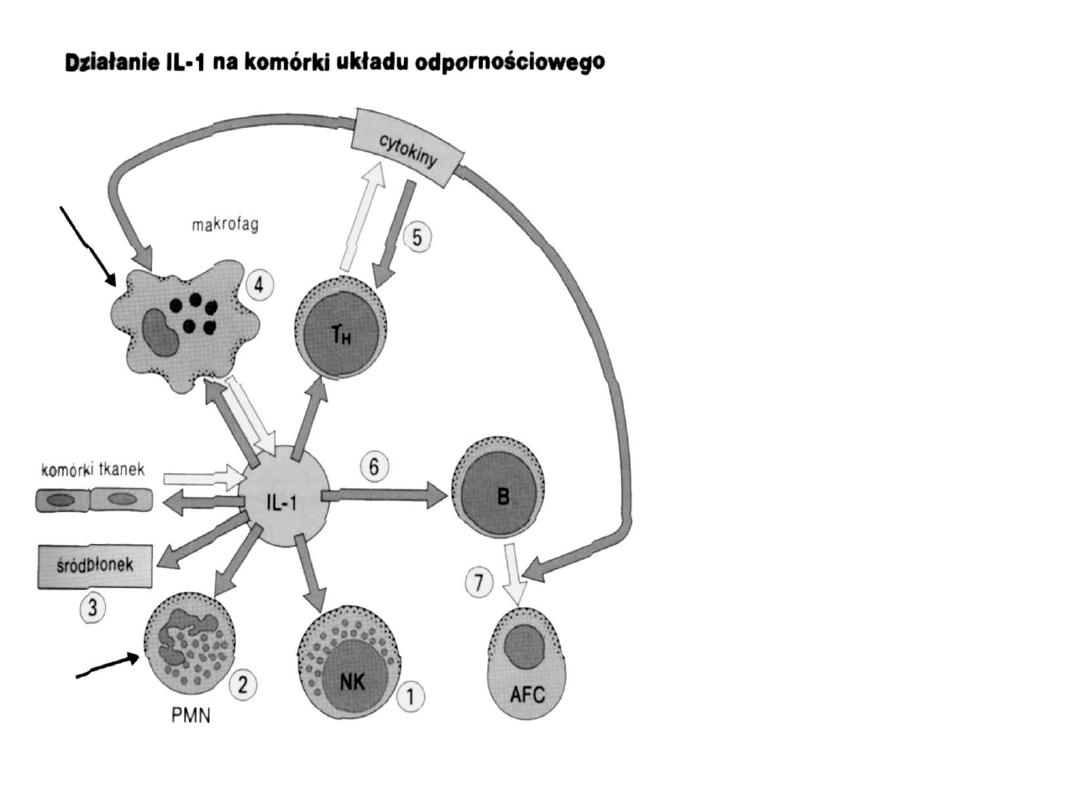
Powstaje w odpowiedzi na zakażenie,
uszkodzenie, antygeny.
1.Wzrost cytotoksyczności NK
2.zwiększona chemotaksja PMN
3.ekspresja cząsteczek adhezyjnych na
komórkach śródbłonka
4.aktywność cytotoksyczna makrofagów
5.proliferacja Th, ekspresja R - Il-2
6.proliferacja B
7.różnicowanie w kom.plazmatyczne
Wyszukiwarka
Podobne podstrony:
Ćwiczenie 7 Odporność komórkowa swoista
Komórkowe usługi EDGE
Odpornosc swoista i nieswoista
Cw 1 ! komorki
Odporność swoista
Elektroforeza DNA komórkowego BioAut1, BioAut2 i Ch1
Terapia komórkowa w neurologii
W2 Chemiczne skladniki komorki
komórka
Swoiste i nieswoiste zapalenie kości i stawów
Cykl życiowy komórki
Mechanizmy swoistej immunoterapii alergii 3
Biofizyka komórki II Propagacja impulsu
komórka roślinna i tkanki roślinne
W03b Komórkowe i molekularne podłoże zapaleń
Potencjał czynnościowy mięśniowej komórki roboczej serca1
więcej podobnych podstron