Dlaczego sos czosnkowy?
Bo notatki z mikrobiologii
Metabolizm – katabolizm – procesy degradacji.
Anabolizm – procesy... nie no, to już jest nudne.
Źródła energii:
energia świetlna - ~foto
energia chemiczna - ~niefoto ...chemo
Źródła protonów i elektronów
nieorganiczne - ~lito
organiczne - ~organo
Źródła węgla:
wiązanie dwutlenku węgla – auto
związki organiczne – hetero – heterotrofy mogą rozkładać różne związki dzięki wykorzystaniu
enzymów przeprowadzących ~lizę odpowiednich substancji, które są zbyt duże, aby przeszły przez
osłony komórkowę. Substancje te są rozkładane do związków prostych, które ulegają dalszemu
metabolizowaniu. Mogą być to tłuszcze, białka, polisacharydy.
Przykłady enzymów:
proteazy – hydrolizują białka
lipazy – kasują tłuszcze
nukleazy – kasują kwasy nukleinowe
celulazy – kasują wiadomo co
amylazy – koszą skrobię.
Cza umieć rozróżniać proteazy od peptydaz.
Proteazy rozkładają białka do peptydów, podczas gdy peptydazy kasują te peptydy do
aminokwasów. Procesy przez nie przeprowadzane można rozpoznać po nazwach enzymów –
proteazy = od protein, peptydazy = od peptydów.
Po rozłożeniu białek do peptydów działają odpowiednie aminopeptydazy lub karboksypeptydazy,
rozkładające aminokwasy do lotnych kwasów tłuszczowych i amin. Z kolei aminy są kasowane do
alkoholi i NH
3.
Proces ten odbywa się w warunkach beztlenowych
W warunkach tlenowych natomiast:
Z aminokwasów na drodze fosforylacji oksydacyjnej powstaje dwutlenek węgla, a także woda,
amoniak i H
2
S.
Ponoć cystyna ulega oksydacyjnej deaminacji w ten sposób, że powstaje pirogronian, siarkowodór
+ amoniak... ale skąd u diabła bierze się siarkowodór (jaki mechanizm to warunkuje) i dlaczego
proces ten nie zachodzi w cysteinie?
W każdym razie ogólny schemat oksydacyjnej deaminacji jest taki, że aminokwas przy
przeniesieniu elektronów na odpowiednie flawoproteiny jest utleniany z jednoczesnym odłączeniem
grupy aminowej w postaci amoniaku. Utlenienie doprowadza do powstania odpowiedniego alfa-
ketokwasu.
Podział ze względu na wymagania pokarmowe
Prototrofy: potrafią wykorzystywać jeden związek jako źródło węgla, protonów i elektronów oraz
energii.
Np. E. coli, gdy wykorzystuje glukozę.
Auksotrofy:
Potrzebują do wzrostu więcej składników organicznych, które wykorzystują w swoim
metabolizmie. Z jednego związki np. czerpią węgiel, z innego energię, z jeszcze innego azot.
Związki te stanowią dla nich tzw. czynniki wzrostowe i mogą być to aminokwasy, zasady azotowe
itd.
Najłatwiej przyswajalne źródła węgla
Cukry proste
Glicerol
Mannitol
Kwas mlekowy
Metylotrofy:
Mikroorganizmy zdolne do wykorzystywania C1-źródeł węgla innych, niż dwutlenek węgla. Przy
czym trzeba zauważyć, że źródło C1 nie znaczy, że wykorzystywane muszą być związki
jednowęglowe. Ograniczenie sprowadza się do tego, że w związku nie może być połączenia węgiel-
węgiel. Przykładowo mikrobusy takie spokojnie utlenią trimetyloaminę.
Metanotrofia:
Tu zabawa jest de facto ograniczona do utleniania metanu i ponoć jego pochodnych.
Rozkład cukrów:
Załóżmy, że mamy do czynienia z polimerami takimi, jak skrobia. Skrobia składa się z amylozy i
amylopektyny. O ile w amylozie występują wiązania glikozydowe alfa1,4, tak w amylopektynie
występują rozgałęzienia, które są połączone prostopadle z łańcuchem cukrowym wiązaniami alfa1,6
Żeby rozłożyć enzymatycznie takie badziewie, nasza komóreczka angażuje szereg enzymów, które
są ładne.
alfa-amylaza: tnie w środku łańcucha, produktem są różne, kwadratowe i podłużne maltodekstryny.
Beta-amylaza: jest zdecydowanie bardziej Emo, trzyma się na uboczu i tnie (nie się) na końcach,
odcinając dwie cząsteczki glukozy, a więc maltozę.
Pullulanaza – jak sama nazwa nie wskazuje, enzym ten kasuje wiązanie alfa1,6
Glukoamylaza – bardzo skąpa i oszczędna, zadowala się ucinaniem po jednej cząsteczce glukozy z
końca łańcuchów.
maltaza
... która robi łupu cupu cząsteczce maltozy, w wyniku czego powstaje..... ;>......... no bo co
innego..... jak nie glukoza?
***Jak rozpoznać, że skrobia na szalce została rozłożona?
Polać żywotkom płynu Lugola (jod rozpuszczony w jodku potasu), który barwi skrobię na
fioletowo.
Sprawa jest prosta – jak mikroby wsiupały nam skrobię, to miejsca, w których to zrobiły, nie
zabarwią się na fioletowo

A jak to jest z laktozą?
Laktoza to nic innego, jak glukoza+galaktoza.
Enzym, który zajmuje się tą „parą” zwany jest Beta-galaktozydazą.
O... mam w zeszycie napisane, że laktoza wywołuje alergię.
I dobrze.
Chociaż... mleko jest nawet dobre do kawy.
Jak sprawdzić, że jakieś żywotko metabolizuje laktozę?
W sposób powszechny, prawidłowo-rzeczowy: wykorzystujemy podłoże różnicujące EMB. Skrót
EMB pochodzi od eosine methylene blue. A więc w skład podłoża wchodzi eozyna i błękit
metylenowy.
Nie dość, że te chemikalia hamują wzrost bakterii gram+, to jeszcze potrafią wskazywać, co
metabolizuje laktozę, a co nie. Bakteryjki, które to robią mają na tym podłożu zielonkawy blask.
Gdybanie.value=1:
W tym podłożu najprawdopodobniej błękit metylenowy nie pełni specjalnej roli jako wskaźnik...
gdyż jest to raczej wskaźnik oksydoredukcyjny, a nie wskaźnik pH.
Tym czasem podczas metabolizmu laktozy uwalnia się odpowiedni kwas. Zakwaszenie środowiska
protonami powoduje sprotonowanie eozyny, której dzięki temu zmienia się układ wiązań
chromoforowych, dlatego pochłania ona światło o innej długości fali, przez co emitowana barwa
dopełniająca jest taka, a nie inna.
Gdybanie.value=0
Jedziem dalej: celuloza
Celuloza -----celulazy------> Celobioza ----------celobiazy----> glukoza
No... bez komentarza.
LIPIDY
Jest to związek wielkocząsteczkowy i nie może być pobierany bezpośrednio do cytoplazmy, a musi
ulec strawieniu przez enzymy zewnątrzkomókowe – lipazy. Te lipazy hydrolizują lipidy w efekcie
końcowym do glicerolu i do kwasów tłuszczowych wchodzących w skład tych lipidów.
Lipazy występują u wielu bakterii należących do różnych typów taksonomicznych, np:
–
Bacillus
–
Pseudomonas... np. Pseudomonas fluorescens
–
Propionibacterium
Są to bakterie, szczególnie Bacillus i Propionibacterium, których lipazy, proteazy i amylazy
wytwarzane przez nie są wykorzystywane w przemyśle do produkcji detergentów. Tak więc
ektoenzymy mają zastosowanie przez człowieka.
Utlenianie zredukowanych form azotu:
W nazwie przedrostek „Nitroso”, amoniak jest utleniany dwuetapowo.
Najpierw następuje jałowa reakcja, w której nie powstaje ATP. Reakcja przeprowadzana jest przez
monooksygenazę amoniakową. Jak nazwa wskazuje, enzym ten pakuje do amoniaku cząsteczkę
tlenu.
NH3 + O2 + 2e- + 2H+ ---> NH2OH + H2O
Kolejna reakcja nie jest już jałowa energetycznie. Następuje w niej utlenienie hydroksyloaminy do
azotanu (III). Reakcja jest przeprowadzana przez oksydoreduktazę hydroksyloaminową i

towarzyszy jej przeniesienie elektronów na łańcuch oddechowy:
NH2OH +H2O + 0,5O2 ---> NO2- + H2O + H+
Bakterie utleniające sole kwasu azotowego (III) mają przedrostek „Nitro” i w reakcji utlenienia tego
związku do azotanu (V) uczestniczy oksydoreduktaza azotynowa
A reakcja przebiega tak:
NO2- + 0,5O2 --> NO3-
Bakterie wiążące azot
Bakteryjki te występują powszechnie w glebie.
Posiadają one enzym – nitrogenazę – która uczestniczy w następującej reakcji:
N2 + 8H+ +8e- +16ATP --> 2NH3 + H2 + 16ADP + 16Pi
NITROGENAZA:
Jest to enzym, który warunkuje wiązanie azotu cząsteczkowego. A więc potrafi rozerwać 3 silne
wiązania, jakie łączą 2 atomy azotu i zredukować ten azot w rezultacie do amoniaku.
Budowa nitrogenazy
Sama nitrogenaza składa się z dwóch multimerycznych części
reduktaza nitrogenazy – białko Fe
nitrogenaza właściwa – FeMo – oprócz żelaza zawiera molibden.
Jak działa nitrogenaza?
Najpierw reduktaza nitrogenazy przenosi elektrony na nitrogenazę, a sama nitrogenaza dokonuje
reakcji redukcji azotu do amoniaku.
Jest to reakcja kilkuetapowa.
Lustereczko powiedz przecie, kto jest najbardziej wydajnym enzymem redukującym azot
cząsteczkowy na świecie?
- Ty, nitrogenazo, ale masz łupież.
Nie jest to enzym doskonały! Zamiast wykorzystywać sześć elektronów do reakcji redukcji – jakie
są rzeczywiście potrzebne, wykorzystuje aż 8 elektronów, dlatego, że dwa elektrony przenosi na
dwa protony i w wyniku tej reakcji produkowany jest wodór cząsteczkowy.
Nic więc dziwnego, że stwory te wykształciły hydrogenazy, które zapobiegają marnotrawstwu
wodoru, ale mniejsza o to, bo tego na ćwiczenia niet.
Nic więc też dziwnego, że bakterie te korzystają z azotu cząsteczkowego w ostatecznej
ostateczności ostatecznie przypieczętowanej tym, że w środowisku nie ma innych źródeł azotu.
Jeżeli tylko pojawi się coś innego, to mikroby te się za to łapią.
Logiczne jest więc to, że gdy chcemy wykazać wzrost bakterii wiążących azot cząsteczkowy,
powinniśmy użyć podłoża bezazotowego.
A teraz coś kompletnie innego:
Nitrogrnaza jest enzymem bardzo wrażliwym na tlen. Clostridium czy Desulovibrio
nie mają
żadnego problemu, bo są beztlenowe i enzym ten w zasadzie nigdy nie jest unieczynniany.
Ale takie coś, jak tlenowy Azotobacter ma zonka... ale chwila! Nic nie łączy tak bakterii, jak śluz.
Śluz, przez który bardzo kiepsko dyfunduje tlen. Dlatego cechą charakterystyczną kolonii
Azotobacter jest ich... śluzowaty charakter.

SIARKA (bardziej pod egzamin)
Siarka występuje w komórce przede wszystkim w aminokwasach siarkowych – cysteina, metionina.
Ale także w koenzymie A.
Bakterie i archeony potrafią wykorzystać najróżniejsze związki siarki, jako źródło pierwiastka, a
więc tiosiarczany, siarczany, a także aminokwasy zawerające siarkę – w szczególności znakomitym
źródłem siarki dla archeonów i bakteri chemoorganohetero jest cysteina. Czasami mogą sobie
łyknąć siarkofruta i też im dobrze. Siarkowodór, chociaż siarka jest tam w formie zredukowanej tak
jak w związkach organicznych nie jest dobrym źródłem siarki dla mikrobów, bo jest dla nich
toksyczny... ale są takie, które wymagają siarkowodoru jako źródła siarki. Są nimi np. metanogenne
archeony.
Są to archeony beztlenowe, które wykorzystują dwutlenek węgla jako końcowy akceptor
elektronów... a że „rodzą metan”, to go produkują. Jako, że żyją w środowiskach beztlenowych,
gdzie siarka występuje w formie zredukowanej, to przystosowały się do wykorzystywania
siarkowodoru jako źródła siarki.
Niektóre organizmy prokariotyczne potrafią wykorzystać także siarkę pierwiastkową jako źródło
siarki, a także różnego rodzaju sulfoniany, estry siarczanów.
Sama E. coli potrafi wykorzystać wręcz niesamowitą ilość różnych dziwadeł zawierających siarkę
jako źródło tego pierwiastka, ale znakomita większość organizmów jako źródlo siarki wykorzystuje
siarczan albo cysteinę.
Każdy związek organiczny pochodzenia biogennego zawierający siarkę będzie mógł być
wykorzystany przez jakąś grupę prokariotów jako źródło siarki.
Cysteina jest znakomitym źródlem siarki, bo wystarczy grupę SH przenieść na inny związek, w
którym wymagana jest siarka, natomiast siarczan może być wykorzystany jako źródło siarki
dopiero po zredukowaniu.
Do tego, by siarczan mógł ulec redukcji ASYMILACYJNEJ (siarczan wykorzystywany jako źródło
siarki). Dla odróżnienia – mówimy o redukcji DYSYMILACYJNEJ, kiedy bakteria jest zdolna do
oddychania beztlenowego i siarczan jest wykrozystywany jako końcowy akceptor elektronów.
Redukcja asymilacyjna siarczanu zachodzi w cytoplazmie. Siarczan ten musi być najpierw
aktywowany i ta aktywacja zachodzi przy udziale dwóch enzymów oraz ATP.
Sulfurylaza ATP przekształca ten siarczan adenozyno-5-fosfosiarczan (APS). Następnie potrzeba
następnej cząsteczki ATP oraz następnego enzymu – kinaza APS – kinaza adenozyno-5-
fosfosiarczanu, która wprowadza następną grupę fosforanową do związki i powstaje fosfosiarczan
fosfoadenozyny, w skrócie PAPS. Dopiero w fosfoadenozynofosfosiarczanie siarka może ulec
redukcji i sulfotransferaza PAPS redukuje siarczan do siarczynów, a reduktaza siarczynowa
redukuje siarczyn do H2S. Ten H2S – zredukowana siarka, zostaje włączona do cysteiny z udziałem
enzymu syntazy cysteinowy, a konkretnie grupa siarczkowa zostaje włączona do O-acetyloseryny.
W rezultacie z siarczanu powstaje cysteina, która jest znakomitym donorem zredukowanej siarki w
reakcjach syntezy wszystkich związków zawierających ten pierwiastek w komórce bakteryjnej.
Tak więc mamy do czynienia z redukcją asymilacyjną siarczanów.
Jeżeli w podłożu będzie dostępna cysteina, to chemoorganoheterotrofy NIE BĘDA wydatkowały
energii na redukcję siarczanów, a będą wykorzystywały cysteinę jako źródło siarki.. .ale bakterie
chemolitoautotroficzne, czy fotolitoautotroficzne, które nie dysponują często systemami transportu
aminokwasów i nie mają też enzymów, które umożliwiają wykorzystanie cysteiny jako źródło
siarki, będą musiały wykorzystywać nieorganiczne źródła siarki, jak siarczan, czy tiosiarczan.
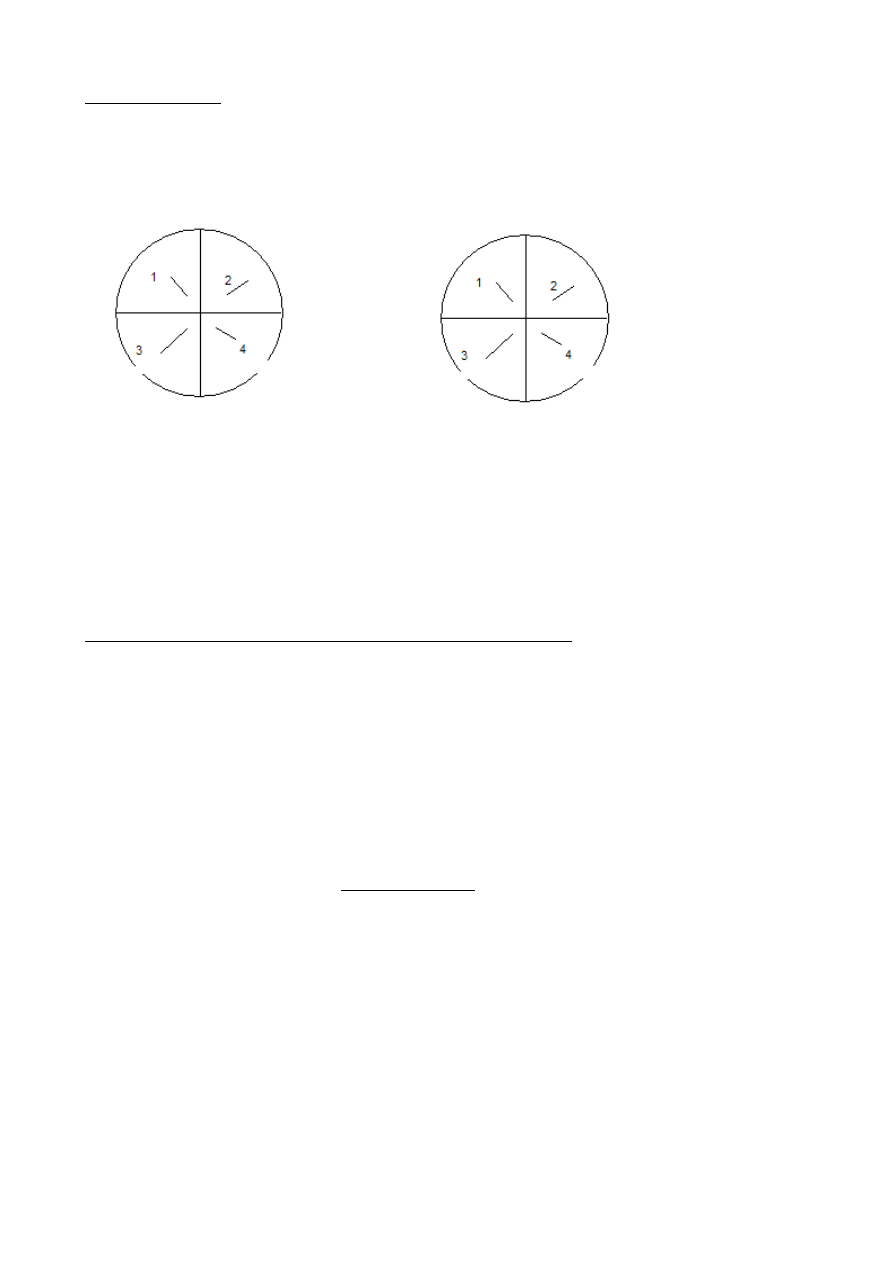
Część praktyczna
Agar odżywczy
Podłoże AB (mineralne)
1. Bacillus subtilis
2. Halothiobacillus neapolitanus
3. Paracoccus versutus
4. Micrococcus luteus
Powyższe doświadczenie pozwala ustalić, jaki dane żywotko posiada profil odnośnie źródła węgla i
donora elektronów. A więc czy jest chemoorganoheterotrofem, czy chemolitoautotrofem.
Czyli jaki będzie profil metaboliczny bakteryjek, które tam urosną?
Agar odżywczy zawiera organiczne źródło węgla, a więc bakterie, które będą mogły je
wykorzystywać, będą heterotrofami. Będą też organotrofami, ponieważ jedzą organy kościelne, co
powoduje korozję piszczałek. Będą też organotrofami m.in. dlatego, że jako źródło protonów i
elektronów do zredukowania NAD będą wykorzystywać związki organiczne z agaru odżywczego.
Wreszcie będą chemo... bo jako źródło energii wykorzystują związki chemiczne.
Teraz cuś o podłożu AB
Jest to podłoże mineralne, które zawiera tiosiarczan. Tiosiarczan jest utleniany przez bakterie, a
powstające wówczas kwaśne metabolity powodują zmianę pH, która jest wykazywana poprzez
dodanie 2ml czerwieni fenolowej. Powyżej pH 8.0 ma ona kolor taki, na jaki wskazuje jej nazwa.
Poniżej pH 6,6 staje się żółta i wskazuje na to, że żywotka dają tam sobie radę.
Profil żywotka, które tam rośnie to chemolitoautotrof:
A jest tak dlatego, że: chemo – bo nie używa światła jako źródła energii... i nie dziwota, bo skąd w
szafie światło.
Lito – gdyż donorem elektronów jest związek nieorganiczny – w tym wypadku tiosiarczan.
Autotrof – źródłem węgla jest jego dwutlenek – w składzie pożywki węgiel NIE WYSTĘPUJE.
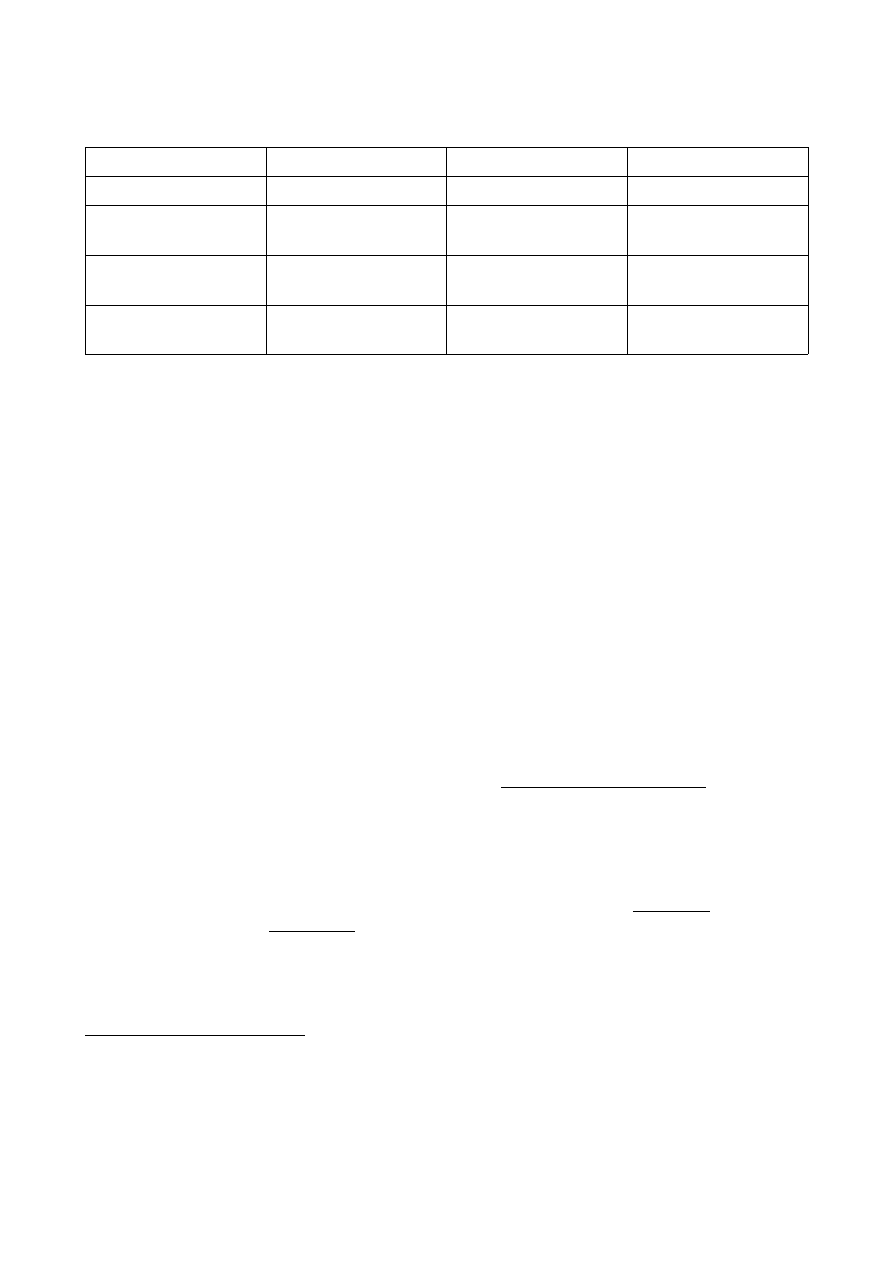
A to jest ładna tabelka:
Żywotko
AO
AB
TYP POKARMOWY
B. subtilis
+
-
chemoorganoheterotrof
Halothiobacillus
neapolitanus
-
+
chemolitoautotrof
Paracoccus versutus
++
+
Chemolitoautotrof
warunkowy
Micrococcus luteus
+
-
Chemoorganoheterotro
f
–
[Nie rośnie]
+ [Rośnie ok]
++ [Dla podkreślenia, że rośnie lepiej na agarze odżywczym, niż podłożu mineralnym]
Obecność nitryfikatorów w glebie
Bierzemy grudkę gleby, rozrabiamy ją z wodą i przenosimy na podłoże mineralne ze źródłem azotu
w postaci soli amonowej (NH4)6Mo7)24. Oczywiście jest też niezaszczepiona kontrola.
Po inkubacji do obu probówek dodajemy kropli mieszaniny alfa-naftyloaminy z kwasem
sulfanilowym lub odczynnik firmy Merck (i chyba tego ustrojstwa używało się na ćwiczeniach).
Pojawienie się różowego zabarwienia świadczy o pojawieniu się azotynów w próbie.. a więc –
bakteryjki utleniły sobie azot w postaci amonowej do azotynów. I takie też były wyniki – różowe
zabarwienie pojawiło się na granicy faz.
Obecność bakterii wiążących azot w glebie:
Co nieco już tam wyżej o nich napisałem, więc nie będę się powtarzał.
W każdym razie: sialiśmy na mineralne podłoże bezazotowe bakterie z grudki gleby. Jako, że
panują tam warunki tlenowe, wyrósł Azotobacter w postaci śluzowatej błonki.. wiadomo dlaczego ;]
Nie pamiętam, co tam dalej robiliśmy, ale chyba stosowaliśmy płynną pożywkę bezazotową, która
wypełniała probówkę po same brzegi. Zapewniało to warunki beztlenowe. Na samym dole wyrosły
śmierdziele. Dlaczego na dnie? Bo tam najmniej tlenu. Clostridium acetobotulinum, pewnie było
tam pełno innych bakterii z rodzaju Clostridium... może jakieś perfringens.. hm.. w każdym razie
dzięciołki te przeprowadzają fermentację masłową i to nie pachnie za ładnie.
Bez odpowiedzi pozostaje dla mnie to, skąd te bakteryjki biorą azot cząsteczkowy w zamkniętej
fiolce. Na dół nie dochodzi za bardzo tlen, ale nie dochodzi też specjalnie azot.
Hmm... jedyne, co mi przychodzi do głowy, to to, że albo bakterie te nie są wrażliwe na tlen w
niewielkiej ilości (np. posiadają jakieś mechanizmy typu leghemoglobina u Rhizobium – oczywiście
tutaj cały czas mowa o Clostridium, które nie mają tego wynalazku) i wystarczą im niewielkie
ilości azotu.
Żelazo
Tego chyba nie było robionego na ćwiczeniach, ale podany był przykład: żelazo potrafi utleniać
Acidithiobacillus ferrooxidans. Może to robić w niskim pH... może dlatego, że żelazo na II stopniu
utlenienia jest wtedy nieco stabilniejsze [tak było chyba podane w skrypcie], chociaż nie wydaje mi
się, aby to do końca była prawda, bo żelazo na II stopniu utlenienia jest ogólnie dość mało stabilne i
ulega utlenieniu do III... ale załóżmy, że to, co jest napisane w skrypcie na egzamin jest prawdą.
Wykorzystywanie różnych źródeł węgla
Wykorzystano tu trzy rodzaje podłóż...:
Agar + skrobia
Agar + mleko
agar z tłuszczem
1. Escherichia coli
2. Bacillus subtilis
3. Pseudomonas fluorescens
Agar odżywczy + skrobia
Żywotko
Rośnie ($), nie rośnie (&)
E. coli
&
B. subtilis
$
Agar odżywczy + mleko
Żywotko
Rośnie ($), nie rośnie (&)
E. coli
&
B. subtilis
$
Agar odżywczy + tłuszcz
Żywotko
Rośnie ($), nie rośnie (&)
E. coli
&
Pseudomonas
fluorescens
$
Wykorzystano także podłoże EMB
Na trzeciej stronie opisano charakterystykę podłoża EMB. Dla przypomnienia: inhibicja wzrostu
gram+, gram- zezwolenie na wzrost.
Dodatkowo typ dziki (wild type), naturalnie metabolizujący laktozę, będzie lśnił na zielonkawo.
Lac -, czyli mutant, nie powinien... i tak jest w istocie. Zresztą prędzej spodziewać się można
hiszpańskiej inkwizycji, niż aby mutant Lac- lśnił na zielonkawo

NOBODY EXPECTS THE SPANISH INQUISITION!!!
eee.. tak.
Komentarz do wykorzystania różnych źródeł węgla przez bakterie:
Po inkubacji hodowli w różny sposób uwidoczniano to, czy bakteryjki potrafią wcinać różne
związki, czy też nie potrafią:
Agar odżywczy + skrobia: Hodowlę zalano płynem Lugola, którego składnik wiążąc się ze
strukturą polisacharydu, jakim jest skrobia, wybarwia ten wielocukier na kolor granatowoczarny.
Zhydrolizowana przez opisane na początku enzymy skrobia nie jest barwiona przez płyn lugola,
dlatego pojawią się typowe jasne łysinki w miejscach, gdzie została zhydrolizowana skrobia.
Jak widać, E. coli nie potrafi hydrolizować wielocukrów.
Program: hydroliza.SAS
Start;
gdybanie.value=1;
E. coli żyje w przewodzie pokarmowym człowieka i innych zwierząt;
E. coli musiała przywyknąć do pobierania zhydrolizowanych przez amylazy cukrowców;
E. coli więc, mimo bycia bakterią gram-, które w przestrzeni peryplazmatycznej posiadają od
zadziubdziusiowania różnych enzymów, nie produkuje enzymów hydrolitycznych;
gdybanie.value=0;
End;
Agar odżywczy + mleko
O, tutaj to się cyrk zaczyna. Jak zwykle przy omawianiu mleka.
Co próbowaliśmy wykazać w tym doświadczeniu?
Próbowaliśmy wykazać, czy nasza bakteryjka dysponuje enzymem hydrolizującym kazeinę... i
tylko tyle.
Mimo że znaczek „&” wskazuje, że E.coli „nie rośnie” na mleku, to nie jestem przekonany, czy jest
to do końca poprawne.
Owszem, nie ma proteaz odpowiedzialnych za koszenie kazeiny, dlatego na podłożu nie pojawiają
się łysinki-ciapeczki (przejaśnienia), ale nie jestem do końca przekonany, czy to, że ona tam „nie
rośnie”, a co mam zapisane w zeszycie, jest prawidłowe.
Dlatego, że przecież dodaliśmy tam agar odżywczy. W agarze odżywczym znajduje się
przyswajalne źródło azotu w postaci aminokwasów. Bakteria więc powinna sobie normalnie rosnąć,
wykorzystując laktozę z mleka oraz źródło azotu z agaru odżywczego. Zwłaszcza, że to prototrof.
/pytanie na konsultacje/
Mleko jest obrzydliwe i nie wiem, jak ludzie mogą to pić, ale bez przesady, to bakteria.
W batalii wygrał B. subtilis, który posiada odpowiednie proteazy.
Wydaje mi się, że E. coli nie posiada proteaz z takiego samego powodu, z jakiego nie hydrolizuje
skrobii...
Agar odżywczy + tłuszcz
Teraz sprawa rozchodzi się o to, czy nasze małe żywotka posiadają odpowiednie lipazy.
Jak zwykle E. coli dostaje po nerkach (nerkach filozoficznych. E. coli jest prostym organizmem i
nie posiada nerek) i nie potrafi hydrolizować tłuszczów.
Hodowlę zalewamy Siarczanem miedzi... W wyniku rozkładu tłuszczów powstaje glicerol + kwasy
tłuszczowe, a także aldehydy. Stąd pochodzą grupy OH (o ile czegoś nie pochrzaniłem), które dają
Cu(OH)
2
, który to daje szmaragdowe zabarwienie na szalce....z Pseudomonas fluorescens, tak więc
widać, że potrafi ona hydrolizować triacyloglicerole.
W 1990 roku w Burkina Faso komentator sportowy Jacek Gmoch założył się z lokalnym przywódcą
plemiennym, o to, który szczep bakterii przygotowany przez zgromadzenie magów lepiej upłynni
żelatynę. Polak postawił na
B. subtilis.
Wódz nie wiedział, że w sytuacji, gdy w Polsce nie ma
stadionów ludzie sportu mają czas na zgłębianie innych spraw. To był jego błąd...
Mamy trzy probówki. W jednej jest żelatyna – sama.
Jest to też próba kontrolna.
Probówka nr2: żelatyna + E. coli
Probówka nr3: żelatyna + B. subtilis
Wyniki:
Kontrola czysta
Probówka nr2: E. coli rośnie w miejscu wkłucia, ale nie upłynnia żelatyny.
Probówka nr3: B. subtilis upłynnia podłoże.
Wnioski:
E. coli nie ma żelatynazy, a B. subtilis ma obciach, bo .. żelatynaza.. jejku, co za nazwa.
Wykorzystywanie różnych źródeł azotu u mikrobów:
Jak mawia stare przysłowie XIII-wiecznych anglosaskich archeologów: „im bardziej zredukowane
źródło azotu, tym chętniej pobieranym jest”.
Jak uczy życie, czasami podania ludowe bywają potwierdzane praktyką laboratoryjną i analityczną.
Tym razem XIII-wieczni anglosascy archeolodzy również się nie mylili:
Zredukowane źródła azotu są przez bakterie chętnie pobierane, gdyż potrzeba mniej energii, aby
wykorzystać je jako źródło azotu.
Wyobraźmy sobie następującą sytuację: jesteśmy przeciętnym studentem, mamy ochotę na frytki.

W ogródku mamy ziemniaki. Wykopanie ich, obranie i przygotowanie z nich frytek jest znacznie
bardziej pracochłonne, niż kupienie gotowych frytek w sklepie.
Bakteria ma podobnie z azotem. Zredukowany azot w postaci amonowej jest dla nich paczką z
frytkami. Amoniak ten przy pomocy syntetazy glutaminy jest włączany do glutaminy, a więc
wchodzi w skład bakteryjnych aminokwasów.
Również świetnie przyswajalne są gotowe aminokwasy z wszelakich mięsnych hydrolizatów.
Kiedy jednak nie ma zredukowanych form azotu w środowisku....
To wtedy trzeba wziąć motykę i zacząć kopać ziemniaki na frytki.
A więc bakteria musi sobie najpierw zredukować azotany do takiej formy, jaka może być
wykorzystana przez syntetazę glutaminy i zachodzi do dzięki reduktazie azotanowej asymilacyjnej,
która redukuje azotan do azotynu.
Azotyn do amoniaku jest redukowany już poprzez reduktazę azotynową. Związkami pośrednimi w
procesie redukcji są prawdopodobnie nitroksyl i hydroksyloamina.
Problem pojawia się jednak tutaj, że nie wszystkie bakterie mają enzymatyczne motyki...
Zrobiliśmy więc doświadczenie, aby znaleźć, która z bakterii jest powiernikiem motyki:
Źródło azotu
E. coli
B. subtilis
NH4
+
+
HNO3
-
+
Hydrolizat kazeiny
+ +
+ +
++ oznacza, że bakteria rośnie sobie lepiej, niż gdy ma w tabelce jeden plus.
No... to chyba nie wymaga komentarza.
Dlatego skomentuję: E. coli nie posiada reduktazy azotanowej asymilacyjnej... co nie znaczy, że w
warunkach beztlenowych nie może przy pomocy reduktazy azotanowej dysymilacyjnej
wykorzystywać azotanów jako akceptorów elektronów, ale to inna para skarpet.
Bacillus subtilis posiada z kolei reduktazę azotanową asymilacyjną i ciekawostka: posiada też
dysymilacyjną.
Żeby dopełnić obrzędu znęcania się nad nieszkodliwymi mikroorganizmami, sprawdzono, które
bakteryjki są prototrofami, a które auksotrofami.
Przygotowano podłoże dla prototrofa, w któym oprócz soli Davisa znajduje się glukoza – jedno
źródło węgla.
Przygotowano też podłoże Davisa dla auksotrofa wzbogacone o tiaminę i tyminę... nie mam
zielonego pojęcia, po co.. chyba tylko po to, żeby pokazać, że w obrębie jednego gatunku mogą
istnieć szczepy będące auksotrofami i prototrofami. Nie pamiętam szczegółów, ale to wyglądało
tak, że jednen szczep nie potrafił rosnąć bez pewnego składnika, podczas gdy inny mógł. Tak
naprawdę, wydaje mi się, że trzecia kolumna tej tabelki mogłaby nie istnieć, bo skoro bakteria
rośnie na agarze odżywczym, a nie rośnie na podłożu dla prototrofa, to jest auksotrofem.
W praktyce wyglądało to tak:
(trzeba przewinąć w dół lub odwrócić kartkę, bo zrobiłem do tego tabelkę)
O, jest tutaj:
Żywotko
Agar odżywczy
Podłoże dla prototrofa
(Sole Davisa +
glukoza)
Podłoże
dla
auksotrofa
E. coli (wt) – wild type +
+
+
E. coli AB 1157
+
-
-
E. coli MG 1693
+
-
+
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Miejsce na komentarz po konsultacjach.
Wnioski ogólne:
Typ dziki E. coli jest prototrofem. Dla szczepu AB 1157 podłoże dla auksotrofa opisane wcześniej
to za mało, aby wyrósł. Potrzebuje on pewnych dodatkowych składników, których nie
dostarczyliśmy do podłoża.
W ten oto sposób przebrnięto przez brutalny i niebezpieczny świat metabolizmu łagodnych i
zupełnie niegroźnych mikroorganizmów i można by rzec, że znamy się na metabolizmie
bakteryjnym...
... gdyby nie procesy oddechowe.

Procesy oddechowe u mikroorganizmów:
Można by rzec, że istotą oddychania jest produkcja ATP oraz reduktorów w postaci NADH.
Odbywa się to kosztem utlenienia pewnych substancji, które są donorami elektronów.
W oddychaniu tlenowym elektrony z NADH przenoszone są na coraz to kolejne przekaźniki, przy
jednoczesnym wyrzucie protonów poza błonę (mikroorganizmy nie mają mitochondriów, więc ich
łańcuchy oddechowe zlokalizowane są na błonie komórkowej) komórkową i ich powrót przez błonę
wiąże się z syntezą ATP przy udziale odpowiednich... syntetaz ATP. Proces ten wymaga pewnego
ostatecznego akceptora elektronów, dzięki któremu przenośniki elektronów mogą ulec reutlenieniu i
pobrać kolejne protony/elektrony. U organizmów tlenowych, ostatecznym akceptorem elektronów
jest tlen, który ulega redukcji do wody.
O ile fermentacja może w pewnych warunkach zachodzić w komórkach eukariotycznych i w
intensywnie pracujących mięśniach bywa wręcz faworyzowana bardziej, oddychanie tlenowe, w
wyniku którego wytwarzana ilość ATP jest niedostateczna, tak oddychanie beztlenowe zachodzi już
tylko u bakterii i archeonów.
Oddychanie beztlenowe jest niczym innym, jak ... oddychaniem bez tlenu, a więc wykorzystaniem
innych akceptorów elektronów, niż tlen. Akceptorem tym mogą być siarczany, azotany itd. itp.
Z kolei fermentacja jest procesem, gdzie występuje wewnętrzny akceptor elektronów,
wyprodukowany w komórce bakteryjnej, dzięki któremu może zajść reutlenienie NAD i glikoliza
może mieć ciągłość.
Ale, żeby wszystko miało swoją nazwę:
Tlenowce względne:
Tlenowce warunkowe/względne wykorzystują tlen w metabolizmie i zawsze rosną lepiej, gdy jest
tlen w środowisku, ale gdy tlenu nie ma, to radzą sobie, bo przerzucają się na fermentację, bądź
oddychają beztlenowo. Przykład: E. coli. Najlepiej rośnie, gdy dostęp tlenu jest bardzo dobry, co
oznacza, że w labie hodujemu ją z wytrząsaniem i napowietrzaniem.
Jeżeli nie ma tlenu, to E. coli
należąca do Enterobacteriacae przeprowadza fermentację kwasów
mieszanych... a potrafi i oddychać beztlenowo. Jest to zresztą związane z ich trybem życia.
Tlenowce bezwzględne:
Zwierzęta, np.: ludzie, myszy, kozy, owce i wiele innych. Właściwie to wszystkie zwierzęta.
Mikroaerofil:
Te najbardziej kapryśne. Bez tlenu nie jest im dobrze, ale gdy za dużo tlenu, to też jakoś tak
nieswojo. Przykładem jest Campylobacter jejuni, który mieszka w miejscowości Rozwolnienie
Dolne i jest odpowiedzialny za biegunki. Maksymalna zawartość tlenu atmosferycznego dla tej
bakterii jest dość niska. Historia związana z tą bakterią jest taka, że gdy powoływano konwent
biegunkowych arcymagów do badania, co też te biegunki powoduje, to bakteria ta ginęła w trakcie
transportu, dlatego magowie przez spory czas nie doceniali jej roli. Dopiero odpowiednie metody
hodowli w warunkach obniżonej zawartości tlenu pozwoliły rozwiązać rozwolnioną zagadkę.
Innym przykładem mikroaerofila jest Magnetospirillum magnetotacticum. Bakteria ta posiada
specjalne struktury – magnetosomy, dzięki którym kieruje się w kierunku bieguna Ziemi, a więc
zanurza się głęboko w wodę, gdzie stężenie tlenu jest zdecydowanie mniejsze, niż na powierzchni.
Beztlenowce
Nie wykorzystują tlenu jako końcowego akceptora elektronów, czyli będą miały albo metabolizm
fermentacyjny (taki mają różnego rodzaju laseczki należące do rodzaju Clostridium Clostridium
perfringens – bakteria zgorzeli gazowej
Metaboilzm taki prowadzą też bakterie mlekowe – mtabolizm fermentacyjny.
Są też takie beztlenowce, które mają metabolizm oddechowy, a więc łańcuch oddechowy, tylko

wykorzystują inny akceptor, niż tlen.
Wśród beztlenowców są dwie grupy:
–
aerotolerancyjne
– chociaż nie wykorzystują tlenu, to tolerują jakiś okres przebywania w
środowisku tlenowym i tlen nie zabija ich natychmiast. Ta tolerancyjność zależy od mikroba:
przykład – laseczka zgorzeli gazowej (zakaża rany). Musi toleroawać pewną ekspozycję na tlen.
–
Beztlenowce bezwzględne
– nawet krótka ekspozycja na tlen im szkodzi. Przykład – bakterie
redukujące siarczany, archeony redukujące siarczany, archeony metanogenne, bakterie
homoacetogenne.
Beztlenowce bezwzględne należy hodować w anaerostatach. Są to rządzenia do przechowywania
różnych żywotek „bez tlenu”, a dokładniej z obniżonym jego stężeniem, gdyż znajduje się tam
związek, który wiąże tlen i obniża jego stężenie.
Inna metoda hodowli bakterii w atmosferze beztlenowej, to metoda na „Resident Evil”. Któż nie
pamięta wstępniaka z tego filmu, gdzie „naukowiec” wkładając ręce do odpowiednich rękawic
zamontowanych jako część komory kradnie próbkę wirusa i zmienia pół miasta w żywe trupy.
Tam jest dość podobnie... ale tylko pod względem rękawic i komory, w której jest atmosfera
beztlenowa. Najczęściej po prostu komora taka przewiewana jest mieszaniną gazów neutralnych.
Bogatsze laboratoria mogą mieć nawet całe pomieszczenia przeznaczone do pracy z bakteriami
beztlenowymi.
Dlaczego beztlenowce bezwzględne są tak wrażliwe na tlen?
Tlen w formie podstawowej to tzw. tlen tripletowy, natomiast jeśli pewne związki występujące w
komórce, jak chlorofile, bakteriochlorofile, cytochromy, czy flawiny zostaną wzbudzone przez
światło i przekażą energię tego wzbudzenia właśnie na cząsteczkę tlenu tripletowego, to zostaje on
przekształcony w tlen singletowy, a jest to bardzo reaktywny czynnik utleniający, który działa
toksycznie na komórki.
W przypadku bakterii występujących bezpośrednio w powietrzu, które są wrażliwe na
promieniowanie UV, występują u nich karotenoidy, które przekształcają tlen singletowy ponownie
w tripletowy.
W czasie procesów oddechowych mogą powstawać następujące ROS:
1) anionorodnik ponadtlenkowy
O2 + e- ----> O2
-.
2) Nadtlenek wodoru
O2-. + e + 2H+ ---> H2O2
3) Rodnik hydroksylowy
H2O2 + e- + H+ --> H2O + OH
.
Anionorodnik ponadtlenkowy jest bardzo reaktywny i może spowodować zniszczenie lipidów i
innych składników komórkowych. Jest najprawdopodobniej tworzony w małej ilości w czasie
normalnych procesów oddechowych. Powstaje też w wyniku połączoneo działania światła i
barwników. Flawiny, flawoproteiny, chinony, białka żelazowo-siarkowe przeprowadzają
jednoelektronową redukcję O2 do O2
-.
Nadtlenek wodoru
Powstaje w czasie normalnych procesów oddechowy przez dwuelektronową redukcję tlenu, co
zwykle zachodzi przy udziale flawoprotein.

Rodnik hydroksylowy
Jest najbardziej reaktywną formą tlenu. Jest nasilniejszym ze znanych czynników utleniających,
zdolnym do zaatakowania każdej cząsteczki organicznej na terenie komórki. Ma on bardzo krótki
czas trwania (1/10 000 s)
Organizmy tlenowe posiadają dodatkowo szereg enzymów, które pozwalają im radzić sobie z
reaktywnymi formami tlenu.
1) Dysmutaza ponadtlenkowa
2O2-. + 2H+ ---> O2 + H2O2
Dysmutaza ponadtlenkowa
W przypadku E. coli w centrum aktywnym dysmutazy ponadtlenkowej występują atomy żelaza
(dysmutaza ponadtlenkowa jest takim fajnym enzymkiem, że u różnych organizmów występują
różne metale w centrum aktywnym, jak miedź, czy cynk)
Fe3+~ENZYM + O2−. → Fe2+~ENZYM+ O2
Fe2+~ENZYM + O2−. + 2H+ → Fe3+~ENZYM + H2O2.
Tak więc atom żelaza w centrum aktywnym enzymu jest dresiarzem. Łapie niewinną cząsteczkę
anionorodnika ponadtlenkowego, zabiera mu elektron, redukując (tudzież zniżając) się do jeszcze
niższego poziomu, niż wcześniej i wypuszcza już nie anionorodnik ponadtlenkowy, a tlen..
pozbawiony swojego elektronu.
O ile jednak na terenie Polski sytuacja, w której dresiarz płaci komuś za szkody jest nie do
pomyślenia, o tyle sądownictwo bakteryjne działa nadzwyczaj sprawnie. Bakterie dysponują w
pewnym względzie dość wysoką kulturą (stąd też określenie kultury bakterii), gdyż sędzia nakazuje
atomowi żelaza związanemu z enzymem nie dość, że oddać skradziony elektron, to jeszcze
pozwolić na dołączenie się dwóch protonów. Dochodzi wtedy do reutlenienia żelaza, a
zredukowana cząsteczka to nic innego, jak H2O2.
Na następnej stronie jest jeszcze kilka innych fajnych rysunków i reakcji.

2) Katalaza
2H2O2 --> O2 + 2H2O
Obrazek dla lepszego efektu. To ładne w kolorze.
Katalaza jest czterołańcuchowym tetramerem, z których każdy ma długość 500 aminokwasów.
Posiada cztery grupy hemowe, które pozwalają enzymowi reagować z nadtlenkiem wodoru.
Dlaczego katalaza potrzebuje 2 cząsteczki nadtlenku wodoru? - absolutnie nieprzydatne na
ćwiczenia, ale może komuś łatwiej będzie zapamiętać.
Reakcja przeprowadzana przez katalazę przebiega w dwóch etapach:
H2O2 + Fe(III)-E → H2O + O=Fe(IV)-E(.+)
H2O2 + O=Fe(IV)-E(.+) → H2O + Fe(III)-E + O2
Fe()-E oznacza tutaj centrum żelazowe grupy hemowej „przyklejone”;) do enzymu. Fe(IV)-E(.+)
jest mezomeryczną formą Fe(V)-E, co oznacza, że żelazo nie jest tu kompletnie utlenione do +V,
ale dostaje pewien dodatkowy elektron od hemu.
Jak nadtlenek wodoru pcha się z butami do centrum aktywnego enzymu, reaguje z Asparaginianem
w pozycji 147 i histydyną w pozycji 74, powodując skok protonu między atomami tlenu.
Uwolniony atom tlenu koordynuje, uwalniając nowo utworzoną cząsteczkę wody i Fe(IV)=O. Z
kolei ten reaguje z kolejną czsteczką nadtlenku wodoru sprawiając, że odtwarza się Fe(III)-E przy
wypluciu tlenu cząsteczkowego, a to, co jeszcze pozostaje, to cząsteczka wody.
Odtworzona forma Fe(III)-E może wejść w kolejną reakcję i przyłączyć następny atom tlenu.
Jest to enzym bardzo szybki i aktywny: jedna molekuła potrafi rozłożyć milion cząsteczek
nadtlenku wodoru w ciągu sekundy.
3) Peroksydaza
H2O2 + NADH + H+ ----> 2H2O + NAD
To też ładne.

Nasze tlenowe żywotka mają więc nieco łatwiejsze życie, niż ich beztlenowi koledzy, gdyż ci
drudzy nie mają wszystkich, bądź niektórych enzymów służących do dekapitowania reaktywnych
form tlenu.
Taki mikroaerofil, jak Campylobacter jejuni nie ma np. katalazy, więc jak go przewietrzymy, to jest
mu bardziej smutno, niż E. coli
Wreszcie należy zauważyć, że powyższe enzymy na różnych etapach blokują powstawanie rodnika
hydroksylowego, który jest niesłychanie wrednym badziewiem.
Hodowla względnych beztlenowców:
Jak widać, hodowla bezwzględnych beztlenowców jest dość niewygodna. Trudno wyobrazić sobie
grupę 12 studentów w sali pełnej azotu z butlami tlenowymi przy boku. Nie zawsze też są komory i
anaerostaty, dlatego na zajęciach męczymy warunkowe beztlenowce, które możemy hodować na
rozmaite sposoby:
–
usuwając tlen i chroniąc bakteryjki przed jego działaniem
–
siejąc na jednej szalce bakterie tlenowe i beztlenowe. Szalkę rzecz jasna obwiązujemy
parafilmem. Wówczas bakterie tlenowe zużyją część tlenu i ich wzrost zostanie zahamowany,
podczas gdy pozwoli to na wzrost bakterii beztlenowych.
–
W płynie:
Można stosować wysoki słup podłoża. Im więcej tlenu pod korek, tym mniej powietrza.
Dodatkowo można zabezpieczyć hodowlę parafiną, przez którą tlen nie będzie za bardzo
dyfundował.
–
Dodatkowo zawsze można posiać na niskim słupie, by sprawdzić, czy bakteryjka radzi sobie
równie dobrze, czy lepiej.
–
A i można dodać sacharozy, która obniża potncjał redukcyjny... choć my na ćwiczeniach
dodajemy glukozy. Wiele reakcji enzymatycznych to reakcje oksydoredukcyjne, gdzie jeden
element karuzeli się utlenia, drugi redukuje. Zdolność organizmu do przeprowadzania reakcji
oksydoredukcyjnych zależy od potencjału redukcyjnego.
Wykazano, że tlenowe mikroorganizmy mogą być aktywne tylko w zakresie dodatnich wartości
potencjału redukcyjnego, podczas gdy beztlenowce dają sobie radę w niższym potencjale.
–
Podgrzanie i szybkie schłodzenie: wraz ze zwiększaniem się temperatury cieczy,
rozpuszczalność gazów w niej maleje. Jeśli dodamy agaru i szybko schłodzimy, to ograniczymy
prądy konwekcyjne i mieszanie, przez co tlen nie będzie z dużą wydajnością dyfundował do
żelu.
–
Zastosowanie anaerostatów.
Jak bakterie pozyskują energię?
W wyniku fosforylacji oksydacyjnej – a więc podczas powrotu protonów przez ATP-azy i
produkcję ATP. Ogólnie... łańcuch oddechowy.
W wyniku fosforylacji substratowej – reakcji chemicznej, która ma miejsce, gdy reszta fosforanowa
zostanie przeniesiona bezpośrednio do ADP przy wykorzystaniu energii organicznego substratu.
Ten sposób ładowania ATP nie wymaga udziału tlenu i zachodzi w glikolizie oraz cyklu Krebsa.
Elektrony płyną ze związków o niższym potencjale do związków o potencjale wyższym.
Oczywiście w komórkach dzieje się to stopniowo – elektrony człapią sobie powoli w kierunku
związków o wyższym potencjale, a te przekazują je na związki o jeszcze wyższym potencjale itd.
Można powiedzieć, że im niższy potencjał oksydoredukcyjny ma donor elektronów i im wyższy
potencjał oksydoredukcyjny ma akceptor, tym więcej energii uzyskamy, dlatego, że po drodze
zwiększy się możliwa liczba przekaźników pośrednich, które będą mogły pośredniczyć w
przekazaniu protonu na zewnątrz błony.
Słowem – im z większej wysokości skaczemy, tym z większym impetem rąbniemy na podłogę.
Tak to już jest w przyrodzie, że układ tlen/woda ma najwyższy potencjał oksydoredukcyjny i inne
akceptory mają niższy.
Dlatego więc łańcuchy oddechowe oparte na innych akceptorach będą krótsze, a więc i zysk
energetyczny będzie niższy.
Przykłady akceptorów:
Siarka
tlen
azotany
siarczany
związki organiczne
Kurczę, już dawno tabelek żadnych nie było. Nieprofesjonalnie to wygląda.
Przykłady nieorganicznych akceptorów
Przykłady organicznych akceptorów
NO3 – akceptor podczas denitryfikacji.
Produktem jest zredukowana forma, czyli NO2
Sulfotlenek dimetylu – siarczek dimetylu
SO4 do SO3 – oddychanie siarczanowe
Tlenek trimetyloaminy - trimetyloamina
Fe3+ do Fe2+ - żelazowe
Fumaran - bursztynian
CO2 do CH4 – bakterie metanogenne
CO2 do CH3COO- bakterie homoacetogenne
Siarkofrutacja ;>
... fermentacja:
Glukoza w glikolizie daje ATP. Zredukowany zostaje NAD do NADH i szafa gra... ale zapasów
NADH nie ma nieskończoność. O ile w łańcuchu oddechowym NAD zostawał reutleniony po
oddaniu elektronów na ostateczny akceptor, tak tu, łańcucha oddechowego niet.
Ale jak się nie ma, co się lubi, to się... kradnie lub korzysta z tego, co jest:
W najprostszej fermentacji akceptorem końcowym jest pirogronian.
Ten pirogronian zostaje zredukowany, NAD jest zregenerowany i może ponownie wchodzić do
glikolizy jako akceptor elektronów i powstaje produkt końcowy fermentacji – w tym wypadku
mleczan.
Fermentacja jest więc sposobem uzyskania energii, gdzie zw. Organiczny jest utleniany, ATP
powstaje w wyniku fosforylacji substratowej, w wyniku przeniesienia fosforanu ze związku o
wysokim potencjale przenoszenia grup fosforanowych na ADP.
Takich związków jest sporo, więc pewnego dnia zebrał się krąg magów, którzy ustalili, że odtąd
fermentacje będą nazywały się od głównego produktu powstającego w reakcji fermentacji.
–
fermentacja mlekowa
–
fermentacja masłowa
–
fermentacja alkoholowa
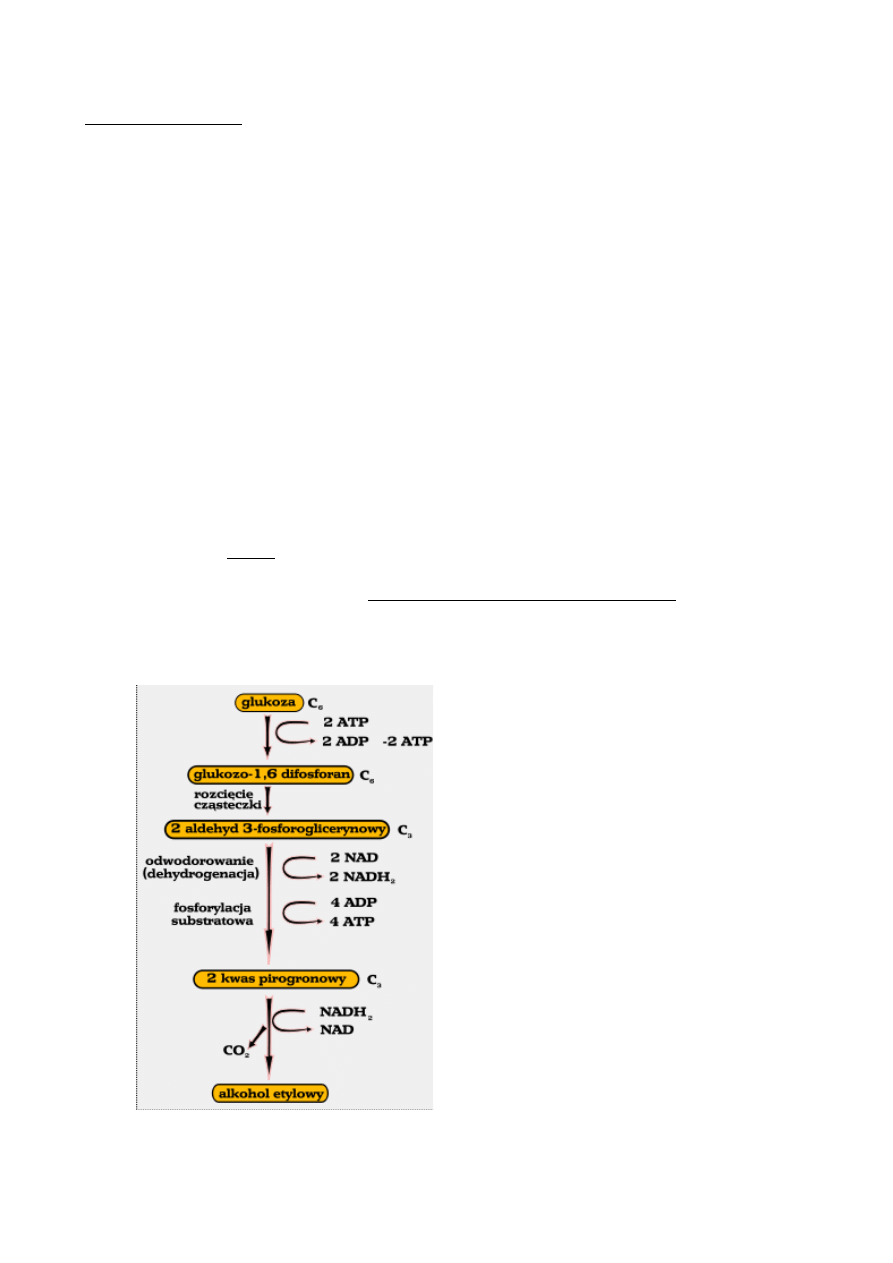
Rodzaje fermentacji
1. fermentacja homomlekowa
np. od glukozy do mleczanu. Końcowym akceptorem jest pirogronian, a proces ten
przeprowadzają np. Lactobacillus acidofilus, E. faecalis, Streptococcus lactis
2. fermentacja heteromlekowa
Kiedy oprócz mleczanu pojawiają się jeszcze jakieś produkty, np:
glukoza -> CO2 + mleczan + etanol
Końcowe akceptory to np. pirogronian i aldehyd octowy (z niego powstaje etanol).
3. Czyli fermentacja typu Enterobacteriacae – przeprowadzają ją bakterie z tej rodziny. Do tej
rodziny należy Esherichia, Proteus, Salmonella, Schiegella. Wszystkie te baktrie fermentują
glukozę wytwarzając jako produkty różnego rodzaju kwasy organiczne – stąd nazwa =
fermentacja kwasów mieszanych. Cieżko powiedzieć coś o akceptorach, ale na pewno
jednym z nich jest pirogronian, skoro powstaje mleczan. Na pewno jesnym z akceptorów
jest aldehyd glicerynowy, skoro powstaje etanol.
Ale np. sposób powstawania octanu i bursztynianu jest bardziej skomplikowany.
Ważne, by wiedziec, że produktami tej fermentacji są różne kwasy organiczne, a opróćz
tego etanol, CO2, może być też wodór, jeśli bakteria, która przeprowadza fermentację ma
odpowiednie enzymy rozkładające kwas mrówkowy do CO2 i wodoru. Jeśli nie ma, to ten
wodór nie bywa produktem fermentacji. Mogą być i inne produkty fermentacji kwasów
mieszanych w zależności od warunków środowiska.
Przykład u E. coli: glukoza ---> mleczan + etanol + bursztynian + CO2 + H2
końcowe akceptory – różne
Przykład – Enterobacteriaceae (Escherichia, Proteus, Salmonella, Shigella)
+ coś tam z zeszytu:
etanol --> 2-3-butano-diol --> mleczan --> octan --> mrówczan --> H2 i CO2.
4. Fermentacja alkoholowa:
C6H12O6 ---> 2CO2 + 2C2H5OH
[ ]
[ ] -> kranik, którym zbieramy etanol.
[ ]

Fermentacja alkoholowa: główny akceptor – aldehyd octowy. Przykład: drożdże, Zymomonas
Oddychanie beztlenowe.
Denitryfikacja.
Denitryfikacja jest przykładem oddychania beztlenowego, gdzie akceptorem jest azotan(III) oraz
coraz bardziej zredukowane formy azotu.
NO3- -> NO2- -> NO -> N2O -> N2 (uwalnia się do atmosfery)
1. NO3 – NO2 – reduktaza azotanowa dysymilacyjna (należy odróżniać ją od asymilacyjnej, która
jest enzymem cytoplazmatycznym, którego synteza jest hamowana przez amoniak. Asymilacyjna
uczestniczy w redukcji azotanów w celu wykorzystania ich jako źródeł azotu).
Reakcja: NO3- + 2e- + 2H+ ---> NO2- + H2O
2,Reduktaza azotynowa
NO2- + 2e- + 2H+ ---> NO + H2O
Korzyść dla komórki w tej reakcji to pozbycie się toksycznych azotynów.
3, Reduktaza tlenku azotu
2NO + 2e- + 2H+ ----> N2O + H2O
4, Reduktaza podtlenku azotu
N2O + 2e- + 2H+ ----> N2 + H2O
Bakterie o tym profilu metabolicznym to np. Paracoccus, Pseudomonas (Proteobacteria), niektóre
bakterie gramdodatnie, jak Bacillus, czy Streptomyces.
Przykłady konkretnych gatunków: Pseudomonas stutzeri
Paracoccus denitrificans
Zwykle denitryfikatorami są warunkowe tlenowce, dla których rzecz jasna tlen jest lepszym
akceptorem, niż azotan, gdyż łańcuch oddechowy jest dłuższy i pozwala na uzyskanie większej
ilości ATP. Jeśli jednak próbujemy je wydusić, to się nie dają, bo przestawiają się na metabolizm
beztlenowy.
Oranie pola... wzrost kapusty i.. denitryfikacja
Co to ma ze sobą wspólnego?
Jeśli przyjrzymy się procesowi orania pola, zauważymy, że orając pole przewietrzamy glebę, a
wtedy wybijamy z łepetyny denitryfikację wszystkim żywotkom, które się poddusiły.
W związku z tym gleba nie zubaża się w azotany.
Drugi szkodliwy skutek denitryfikacji to to, że podtlenek azotu pod wpływem światła w górnych
warstwach atmofery zostaje zamieniony w tlenek azotu, a ten tlenek azotu poprzez ozon zostaje
przekształcony i utleniony do azotynu i te azotyny w postaci kwaśnych deszczów upadają na
ziemię. Ponadto utrata ozonu w tej reakcji również jest dla nas niekorzystna, zwłaszcza pod
względem estetycznym, gdyż to źle robi na mózg producentom filmowym.
Patrz: Two Days Before The Day After Tomorrow.
...zdecydowanie.

Część praktyczna:
1. Fermentacja mleka.
Do probówek zawierających odtłuszczone mleko z lakmusem wsiano E. faecalis, E. coli i B.
subtilis, czwartą probówkę pozostawiono jako próbę kontrolną.
2. Inkubowano i obserwowano zmianę kolorków oraz zmiany w wyglądzie pożywki.
3. Na podstawie zmian określono zdolność bakteryjek do fermentacji i peptonizacji mleka.
W środowisku kwaśnym białka ulegają wytrącaniu, dlatego w probówce, gdzie zaszczepiono
bakterie zdolne do przeprowadzania tego procesu wytrąci się kazeina jako skrzep kwaśny. Lakmus
zmieni barwę na różową, co potwierdzi zakwaszenie.
Wyniki
E. coli – przeprowadza fermentację kwasów mieszanych, a więc:
Lakmus zmienił kolor na różowy (obniżenie pH), pojawił się skrzep kwaśny, dodatkowo
zmasakrowany przez wydzielające się pęcherzyki gazu,
B. subtilis – nie fermentuje laktozy, ale wykazuje zdolność do peptonizacji kazeiny po jej
uprzednim wytrąceniu przez podpuszczkę (powoduje ona denaturację białka). W tym wypadku
obserwuje się alkalizację mleka – zmiana barwy lakmusu na niebieską. Jako, że B. subtilis ma
zdolności proteolityczne, skrzep będzie upłynniony.
E. faecalis
Fermentacja homomlekowa, a więc w środowisku pojawia się mleczan, lakmus barwi się na
różowo, nie ma pęcherzyków gazu – skrzep gładki.
2. Test redukcji błękitu metylenowego jako demonstracja intensywności procesu
oddechowego:
Im mniej silniej pobierany jest tlen z otoczenia w procesach oddechowych, tym błękit
metylenowy bardziej się odbarwia. Mieszanie probówki powoduje natlenienie próbki i
ponowne zabarwienie się błękitu metylenowego na niebiesko.
Metabioza
Następowanie po sobie w mleku różnych środowisk. Przykładowo zmiana pH przez bkterie ułatwia
życie innym organizmom.
Przykład:
Bakterie mlekowe -------pH w dół------> grzyby -----------> propionibacterium -------->bakterie
gnilne.
Określenie stosunku bakterii do tlenu
a) przygotowane w probówkach podłoża zaszczepić kroplą nocnej hodowli bulionowej wybranego
szczepu.
–
bulion odżywczy z dodatkiem 0,5% glukozy – wysoki słup podłoża;
–
bulion odżywczy – niski słup podłoża
Przed posiewem probówki z wysokimi słupami podłoże zagrzać we wrzącej łaźni i szybko
schłodzić.
b) Po posiewie – wysoki słup podłoża należy zalać jałową parafiną.
WYNIKI I WNIOSKI
Żywotko
Słup wysoki
Słup niski
E. coli
+
+
B. subtilis
-
+
P. fluorescens
-
+
Seracia marcescens
+
+
Micrococcus luteus
+
++
Pseudomonas stutzeri
+
+
Enterococcus faecalis
+
+
S. marcescens – względny tlenowiec. Dodatkowo na niskim słupie pojawiło się różowe
zabarwienie. Dostępność tlenu i niska temperatura powodują wydzielanie się barwnika u tej
bakterii.
M. luteus – z tego wynika, że jest tlenowcem względnym
MI. o... Open Office potraktował to jako podpunkt.
Enterobacteriacae – beztlenowce względne – żyją sobie w kiszkach, gdzie tlenu jest mniej, ale
dobrze sobie radzą w środowisku tlenowym.
Są też dwa tlenowce bezwzględne. Wiadomo jakie.
A teraz wszyscy grzecznie robimy bakteryjkom catalarmageddon:
Czyli zalewanie szalki z mikrobami wodą utlenioną i patrzenie, jak pojawiają się bąbelki.
Żywotko
Katalaza
E. faecalis
-
M. luteus
+
B. subtilis
+
E. coli
-

Oddychanie azotanowe
W probówkach znajduje się bulion odżywczy + KNO3. Zapewnialiśmy żywotkom w miarę stabilne
warunki beztlenowe i później patrzyliśmy po inkubacji, co im się stało:
Były 3 probówki, jedna pozostawiona jako kontrola, w drugiej E. coli, w trzeciej P. stutzeri
Żywotko
Gaz
Obecność NO2
E. coli
-
+
P. stutzeri
+
-
Jeżeli bakteria jest denitryfikatorem uwalnia się azot, który gromadzi pod postawionym do góry
nogami dnem rurki Durhama.
Po dodaniu odczynnika Mercka w probówce z E. coli pojawiła się czerwona barwa, a więc oznacza
to, że w środowisku pojawiły się azotyny.
Żywotko to ma więc reduktazę dysymilacyjną – NO2 się kumuluje i nie ma dalszych etapów
denitryfikacji.
P. stutzeri jest typowym denitryfikatorem.
Genoyp – informacja genetyzna zapisana na DNA
Prokarioty: szybko się mnożą
mają nieduży genom
intronów niet
można uzyskiwać klony
Jak zapisujemy genotyp?
F
-
108 pro met thy str
r
lac
F- nie posiada plazmidu
pro, met, thy -wymaga danego aminokwasu do wzrostu i bez niego jest zdechnięta.
Lac – nie fermentuje laktozy
str
r –
oporna na streptomycynę
str
s –
nieoporna na streptomycynę.
Fenotyp
Fenotyp zapisuje się dużą literą
Pro
+
- rośnie bez proliny
Pro
-
- nie potrafi rosnąć bez proliny
Mutacje...
zaraz... czemu ja to piszę, przecież to wiem.
Rekombinacje
Proces, gdzie następuje przerwanie ciągłości jednej lub obu nici cząsteczki DNA i połączenie z
ejdno lub dwuniciowym fragmentem innej cząsteczki DNA. Główny jej mechanizm to pęknięcie i
ponowne połączenie (and. breakage and rejoining)
homologiczna – zachodzi między cząsteczkami o komplementarnych sekwencjach
nukleotydowych
rekombinacja nieuprawniona – gdy rekombinujące cząsteczki wykazują
a) homologię ogranicznoą do bardzo krótkich odcinków – rekombinacja zlokalizowana
(specyficzna wobec miejsca)
transformacja
„goły” DNA wnika do komórki i zachodzi rekombinacja. Elektroporacja lub jak pierun brzdęknie w
rzekę.
transdukcja
fagi
transfekcja
Wprowadzanie obcego DNA do komórki, np. poprzez elektroporację.
Dobra, tyle głupot.
Jedyna radosna kwestia, jaka mi pozostaje, to to, dlaczego niby w sytuacji, w której żywotko ma
chromosom o takiej charakterystyce:
-----thy-------------met--------pro-----ORI
powstaje następujący transkoniugant:
Met+ Str
r
. Skoro uciachało coś za met, to logiczne się wydaje, że złapało i pro.

„Mikrobiologia środowiskowa”
No wai.
Nie piszę tego.
I z góry dziękuję każdemu, komu zechce się te ćwiczenia obrobić lub zostawić na jakimś kserze
lub czymś tam. Nie ma też nic za darmo.
Czcigodny notatek dostarczyciel ma szansę na otrzymanie dwóch puszek tuńczyka (obecnie
dysponuję wersją w sosie własnym i oleju).
.... oryginał posiada wmontowany otwieracz, a zdjęcie wziąłem z Google.
Wyszukiwarka
Podobne podstrony:
prezentacja mikro Kubska 2
Mikro w 1
7 Mikro i makro elementy naszej diety
Wykład 3 Mikro 1 Econ
wyk ad4 Mikro
mikro wykresy super
02a MIKRO
kol2 2006
02 01 11 11 01 44 an kol2 1 7id 3881
Zestaw 4 Mikro
SCCIAGI Z EKO!, studia UMK, Podstawy ekonomii (mikro i makro)
MIKRO ŚCIĄGI Z WYKŁADU, studia, studia II rok, mikrobiologia, mikro egz, Ściągi RAZY 2
mikro c 5 sc, Weterynaria Lublin, Weterynaria 1, Mikrobiologia
EGZAMIN Z MIKRO!!!, Medycyna Warszawski Uniwersytet Medyczny, Mikrobiologia
więcej podobnych podstron