Ćwiczenie
2
Opracowanie:
lek. wet. Jan P. Madej
Materiały do ćwiczeń dla
Wydziału Medycyny
Weterynaryjnej
Testy immunoenzymatyczne
Przeciwciała monoklonalne

Testy fazy stałej:
• test ELISA
• immunoblotting

Test immunoenzymatyczny ELISA
(Enzyme-Linked Immunosorbent Assay)
Cechy testu ELISA:
• obecność fazy stałej
• wykorzystanie przeciwciał połączonych z enzymem
(AP, HRPO), który powoduje przejście bezbarwnego
substratu w barwny produkt

I etap
opłaszczanie płytki

I etap
opłaszczanie płytki
II etap
blokowanie

I etap
opłaszczanie płytki
II etap
blokowanie
III etap
badany materiał

I etap
opłaszczanie płytki
II etap
blokowanie
III etap
badany materiał
IV etap
przeciwciało koniugowane
z enzymem

I etap
opłaszczanie płytki
II etap
blokowanie
III etap
badany materiał
IV etap
przeciwciało koniugowane
z enzymem
V etap
chromogen

1 – przeciwciało kozy anty-
białka surowicy królika
(etap I przeciwciała)
2 – normalna surowica kozy
Kontrola negatywna:
• dołek F opłaszczony albuminą
• dołek G bez I-go przeciwciała
1
2
A
1:500
1:500
B
1:1500
1:1500
C
1:4500
1:4500
D
1:13 500 1:13 500
E
1:40 500 1:40 500
F
Alb (-)
Alb (-)
G
K (-)
K (-)
H
Blank
Blank
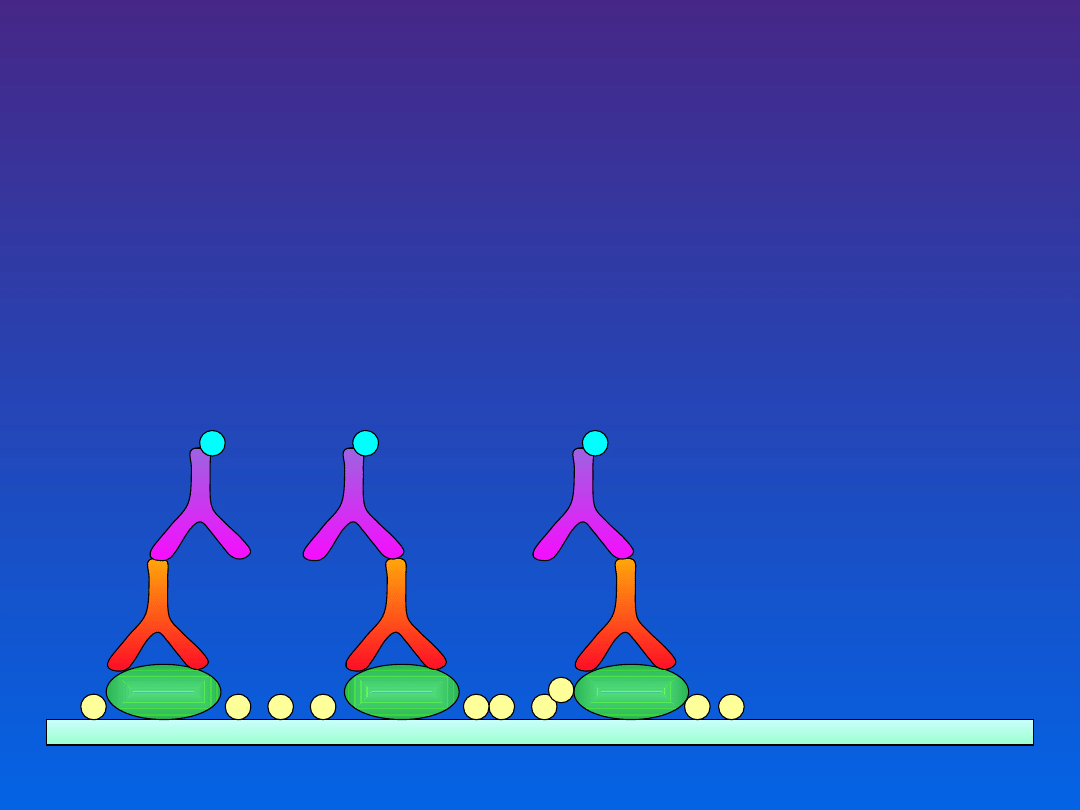
I etap
opłaszczanie płytki
II etap
blokowanie
III etap
badany materiał
IV etap
przeciwciało koniugowane
z enzymem
V etap
chromogen
Wykrywanie Ab
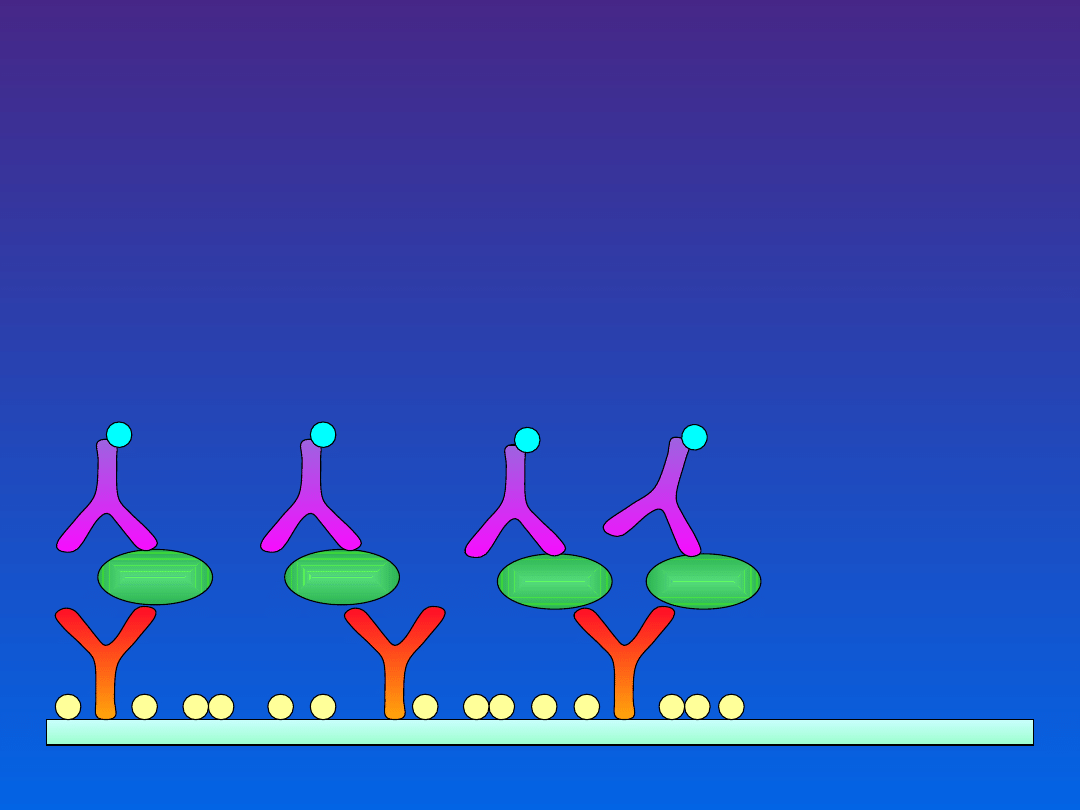
Wykrywanie Ag
I etap
opłaszczanie płytki
II etap
blokowanie
III etap
badany materiał
IV etap
przeciwciało koniugowane
z enzymem
V etap
chromogen
Najczęstsze niepowodzenia przy przeprowadzaniu testu ELISA
Problem
Proponowane rozwiązanie
1. Absorbancja kontroli z PBS
zamiast
próbki badnej >0.1
Absorbancja kontroli negatywnej
>0.2
l. Zwiększyć liczbę płukań, lepsze blokowanie
(albumina, odtłuszczone mleko, żelatyna itp.
Zwiększyć rozcieńczenie koniugatu lub użyć
koniugat oczyszczony przy pomocy
chromatografii powinowactwa, dodać do buforu
płuczącego 1-5% normalnej surowicy gatunku,
którego przeciwciała są używane do produkcji
koniugatu
2. Absorbancja kontroli wysoce
pozytywnej <0.5
2. Sprawdzić etap opłaszczania, zwiększyć
czystość antygenów lub przeciwciał używanych
do opłaszczania, wydłużyć czas inkubacji
pierwszego przeciwciała lub antygenu,
wprowadzić modyfikacje prowadzące do
amplifikacji systemu
3. Wartości absorbancji próbek
bardziej rozcieńczonych są
wyższe od próbek mniej
rozcieńczonych
3. Zwiększyć rozcieńczenie próbek
4. Wszystkie odczyty poniżej
wartości
0.1
4. Sprawdzić stabilność substratu i buforu,
sprawdzić pH buforu dla substratu, sprawdzić
okres przydatności płytek i koniugatu
5. Wyniki testu nie odpowiadają
stanowi klinicznemu pacjenta
5. Sprawdzić ewentualność występowania
przeciwciał heterofilowych

ZASTOSOWANIE
Wykrywanie przeciwciał przeciwko wirusom:
• enzootycznej białaczki u bydła
• niedokrwistości zakaźnej u koni
• pomoru u świń
• choroby Aujesky u świń
• antygenów wirusa białaczki u kotów

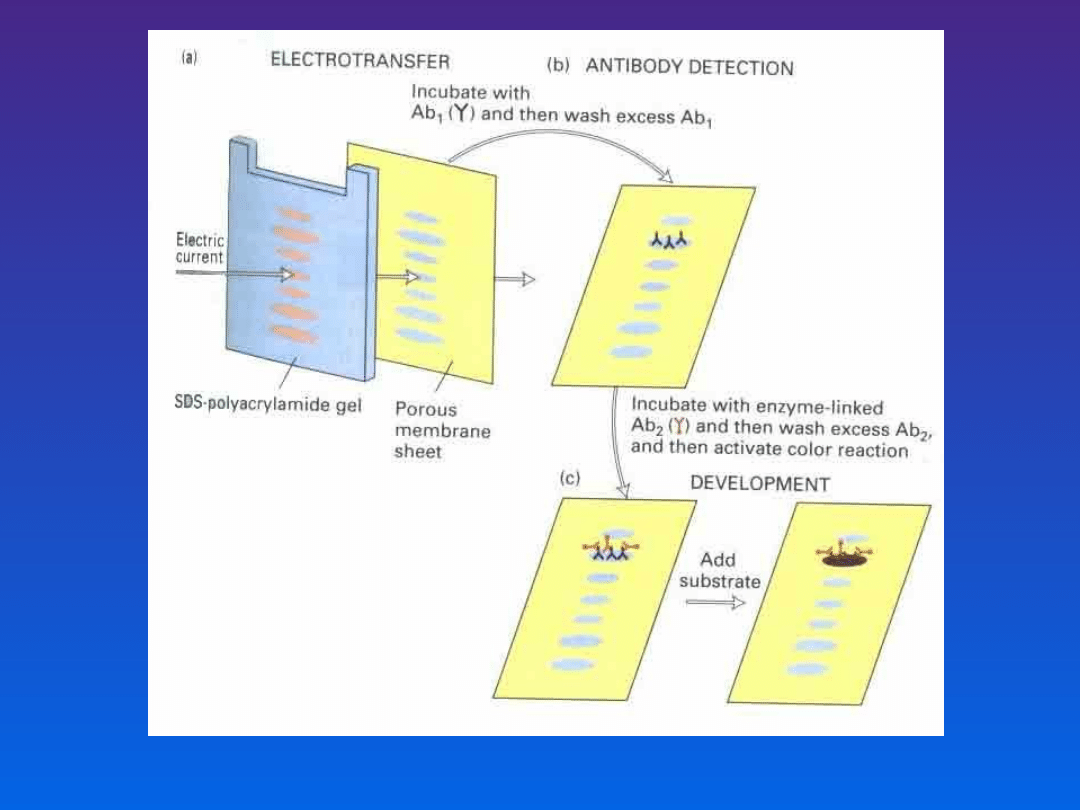
Obejmuje dwa etapy:
• rozdział elektroforetyczny w żelu (PAGE)
• immunochemiczna identyfikacja
antygenów
PAGE – poliacrylamide gel electrophoresis
elektroforeza w żelu poliakrylamidowym
SDS-PAGE – sodium dodecyl sulphat pliacrylamide gel
electrophoresis
elektroforeza w żelu poliakrylamidowym
z dodatkiem siarczanu dodecylu sodu
IMMUNOBLOTTING

Służy do określania ważnych cech Ag
białkowych:
• obecność i ilość Ag
• względny ciężar właściwy łańcuchów polipeptydowych
• stopień oczyszczenia Ag
• szczególnie polecany w pracy nad Ag nierozpuszczalnymi,
trudnymi do znakowania, ulegającymi łatwej degradacji
• określanie obecności, ilości i swoistości przeciwciał z
surowic poliklonalnych oraz ich oczyszczanie
• w połączeniu z metodą immunoprecypitacji – wykrywanie
niewielkich ilości Ag i interakcji pomiędzy antygenami
(Ed. Harlow, D Lane Antibodies. A Laboratory manual,Cold Spring Harbor laboratory, 1988)

Metoda obejmuje następujące
czynności:
• Preparacja próbki antygenu
• Rozdział elektroforetyczny w żelu
• Transfer rozdzielonych antygenów na błonę
np. nitrocelulozową (blotting)
• Blokowanie miejsc nieswoistego wiązania
• Etap przeciwciała
• Detekcja kompleksu antygen przeciwciało
(Ed. Harlow, D Lane Antibodies. A Laboratory manual,Cold Spring Harbor laboratory, 1988)
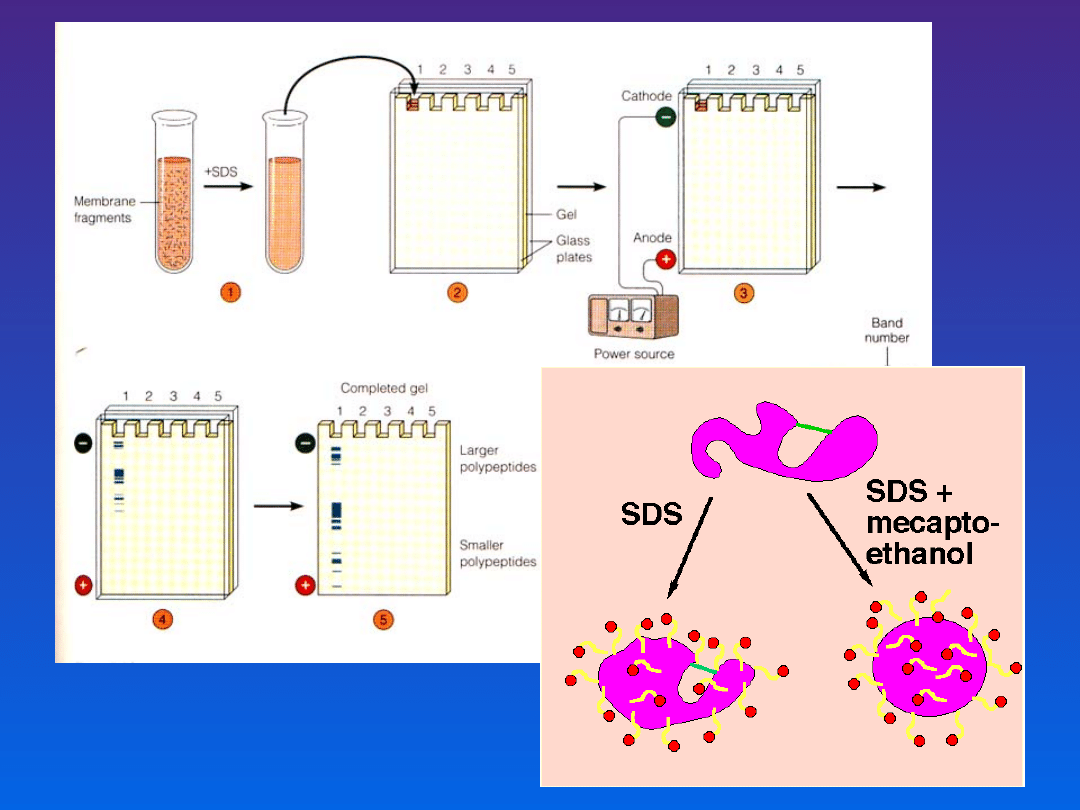
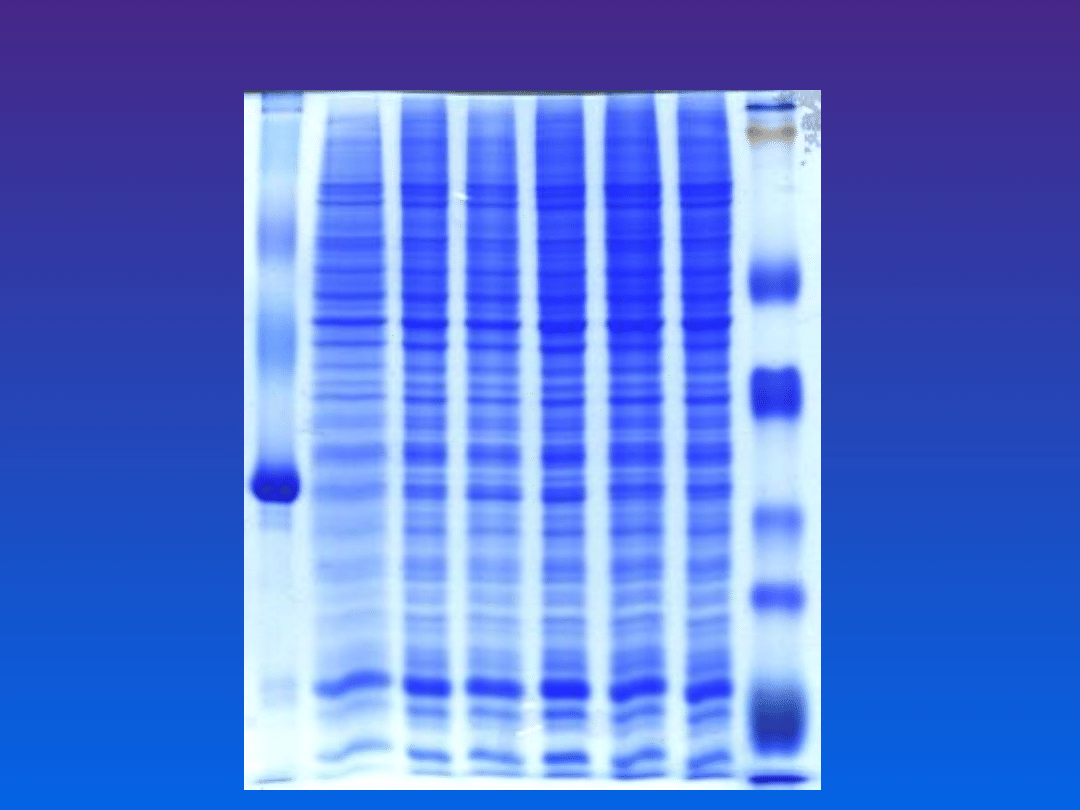
Żel barwiony metodą Coomassie

http://starklab.slu.edu/Bio104/
Plcwest.jpg
http://www-
biology.ucsd.edu/labs/aroian/protocols/sandwich.gif

OGNISKOWANIE IZOELEKTRYCZNE
IEF
– isoelectric focusing
Polega na rozdziale Ag (najczęściej białek) zgodnie z
ich punktem izoelektrycznym czyli pH, w którym się
zatrzymują.

ELEKTROFOREZA DWUKIERUNKOWA
(two-dimenssional electrophoresis)
Przebiega w 2 etepach:
1. ogniskowanie izoelektryczne (IEF)
2. SDS-PAGE
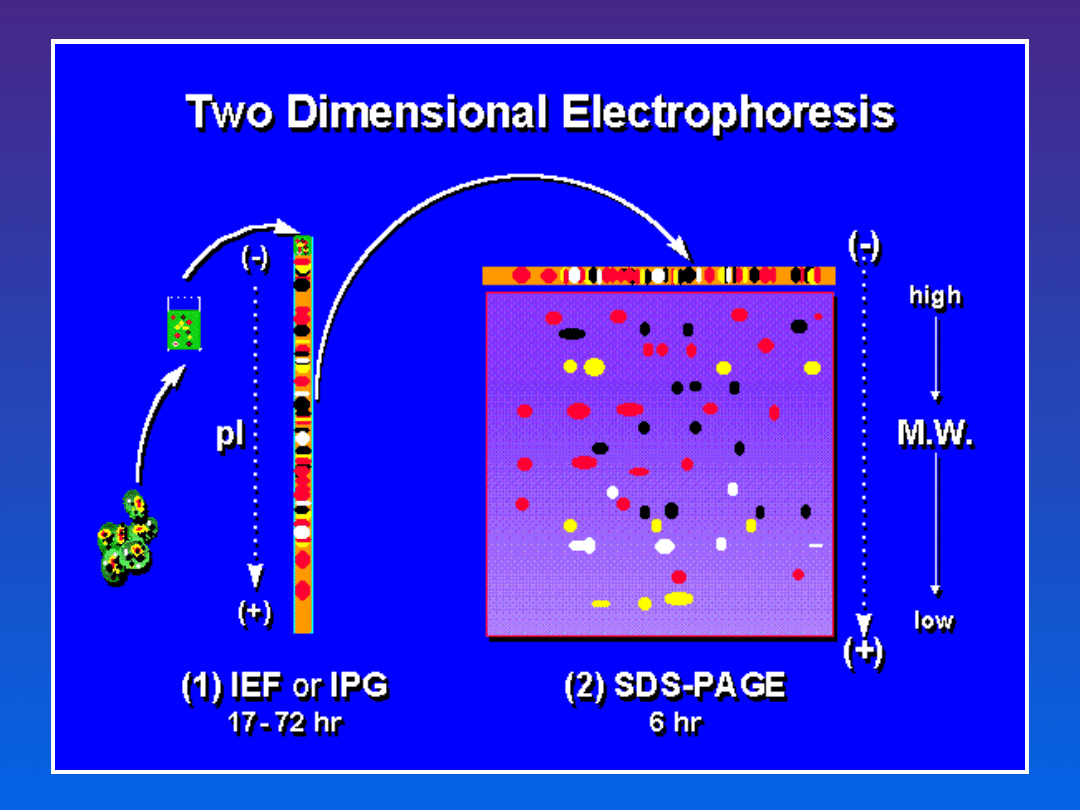

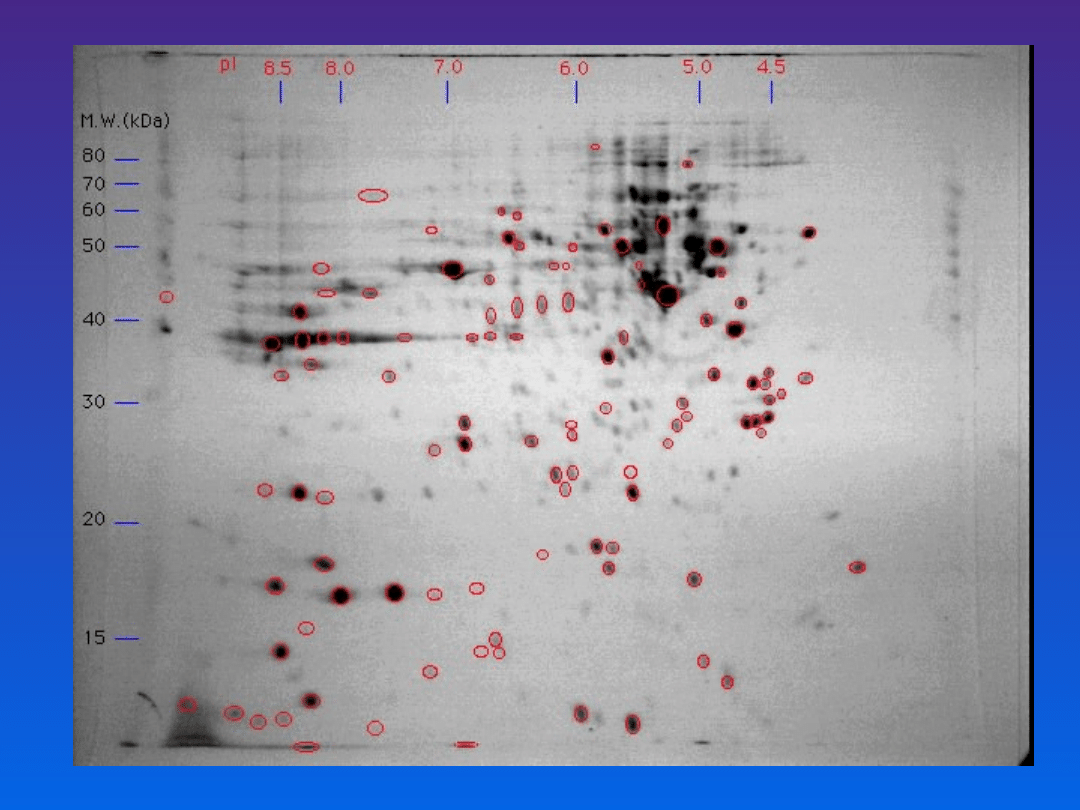


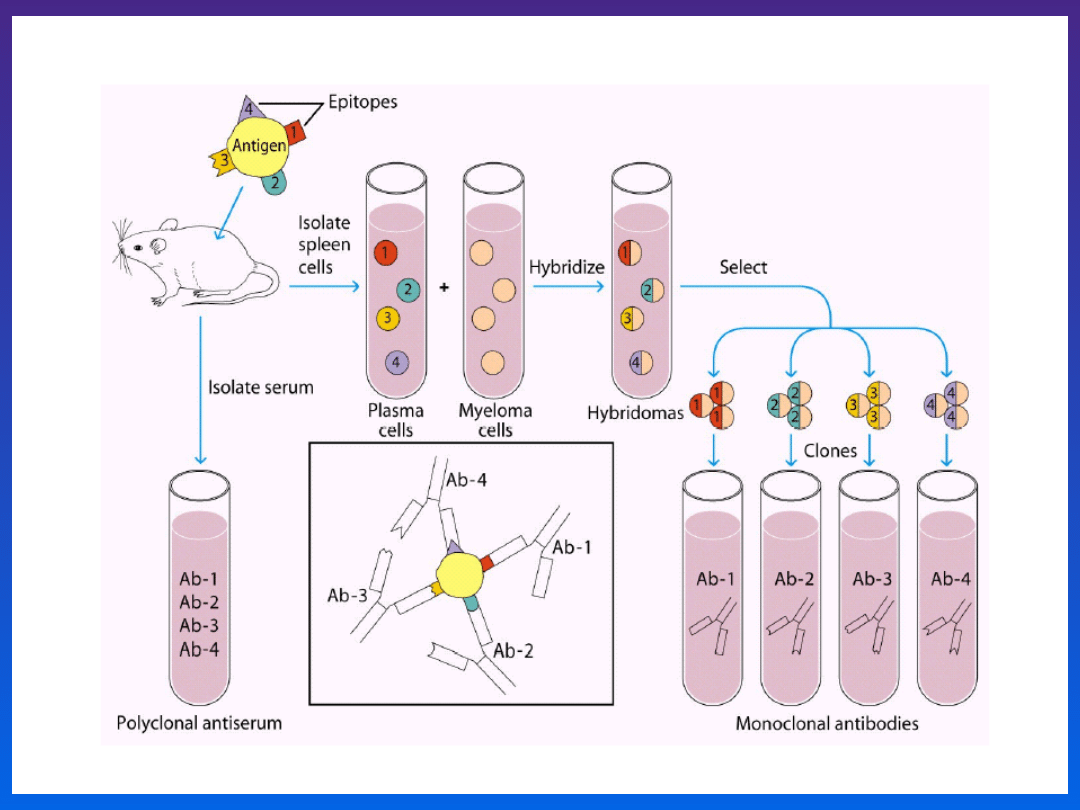
Przeciwciała monoklonalne
mAb (Monoclonal AntiBodies)
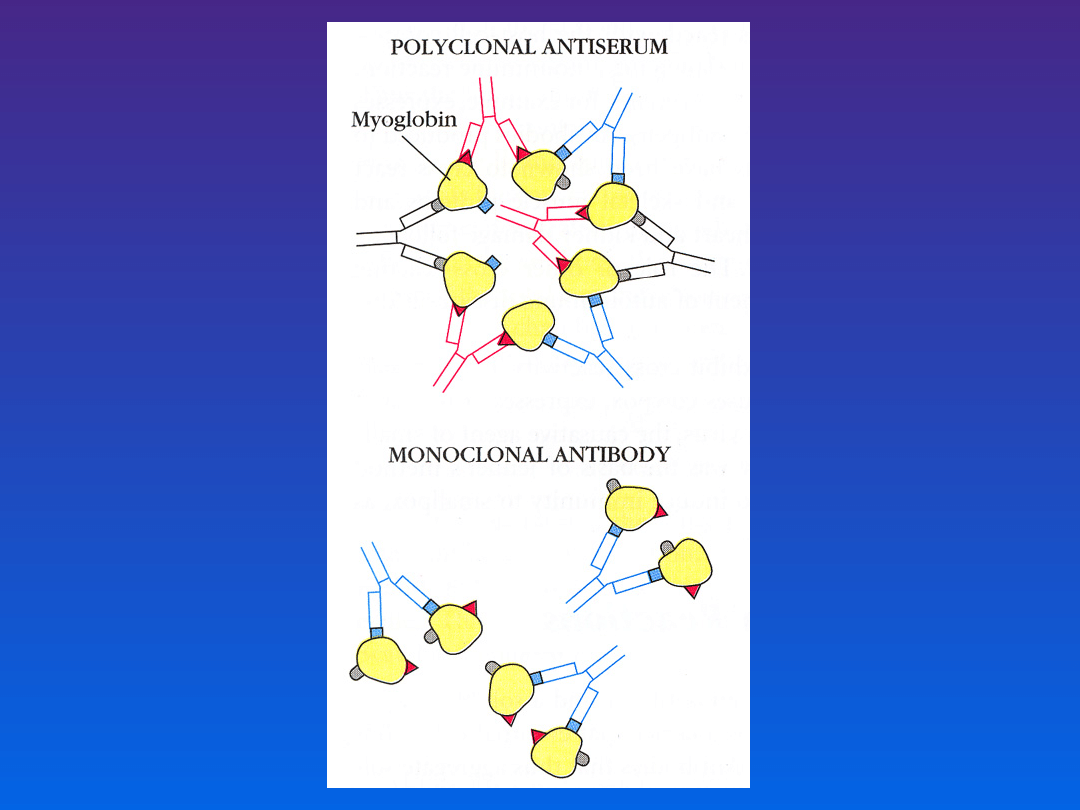
Są to przeciwciała rozpoznające jeden epitop na danym
antygenie, a więc wykazują jednakową swoistość.
Nazwa wywodzi się stąd, że wszystkie takie przeciwciała są
otrzymywane z jednego klonu limfocytów B
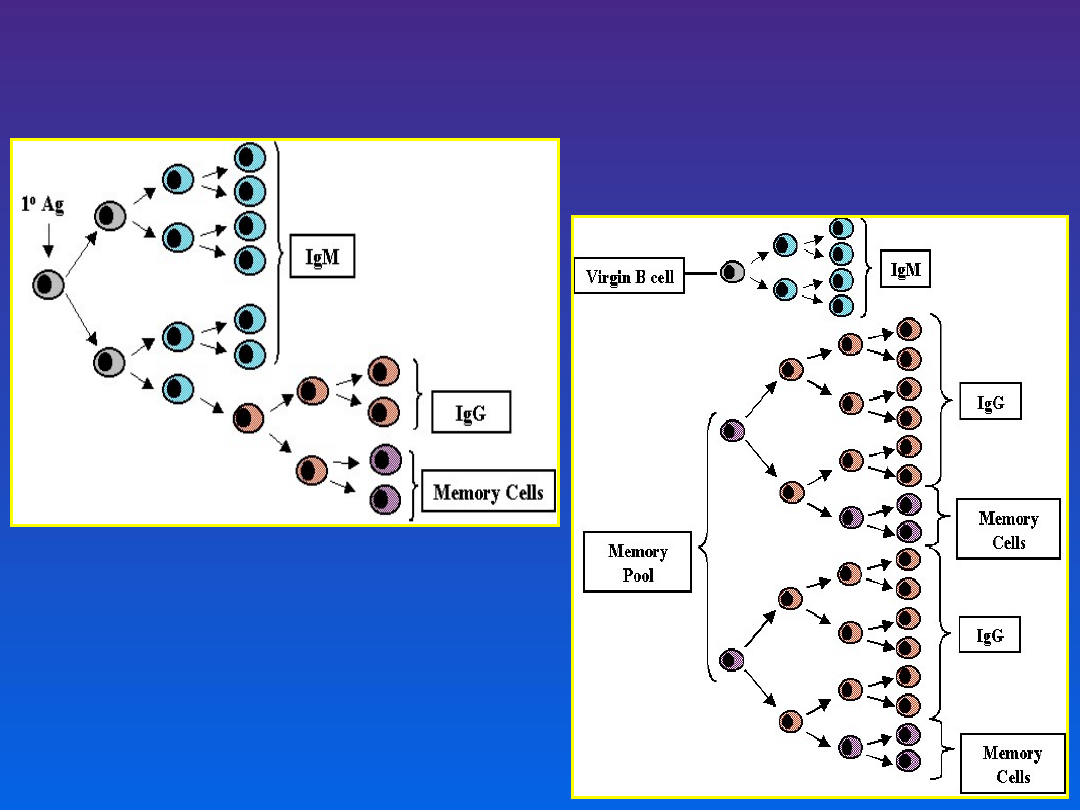
Limfocyty pamięci decydują o ilości i klasie
syntetyzowanych przeciwciał
(University of South Carolina)
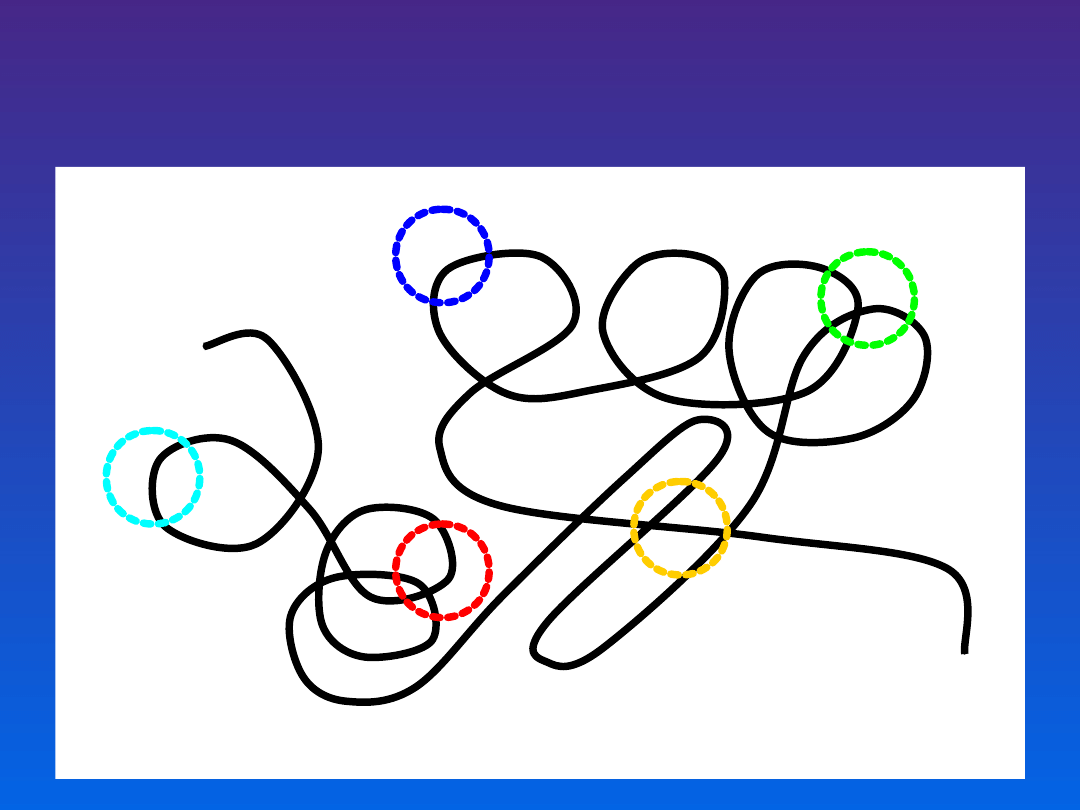
Antygeny są z reguły
wielodeterminantowe
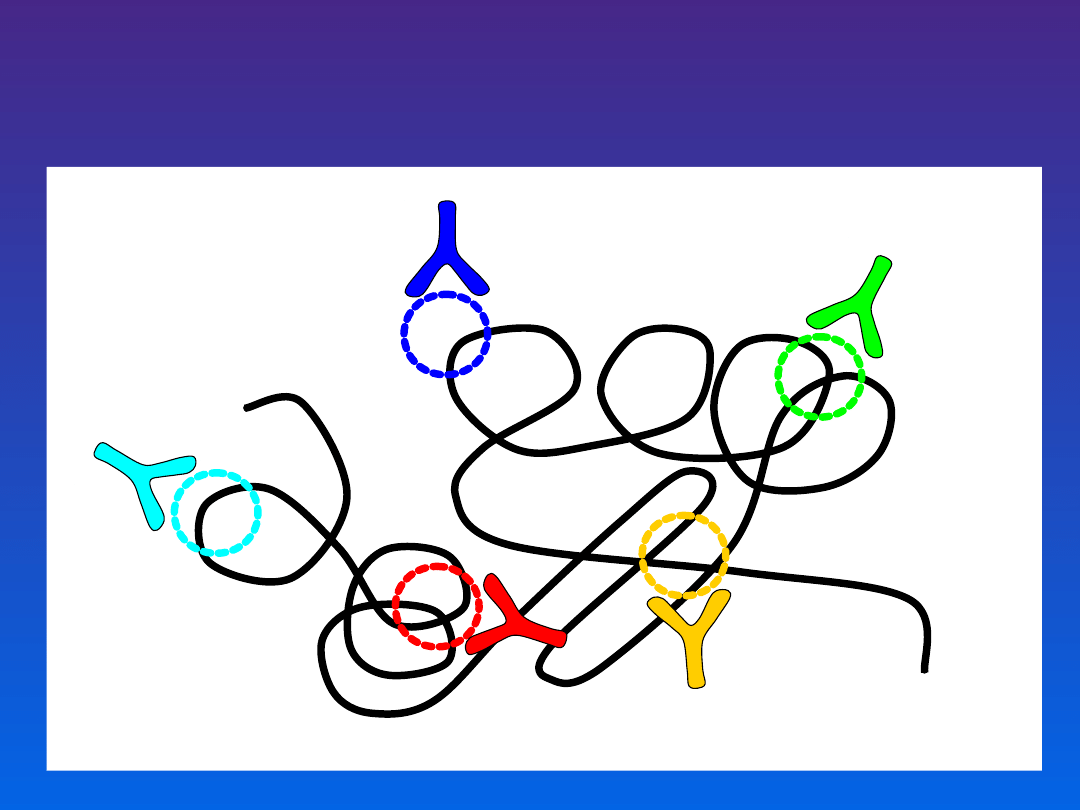
i angażują wiele klonów komórek
do produkcji przeciwciał

Produkcja przeciwciał
monoklonalnych zakłada uzyskanie 1
klonu komórkowego produkującego
przeciwciała skierowane przeciwko 1
determinancie antygenowej
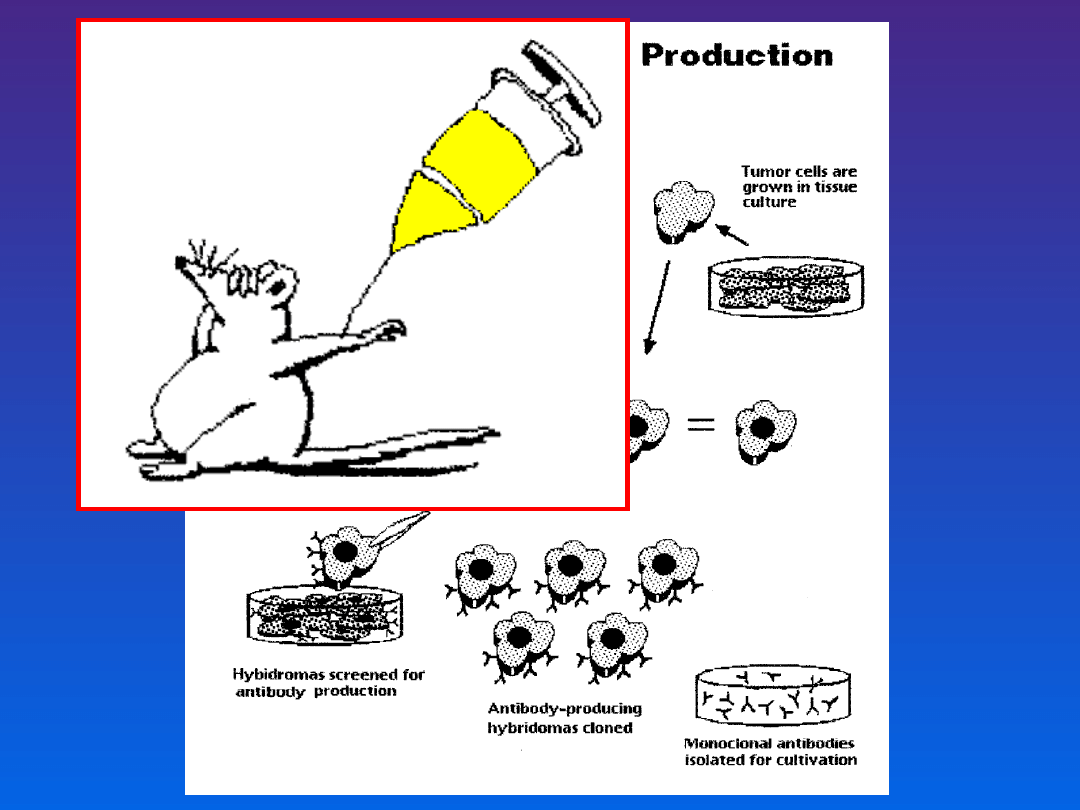
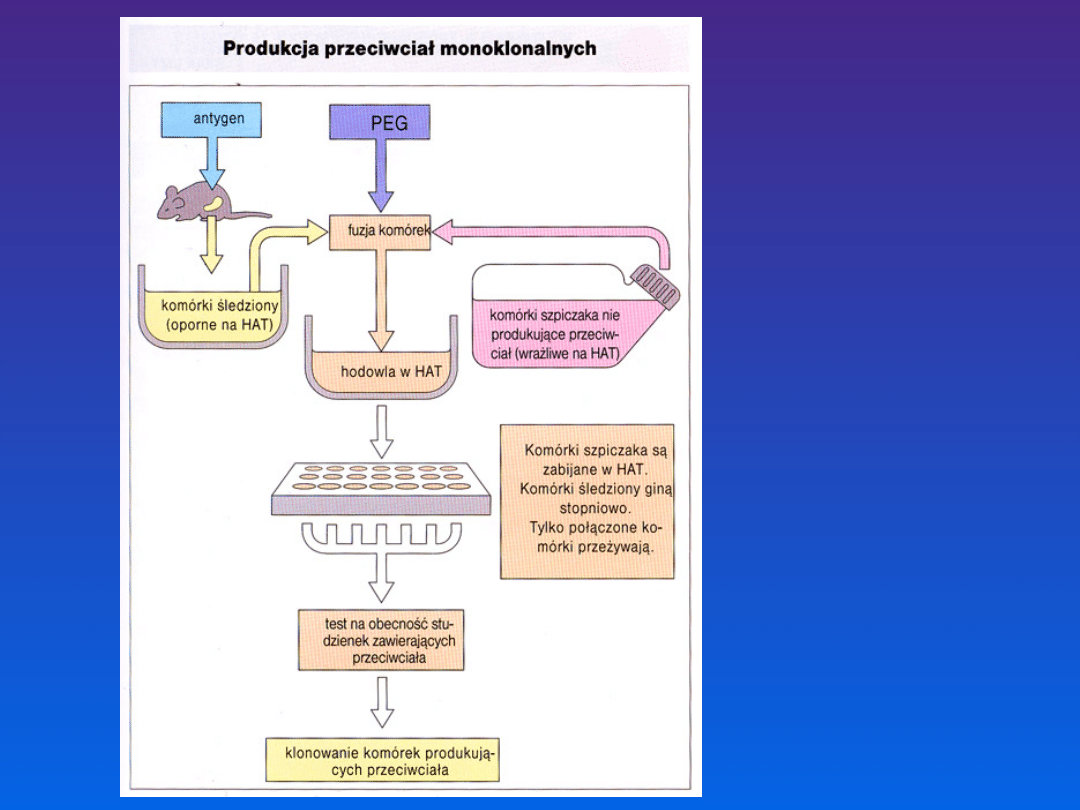
PEG – glikol polietylenowy
HAT – mieszanina hipoksantyny,
aminopteryny i tymidyny
Roitt I., Brostoff J., Male D.: Immunologia 1998
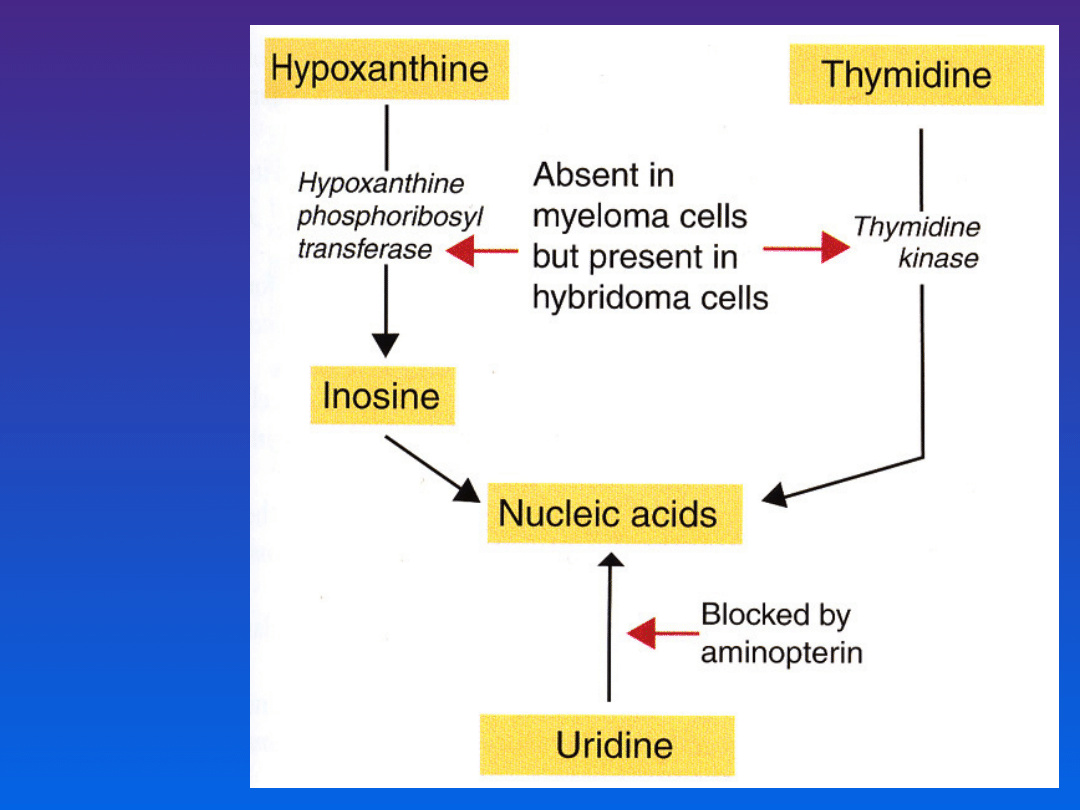
HAT
Cecha
Surowica
poliklonalna
(konwencjonalna)
Przeciwciała monoklonalne
Koncentracja swoistych Ab
0,1 – 1,0 mg/ml
0,5 – 5,0 mg/ml w płynie
otrzewnowym
5,0 – 25 mg/ml w nadsączu z
hodowli
Koncentracja nieswoistych
Ab
10 mg/ml
0,5 – 1,0 mg/ml w płynie
otrzewnowym
BRAK w nadsączu wolnym od
surowicy
Swoistość
przeciw wszystkim
determinantom
antygenowym materiału
użytego do immunizacji
przeciw jednej determinancie
antygenowej materiału użytego do
immunizacji
Powinowactwo
mieszanina przeciwciał o
różnym powinowactwie
stałe – wysokie lub niskie
Aktywność krzyżowa
z reguły występuje
w normalnych warunkach BRAK
jednak nie można całkowicie
wykluczyć
Reakcja precypitacji
TAK
NIE
Klasy i podklasy
immunoglobulin
typowe spektrum
tylko jedna klasa lub podklasa
Właściwości fizykalne
typowe spektrum
indywidualne własności
Neumeier R. Biu7 (1984) 14:97-102
Właściwości surowic odpornościowych
i przeciwciał monoklonalnych
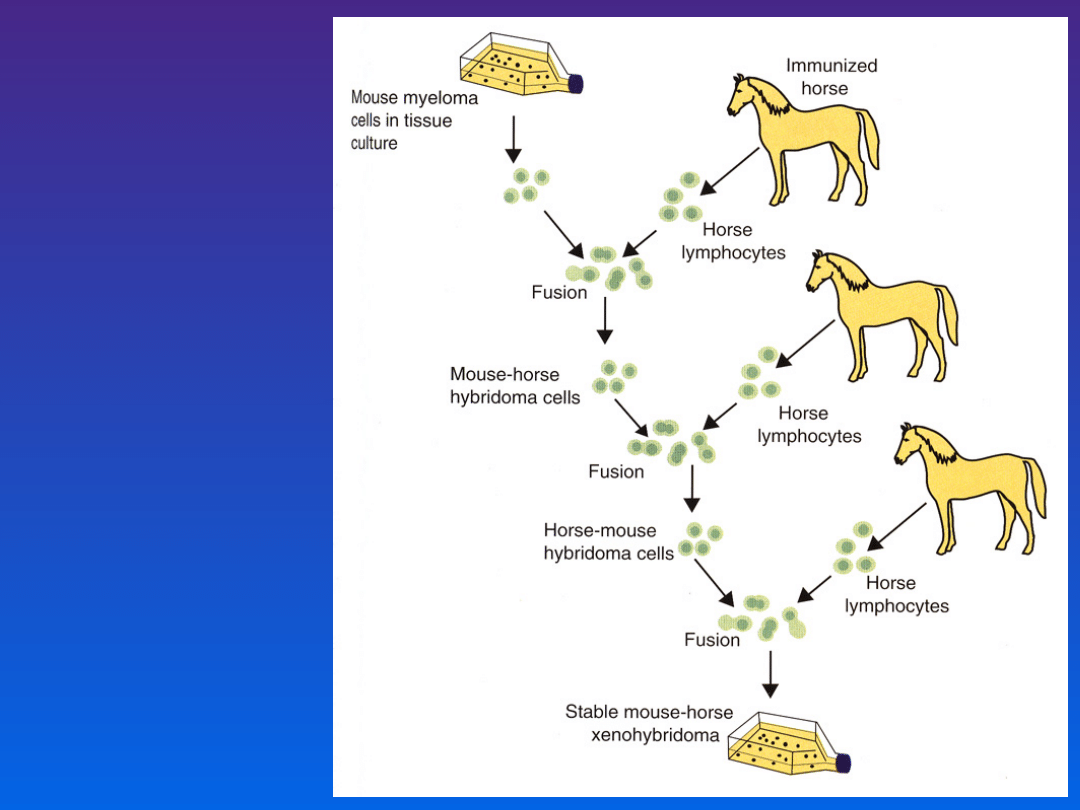
Xenohybrydomy

CD
Funkcja
limf. B
limf. T
NK
Monocyty
Neutrofil
e
Th
Tc
γδ
CD45
przenoszenie sygnału,
różne izoformy
(45R, 45RO, 45RA, 45RB)
+
+
+
+
+
+
(brak u
bydła)
+
CD14
receptor dla LPS
–
–
–
–
–
+
–
CD2
cząsteczka adhezyjna,
przenoszenie sygnału
–
+
+
–
+
–
–
CD3
przenoszenie sygnału
–
+
+
+
–
–
–
CD4
cząsteczka adhezyjna,
przenoszenie sygnału
–
+
zwykle
–
zwykle
–
–
sporadycznie
–
CD5
nieznana
+
+
+
+
–
–
–
CD 8
cząsteczka adhezyjna,
przenoszenie sygnału
–
–
zwykle
+
zwykle
–
–
sporadycznie
–
CD16
FcγR III
–
–
–
–
+
+
+
CD19
składowa BCR,
przenoszenie sygnału
+
–
–
–
–
–
–
CD21
CR2 – receptor C3d,
składowa BCR
+
–
–
–
–
po aktywacji
–
CD18
łańcuch β2 integryny
+
+
+
+
+
+
+
CD11a
LFA-1
+
+
+
+
+
+
+
CD11b
część Mac-1
subpopul
acje
subpop
ulacje
subpop
ulacje
+
+
+
CD11c
subpopul
acje
subpop
ulacje
subpop
ulacje
głównie
makrofagi
WC1
–
–
–
+
–
–
–

Immunotoksyny
– połączenia przeciwciał monoklonalnych
z toksynami. Koniugaty te po przyłączeniu się do
danego Ag (np. na powierzchni komórki nowotworowej)
mogą niszczyć komórkę niosącą ten antygen. Można
także połączyć toksynę jedynie z częścią zmienną
przeciwciała.
Immunotoksyny
mAb + Leki
Takie koniugaty mogą dostarczać lek bezpośrednio
do chorego miejsca, np. nowotworu (mniejsza
dawka leku, ograniczone efekty uboczne leku –
ważne w chemioterapii)

mAbs +
izotopy
• umożliwiają lokalne "naświetlenie" komórek
nowotworowych (zmniejszenie dawki promieniowania
oraz bardziej precyzyjne naświetlenie)
• zwalczenie małych skupisk tk. nowotworowych, które
nie mogą być wykryte
• przy pomocy detektorów promieniowania -
diagnostyka miejsc występowania przerzutów

Abzymy
Są to przeciwciała o możliwościach katalitycznych,
które mogą przeprowadzić substrat w produkt
poprzez
związek
pośredni,
analogicznie
do
enzymów. Abzymy otrzymuje się z przeciwciała
monoklonalnego przeciwko antygenowi podobnemu
do stadium przejściowego reakcji enzymatycznej.
Są o wiele mniej skuteczne od enzymów, ale prawdopodobnie znajdą
zastosowanie w katalizie niespotykanych w przyrodzie reakcji

Przeciwciała o podwójnej
swoistości
• mogą reagować z dwoma różnymi antygenami
• sprzężeniu ze sobą dwóch kompletnych
przeciwciał monoklonalnych
• zastosowanie w leczeniu nowotworów - jedna
część przeciwciała łączy się z komórką
nowotworową, druga zaś z limfocytem T.

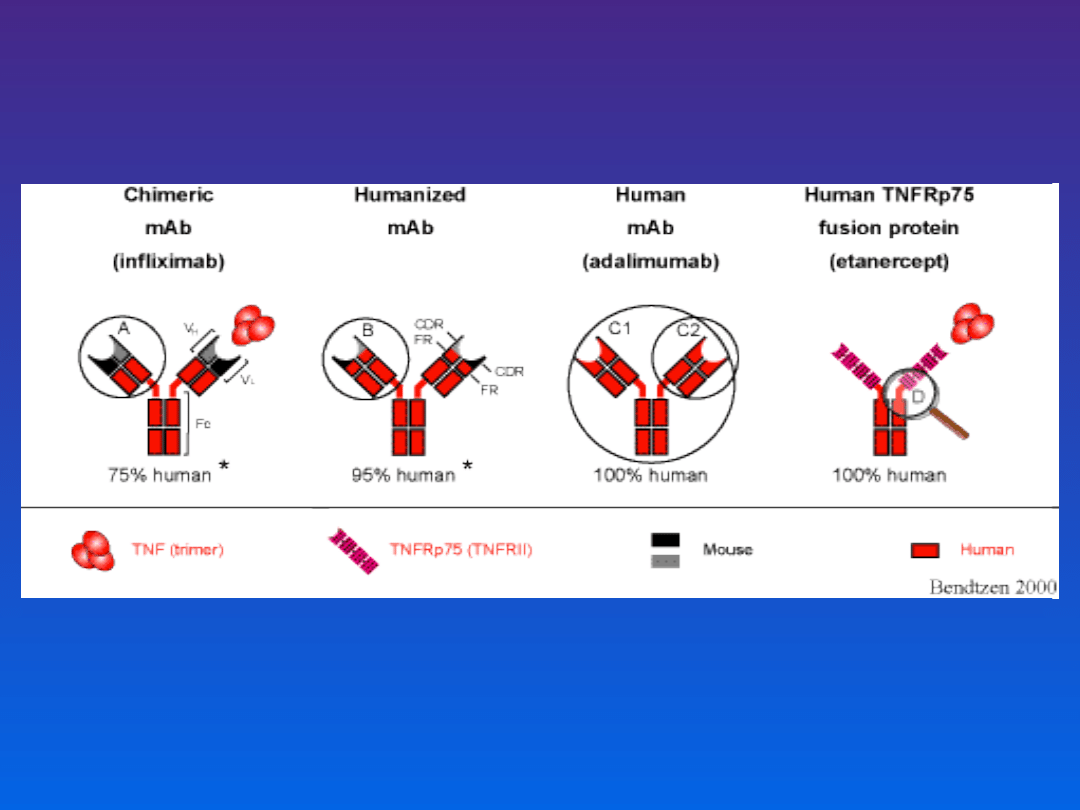
Przeciwciała chimeryczne i
"uczłowieczone"
Przeciwciała chimeryczne
- większość łańcucha
polipeptydowego stanowi białko ludzkie,
natomiast część zmienna lub jej najważniejsze
fragmenty są pochodzenia mysiego
Jeśli wymienione zostały tylko regiony
hiperzmienne, to takie przeciwciała nazywamy
"uczłowieczonymi"
(ang. humanized antibody)

Zastosowanie przeciwciał
monoklonalnych
• w terapii nowotworów
– np. Mylotarg używany w
leczeniu ostrej białaczki szpikowej i będący
koniugatem mAb anty-CD33 ze złożonym
oligosacharydem indukującym rozcinanie DNA.
• immunosupresja w transplantologii
– możliwość
wybiorczego hamowania odpowiednich subpopulacji
limfocytów
• immunosupresja w chorobach o podłożu zapalnym
–
Ab skierowane przeciwko cytokinom wywołującym
patologię
• blokowanie krzepnięcia krwi
– blokowanie
receptorów płytek wiążących się z fibrynogenem (u
pacjentów po angioplastyce)

• neutralizacja toksyn
– lepsza od stosowania
surowic (np. w leczeniu tężca), gdyż pacjenta nie
obciąża się balastem białkowego w postaci białek
surowicy obcego gatunku
• badania diagnostyczne
w laboratorium
analitycznym (testy ELISA i RIA)
• oczyszczanie różnych substancji na kolumnach
z
opłaszczonym mAb

Główne problemy terapii z użyciem
mAb
• Reakcja odpornościowa ludzkiego organizmu
Ze względu na trudność w pozyskaniu i hodowli
ludzkich linii szpiczakowych oraz etyczne przeszkody
w immunizacji ludzi do fuzji używa się komórek
mysich.
• Immunotoksyny
mogą przypadkowo uszkadzać inne
komórki organizmu, nie tylko te, które są ich celem.
Stosuje się także immunotoksyny bazujące na przeciwciałach o
podwójnej swoistości, przeciwko np. dwóm różnym antygenom
nowotworowym.
• powolna migracja do tkanek
(mAb są dużymi
cząsteczkami). Problem ten jest rozwiązywany przez
próby wiązania toksyn i leków z samymi częściami
zmiennymi przeciwciał.
• duże koszty otrzymania
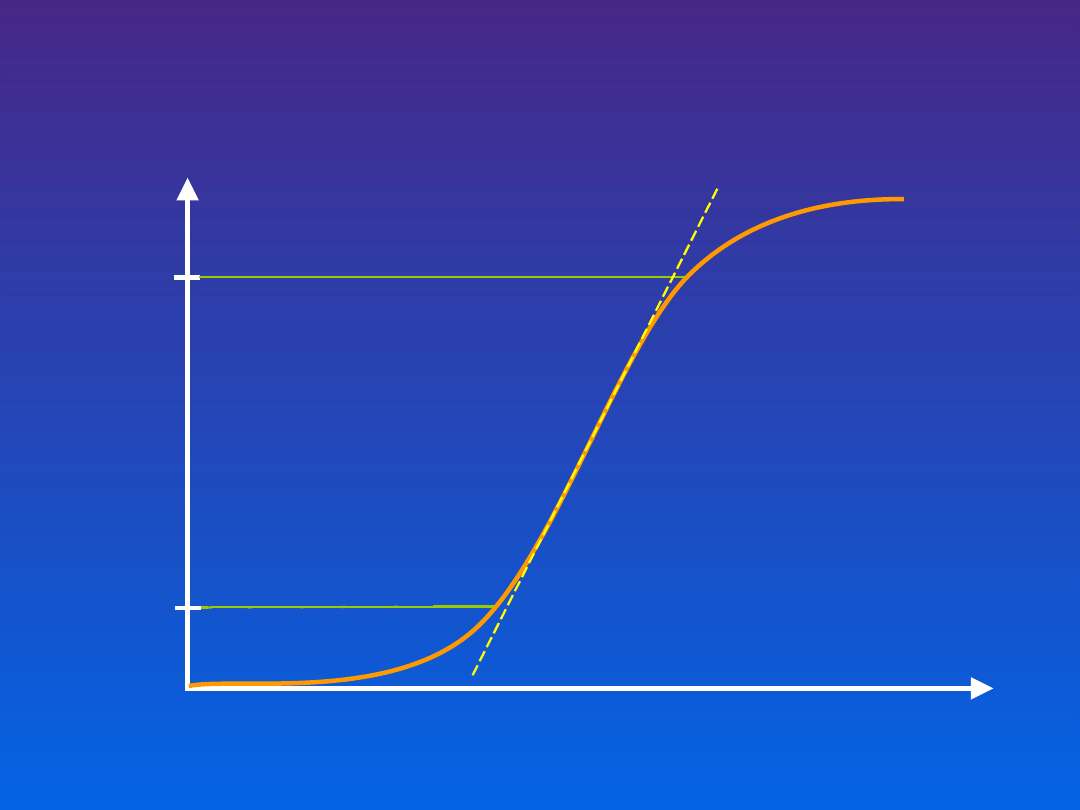
Ekstynkcja
[492nm]
1,0
ELISA
Stężenie

Dziękuję za uwagę
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
Wyszukiwarka
Podobne podstrony:
Ćw 04 Immunologiczne zróżnicowanie limfocytów Testy rozetkowe
Testy immunologiczne
Testy immunologiczne i zjawisko?gocytozy
Epidemiologia Weterynaryjna Ćw, Testy diagnostyczne I i II zadania 19, Testy diagnostyczne
Immunologia ćw.12, Immunologia
Imm Cw 5 Podstawy immunohematologii
cw 1 testy lateksowe
02 budowa Ig, Testy immunologiczne(1)
2010 testy immunolgiczne
ćw 3-opracowanie, immunologia
Cw 5 Podstawy immunohematologii
cw 1 testy lateksowe
testy, Immunologia, inne
TESTY IMMUNOLOGICZNE tabelka
więcej podobnych podstron