
KONTROLA
BIOLOGICZNA W
PROCESIE STERYLIZACJI
MEDYCZNEJ
Aneta Tyrcz
Katowice 24.06.2014

Kontrola biologiczna w procesie sterylizacji
medycznej
Sterylizacja jest przykładem procesu,
którego wyników nie jesteśmy w stanie
sprawdzić poprzez zbadanie produktu
finalnego.
Dlatego:
Przeprowadza się walidację
Przebieg procesu sterylizacji rutynowo
monitoruje
A urządzenia są konserwowane [EN ISO 14937]

Kontrola biologiczna w procesie sterylizacji
medycznej
„Sterylizacja, to zwalidowany proces
stosowany w celu uczynienia produktu
wolnym od zdolnych do życia
drobnoustrojów”
[PN-EN ISO 14937]
Każda procedura sterylizacji
powinna
zostać
poddana walidacji stanowiącej dowód, że
proces sterylizacji:
obejmował określone warunki,
ma odpowiednie działanie bakteriobójcze
jest zarówno niezawodny jak i powtarzalny.

Kontrola biologiczna w procesie sterylizacji
medycznej
Do kontroli i monitorowania procesu
służą wskaźniki chemiczne oraz
wskaźniki biologiczne, które w prosty
sposób umożliwiają wykrycie
ewentualnych błędów.
?

Zagadnienia związane ze sterylizacją wyrobów
medycznych, kontrolą procesu regulują między
innymi:
Dyrektywa wspólnoty europejskiej dla wyrobów medycznych 93/42
EEC
Ustawa z dnia 20 maja 2010 r. o wyrobach medycznych Dz.U.
2010 nr 107 poz. 679
Wytyczne sterylizacji wyrobów medycznych i innych przedmiotów
wielorazowego użycia wykorzystywanych przy udzielaniu
świadczeń zdrowotnych oraz innych czynności podczas których
może dojść do przeniesienia choroby zakaźnej lub zakażenia.
Normy:
EN ISO 14937:2009 Sterylizacja produktów stosowanych w ochronie
zdrowia Wymagania dotyczące charakterystyki oraz opracowywania
i rutynowej kontroli procesu sterylizacji wyrobów medycznych
PN EN ISO 17665:2008
Sterylizacja produktów stosowanych w ochronie zdrowia - Ciepło
wilgotne - Wymagania dotyczące opracowywania, walidacji i
rutynowej kontroli procesu sterylizacji wyrobów medycznych
PN-EN ISO 14161
Sterylizacja produktów stosowanych w ochronie zdrowia. Wskaźniki
biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
PN-EN ISO 11138-1:2008 Sterylizacja produktów stosowanych w
ochronie zdrowia - Wskaźniki biologiczne

Wytyczne sterylizacji wyrobów medycznych i innych przedmiotów
wielorazowego użycia wykorzystywanych przy udzielaniu świadczeń
zdrowotnych oraz innych czynności podczas których może dojść do
przeniesienia choroby zakaźnej lub zakażenia.
2011r.
Wytwarzanie wyrobów sterylnych, podlega
specjalnym wymaganiom i powinno
przebiegać zgodnie z ustalonymi i
zwalidowanymi procedurami i procesami
technologicznymi.
Podstawą kontroli procesów sterylizacji jest
zastosowanie odpowiednich dla danej metody
wskaźników fizycznych, chemicznych i
biologicznych, umożliwiających sprawdzenie
sprawności urządzeń i monitorowanie
parametrów procesu na każdym jego etapie.

cd. Wytyczne sterylizacji wyrobów medycznych
Zakres kontroli każdego cyklu oraz
okresowej kontroli procesu jest uzależniony
od metody sterylizacji, zakresu walidacji,
rozwiązania przestrzennego i funkcjonalnego
oraz zakresu wykonywanych usług.
Kontroli podlega każdy cykl sterylizacyjny.
Dobór metod kontroli powinien być zgodny z
zaleceniami wytwórcy sterylizatora i
wskazaniami polskich norm, a o wyborze
wskaźników i testów, ich użyciu i liczbie
decyduje osoba odpowiedzialna za nadzór nad
procesem sterylizacji.

cd. Wytyczne sterylizacji wyrobów medycznych
Kontrola każdego cyklu sterylizacji
polega na:
Rejestracji parametrów procesu oraz
kontroli wskaźnikami chemicznymi 5 lub 6
klasy.
W innych przypadkach – wskazane jest
zastosowanie wskaźników chemicznych
klasy 5 lub 6 i wskaźników biologicznych.

cd. Wytyczne sterylizacji wyrobów medycznych
Wskaźniki biologiczne należy stosować
zgodnie z ich przeznaczeniem wskazanym
przez wytwórcę, w szczególności należy
ściśle przestrzegać, zaleceń dotyczących
zasad stosowania, warunków hodowli i
przechowywania.
Zastosowanie wskaźników biologicznych
zależy od metody sterylizacji:
Sterylizacja niskotemperaturowa w każdym
cyklu.

cd. Wytyczne sterylizacji wyrobów medycznych
Sterylizacja parowa:
Nie rzadziej niż raz na trzy miesiące oraz po każdym
usunięciu awarii;
W każdym cyklu, gdy nie jest dostępny automatyczny
pomiar i zapis parametrów krytycznych procesu.
Liczba zastosowanych podczas kontroli
wskaźników biologicznych uzależniona jest od:
wielkości komory sterylizatora,
rodzaju kontroli (bieżąca cyklu, okresowa, potwierdzająca
skuteczność procesu),
miejsca lokalizacji wskaźnika (pakiet reprezentatywny, PCD
wsadu.

cd. Wytyczne sterylizacji wyrobów medycznych
Wynosi odpowiednio:
W przypadku sterylizatorów o pojemności poniżej
jednej jednostki wsadu co najmniej dwa wskaźniki
w pakietach reprezentatywnych dla całego wsadu
umieszczonych w miejscu o najtrudniejszym
dostępie czynnika sterylizującego lub jeden w tzw.
PDC - symulacja wsadu.
W przypadku sterylizatorów o pojemności jednej
jednostki lub powyżej co najmniej trzy wskaźniki
umieszczone w pakietach reprezentatywnych dla
całego wsadu umieszczonych w miejscu o
najtrudniejszym dostępie czynnika sterylizującego
lub jeden w tzw. PDC - symulacja wsadu.

cd. Wytyczne sterylizacji wyrobów medycznych
Orzekanie o sterylności i zwalnianie
wsadu po sterylizacji odbywa się:
zgodnie z udokumentowanymi procedurami
na podstawie oceny zapisów parametrów
krytycznych określonych dla danego
procesu sterylizacji
oraz
odczytu wskaźników biologicznych lub
wskaźników chemicznych.

Wytyczne do dezynfekcji i sterylizacji w
Wytyczne do dezynfekcji i sterylizacji w
zakładach opieki zdrowotnej, CDC 2008
zakładach opieki zdrowotnej, CDC 2008
Proces sterylizacji powinien być rutynowo
monitorowany za pomocą kontroli:
parametrów fizycznych procesu,
wskaźników chemicznych i biologicznych.
Wskaźniki chemiczne powinny być stosowane w
połączeniu ze wskaźnikami biologicznymi.
Nie powinny ich zastępować, ponieważ wskaźniki
chemiczne wskazują na fakt sterylizacji (sterylizację w
czasie, przetworzenie), ale nie dowodzą skuteczności
sterylizacji (zabicia mikroorganizmów).
Wskaźniki biologiczne składają się z odpornych
zarodników mikroorganizmów, można zatem
ocenić (zmierzyć) skuteczność procesu sterylizacji
(moc zabijania).

cd. Wytyczne CDC
cd. Wytyczne CDC
Każdy proces sterylizacji należy kontrolować/
testować zarówno parę wodną, jak również inne
metody sterylizacji niskotemperaturowej.
Zalecana jest kontrola wskaźnikami chemicznymi
i biologicznymi podczas instalacji, przeniesienia,
awarii/ naprawie – celem potwierdzenia
prawidłowego funkcjonowania przed
wprowadzeniem do rutynowego stosowania.
Zaleca się przeprowadzenie trzech kolejnych cykli
kontrolnych. Sterylizator nie zostaje przywrócony
do użytkowania, dopóki wszystkie biologiczne
wskaźniki nie są ujemne i wskaźniki chemiczne
nie wykażą prawidłowej odpowiedzi.

cd. Wytyczne CDC
cd. Wytyczne CDC
Wskaźniki biologiczne są to wskaźniki
procesowe, które bezpośrednio nadzorują
śmiertelność danego proces sterylizacji.
Zarodniki stosowane do monitorowania
procesu sterylizacji wykazują odporność
na czynnik/ środek sterylizujący i są
bardziej odporne niż obciążenia
biologiczne znajdujące się na
urządzeniach medycznych.

cd.Wytyczne CDC
cd.Wytyczne CDC
Sterylizatory parowe i sterylizatory
niskotemperaturowe powinny być monitorowane co
najmniej raz w tygodniu za pomocą odpowiednich,
dostępnych w handlu wskaźników biologicznych.
Jeżeli sterylizator pracuje codziennie (np.. Kilka cykli
dziennie), zaleca się codzienne stosowanie
wskaźników biologicznych.
Pozwala to na wcześniejsze wykrycie awarii sprzętu lub błędu
proceduralnego.
Każdy wsad zawierający implanty powinien być
monitorowany wskaźnikiem biologicznym.
Jeżeli to możliwe materiał powinien być wydany dopiero po
uzyskaniu prawidłowych wyników kontroli biologicznej.

cd. Wytyczne CDC
cd. Wytyczne CDC
Do kontroli biologicznej można stosować
wskaźniki biologiczne o szybkim odczycie.
Układ ten wykrywa obecność metabolitów kwasu
wytwarzanego podczas wzrostu G.
stearothermophilus (odczyt fluorescencyjny).
Wskaźniki te dostarczają szybkiej i
wiarygodnej informacji o skuteczności
procesu.

cd. Wytyczne CDC
cd. Wytyczne CDC
Pakiety kontrolne ze wskaźnikami
biologicznymi powinny być ujednolicone.
Ułatwia to interpretację wyników.
Pakiet testowy umieszcza się w miejscu
najbardziej krytycznym.
Najczęściej jest to obszar w przedniej, dolnej
części sterylizatora w pobliżu odpływu.
Zaleca się kontrolować żywotność
wskaźników biologicznych.

EN ISO 14937:2009
Sterylizacja produktów stosowanych w ochronie zdrowia. Wymagania dotyczące charakterystyki
oraz opracowywania i rutynowej kontroli procesu sterylizacji wyrobów medycznych
10. Rutynowe monitorowanie i kontrola
10.1 Celem rutynowego monitorowania i
kontroli jest wykazanie, że produkt został
poddany zwalidowanemu i określonemu
procesowi sterylizacji.
10.2 Powinny istnieć dowody uzyskane
drogą pomiarów, uzupełnione jeśli to
niezbędne o wskaźniki biologiczne lub
wskaźniki chemiczne, świadczące o tym, że
proces sterylizacji został przeprowadzony w
zakresie określonych tolerancji.

cd. EN ISO 14937:2009
Wymagania dotyczące charakterystyki oraz opracowywania i rutynowej kontroli procesu
sterylizacji wyrobów medycznych
7.3 Powinien być określony i utrzymany
system w celu zapewnienia, że stan
produktu poddawanego sterylizacji,
obejmujący poziomy zanieczyszczenia
mikrobiologicznego, organicznego i
nieorganicznego jest kontrolowany i nie
wpływa na skuteczność procesu
sterylizacji.
Skuteczność w/w wykazana [zapisy]

cd. EN ISO 14937:2009
Wymagania dotyczące charakterystyki oraz opracowywania i rutynowej kontroli procesu
sterylizacji wyrobów medycznych
8.3 Jeżeli wskaźniki biologiczne są stosowane
jako część ustalenia procesu sterylizacji,
powinny:
Być zgodne z ISO 11138
Wykazywać oporność na czynnik sterylizujący
odpowiednio do zanieczyszczenia
mikrobiologicznego, produktu przeznaczonego do
sterylizacji;
Być umieszczane albo w produkcie, w miejscach
określonych jako najtrudniejsze do uzyskania
warunków sterylizacji, albo w przyrządzie testowym
procesu (PCD).

cd. EN ISO 14937:2009
Wymagania dotyczące charakterystyki oraz opracowywania i rutynowej kontroli procesu
sterylizacji wyrobów medycznych
11. zwalnianie produktu po sterylizacji
Powinna zostać określona procedura
zwalniania produktu po sterylizacji.
Zwalnianie parametryczne powinno być
stosowane tylko wtedy, gdy wszystkie
parametry procesu są określone,
kontrolowane i bezpośrednio monitorowane.
Jeżeli do monitorowania procesu sterylizacji
zostały użyte wskaźniki biologiczne lub
chemiczne, to wyniki z ekspozycji tych
wskaźników powinny być włączone do
kryteriów zwalniania produktu po sterylizacji.

EN ISO 17665-1:2008
Sterylizacja produktów stosowanych w ochronie zdrowia - Ciepło wilgotne -
Część 1: Wymagania dotyczące opracowywania, walidacji i rutynowej kontroli procesu sterylizacji
wyrobów medycznych
10. Rutynowe monitorowanie i kontrola
10.1 Rutynowe monitorowanie i kontrola powinno
być przeprowadzane w każdym cyklu pracy [stan
eksploatacyjny urządzenia – przeciek powietrz,
jakość, penetracja pary, proces sterylizacji]
10.4 przeprowadzenie procesu sterylizacji
powinno być zweryfikowane na podstawie
wyników wskaźników chemicznych lub systemów
wskaźników biologicznych, jeżeli stosowane, i
przez potwierdzenie, że w określonych
tolerancjach, dane zarejestrowane z rutynowego
monitorowania są zgodne z danymi z walidacji
[temperatura sterylizacji, ciśnienie w komorze].

cd. EN ISO 17665-1:2008
Część 1: Wymagania dotyczące opracowywania, walidacji i rutynowej kontroli procesu sterylizacji
wyrobów medycznych
11. Zwalnianie produktu po sterylizacji
11.1 Powinny być określone procedury
przeglądu zapisów i zwalniania produktu po
procesie sterylizacji. Procedura powinna
określać wymagania dotyczące uznania
procesu sterylizacji za prawidłowy. Jeśli
wymaganie nie jest spełnione, produkt
powinien zostać uznany za niezgodny
[odpowiednie działania korygujące/
zapobiegawcze].
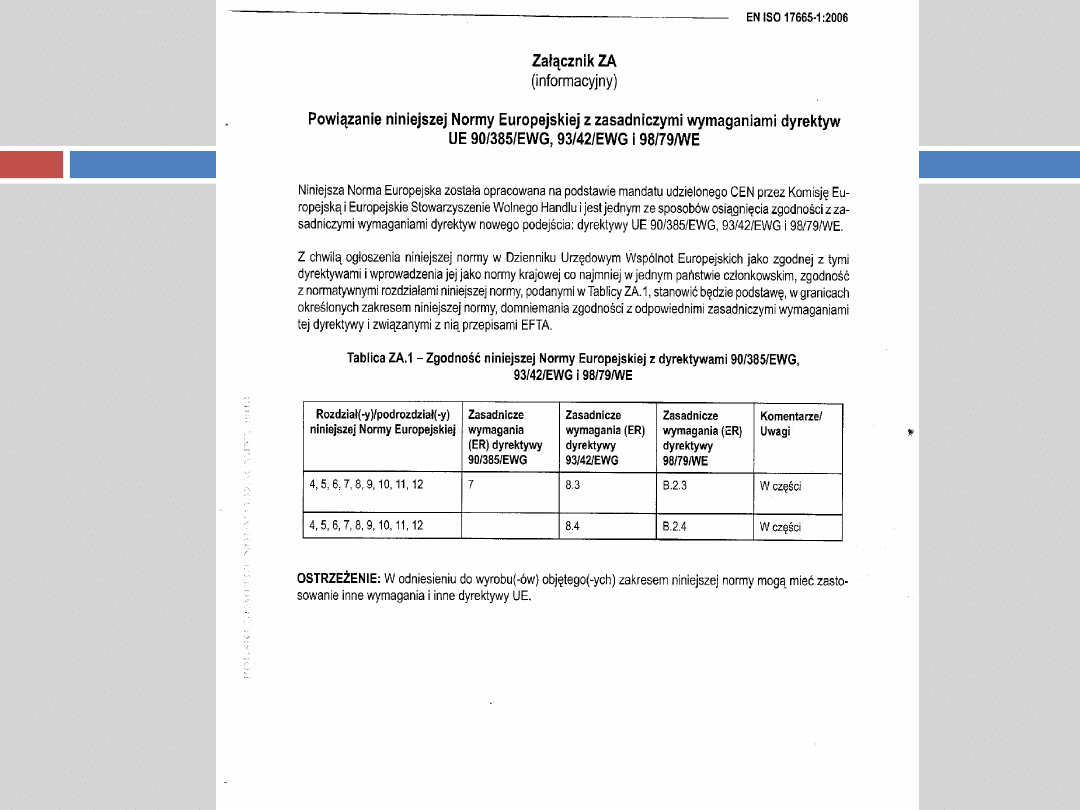

PN-EN ISO 14161
Sterylizacja produktów stosowanych w ochronie zdrowia. Wskaźniki
biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników.
Zawiera wytyczne dotyczące wyboru,
stosowania i interpretacji wyników
uzyskanych z zastosowaniem wskaźników
biologicznych, do oceny przebiegu walidacji
i kontrolowania procesów sterylizacji.
Zaleca się, aby użytkownik wybrał wskaźnik
biologiczny, który jest odpowiedni do
stosowania w danym procesie.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Zaleca się, aby w wykazywaniu
skuteczności procesu sterylizacji
wskaźniki biologiczne były zawsze
używane w połączeniu z fizycznymi i/ lub
chemicznymi parametrami.
W przypadku, gdy fizyczne i/ lub
chemiczne zmienne procesu sterylizacji
wykraczają poza określone granice,
zaleca się ocenić parametry procesu.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Na działanie wskaźnika biologicznego
mogą negatywnie wpływać:
warunki przechowywania
transportu przed jego użyciem,
użycie wskaźnika biologicznego,
parametry pracy sterylizatora lub
techniki zastosowane po ekspozycji w procesie.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Zaleca się zauważyć, że wskaźniki
biologiczne nie są przeznaczone do
wskazywania, że produkty oraz każdy
poddawany sterylizacji wsad jest sterylny.
Wskaźniki biologiczne są wykorzystywane
do badania skuteczności danego procesu
sterylizacji i zastosowanego sprzętu przez
ocenę zabijania drobnoustrojów zgodnie z
koncepcją zapewnienia poziomu
sterylności.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
4. Postanowienia ogólne
Wskaźniki biologiczne są określone w ISO
11138 1-3, gdzie podano wymagania
dotyczące wytwarzania systemów
wskaźników biologicznych, w których
biologicznym składnikiem jest
drobnoustrój, taki jak bakteryjna
ednospora lub inna mikrobiologiczna
forma.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Wskaźnik biologiczny reprezentuje
utrudnienie mikrobiologiczne w procesie
sterylizacji i jest używany do
potwierdzenia,
że proces sterylizacji ma możliwość
inaktywacji drobnoustrojów, które mają
znaną odporność na wzorcowy proces
sterylizacji… .

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Zaleca się, aby użytkownik zapewnił, że
wskaźnik biologiczny był walidowany do
użycia w określonym zakresie stosowanych
warunków sterylizacji.
Obowiązkiem osób odpowiedzialnych za
sterylizacje produktu jest, zapewnienie, aby
rodzaj wskaźnika biologicznego
stosowanego do walidacji i/ lub rutynowej
kontroli danego procesu sterylizacji był
odpowiedni.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Zaleca się, aby osoby używające
wskaźniki biologiczne do walidacji i/ lub
rutynowej kontroli sterylizacji
były odpowiednio przeszkolone w ich
stosowaniu.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
5.Właściwości wskaźników biologicznych
5.1 Wskaźniki biologiczne zapewniają
bezpośrednią ocenę biobójczej
skuteczności procesu sterylizacji.
Stosowane wraz z metodami kontroli
fizycznej i/ lub chemicznej procesu,
mogą zapewnić ocenę skuteczności
danego procesu sterylizacji.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
5.1 Zaleca się, aby proces sterylizacji był
uznany za prawidłowy,
wyłącznie jeśli zostały osiągnięte pożądane
fizyczne i/ lub chemiczne parametry i
wyniki mikrobiologiczne,
określone przez właściwe metody przebiegu
cyklu,
walidację i program kontrolujący.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Wskaźnik biologiczny składa się z:
Nośnika
Opakowania
Składnika mikrobiologicznego (określona populacja organizmów
testowych)
Rodzaje:
samodzielne wskaźniki biologiczne (fiolka);
inne – zaszczepiony nośnik w opakowaniu pierwotnym.
Forma i konstrukcja wskaźnika biologicznego mogą
powodować unikalne oporności i mogą różnić się
zależnie od tego, czy wskaźnik biologiczny jest
przeznaczony do użycia w ocenie przebiegu i
walidacji procesu sterylizacji, czy też rutynowej
kontroli.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
5.4.1 Oporność wskaźników
biologicznych różni się w zależności od
metod wytwarzania i warunków badania.
….
Wymaga się od użytkowania
udokumentowania rozmieszczenia
wskaźników biologicznych w komorze
sterylizatora.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
7. Wskaźniki biologiczne do oceny skuteczności
procesu.
Występują duże różnice w procesach
sterylizacji uwzględniające parametry pracy i
rodzaje produktów, które są sterylizowane. …
W celu wykazania skuteczności procesu
sterylizacji
zaleca się, aby wskaźniki biologiczne
zawsze
były
stosowane w połączeniu z właściwymi fizycznymi
i/ lub chemicznymi pomiarami parametrów
procesu.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Cd.7 Nie można podać ogólnej informacji dotyczącej
liczby wskaźników biologicznych na objętość
komory sterylizatora,
ponieważ zależy ona od powtarzalności cykli tak samo
jak od możliwości zróżnicowania parametrów procesu w
całym wsadzie podczas sterylizacji.
Zaleca się wybrać odpowiednią liczbę wskaźników
do stosowania na podstawie
zgromadzonych danych wynikających ze stosowania
wskaźników i/ lub badań zanieczyszczenia
mikrobiologicznego, jak również
dokumentacji rozkładu czynnika sterylizującego.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
8. Wskaźniki biologiczne stosowane do walidacji
sterylizacji.
Jeśli wskaźniki biologiczne są stosowane do
walidacji procesu, zaleca się rozważenie
rodzaju wskaźników, które mogą być
stosowane do rutynowej kontroli.
Różne wskaźniki biologiczne mogą zapewnić
różne poziomy utrudnienia procesu sterylizacji.
Jeżeli do walidacji i rutynowej kontroli
stosowane są różne wskaźniki, zaleca się je
włączyć do badań walidacji … .

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
9. Wskaźniki biologiczne do rutynowej kontroli.
Stosowanie wskaźników biologicznych może
nie być wymagane, gdyż może to przedstawiać
niewielką wartość w rutynowej kontroli
niektórych procesów sterylizacji
(np.. Ciepłem wilgotnym, patrz ISO 11134, ISO 13683).
W procesach, w których zwalnianie
parametryczne jest nieosiągalne,
wskaźniki biologiczne zapewniają najlepszą
możliwą alternatywę w celu wykazania
biobójczości drobnoustrojów w procesie sterylizacji.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
Cd.9
Rodzaj i umieszczenie wskaźnika biologicznego powinno być
zgodne z miejscami określonymi podczas oceny sterylizacji
lub walidacji.
Różnice należy udokumentować.
Wskaźniki biologiczne umieszcza się w miejscach
reprezentujących największe utrudnianie procesu sterylizacji.
Rozmieszczenie wskaźników powinno być stałe.
Proces uznaje się za prawidłowy jedynie wtedy, gdy żądane
fizyczne i/ lub chemiczne parametry były uzyskane,
a wyniki
mikrobiologiczne zinterpretowane
i oba
uznano za zgodne z żądanymi kryteriami.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
10. Wyniki
Zaleca się , aby kryteria zatwierdzania
procesu sterylizacji jako zadowalającego
były określone podczas oceny cyklu sterylizacji,
z zastosowaniem odpowiednich norm dotyczących
walidacji i kontroli procesu sterylizacji.
Zaleca się, aby rutynowe procedury były
ustanowione i przestrzegane
w celu uzyskania rzetelnych wyników
oraz przeprowadzane przez wyszkolony personel,
z użyciem właściwego sprzętu.

cd. PN-EN ISO 14161
Wskaźniki biologiczne. Wytyczne dotyczące wyboru, stosowania i interpretacji
wyników
14. Personel odpowiedzialny za
umieszczenie wskaźnika,
wyjęcie,
badanie
i inne postępowanie ze wskaźnikiem
biologicznym
powinien być właściwie przeszkolony.
Szkolenie zaleca się udokumentować,
a jego skuteczność okresowo oceniać.

PN-EN ISO 11138
Sterylizacja produktów stosowanych w ochronie zdrowia - Wskaźniki
biologiczne
PN-EN ISO 11138-1:2008 Część 1: Wymagania ogólne
Podano wymagania ogólne dotyczące produkcji, etykietowania, metod badań i
charakterystyk działania wskaźników biologicznych, z uwzględnieniem
zaszczepionych nośników i zawiesin, oraz ich składników przeznaczonych
do użycia podczas walidacji i rutynowego monitoringu procesów sterylizacji.
PN-EN ISO 11138-2:2011 Część 2: Wskaźniki biologiczne dla procesów
sterylizacji tlenkiem etylenu
Podano szczegółowe wymagania dotyczące organizmów testowych, zawiesin,
zaszczepionych nośników, wskaźników biologicznych i metod badania
przeznaczonych do oceny działania sterylizatorów i procesów sterylizacji
wykorzystujących gazowy tlenek etylenu jako czynnik sterylizujący w
temperaturach sterylizacji w zakresie od 29 °C do 65 °C
PN-EN ISO 11138-3:2011 Część 3: Wskaźniki biologiczne dla procesów
sterylizacji ciepłem wilgotnym
Podano szczegółowe wymagania dotyczące organizmów testowych, zawiesin,
zaszczepionych nośników, wskaźników biologicznych i metod badania
przeznaczonych do oceny działania procesów sterylizacji wykorzystujących
ciepło wilgotne jako czynnik sterylizujący

cd. PN-EN ISO 11138
Sterylizacja produktów stosowanych w ochronie zdrowia - Wskaźniki
biologiczne
Dla zaszczepionych nośników lub
wskaźników biologicznych przeznaczonych
do rutynowej kontroli nominalna liczba
zdolnych do życia organizmów powinna
wynosić
≥ 1,0x10
5
na jednostkę
oraz powinna być ustalona z dokładnością nie
większą niż 0,1x10
5
[walidacja procesu ≥ 1,0x10
6
]

cd. PN-EN ISO 11138
Sterylizacja produktów stosowanych w ochronie zdrowia - Wskaźniki
biologiczne
Dla każdej serii wskaźników biologicznych
lub zaszczepionych nośników wytwórca
powinien ustalić
wartość D w minutach z dokładnością do jednej
dziesiątej.
Wartość D wartość D10 czas lub dawka wymagana dla osiągnięcia 90% inaktywacji populacji
badanych drobnoustrojów w warunkach ustalonej dawki.
Wartość D powinna być ustalona w co
najmniej
trzech różnych temperaturach z zakresu 110
0
C
do 130
0
C

cd. PN-EN ISO 11138
Sterylizacja produktów stosowanych w ochronie zdrowia - Wskaźniki
biologiczne
Na każdym opakowaniu wskaźników
biologicznych powinny być informacje:
Nazwa organizmu testowego
Numer uznanej kolekcji szczepów
Nominalna liczba organizmów testowych
na jednym nośniku
Jednorazowy kod pozwalający na
odtworzenie procesu wytworzenia
Liczba wskaźników
Zalecone warunki przechowywania
Data ważności

cd. PN-EN ISO 11138
Sterylizacja produktów stosowanych w ochronie zdrowia - Wskaźniki
biologiczne
Nazwa i adres wytwórcy
Proces sterylizacji lub zakres procesów
sterylizacji, do których wskaźniki są przeznaczone
Instrukcja użycia, powinna zawierać warunki
hodowli po ekspozycji w procesie sterylizacji
Oporność badanych organizmów wyrażona jako
wartość D dla 121
0
C, z wyjątkiem przypadku gdy
wskaźnik jest przeznaczony tylko do procesu o
jednej, ściśle określonej temperaturze i czasie
ekspozycji, wówczas należy określić wartość D dla
tej określonej temperatury;
Wartość z, tam gdzie została określona

Kontrola biologiczna w procesie
sterylizacji medycznej – podsumowanie
Kontrola procesu sterylizacji fizyczna, chemiczna i
biologiczna
Sterylizacja niskotemperaturowa kontrola każdego cyklu
Sterylizacja para wodna 1x 3 miesiące; wytyczne CDC
1x tydzień/ każdego dnia, każdy cykl zawierający
implanty
Liczba zastosowanych wskaźników uzależniona od
wielkości komory/ rodzaju sterylizowanego materiału.
[normy – liczba uzależniona od zgromadzonych danych,
zanieczyszczenia mikrobiologicznego, dokumentacji
rozkładu czynnika sterylizującego, im większa
różnorodność parametrów procesu tym większa ilość
wskaźników]

Kontrola biologiczna w procesie
sterylizacji medycznej – podsumowanie
Wskaźniki biologiczne potwierdzają bójczośc procesu
sterylizacji (wiarygodne jeżeli kontrola jest powtarzalna).
Zgodne z normą 11138, stosowane zgodnie z zaleceniem
producenta, umieszczone w miejscu najbardziej krytycznym.
Nominalna liczba zdolnych do życia organizmów ≥ 10
5
, 10
6
–
walidacja
Wskaźniki biologiczne nie są przeznaczone do wskazywania,
że produkty oraz każdy poddawany sterylizacji wsad jest
sterylny. [SAL – funkcja wykładnicza, oś redukcji
drobnoustrojów].
Orzekanie o sterylności na podstawie ustalonej procedury
oceny zapisów parametrów krytycznych procesu, odczytu
wskaźników.

Kontrola biologiczna w procesie sterylizacji
medycznej
W normach międzynarodowych wymaga się, aby
przypadkowe zanieczyszczenie mikrobiologiczne wyrobu
medycznego przed sterylizacją zostało
zminimalizowane.
Jeżeli wymagania normy są spełnione, umożliwiają
prowadzenie procesu sterylizacji o odpowiednim
działaniu bójczym.
Ponadto zgodność z wymaganiami, zapewnia, że proces
sterylizacji jest zarówno niezawodny, jak i odtwarzalny,
tak więc założyć można z uzasadnioną ufnością, że
istnieje małe prawdopodobieństwo znalezienia zdolnego
do życia drobnoustroju na wyrobie medycznym po
sterylizacji.

Grunt, to mieć
proces pod
kontrolą
Strona czysta
Strona brudna
Strona sterylna
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
Wyszukiwarka
Podobne podstrony:
WSKAŹNIKI DO KONTROLI PROCESÓW STERYLIZACJI
kontrola cyklu komorkowego i smierc komorki, BIOLOGIA UJ LATA I-III, ROK II, semestr I, biologia kom
hand-out agresja, BIOLOGIA UJ LATA I-III, ROK III, dydaktyka, psychologia, Nowy folder
METODY BIOLOGICZNE W KONTROLI JAKOŚCI WODY
Nowy Porządek Świata – Plan kontroli waszych pieniędzy i waszej żywności
biologia praca kontrolna str 2
Dezynfekcja, sterylizacja, kontrola sterylizacji
lista kontrolna czynniki biologicznepl
Nowy regulamin cwiczen, Biologia UWr, II rok, Fizjologia Zwierząt
NOWY DOKUMENT PROGRAMU MICR, biologia
Praca kontrolna - Gimnazjum V semestr - biologia, Inne
kontrola ekspresji genów, Licencjat, Semestr IV, biologia molekularna
Toxoplazma gondii-sciagi, Medycyna, Biologia medyczna, Giełdy, Ściągi, Nowy folder
DNO miednicy masaż., Medyczne Studium Zawodowe ul. Szamarzewskiego, Sterylizacja medyczna, TSM, sem.
Lk Dezynfekcja i sterylizacja, Listy-Kontrolne-DOC
biologia praca kontrolna str 1
Kontrola stanu czystości wód metodami biologicznymi
PRACA KONTROLNA NR 2 Z BIOLOGII SEMESTR II
więcej podobnych podstron