Bioenergetyka
Elementy chemii
A + B
C + D
K = [C] [D]/ [A] [B]
ΔG= - RT ln K
Reakcja egzoergiczna
Reakcja endoergiczna

K
ΔG [cal/mol]
0.001
+4089
0.1
+1363
1
0
10
-1369
100
- 2726

Ciepło spalania [ 1 g]
Cukry
4,1 kcal
Glukoza
3,75 kcal
Lipidy
9,3 kcal
Proteiny
4.1 kcal

Kierunki reakcji
Glu-1-P = Glu-6-P E1: fosfoglukomutaza
ΔG= - 1740 cal/mol
ΔG= -RTlnK; K=19,0
Reakcje następcze
A
B
B
C
A
C
ΔG 1
ΔG 2
ΔG = ΔG 1 - ΔG 2
6-Glu-1-P = Glu-6-P - 1740 cal/mol
Glu-6-P = Fru-6-P + 400 cal/mol
Glu-1-P = Fru-6-P - 1340 cal/mol
Fosforany.Nośniki energii
Fosfoenolo pirogronian
- 14.8 kcal / mol
Fosforan kreatyny
- 10.3 kcal
ATP = ADP + P
- 7.3 kcal
ADP = AMP + P
- 7.3 kcal
AMP = A + P
- 3.4 kcal
Glu-1-P = Glu + P
- 5.0 kcal
Glu-6-P = Glu + P
- 3.8 kcal

Katabolizm
• Zysk energetyczny
• Synteza
• Transport
• Ruch
• Równowaga
materiałowa
• Procesy degradacji
• Węglowodany
• Białka
• Lipidy
• węglowodory
Prototrofy D-glukoza----- składniki komórkowe
Auksotrofy D-glukoza + dodatki----- składniki komórkowe

Substraty energetyczne
• ½ O2 + 2H+ + 2e- = H2O
• Oddychanie tlenowe
• Związek utleniony + e- = związek zredukowany
• Fermentacja beztlenowa
• CO2 + e- = CH4
• Fermentacja metanowa
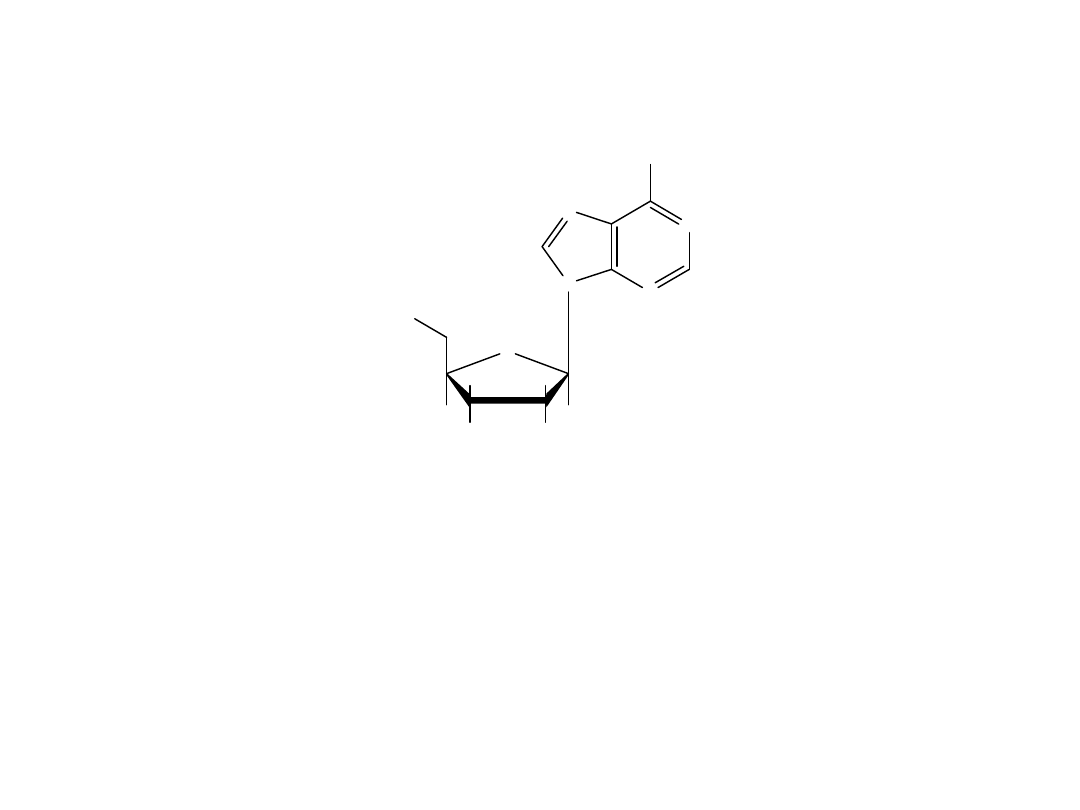
ATP
N
N
N
N
NH
2
O
OH
OH
H
H
H
H
P
3
O
ATP + H2O = ADP + P - 7.3 kcal/mol
Synteza biomolekuł E.coli [ATP] 7.90 mM
Transport przez membrany
[ADP] 1.04 mM
Praca mechaniczna, ruch
Przekaz informacji
Katalizatory: kinazy

Katabolizm Glukozy
D-Glu
Kwas mlekowy
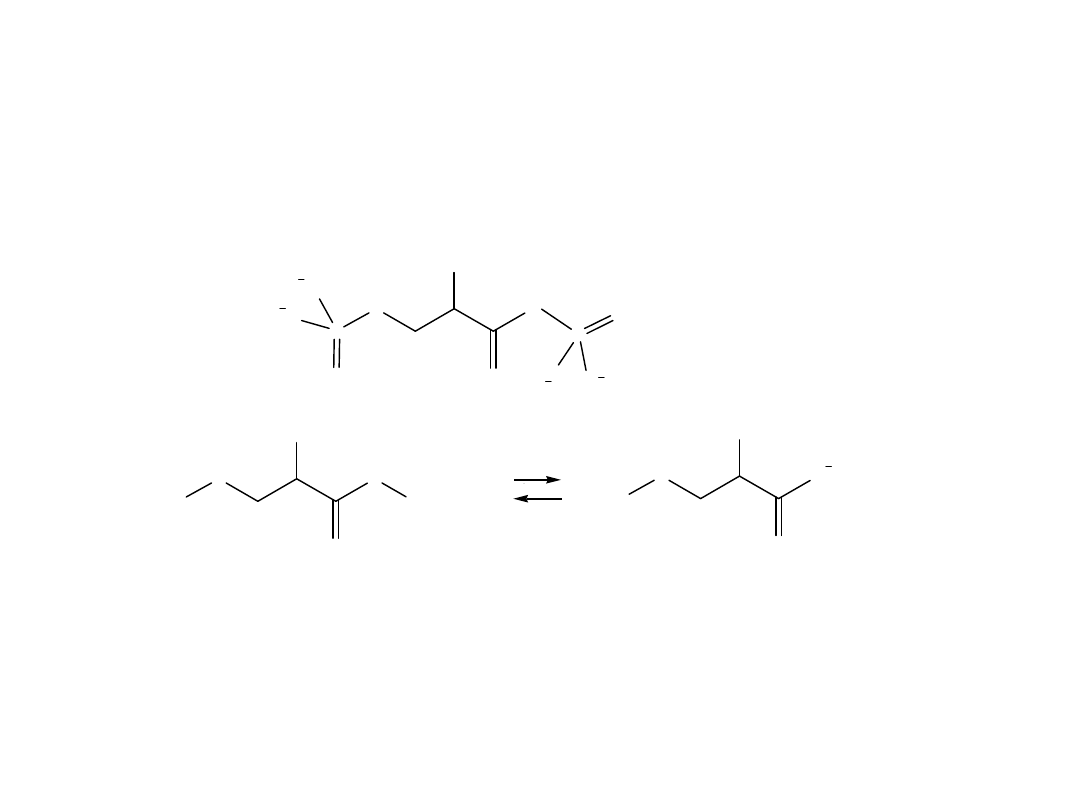
O
P
O
O
O
O
OH
O
P
O
O
O
O
P
O
OH
O
P
Mg
2+
O
P
O
OH
O
+ ATP
ADP
+
Fosforylacja substratowa
G= - 11,8 kcal/mol
3-fosfoglicerofosforan
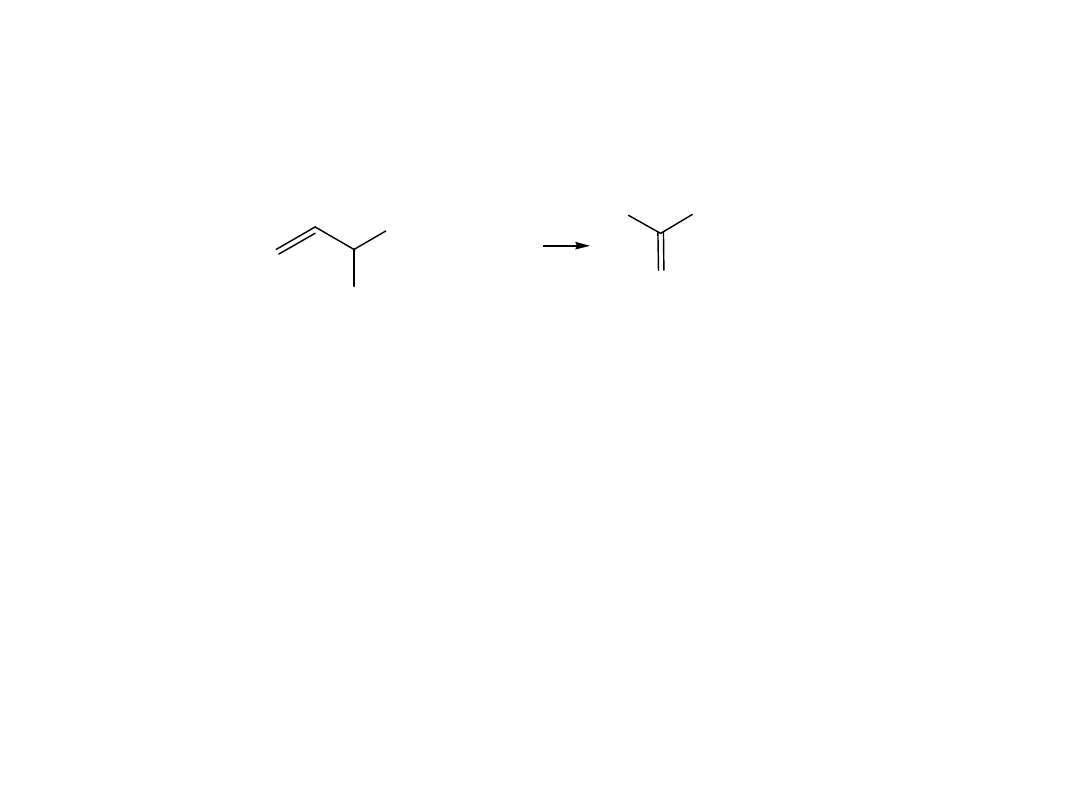
Fosforylacja substratowa
COO
-
OP
+ ADP
H
3
C
O
COO
-
+ ATP
Fosfoenolopirogronian
PEP
G= - 14,8 kcal/mol
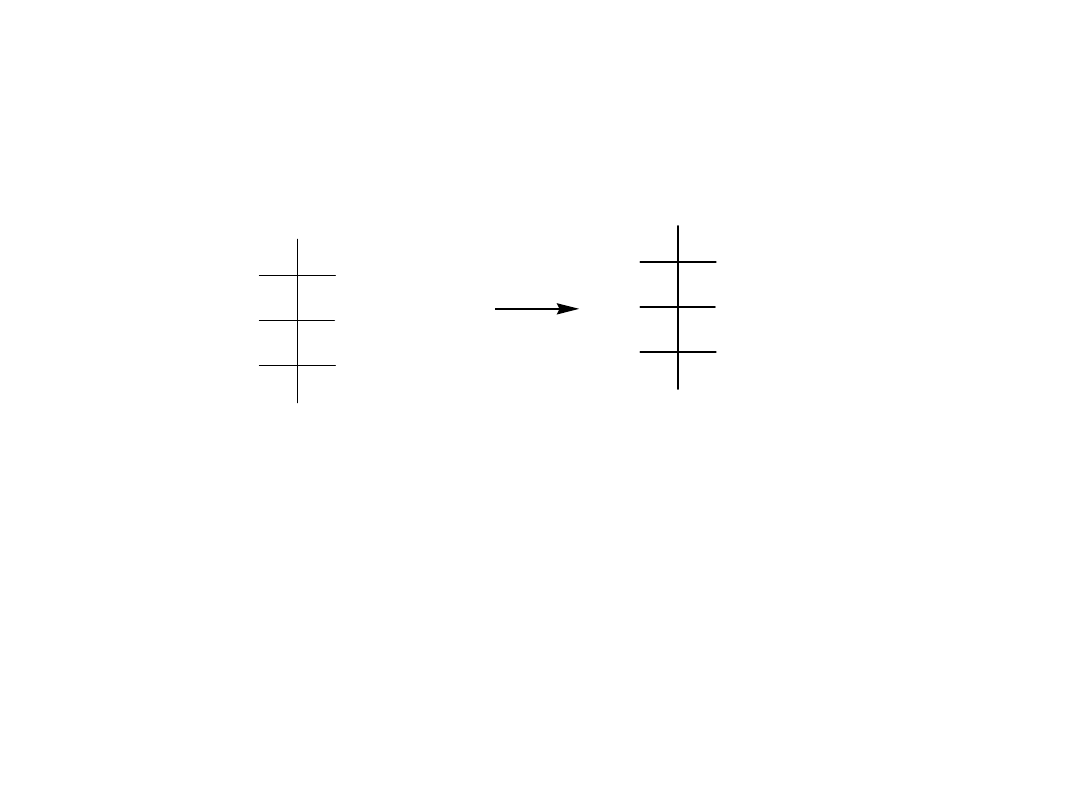
Fosforylacja substratowa
OH
H
H
H
OH
OH
H
H
+ ATP
OH
H
H
H
OH
OP
H
H
+ ADP
G
0
= - 2,2 kcal/mol

Reakcje ox-redox
A + e- = B Eox 0= a [V]
C + e- = D Ered 0= c [V]
a > c
A + D = C + D E0= Ered 0 - Eox
0
H
3
C
O
OH
O
+ e-
H
3
C
O
OH
OH
E
0
= - 0,32 V
NAD
+
+ e-
NADH + H
+
E
0
= - 0,19 V
H
3
C
O
OH
O
H
3
C
O
OH
OH
E
0
= + 0,13 V
+ NADH + H
+
NAD
+
+
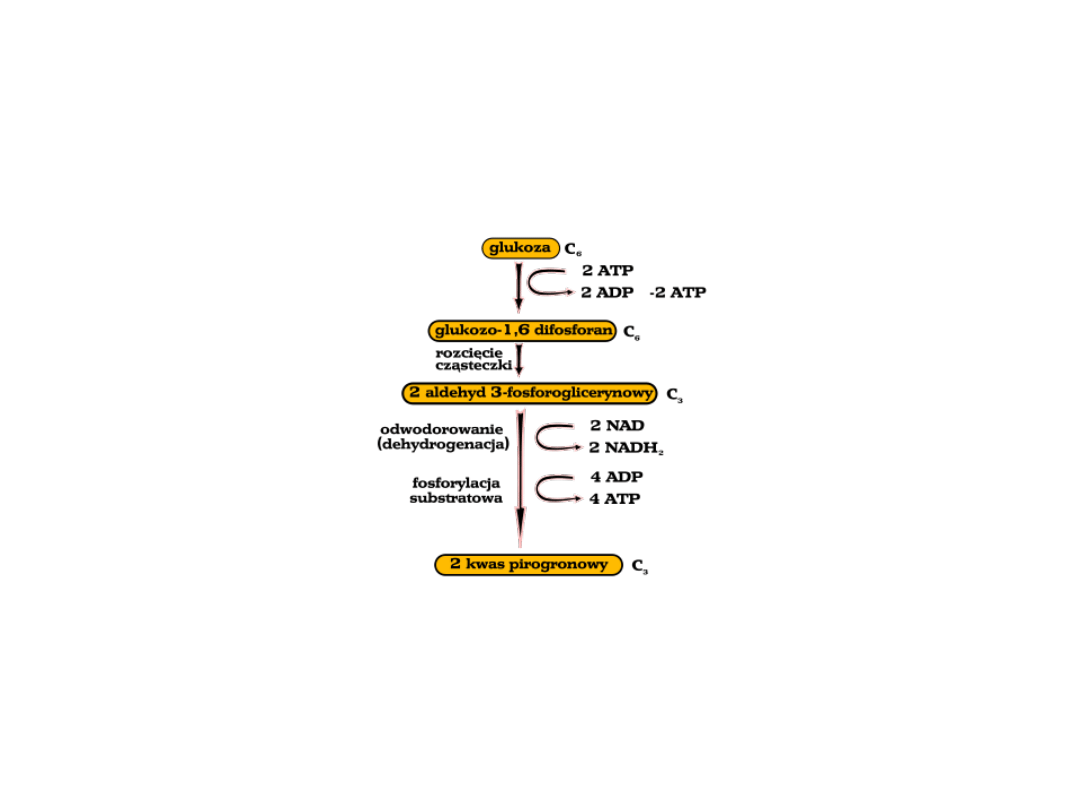
Glikoliza
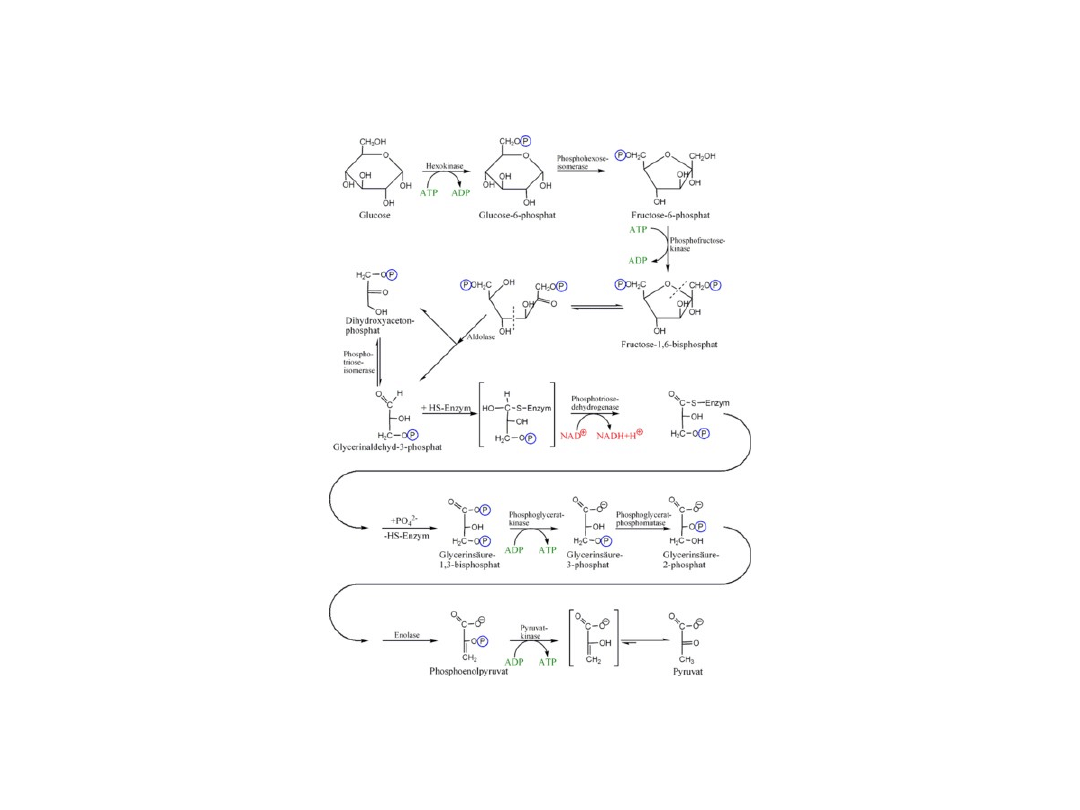
Glikoliza
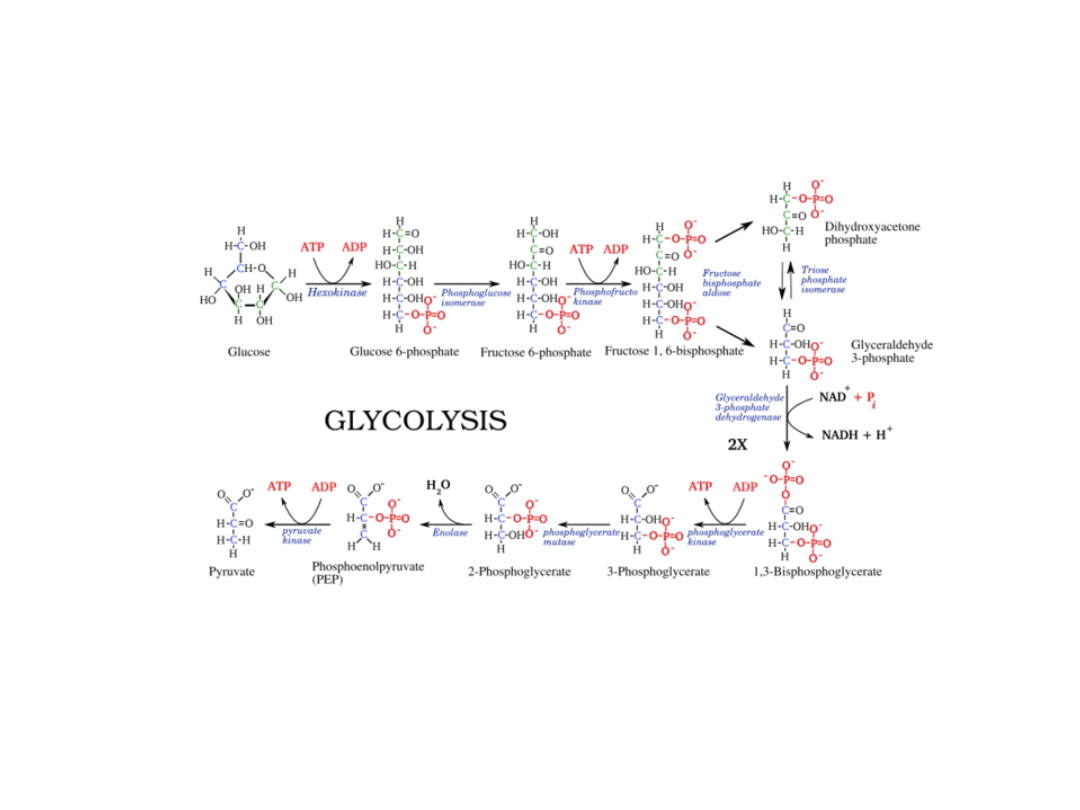
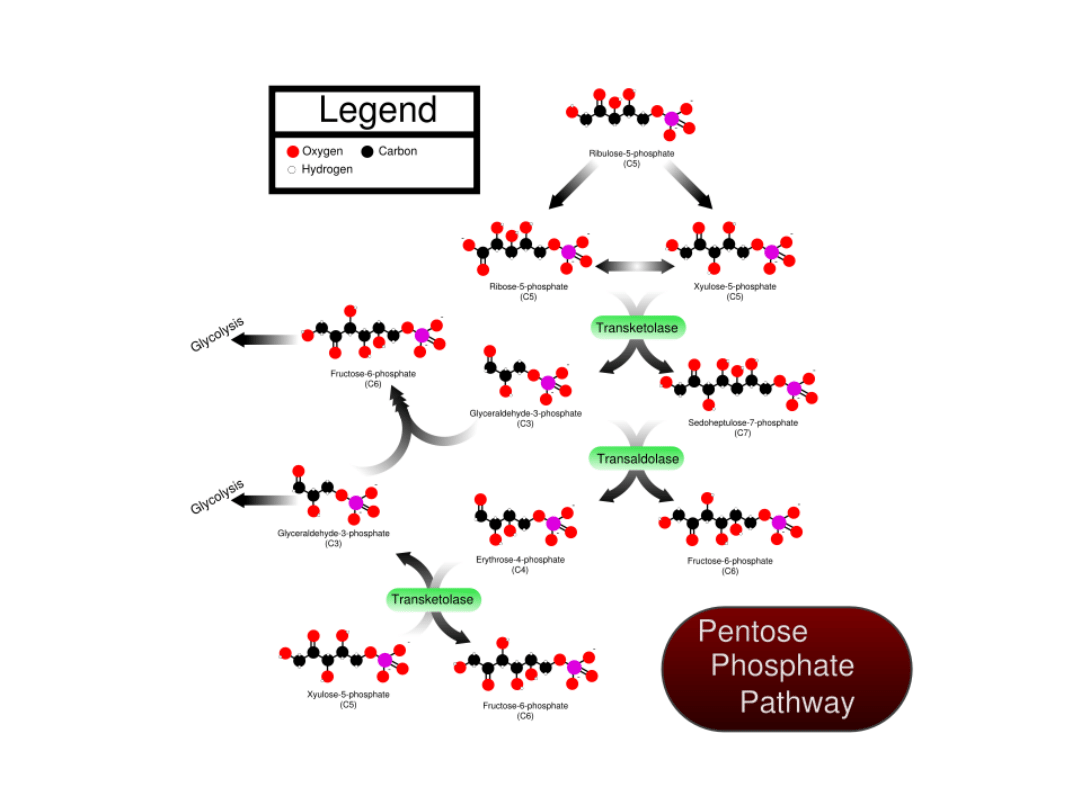
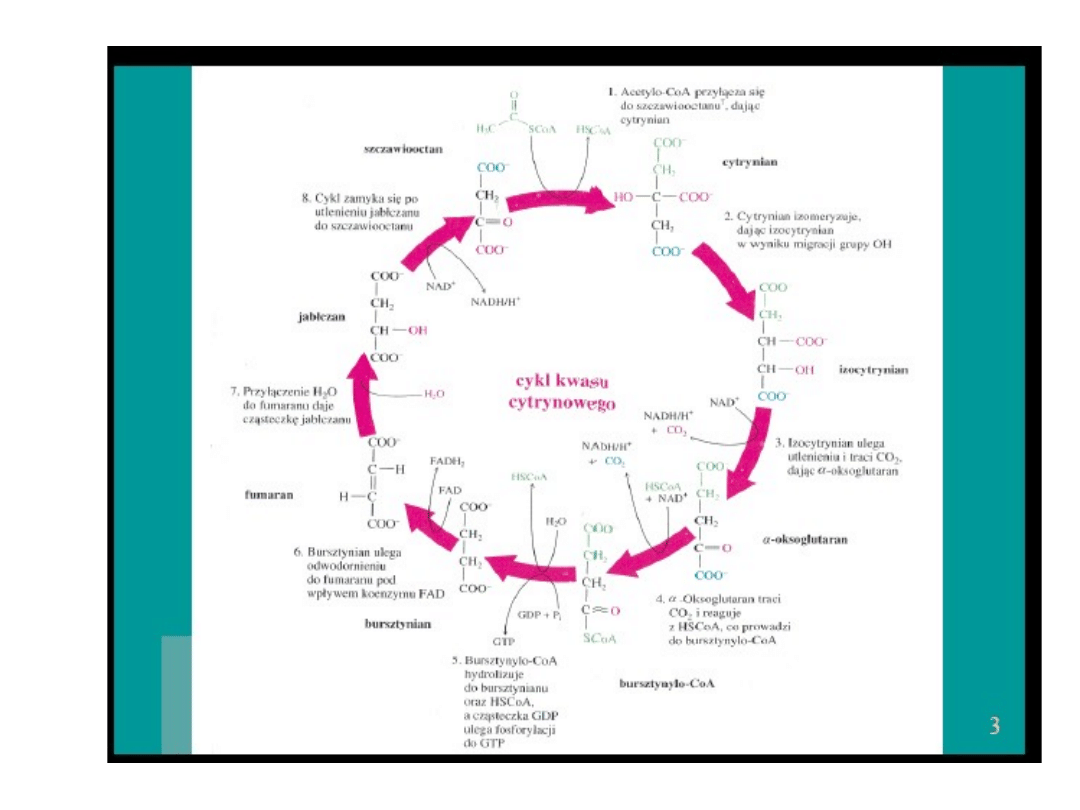
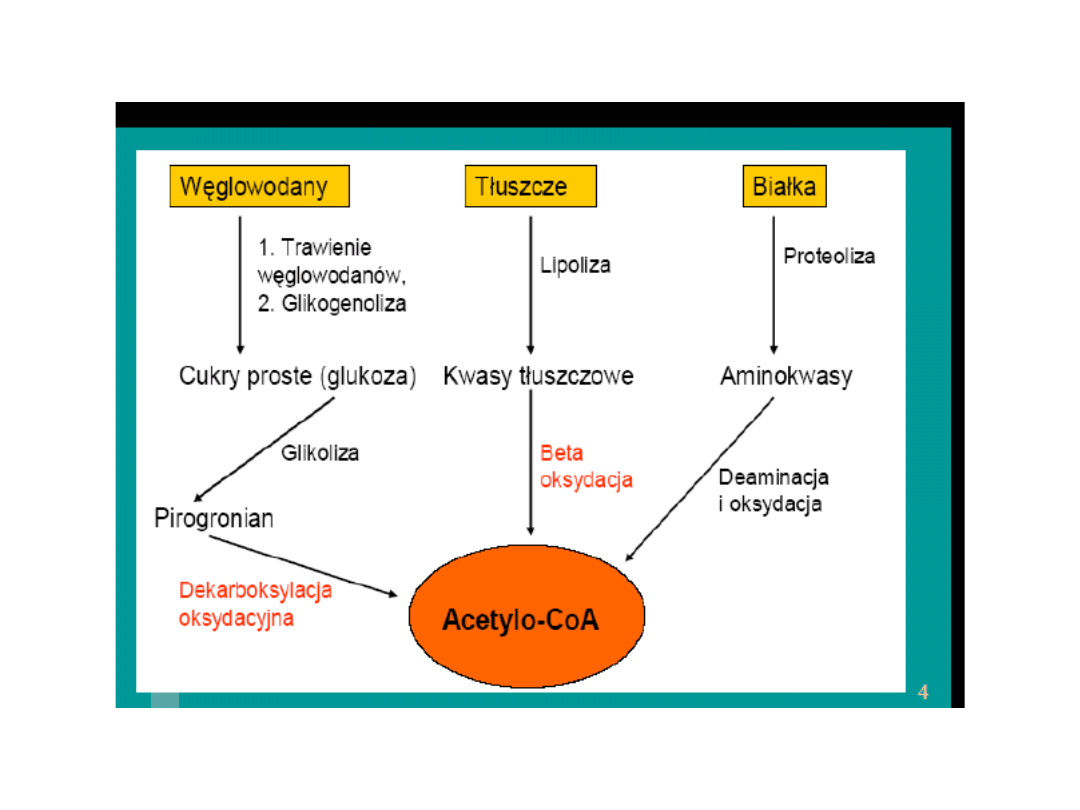


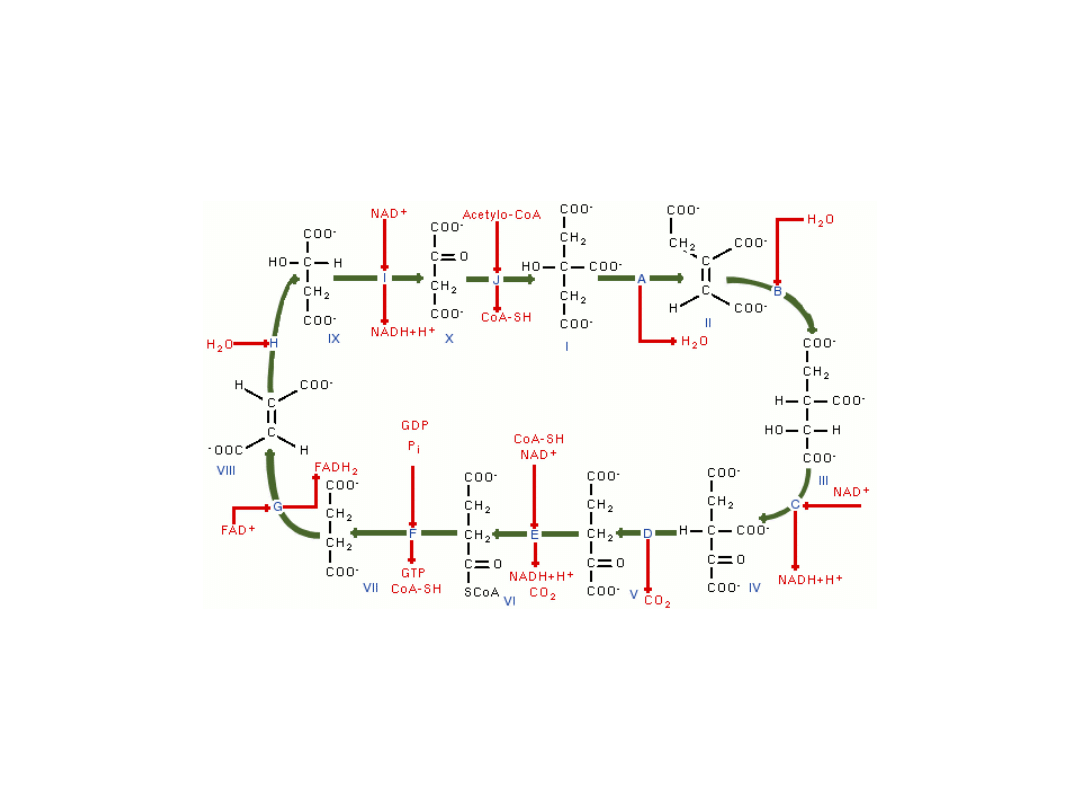
Sumarycznie równanie cyklu Krebsa przedstawia się
następująco:
acetylo-CoA + 3NAD+ + FAD + GDP + Pi + 2H2O =
2CO2 + 3NADH + FADH2 + GTP + 2H+ + CoA

Enzymy biorące udział w cyklu Krebsa
Syntataza cytrynianowa – jest dimerem u ssaków składającym się z
podjednostek o idealnej masie . Każde z miejsc aktywnych jest
umieszczone w szczelinie znajdującej się miedzy małą i duża domeną
każdej podjednostki w pobliżu styku obu podjednostek. Badania
wykazały ,że podczas katalizy ulega znacznym zmianom konfirmacyjnym.
Katalizuje reakcję kondensacji przez bliskie zestawienie substratów ,
odpowiednie ich zlokalizowanie przestrzenne i polaryzację odpowiednich
wiązań .

Akonitaza –białko żelazowo -siarkowe czyli białko
mające w składzie żelazo niehemowe . W centrum
enzymu są 4 atomy żelaza ,nie wbudowane w grupę
hemową.Tworzą one kompleks z 4 atomami siarki
nieorganicznej i 3 atomami siarki cysteiny.Centrum
zawierające żelazo wspólnie z innymi grupami enzymu
ułatwia reakcję odłączenie i przyłączenia wody .Centrum
enzymu charakteryzuje się mała stabilnością.

Dehydrogeneza izocytrynianowa – katalizuje
dekarboksylację oksydacyjną izocytrynianu , produktem
pośrednim tej reakci jest szczawiobursztynian
(niestabilny β-ketokwas). Podczas połączenia z enzymem
traci dwutlenku węgla i powstaje α-ketoglutaran.

Tiokinaza bursztynianowa –heterodimer zlożony z
podjednostek , jej działanie to przeniesienie grupy
fosforanowej najpierw do bursztynylo-CoA a następnie do
difosforanu nukleozydu .

Dehydrogenaza bursztynianowa białko żelazo-
siarkowe , zawiera 3 różne rodzaje ugrupowań żelazo-
siarkowych 2 Fe-2S ,3Fe-4S,4Fe-4S .Łączty się
bezpośredni z łańcuchem oddechowym , stanowi pomost
między cyklem kwasu cytrynowego a syntezą ATP.

Fumaraza – katalizuje przyłączenie atomu wodoru i
grupy hydroksylowej w układzie trans. Grupa
hydroksylowa przyłączana jest tylko z jednej strony
podwójnego wiązania fumaranu , dzięki czemu tworzy się
wyłącznie izomer L-jabłczanu.

Dehydrogenaza jabłczanowa – katalizuje reakcję
utlenienia do szczawianooctanu , akceptor wodoru jest
NAD+.

Dehydrogenaza jabłczanowa – katalizuje reakcję
utlenienia do szczawianooctanu , akceptor wodoru jest
NAD+.

PODSUMOWANIE
Substraty
/
Produkty
/
Koenzym
y
Koenzym
y
X.
S zczawio
octan
+ Acetylo-
CoA
I.
Cytrynian
A.
Akonitaza
Dehydrata
cja
H
2
O
II. cis -
Akonitan
B.
Akonitaza
Hydratacj
a
H
2
O
III.
Izocytryni
an
C.
Dehydrog
enaza
izocytryni
anowa
Utlenianie NAD
+
NADH +
H
+
IV.
S zczawio
bursztyni
an
D.
Dehydrog
enaza
izocytryni
anowa
Dekarbok
sylacja
H
+
CO
2
E .
Dehydrog
enaza
NAD
+
+
NADH +
H
+
ketoglutar
anowa
CoA-S H
0
GDP
GTP +
+ P
CoA-S H
VII.
bursztyni
an
G.
Dehydrog
enaza
bursztyni
anowa
Utlenianie FAD
FADH
2
VIII.
Fumaran
H.
Fumaraza
Addycja
H
2
O
H
2
O
IX. L -
J ablczan
I.
Dehydrog
enaza
jablczano
wa
Utlenianie NAD
+
NADH +
H
+
X.
S zczawio
octan
CoASH +
H
+
V.
Ketoglutar
an
Dekarbok
sylacja
oksydacyj
na
Czastecz
ka
Enzym
Typ
reakcji
J .
S yntaza
cytrynian
owa
Kondensa
cja
VI.
bursztyny
lo-CoA
F.
Tiokinaza
bursztyni
anowa
Hydroliza
H
2
O
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
Wyszukiwarka
Podobne podstrony:
Wykład 4 Podstawy prawne finansów publicznych
Idea holizmu - wykład 2, podstawy pielęgniarstwa
wykłady z podstaw ekonomii
Konspekt wykładów z Podstaw automatyki wykład 5
Zagadnienia egzaminacyjne PF3-09, SKRYPTY, NOTATKI, WYKŁADY, Podstawy Fizyki 3, wykład
1 wykład Podstawowe pojęcia i przedmiot ekonomi
Wykład 1 - Podstawy organizacji, zarządzanie bhp
Wykład -Podstawy turystyki, Turystyka i Rekreacja, Podstawy turystyki
ZFP wykład 4, podstawy finansów przedsiębiorstwa
Projektowanie baz danych Wykłady Sem 5, pbd 2006.01.07 wykład03, Podstawy projektowania
wykład 3 - podstawy zarządzania - 10.01.2010
wykłady, Podstawy kinezjologi, Podstawy kinezjologi
Wykład 7 PODSTAWOWE ELEMENTY ORGANIZOWANIA
Wykłady Podstawy Fizjologii Człowieka
Wyklad I - podstawy prawne psychiatrii, Psychopatologia
2)WYKŁAD 2 PODSTAWOWE KRYTERIA KLASYFIKACJI ODPADÓW
więcej podobnych podstron