
METABOLIZM
LIPIDÓW
Katedra i Zakład Biochemii
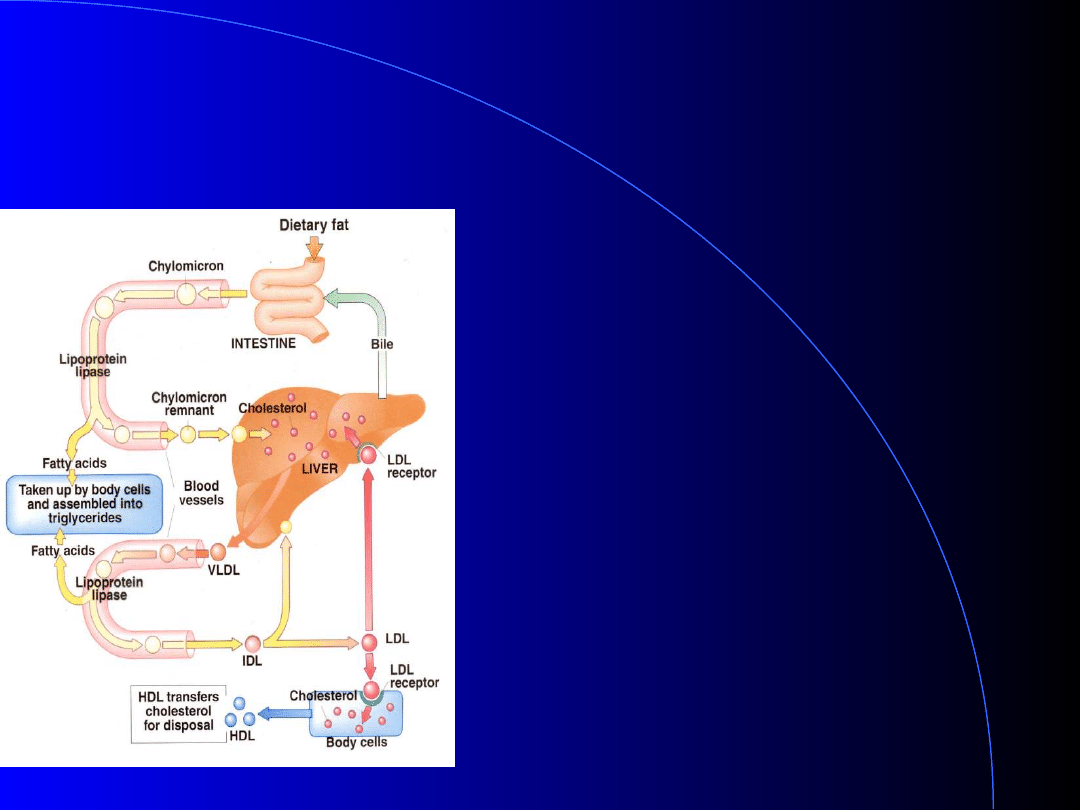
TRANSPORT LIPIDÓW W
TRANSPORT LIPIDÓW W
ORGANIZMIE I POMIĘDZY
ORGANIZMIE I POMIĘDZY
TKANKAMI
TKANKAMI
• WKT „wolne kwasy tłuszczowe
”
- związane z albuminami –
absorbowane w jelicie
i przenoszone
do wątroby, mięśni i adipocytów oraz
endogenne KT
pochodzące głównie
z tkanki tłuszczowej transportowane do
wątroby i mięśni, a także pozostałych
wykorzystujących je tkanek
b)
Lipoproteiny
– chylomikrony,
VLDL, LDL, IDL i HDL
c)
„ciała ketonowe”
– acetooctan
i β-hydroksymaślan
Chylomikrony
Chylomikrony
Transportują lipidy diety z enterocytów do
tkanek organizmu
Większość lipidów to triglicerydy
Mało białka
–
ApoA-I, ApoA-II, ApoB-48, ApoC
Resynteza: TAG, EstryCh i
Fosfolipidy
Apolipoproteina B-48
Wit. rozp. tłuszczach
do limfy do krwi
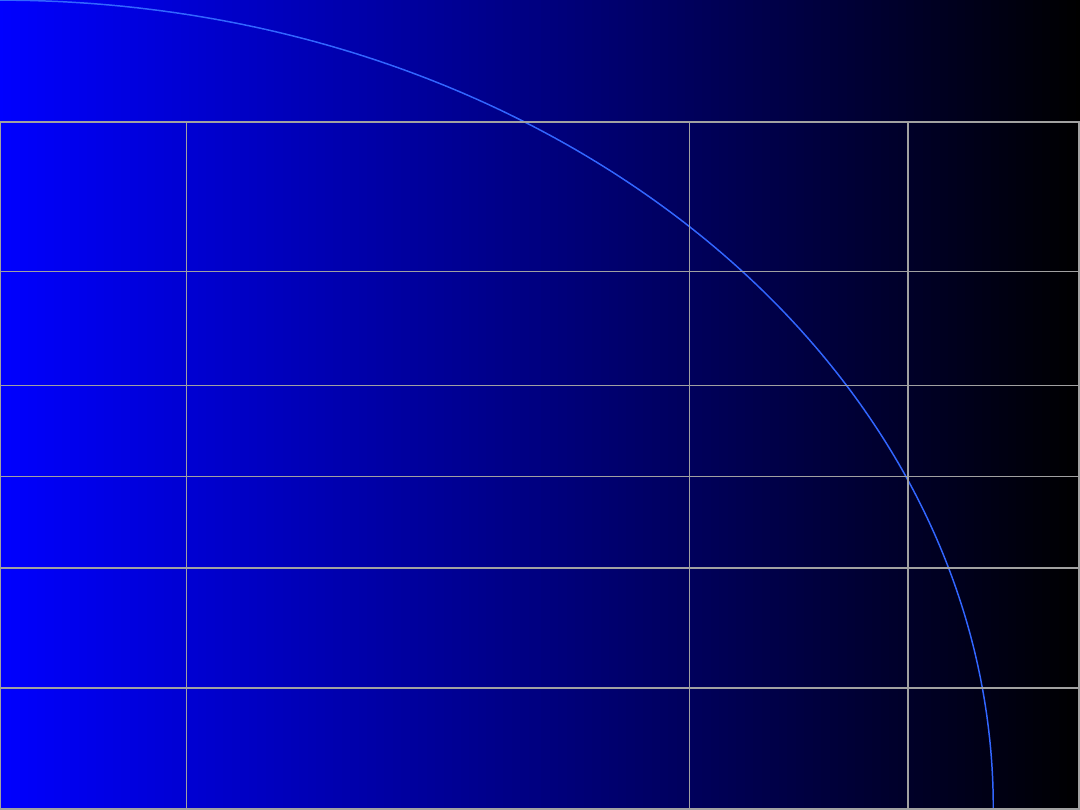
Tab. 1 Rodzaje kwasów tłuszczowych
Ogólny wzór strukturalny kwasu tłuszczowego
(CH
3
(CH
2
)
n
COOH)
n – liczba parzysta
Kwasy
tłuszczo
we
Wzór
Liczba
wiązań
podwójnyc
h
Liczba
atomów
C
Palmityni
an
CH
3
-(CH
2
)
14
COOH
-
16
Stearynia
n
CH
3
-(CH
2
)
16
COOH
-
18
Oleinian
CH
3
-
(CH
2
)
7
CH=CH(CH
2
)
7
C
OOH
1
18
Linolan
CH
3
-(CH
2
)
4
-
(CH=CHCH
2
)
2
(CH
2
)
6
C
OOH
2
18
Linolenia
n
CH
3
-CH
2
-
(CH=CHCH
2
)
3
(CH
2
)
6
C
OOH
3
18
C16:0
C18:0
C18:1,
9
C18:2,
9,12
C18:3,
9,12,15
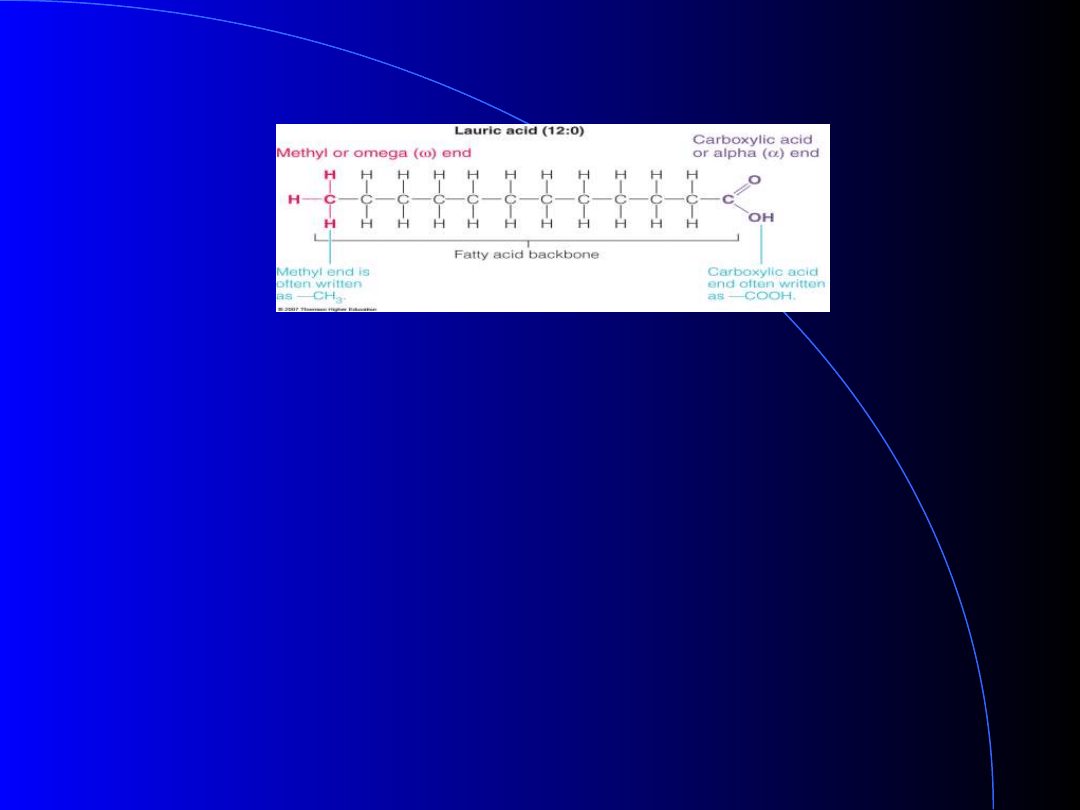
Kwasy Tłuszczowe jako źródło
Kwasy Tłuszczowe jako źródło
energii
energii
α- oksydacja – retikulum endoplazmatyczne, mitochondria – służy prawdopodobnie
utlenianiu nietypowych KT (np. z gr. –CH
3
) [utl. C 2 poprzez –OH
i usunięcia C 1 jako CO
2
,
z utlenieniem –OH do –COOH – skrócenie o 1C
β - oksydacja – mitochondria – energia, udział karnityny, acetylo-CoA;
peroksysomy – skracanie KT n > 20C, rozgałęzionych, hydroksylowanych,
brak udziału karnityny i zysku energii
ω – oksydacja – retikulum endoplazmatyczne – metabolizm nietypowych KT (w tym
hydroksykwasów poprzez utlenienie ostatniego węgla (CH
3
-
)
do grupy –COOH,
powstawanie krótkich kwasów dikarboksylowych

Synteza kwasów tłuszczowych
Synteza kwasów tłuszczowych
-lipogeneza
-lipogeneza
Syntaza KT
acetylo-CoA + 7 malonylo-CoA + 14
(NADPH + H
+
)
kwas palmitynowy (16 C) + 7 CO
2
+ 14
NADP
+ 8 CoA +
6 H
2
O
Acetylo~CoA łączy się z malonylo~CoA
7 kolejnych etapów katalizowanych przez
wielofunkcyjny enzym
syntazę kwasów tłuszczowych
Proces aktywny w tkance tłuszczowej, w gruczołach
mlekowych
w czasie laktacji
Granica - 16 C (palmitynian)
Kluczowymi enzymami regulacyjnym są:
karboksylaza acetylo~CoA (powstaje
malonylo~CoA)
syntaza kwasów tłuszczowych
Synteza
Synteza
de novo
de novo
Kwasów
Kwasów
Tłuszczowych
Tłuszczowych
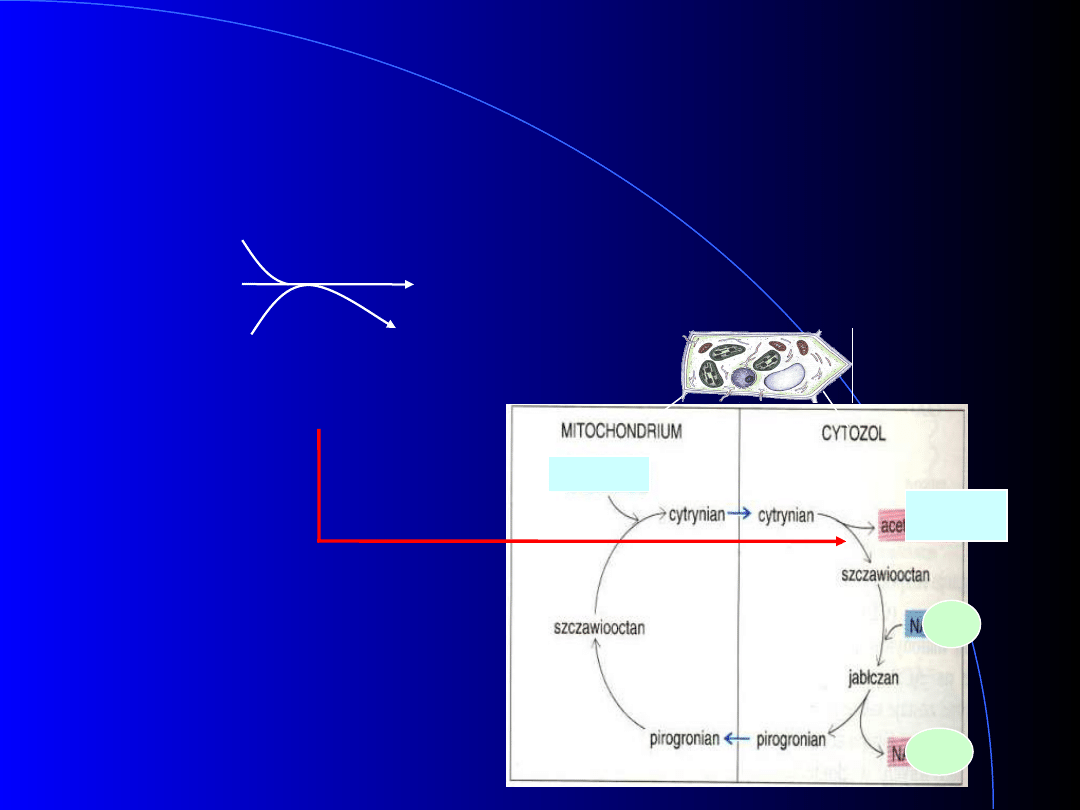
źródło acetylo~CoA w cytozolu
źródło acetylo~CoA w cytozolu
cytrynian
szczawiooctan +
acetylo~CoA
CoA
ATP
ADP + Pi
Liaza cytrynianowa
acetylo-CoA
acetylo-CoA
NADH
NADPH
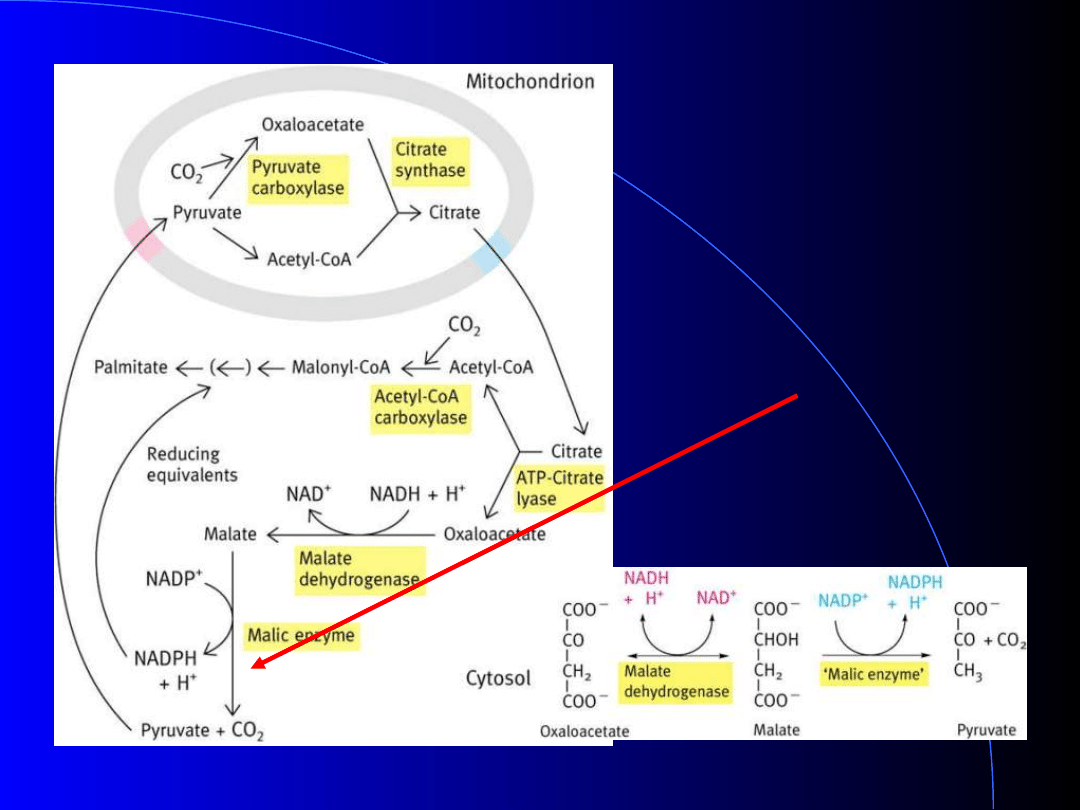
Źródło
NADPH
Cykl pentozowy
dehydrogenaza G6P (NADP)
oraz

Synteza malonylo~CoA
Synteza malonylo~CoA
Acetylo~CoA
Malonylo~CoA
CO
2
ATP
ADP + Pi
Karboksylaza acetylo~CoA
biotyna
(HCO
3
-
)
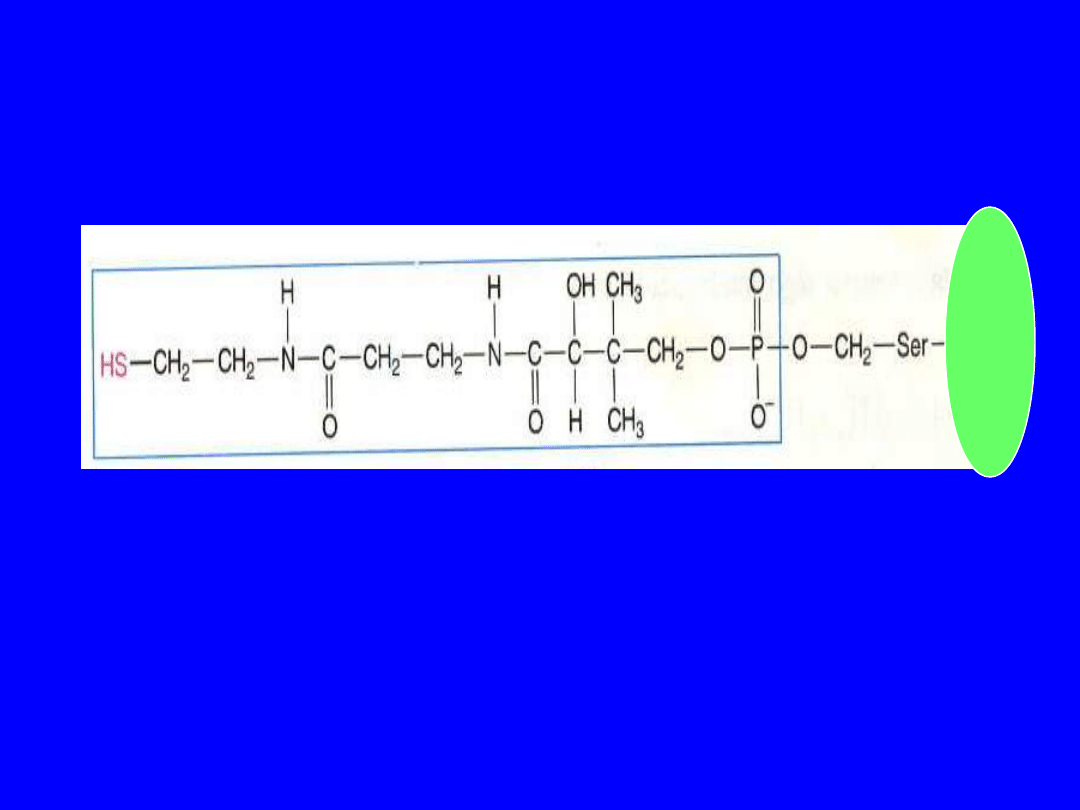
fosfopantoteina –
grupa prostetyczna ACP
ACP
Synteza kwasów tłuszczowych
Synteza kwasów tłuszczowych
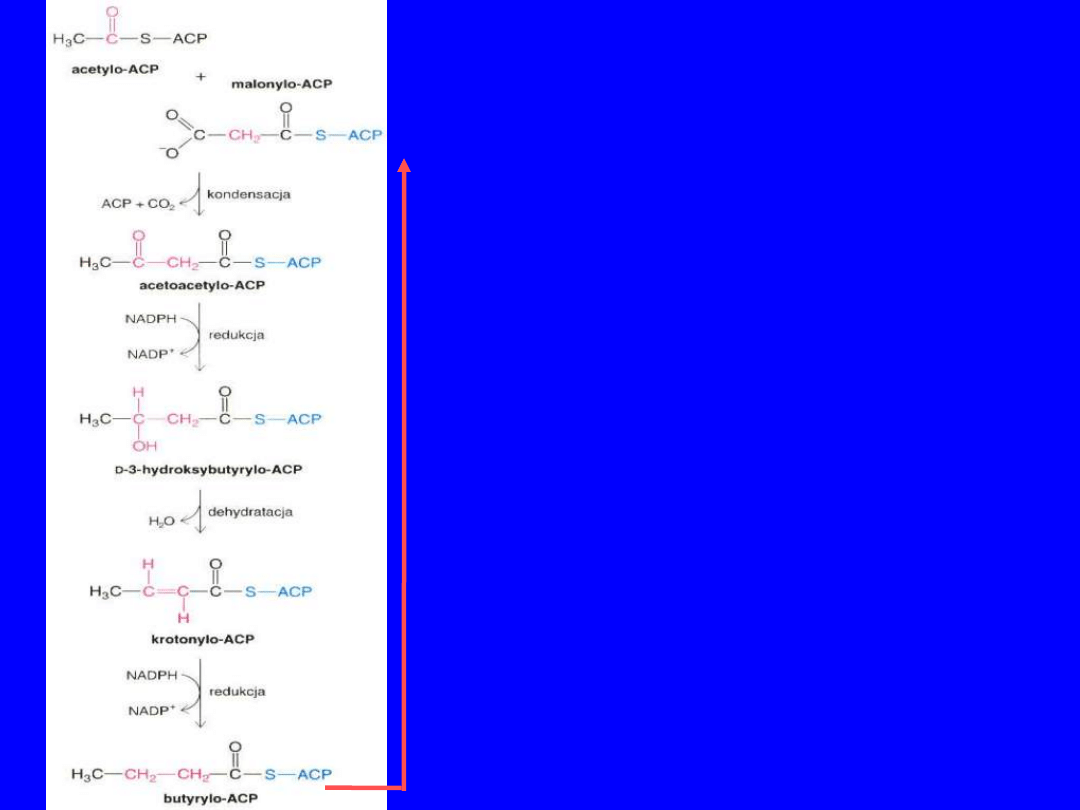
w drugim cyklu syntezy KT
butyrylo-
ACP
kondensuje
z malonylo-
ACP
tworząc β–ketoacylo-
ACP
,
który w wyniku redukcji, dehydratacji
i ponownej redukcji jest przekształcany
do acylo-
ACP
.
Acylo-
ACP
rozpoczyna trzeci cykl syntezy
kwasów tłuszczowych.
Synteza kwasów tłuszczowych
Synteza kwasów tłuszczowych
REGULACJA allosteryczna
REGULACJA allosteryczna
Acetylo~CoA
Malonylo~CoA
CO
2
ATP
ADP + Pi
Karboksylaza acetylo-CoA
biotyna
Cytrynian palmitoilo~CoA
+
--
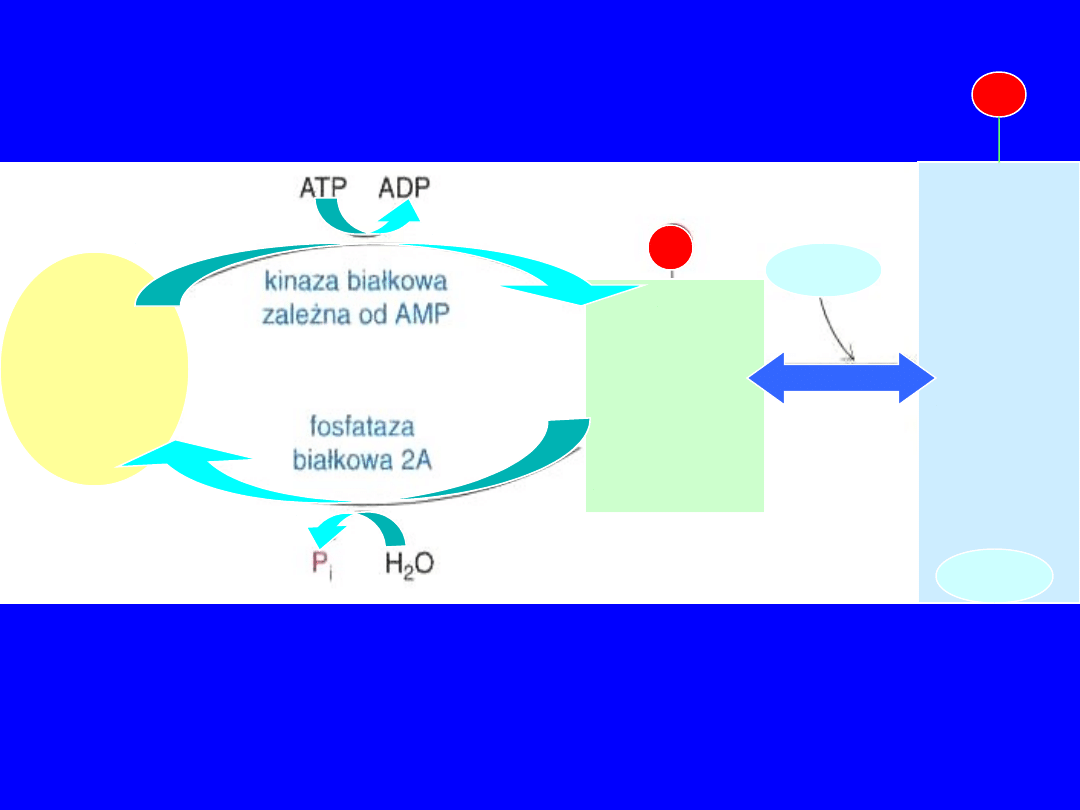
aktywna
karboksylaza
acetylo-CoA
(forma
nieufosforylowana
)
nieaktywna
karboksylaza
acetylo-CoA
(forma
ufosforylowana
)
częściowo
aktywna
karboksylaza
acetylo-CoA
cytrynian
cytrynian
P
P
REGULACJA
REGULACJA
Acetylo~CoA
Malonylo~CoA
CO
2
ATP
ADP + Pi
Karboksylaza acetylo-CoA
(aktywna)
Karboksylaza acetylo-CoA
-P
(nieaktywna)
biotyna
Synteza malonylo~CoA
Synteza malonylo~CoA
regulacja hormonalna
regulacja hormonalna
P
i
Fosfataza
białkowa
+
Insulina
(w krótkim czasie –P)
(na dłużej przez
indukcję syntezy tego enzymu)
ATP
ADP
_--_
Glukagon
adrenalina

Wydłużanie kwasów tłuszczowych
i wprowadzanie wiązań
podwójnych
U Eukariontów wydłużanie KT dłuższych niż palmitynian (C16)
i tworzenie wiązania podwójnego są katalizowane przez enzymy
zlokalizowane na powierzchni gładkiego retikulum
endoplazmatycznego.
Donorem
jednostek dwuwęglowych jest
malonylo-CoA,
a wydłużny KT jest związany z CoA,
a nie z ACP.
Wprowadzenie wiązania podwójnego wymaga aktywności
3 enzymów:
reduktazy cytochromu b
5
[NADH, O
2
],
cytochromu b
5
i desaturazy. Δ
9
,
Δ
6
,
Δ
5
,
Δ
4

Wiązania podwójne
W organizmach ssaków
nie występują
enzymy
zdolne do tworzenia wiązań podwójnych w położeniu
dalszym niż przy węglu
C9.
Dlatego ssaki
nie potrafią
syntetyzować
NNKT
kwas linolowy
C18: cis - Δ
9
, Δ
12
(
ω-6)
do syntezy kwasu arachidonowego
kwas linolenowy
C18: cis - Δ
9
, Δ
12
, Δ
15
(
ω-3)
przekształcany do kwasu dokozaheksaenowego (DHA)
C 22:6 & kwasu eikozapentaenowego (EPA) C 20:5

Funkcje Niezbędnych Kwasów
Funkcje Niezbędnych Kwasów
Tłuszczowych
Tłuszczowych
Eikozanoidy
–
Lipidowe mediatory zapalenia
syntetyzowane z kwasu
arachidonowego i EPA
–
Zawierają
Prostaglandyny
Prostacykliny
Tromboksany
Leukotrieny
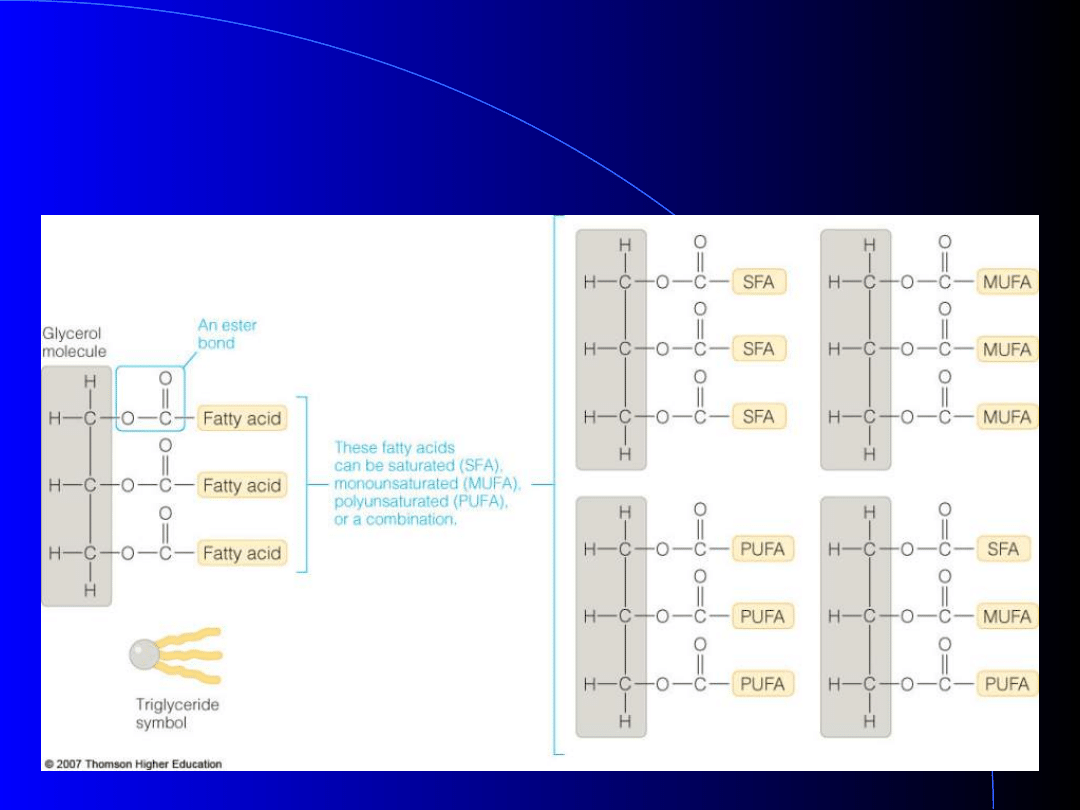
Tłuszcze obojętne stanowią
materiał
zapasowy

Funkcje Triglicerydów
Funkcje Triglicerydów
Dostarczają niezbędne KT do
funkcjonowania organizmu
Produkcja energii
Izolacja
Ochrona
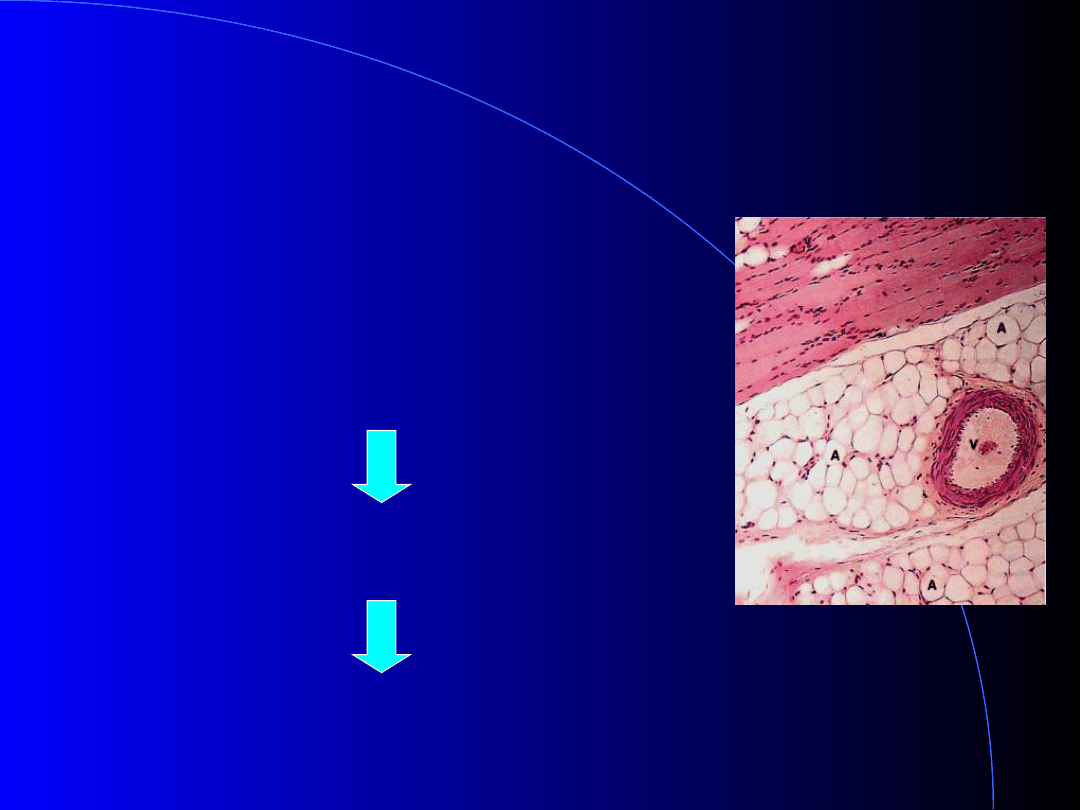
Rezerwa Energetyczna
Rezerwa Energetyczna
Adipocyty
Podskórna tkanka tłuszczowa
Trzewna tkanka tłuszczowa
Nadmiar energii
Insulina stymuluje
magazynowanie
triacylogliceroli
Lipogeneza
(Synteza KT &
triacylogliceroli)
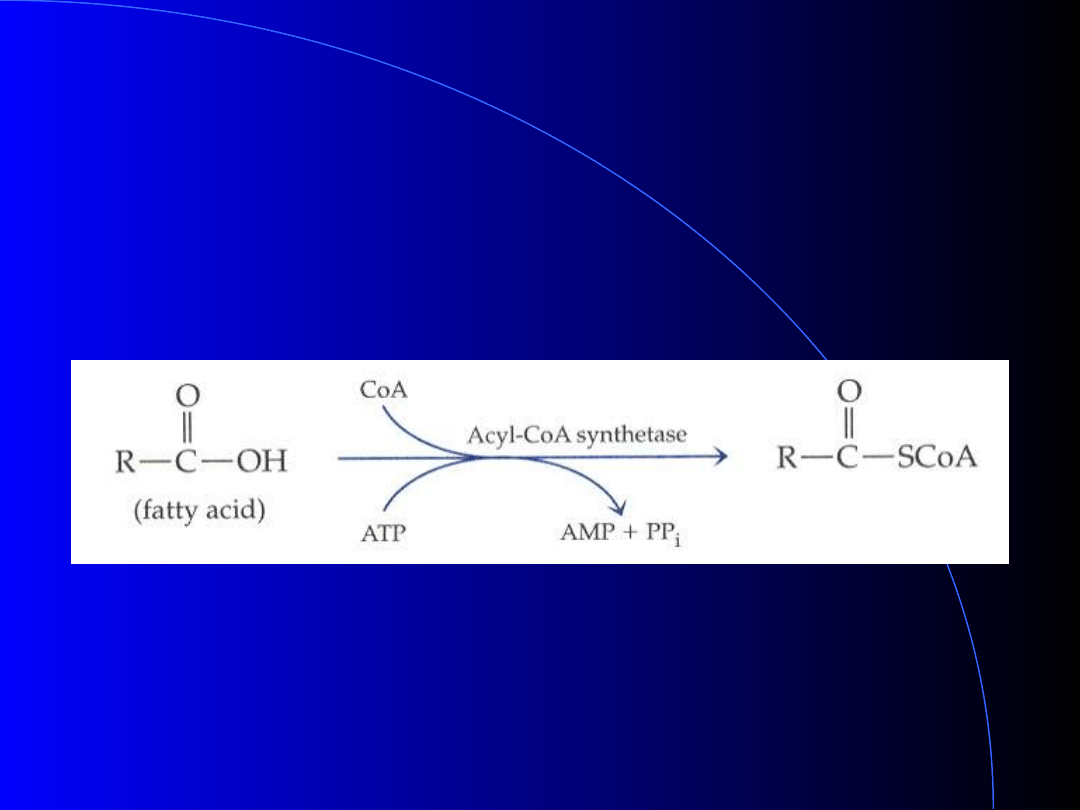
Aktywacja Kwasów
Aktywacja Kwasów
Tłuszczowych
Tłuszczowych
Dodanie CoA
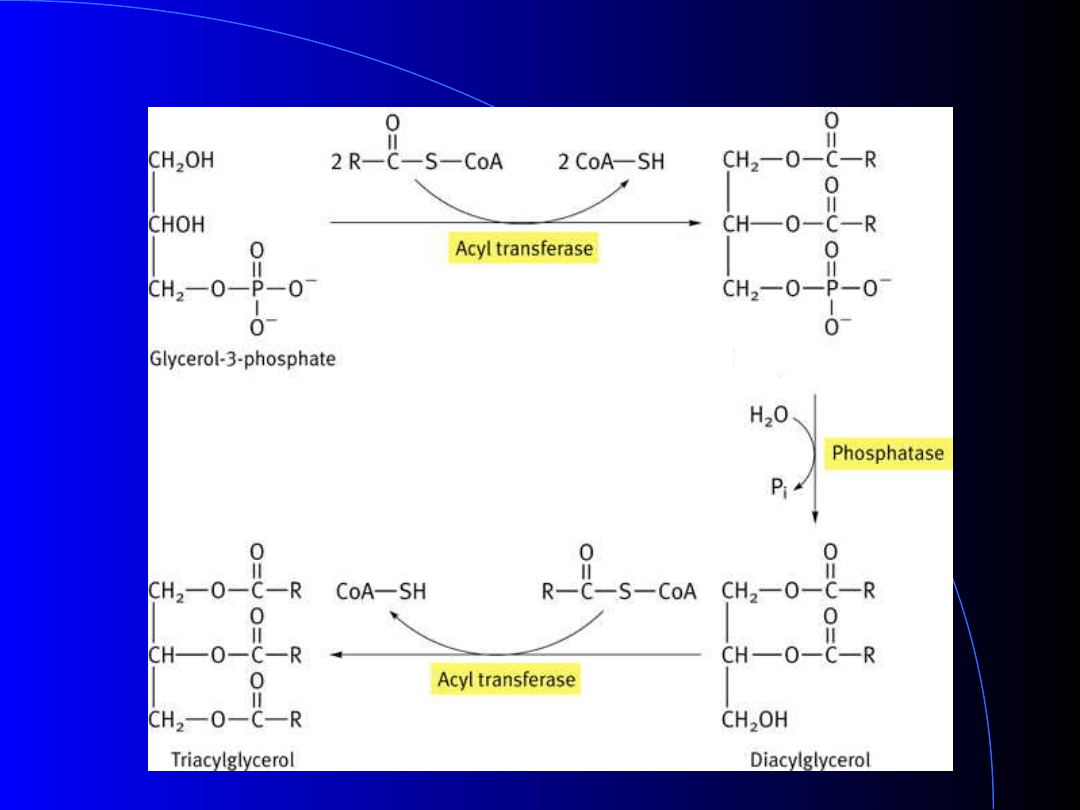
Synteza triacylogliceroli –
lipogeneza
Kwas fosfatydowy
H
2
C
OH
C
HO
H
H
2
C O P
H
2
C
OH
C
H
2
C O P
O
sn-glycerol -3P
ATP
ADP
glycerol
glycerol
kinase
minor
pathway
glycerol-3P
dehydrogenase
NADPH+H
+
NAD
dihydroxyacetone-
phosphate
glycolysis
insulin
+
major
pathway
3 acyl-CoA
Triacylglycerol
Lipogeneza
w wątrobie i tkance tłuszczowej
P-dihydroksyaceton
kinaza
glicerolowa
dehydrogenaza
3P-glicerolu

Metabolizm Lipidów
Metabolizm Lipidów
Złożonych
Złożonych
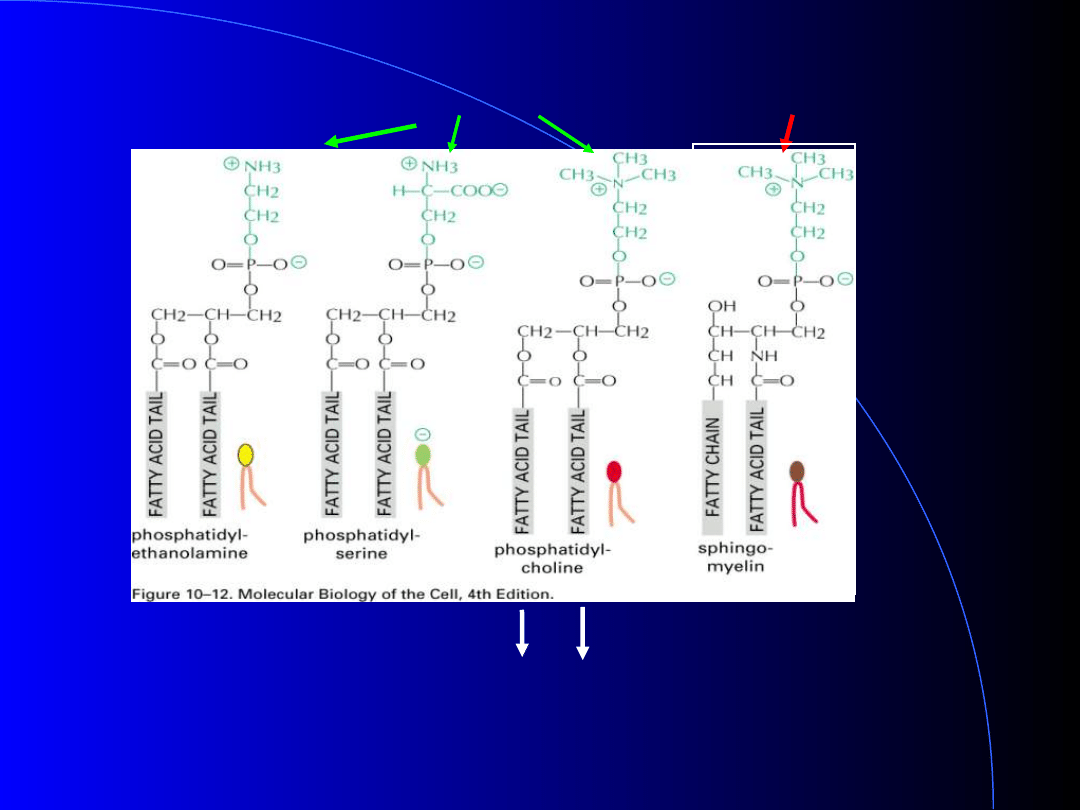
Fosfolipidy: glicerofosfolipidy, sfingofosfolipidy
kwas palmitynowy w pozycji sn1 i sn2
+ białka = surfaktant (dipalmitoilolecytyna)

Synteza Lipidów Złożonych
Synteza Lipidów Złożonych
Glicerofosfolipidy
[1]
kwas fosfatydowy + CTP
=> CDP-diacyloglicerol + PP
i
CDP-diacyloglicerol + cholina (etanoloamina, seryna,
inozytol) =>
lecytyna
(fosfatydyloetanoloamina,
fosfatydyloseryna,
4,5-difosfoinozytyd) + CMP
[2]
DAG + CDP-cholina
(CDP-etanoloamina, CDP-seryna,
CDP-inozytol) =>
lecytyna
(fosfatydyloetanoloamina,
fosfatydyloseryna, 4,5-difosfoinozytyd) + CMP
[3] wzajemne przekształcenia fosfolipidów pomiędzy sobą –
udział
m.in. metylacji i SAM jako dawcy grup –CH
3
fosfatydyloetanoloamina + 3 SAM => fosfatydylocholina
(lecytyna)
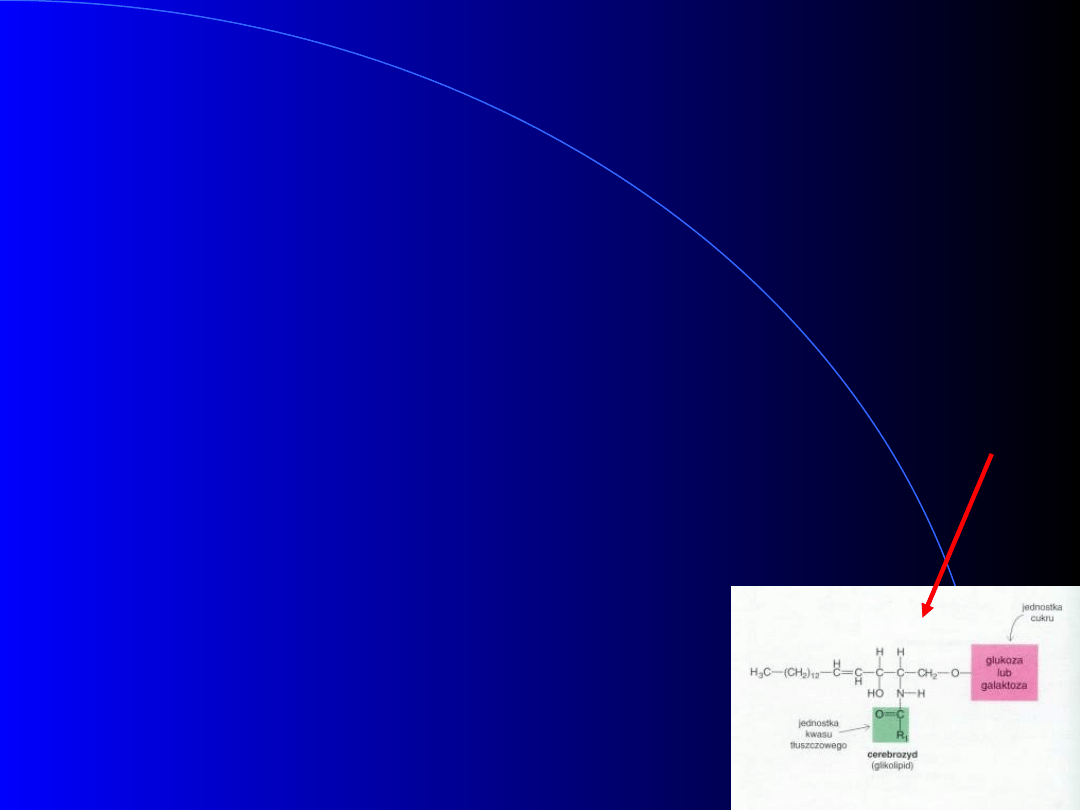
Synteza Lipidów Złożonych
Synteza Lipidów Złożonych
• Sfingofosfolipidy
palmityloCoA + seryna => => => sfingozyna
sfingozyna + acyloCoA => ceramid
Ceramid + CDP-cholina => sfingomielina
Ceramid + UDP-glukoza lub UDP-galaktoza => cerebrozydy
Cerebrozydy + UDP-monosacharyd (+CMP-NANA) =>
gangliozydy
Gangliozydy oparte na sfingozynie – to co odróżnia
grupy A, B i 0 krwi człowieka
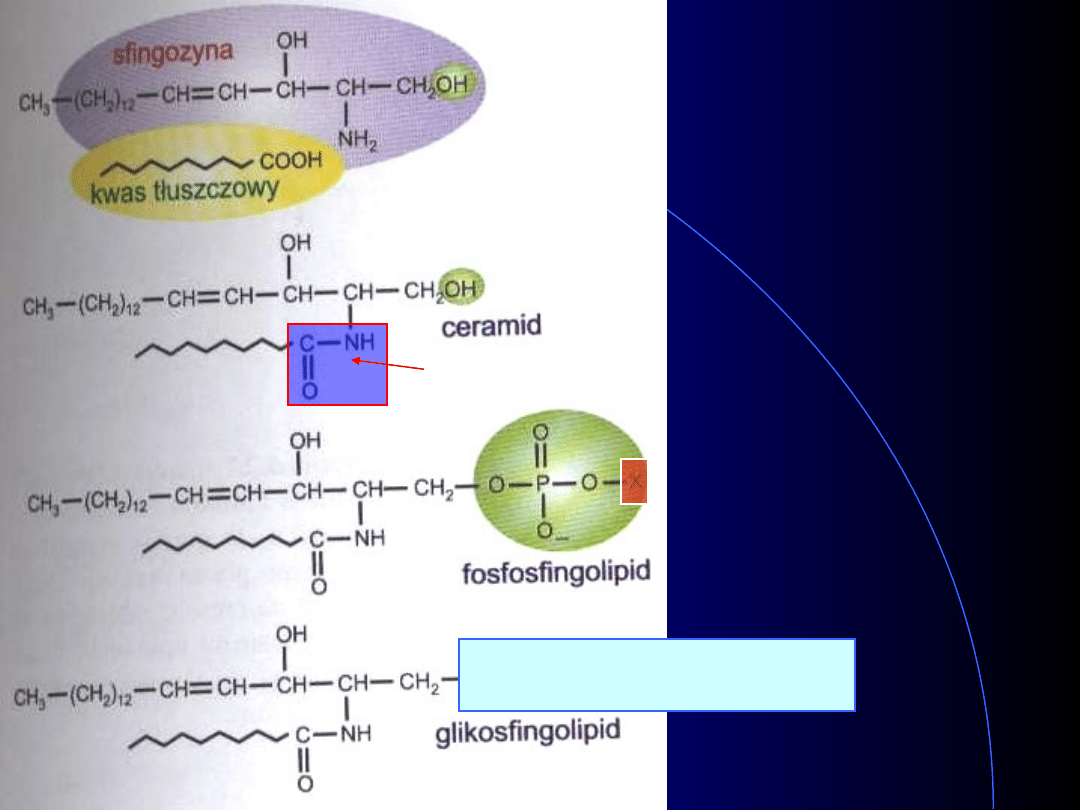
wiązanie amidowe (wiązanie peptydowe)
X- cholina, etanoloamina,
seryna, inozytol lub
inny związek
O – mono- lub oligosacharyd
X
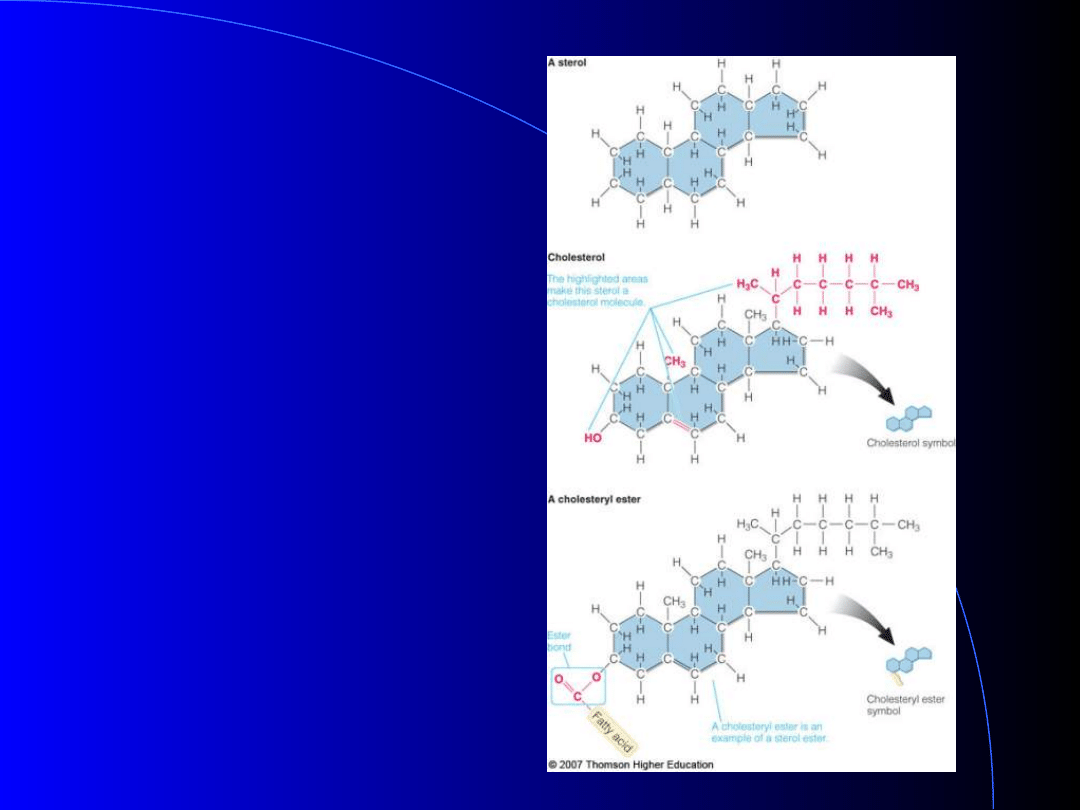
Sterole &
Sterole &
Estry Steroli
Estry Steroli
Steroid
cyklopentanoperhydrofenantren

Synteza Cholesterolu
Synteza Cholesterolu
Całkowita dzienna synteza cholesterol –
ok. 700mg/24 h
Zaleca się spożycie 300 mg/dzień
W wątrobie powstaje do 50%
endogennego cholesterolu, 10% w
jelitach. Wszystkie komórki jądrzaste są
zdolne do syntezy cholesterolu.
Enzymy syntezy znajdują się we frakcji
mikrosomalnej i cytosolowej komórki
cholestero
l
acetoacetylo-
CoA
+
acetylo-CoA
+
H
2
O
3-hydroksy-3-metylo-
glutarylo-CoA
(HMG-CoA
)
mewalonian
reduktaza
w cytosolu
(mikrosomy)
Enzym
rozszczepiający
w
mitochondriach
acetylo-CoA
acetooctan
2 x acetylo-CoA
syntaza
HMG-CoA
Cytozolowa tiolaza
NADPH
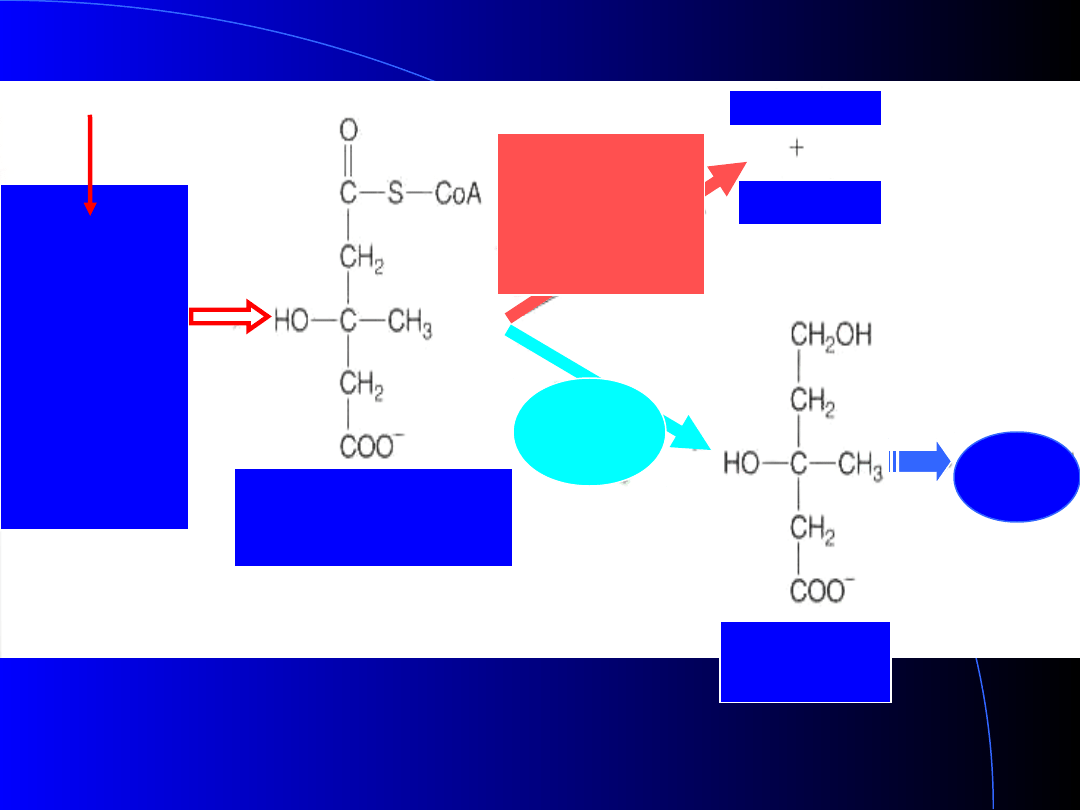
mewalonian 5-fosfomewalonian
5-pirofosfomewalonian
pirofosforan
izopentenylu
ATP
ATP
ATP
cholesterol
C6
C6
C6
C5
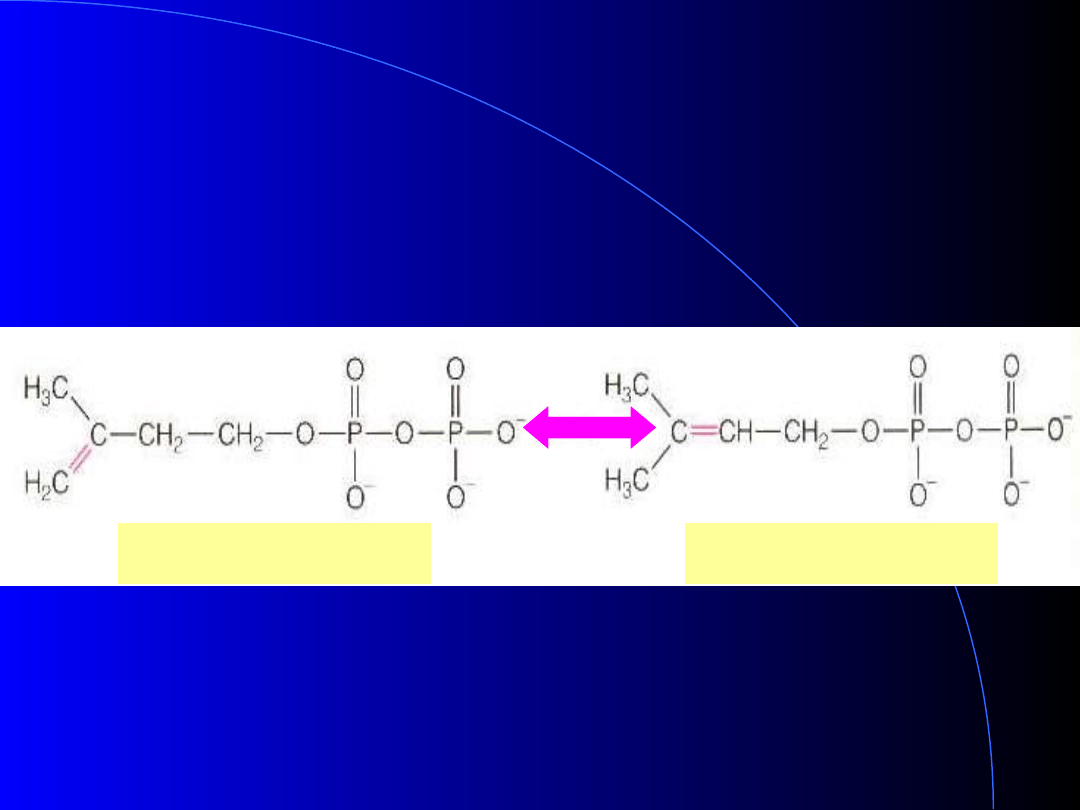
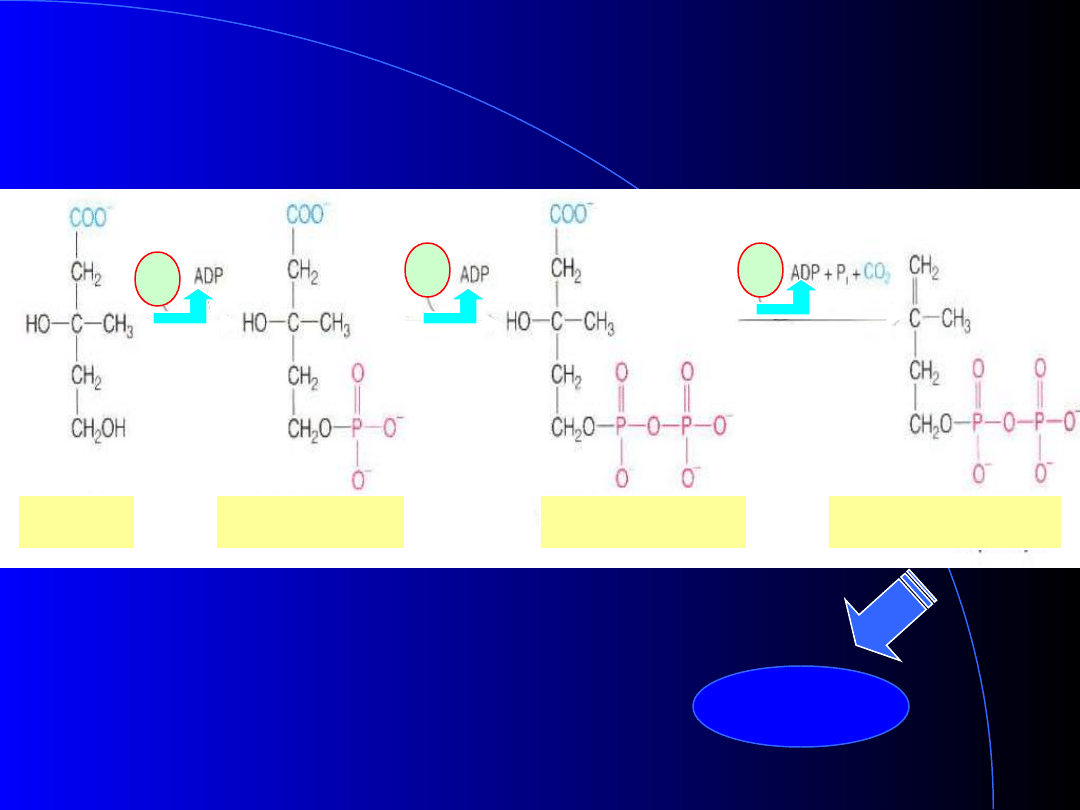
izomeryzacja
pirofosforan izopentenylu
dimetyloallilopirofosforan
C5
C5
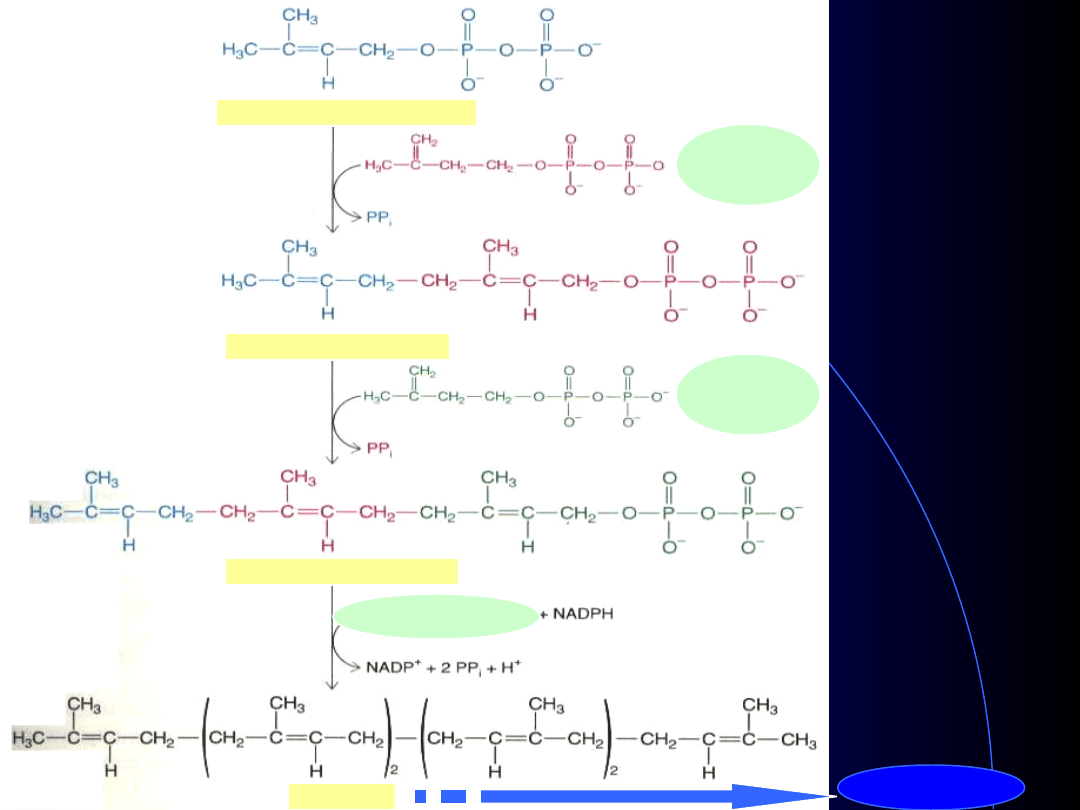
dimetyloallilopirofosforan
pirofosforan geranylu
pirofosforan farnezylu
skwalen
cholesterol
pirofosforan
izopentenylu
pirofosforan
izopentenylu
pirofosforan
farnezylu
C5
C5
C10
C5
C15
C15
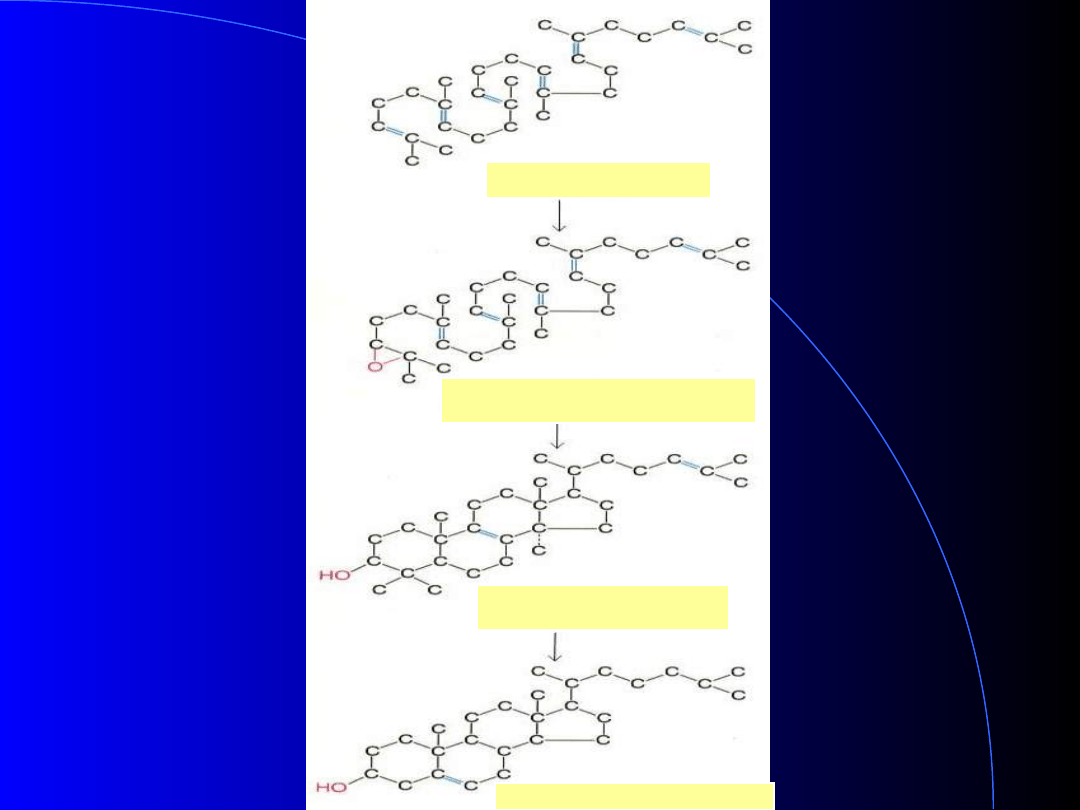
skwalen (30 at. C)
epoksyd skwalenu (30 at. C)
lanosterol (30 at. C)
cholesterol (27 at. C)
3
4
1
5
19
8
18
14
21
24
26
27
3
1
4
5
19
8
18
21
24
27
26
A
B
C
D
A
B
C
D
3CH
3
dolichol i
ubichinon

Regulacja syntezy cholesterolu
Regulacja syntezy cholesterolu
Kluczowy enzym - reduktaza HMG-CoA.
[1] hamowanie allosteryczne przez metaboliczne
pochodne
mewalonianu i cholesterolu
[2] hamowanie przez modyfikacje kowalencyjna –
fosforylacja zależna od glukagonu (kaskada z
udziałem
cAMP i kinazy białkowej A)
P-enzym – nieaktywny
[3] aktywacja przez uzależnioną od insuliny
defosforylację
(aktywny)
(fosfataza fosfobiałkowa);
insulina stymuluje ekspresję genu reduktazy
Statyny
Obniżają poziom cholesterolu we krwi przez hamowanie
syntezy
cholesterolu (kompetycyjny inhibitor reduktazy HMG-CoA).

Cholesterol
Cholesterol
Cholesterol NIE jest związkiem dostarczającym energii
Jest transportowany do wątroby i usuwany do żółci
–
55% jako cholesterol
–
45% jako
kwasy żółciowe
Kwas cholowy i chenodeoksycholowy (pierwotne
kwasy ż.) (synteza 0.5 g/dzień)
Skonjugowane z glicyną lub tauryną
– Kwas glikocholowy lub taurocholowy
synteza hormonów steroidowych
-
kora nadnerczy,
gonady
synteza witaminy D
3
– wątroba, nerka
Estry cholesterolu = forma magazynowania
cholesterolu w komórce, zasadnicza postać
przenoszenia cholesterolu w lipoproteinach.
COOH
OH
HO
OH
3
7
12
COOH
OH
HO
3
7
12
COOH
HO
3
7
12
COOH
HO
OH
3
7
12
CHOLIC ACID
CHENODEOXYCHOLIC ACID
7-dehydroxylation
7-hydroxylation
7-dehydroxylation
DEOXYCHOLIC ACID
LITHOCHOLIC ACID
PRIMARY BILE ACIDS
SECONDARY
BILE ACIDS
Kwasy żółciowe (C 24)
NADPH
Cyt P450
wątroba
Bakterie jelitowe
Bakterie jelitowe
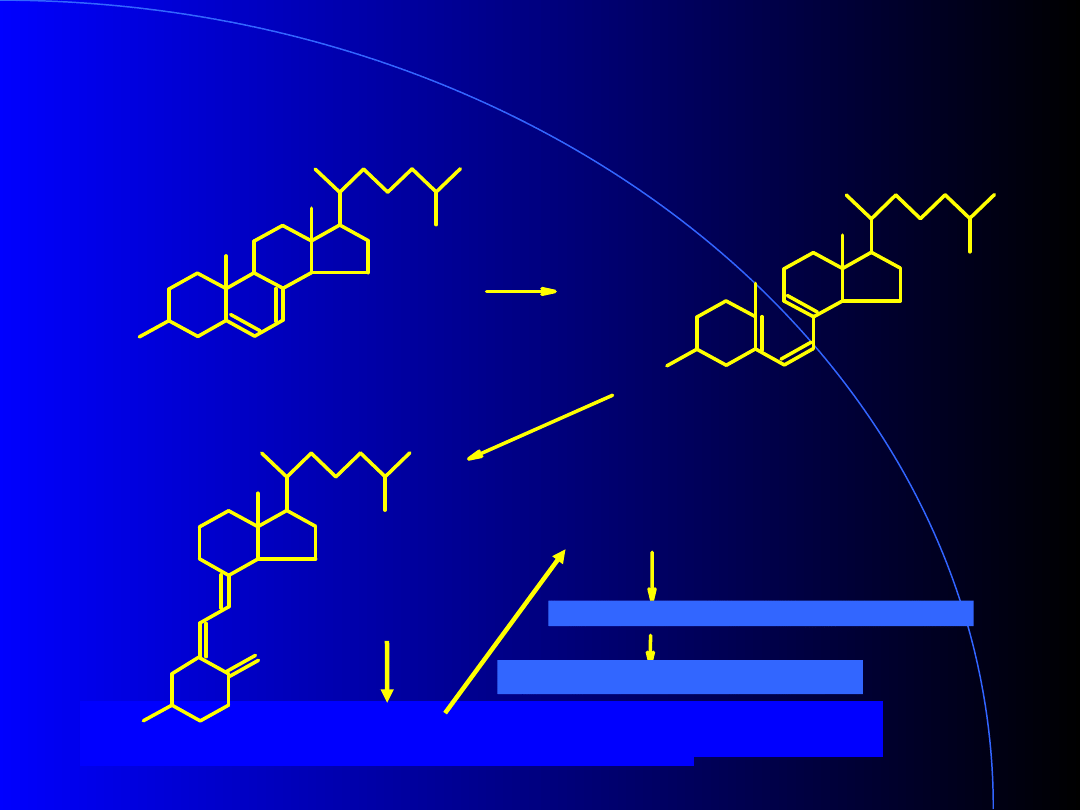
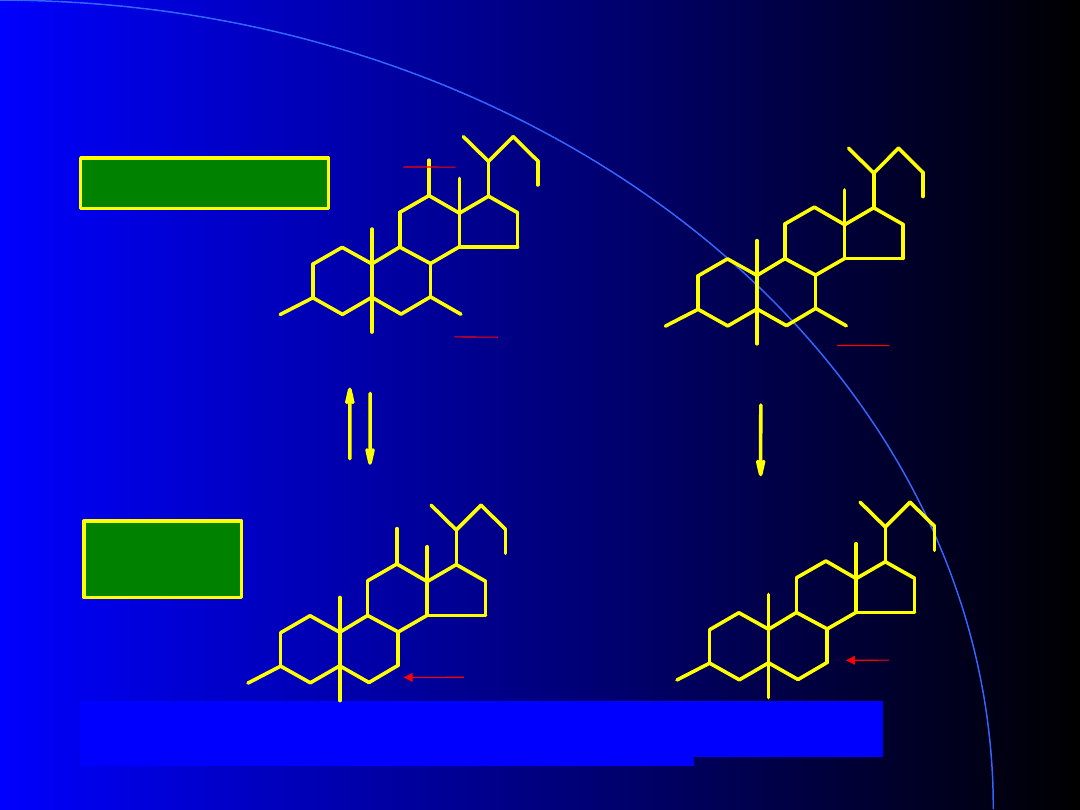
Previtamin D3
HO
HO
CH2
HO
UV
7-Dehydrocholesterol
Vitamin D3
(cholecarciferol)
Vit D3 + receptor
calcium binding protein mRNA transcription
absorption of calcium in the intestine
Cholesterol – prekursor witaminy D
3
1,25(OH)
2
cholekalciferol
Absorpcja Ca
+2
w jelicie
Transkrypcja mRNA- białka wiążącego Ca
+2
Hormony steroidowe
Hormony steroidowe
Cholesterol (C27)
Cholesterol (C27)
ACTH
ACTH
pregnenolon
pregnenolon
(C21)
(C21)
progestageny
progestageny
(C21)
(C21)
(progesteron -
(progesteron -
prekursor)
prekursor)
glikokortykosteroidy
glikokortykosteroidy
(C21)
(C21)
androgeny
androgeny
(C19)
(C19)
kortyzol
kortyzol
mineralokortykosteroidy
mineralokortykosteroidy
(C21)
(C21)
aldosteron
aldosteron
estrogeny
estrogeny
(C18)
(C18)
ACTH
ACTH
–
–
aktywacja cyklazy adenylanowej (cAMP ),
aktywacja cyklazy adenylanowej (cAMP ),
zwiększenie akt. PKA w tkance rdzenia akt.
zwiększenie akt. PKA w tkance rdzenia akt.
enzymu odcinającego łańcuch boczny, który
enzymu odcinającego łańcuch boczny, który
przekształca cholesterol do pregnenolonu.
przekształca cholesterol do pregnenolonu.
Zasadniczy efekt fizjologiczny ACTH to produkcja
Zasadniczy efekt fizjologiczny ACTH to produkcja
glikokortykosteroidów.
glikokortykosteroidów.
NADPH
Cyt. P450, O
2
eikozanoidy
prostanoidy
leukotrieny
prostaglandyny
prostacyklina
tromboksany
Eikozanoidy – pochodne arachidonianu C 20
Eikozanoidy – pochodne arachidonianu C 20
kwas arachidonowy
leukotrieny
PGG
2
prostaglandyna H
2
Prostacyklina
PGI
2
inne
tromboksan A
2
prostaglandyny F
2,
E
2
5-lipooksygenaza (LPO)
Aspiryna
(nieodwracalny inhibitor)
COX-1
Peroksydaza, GSH
COX-2 cyklooksygenaza
aspiryna (kwas acetylosalicylowy)
E-
Ser-OH
cyklooksygenaza (aktywna)
E-
Ser-O
-C-CH
3
O
cyklooksygenaza (nieaktywna)
Hamowanie COX przez kwas acetyloasalicylowy

Katabolizm Lipidów –
Katabolizm Lipidów –
mobilizacja zapasów tłuszczu
mobilizacja zapasów tłuszczu
i utlenianie KT
i utlenianie KT
Lipoliza
Transport KT
Pobieranie KT, aktywacja i utlenianie

Lipoliza
Lipoliza
Rozpad triacylogliceroli do glicerolu +
3 kwasów tłuszczowych (wolnych)
–
Lipaza hormono-wrażliwa w tkance
tłuszczowej
–
Lipaza lipoproteinowa w nabłonku naczyń
krwionośnych
Wolne kwasy tłuszczowe, zwane też
nie-zestryfikowanymi kwasami
tłuszczowymi (transport z albuminami)
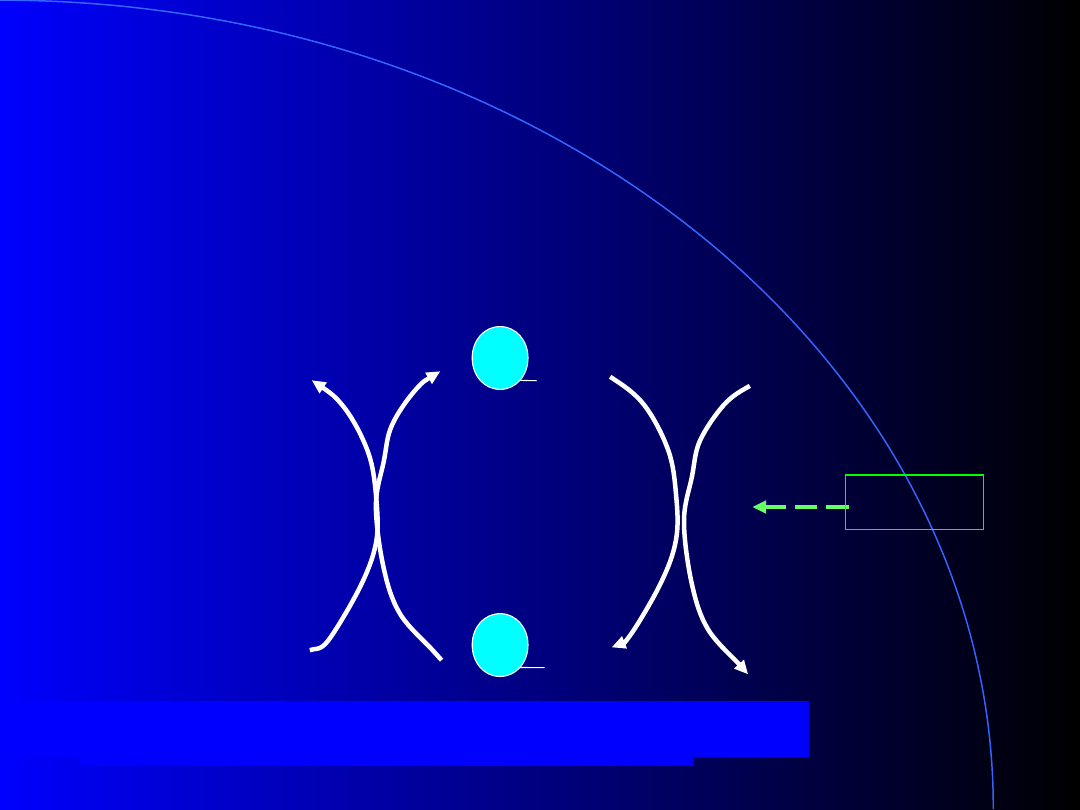
Aktywacja lipazy hormono-
wrażliwej
w tkance tłuszczowej
Lipaza hormono-wrażliwa
(nieaktywna
)
Lipaza hormono-wrażliwa
(aktywna)
OH
O-
P
ATP
ADP
+
cAMP
kinaza białkowa
P
i
H
2
O
fosfataza
Stymulowana
przez:
-niski poziom
insuliny
podczas
hypoglikemii
-glukagon
- ćwiczenia
sportowe
- stres
fizjologiczny
adrenalina

Katabolizm Lipidów –
Katabolizm Lipidów –
wykorzystanie
wykorzystanie
glicerolu
glicerolu
Glicerol
glicerol
3-P glicerol
fosforan
dihydroksyacetonu
kinaza
glycerolowa
ATP
ADP
NAD
+
NADH + H
+
glukoneogeneza
glikoliza
dehydrogenaza
3-P glycerolowa
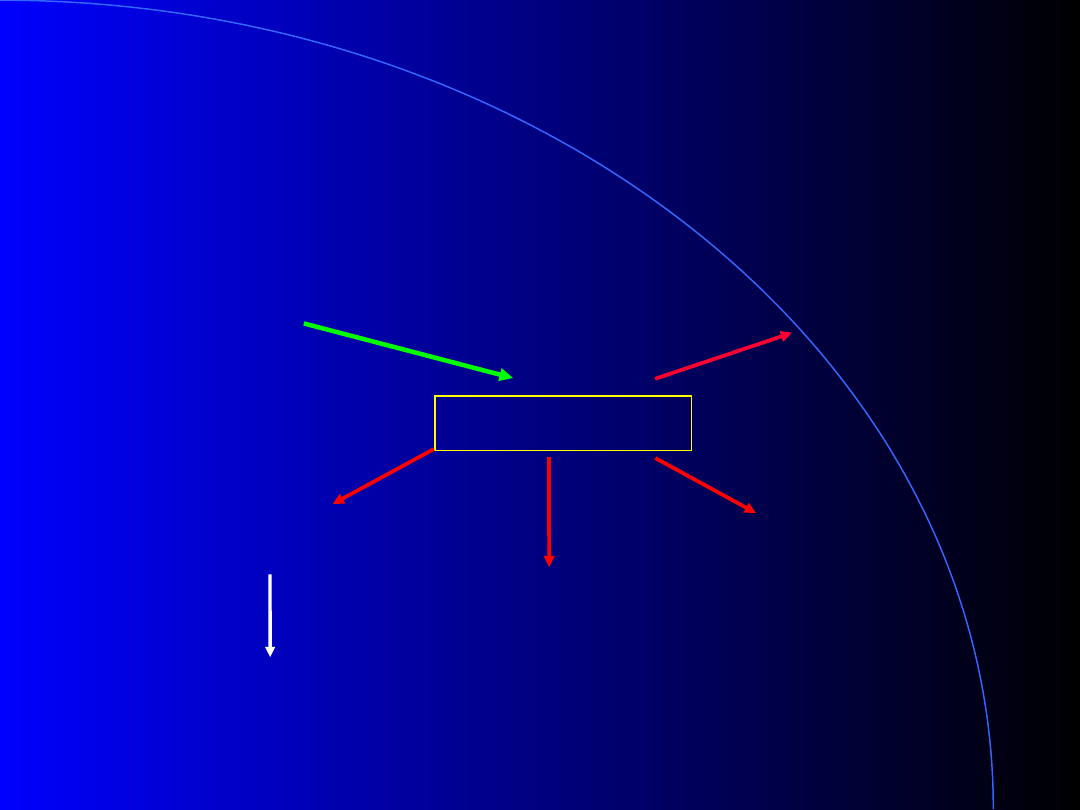
Wykorzystanie acetylo~CoA
Wykorzystanie acetylo~CoA
Acetylo~CoA
Cykl Krebsa
Synteza
kwasów
tłuszczowych
Ciała Ketonowe
Cholesterol
KT, glukoza, aminokwasy
ATP

Ketony
Ketony
β-oksydacja prowadzi do produkcji
znacznych ilości acetylo~CoA
Jeśli brakuje szczawiooctanu, wtedy
acetylo~CoA nie przechodzi przez
cykl Krebsa i jest przekształcany do
ciał ketonowych
–
Niski poziom glikolizy prowadzi do
zmniejszonej produkcji szczawiooctanu

Ciała ketonowe – alternatywne
Ciała ketonowe – alternatywne
źródło energii dla tkanek
źródło energii dla tkanek
obwodowych
obwodowych
Acetooctan, β-hydroksymaślan,
aceton
Acetylo~CoA + acetylo~CoA = acetoacetylo~CoA
acetoacetylo~CoA + acetylo~CoA = HMG~CoA
HMG~CoA
acetooctan
Liaza HMGCoA
CO
2
aceton
NAD
+
β
-hydroksymaślan
NADH+H

Ciała ketonowe – alternatywne
Ciała ketonowe – alternatywne
źródło energii dla tkanek
źródło energii dla tkanek
obwodowych
obwodowych
W wątrobie acetooctan i β-hydroksymaślan
nie są
utleniane, lecz wędrują do tkanek obwodowych,
gdzie mogą być przekształcone z powrotem do
acetylo~CoA i utlenione via cykl Krebsa.
–
mózg, serce, mięśnie szkieletowe, nerki
β-hydroksymaślan acetooctan
bursztynylo~
CoA
bursztynian
acetoacetylo~
CoA
2 acetylo~CoA
tioforaza
NAD
+
NADH+H
+
X
X – dh. 3-hydroksymaślanu
(brak w wątrobie)
Ketoza
Ketoza
Występuje, gdy synteza ciał
ketonowych przewyższa
wykorzystanie
Choroba - ketoacidoza
–
Cukrzyca typu 1
(zależna od insuliny)
Insulina Glukagon
Lipoliza
Wolne kwasy tłuszczowe w osoczu
Wyrzut ciał ketonowych z wątroby
Ketoacidoza
ketonemia/ketonuria

Degradacja fosfolipidów
a. fosfolipazy
O
CH
2
- O
- C – R
1
O
R
2
- C – O -CH
CH
2
– O -
P - X
A
1
A
2
C
D
głównie
rośliny
Sok trzustkowy, tkanki
Uwalnia kw. arachidonowy.
Obecna w jadzie węży i
pszczół.
Jest hamowana przez gliko-
kortykoidy (kortyzol)
tkanki
Lizosomy wątroby
Uwalnia wtórne przekaźniki.
Patogenne bakterie produkują.
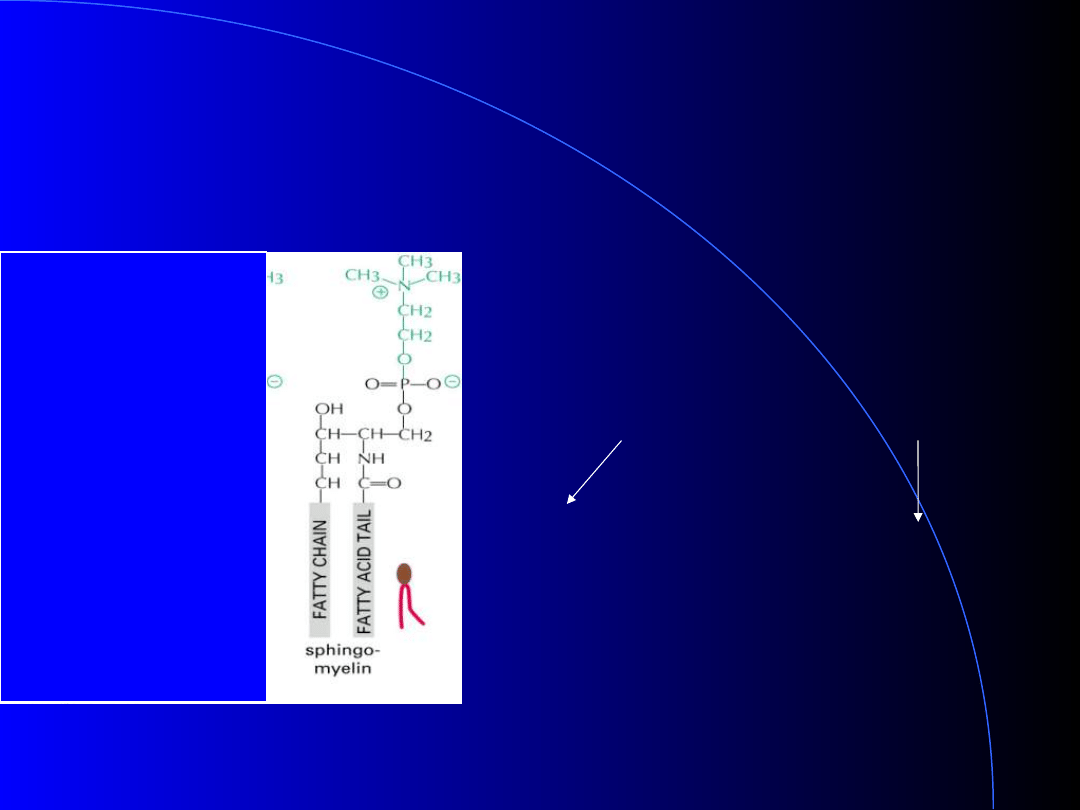
Degradacja sfingomieliny
b)
Sfingomielinaza
Enzym lizosomalny
Uwalnia P-cholinę
Zostaje ceramid -----
ceramidaza
Odpowiedź na stres
KT +
Sfingozyna - hamuje
kinazę białkowa C
Choroba Niemana-Picka – sfingomielina nie jest rozkładana. Brak
sfingomielinazy – rodzaj fosfolipazy C.

Transport niezestryfikowanych
Transport niezestryfikowanych
KT
KT
Krążą we krwi w połączeniu z
albuminami.
Transportowane są do tkanek, które
potrzebują energii.
Nie są wykorzystywane przez
erytrocyty (brak mitochondriów) oraz
przez mózg (brak przepuszczalności
przez barierię krew-mózg).

Krążenie tłuszczu obojętnego
i cholesterolu w organizmie
a) Pobieranie tłuszczu obojętnego z chylomikronów
do komórki
TAG
tkanka tłuszczowa – przechowanie
gruczoły mleczne – wydzielanie
mięśnie i inne tkanki – produkcja
energii
wątroba
Wolne kwasy tłuszczowe swobodnie przechodzą
przez błonę,
TAG nie, dlatego muszą być hydrolizowane w
naczyniach
włosowatych przez
lipazę lipoproteinową
(zewnętrzna strona komórek wyściełających
naczynia krwionośne, związana przez siarczan
heparanu)
do glicerolu i kwasów tłuszczowych.
LIPAZA LIPOPROTEINOWA

b) krążenie TAG i cholesterolu w organizmie
Wątroba jest głównym źródłem lipidów i cholesterolu krążących
we krwi w formie lipoprotein (poza chylomikronami).
Wątroba syntetyzuje TAG z glukozy i innych metabolitów,
poza tym dostaje ~ 10% zaabsorbowanego tłuszczu z diety
(remnanty chylomikronów).
Wątroba eksportuje TAG w postaci VLDL.
Wątroba - główny dostawca tłuszczu do mięśni i tkanki tłuszczowej
Wątroba – główne miejsce syntezy cholesterolu w organizmie.
Dostaje go również z diety via remnanty chylomikronów. Eksportuje
go w postaci VLDL, które są przekształcane w LDL.
Jest również
odwrotny kierunek
transportu cholesterolu
tkanki obwodowe
wątroba

Lipaza lipoproteinowa
Ściany naczyń włosowatych tkanki tłuszczowej, serca i
gruczołów
mlecznych mają dużo lipazy lipoproteinowej. Wątroba dorosłych
osób nie ma tego enzymu.
Ilość tego enzymu zależy od stanu fizjologicznego organizmu,
np. dużo insuliny/mało glukagonu wzrost ilości
lipazy lipoproteinowej
remnanty chylomikronów z całym cholesterolem
i jego estrami oraz ~ 10% wyjściowego TAG
pobierane są przez wątrobę (transport receptorowy –
endocytoza)

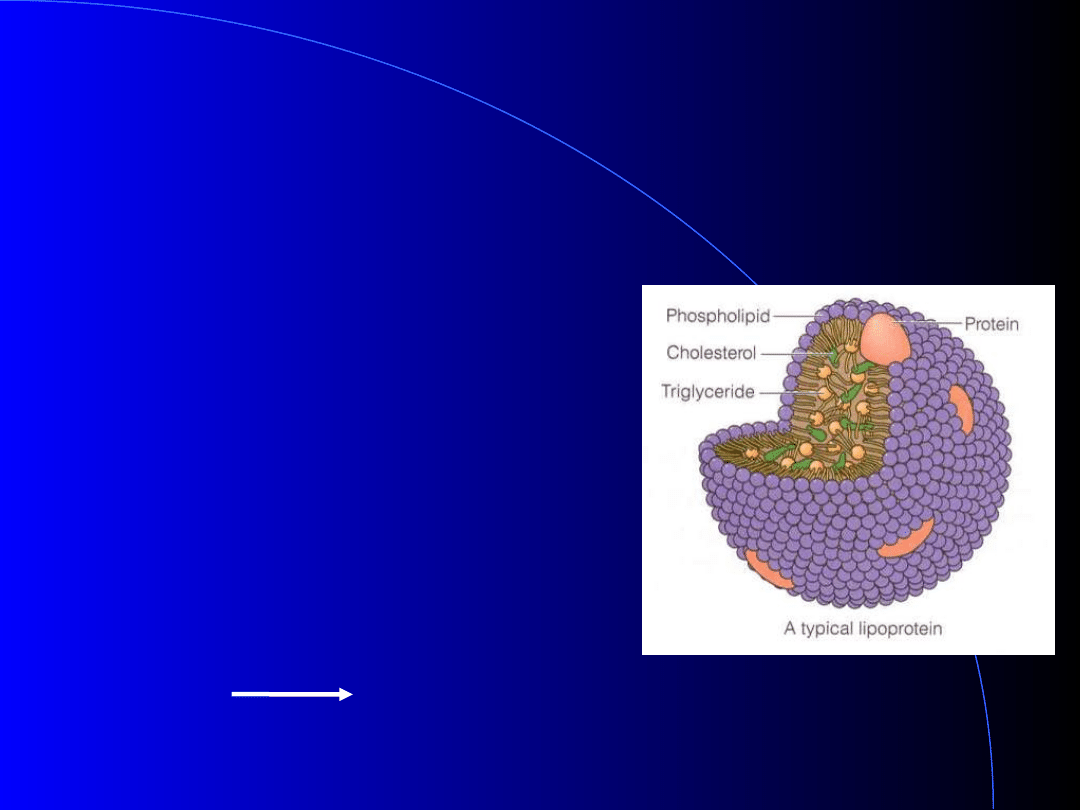
Skład Lipoprotein
Skład Lipoprotein
50
21
15
8
2
Białka
(%)
50
79
85
92
98
Lipidy
(%)
1.063-
1.21
1.019-
1.063
1.006-
1.019
<1.006
<1.006
Gęstość
(g/mL)
HDL
LDL
IDL
VLDL
Chylomikro
n

Apolipoproteiny
apoB
48
w chylomikronach
apoB
100
w VLDL, LDL
Rola: -
ukierunkowanie transportu
np. apoB
100
na LDL wiąże je do receptora LDL
apoE na remnantach chylomikronów wiąże je z wątrobą
-
aktywacja enzymów
np. apoCII na chylomikronach konieczna jest do
aktywacji lipazy lipoproteinowej
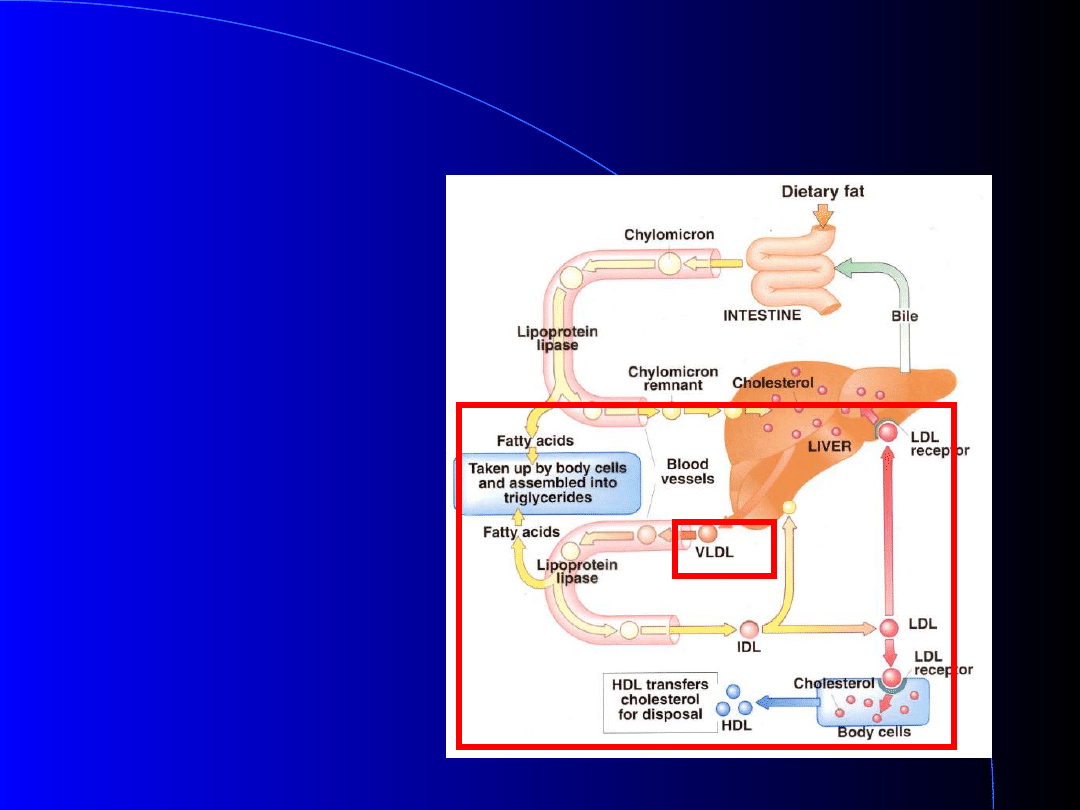
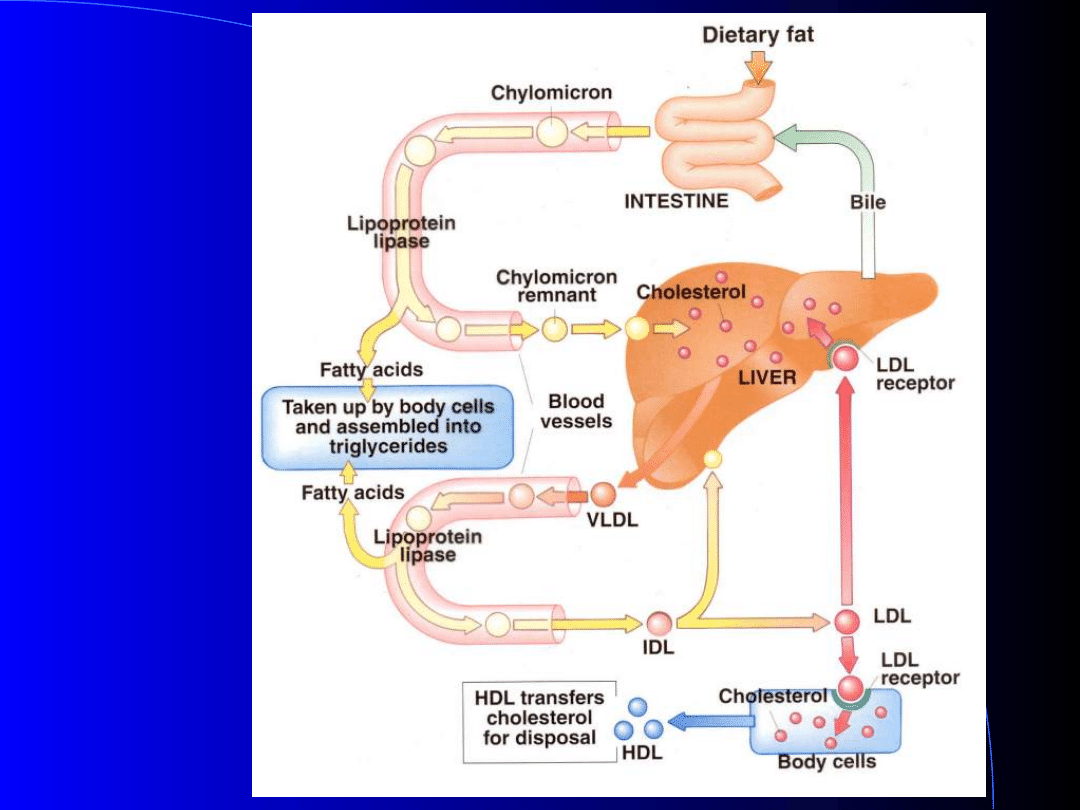
Synteza VLDL w wątrobie
VLDL dostarczają
lipidy do tkanek
obwodowych (TAG)

Zalecany poziom lipidów
Zalecany poziom lipidów
krwi
krwi
Całkowity cholesterol: <190 mg/dl
LDL cholesterol: 100-130 mg/dl optymalne
HDL cholesterol: małe u mężczyzn <40
mg/dl
małe u kobiet <46 mg/dl
Triglicerydy: >150 mg/dl (za wysokie)
Dane wg Europejskiego Towarzystwa Kardiologicznego

Lipoproteiny i ryzyko chorób UK
Lipoproteiny i ryzyko chorób UK
LDL – pozytywna korelacja
HDL - negatywna korelacja

Wpływ lipidów na lipoproteiny i
Wpływ lipidów na lipoproteiny i
ryzyko chorób układu krążenia
ryzyko chorób układu krążenia
Cholesterol w diecie
–
Brak efektu na cholesterol we krwi
Nasycone KT
–
Wzrost LDL
Kwasy Trans
–
Wzrost LDL i spadek HDL
Jedno-nienasycone KT
–
Spadek LDL
Omega-3 (n-3) wielonienasycone KT
–
Obniżenie cholesterolu we krwi

Wybrane choroby związane z
Wybrane choroby związane z
metabolizmem lipoprotein
metabolizmem lipoprotein
1. ABETALIPOPROTEINEMIA
1. ABETALIPOPROTEINEMIA
Brak białka B-48
Brak białka B-48
- brak
- brak
lipoprotein (LDL) w osoczu.
lipoprotein (LDL) w osoczu.
Nie są syntetyzowane VLDL i chylomikrony. Nagromadzenie tłuszczu
Nie są syntetyzowane VLDL i chylomikrony. Nagromadzenie tłuszczu
w komórkach endotelialnych jelita i w wątrobie. Osłabienie i degeneracja
w komórkach endotelialnych jelita i w wątrobie. Osłabienie i degeneracja
mięśni oraz nerwów
mięśni oraz nerwów
2. RODZINNY NIEDOBÓR
2. RODZINNY NIEDOBÓR
LIPOPROTEIN
LIPOPROTEIN
- CHOROBA WYSPY
- CHOROBA WYSPY
TANGIER
TANGIER
Brak białka A-I
Brak białka A-I
- nie powstają HDL, estry cholesterolu są odkładane
- nie powstają HDL, estry cholesterolu są odkładane
w komórkach układu siateczkowo-śródbłonkowego; pomarańczowy kolor
w komórkach układu siateczkowo-śródbłonkowego; pomarańczowy kolor
migdałków, powiększona wątroba i śledziona.
migdałków, powiększona wątroba i śledziona.
A.
HYPOLIPOPROTEINEMI
E

B. HYPERLIPOPROTEINEMIE
1. RODZINNY NIEDOBÓR LIPAZY LIPOPROTEINOWEJ (typ I)
1. RODZINNY NIEDOBÓR LIPAZY LIPOPROTEINOWEJ (typ I)
- 4 000 mg% lipidów we krwi, nienormalnie wysokie stężenie
- 4 000 mg% lipidów we krwi, nienormalnie wysokie stężenie
chylomikronów. Wysokie VLDL, niskie stężenie LDL i HDL
chylomikronów. Wysokie VLDL, niskie stężenie LDL i HDL
2. RODZINNA HIPERCHOLESTEROLEMIA (typ II)
2. RODZINNA HIPERCHOLESTEROLEMIA (typ II)
Brak receptorów LDL
Brak receptorów LDL
- stężenie cholesterolu we krwi dochodzi do 1000 mg%
- stężenie cholesterolu we krwi dochodzi do 1000 mg%
(przed 10-tym rokiem życia). Hiperbetalipoproteinemia
(przed 10-tym rokiem życia). Hiperbetalipoproteinemia
(LDL). Rozwój miażdżycy, udary i zawały serca.
(LDL). Rozwój miażdżycy, udary i zawały serca.
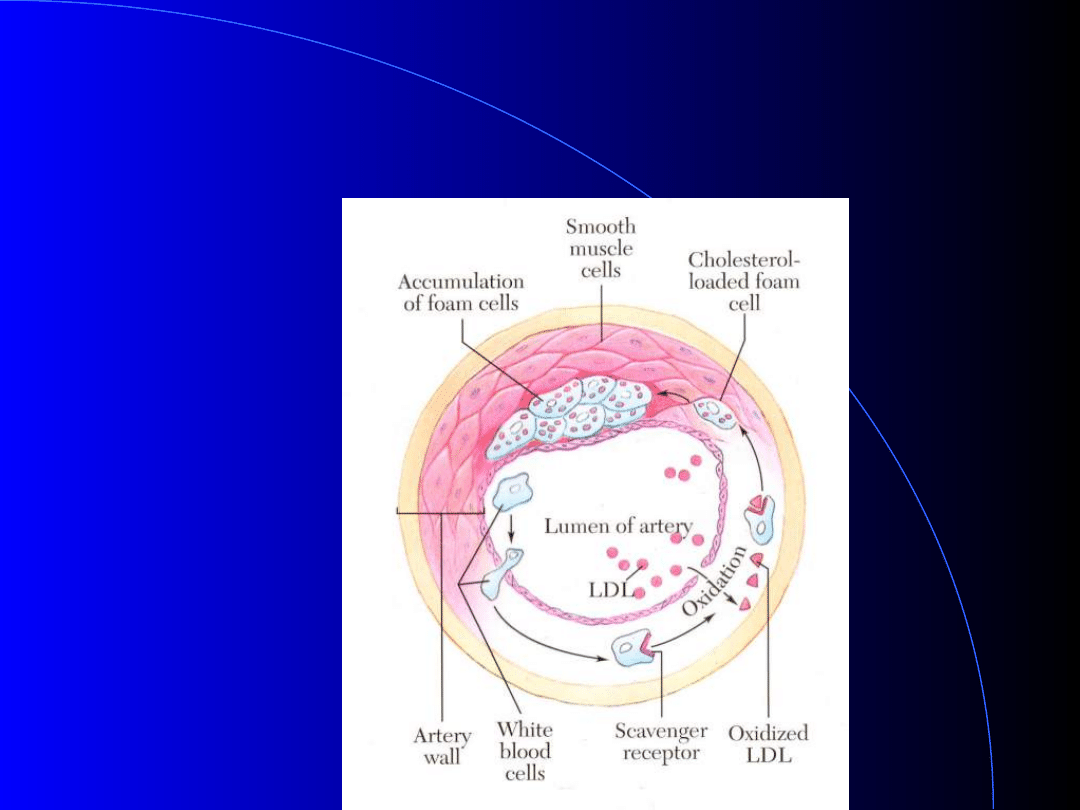
LDL i atherosclerosis
LDL i atherosclerosis
Document Outline
- Slide 1
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
Wyszukiwarka
Podobne podstrony:
Metabolizm lipidów (1)
IV metabolizm lipidow i sterydow
METABOLIZM LIPIDOW cz II RM
METABOLIZM LIPIDOW
Metabolizm lipidów 3
METABOLIZM LIPIDÓW cz I wykład RM
Metabolizm lipidów
METABOLIZM LIPIDÓW cz I RM
Metabolizm lipidów w komórkach nowotworowych
metabolizm lipidów
Metabolizm lipidów (1)
Metabolizm lipidów cz
07 Patofizjologia zaburzeń gospodarki lipidowej zespół metaboliczny
Uwarunkowania genetyczne zespołu metabolicznego i zaburzeń
więcej podobnych podstron