

•
amfetamina została zsyntezowana w 1887r. przez Edeleano,
•
jej właściwości opisano po raz pierwszy w 1927r.
•
jako lek została wprowadzona do użytku w 1932r. przez firmę Smith, Kline i French
•
w czasie II wojny światowej oraz wojny w Korei była stosowana jako środek stymulujący przez
żołnierzy amerykańskich w przypadku skrajnego wyczerpania walką
•
po wojnie w Japonii amfetamina była powszechnie dostępna w aptekach, co zaowocowało
uzależnieniem od niej znacznego procentu społeczeństwa
•
w ZSRR w czasach stalinowskich była podawana robotnikom w celu zintensyfikowania ich pracy
•
do końca lat 60. XX wieku była legalnym lekiem w USA który można było kupić w aptekach bez
recepty; stosowali je masowo kierowcy ciężarówek ale liczne wypadki śmierci z wyczerpania i
powodowane prze nich wypadki były przyczyną wycofania amfetaminy z legalnego obrotu
•
w latach sześćdziesiątych była popularnym lekiem stosowanym w terapiach odchudzających
•
jej popularność znacznie wzrosła w latach 80. XX wieku wśród młodych ludzi, głównie za sprawą
uczestników wielodniowych imprez

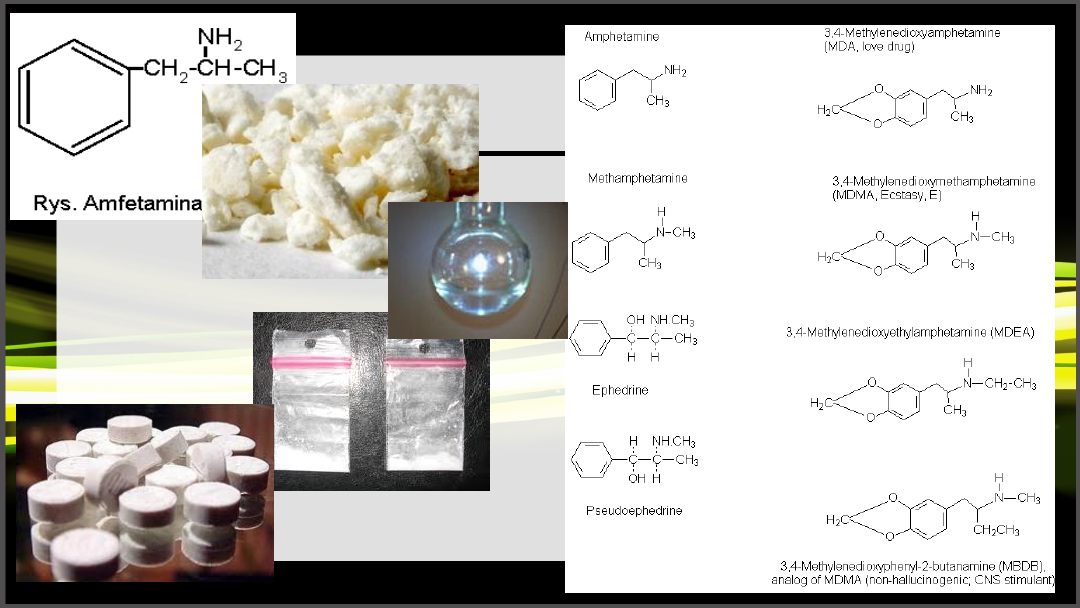
• amfetamina (d-N-α-dimetylofenyloetloamina) jest prototypem leków
psychostymulacyjnych
• stosowane są jej pochodne: metamfetamina, deksamfetamina
• zarówno amfetamina jak i jej pochodne są fenyloaminami
• amfetamina i jej pochodne będąc antagonistami receptorów
adrenergicznych w ośrodkowym i obwodowym układzie nerwowym,
powodują uwolnienie katecholamin i blokują wychwyt zwrotny dopaminy,
adrenaliny i noradrenaliny
• amfetamina ze względu na takie właściwości początkowo była stosowana
w leczeniu astmy i schizofrenii, później lista jej zastosowań wydłużyła się
o leczenie alkoholizmu, epilepsji, narkolepsji, hiperkinezy, choroby
Parkinsona, depresji, manii, migreny

• fenyloamina sympatykomimetyczna, strukturalnie podobna do
noradrenaliny i dopaminy
• amfetamina jest higroskopijną, bezbarwną cieczą o silnie
zasadowym odczynie
• w postaci wolnej zasady na gorąco matowi szkło sodowe oraz
niszczy gumę
• niezbyt przyjemny i charakterystyczny "mysi" zapach
• wolna zasada pozostawiona na ciele przez dłuższy czas powoduje
trudno gojące się oparzenia, połknięta uszkadza ścianę żołądka
powodując dotkliwy ból

• w celu zwiększenia trwałości przeprowadza się ją w sole amoniowe:
– siarczan diamfetaminy
– chlorowodorek amfetaminy,
– stosuje się również jednozasadowy fosforan amfetaminy lub winian
diamfetaminy
• wszystkie sole amfetaminy są białymi proszkami o gorzkim smaku
• sole rozpuszczają się w wodzie lepiej niż siarczan i nie są
higroskopijne
• amfetamina i jej pochodne to substancje lipofilne o okresie
półtrwania wynoszącym od 8 do 30 godzin

• zarówno amfetamina jaki i
metamfetamina mogą być podawane
wszystkimi możliwymi drogami:
– doustnie
– dożylnie
– palone
– wdychane przez nos

• w przypadku przyjęcia doustnego związki szybko się wchłaniają z przewodu
pokarmowego osiągając maksymalne stężenie po 1h.
• dostępność biologiczna palonej wynosi 90%
• maksymalne stężenie amfetaminy podanej w tych samych dawkach,
co metamfetamina jest znacznie mniejsze
• substancje te podlegają przemianom metabolicznym w wątrobie
• ich wydalanie zależy od pH moczu, kwaśny odczyn sprzyja usuwaniu
niezmienionej postaci leku (np. w warunkach normalnych w ciągu 24 godzin
w formie nie zmienionej wydalane jest około 30% przyjętej
dawki a przy kwaśnym pH moczu wartość ta wzrasta
do 74% natomiast przy zasadowym maleje do 1%)
• okres półtrwania wynosi od 10 do 30 godzin

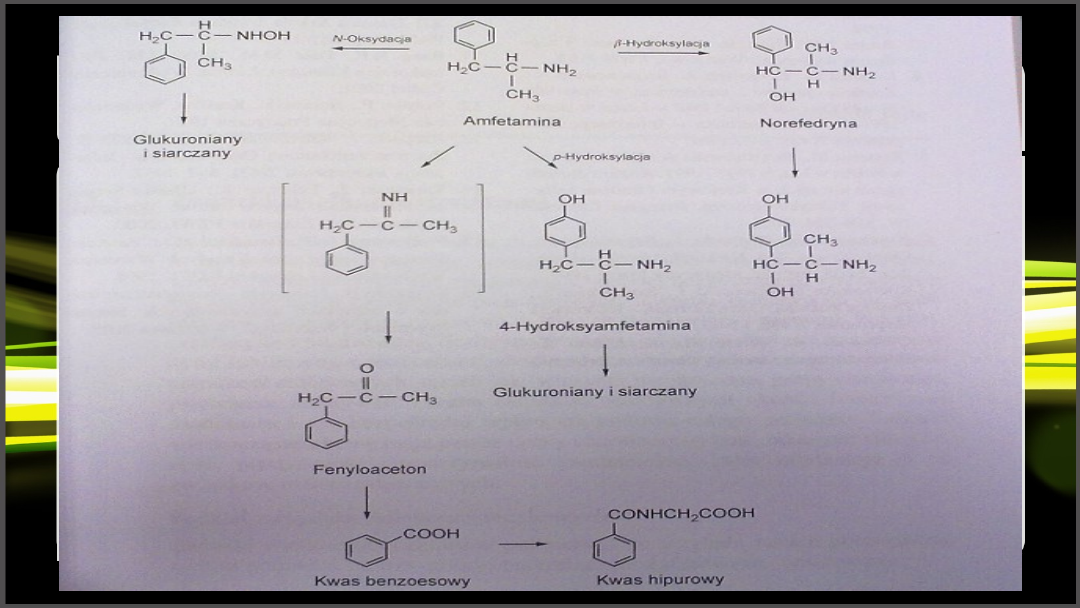
• przemiany metabiliczne amfetaminy i jej pochodnych zachodzą w
wątrobie
• główne drogi przemian to:
– hydroksylacja pierścienia aromatycznego do p-hydroksyamfetaminy i
norefedryny
– oksydatywna deaminacja do ketonu bezzylometylowego (fenyloacetonu),
który może ulegać dalszej degradacji do kwasu benzoesowego
– β-hydroksylacja łańcucha bocznego.
• metamfetamina ulega przemianie w wyniku procesu N-dmetylacji do
amfetaminy
• metabolity amfetaminy mogą byc wydalane w postaci wolnej lub
sprzężone z kwasem glukuranowym lub glukozą
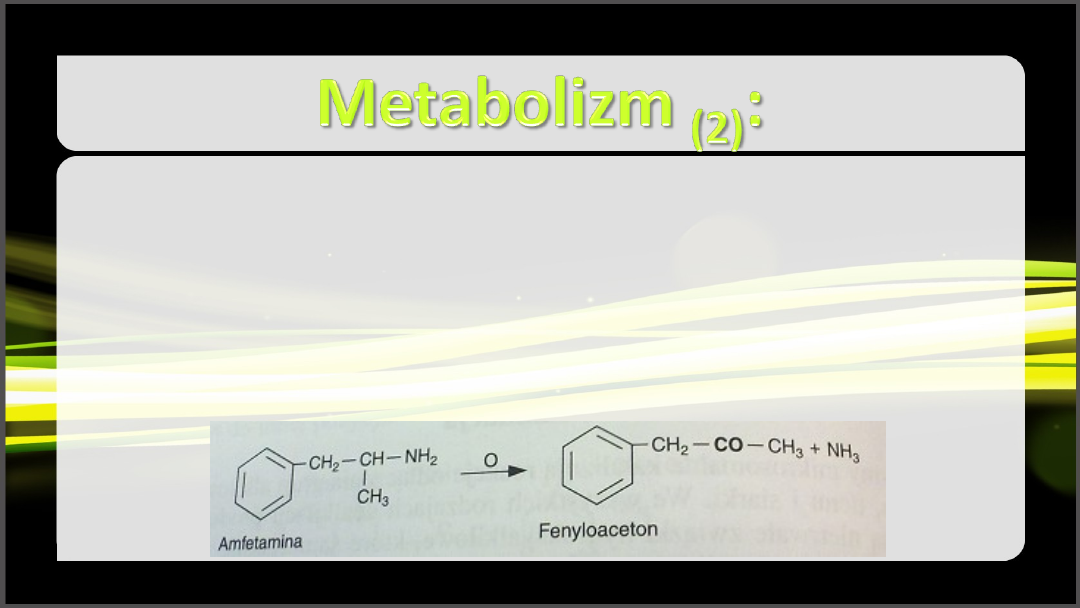
• najczęstszym szlakiem metabolizmu amfetaminy jest oksydatywna deaminacja
– zachodzi w siateczce sródplazmatyczenj pod wpływem oksydazy aminowej w
obecności NADPH i tlenu cząsteczkowego
– następuje utlenienie amin do ketonów
– niektóre aminy alifatyczne pod wpływem monoaminooksydazy i diaminooksydazy
ulegają deaminacji do odpowiednich aldehydów, alkoholi i ketonów
– fizjologiczna rola tych enzymów to przemiana amin endogennych (np. katecholamin)

• amfetaminy działają na neurony dopaminergiczne,
adrenergiczne i serotonergiczne w ośrodkowym i obwodowym
układzie nerwowym
• w OUN dotyczy to szczególnie dopaminy, a w układzie
obwodowym- adrenaliny
• powodują one zwiększenie przechodzenia neurotransmiterów
do przestrzeni synaptycznej oraz hamują ich wychwyt zwrotny
• wszystko to powoduje ze substancje te charakteryzują się
działaniem sympatykomimetycznym i powoduje silne
pobudzenie układu nerwowego, głównie OUN

• Stężenie w krwi w μg/cm
3
– Lecznicze > 0,03
– Toksyczne >0,5
– Śmiertelne > 1

• tachykardia
• ból w klatce piersiowej
• nadciśnienie tętnicze
• zagrażająca wyciu zapaść sercowo –
naczyniowa
• możliwe nieodwracalne uszkodzenie
drobnych naczyń mózgowych
prowadzące do udarów
• w ostrym przedawkowaniu występuje
nagła depresja OUN, która w ciągu paru
minut może zakończyć się zgonem
• ból glowy
• bezsenność
• nudności

• obraz kliniczny pozwalający na
zdiagnozowanie zatrucia amfetaminą i jej
pochodnymi
• objawy zatrucia obejmują następujące układy:
–
sercowo-naczyniowy
–
nerwowy
–
nerwowy współczulny
–
inne

• układ sercowo-naczyniowy:
– kołatanie serca
– tachykardia
– nadciśnienie
– encefalopatia nadciśnieniowa
– ból klatki piersiowej
– zaburzenia rytmu
– niedokrwienie serca
– skurcz naczyń

• układ nerwowy:
– ostra psychoza
– urojenia
– paranoja (może trwać kilka
dni)
– drgawki
– krwawienie śródczaszkowe
– skurcz naczyń
– bardzo wysoka gorączka
– euforia
– niepokój
– pobudzenie zagrażając życiu
– hiperrefleksja
– anoreksja
– zwiększone czuwanie i
koncentracja
– spadek zmęczenia

• współczulny układ nerwowy:
– rozszerzenie źrenic
– pocenie się
– nudności
– drżenia
– szybkie oddychanie
• inne objawy:
– rabdomioliza
– niedokrwienne zapalenie okrężnicy
– obrzęk płuc
– prężenia mięśni
– jeżenie się włosów
– retencja moczu

• związane są z przewlekłym stosowaniem amfetaminy u
narkomanów
• należą tu miedzy innymi:
– martwicze zapalenie naczyń, które może prowadzić do:
• niewydolności nerek
• zapalenia trzustki
• zawału mózgu
• krwawień i krwotoków
– kardiomiopatie:
• uszkodzenie serca
• zaburzenia rytmu
• niedokrwienie

– wzrost ryzyka:
• infekcji HIV i AIDS
• zapalenia wątroby
• zapalenia wsierdzia
• ropni płuc i tkanek miękkich
• zapalenia szpiku przy stosowaniu dożylnym
– psychoza amfetaminowa o charakterze majaczeniowo-urojeniowym
(omamy słuchowe i urojenia prześladowcze)
– długotrwałe stosowanie amfetaminy i metamfetaminy często
prowadzi do stanów przypominających objawy schizofrenii

• stężenie amfetaminy u osób zatrutych w surowic wynoszą 105-560ng/ml
• nieliczne badania wykazują, że stężenie w mleku karmiącej matki jest dużo
wyższe niż w osoczu
• w przypadku zatruć śmiertelnych stężenia metametaminy wynoszą: 0,05-
9,3μg/ml (a wartość medialna 0,42-1,84 μg/ml
• więcej metamfetaminy (2-krotnie) znajduje się w surowicy płodu niż
uzależnionej matki
• stężenia obu związków zarówno we krwi, jak i tkankach (wątroba, mięśnie) są
stabilne i nie ulegają zmianom nawet przez 2lata
• wyniki stężeń obu ksenobiotyków należy interpretować z dużą ostrożnością ze
względu na możliwość ich powstawania w wyniku metabolizmu wielu leków
(np. selegiliny, benzfetaminy, klobenzoreksu, deprenylu, fenetyliny,
fenylaminy i innych)

• podstawowym, przesiewowym badaniem są test
wykrywający obecność amfetaminy w moczu np.:
– AMFETAMINA TEST – test jakościowy o czułości 1000 ng/ml służący
do wykrywania obecności amfetaminy w ludzkim moczu; test
wykrywa amfetaminę w moczu badanej osoby do 3 dni od momentu
zażycia
– Testy Multi-drug - umożliwiają przy pomocy jednego badania
wykrycie i identyfikację narkotyków z 10 różnych grup jednocześnie
(amfetamina, barbituraty, benzodiazepiny,
kokaina, metamfetamina, opiaty,
MDMA(Ecstasy), fencyklidyny - PCP,
trójcykliczne antydepresanty oraz marihuana - THC)

• wykonanie testu z moczu:
– oznaczenie powinno być wykonane z próbki świeżego moczu.
– przed przystąpieniem do wykonania testu upewnić się, że płytka w foliowym
opakowaniu ma temperaturę pokojową (20 - 30°C).
– wyjąć płytkę testową z foliowego opakowania.
– pobrać próbkę moczu przy pomocy jednorazowej pipetki i wkroplić powoli 4 krople do
okrągłego okienka na płytce testowej; podczas nakrapiania moczu pipetkę należy cały
czas trzymać w pozycji pionowej, w odległości ok. 1 cm od powierzchni płytki tak, aby
umożliwić wytworzenie się pełnych kropli, bez pęcherzyków powietrza; za duża lub za
mała objętość próbki ma wpływ na poprawne wykonanie testu
– odczytać wynik po czasie 3 do 8 minut od momentu nakropienia próbki moczu na
płytkę testową
– UWAGA: Nie należy brać pod uwagę wyniku otrzymanego po czasie dłuższym niż 8
minut; z upływem czasu intensywność barwy prążków na płytce testowej może ulec
zmianie lub może pojawić się nowy prążek
• interpretacja wyników z moczu – wynik negatywny
Pojawiają się dwa barwne prążki: w strefie testowej T i kontrolnej C (intensywność
barwy prążka testowego może być słabsza lub mocniejsza niż prążka
kontrolnego). W badanym moczu nie stwierdza się obecności narkotyku.
UWAGA: Nie należy sugerować się intensywnością barwy prążka w strefie testowej
T.

• interpretacja wyników z moczu – wynik pozytywny
Pojawia się tylko jeden barwny prążek: w strefie kontrolnej C. Brak barwnego
prążka w strefie testowej T.
W badanym moczu stwierdza się obecność narkotyku.

•
w ocenie laboratoryjnej zatruć amfetaminą i metamfetaminą należy mieć na uwadze reakcje
krzyżowe z innymi substancjami w badaniach przesiewowych moczu, należy je potwierdzić
metodami czulszymi
•
materiałem do badan (poza moczem) może być również:
–
krew
–
włosy
–
paznokcie
–
materiał pośmiertny
•
amfetamina i jej pochodne są wykrywalne w moczy po 2-4 dniach od zażycia a
stężenia
tych związków zarówno we krwi, jak i tkankach (wątroba, mięśnie) są stabilne i nie
ulegają zmianom nawet do 2 lat
•
substancje które mogą dawać reakcję krzyżową to np.:
–
efedryna
–
fentermina
–
MDMA
–
prokainamidy

•
metody oznaczania amfetaminy i jej metabolitów:
–
radioimmunologiczne(RIA)
–
imimmoenzymatyczne(EIA)
–
immunofluorescencyjne w świetle spolaryzowanym (FPIA)
–
TLC - wynik badania nie może stanowić dowodu obecności narkotyku
–
GC
–
HPLC
–
GC/MS - jest najbardziej czułą i specyficzną metodą potwierdzania obecności narkotyku w
próbce
oparte na
hamowaniu
aglutynacji
lateksowej
odznaczają się wysoką czułością i specyficznością, mogą więc służyć do
potwierdzania przypuszczalnie dodatnich wyników prób skrinignowych.

• dodatkowe badania wykonuje się w zależności od stanu klinicznego
pacjęta
– elektrolity
– równowaga kwasowo-zasadowa
– gazometria krwi tętniczej
– CPK
– stężenie acetoaminofenu (który może być przyjmowany razem z amfetaminą)
– EKG
• uniesienie lub obniżenie załamka ST w celu wykluczenia niedokrwienia czy zawału
• należy wykluczyć zażycie innych substancji jak np. poszerzenie odcinka QRS w zatruciu
trójpierścieniowymi lekami przeciwdepresyjnymi
– tomografia komputerowa głowy u pacjentów z bólami głowy, zaburzeniami
neurologicznymi czy drgawkami
– zdjęcie RTG klatki piersiowej

•
przygotowanie próbki : ekstrakcja ciecz – ciecz:
–
polega zwykle na hydrolizie moczu, jego ekstrakcji i oczyszczaniu oznaczonego składnika;
postępowanie powinno dawać wysoki odzysk, niezbędny do uzyskania w ekstrakcie ilości
substancji wystarczającej do dalszego badania
–
w przypadku analizy amfetaminy i jej analogów hydroliza nie jest potrzebna; ekstrakcje z moczu
można prowadzić za pomocą rozpuszczalników organicznych (np. chlorku metylenu) lub
specjalnych kolumienek ekstrakcyjnych
–
ekstrakcję przy pomocy rozpuszczalników organicznych przeprowadzą się w środowisku
alkalicznym, gdy grupa aminowa jest wolna; wartość pH dla amfetaminy wynosi 9,9 a dla
metamfetaminy 10,1 natomiast pH do którego należy doprowadzić mocz, aby odzysk był
optymalny, wynosi 11
–
postępowanie z próbką opisane przez Hornbecka i Czarnego:
• do probówki na 50 ml odpipetowuje się 2 ml moczu i dodaje kolejno: 2 ml 1 M roztworu wodorotlenku
sodowego, 5 ml wody i 20 ml chlorku metylenu (dichlorometanu)
• zamkniętą próbówkę wytrząsa się, wiruje przy małej szybkości przez 5 minut i odrzuca górną
warstwę
• pozostałość odparowuje się do sucha w strumieniu azotu, rozpuszcza w niewielkiej ilości metanolu i
nanosi na płytkę chromatograficzną

•
przygotowanie próbki: ekstrakcja w fazie stałej (Solid Phase Extraction - SPE)
–
przy użyciu przygotowywanych fabrycznie kolumienek ekstrakcyjnych, ma szereg zalet (oszczędność
czasu, małe objętości zużywanych odczynników oraz unikniecie kłopotów związanych z powstawaniem
emulsji, co zdarza się często przy ekstrakcji ciecz-ciecz ); mankamentem jest jednak dość wysoka cena
kolumienek
–
wypełnienie kolumienek stanowi kizelgur (diatomaceous earth) lub krzemionka zawierająca grupy nie
polarne (octadecyl silica), kationowymienne lub z podstawnikami mieszanymi (nie polarnymi i
jonowymiennymi)
–
postępowanie z kolumienką wypełnioną silnym kationitem
• Kolumienkę o pojemności 1 ml przemywa się pod próżnią metanolem (2 ml), wodą ( 1 ml) i kwasem
fosforowym (0,5 ml, 10 mM)
• mocz (1 ml) i kwas fosforowy (0,5 ml, 10 mM) miesza się starannie w probówce i wlewa do kolumienki
• kolumienkę suszy się powietrzem przez około 30 sekund i płucze kolejno kwasem fosforowym (1 ml, 10
mM), kwasem octowym (0,5 ml, 0,1 mM) i metanolem (1 ml)
• po powtórnym wysuszeniu kolumienki (powietrze, 30 sek.) aminy eluuje się 2 ml metanolu z dodatkiem
stężonego roztworu amoniaku (3% v/v)
• ekstrakt odparowuje się do sucha pod próżnią lub w strumieniu azotu
• suchą pozostałość, po rozpuszczeniu w niewielkiej ilości metanolu, nanosi się na płytkę chromatograficzną.

• rozwijanie chromatogramu:
– normalny układ faz
• na żelu: silica-gel 60 F254s
• układ rozwijający: mieszanina toluenu, acetonu, 94% etanolu i 25% NH.OH
w stosunku 45:45:7:3 v/v
– odwrócony układ faz (Reversed Phase - RP)
• na żelu: RP-18 F254s
• układ rozwijający: mieszanina metanolu, wody i 37% HC1 w stosunku
50:50:1 (v/v)
– ponieważ w fazie normalnej i odwróconej działają różne mechanizmy rozdzielcze,
możliwości identyfikacyjne metody z jednoczesnym użyciem obu faz są większe
niż przy zastosowaniu dwóch układów normalnych

•
wykrywanie plam:
–
Przed przystąpieniem do wywoływania plam, płytki należy wysuszyć w temperaturze pokojowej, w piecu o
temperaturze 120"C, lub przy użyciu gorącego powietrza
–
dla prawidłowej barwy plam ważne jest usuniecie z płytki śladów amoniaku
–
do wywoływania stosuje się 0,5% roztwór Fast Black K (FBK), który daje z amfetaminą i jej analogami plamy
o zróżnicowanym zabarwieniu; FBK reaguje ponadto z fenolami, aryloaminami i niektórymi związkami
heterocyklicznymi
–
barwy plam amfetaminy i jej analogów strukturalnych po wywołaniu -FBK można podzielić na 2 grupy
• czerwona i czerwonopomarańczowa, które dają alifatyczne i aromatyczne aminy II-rzędowe
• fioletowa i fioletowoniebieska, charakterystyczne dla alifatycznych i aromatycznych amin I-rzędowych
(tabelka)
• w zależności od rodzaju związku i warunków wywoływania aminy I-rzędowe mogą dawać także barwę
czerwonofioletową lub nawet czerwoną
• aminy III-rzędowe, np. imipramina, w zasadzie nie reagują z FBK.
–
do wywoływania amfetaminy i jej analogów można również użyć 10% roztwór ninhydryny w etanolu, którym
spryskuje się płytkę i ogrzewa ją w piecu przy 120
o
C przez przynajmniej 15 min; amfetamina i inne aminy I-
rzędowe dają zabarwienie fioletowe i różowe, a II-rzędowe, np. metamfetamina - plamy bardziej intensywne

•
tabelka przedstawia ruchliwość chromatograficzna i
zabarwienie z FBK amfetaminy i jej strukturalnych
analogów
•
objaśnienia do tabelki:
–
FBK = Fast Black K Salt
–
hRf = (droga przebyta przez cząsteczke narkotyku) / (droga
przebyta przez czoło fazy ruchomej) x 100 (wartości A
5
, B
6
, C
7
,
D
8
)
–
F = barwa fioletowa lub fioletowoniebieska
–
C = barwa czerwona lub czerwonopomarańczowa
–
układ A: Toluen 45 -aceton 45 -94% etanol 7 -25% NR - 3 (Płytki:
silica-gel F,")
–
układ B: Metanol 100 - 25% NH, 1,5 (Płytki: silica-gel 60 F:54 )
–
układ C: Octan etylu 85 - metanol l O - 25% N H, 3 (Płytki: silica-
gel 60 F254)
–
układ D: Metanol 50 - woda 50 - 35% HCL l (Płytki: RP - 18 F,Ms).

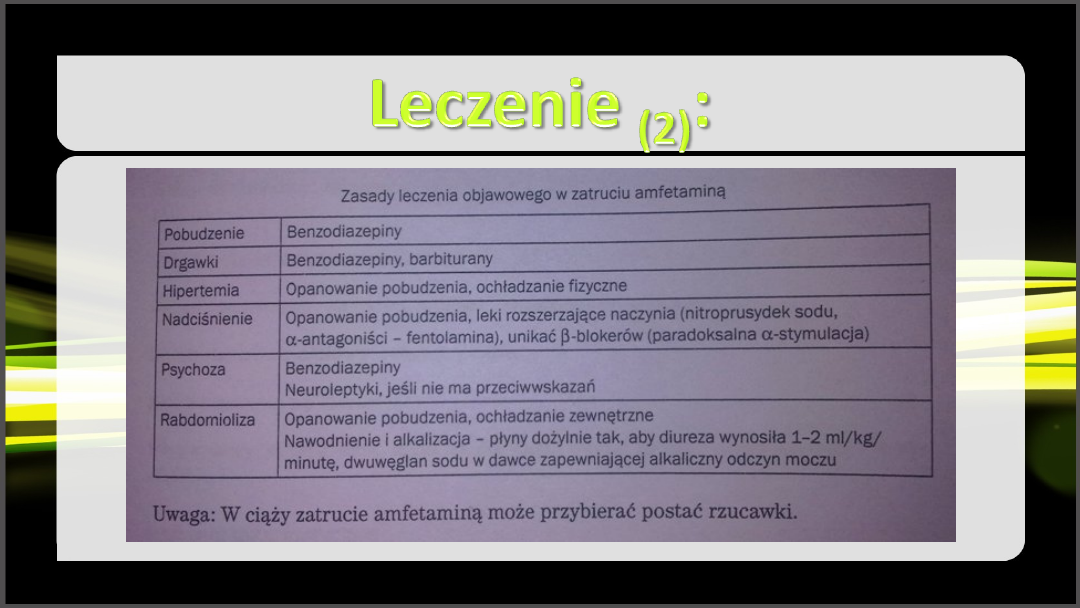
• w zatruciu amfetaminą stosuje się leczenia objawowe, nie
ma specyficznych odtrutek
• w zatruciu doustnym celowe jest wykonanie prowokacji
wymiotów lub płukanie żołądka, a następnie podanie węgla
aktywowanego
• w celu przyspieszenia wydalanie amfetaminy z organizmu
można stosowa wymuszoną diurezę po uprzednim
zakwaszeniu moczu chlorkiem amonowym
• w bardzo ciężkich zatruciach należy zastosować
hemoperfuzję przez kolumny z węglem aktywowanym

• zgodnie z Ustawą o przeciwdziałaniu narkomanii:
– zgodnie z podziałem substancji psychotropowych, określonym przez załącznik nr
2 do ustawy na grupy I-P, II-P, III-P i IV-P amfetamina należy do grupy II-P
– środki odurzające grup I-N i II-N oraz substancje psychotropowe grup II-P, III-P i
IV-P mogą być używane wyłącznie w celach medycznych, przemysłowych lub
prowadzenia badań
– środki odurzające grup I-N, II-N i IV-N, substancje psychotropowe grup I-P, IIP, III-
P i IV-P lub prekursory kategorii 1 może wytwarzać, przetwarzać lub przerabiać,
w celu prowadzenia badań naukowych, wyłącznie jednostka naukowa, w zakresie
swojej działalności statutowej, po
uzyskaniu zezwolenia Głównego
Inspektora Farmaceutycznego określającego
środki lub substancje, które mogą być przedmiotem
wytwarzania, przetwarzania lub przerobu.

– preparaty zawierające środki odurzające grup I-N, II-N i III-N lub substancje
psychotropowe grup II-P, III-P i IV-P, które zostały dopuszczone do obrotu jako
produkty lecznicze na podstawie przepisów prawa farmaceutycznego, może
posiadać, w celach medycznych, po uzyskaniu zgody wojewódzkiego
inspektora farmaceutycznego, zakład opieki zdrowotnej niemający apteki
szpitalnej, zakład leczniczy dla zwierząt oraz lekarz,
lekarz dentysta lub lekarz weterynarii, prowadzący
praktykę lekarską, a także inny podmiot,
którego działalność wymaga
posiadania i stosowania tych
preparatów

•
Toksykologia współczesna, pod red. Witolda Seńczuka, wyd. PWZL, s.106, 319-320.
•
Ostre zatrucia, Lech Panasiuk, Elżbieta Szponar, Jarosław Szponar, wyd. PWZL, Warszawa
2010, s. 137-139.
•
Toksykologia wybrane zagadnienia, pod red. Jerzego Brandysa, Wyd. Uniwersytetu
Jagiellońskiego, Kraków 1999, s. 154-166.
•
Toksykologia kliniczna, pod red. Tadeusza Bogdanika, wyd. PWZL, Warszawa 1988, s. 277-
278.
•
Podstawy toksykologii – kompendium dla studentów szkół wyższych, pod red. Jerzego K.
Piotrowskiego, Wyd. Naukowo – Techniczne, Warszawa 2006, 2008, s.385-388, 400-401.
•
Vademecum zatruć, Robert H. Dreisbach, wyd PWZL, Warszawa 1995, s.370-374.
•
Zarys toksykologii klinicznej, pod red. Janusza Pacha, Wyd. Uniwersytetu Jagiellońskiego,
Kraków 2009, s. 409-412.
•
źródło internetowe: http://www.transactor.pl/dok/testymoczu.pdf
•
źródło internetowe:
http://talk.hyperreal.info/
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
Wyszukiwarka
Podobne podstrony:
Amfetamina i jej pochodne(2)
Amfetamina i jej pochodne
Amfetamina i jej pochodne(1) ppt
Amfetamina i jej pochodne(2)
Rola witaminy C i jej pochodnych w metabolizmie skóry
Rola witaminy C i jej pochodnych w metabolizmie skór2
Rola witaminy C i jej pochodnych w metabolizmie skóry część II
23 PRZETACZANIE KRWI I JEJ POCHODNYCH
Rola witaminy C i jej pochodnych w metabolizmie skór1
Rola witaminy C i jej pochodnych w metabolizmie skóry
Amantadyna i jej pochodne leki o wielu możliwościach
6 Pochodna i jej zastosowanie
Opcje i instrumenty pochodne (26 stron), Opcja jest to umowa dająca jej posiadaczowi prawo do wykona
1 Filozofia â pochodzenie nazwy od czego się zaczyna jakie są jej przesłanki
12. Definicja pochodnej funkcji jednej zmiennej w punkcie i przykład jej interpretacji, Studia, Seme
Teksty, Syro-palestyna, Nazwa Palestyna pochodzi od ludu Filistynów, którzy osiedlili się na jej wyb
więcej podobnych podstron