
Zestawienie skrótów
Zestawienie skrótów
ACE - konwertaza angiotensyny
ASA - kwas acetylosalicylowy
AV - przedsionkowo-komorowy
BMI - wskaźnik masy ciała
CABG (coronary artery bypass graft) - pomostowanie tętnic wieńcowych
ChW - choroba wieńcowa
HDCz - heparyna drobnocząsteczkowa
HDL-C - cholesterol frakcji HDL
HNF - heparyna niefrakcjonowana
ICD (implantable cardioverter-defibrillator) - wszczepiany kardiowerter-
defibrylator
LBBB (left bundle-branch block) - blok lewej odnogi pęczka Hisa
LDL-C - cholesterol frakcji LDL
LVEF (left ventricular ejection fraction) - frakcja wyrzutowa lewej komory
nie-HDL-C - cholesterol nie-HDL
NSLPZ - niesteroidowe leki przeciwzapalne
OIOK - oddział intensywnej opieki kardiologicznej
PCI (percutaneous coronary intervention) - przezskórna interwencja
wieńcowa
SaO2 - wysycenie tlenem hemoglobiny krwi tętniczej
STEMI (ST-elevation myocardial infarction) - świeży zawał serca z
uniesieniem ST

Naczynia wieńcowe serca
Serce człowieka unaczynione jest przez tętnice wieńcowe.
Wyróżniamy dwie główne tętnice wieńcowe, które odchodzą
od aorty wstępującej w tzw. zatokach aorty (Valsalvy). Jest to
lewa i prawa tętnica wieńcowa.
Tętnice wieńcowe zaopatrują wyłącznie ścianę serca
(dodatkowo oddają drobne gałązki do aorty i pnia płucnego).
W przypadku gdy światło jednego z naczyń wieńcowych
zostanie zamknięte (np. w wyniku pęknięcia blaszki
miażdżycowej) dochodzi do zawału mięśnia sercowego w
obszarze unaczynionym przez dane naczynie.

Naczynia wieńcowe serca
Początkowo prawa i lewa tętnica wieńcowa biegną razem w
obrębie tzw. bruzdy wieńcowej. W dalszym przebiegu lewa
tętnica wieńcowa układa się w bruździe międzykomorowej
przedniej a prawa w bruździe międzykomorowej tylnej.
Tętnice wieńcowe układają się na powierzchni serca wężowato,
dzięki czemu praca serca (skurcz i rozkurcz) nie powoduje
wzrostu oporów przepływu.
W około 80% przypadkach lewa tętnica wieńcowa ma większą
średnicę od prawej. Rozkurcz komór jest momentem kiedy
krew może swobodnie przepływać przez tętnice wieńcowe.

Naczynia wieńcowe serca
Lewa tętnica wieńcowa (arteria coronaria sinistra)
odchodzi w lewej zatoce aorty w postaci krótkiego pnia
(ok.1 cm), który następnie dzieli się na
- gałąź miedzykomorową przednią = przednią zstępującą
(LAD - left anterior decsending)
- gałąź okalającą (Cx - circumflexus).
Od LAD odchodzą drobniejsze odgałęzienia takie jak
gałąź skośna lewej tętnicy wieńcowej zstępującej (D),
tętnice przegrodowe (S). Od pnia gałęzi okalającej (Cx)
odchodzą tętnica okalająca przedsionka lewa (LAC) i
gałęzie brzeżne.

Naczynia wieńcowe serca
Prawa tętnica wieńcowa - RCA - right coronary artery -
(arteria coronaria dextra) odchodzi w prawej zatoce aorty.
Jedną z pierwszych gałęzi odchodzących od prawej tętnicy
wieńcowej jest gałąź węzła zatokowego (SN), która
unaczynia węzeł zatokowo-przedsionkowy.
Następnie odchodzi od niej gałąź komorowa prawa (RV) i
gałąź przedsionkowa prawa (RA).
W dalszym odcinku z prawej tętnicy wieńcowej
wyodrębnia się tętnica brzeżna i tętnica zstępująca tylna
(PD).

Zakres unaczynienia tętnic wieńcowych:
Tętnica wieńcowa lewa :
lewa komora serca
lewy przedsionek
2/3 przednie przegrody międzykomorowej
mięśnie brodawkowate komory lewej
Tętnica wieńcowa prawa :
prawa komora serca
prawy przedsionek
1/3 tylna przegrody międzykomorowej
mięśnie brodawkowate komory prawej
Mięsień brodawkowaty przedni komory prawej otrzymuje także
zaopatrzenie w krew z tętnicy wieńcowej lewej. Mięsień brodawkowaty
tylny komory lewej otrzymuje dodatkowo krew z tętnicy wieńcowej
prawej.

Czynność mechaniczna serca. Hemodynamika.
Podstawową czynnością układu krążenia jest zapewnienie
przepływu krwi w naczyniach. Układ krążenia jest niezbędny
do zapewnienia następujących funkcji :
• transportowanie tlenu i substratów odżywczych do tkanek;
• usuwanie dwutlenku węgla i produktów przemiany materii
ze wszystkich tkanek organizmu;
• regulacja temperatury organizmu poprzez skórną regulację
przepływu krwi;
• bierze udział w reakcjach odpornościowych organizmu -
transport przeciwciał, leukocytów do miejsca infekcji;
• transport hormonów;

Czynność mechaniczna serca. Hemodynamika.
Podczas rozkurczu komór krew napływa z przedsionków przez
otwarte zastawki przedsionkowo-komorowe. Skurcz mięśniówki
przedsionków wyprzedza skurcz mięśniówki komór serca, więc
krew swobodnie zostaje wtłoczona podczas skurczu przedsionków
do komór serca.
Ciśnienie skurczowe w lewej komorze jest pięciokrotnie wyższe od
ciśnienia skurczowego w komorze prawej. Mimo tej różnicy ciśnień
objętość krwi wyrzucanej z komór podczas ich skurczu jest
zbliżona.
Objętość wyrzutowa serca - SV (stroke volume) - jest to objętość
krwi wytłoczona przez jedną z komór serca podczas jej skurczu. U
dorosłego mężczyzny objętość krwi wytłoczonej przez komorę
podczas skurczu wynosi około 70-75 ml.

Czynność mechaniczna serca. Hemodynamika.
Pojemność minutowa (cardiac output) - jest to pojemność krwi
wytłoczonej przez jedną z komór w czasie jednej minuty.
Pojemność minutową oblicza się mnożąc objętość wyrzutową
przez liczbę skurczów w czasie jednej minuty.
Objętość wyrzutowa serca jest zależna od kilku czynników, do
których zalicza się między innymi: ciśnienie tętnicze,
kurczliwość komór, objętość krwi w komorze na początku jej
skurczu.
Wskaźnik sercowy (cardiac index) - jest to wskaźnik, który jest
stosunkiem pojemności minutowej serca do powierzchni ciała.
Pojemność minutowa serca w spoczynku przeliczona jest na 1
metr kwadratowy powierzchni ciała (ok. 3,2 L/min./metr
kwadratowy).

Zawał serca i jego następstwa są główną przyczyną zgonów
w Polsce. Spośród 1 miliona pacjentów z chorobą
niedokrwienną serca na zawał zapada każdego roku 10%, tj.
około 100.000 osób. Bezpośrednią przyczyną zawału jest u
90% chorych całkowite zamknięcie tętnicy przez zakrzep
uruchomiony pęknięciem blaszki miażdżycowej zwężającej
tętnicę.
Mimo postępu diagnostyki i terapii, roczna śmiertelność
związana z zawałem przekracza 40%: w okresie
przedszpitalnym sięga 23-35% (najwięcej osób ginie w ciągu 1
godz. od wystąpienia objawów), w okresie szpitalnym 7-15% i
w okresie pierwszego roku po zawale wynosi 5-10% - zależnie
od stosowanych metod leczenia.

Wśród pacjentów z chorobą wieńcową i populacji
wysokiego ryzyka zawału należy prowadzić edukację, mającą
na celu skrócenie czasu między wystąpieniem bólu a
wezwaniem karetki pogotowia.
Należy również poprawić szybkość transportu chorych
z zawałem do szpitala i skrócić nieuzasadnione opóźnienie
czasu rozpoczęcia leczenia fibrynolitycznego - między
przybyciem chorego na izbę przyjęć a rozpoczęciem
podawania leku fibrynolitycznego (obecnie upływa średnio
ponad godzina).

Celem leczenia jest
• redukcja śmiertelności,
• zmniejszenie obszaru zawału i dysfunkcji lewej komory,
• poprawa bilansu tlenowego mięśnia sercowego
• oraz zwalczanie innych następstw zawału (groźne zaburzenia rytmu,
mechaniczne powikłania, niewydolność serca).
Oceny stanu chorych i ich rokowania w zawale serca można dokonać
w oparciu o proste objawy kliniczne ujęte w klasyfikacji Killipa i
Kimballa.
Klasa
Objawy kliniczne
Częstość
występowani
a
w %
Przybliżona
śmiertelno
ść
w %
I
Bez rzężeń nad płucami i III tonu serca
30 - 40
8
II
Rzężenia obejmujące mniej niż 50% pól płucnych
lub III ton
30 - 40
30
III
Rzężenia ponad 50% pól płucnych (obrzęk płuc)
5 - 10
44
IV
Wstrząs zawałowy
10
80 - 100

Najczęstsze powikłania zawału serca
obejmują:
• zaburzenia rytmu i przewodzenia,
• niewydolność serca (obrzęk płuc,
wstrząs),
• ostrą niewydolność mitralną,
• pęknięcie wolnej ściany lewej komory,
• pęknięcie przegrody komorowej,
• tętniak lewej komory,
• zakrzepy i zatory.

Chorzy z różnymi postaciami niestabilnej choroby wieńcowej i
odpowiadającym im ryzykiem zgonu lub zawału serca
1. Niestabilna choroba wieńcowa wysokiego ryzyka:
•ból spoczynkowy przedłużający się > 20 min
•obrzęk płuc związany najprawdopodobniej z wystąpieniem niedokrwienia
•dławica spoczynkowa z dynamiką zmian odcinka ST o co najmniej1 mm
•blok odnogi pęczka Hisa lub nowy obraz utrwalonego częstoskurczu
komorowego w EKG
•dławica z wystąpieniem nowego lub pogorszeniem istniejącego szmeru
niedomykalności mitralnej
•dławica z występującym osłuchowo trzecim tonem, nowymi objawami
zastoju lub pogorszeniem objawów zastoju w płucach
•dławica z towarzyszącą hipotonią oraz bradykardią lub tachykardią
•wiek > 75 r.ż
•znacznie podwyższone markery martwicy mięśnia sercowego (np.
troponina T > 0,1 ng/ml)

Chorzy z różnymi postaciami niestabilnej choroby wieńcowej i
odpowiadającym im ryzykiem zgonu lub zawału serca
2. Niestabilna choroba wieńcowa pośredniego ryzyka
•ból spoczynkowy, który trwał > 20 min, ale ustąpił oraz umiarkowane lub
wysokie prawdopodobieństwo choroby wieńcowej
•dławica spoczynkowa < 20 min lub ustępująca w spoczynku bądź po
podjęzykowym podaniu azotanu
•dławica występująca w nocy
•dławica z dynamiką zmian załamka T
•patologiczny załamek Q lub obniżenie odcinka ST o co najmniej 1 mm w
spoczynku, w kilku odprowadzeniach lokalizujących (ściana przednia, dolna,
boczna)
•wiek > 70 r.ż.
•wywiad przebytego zawału serca lub rewaskularyzacji wieńcowej, lub
wcześniejszego stosowania kwasu acetylosalicylowego, lub choroby
miażdżycowej innych naczyń niż naczynia wieńcowe
•średnio podwyższone markery martwicy mięśnia sercowego (np. troponina
T> 0,01 ng/ml, ale < 0,1 ng/ml)

Chorzy z różnymi postaciami niestabilnej choroby wieńcowej
i odpowiadającym im ryzykiem zgonu lub zawału serca
3. Niestabilna choroba wieńcowa niskiego ryzyka
•większe niż dotychczas częstość, nasilenie lub czas trwania
dławicy
•dławica wywołana przez małe obciążenia - klasa 3 CCS
•dławica de novo między 2 tygodniem a 2 miesiącem
•EKG - prawidłowe lub bez dynamiki zmian
•bez podwyższonej wartości markerów martwicy miokardium we
krwi

Podstawowe znaczenie w diagnostyce bólów
zlokalizowanych w klatce piersiowej stanowi wstępny
zapis EKG. Na podstawie badania EKG można wnosić o
wystąpieniu niedokrwienia, analizując zarówno odcinek
ST, jak i załamki T. Zmianami charakterystycznymi dla
ostrych zespołów wieńcowych są:
• nowe uniesienie odcinka ST w punkcie J powyżej
• 0,2 mV w odprowadzeniach VI—V3
• 0,1 mV w pozostałych odprowadzeniach (ostre
zespoły wieńcowe z przetrwałym uniesieniem ST)
• obniżenie ST lub zmiany kształtów załamka T (ostre
zespoły wieńcowe bez przetrwałego uniesienia ST).

Na podstawie 12-odprowadzeniowego EKG można chorych podzielić na
tych z przetrwałym uniesieniem odcinka ST oraz na tych bez
przetrwałego uniesienia odcinka ST. W grupie chorych z ostrym
zespołem wieńcowym bez przetrwałego uniesienia ST można wyróżnić
kolejne typy ostrych zespołów wieńcowych na podstawie wstępnego
elektrokardiogramu.
Drugim podziału chorych z ostrym zespołem wieńcowym, zwłaszcza bez
przetrwałego uniesienia odcinka ST, jest obok stanu klinicznego i zmian
w EKG także wyjściowe stężenie markerów biochemicznych martwicy
mięśnia sercowego, oparte na oznaczaniu troponiny lub frakcji
izoenzymu kinazy kreatynowej (CK-MB). Oznaczenie stężenia tych
markerów pozwala na odróżnienie zawałów serca od niestabilnej
choroby wieńcowej. Dalsza ewolucja zmian elektrokardiograficznych
uzasadnia tradycyjny podział zawałów serca zarówno na te z załamkiem
Q, jak i na te bez odłamka Q.
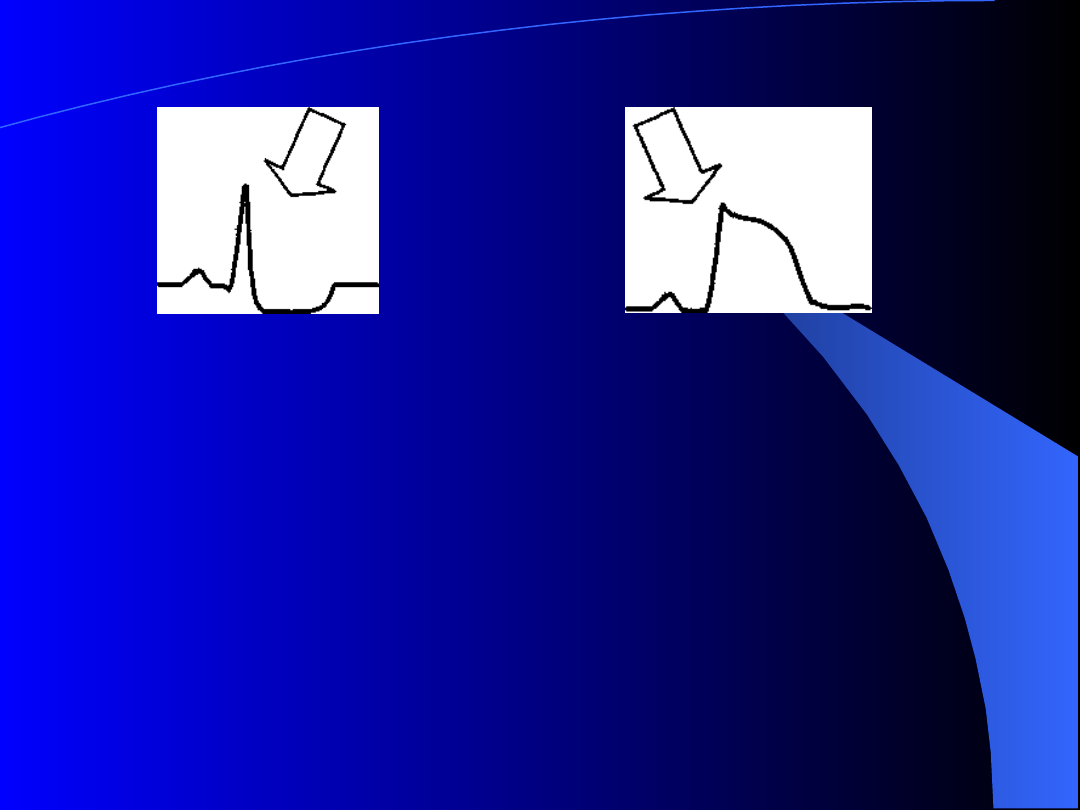
bez przetrwałego uniesienia ST
z przetrwałym uniesieniem ST
OZW z przejściowym uniesieniem ST
OZW z obniżeniem ST
OZW z odwróceniem załamków T
OZW z pseudonormalizacją T
OZW ze spłaszczeniem T
OZW bez zmian w EKG
Podział chorych z bólem wieńcowym w zależności od obrazu
EKG - wstępne rozpoznanie poszczególnych typów ostrych
zespołów wieńcowych
O dokonaniu się zawału mięśnia sercowego można wnosić na podstawie
obecności jakiegokolwiek załamka Q w odprowadzeniach VI-V3 lub
załamka Q o szerokości > 0,03 s w odprowadzeniach: I, II, aVL, aVF, V4,
V5 lub V6.

Za zawał uważa się obecnie każdą martwicę mięśnia sercowego
spowodowaną niedokrwieniem, niezależnie od rozmiarów, podstawowym
zaś kryterium oceny martwicy jest wzrost stężenia troponin i/lub CK-MB.
Rozpoznanie można oprzeć na stwierdzeniu typowego wzrostu i
stopniowego spadku troponiny lub szybkiego wzrostu i spadku CK-MB,
przy współistnieniu
- typowego wywiadu dolegliwości bólowych,
- lub pojawienia się w zapisie EKG patologicznego załamka Q lub
obecności zmian o charakterze niedokrwiennym w zapisie EKG
(uniesienie, obniżenie odcinka ST),
-lub w sytuacji zabiegu na tętnicach wieńcowych (np. angioplastyka
wieńcowa).
O martwicy kardiomiocytów świadczy charakterystyczny, skorelowany z
obszarem martwicy, wzrost stężenia lub aktywności biochemicznych
markerów niedokrwienia, oznaczanych we krwi.

Ponieważ definicja zawału opiera się na oznaczeniach
biochemicznych, należy ściśle rozróżnić sytuację, gdy można mówić
wyłącznie o ostrych zespołach wieńcowych (sytuacja rozpoznania
wstępnego przy przyjęciu chorego, gdy do dyspozycji pozostaje
jedynie EKG, a nie ma jeszcze wyników oznaczeń enzymatycznych)
oraz gdy rozpoznajemy zawał serca lub niestabilną chorobę
wieńcową.
Tak więc, nawet gdy pacjent prezentuje cechy kliniczne „świeżego
zawału serca" w tradycyjnym rozumieniu z obecnością
charakterystycznej fali Pardeego w zapisie EKG, powinno się używać
w stosunku do tego pacjenta pojęcia „ostrego zespołu wieńcowego z
przetrwałym uniesieniem ST" dopóty, dopóki nie będzie się
dysponować wynikami biochemicznych oznaczeń CK-MB lub
troponiny.

Stąd też coraz częściej odstępuje się od wyróżniania zawału serca Q lub
non-Q na rzecz operowania pojęciem zawału serca z uniesieniem ST w
fazie ostrej (ST-elevation myocardial infarction - STEMI) lub zawału
serca bez uniesienia ST w fazie ostrej choroby (Non-ST elevation
myocardial infarction — NSTEMI).
Grupę chorych z NSTEMI łączy wiele - pod względem patofizjologii i
dalszego postępowania terapeutycznego - z pacjentami z ostatecznie
rozpoznaną niestabilną chorobą wieńcową (unstable angina - UA),
dlatego też obie grupy są określane często łącznie jako UA/NSTEMI.
Proponowany sposób klasyfikacji wiąże się również z bardziej swoistym
doborem markerów martwicy miokardium w każdej z grup (troponiny w
grupie UA/NSTEMI, natomiast CK-MB w grupie STEMI).

Można wyróżnić obecnie cztery podstawowe typy
ostrych zespołów wieńcowych:
• niestabilną chorobę wieńcową, niestabilną dławicę
piersiową (UA),
• zawał serca z uniesieniem ST (STEMI),
• zawał serca bez uniesienia ST (NSTEMI),
• nagły zgon sercowy.

Lokalizacja zawału według obecności załamka Q
Lokalizacja zawału według obecności załamka Q
Przegrodowy
V1 – V2
Przedni
V3 – V4
Przednioprzegrodo
wy
V1 – V4
Boczny
I, aVL, V6
Przednioboczny
I, aVL, V3 – V6
Rozległy przedni
I, aVL, V1 – V6
Wysoki boczny
I, aVL, V3 – V4
Dolny
II, III, aVF
Koniuszkowy
II, III, aVF, jedno z V1 – V4
Tylny
R > 0,04 sek i R/S > 1 (Q-
ekwiwalent) z obniżeniem ST w
V1 – V2
Prawej komory
Uniesienie ST w V1 – V2, V3R –
V4R

Klasyfikacja zaleceń i danych naukowych
Klasyfikacja zaleceń i danych naukowych
klasa zalecenia
I - stany, w których określone postępowanie (diagnostyczne lub lecznicze)
jest korzystne, przydatne i skuteczne, na co wskazują wyniki badań i(lub)
powszechnie akceptowana opinia (oznacza: zdecydowanie stosować -
przyp. red.)
II - stany, w których wyniki badań i(lub) opinie co do przydatności lub
skuteczności określonego postępowania nie są zgodne (oznacza: raczej
stosować - przyp. red.)
IIa - wyniki badań lub panujące opinie przemawiają za przydatnością lub
skutecznością określonego postępowania
IIb - przydatność lub skuteczność określonego postępowania jest słabiej
potwierdzona przez wyniki badań lub panujące opinie
III - stany, w których określone postępowanie jest nieprzydatne lub
nieskuteczne, a w niektórych przypadkach może być szkodliwe - na co
wskazują wyniki badań i(lub) powszechnie akceptowana opinia (oznacza:
nie stosować - przyp. red.)
stopień wiarygodności danych
A - dane pochodzące z licznych badań klinicznych z randomizacją lub z
metaanaliz
B - dane pochodzące z jednego badania z randomizacją lub z badań bez
randomizacji
C - uzgodniona opinia ekspertów, opisy przypadków, standardowe
postępowanie

1. Postępowanie przedszpitalne
· Chory na chorobę wieńcową, któremu wcześniej przepisano
nitroglicerynę, powinien w razie wystąpienia dyskomfortu lub bólu w
klatce piersiowej zażyć JEDNĄ dawkę nitrogliceryny podjęzykowo. Jeśli
w ciągu 5 minut po zażyciu nitrogliceryny dyskomfort lub ból w klatce
piersiowej się nie zmniejsza lub nasila, chory (lub osoba z którą
przebywa) powinien niezwłocznie wezwać telefonicznie pogotowie
ratunkowe [I/C].
· Personel pogotowia ratunkowego powinien podać choremu z bólem w
klatce piersiowej budzącym podejrzenie zawału serca kwas
acetylosalicylowy (ASA, 162-325 mg), jeżeli lek ten nie jest
przeciwwskazany lub chory nie przyjął go już sam [I/C].
· Zastosowanie przedszpitalnego leczenia fibrynolitycznego jest
uzasadnione w sytuacji, gdy personel karetki pogotowia może ustalić
rozpoznanie świeżego zawału serca z uniesieniem ST (STEMI) na
podstawie 12-odprowadzeniowego elektrokardiogramu (EKG) [IIa/B].

Postępowanie przedszpitalne
· Niezwłoczne przewiezienie (czas od przybycia do opuszczenia
pierwszego szpitala <30 min) do ośrodka, w którym wykonuje się
cewnikowanie serca i szybką rewaskularyzację (PCI lub CABG) jest
wskazane w przypadku chorego na STEMI:
- we wstrząsie kardiogennym, jeśli zabieg można wykonać w ciągu 18
godzin od wystąpienia wstrząsu [I/A dla chorych w wieku <75 lat; IIa/B
dla chorych w wieku >=75 lat],
- z przeciwwskazaniami do leczenia fibrynolitycznego [I/B],
- obciążonych szczególnie dużym ryzykiem zgonu, w tym z ciężką
zastoinową niewydolnością serca [IIa/B].

Postępowanie na oddziale ratunkowym
Uwagi ogólne
· Wszystkim chorym przyjmowanym na oddział ratunkowy z powodu
dyskomfortu w klatce piersiowej lub innych dolegliwości wskazujących na
STEMI lub niestabilną dławicę piersiową należy przyznać bezwzględne
pierwszeństwo podczas selekcji oraz ocenić ich stan i leczyć na podstawie
wcześniej ustalonego protokołu postępowania w razie bólu w klatce
piersiowej.
· U chorych na STEMI czas od przybycia do szpitala do rozpoczęcia
dożylnego leczenia fibrynolitycznego (door-to-needle time) nie powinien
przekraczać 30 minut, a czas od rozpoczęcia hospitalizacji do napełnienia
balonu podczas PCI (door-to-balloon time) nie powinien przekraczać 90
minut.

Rozpoznanie różnicowe STEMI
stany zagrażające życiu
· rozwarstwienie aorty
· zator tętnicy płucnej
· przebity wrzód trawienny
· odma opłucnowa prężna
· pęknięcie przełyku z zapaleniem śródpiersia (zespół Boerhaavego)
inne stany sercowo-naczyniowe
· zapalenie osierdzia
· nietypowa dławica piersiowa
· wczesna repolaryzacja
· zespół Wolffa, Parkinsona i White'a (WPW)
· głębokie odwrócone załamki T sugerujące uszkodzenie ośrodkowego
układu nerwowego lub koniuszkową kardiomiopatię przerostową
· przeciążenie lewej komory
· zapalenie mięśnia sercowego
· hiperkaliemia
· bloki odnóg pęczka Hisa
· dławica naczynioskurczowa
· kardiomiopatia przerostowa

Rozpoznanie różnicowe STEMI
stany inne niż sercowo-naczyniowe
· choroba refluksowa lub skurcz przełyku
· ból ściany klatki piersiowej
· ból opłucnowy
· choroba wrzodowa
· napad paniki
· kolka żółciowa lub ból trzustkowy
· dyskopatia szyjna lub ból neuropatyczny
· ból psychogenny

2.2. Rozpoznanie
2.2.1. Wywiad
· Należy ustalić, czy chory wcześniej przebył epizody niedokrwienia mięśnia
sercowego (stabilną lub niestabilną dławicę piersiową, zawał serca, CABG
lub PCI). Ocena skarg chorego powinna się skupiać na dyskomforcie w
klatce piersiowej, towarzyszących mu dolegliwościach, nadciśnieniu
tętniczym, cukrzycy, możliwości rozwarstwienia aorty, ryzyku krwawienia i
objawach niedokrwienia mózgu (np. nagłe niedowidzenie, zaburzenia mowy,
utrata pamięci, osłabienie mięśni twarzy lub kończyny bądź niezgrabność,
drętwienie twarzy lub kończyn bądź utrata czucia, ataksja lub zawroty głowy)
[I/C].
2.2.2. Badanie przedmiotowe
Badanie powinno obejmować ocenę:
- oddychania,
- tętna i ciśnienia krwi,
- skóry (zimna, wilgotna i blada lub sina jest objawem wstrząsu),
- żył szyjnych (ich poszerzenie może wskazywać na niewydolność prawej
komory),
- osłuchową płuc (trzeszczenia lub rzężenia mogą wskazywać na
niewydolność lewej komory),
- osłuchową serca pod kątem szmerów i cwału (ich obecność może
wskazywać na powikłania zawału serca),
- neurologiczną pod kątem objawów udaru mózgu (stanowi
przeciwwskazanie do leczenia fibrynolitycznego).

Elektrokardiogram
· 12-odprowadzeniowy EKG wykonany na oddziale ratunkowym jest
podstawą decyzji o leczeniu, ponieważ uniesienie odcinków ST wyróżnia
chorych odnoszących korzyść z leczenia reperfuzyjnego.
· U wszystkich chorych z dyskomfortem w klatce piersiowej (lub
równoważnikiem dławicy) bądź z innymi objawami wskazującymi na STEMI
należy w ciągu 10 minut od przybycia na oddział ratunkowy wykonać 12-
odprowadzeniowy EKG [I/C].
· Jeżeli na podstawie pierwszego EKG nie można rozpoznać STEMI, a u
chorego nadal występują dolegliwości oraz istnieje duże podejrzenie
STEMI, należy wykonywać seryjne badania EKG co 5-10 minut lub
prowadzić ciągłe, 12-odprowadzeniowe monitorowanie odcinków ST w celu
wykrycia ich uniesienia [I/C].
· U chorych ze STEMI ściany dolnej należy wykonać EKG z odprowadzeń
prawostronnych w celu oceny, czy występuje uniesienie odcinków ST
wskazujące na zawał prawej komory [I/B].

Badania laboratoryjne
· U chorych na STEMI ze współistniejącym uszkodzeniem mięśni
szkieletowych należy wykorzystywać swoiste dla serca troponiny jako
optymalne biomarkery uszkodzenia mięśnia sercowego [I/C].
· U chorych z uniesieniami odcinków ST w 12-odprowadzeniowym EKG i z
podmiotowymi objawami STEMI należy natychmiast rozpocząć leczenie
reperfuzyjne, nie uzależniając go od wyników oznaczeń biomarkerów [I/C].
· Rozpoznając ponowny zawał serca w ciągu 18 godzin od wystąpienia
STEMI, nie należy polegać na seryjnych pomiarach biomarkerów [III/C].
· Seryjne oznaczenia biomarkerów mogą być użyteczne jako dodatkowy
nieinwazyjny dowód reperfuzji tętnicy odpowiedzialnej za zawał u chorych,
u których w ciągu pierwszych 24 godzin po leczeniu fibrynolitycznym nie
wykonano koronarografii [IIa/B].

Badania laboratoryjne
Poza oznaczeniami w surowicy biomarkerów uszkodzenia serca istotny
wpływ na postępowanie z chorymi na STEMI ma jeszcze kilka innych
badań rutynowych:
- pełna morfologia krwi z liczbą płytek,
- INR i aPTT,
- elektrolity (w tym stężenie magnezu) w surowicy,
- mocznik i kreatynina w surowicy,
- glukoza w surowicy,
- lipidy w surowicy.
Badania te powinno się zlecać podczas pierwszego kontaktu z chorym,
ale nie należy opóźniać decyzji o leczeniu do czasu uzyskania wyników
[I/C], ponieważ w STEMI zasadniczą rolę odgrywa czas upływający do
wdrożenia leczenia.

Badania obrazowe
· U chorych na STEMI należy wykonać przyłóżkowy radiogram klatki
piersiowej, lecz nie powinno to opóźniać zastosowania leczenia
reperfuzyjnego (jeżeli nie podejrzewa się przeciwwskazania, takiego
jak rozwarstwienie aorty) [I/C].
· Aby odróżnić STEMI od rozwarstwienia aorty u chorych, u których
początkowo rozpoznanie nie jest jasne, należy się posłużyć badaniami
obrazowymi, takimi jak przyłóżkowy radiogram klatki piersiowej,
echokardiografia przezklatkowa lub przezprzełykowa, tomografia
komputerowa lub rezonans magnetyczny [I/B].
· Uzasadnione jest przyłóżkowe wykonanie echokardiografii w celu
ustalenia rozpoznania STEMI i oceny ryzyka u chorych z bólem w
klatce piersiowej przy przyjęciu na oddział ratunkowy, zwłaszcza jeśli
rozpoznanie STEMI utrudnia blok lewej odnogi pęczka Hisa (LBBB)
lub elektrostymulacja serca, bądź istnieje podejrzenie STEMI w
obrębie tylnej ściany z obniżeniem odcinków ST nad przednią ścianą
serca [IIa/B].

Leczenie
2.3.1. Tlen
· Należy podawać tlen chorym, u których wysycenie tlenem hemoglobiny krwi
tętniczej (SaO2) jest zmniejszone (<90%) [I/B].
· Uzasadnione jest podawanie tlenu wszystkim chorym z niepowikłanym STEMI w
ciągu pierwszych 6 godzin [IIa/C].
2.3.2. Nitrogliceryna
· Chorzy, u których utrzymuje się dyskomfort typu niedokrwiennego, powinni
otrzymywać podjęzykowo nitroglicerynę (0,4 mg) co 5 minut, łącznie 3 dawki, po
czym należy rozważyć potrzebę dożylnego podania nitrogliceryny [I/C].
· Dożylne leczenie nitrogliceryną jest wskazane w celu łagodzenia utrzymującego się
dyskomfortu niedokrwiennego, kontrolowania nadciśnienia tętniczego lub
opanowania zastoju w krążeniu płucnym [I/C].
· Proponowane dawkowanie dożylne nitrogliceryny: wlew początkowo 5-10 µg/min,
zwiększany o 5-20 µg/min do chwili ustąpienia objawów lub obniżenia się średniego
ciśnienia tętniczego o 10% względem wartości wyjściowej u chorych bez
nadciśnienia, a o 30% u chorych z nadciśnieniem.
· Nie należy podawać azotanów chorym:
- ze skurczowym ciśnieniem tętniczym <90 mm Hg lub obniżonym o 30 mm Hg
względem wartości wyjściowej [III/C],
- ze znaczną bradykardią (<50/min) [III/C],
- z tachykardią (>100/min) [III/C],
- z podejrzeniem zawału prawej komory [III/C]

2.3.3. Leczenie przeciwbólowe
· Lekiem przeciwbólowym z wyboru do uśmierzenia bólu towarzyszącego STEMI
jest siarczan morfiny (w dawkach 2-4 mg i.v. zwiększanych o 2-8 mg i.v. i
powtarzanych co 5-15 minut) [I/C].
2.3.4. ASA
· Wszyscy chorzy, którzy nie przyjęli ASA przed przybyciem do szpitala, powinni
otrzymać ASA. Początkowa dawka powinna wynosić od 162 mg [I/A] do 325 mg
[I/C].
2.3.5. Beta-blokery
· U chorych bez przeciwwskazań należy szybko zastosować doustne leczenie beta-
blokerem, niezależnie od równoczesnego leczenia fibrynolitycznego lub
wykonywania pierwotnej PCI [I/A].
· Uzasadnione jest też szybkie podanie beta-blokerów dożylnie, zwłaszcza jeżeli
występuje tachyarytmia lub nadciśnienie tętnicze [IIa/B].
Przeciwwskazania:
•
blok I° z PQ ponad 0,24 s oraz blok II° i III°,
•
wywiady dychawicy oskrzelowej,
•
niewydolność serca z rzężeniami ponad 1/3 dolną płuc,
•
bradykardia poniżej 50/min.,
•
ciśnienie skurczowe poniżej 100 mmHg,
•
ciśnienie zaklinowane w tętnicy płucnej ponad 20 mmHg.

Leczenie reperfuzyjne
· U wszystkich chorych na STEMI należy szybko ocenić, czy nadają się
oni do leczenia reperfuzyjnego i (jeśli nie ma przeciwwskazań)
natychmiast je wdrożyć [I/A].
· Wybierając metodę leczenia reperfuzyjnego, należy rozważyć:
- czas od wystąpienia dolegliwości,
- ryzyko STEMI,
- ryzyko krwawienia związane z leczeniem fibrynolitycznym,
- czas potrzebny na transport chorego do pracowni wykonującej PCI.
· Jeżeli czas od wystąpienia objawów STEMI nie przekracza 3 godzin i
wybór strategii inwazyjnej nie spowoduje opóźnienia, to żadna z metod
(leczenie fibrynolityczne albo PCI) nie ma pierwszeństwa nad drugą.

Leczenie reperfuzyjne
· Leczenie fibrynolityczne preferuje się na ogół, jeżeli:
a) chory wcześnie zgłosił się po pomoc (do 3 godzin od wystąpienia
objawów STEMI, a strategia inwazyjna wiąże się z opóźnieniem),
b) nie ma możliwości wyboru strategii inwazyjnej
- pracownia cewnikowania serca jest zajęta lub niedostępna,
- istnieją trudności w uzyskaniu dostępu naczyniowego,
c) strategia inwazyjna wiąże się z opóźnieniem leczenia
- przedłużony transport,
- różnica między czasem od przybycia do szpitala do napełnienia balonu a
czasem od rozpoczęcia hospitalizacji do wdrożenia leczenia
fibrynolitycznego (dotyczy leków swoistych dla fibryny, takich jak
alteplaza) wynosi ponad 1 godzinę,
- czas od wezwania pomocy medycznej lub rozpoczęcia hospitalizacji do
napełnienia balonu wynosi ponad 90 minut.

Leczenie reperfuzyjne
· Strategię inwazyjną preferuje się na ogół, jeżeli:
a) dostępna jest pracownia cewnikowania serca
- czas od wezwania pomocy medycznej lub rozpoczęcia hospitalizacji do
napełnienia balonu wynosi poniżej 90 minut,
- różnica między czasem od przybycia do szpitala do napełnienia balonu a
czasem od rozpoczęcia hospitalizacji do wdrożenia leczenia
fibrynolitycznego (dotyczy leków swoistych dla fibryny, takich jak alteplaza)
wynosi poniżej 1 godziny,
b) STEMI obciążony dużym ryzykiem
- wstrząs kardiogenny,
- >=3 klasa Killipa,
c) występują przeciwwskazania do leczenia fibrynolitycznego,
d) późne zgłoszenie się do szpitala (objawy STEMI wystąpiły wcześniej niż
przed 3 godzinami),
e) rozpoznanie STEMI budzi wątpliwości.

Ważne różnice między wytycznymi amerykańskimi a europejskimi dotyczą leczenia
reperfuzyjnego. Zgodnie wskazuje się na potrzebę skrócenia opóźnienia tego
leczenia i w związku z tym korzyści stosowania leczenia fibrynolitycznego w fazie
przedszpitalnej. W wytycznych amerykańskich podkreśla się znaczenie opóźnienia
leczenia za pomocą PCI w stosunku do leczenia fibrynolitycznego. Jeżeli różnica
czasów "door to balloon" i "door to needle" przekracza 60 minut, to zniwelowana
zostaje przewaga leczenia inwazyjnego nad leczeniem fibrynolitycznym. W
wytycznych amerykańskich postuluje się także, aby opóźnienie rozpoczęcia leczenia
fibrynolitycznego nie przekraczało 30 minut od przyjazdu karetki pogotowia do
chorego, a opóźnienie pierwotnej PCI nie przekraczało 90 minut. Jeżeli pacjent
trafia najpierw do szpitala bez pracowni hemodynamicznej, to czas od przybycia do
opuszczenia tego szpitala powinien być krótszy niż 30 minut.
Wytyczne amerykańskie wyodrębniają pierwsze 3 godziny od początku objawów, w
czasie których nie stwierdza się przewagi leczenia inwazyjnego nad
fibrynolitycznym. Nowością jest stwierdzenie, że jeśli czas od wystąpienia objawów
nie przekracza 3 godzin i wybór strategii inwazyjnej nie spowoduje opóźnienia, to
żadna z metod nie ma przewagi nad drugą. Podejmując decyzję o sposobie leczenia
reperfuzyjnego, należy uwzględnić dodatkowe czynniki przemawiające bądź za
strategią inwazyjną, bądź za leczeniem fibrynolitycznym. Leczenie reperfuzyjne
trzeba podjąć, nie czekając na wyniki oznaczeń markerów uszkodzenia serca.

Porównanie leków fibrynolitycznych
Streptokinaza
Alteplaza (t-PA)
dawkowanie
1,5 mln j. i.v. w ciągu 30-60
minut
i.v., bolus 15 mg, następnie
wlew 0,75 mg/kg (maks. 50
mg) w ciągu 30 minut i 0,5
mg/kg (maks. 35 mg) w
ciągu kolejnych 60 minut
reakcje alergiczne
(najczęściej hipotonia)
tak
nie
zmniejszenie stężenia
fibrynogenu we krwi
duże
niewielkie
skuteczność
drożność po 90 minutach
50%
75%
Stosowane leki
streptokinaza
APSAC – acylowany kompleks streptokinazy z plazminogenem
tkankowy aktywator plazminogenu (TPA)
rekombinowany TPA – rTPA (reteplase)
urokinaza

Wskazania do leczenia fibrynolitycznego
· Leczenie fibrynolityczne należy zastosować, jeżeli nie ma przeciwwskazań, u
chorych, u których objawy STEMI wystąpiły w ciągu ostatnich 12 godzin, a w 12-
odprowadzeniowym EKG stwierdza się:
- uniesienie ST o ponad 0,1 mV przynajmniej w 2 kolejnych odprowadzeniach
przedsercowych lub przynajmniej w 2 sąsiadujących odprowadzeniach kończynowych
[I/A; IIa/B, jeśli dolegliwości rozpoczęły się 12-24 godzin wcześniej i nadal się
utrzymują]
- świeży lub prawdopodobnie świeży LBBB [I/A].
· Zastosowanie leczenia fibrynolitycznego jest uzasadnione u chorych na STEMI z
dolegliwościami, które rozpoczęły się w ciągu ostatnich 12 godzin, a w 12-
odprowadzeniowym EKG stwierdza się cechy zawału tylnej ściany serca (wysokie
załamki R w przedsercowych odprowadzeniach prawokomorowych i obniżenie
odcinków ST w V1-V4, zwłaszcza gdy załamki T są dodatnie; w razie klinicznego
podejrzenia zawału ściany tylnej pomocne bywa uzyskanie EKG z dodatkowych
odprowadzeń V7-V9) [IIa/C].
· Nie należy stosować leczenia fibrynolitycznego u chorych bez dolegliwości, z
zawałem z obniżeniem odcinka ST, u których objawy STEMI pojawiły się wcześniej niż
przed 24 godzinami [III/C].

Przeciwwskazania i środki ostrożności dotyczące leczenia
fibrynolitycznego w zawale serca z uniesieniem ST
przeciwwskazania bezwzględne
· jakiekolwiek wcześniej przebyte krwawienie śródczaszkowe
· rozpoznana nieprawidłowość organiczna naczyń mózgowych (np. wada
rozwojowa tętniczo-żylna)
· rozpoznany złośliwy nowotwór wewnątrzczaszkowy (pierwotny lub
przerzutowy)
· udar niedokrwienny mózgu w ciągu ostatnich 3 (6) miesięcy z wyjątkiem
świeżego udaru niedokrwiennego mózgu w ciągu ostatnich 3 godzin
· podejrzenie rozwarstwienia aorty
· czynne krwawienie lub skaza krwotoczna (z wyjątkiem krwawienia
miesiączkowego)
· poważny zamknięty uraz głowy lub twarzy w ciągu ostatnich 3 miesięcy
· przebyty w ciągu 3 ostatnich tygodni duży uraz (zabieg operacyjny)
· krwawienie z przewodu pokarmowego w ciągu ostatnich 30 dni

Przeciwwskazania i środki ostrożności dotyczące leczenia
fibrynolitycznego w zawale serca z uniesieniem ST
przeciwwskazania względne
· przewlekłe ciężkie, źle kontrolowane nadciśnienie tętnicze w wywiadach
· ciężkie, niekontrolowane nadciśnienie tętnicze podczas wstępnego badania
(ciśnienie skurczowe >180 mm Hg lub rozkurczowe >110 mm Hg)
· w wywiadach udar niedokrwienny mózgu wcześniej niż przed 3 (6) miesiącami,
otępienie lub inna patologia wewnątrzczaszkowa nieujęta w przeciwwskazaniach
· przemijające niedokrwienie mózgu w poprzedzających 6 miesiącach
· powikłana urazem lub przedłużona (>10 min) resuscytacja krążeniowo-oddechowa
lub duży zabieg operacyjny (w ciągu ostatnich 3 tygodni)
· ostatnio przebyte (w ciągu 2-4 tygodni) krwawienie wewnętrzne
· nakłucia naczyń, których nie można ucisnąć
· w przypadku streptokinazy: wcześniejsze niż przed >5 dniami zastosowanie leku lub
wcześniejsza reakcja alergiczna na te leki
· ciąża lub okres 1 tygodnia po porodzie
· czynny wrzód trawienny
· aktualne stosowanie antykoagulantów doustnych: im większy INR, tym większe
ryzyko krwawienia
· zaawansowana choroba wątroby
· infekcyjne zapalenie wsierdzia

Ocena skuteczności leczenia reperfuzyjnego
· Uzasadnione jest monitorowanie uniesienia ST, rytmu serca i objawów
klinicznych przez 60-180 minut po rozpoczęciu leczenia fibrynolitycznego.
Do objawów wskazujących na reperfuzję, które można ocenić
nieinwazyjnie, należą: ustąpienie dolegliwości, utrzymywanie się lub
powrót stabilności hemodynamicznej lub elektrycznej oraz zmniejszenie o
przynajmniej 50% wyjściowego uniesienia odcinków ST w kontrolnym EKG
po upływie 60-90 minut od rozpoczęcia leczenia [IIa/B].
· Utrzymywanie się niesłabnącego bólu niedokrwiennego w klatce
piersiowej, nieustępowanie charakterystycznego uniesienia odcinków ST
oraz niestabilność hemodynamiczna i(lub) elektryczna służą powszechnie
za wskaźniki nieudanej reperfuzji farmakologicznej i potrzeby rozważenia
ratunkowej PCI. W tym czasie może być konieczne energiczne,
wspomagające leczenie zachowawcze.

Krwawienie śródczaszkowe jako powikłanie leczenia fibrynolitycznego
· Przyjmuje się, że wystąpienie zmian stanu neurologicznego (objawy
takie jak wzrost ciśnienia tętniczego, ból głowy, nudności, wymioty,
zaburzenia świadomości, ogniskowe ubytki neurologiczne, drgawki)
podczas leczenia reperfuzyjnego lub po nim, zwłaszcza w ciągu
pierwszych 24 godzin, jest spowodowane krwawieniem śródczaszkowym,
o ile się nie dowiedzie, iż jest inaczej. Należy wstrzymać leczenie
fibrynolityczne, przeciwpłytkowe i przeciwkrzepliwe, dopóki badanie
obrazowe mózgu nie wykaże, że nie ma krwawienia śródczaszkowego
[I/A].
· U chorych na STEMI, którzy doznali krwawienia śródczaszkowego,
należy uzyskać konsultację neurologiczną i(lub) neurochirurgiczną bądź
hematologiczną, w zależności od okoliczności klinicznych [I/C].

Krwawienie śródczaszkowe jako powikłanie leczenia fibrynolitycznego
· Chorym z krwawieniem śródczaszkowym należy podawać świeżo
mrożone osocze (2 j. [lub 10 j. krioprecypitatu]), protaminę (w celu
zniesienia działania heparyny) lub koncentrat krwinek płytkowych (6-8
j.), w zależności od okoliczności klinicznych [I/C].
· U osób z krwawieniem śródczaszkowym uzasadnione są:
a) optymalizacja ciśnienia tętniczego i glikemii [IIa/C],
b) obniżenie ciśnienia śródczaszkowego
- wlewem mannitolu (bolus 0,5-1,0 g/kg, następnie 0,25 g/kg co 6 h;
osmolalność surowicy 300-310 mOsm) oraz
- poprzez intubację dotchawiczą i hiperwentylację [IIa/C],
c) rozważenie operacyjnego usunięcia krwiaka śródczaszkowego [IIa/C].

Przezskórna interwencja wieńcowa
Koronarografia
· Diagnostyczną koronarografię należy wykonać u:
a) kandydatów do pierwotnej lub ratunkowej PCI [I/A],
b) chorych we wstrząsie kardiogennym, którzy są kandydatami do
rewaskularyzacji [I/A],
c) kandydatów do operacji naprawczej pęknięcia przegrody
międzykomorowej lub dużej niedomykalności zastawki dwudzielnej [I/B],
d) chorych z utrzymującą się niestabilnością hemodynamiczną i(lub)
elektryczną [I/C].
· Nie należy wykonywać koronarografii u pacjentów z zaawansowanymi
chorobami współistniejącymi, u których ryzyko związane z zabiegiem
rewaskularyzacyjnym prawdopodobnie przeważa nad korzyściami [III/C].

Pierwotna PCI
Należy podejmować pierwotną PCI, jeżeli jest ona
bezzwłocznie dostępna, u chorych na STEMI (w tym
zawał tylnej ściany serca) lub z zawałem ze świeżym lub
przypuszczalnie świeżym LBBB, których można poddać
PCI w obrębie tętnicy odpowiedzialnej za zawał w ciągu
12 godzin od wystąpienia objawów, jeżeli zabieg będzie
wykonany w odpowiednich ramach czasowych
(napełnienie balonu w ciągu 90 minut od zgłoszenia się
chorego).

Pierwotna PCI
· Pierwotna PCI jest wskazana w następujących sytuacjach:
a) chory na STEMI niekwalifikujący się do leczenia fibrynolitycznego, który zgłasza się
w ciągu 12 godzin od wystąpienia objawów [I/C];
b) objawy STEMI trwają =<3 godziny i spodziewana różnica między czasem od
przybycia chorego do szpitala do napełniania balonu a czasem od przybycia chorego do
rozpoczęcia leczenia fibrynolitycznego wynosi =<1 godzinę [I/B] (jeśli >1 godzinę, to
na ogół preferuje się leczenie fibrynolityczne [I/B; dotyczy leków swoistych dla fibryny,
takich jak alteplaza]);
c) objawy STEMI trwają >3 godziny, a czas od wezwania pomocy medycznej lub
rozpoczęcia hospitalizacji do napełnienia balonu nie przekroczy 90 minut [I/B];
d) chory z uniesieniem ST lub z LBBB, u którego w ciągu 36 godzin od wystąpienia
zawału rozwija się wstrząs, jeżeli nadaje się do rewaskularyzacji, którą można wykonać
w ciągu 18 godzin od wystąpienia wstrząsu, i zgadza się na leczenie inwazyjne [I/A dla
chorych w wieku <75 lat; IIa/B dla chorych w wieku >=75 lat];
e) chory z ciężką zastoinową niewydolnością serca lub obrzękiem płuc (3 klasa
Killipa), u którego dolegliwości wystąpiły w ciągu ostatnich 12 godzin [I/B];
f) chory, u którego objawy STEMI wystąpiły w ciągu ostatnich 12-24 godzin, w razie co
najmniej jednej z następujących okoliczności:
- ciężka zastoinowa niewydolność serca [IIa/C],
- niestabilność hemodynamiczna lub elektryczna [IIa/C],
- utrzymujące się objawy niedokrwienne [IIa/C].

Pierwotna PCI
· Podczas pierwotnej PCI przeprowadzanej u chorego w stabilnym stanie
hemodynamicznym nie powinno się podejmować PCI w obrębie tętnicy,
która nie jest odpowiedzialna za zawał [III/C].
· U chorych niemających dolegliwości przez >12 godzin od wystąpienia
STEMI nie powinno się przeprowadzać pierwotnej PCI, jeżeli są oni
stabilni hemodynamicznie i elektrycznie [III/C].
· Można rozważyć wykonywanie pierwotnej PCI w szpitalach bez oddziału
kardiochirurgicznego, pod warunkiem że istnieje sprawdzony plan
szybkiego transportu na kardiochirurgiczną salę operacyjną w pobliskim
szpitalu, z zapewnieniem właściwego wsparcia hemodynamicznego
podczas przenoszenia [IIb/B].

Ułatwiona PCI
· Ułatwiona PCI (strategia polegająca na wykonywaniu zaplanowanej
PCI niezwłocznie po wstępnym leczeniu farmakologicznym z
zastosowaniem pełnej dawki leku fibrynolitycznego lub połowy tej dawki
w skojarzeniu z inhibitorem płytkowej glikoproteiny IIb/IIIa) może pełnić
rolę strategii uzyskiwania reperfuzji u chorych obciążonych dużym
ryzykiem, jeżeli nie można przeprowadzić niezwłocznie PCI, a ryzyko
krwawienia jest małe [IIb/B].
Nie zaleca się ułatwionej PCI jako postępowania rutynowego. Obecnie
prowadzone badania dostarczą danych na temat skuteczności,
bezpieczeństwa i opłacalności tej metody, a także optymalnego leczenia
farmakologicznego.

Ratunkowa PCI
· Ratunkowa PCI (czyli zabieg wykonany w ciągu 12 godzin od
nieskutecznego leczenia fibrynolitycznego u chorego z utrzymującym się
lub nawracającym niedokrwieniem mięśnia sercowego) jest wskazana w
następujących sytuacjach:
a) chory z uniesieniem ST lub z LBBB, u którego w ciągu 36 godzin od
wystąpienia zawału rozwija się wstrząs, jeżeli nadaje się do
rewaskularyzacji, którą można wykonać w ciągu 18 godzin od
wystąpienia wstrząsu, i zgadza się na leczenie inwazyjne [I/B dla chorych
w wieku <75 lat; IIa/B dla chorych w wieku >=75 lat],
b) chory z ciężką zastoinową niewydolnością serca lub obrzękiem płuc (3
klasa Killipa), u którego dolegliwości wystąpiły w ciągu ostatnich 12
godzin [I/B],
c) chory, u którego występuje co najmniej jedna z następujących
okoliczności:
- niestabilność hemodynamiczna lub elektryczna [IIa/C],
- utrzymujące się objawy niedokrwienne [IIa/C].

PCI po leczeniu fibrynolitycznym
· PCI po leczeniu fibrynolitycznym jest wskazana w następujących
sytuacjach:
a) istnieją obiektywne dowody na ponowny zawał serca [I/C],
b) wystąpienie umiarkowanego lub nasilonego samoistnego lub
sprowokowanego niedokrwienia mięśnia sercowego w okresie
zdrowienia po STEMI [I/B],
c) wystąpienie wstrząsu kardiogennego lub niestabilności
hemodynamicznej,
d) chory z frakcją wyrzutową lewej komory (LVEF) =<0,40, z zastoinową
niewydolnością serca lub z poważnymi komorowymi zaburzeniami rytmu
[IIa/C],
e) jeśli w ostrej fazie STEMI stwierdzono klinicznie jawną niewydolność
serca (nawet gdy późniejsza ocena wykazuje LVEF >0,40) [IIa/C].

Operacyjne leczenie reperfuzyjne w trybie nagłym lub pilnym
· CABG w pilnym u chorych na STEMI jest wskazane w następujących sytuacjach
(pod warunkiem że stan tętnic wieńcowych pozwala na przeprowadzenie operacji):
a) nieudana PCI z utrzymującym się bólem lub niestabilnością hemodynamiczną
[I/B];
b) utrzymujące się lub nawracające niedokrwienie oporne na leczenie zachowawcze u
chorych ze znacznym obszarem zagrożonego mięśnia sercowego, którzy nie są
kandydatami do PCI ani leczenia fibrynolitycznego [I/B];
c) jednoczasowo z operacją naprawczą pozawałowego pęknięcia przegrody
międzykomorowej lub pozawałowej niedomykalności zastawki dwudzielnej [I/B];
d) wstrząs kardiogenny rozwijający się w ciągu 36 godzin od wystąpienia STEMI (z
uniesieniem ST, z LBBB lub z zawałem tylnej ściany serca) u chorego w wieku <75
lat, mającego nasilone zmiany w wielu naczyniach lub w pniu lewej tętnicy
wieńcowej, jeżeli kwalifikuje się on do rewaskularyzacji, którą można wykonać w
ciągu 18 godzin od wystąpienia wstrząsu, i zgadza się na leczenie inwazyjne [I/A;
IIa/B dla chorych w wieku >=75 lat];
e) zagrażające życiu komorowe zaburzenia rytmu w przypadku zwężenia pnia lewej
tętnicy wieńcowej wynoszącego >=50% lub choroby trójnaczyniowej [I/B];
f) chory we wczesnych godzinach (6-12 h) STEMI, niekwalifikujący się do leczenia
fibrynolitycznego i PCI, zwłaszcza jeśli występuje zaawansowana choroba
wielonaczyniowa lub ciężkie zmiany w pniu lewej tętnicy wieńcowej [IIa/B].
· Nie należy przeprowadzać CABG w trybie nagłym u chorych z utrzymującą się
dławicą piersiową i małym obszarem zagrożonego mięśnia sercowego, jeżeli ich stan
hemodynamiczny jest stabilny [III/C], ani u chorych, u których skutecznie uzyskano
reperfuzję w tętnicach nasierdziowych, lecz nie uzyskano reperfuzji w obrębie
mikrokrążenia [III/C].

Leczenie uzupełniające
Zastosowanie leków antytrombinowych w uzupełnieniu leczenia
reperfuzyjnego
Heparyna niefrakcjonowana
· Heparynę niefrakcjonowaną (HNF) należy podawać dożylnie:
a) chorym poddawanym PCI lub CABG [I/C];
b) chorym poddawanym leczeniu reperfuzyjnemu z użyciem alteplazy
(dawkowanie: wstrzyknięcie 60 j./kg [maks. 4000 j.], następnie wlew ze
wstępną szybkością 12 j./kg/h (maks. 1000 j./h) dostosowaną tak, by aPTT
był 1,5-2,5 razy dłuższy od kontrolnego [ok. 50-70 s]) [I/C];
c) chorym otrzymującym streptokinazę i obciążonym dużym ryzykiem
zatorowości w dużym krążeniu (związanym z rozległym zawałem lub
zawałem ściany przedniej, migotaniem przedsionków, wcześniej przebytą
zatorowością lub stwierdzonym zakrzepem w lewej komorze) [I/B].
· U chorych otrzymujących HNF należy codziennie sprawdzać liczbę płytek
krwi [I/C].
· Zalecana dawka HNF dostosowywana do masy ciała, jeżeli stosuje się ją
bez leku fibrynolitycznego, wynosi 60-70 j./kg i.v. we wstrzyknięciu, a
następnie 12-15 j./kg/h we wlewie.
Heparyna drobnocząsteczkowa
· Można rozważyć zastosowanie heparyny drobnocząsteczkowej (HDCz)
zamiast HNF w leczeniu uzupełniającym u chorych w wieku <75 lat, którzy
otrzymują leczenie fibrynolityczne, pod warunkiem że nie występuje istotne
upośledzenie czynności nerek (stężenie kreatyniny w surowicy do 2,5 mg/dl
u mężczyzn i 2,0 mg/dl u kobiet) [IIb/B].

Uważa się obecnie, że stosowanie heparyny razem z SK nie jest konieczne. U
chorych leczonych t-PA stosuje się heparynę dożylnie 5000 j. jako dawkę wstępną, a
następnie około 1000 j./godz. pod kontrolą APTT jako profilaktykę reokluzji - przez
24-48 godz. Wskazaniem do podawania heparyny w zawale serca są:
• nawracające niedokrwienie;
• profilaktyka zatorowości:
• skrzeplina wewnątrzsercowa zwłaszcza grożąca uruchomieniem;
• migotanie przedsionków;
• zakrzepica żylna;
• przedłużające się unieruchomienie chorego.
Leczenie powikłań krwotocznych po leczeniu trombolitycznym
• Małe krwawienia w miejscu wkłuć dają się opanować uciskiem - bez przerywania
leczenia trombolitycznego.
• Wobec istotnego krwawienia: przerwać podawanie leku trombolitycznego,
heparyny i aspiryny.
• Przy ciężkim krwawieniu u chorego otrzymującego heparynę, podać siarczan
protaminy w dawce 1 mg na 100 j. heparyny podanej w ciągu ostatnich 4 godzin
(najwyższa dawka jednorazowa 50 mg).
• Obniżenie hematokrytu poniżej 30% jest wskazaniem do przetoczenia krwi.
• Przy ciężkich krwawieniach lekiem z wyboru jest krioprecypitat w dawce 10 j.,
który zawiera fibrynogen i czynnik VIII. Dawka wstępna może być powtarzana.
• Wskazane jest przetaczanie mrożonego osocza 20 ml/kg lub koncentratu
czynników zespołu protrombiny 20 j. czynnika IX/kg masy ciała.

2.3.7. Leczenie uzupełniające
Leki przeciwpłytkowe
ASA
· ASA (w dawce początkowej 150-325 mg p.o. i podtrzymującej 75-160 mg) należy
stosować codziennie do końca życia u wszystkich chorych po STEMI bez
nadwrażliwości na ten lek [I/A].
Leki przeciwpłytkowe (Tienopirydyny) – hamują agregację płytek
· U chorych poddanych diagnostycznemu cewnikowaniu serca, u których planuje się
PCI, należy rozpocząć leczenie klopidogrelem
· U chorych otrzymujących klopidogrel, u których planuje się CABG, należy zaprzestać
stosowania tego leku na co najmniej 5, a najlepiej 7 dni przed zabiegiem, chyba że
korzyści z pilnej rewaskularyzacji przewyższają zagrożenia związane z nadmiernym
krwawieniem [I/B].
· Klopidogrel jest prawdopodobnie wskazany u chorych poddanych leczeniu
fibrynolitycznemu, którym nie można podać ASA ze względu na nadwrażliwość lub
znaczną nietolerancję ze strony przewodu pokarmowego [IIa/C].
· Tiklopidyna może wywołać neutropenię i małopłytkowość zakrzepową, natomiast
klopidogrel rzadziej wywołuje efekty uboczne i nie wymaga laboratoryjnego
monitorowania leczenia, a ponadto przyjmuje się go raz dziennie, dlatego też jest
preferowany.
Leki blokujące ptkowy receptor IIb/IIIa
· U chorych na STEMI uzasadnione jest jak najwcześniejsze rozpoczęcie leczenia
abciksymabem przed pierwotną PCI (z wszczepieniem stentu lub bez) [IIa/B].

2.3.7. Leczenie uzupełniające
Inne metody leczenia farmakologicznego
Hamowanie układu renina-angiotensyna-aldosteron
· Wszystkim chorym na STEMI z zawałem ściany przedniej, z zastojem w krążeniu płucnym
lub z LVEF <0,40 należy w ciągu pierwszych 24 godzin podać doustnie inhibitor ACE,
jeżeli nie ma hipotonii (skurczowe ciśnienie tętnicze <100 mm Hg lub obniżone o >30
mm Hg w odniesieniu do wartości wyjściowej) lub znanych przeciwwskazań do
stosowania tej grupy leków.
Inhibitory konwertazy angiotensyny powodują rozszerzenie naczyniowego układu
tętniczego (z redukcją oporu obwodowego) oraz żylnego, z następowym obniżeniem
obciążenia wstępnego i następczego serca - z redukcją objętości późnokurczowej i
ciśnienia napełniania lewej komory u chorych z niewydolnością serca (z podwyższeniem
rzutu serca).
Wskazania: niewydolność lewej komory w przebiegu zawału serca, dysfunkcja lewej
komory z obniżeniem frakcji wyrzucania, rozległy zawał serca, nadciśnienie w przebiegu
zawału.
Przeciwwskazania: wstrząs i skurczowe ciśnienie tętnicze poniżej 100 mmHg, neutropenia,
zwężenie zastawki aortalnej i mitralnej, kardiomiopatia przerostowa, nadwrażliwość na
lek, ciężkie zaburzenia i niewydolność wątroby, ciąża. Obowiązuje ostrożność w
stosowaniu tych leków w niewydolności nerek.
Dawkowanie: kaptopryl należy podawać w dawce wstępnej 6,25 mg, a następnie w
dawkach wzrastających, do dwóch-trzech razy dziennie 25-50 mg. Enalapril - w dawce
wstępnej 2,5 mg, stopniowo podwyższając dawkę do 2x2,5-5 mg bądź 1x10 mg.
Uwzględniając podane wskazania zaleca się wczesne stosowanie leków z grupy IKA,
rozpoczynając od bardzo małych dawek w celu uniknięcia niepożądanej hipotensji.

2.3.7. Leczenie uzupełniające
Inne metody leczenia farmakologicznego
Ścisła kontrola glikemii podczas STEMI
· We wczesnej fazie STEMI z hiperglikemią (pierwsze 24-48 godzin)
uzasadniony jest wlew insuliny w celu normalizacji glikemii [I/B dla
chorych z zawałem powikłanym; IIa/B dla chorych z zawałem
niepowikłanym].
Magnez
· Uzasadnione jest uzupełnianie udokumentowanego niedoboru magnezu,
zwłaszcza u chorych otrzymujących leki moczopędne przed wystąpieniem
STEMI [IIa/C].
· Uzasadnione jest leczenie epizodów częstoskurczu komorowego typu
torsade de pointes związanych z wydłużeniem odstępu QT siarczanem
magnezu w dawce 1-2 g podawanej we wstrzyknięciu dożylnym trwającym
>5 minut [IIa/C].

2.3.7. Leczenie uzupełniające
Inne metody leczenia farmakologicznego
Blokery kanału wapniowego
· Uzasadnione jest podawanie werapamilu lub diltiazemu chorych, u
których beta-blokery są nieskuteczne lub przeciwwskazane (np. z powodu
stanów bronchospastycznych), w celu złagodzenia utrzymującego się
niedokrwienia mięśnia sercowego lub zwolnienia szybkiego rytmu komór
w przebiegu migotania lub trzepotania przedsionków po STEMI, jeżeli nie
występuje zastoinowa niewydolność serca, dysfunkcja lewej komory ani
blok przedsionkowo-komorowy [IIa/C].
· Diltiazem i werapamil są przeciwwskazane u chorych na STEMI z
towarzyszącą dysfunkcją lewej komory lub zastoinową niewydolnością
serca [III/A].
· Nifedypina (w postaci preparatu o natychmiastowym uwalnianiu) jest
przeciwwskazana w leczeniu STEMI ze względu na związane z jej
stosowaniem odruchowe pobudzenie układu współczulnego, tachykardię i
hipotonię [III/B].

Zaburzenia hemodynamiczne
Hipotonia
· Chorym bez klinicznych objawów przeciążenia płynami należy szybko
podać płyny we wlewie dożylnym [I/C].
· Należy skorygować zaburzenia rytmu i przewodzenia powodujące
hipotonię [I/C].
· Należy zastosować balonową kontrapulsację wewnątrzaortalną u
chorych, których stan się nie poprawia po zastosowanym leczeniu
· Jeżeli hipotonia nie ustępuje po obciążeniu płynami, należy zastosować
leki obkurczające naczynia [I/C].
· Do oceny powikłań mechanicznych należy wykorzystać
echokardiografię, jeśli nie ocenia się ich metodami inwazyjnymi [I/C].

Zaburzenia hemodynamiczne
Mały rzut serca
Jeśli do oceny lewej komory i przypuszczalnego powikłania mechanicznego nie
zastosowano metod inwazyjnych, to należy do tego celu wykorzystać
echokardiografię [I/C].
Zalecane leczenie stanów małego rzutu minutowego obejmuje:
1- stosowanie leków inotropowych [I/B]:
- gdy ciśnienie tętnicze skurczowe wynosi 70-100 mm Hg i nie ma objawów
wstrząsu, podaje się
dobutaminę 2-20 µg/kg/min i.v.,
- gdy ciśnienie tętnicze skurczowe wynosi 70-100 mm Hg i występują
objawy wstrząsu, podaje
się dopaminę 5-15 µg/kg/min i.v.,
- gdy ciśnienie tętnicze skurczowe wynosi <70 mm Hg, podaje się
noradrenalinę 0,5-30 µg/min
2- kontrapulsację wewnątrzaortalną [I/B],
3- reperfuzję mechaniczną za pomocą PCI lub CABG [I/B],
4- operację naprawczą powikłań mechanicznych [I/B].
Chorym z małym rzutem serca wskutek niewydolności serca jako pompy nie
należy podawać beta-blokerów i antagonistów wapnia [III/B].

Zaburzenia hemodynamiczne
Zastój w krążeniu płucnym
Doraźne cele leczenia to:
- odpowiednie nasycenie tlenem
- zmniejszenie obciążenia wstępnego w celu
usunięcia zastoju w krążeniu płucnym.

Zaburzenia hemodynamiczne
Zastój w krążeniu płucnym
Ze względu na pobudzenie układu współczulnego ciśnienie tętnicze podczas
obrzęku płuc zazwyczaj jest podwyższone.
Chorzy wykazujący tę właściwą reakcję zazwyczaj dobrze znoszą niezbędne leki,
spośród których wszystkie obniżają ciśnienie tętnicze.
Wskutek stosowania jednocześnie kilku leków wywołujących hipotonię może
dojść do jatrogennego wstrząsu kardiogennego, uruchamiającego błędne koło
hipoperfuzji i niedokrwienia.
Jeżeli ostremu obrzękowi płuc nie towarzyszy wzrost ciśnienia tętniczego w
dużym krążeniu, trzeba podejrzewać zagrażający wstrząs kardiogenny.
Jeżeli obrzękowi płuc towarzyszy hipotonia, rozpoznaje się wstrząs kardiogenny.
Tacy chorzy często wymagają wspomagania krążenia lekami inotropowymi i
obkurczającymi naczynia i(lub) balonową kontrapulsacją wewnąrzaortalną w celu
zmniejszenia zastoju w krążeniu płucnym i utrzymania wystarczającego przepływu
tkankowego.

Zaburzenia hemodynamiczne
Zastój w krążeniu płucnym
· U chorych z zastojem w krążeniu
płucnym należy w trybie pilnym
wykonać echokardiografię, aby ocenić
czynność prawej i lewej komory i
wykluczyć powikłania mechaniczne
[I/C].

Zaburzenia hemodynamiczne
3.5.4. Zastój w krążeniu płucnym
· U chorych z zastojem w krążeniu płucnym wskazane jest podawanie:
- tlenu, tak aby SaO2 wynosiło >90% [I/C],
- siarczanu morfiny [I/C],
- inhibitora ACE (rozpoczynając od leku krótko działającego w małej
dawce początkowej, np. 1-6,25 mg kaptoprylu)* [I/A],
- azotanu* [I/C],
- leku moczopędnego (furosemidu w małej lub średniej dawce) w razie
przeciążenia płynami (należy zachować ostrożność u chorych, którzy nie
otrzymują płynów w celu zwiększenia objętości wewnątrznaczyniowej)
[I/C]
* Jeżeli ciśnienie tętnicze wynosi >=100 mm Hg lub nie spadło bardziej
niż o 30 mm Hg poniżej wartości wyjściowej. Chorzy z zastojem w
krążeniu płucnym i granicznym lub niskim ciśnieniem tętniczym często
wymagają wspomagania krążenia lekami inotropowymi i obkurczającymi
naczynia i(lub) balonową kontrapulsacją wewnątrzaortalną w celu
zmniejszenia zastoju w krążeniu płucnym i utrzymania wystarczającego
przepływu krwi.

Zaburzenia hemodynamiczne
Wstrząs kardiogenny
· Jeśli u chorych na STEMI wstrząs kardiogenny nie ustępuje szybko pod
wpływem leczenia farmakologicznego, zaleca się balonową kontrapulsację
wewnątrzaortalną. Jest to metoda stabilizowania stanu chorych do czasu
wykonania angiografii i szybkiej rewaskularyzacji [I/B].
· Wczesną rewaskularyzację (PCI lub CABG) zaleca się u chorych z uniesieniem
ST lub LBBB, u których w ciągu 36 godzin od wystąpienia zawału serca rozwija
się wstrząs, jeżeli nadają się oni do rewaskularyzacji, którą można wykonać w
ciągu 18 godzin od wystąpienia wstrząsu, i chory zgadza się na leczenie
inwazyjne.
· U chorych na STEMI we wstrząsie kardiogennym, którzy nie kwalifikują się do
dalszego leczenia inwazyjnego, należy zastosować leczenie fibrynolityczne, jeżeli
nie występują przeciwwskazania [I/B].
· Do oceny mechanicznych powikłań należy wykorzystać echokardiografię, jeśli
nie zastosowano do tego celu metod inwazyjnych [I/C].

Zaburzenia hemodynamiczne
Zawał prawej komory
· U chorych na STEMI ściany dolnej z upośledzeniem stanu hemodynamicznego
należy ocenić prawostronne odprowadzenie przedsercowe V4R, aby wykryć
uniesienie odcinka ST oraz echokardiogram, by rozpoznać zawał prawej komory
[I/B].
· U chorych na STEMI z zawałem i niedokrwienną dysfunkcją prawej komory
należy:
- w miarę możliwości wcześnie uzyskać reperfuzję [I/C];
- zapewnić synchroniczną czynność przedsionków i komór oraz opanować
bradykardię [I/C];
- wyrównać obciążenie wstępne prawej komory, co zwykle wymaga początkowego
obciążenia płynami u chorych z niestabilnością hemodynamiczną, pod warunkiem że
ciśnienie w żyłach szyjnych jest prawidłowe lub małe [I/C];
- dążyć do normalizacji obciążenia następczego prawej komory, co zwykle wymaga
leczenia współistniejącej dysfunkcji lewej komory [I/C];
- zastosować leki inotropowe w razie niestabilności hemodynamicznej niereagującej
na obciążenie płynami [I/C].
· Po zawale serca, który doprowadził do klinicznie istotnej dysfunkcji prawej
komory, uzasadnione jest odroczenie CABG o 4 tygodnie, aby umożliwić powrót jej
kurczliwości [IIa/C].

Zaburzenia rytmu po STEMI
Komorowe zaburzenia rytmu
· Nie jest wskazane rutynowe zapobiegawcze stosowanie leków antyarytmicznych
(np. lidokainy) w celu tłumienia pojedynczych przedwczesnych pobudzeń
komorowych, par, wstawek przyspieszonego rytmu idiowentrykularnego lub
nietrwałego częstoskurczu komorowego [III/B]. Leczenie wskazane jest wówczas,
gdy arytmia powoduje upośledzenie stanu hemodynamicznego.
Migotanie komór
· Migotanie komór lub częstoskurcz komorowy bez tętna należy leczyć
niezsynchronizowanym wyładowaniem prądu elektrycznego o energii pierwszego
wyładowania jednofazowego 200 J; w razie jego nieskuteczności należy zastosować
drugie wyładowanie - 200-300 J, a w razie potrzeby trzecie - 360 J [I/B].
· Uzasadnione jest leczenie migotania komór lub częstoskurczu komorowego bez
tętna, opornych na wyładowanie elektryczne, amiodaronem (300 mg lub 5 mg/kg we
wstrzyknięciu i.v.), z następczym powtórzeniem niezsynchronizowanego
wyładowania elektrycznego [I/B].
· Należy korygować zaburzeni elektrolitowe i kwasowo-zasadowe (aby stężenie
potasu wynosiło >4,0 mmol/l, a magnezu >2,0 mg/dl) w celu zapobiegania
nawrotom migotania komór po opanowaniu pierwszego epizodu [I/C].

Zaburzenia rytmu po STEMI
Częstoskurcz komorowy wielokształtny
· Trwały (trwający >30 s lub powodujący załamanie
hemodynamiczne) wielokształtny częstoskurcz komorowy
należy leczyć defibrylacją z pierwszym wyładowaniem
jednofazowym o energii 200 J; w razie jego nieskuteczności
drugim - 200-300 J, a gdy jest to konieczne trzecim - 360 J [I/B].

Zaburzenia rytmu po STEMI
Częstoskurcz komorowy jednokształtny
· Epizody trwałego jednokształtnego częstoskurczu komorowego z towarzyszącą
dławicą piersiową, obrzękiem płuc lub hipotonią (ciśnieniem tętniczym <90 mm
Hg) należy leczyć zsynchronizowanym wyładowaniem elektrycznym o energii
pierwszego wyładowania jednofazowego 100 J. W razie jego nieskuteczności
można stosować wyładowania o większej energii. Pożądane jest krótkotrwałe
znieczulenie ogólne, jeżeli nie powoduje istotnych zaburzeń hemodynamicznych.
[I/B]
· Trwały jednokształtny częstoskurcz komorowy bez towarzyszącej dławicy
piersiowej, obrzęku płuc lub hipotonii (ciśnienie tętnicze 90 mm Hg) należy
leczyć:
- amiodaronem: wlew 150 mg w ciągu 10 minut (lub 5 mg/kg), w razie potrzeby
powtarzany co 10-15 minut; alternatywnie wlew 360 mg przez 6 godzin (1
mg/min), a następnie 540 mg przez kolejne 18 godzin (0,5 mg/min); całkowita
dawka z uwzględnieniem dodatkowych dawek podawanych podczas zatrzymania
czynności serca nie powinna przekraczać 2,2 g w ciągu 24 godzin [I/B];
- zsynchronizowaną kardiowersją elektryczną, rozpoczynając od wyładowania
jednofazowego o energii 50 J (konieczne jest krótkotrwałe znieczulenie ogólne)
[I/B];

3.6. Zaburzenia rytmu po STEMI
3.6.2. Arytmie nadkomorowe, w tym migotanie przedsionków
· Trwałe migotanie lub trzepotanie przedsionków u chorych z
upośledzeniem stanu hemodynamicznego lub z utrzymującym się
niedokrwieniem serca należy leczyć co najmniej jedną z następujących
metod:
- zsynchronizowaną kardiowersją z pierwszym wyładowaniem
jednofazowym o energii 200 J w przypadku migotania przedsionków i 50 J
w przypadku trzepotania przedsionków, poprzedzoną - jeżeli tylko jest to
możliwe - krótkotrwałym znieczuleniem ogólnym lub sedacją z
zachowaniem przytomności [I/C];
- w epizodach migotania przedsionków niereagujących na kardiowersję
elektryczną lub nawracających po krótkim okresie rytmu zatokowego
wskazane jest leczenie antyarytmiczne zwalniające odpowiedź komór.
Można w tym celu zastosować dożylnie amiodaron [I/C] lub digoksynę
(głównie w celu zwolnienia czynności komór u chorych z ciężką dysfunkcją
lewej komory i niewydolnością serca) [I/C].

3.6. Zaburzenia rytmu po STEMI
3.6.2. Arytmie nadkomorowe, w tym migotanie przedsionków
· Trwałe migotanie lub trzepotanie przedsionków u chorych z utrzymującym się
niedokrwieniem, lecz bez pogorszenia stanu hemodynamicznego należy leczyć,
stosując:
- beta-bloker (jeśli nie ma przeciwwskazań; metoda preferowana) [I/C],
- diltiazem lub werapamil dożylnie [I/C],
- zsynchronizowaną kardiowersję z pierwszym wyładowaniem jednofazowym o
energii 200 J w przypadku migotania przedsionków i 50 J w przypadku trzepotania
przedsionków, poprzedzoną - jeżeli tylko jest to możliwe - krótkotrwałym
znieczuleniem ogólnym lub podaniem leku sedatywnego niezaburzającego
świadomości [I/C].
· Podczas epizodów trwałego migotania lub trzepotania przedsionków bez
pogorszenia stanu hemodynamicznego lub niedokrwienia wskazane jest
kontrolowanie częstotliwości rytmu komór.
Ponadto u osób z trwałym migotaniem lub trzepotaniem przedsionków należy
stosować leczenie przeciwkrzepliwe.
U chorych, u których migotanie lub trzepotanie przedsionków wystąpiło przed
STEMI, należy rozważyć kardiowersję przywracającą rytm zatokowy [I/C].

3.6. Zaburzenia rytmu po STEMI
· Napadowy nawrotny częstoskurcz nadkomorowy należy ze względu na
szybki rytm leczyć, stosując kolejno:
- masaż zatoki tętnicy szyjnej [I/C],
- adenozynę (jednorazowo 6 mg i.v. w ciągu 1-2 minut; jeżeli nie ma
reakcji, można podać 12 mg i.v. po upływie 1-2 minut, a w razie
konieczności podać jeszcze raz dawkę 12 mg) [I/C],
-metoprolol (2,5-5,0 mg i.v. co 2-5 minut do łącznej dawki 15 mg w ciągu
10-15 minut) lub atenolol (2,5-5,0 mg i.v. przez 2 minuty do łącznej dawki
10 mg w ciągu 10-15 minut) [I/C],
-- diltiazem (20 mg [0,25 mg/kg] i.v. w ciągu 2 minut, a następnie wlew z
szybkością 10 mg/h) [I/C],
-- digoksynę (8-15 g/kg [0,6-1,0 mg u osoby o mc. 70 kg] i.v.; trzeba
pamiętać, że efekt farmakologiczny pojawia się z co najmniej godzinnym
opóźnieniem) [I/C].
· Leczenie przedwczesnych pobudzeń przedsionkowych nie jest wskazane
[III/C].

Doraźne leczenie zaburzeń przewodzenia i bradyarytmii
· W przypadku asystolii komór należy szybko podjąć czynności
resuscytacyjne, obejmujące uciskanie klatki piersiowej oraz stosowanie
atropiny, wazopresyny, adrenaliny i czasowej elektrostymulacji serca
[I/B].
Dysfunkcja węzła zatokowego po STEMI
- Objawową bradykardię zatokową, przerwy rytmu zatokowego trwające
>3 sekundy lub bradykardię zatokową z częstotliwością rytmu serca
<40/min, której towarzyszą hipotonia i objawy upośledzenia
hemodynamicznego w obrębie dużego krążenia, należy leczyć atropiną
we wstrzyknięciu dożylnym w dawce 0,6-1,0 mg.
- Jeżeli bradykardia się utrzymuje, a podano maksymalną całkowitą
dawkę atropiny (2 mg), należy wdrożyć czasową elektrostymulację
przezskórną lub przezżylną (najlepiej przedsionkową). [I/C]
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
Wyszukiwarka
Podobne podstrony:
zawał mięśnia sercowego, Pozostałe Medyczne, Anatomia ogólnie
Zawał mięśnia sercowego, Studia - ratownictwo medyczne, 3 rok, Zawansowane procedury ratunkowe
zawal miesnia sercowego postepowanie
wykład zawał mięśnia sercowego
Prezentacja zawał mięśnia sercowego
ZAWAŁ MIĘŚNIA SERCOWEGO
Zawał mięśnia sercowego, Fizjoterapia, . fizjoterapia
Zawał mięśnia sercowego(1), Pielęgniarstwo
Zawal miesnia sercowego, studia, I rok, patofizjologia
W Zawał mięśnia sercowego czynność mechan, Medycyna Ratunkowa - Ratownictwo Medyczne
Zawal miesnia sercowego, studia, I rok, patofizjologia
Zawał mięśnia sercowego1, Studia - ratownictwo medyczne, 3 rok, Zawansowane procedury ratunkowe
MR Zawał mięśnia sercowego
zawał mięśnia sercowego, Materiały 2 rok Fizjoterapi, Patologia
Zawal miesnia sercowego
więcej podobnych podstron