
Badanie właściwości monosacharydów, disacharydów i
polisacharydów
Reakcje charakterystyczne
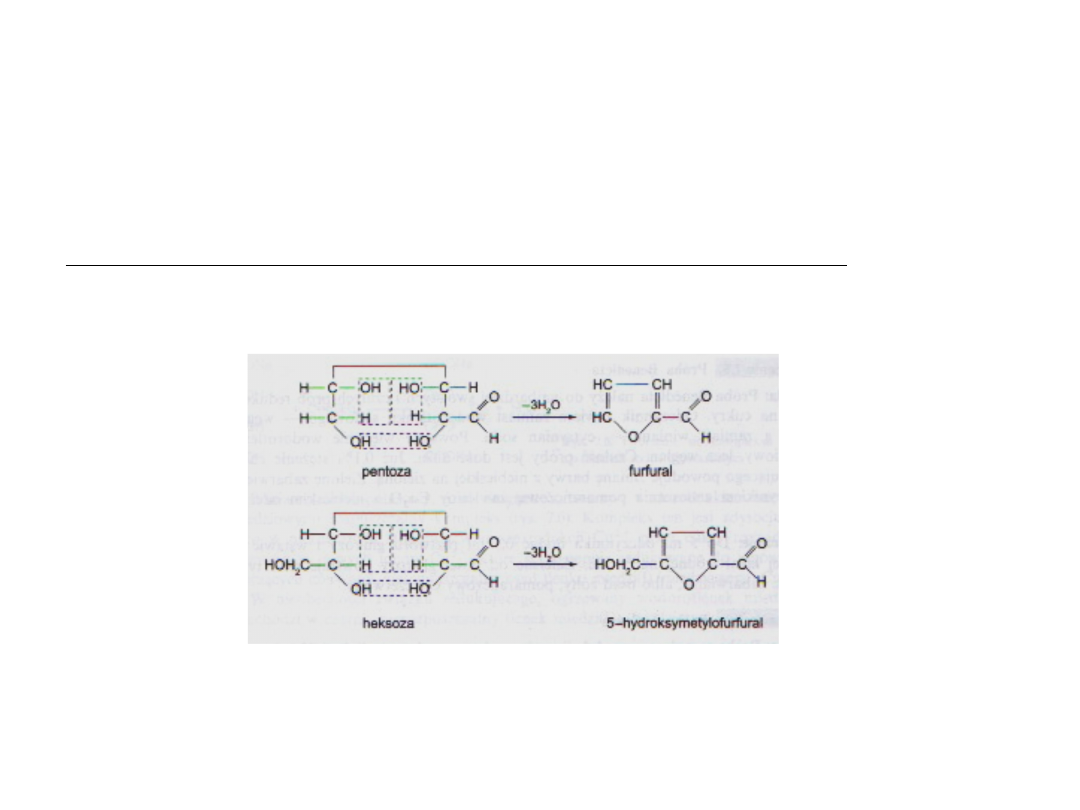
Furfural i 5-
hydroksymetylofurfural
Cukry proste (monosacharydy) , zarowno aldozy jak i ketozy ,
ogrzewane ze stężonymi kwasami solnym lub siarkowym ulegają
odwodnieniu do cyklicznych aldehydow , przy czym z pentoz powstaje
furfural (aldehyd furylowy) natomiast z heksoz 5-
hydroksymetylofurfural (aldehyd 5-hydroksymetylofurylowy)
Furfural oraz 5-hydroksymetylenofurfural mogą kondensować z fenolami i aminami
aromatycznymi lub ich pochodnymi takimi jak a -naftol, antron i tymol oraz floroglucyna,
orcyna i rezorcyna.

Reakcja Molischa z a -
naftolem
Zasada: jest to najbardziej ogolna reakcja na cukry zarowno
wolne jak i związane. Ujemny jej wynik wyklucza obecność
cukru, dodatni zaś nie zawsze jest wystarczający do jego
stwierdzenie ponieważ podobną reakcję dają np. aldehydy
,acetony .Zasada proby polega na powstaniu
czerwonofioletowego zabarwienia w wyniku kondensacji
pochodnych furfuralowych z a - naftolem.
Do roztworu glukozy dodać 1-2 kropli świeżo sporządzonego 10%
etanolowego roztworu a -naftolu. Po dokładnym zmieszaniu , bardzo
ostrożnie! po ściance probowki wprowadzić 1 ml stężonego
roztworu H2SO4 tak, aby była widoczna granica między cieczami. W
miejscu zetknięcia się obu cieczy powstaje czerwono-fioletowy
pierścień. Pierścień zielony określa negatywną reakcję
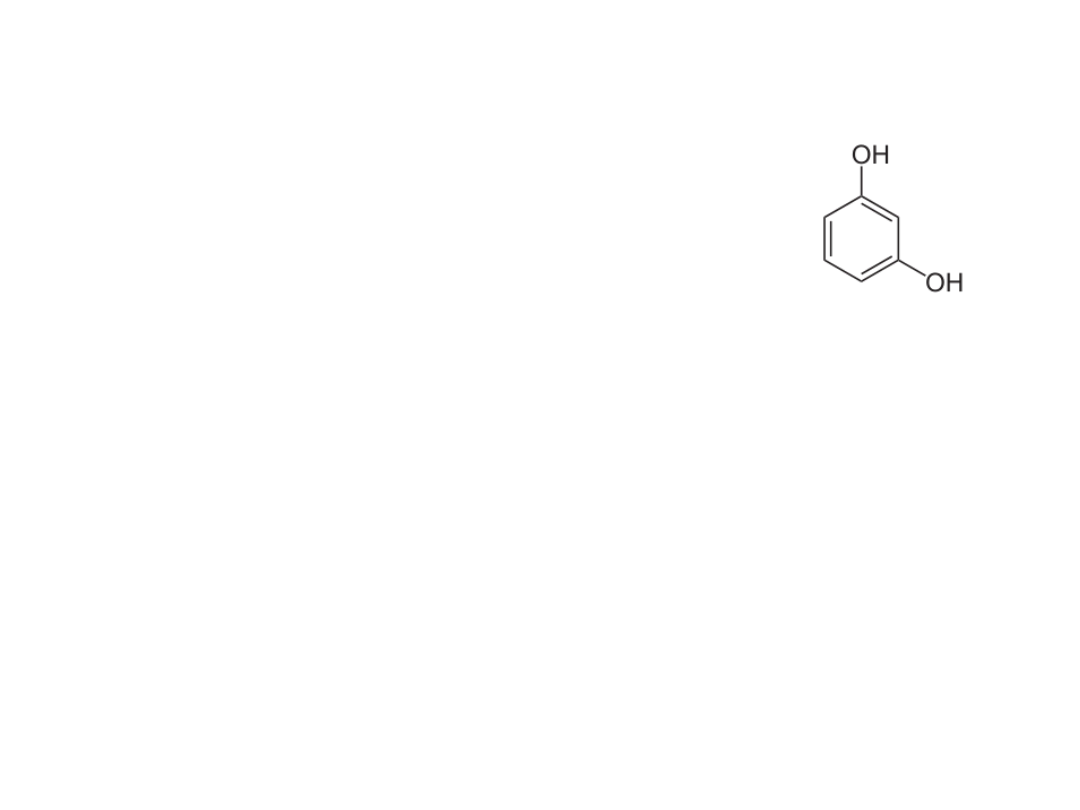
Reakcja Seliwanowa z rezorcyną na
ketozy
Zasada: W reakcji tej barwny związek z rezorcyną daje
hydroksymetylofurfural, powstający dużo łatwiej z ketoz niż z
aldoz pod wpływem działania kwasu solnego. Proba ta pozwala
więc na odrożnienie ketoz od aldoz ponieważ w obecności
rozcieńczonego roztworu HCL tylko ketozy ulegają odwodnieniu w
czasie ogrzewania w temp.100C przez 30 sekund
W obecności ketozy w ciągu 30 sekund powstaje
czerwone zabarwienie. Roztwory aldoz krotko
ogrzewane nie ulegają zabarwieniu. Zabarwienie może
wystąpić po dłuższym ogrzewaniu .

Wykrywanie pentoz: próba
Biala
Zasada: W obecności soli żelaza (III) furfural powstający z
rybozy w środowisku HCl daje z orcyną kompleks o barwie
zielonej

Reakcje redukcyjne
W środowisku zasadowym formy pierścieniowe cukrow
przekształcają się w formy łańcuchowe z odtworzeniem wolnych
grup aldehydowych lub ketonowych. Grupy te nadają cząsteczkom
cukru własności redukcyjne. Aktywna w tych warunkach forma
aldehydowa lub ketonowa redukuje niektore jony metali ciężkich
Szczegolnie łatwo redukują jony metali takich jak : Cu+2, Bi+2,
Ag+1.

Reakcja Trommera
Zasada: Proba ta polega na redukcji przez cukier jonu miedzi Cu+2 do Cu+1
Przebiega ona w
podwyższonej temperaturze w środowisku alkalicznym. Jeżeli ogrzewamy
wodorotlenek miedzi w roztworze alkalicznym to przechodzi on w czarny
nierozpuszczalny tlenek miedzi (II) zgodnie z
reakcją:
CuSO4 + 2NaOH Cu(OH)2 + Na2SO4
Cu(OH)2 CuO + H2O
czarny osad
W obecności cukru-związku redukującego reakcja ta przebiega odmiennie:
2Cu(OH)2 Cu2O + 2H2O + 1/2O2
osad czerwony
Powstają nierozpuszczalne kryształki tlenku miedzi (I) , ktore w zależności od
swojej wielkości
posiadają barwę od żołtej przez pomarańczową do czerwonej. Reakcja ta jest
bardzo czuła i pozwala wykryć nawet ślady cukrow.

Reakcja Fehlinga
Zasada: jest to zmodyfikowana reakcja Trommera, w ktorej
zastosowano winian sodowo-potasowy (sol Seignetta) jako odczynnik
zapobiegający wytrącaniu się jonow Cu+2. tworzy on z jonami Cu+2sol
kompleksową. W ten sposob nadmiar nie zredukowanych jonow Cu+2
pozostaje w roztworze nie przechodząc w czarny tlenek miedzi (II) CuO.
Dalszy przebieg reakcji jest identyczny jak w przypadku reakcji
Trommera.

Próba Benedicta
Zasada: Podobnie jak w probach Tromera i Fehlinga w tej
reakcji redukcji ulegają jony Cu+2 do Cu+1 pod wpływem
cukru. Odczynnikiem utrzymującym jony Cu+2 w roztworze jest
cytrynian sodowy ,pełniący rolę soli Seignetta

Reakcja Tollensa
Zasada:Redukcja soli srebra do srebra metalicznego w środowisku
alkalicznym , w obecności wolnych grup aldehydowych lub
ketonowych cukrow. Reakcja przebiega następująco:
AgNO3 + NH4OH AgOH + NH4NO3
AgOH + 2NH3 Ag(NH3)2OH
2Ag(NH3)2OH + R-CHO 2Ag + R- COONH4 + NH3 + H2O
Po około 10 minutach wydzieli się na ścianach probówki
metaliczne srebro w postaci lustra.

Disacharydy
Disacharydy (dwucukry) składają się z dwoch cząsteczek cukrow prostych
połączonych wiązaniem o- glikozydowym. Wiązanie glikozydowe nie
odznacza się dużą trwałością szczegolnie w obecności jonow wodorowych.
Hydrolizę wiązania glikozydowego można bardzo łatwo przeprowadzić pod
wpływem kwasow, lub enzymatycznie. Enzymy katalizujące tę reakcje
odznaczają się dużą specyficznością działania , zależną nie tylko od rodzaju
składnikow ale i rownież od typu wiązania glikozydowego ( a i b ).
Hydroliza kwaśna (w obecności stężonego H2SO4) lub enzymatyczna (za
pomocą inwertazy) następuje rozpad na glukozę i fruktozę

Wielocukry
Polisacharydy (wielocukry) należą do związkow organicznych najobficiej
występujących w
przyrodzie. Są one produktami polikondensacji monosacharydow połączonych
wiązaniami
glikozydowymi.
Ze względu na budowę chemiczną polisachrydy można podzielić na
homoglikany (jednoskładnikowe: np. skrobia, glikogen, celuloza) i
heteroglikny (wieloskładnikowe: np. chondroityna, heparyna, kwas
hialuronowy).
Roślinną substancja zapasową jest skrobia składająca się z amylozy i
amylopektyny. Zarowno amylopektyna jak i amyloza są hydrolizowane przez
a -amylazę wydzielaną przez gruczoły ślinowe i przez trzustkę.
Komórki zwierzęce magazynują glukozę w postaci glikogenu.
Bardzo ważnym polisacharydem roślinnym jest celuloza pełniąca funkcje
strukturalne , a nie
odżywcze. Jest ona nie rozgałęzionym polimerem reszt glukozy , połączonych
wiązaniami b -1,4-
glikozydowymi. Konfiguracja b pozwala celulozie na tworzenie bardzo
długich , prostych
łańcuchów.
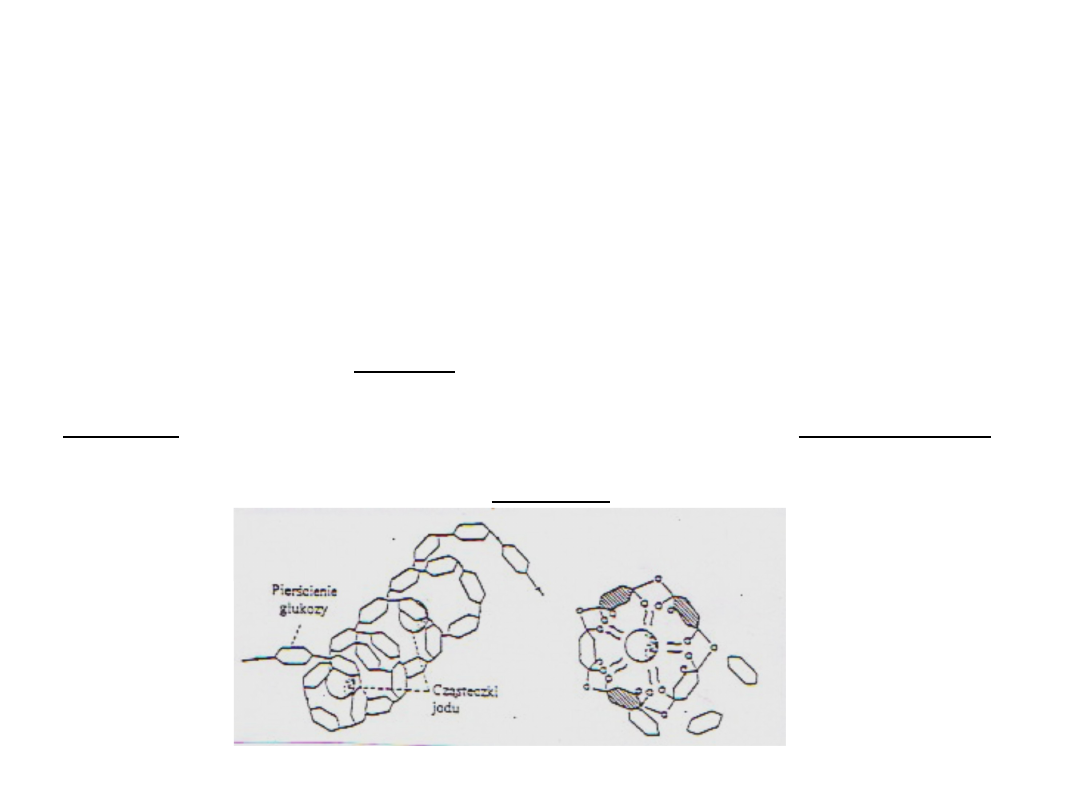
Reakcja wielocukrów z
jodem
Zasada: Cząsteczki jodu wchodzą „do kanału” utworzonego przez
spiralnie skręcone łańcuchy polisacharydu i są „przytrzymywane”
przez tlen przy pierwszym i czwartym atomie węgla każdej cząsteczki
glukozy . Wytwarza się więc łańcuch drobin jodu , wzdłuż ktorego
mogą przesuwać się elektrony , co powoduje pochłanianie światła
przez cały kompleks. Skrobia na wskutek adsorbcji cząstek jodu
barwi się na kolor niebieski.
Amyloza daje z jodem zabarwienie niebieskie, zaś amylopektyna -
fioletowe. Amyloza o konfiguracji liniowej nie jest zdolna do
tworzenia kompleksu z jodem . Glikogen daje zabarwienie jasno-
czerwonobrunatne
Hydroliza kwaśna skrobi
Zasada: skrobia pod wpływem kwasow lub enzymow (a i b
amylazy) ulega hydrolizie do dwucukru maltozy poprzez stadium
dekstryn.
Skrobia skrobia rozpuszczalna dekstryny maltoza
W czasie hydrolizy skrobi tworzą się najpierw dekstryny o dużej
cząsteczce – amylodekstryny (zabarwienie z jodem -fioletowe),
ktore ulegają dalszemu rozkładowi na erytrodekstryny
(zabarwienie z jodem- czerwone).
Powstałe przy dalszej hydrolizie achrodekstryny nie dają
zabarwienia z jodem. Produktem końcowym jest maltoza.

Osazony
Fenylohydrazyna
Monosachardy , zarowno aldozy jak i ketozy oraz disacharydy
redukujące reagują z aminami np. z fenylohydrazyną. W pierwszym etapie
kondensacji z fenylohydrazyną powstają fenylohydrazony, ktore następnie
ulegają utlenieniu. Powstałe związki kondensują z kolejną cząsteczką
fernylohydrazyny, co prowadzi ostatecznie do wytworzenia
difenylohydrazonow czyli osazonow
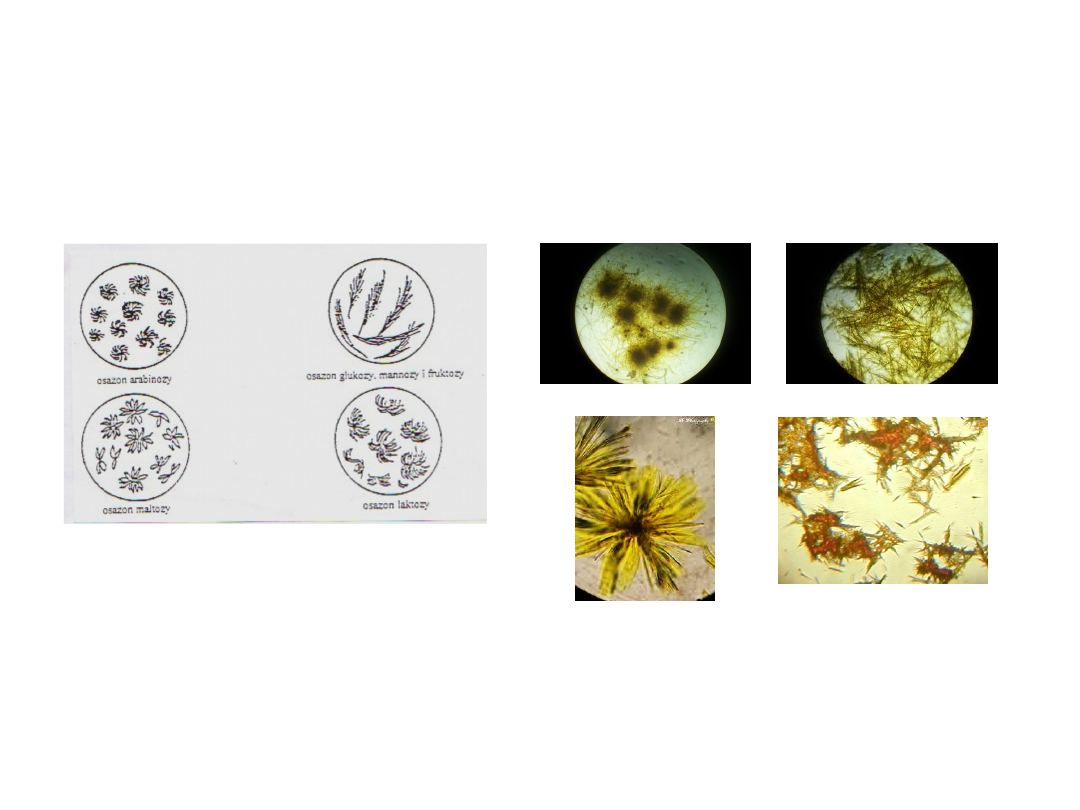
Osazony
Żołto zabarwione kryształy osazony poszczegolnych mono- i
disacharydow rożnią się
temperaturą topnienia i kształtem kryształow co pozwala je
łatwo identyfikować pod
mikroskopem

Schemat oznaczania cukrów
Document Outline
- Slide 1
- Furfural i 5-hydroksymetylofurfural
- Reakcja Molischa z a - naftolem
- Reakcja Seliwanowa z rezorcyną na ketozy
- Wykrywanie pentoz: próba Biala
- Reakcje redukcyjne
- Reakcja Trommera
- Reakcja Fehlinga
- Próba Benedicta
- Reakcja Tollensa
- Disacharydy
- Wielocukry
- Reakcja wielocukrów z jodem
- Hydroliza kwaśna skrobi
- Osazony
- Osazony
- Schemat oznaczania cukrów
Wyszukiwarka
Podobne podstrony:
UP Bioch LIPIDY PREZENTACJA
UP Bioch Biol 2014 wyniki kolokwiów
CUKRY prezentacja
OBLICZENIA BIOCH 2014
Volkswagen Street up! DE 2014
S up prezentacja 1 dobˇr przekroju
prezentacja 1 Stat 2014
Prezentacja SPSS 2014
Prezentacja SSSPZ 02 12 2014 MTomaszewska
prezentacja RPO WZ 2014 2020
Gerbera nakolosanotatki 13-01-2014, OGRODNICTWO UP LUBLIN, ROŚLINY OZDOBNE, ozdobne II semestr
EGZAMIN Z SYSTEMATYKI ZASADY 2014, Leśnictwo UP POZNAŃ 2013, Systematyka roślin
referacik, Weterynaria UP lublin, I rok, Materiały, Ochrona środowiska, referaty prezentacje
Pomoc społeczna, służby społeczne, praca socjalna program prezentacji 2014 15
Prezentacja 2014
prezentacja 2 Stat 2014
Indywidualne prawo pracy prezentacja 2014 2015 2
Cukry - dodatkowe pytania, Weterynaria UP lublin, I rok, Materiały, Chemia, koło organiczna
więcej podobnych podstron