
Ekranowanie j
ą
dra przez elektrony
B
ef
= B
o
(1 –
σσσσ
)
Oddziaływanie spin – spin
sprz
ęż
enie po
ś
rednie (skalarne) J
sprz
ęż
enie bezpo
ś
rednie (dipol – dipol) D
oddziaływanie spinu z niesparowanym elektronem
(metale przej
ś
ciowe, wolny rodnik)
Sprz
ęż
enie kwadrupolowe (j
ą
dra o spinie > 1/2)
(Procesy relaksacyjne)
Podstawowe oddziaływania w cz
ą
steczkach
istotne dla spektroskopii MRJ
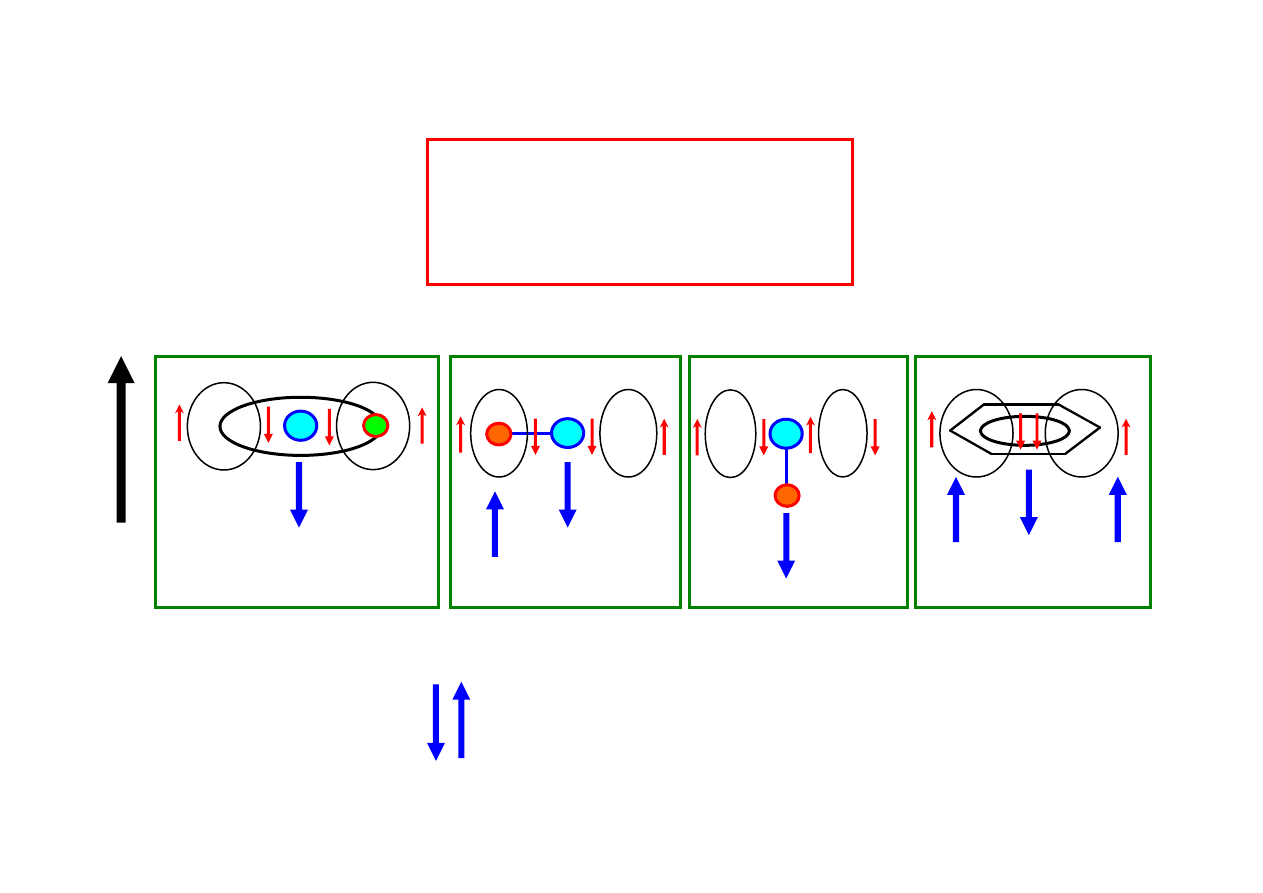
Indukowane pole magnetyczne
Ekranowanie j
ą
dra przez elektrony
B
ef
= B
o
(1 –
σσσσ
)
σσσσ
=(
σσσσ
dia
+
σσσσ
para
) +
σ
σ
σ
σ
AB
+
σσσσ
delok.
przesuni
ę
cie chemiczne (
δδδδ
) = ekranowanie (
σσσσ
) – ekranowanie wzorca (
σσσσ
ref
)
e
σσσσ
dia
+
σσσσ
para
σσσσ
AB
σσσσ
AB
σσσσ
delok.
B
o
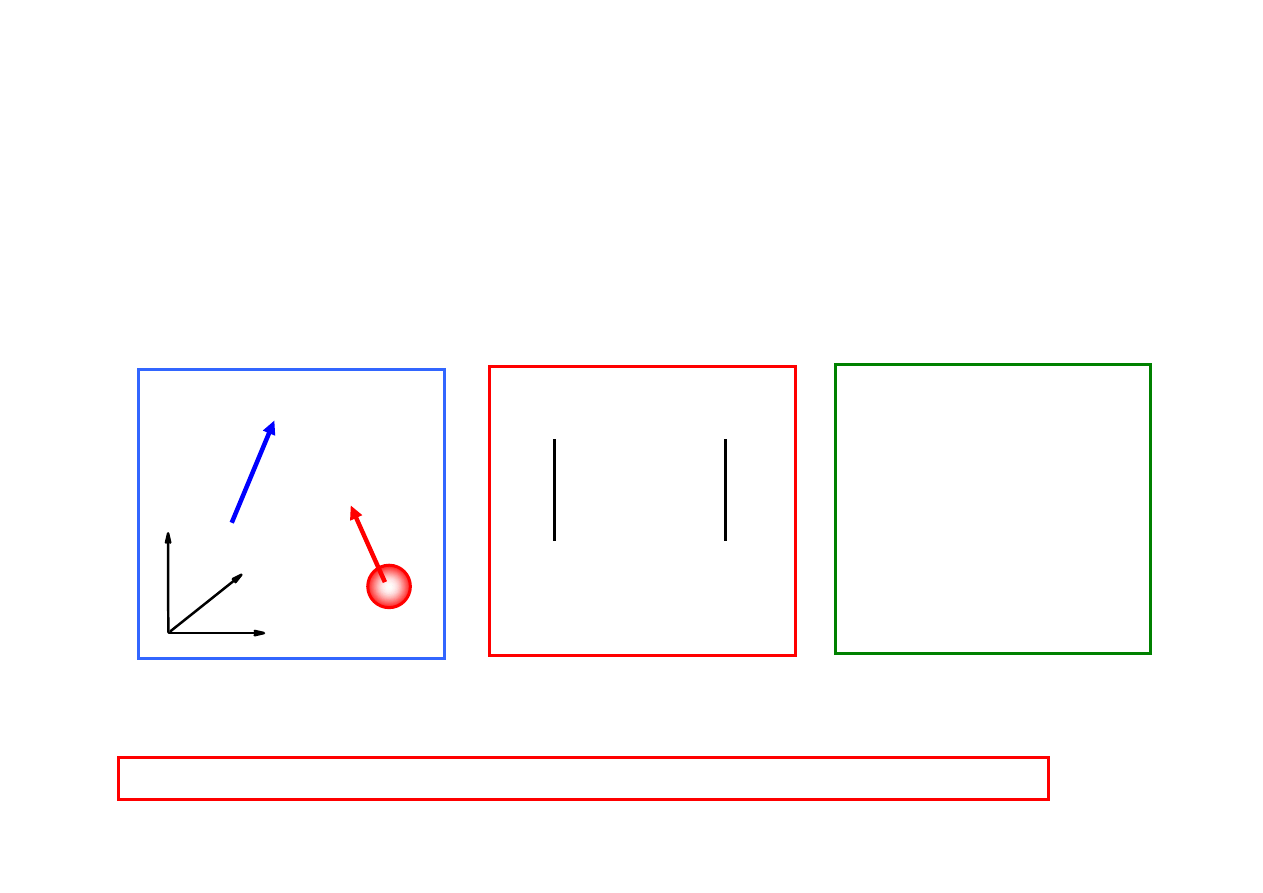
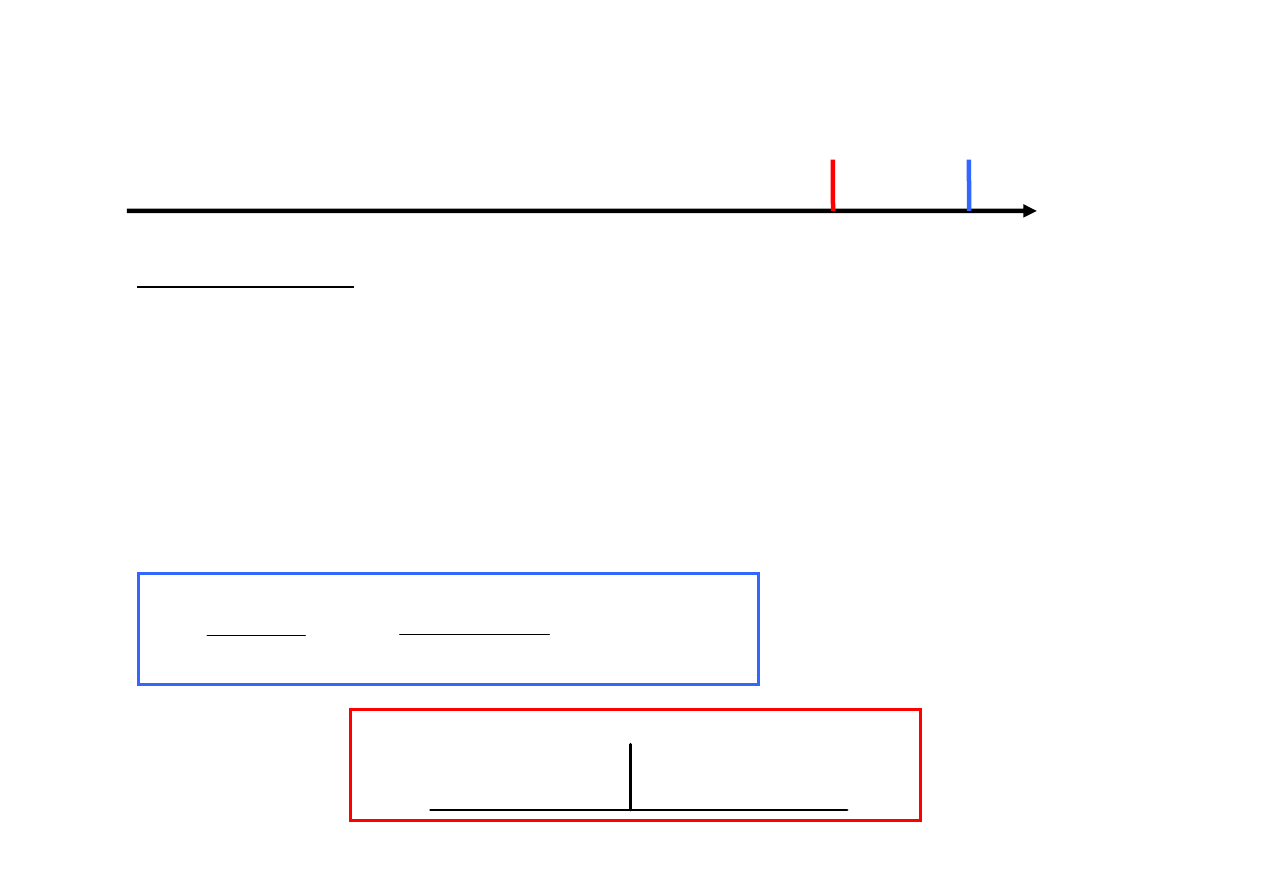
Ekranowanie - wielko
ść
anizotropowa
B
ef
= B
o
(1 –
σσσσ
)
Roztwór
: warto
ść ś
rednia przesuni
ęć
chemicznych (ekranowania)
Ekranowanie (przesuni
ę
cie chemiczne) zale
ż
y od indukcji pola magnetycznego
Anizotropia przesuni
ę
cia chemicznego
: ró
ż
na warto
ść
przesuni
ę
cia chemicznego
(ekranowania) w zale
ż
no
ś
ci od orientacji cz
ą
steczki wzgl
ę
dem pola magnetycznego
σσσσ
B
σσσσ
xx
σσσσ
xy
σσσσ
xz
σσσσ
yx
σσσσ
yy
σσσσ
yz
σσσσ
zx
σσσσ
zy
σσσσ
zz
tensor ekranowania
σσσσ
iso
= 1/3 (
σσσσ
xx
+
σσσσ
yy
+
σσσσ
zz
)
roztwór
νννν
x
-
νννν
ref
νννν
0
νννν
x
-
νννν
ref
νννν
0
=
10
6
[Hz]
[MHz]
" ppm "
δδδδ
=
-
+
wysokie (silne) pole
przesłanianie
niskie (słabe) pole
odsłanianie
MHz
500 130 125 Hz
νννν
x
νννν
ref
Skala przesuni
ęć
chemicznych
δδδδ
(skala ppm)
Poło
ż
enie sygnału:
Cz
ę
sto
ść
rezonansowa
du
ż
e liczby, zale
ż
no
ść
od indukcji pola
(np. 500 130 125 Hz)
magnetycznego (typu aparatu)
Cz
ę
sto
ść
wzgl
ę
dna:
zale
ż
no
ść
od indukcji pola magnetycznego
νννν
x
–
νννν
ref
[Hz]
Skala przesuni
ęć
chemicznych
warto
ść
niezale
ż
na od indukcji pola
ppm (parts per milion)
magnetycznego
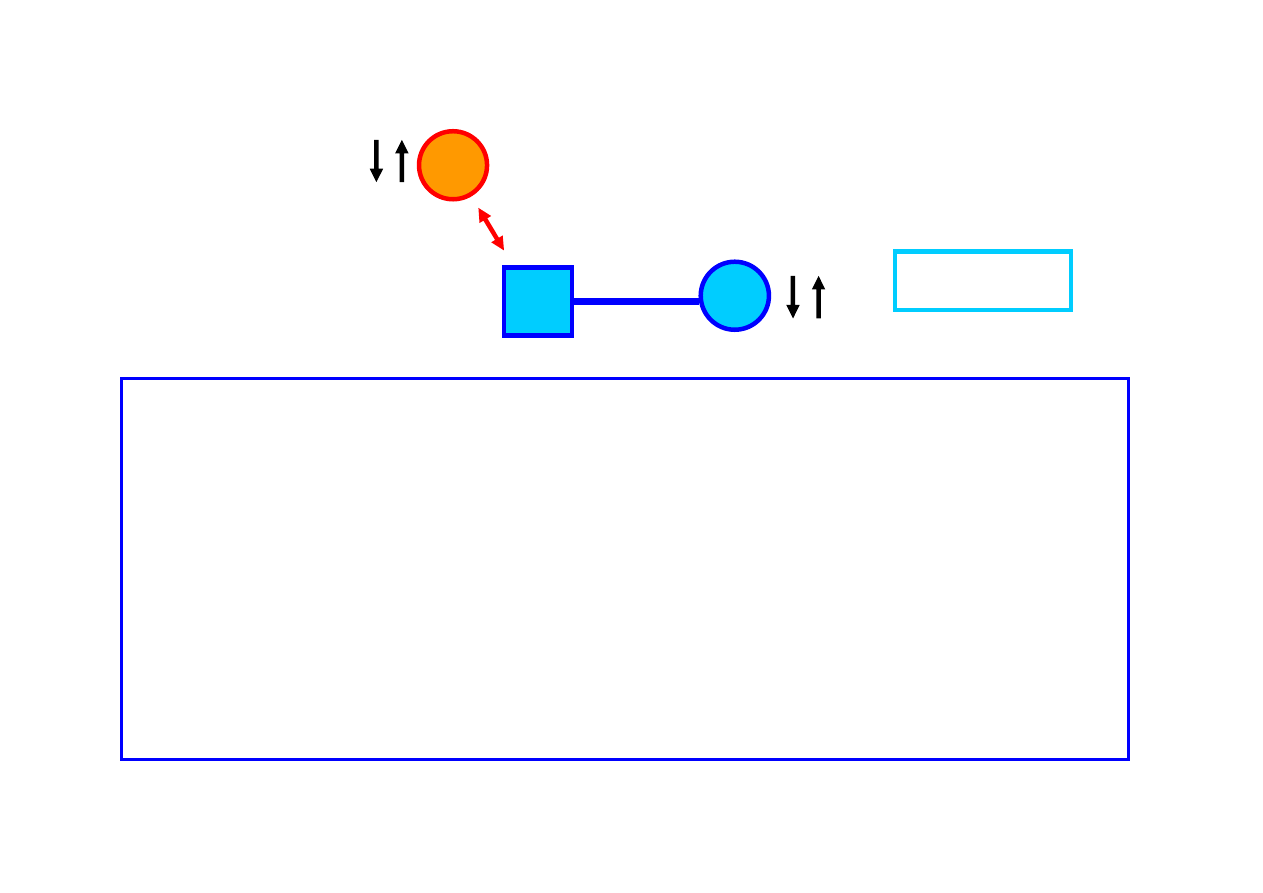
Oddziaływanie spin – spin
- sprz
ęż
enie skalarne J, sprz
ęż
enie po
ś
rednie
- sprz
ęż
enie dipol-dipol D, sprz
ęż
enie bezpo
ś
rednie
Wielko
ść
stałej sprz
ęż
enia jest
niezale
ż
na
od indukcji pola magnetycznego
Wielko
ść
stałej sprz
ęż
enia wyra
ż
amy w hercach („stała sprz
ęż
enia”) (Hz)
Stałe sprz
ęż
enia J i D mog
ą
by
ć
wi
ę
ksze lub mniejsze od 0 ! Uwaga na znak !
„od a do b”
≠≠≠≠
„od –a do b” !!!
w tym drugim przypadku
a
mo
ż
e by
ć
równe
0
!!
H
H
J
H
D
n
J(
1
H-
1
H)
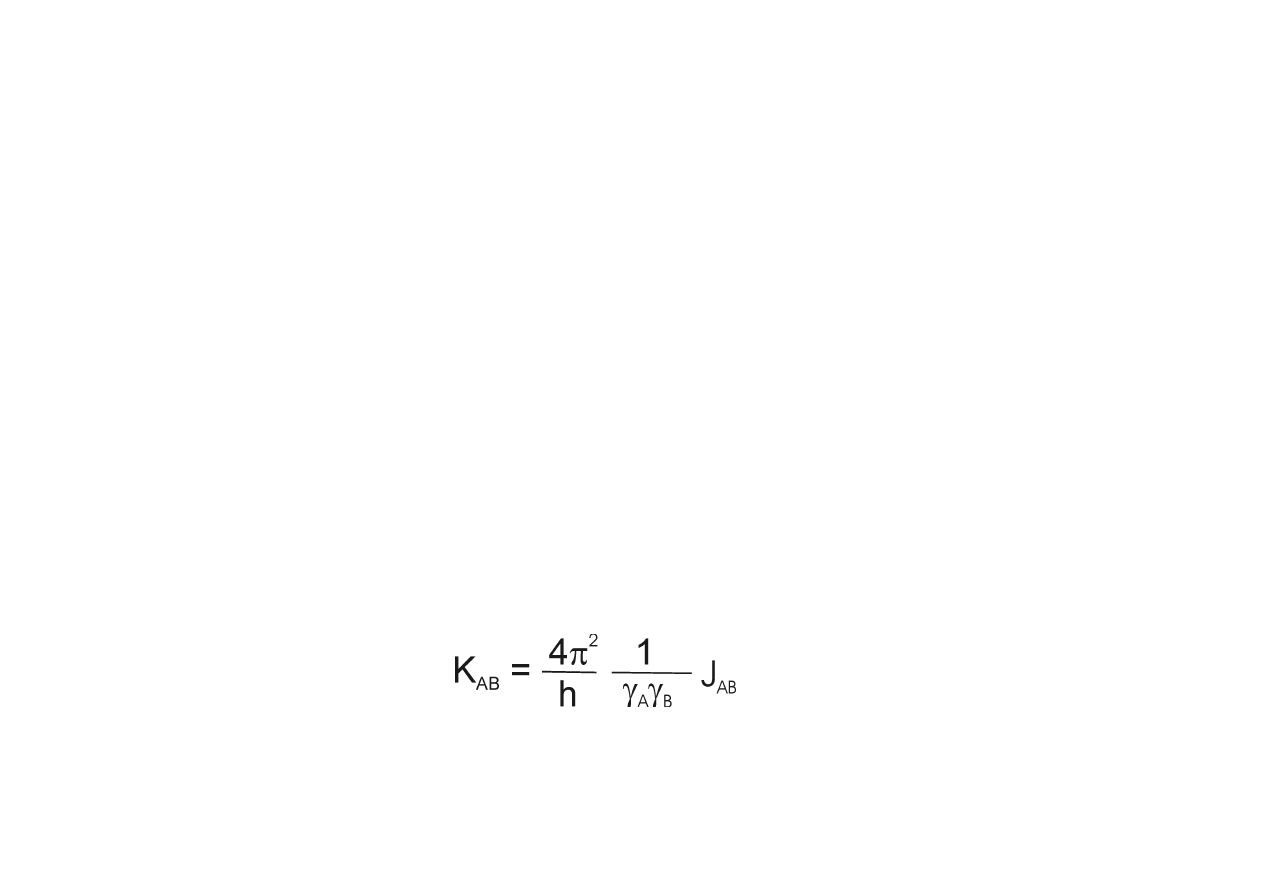
Stała sprz
ęż
enia J mo
ż
e mie
ć
warto
ść
mniejsz
ą
lub wi
ę
ksza od zera
Warto
ść
bezwzgl
ę
dna J: od 0 do 9000000 Hz (!!)
Sprz
ęż
enie J składa si
ę
z czterech członów eksperymentalnie nierozró
ż
nialnych,
ale istotnych w przypadku oblicze
ń
teoretycznych
*
J jest wielko
ś
ci
ą
anizotropow
ą
, zale
ż
y od orientacji cz
ą
steczki
Sprz
ęż
enie J jest funkcj
ą
struktury elektronowej molekuły i współczynników
magnetogirycznych obu j
ą
der
Zredukowana stała sprz
ęż
enia K
AB
:
SPRZ
Ęś
ENIE SKALARNE (PO
Ś
REDNIE) J
*
zgodnie z nierelatywistyczn
ą
teori
ą
Ramseya,
N. F. Ramsey, Physical Review, 1953, 91, 303
Obliczanie parametrów MRJ
Reguły empiryczne (np. metoda inkrementów, zale
ż
no
ś
ci Karplusa)
Metody MQ
nierelatywistyczne (Gaussian, Dalton, ......)
relatywistyczne (ADF, ....)
Gaussian:
#
nmr=giao
b3pw91/6-311++g(2d,p) ..........
#
nmr=(giao,spinspin)
b3pw91/6-311++g(2d,p) ..............
wynik:
Tensor ekranowania (warto
ś
ci
σσσσ
), istotna jest warto
ść
izotropowa („isotropic”)
δδδδ
obl.
=
σσσσ
obl. ref
-
σσσσ
obl.
Cztery człony stałej sprz
ęż
enia (J oraz K):
kontaktowy Fermiego (Fermi contact, FC)
spinowo-dipolowy (spin-dipolar, SD)
paramagnetyczny spinowo-orbitalny (paramagnetic spin-orbit, PSO)
diamagnetyczny spinowo-orbitalny (diamagnetic spin-orbit, DSO)
„Total”
O
C
H
3
CH
3
C
H
3
δδδδ
eksp.
= 0.944
δδδδ
obl.
– 0.054
δδδδ
eksp.
= a
δδδδ
obl.
+ b
a = 1 ??
b = 0 ??
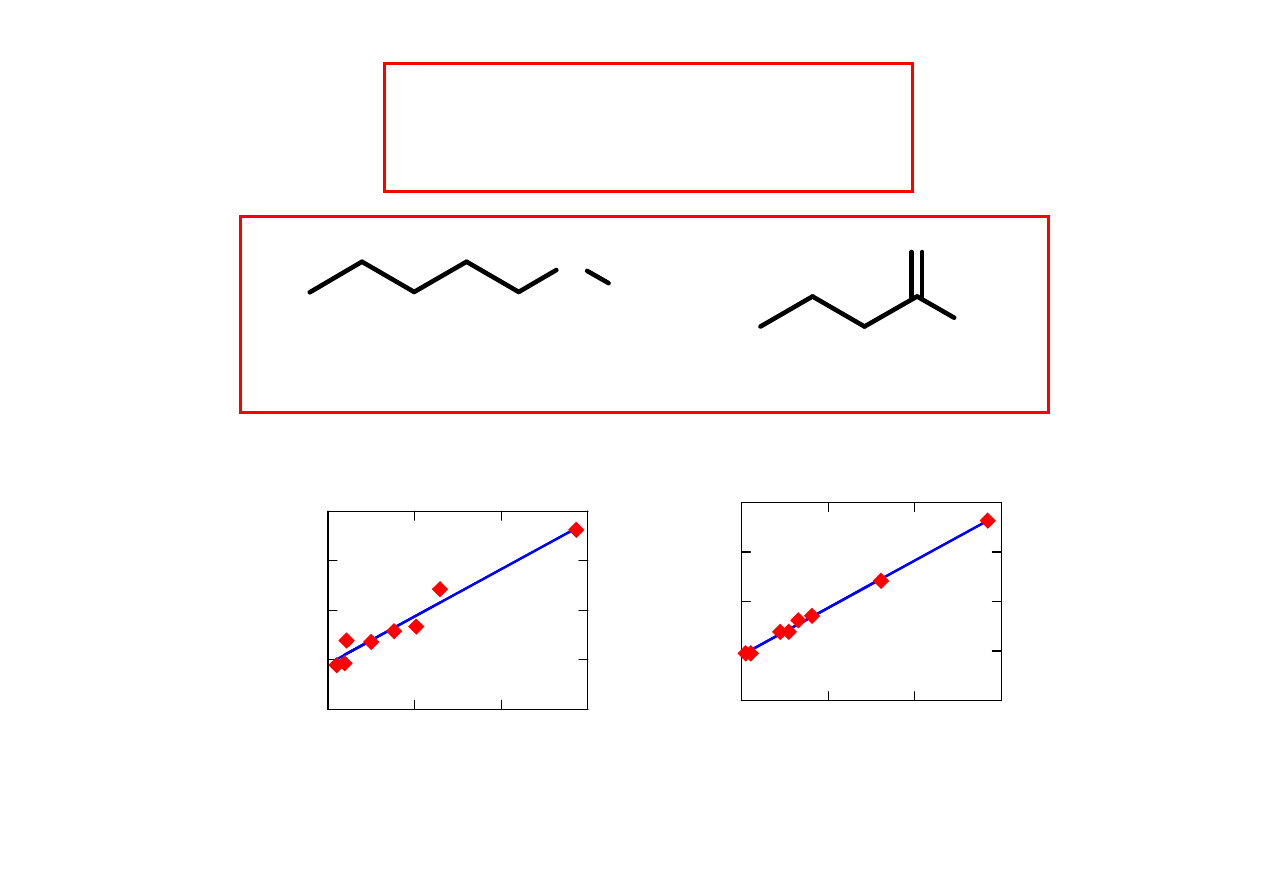
Obliczone warto
ś
ci
δδδδ
optymalizacja struktury: B3LYP/6-31G(2d)
NMR: B3PW91/6-311++G(2d,p)
0.5
1
1.5
2
2.5
3
0.5
1
1.5
2
2.5
0.5
1
1.5
2
2.5
3
0.5
1
1.5
2
2.5
r
2
= 0.997
rms 0.053
eksp.
(ppm)
obl.
(ppm)
eksp.
(ppm)
obl.
(ppm)
r
2
= 0.897
rms 0.287
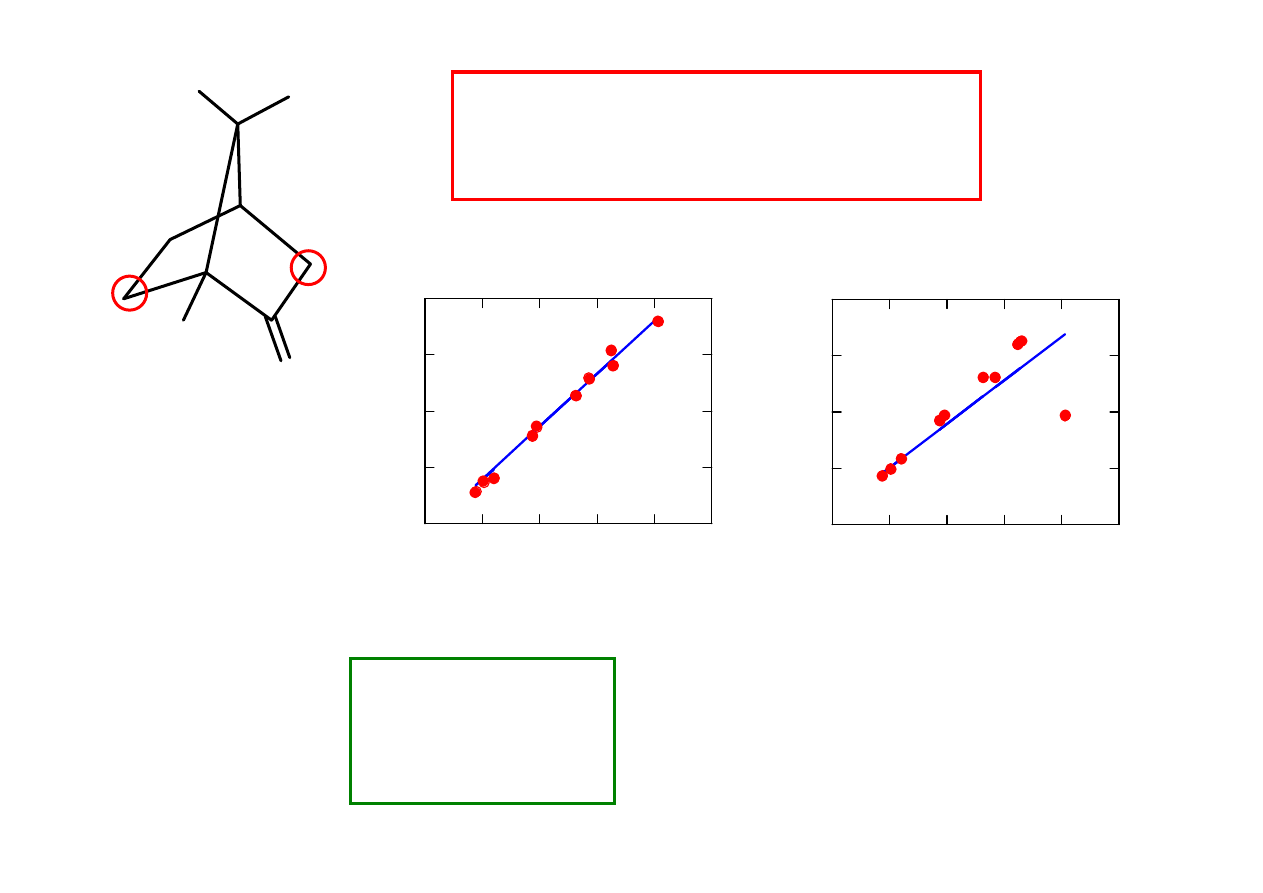
O
H
H
O
(41 rotamerów)
(13 rotamerów)
1
2
3
4
0
1
2
3
4
1
2
3
4
0
1
2
3
4
r
2
= 0.989
rms 0.16
eksp.
(ppm)
obl.
(ppm)
eksp.
(ppm)
obl.
(ppm)
r
2
= 0.999
rms 0.05
Obliczone warto
ś
ci
δδδδ
optymalizacja struktury: B3LYP/6-31G(2d)
NMR: B3PW91/6-311++G(2d,p)
T. Helgaker, M. Jaszu
ń
ski and M. Pecul, Progress in Nuclear Magnetic
Resonance Spectroscopy, 2008, 53, 249
J. Autschbach and S. Zheng, Annual Report on NMR Spectroscopy, 2009, 67, 1
J Vaara, J. Jokisaari, R. E. Wasylishen and D. L. Bryce, Progress in Nuclear
Magnetic Resonance Spectroscopy, 2002, 41, 233
C
H
3
X
H
H
1
2
3
2
J(H1,H3)
X
FC
SD
PSO
DSO
J
eksp.
H
-0.35
+0.31
+3.29
-3.51
-0.26
+2.5
F
-3.89
+0.19
+3.34
-3.52
-3.87
-3.2
NH
2
-2.10
+0.23
+3.31
-3.39
-1.90
0.0
1
J(H1,C2)
H
+135.0
+0.01
+0.55
+0.56
+136.1
Obliczone warto
ś
ci J
optymalizacja struktury: B3LYP/6-31G(2d)
NMR: B3PW91/6-311++G(2d,p)
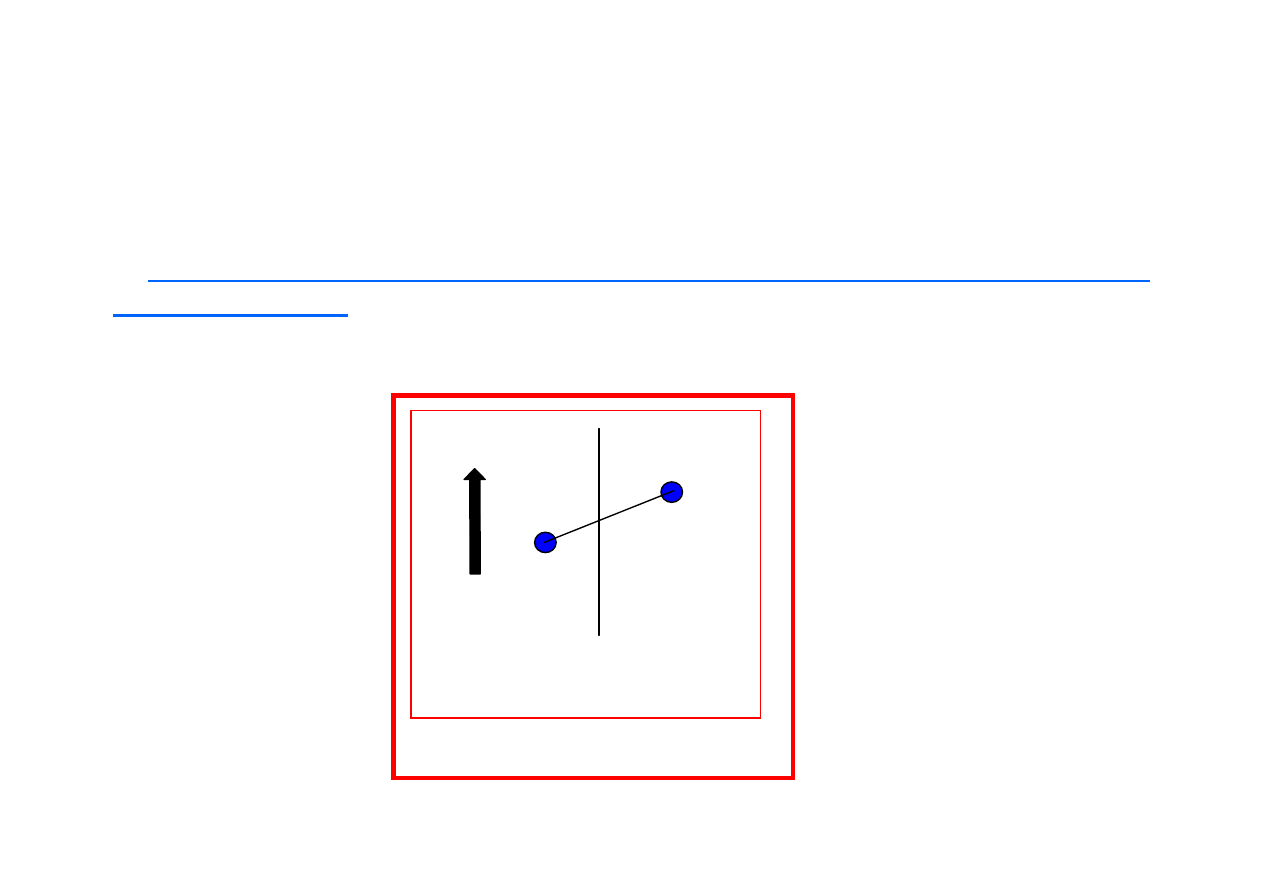
D ~ [
3cos
2
(
αααα
) – 1
] (
r
-3
)
B
o
αααα
αααα
= 54.74
o
D = 0
Wielko
ść
stałej sprz
ęż
enia D zale
ż
y od orientacji sprz
ę
gaj
ą
cych si
ę
atomów wzgl
ę
dem
pola magnetycznego oraz od odległo
ś
ci
r
pomi
ę
dzy atomami
W roztworze sprz
ęż
enie D u
ś
redniaj
ą
si
ę
do zera i nie wpływaj
ą
na struktur
ę
multipletow
ą
widma.
Sprz
ęż
enia D odgrywaj
ą
istotn
ą
rol
ę
w procesach relaksacyjnych (NOE)
SPRZ
Ęś
ENIE BEZPO
Ś
REDNIE D
ODDZIAŁYWANIE SPINU Z NIESPAROWANYM ELEKTRONEM
Niesparowane elektrony wyst
ę
puj
ą
w atomach metali przej
ś
ciowych i wolnych
rodnikach
Wpływ na widmo:
skrócenie czasu relaksacji i poszerzenie sygnałów (
wszystkich !!
)
zmiana przesuni
ę
cia sygnałów (np. kilkaset ppm w przypadku
1
H)
SPRZ
Ęś
ENIE KWADRUPOLOWE
Wyst
ę
puje w j
ą
drach posiadaj
ą
cych moment kwadrupolowy, czyli j
ą
drach o
spinie wi
ę
kszym ni
ż
½.
Wpływ na widmo:
skrócenie czasu relaksacji i poszerzenie sygnałów j
ą
dra o spinie >1/2
Relaksacja:
oddziaływanie
spinów
ze
zmiennym
polem
magnetycznym
generowanymi przez cz
ą
steczk
ę
.
Lr
No
Md
Fm
Es
Cf
Bk
Cm
Am
Pu
Np
U
Pa
Th
Lu
Yb
Tm
Er
Ho
Dy
Tb
Gd
Eu
Sm
Pm
Nd
Pr
Ce
Ac
Ra
Fr
Rn
At
Po
Bi
Pb
Tl
Hg
Au
Pt
Ir
Os
Re
W
Ta
Hf
La
Ba
Cs
Xe
I
Te
Sb
Sn
In
Cd
Ag
Pd
Rh
Ru
Tc
Mo
Nb
Zr
Y
Sr
Rb
Kr
Br
Se
As
Ge
Ga
Zn
Cu
Ni
Co
Fe
Mn
Cr
V
Ti
Sc
Ca
K
Ar
Cl
S
P
Si
Al
Mg
Na
Ne
F
O
N
C
B
Be
Li
He
H
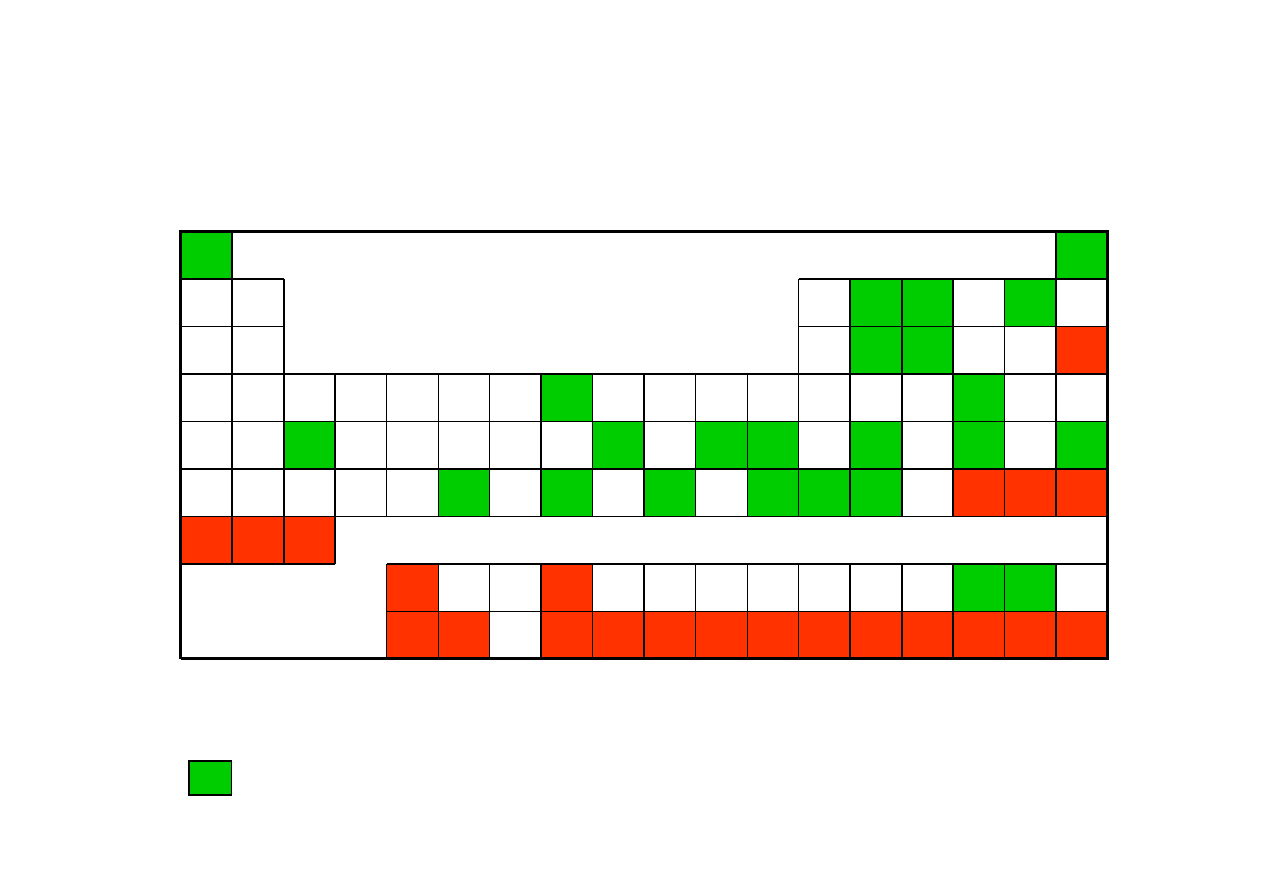
Co mo
ż
na zmierzy
ć
metodami MRJ ?
pierwiastki posiadaj
ą
ce co najmniej jeden izotop o spinie 1/2
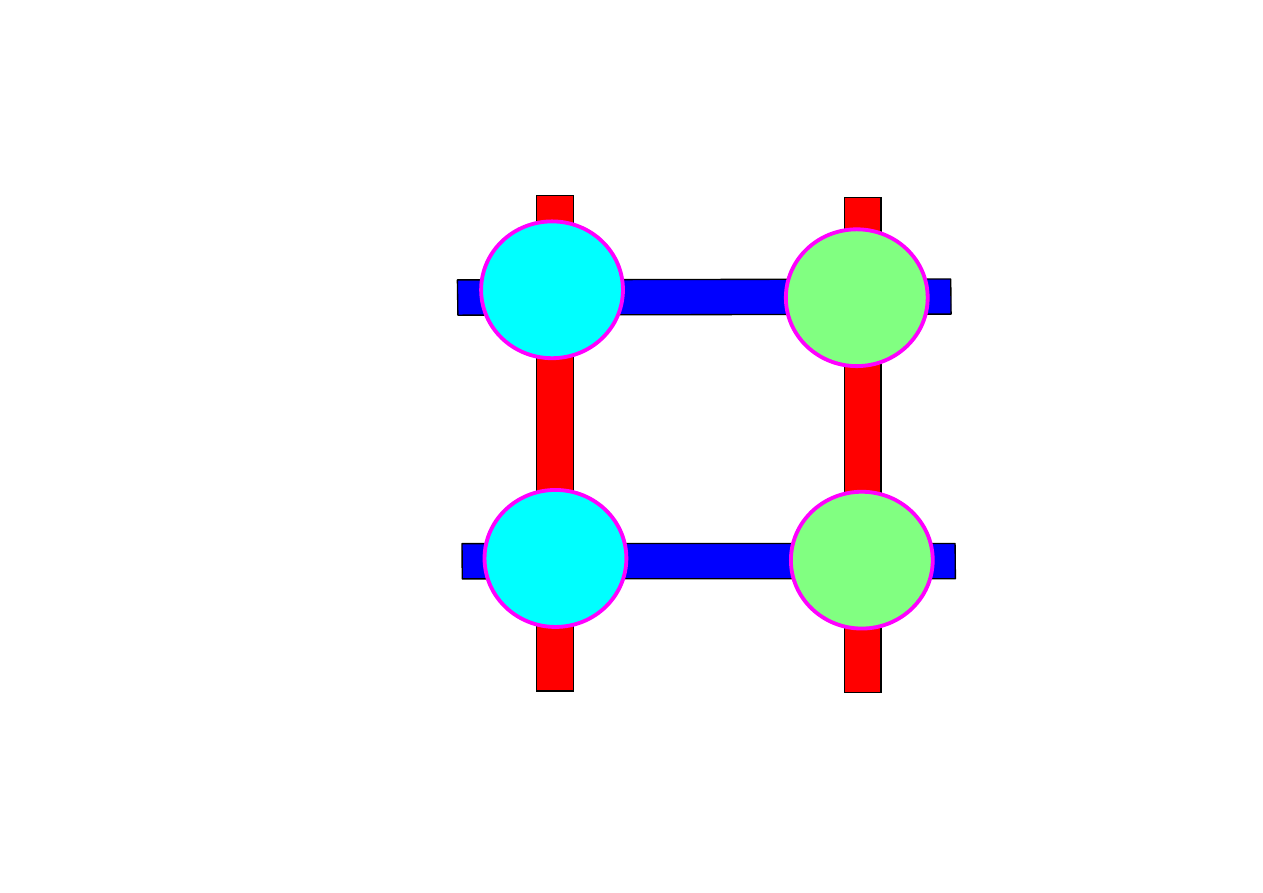
PODZIAŁ IZOTOPÓW
1
H,
19
F,
31
P
3
H,
13
C,
15
N
2
H,
17
O,
33
S
14
N
du
ż
a zawarto
ść
naturalna
mała zawarto
ść
naturalna
spin = 1/2
spin > 1/2
Inny podział: izotopy o małej lub du
ż
ej cz
ę
stotliwo
ś
ci rezonansowej

MAGNETYCZNY REZONANS J
Ą
DROWY WODORU
1
H NMR
, (
2
H NMR,
3
H NMR)
Trzy aktywne izotopy wodoru:
1
H
99.98%
spin ½
500.000 MHz (11.744 T)
2
H
0.02%
spin 1
76.753 MHz (11.744 T)
3
H
0
spin ½
533.317 MHz (11.744 T)
Widmo protonowe,
1
H NMR (
1
H MRJ):
Poło
ż
enie sygnałów (przesuni
ę
cie chemiczne, ppm)
Wzorzec: tetrametylosilan, Si(CH
3
)
4
0 ppm
Typowy zakres przesuni
ęć
chemicznych: 0 – 15 ppm
Struktura sygnałów (krotno
ść
lub multipletowo
ść
, sprz
ęż
enie spin-spin)
Intensywno
ść
sygnałów, intensywno
ść
integralna („całka”)
Skala
δδδδ
(„przesuni
ęć
chemicznych”), skala
ττττ
= 10 -
δδδδ
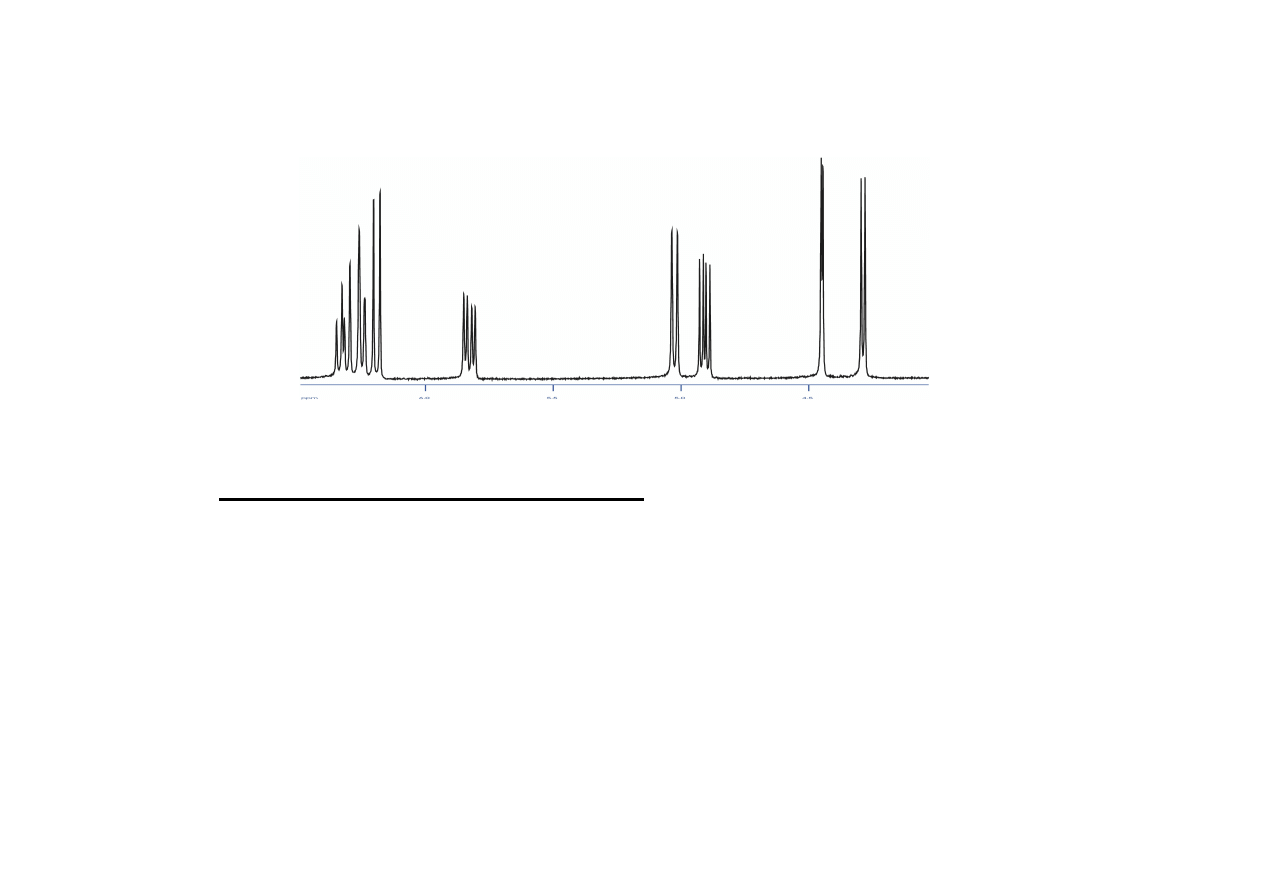
Przykładowe widmo
1
H NMR wykonane w roztworze:
Równocenno
ść
(nierównocenno
ść
) atomów:
równocenno
ść
/nierównocenno
ść
chemiczna
równocenno
ść
/nierównocenno
ść
magnetyczna
Ilo
ść
nierównocennych chemicznie atomów (grup atomów) = ilo
ść
sygnałów
Nierównocenne atomy (grupy atomów) oznacza si
ę
ró
ż
nymi literami alfabetu
Du
ż
a ró
ż
nica przesuni
ęć
chemicznych = litery odległe w alfabecie
Przykłady:
układ AB
układ AMX
układ A
3
X
2
Protony (grupy protonów)
homotopowe
= równocenne chemicznie
Protony (grupy protonów)
enancjotopowe
= równocenne chemicznie
Protony (grupy protonów)
diastereotopowe
= nierównocenne chemicznie
FAZA CIEKŁA – ILO
ŚĆ
SYGNAŁÓW
Metody spektroskopowe i ich zastosowania do identyfikacji zwi
ą
zków organicznych
Praca zbiorowa pod redakcj
ą
W. Zieli
ń
skiego i A. Rajcy, Wydawnictwa Naukowo-Techniczne,
Warszawa, 2000
Spektroskopowe metody identyfikacji zwi
ą
zków organicznych
R.M.Silverstein, F.X.Webster, D.J.Kiemle, Wydawnictwo Naukowe PWN, Warszawa 2007
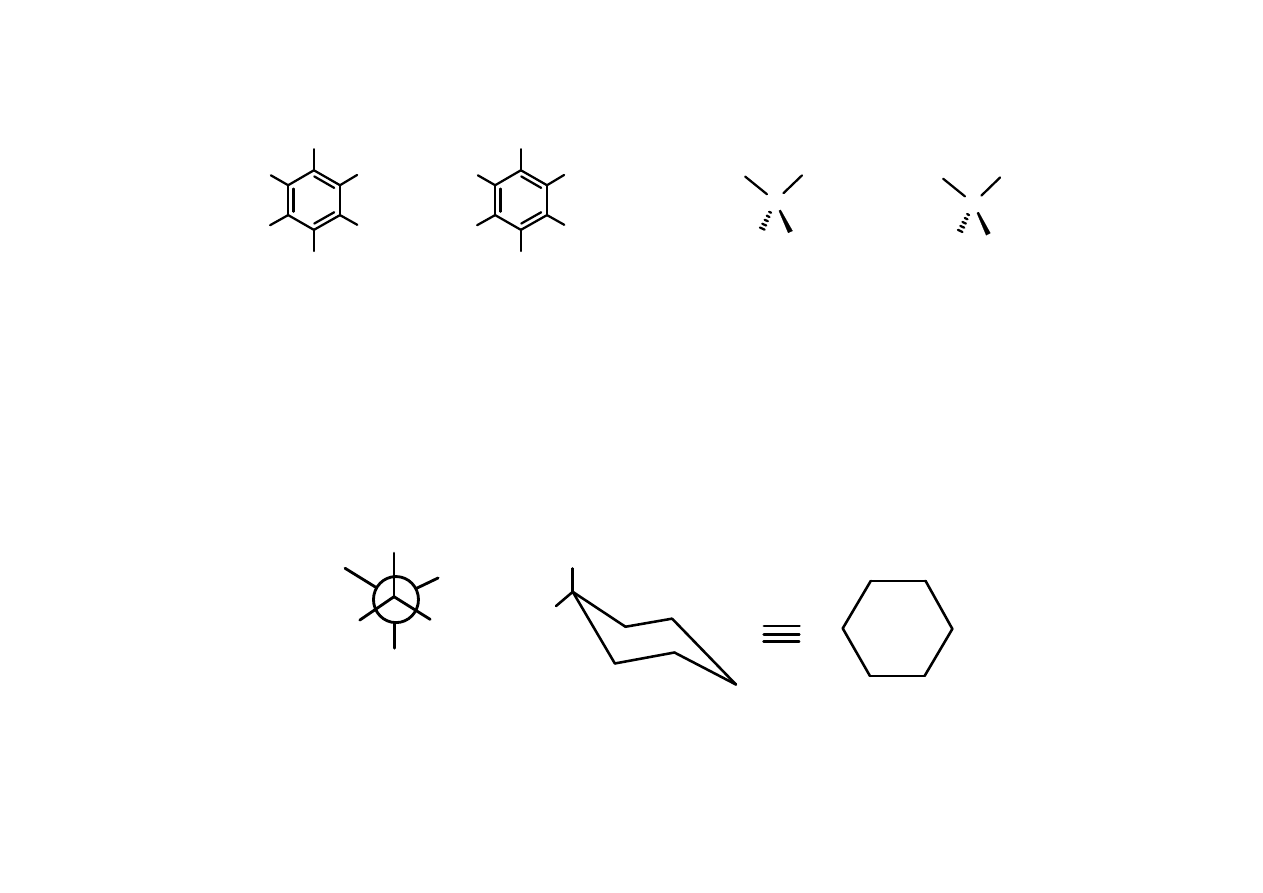
Równocenno
ść
/ nierównocenno
ść
chemiczna atomów
Cl
H
H
H
H
H
Cl
H
H
H
H
H
równocenne
chemicznie
(homotopowe)
nierównocenne
chemicznie
(diastereotopowe)
C
H
H
F
Br
równocenne
chemicznie
(enancjotopowe)
C
H
H
R*
Br
nierównocenne
chemicznie (!)
Br
Cl
Br
H
H
H
???
Hax
Heq
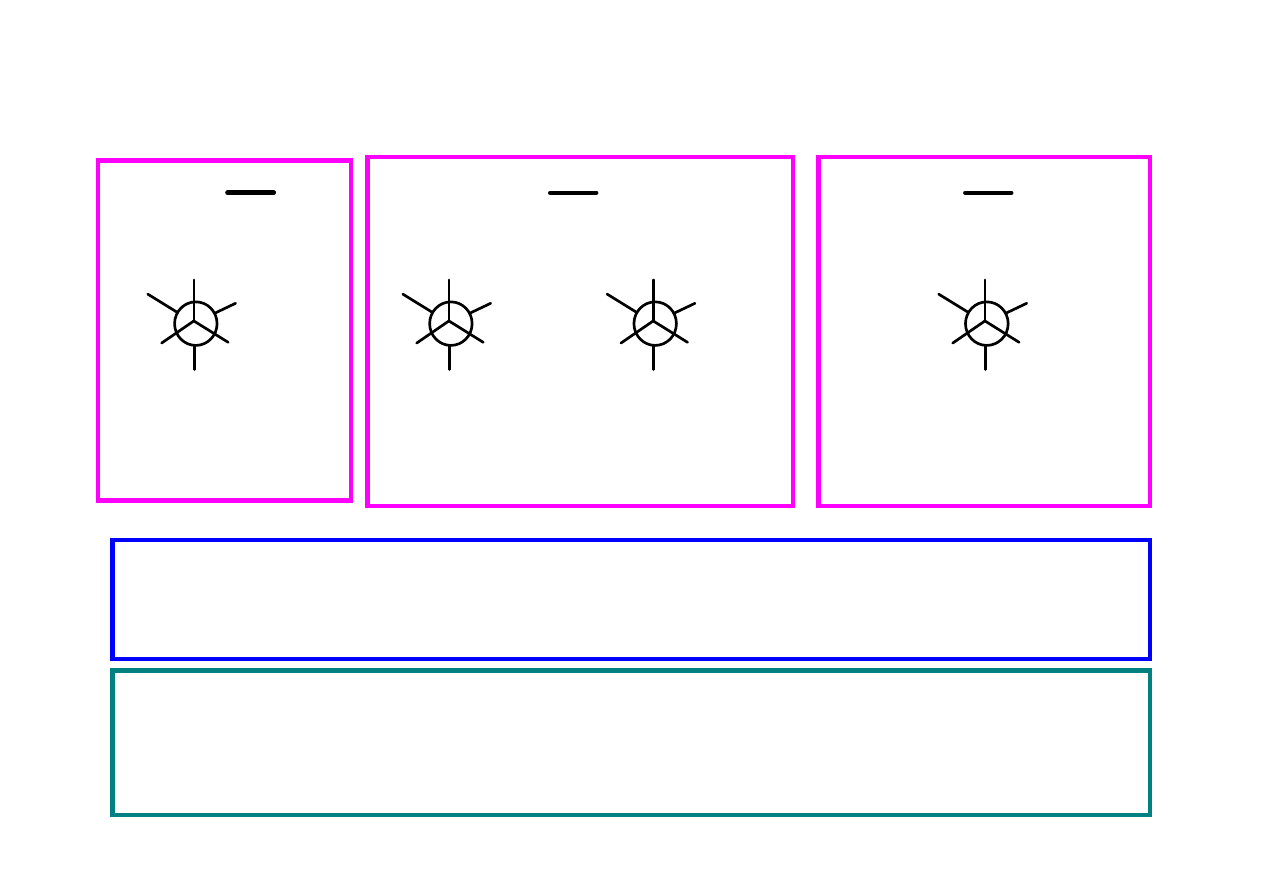
Br
Cl
Br
H
H
H
Br
2
ClC
CH
3
Br
2
ClC
CH
2
R
Br
Cl
Br
H
H
R
Br
Cl
Br
R
H
H
Układ
A
3
(A
2
B ??)
Układ A
2
Układ
A
2
(AB ??)
FBrClC
CH
2
R
Br
Cl
F
H
H
R
Układ AB !!
Atomy wodorów w grupach CH
3
i CH
2
w zwi
ą
zkach ła
ń
cuchowych s
ą
chemicznie
równocenne („u
ś
rednienie” przesuni
ęć
chemicznych)
Wyj
ą
tek:
centrum chiralne obok grupy !!!
Równocenno
ść
/ nierównocenno
ść
chemiczna atomów
Spektroskopia MRJ w fazie ciekłej, w achiralnym
ś
rodowisku,
nie rozró
ż
nia
enancjomerów, a
rozró
ż
nia
diastereoizomery.
(R)(S) = (S)(R), (R)(R) = (S)(S), (R)(S)
≠≠≠≠
(S)(S), ...........
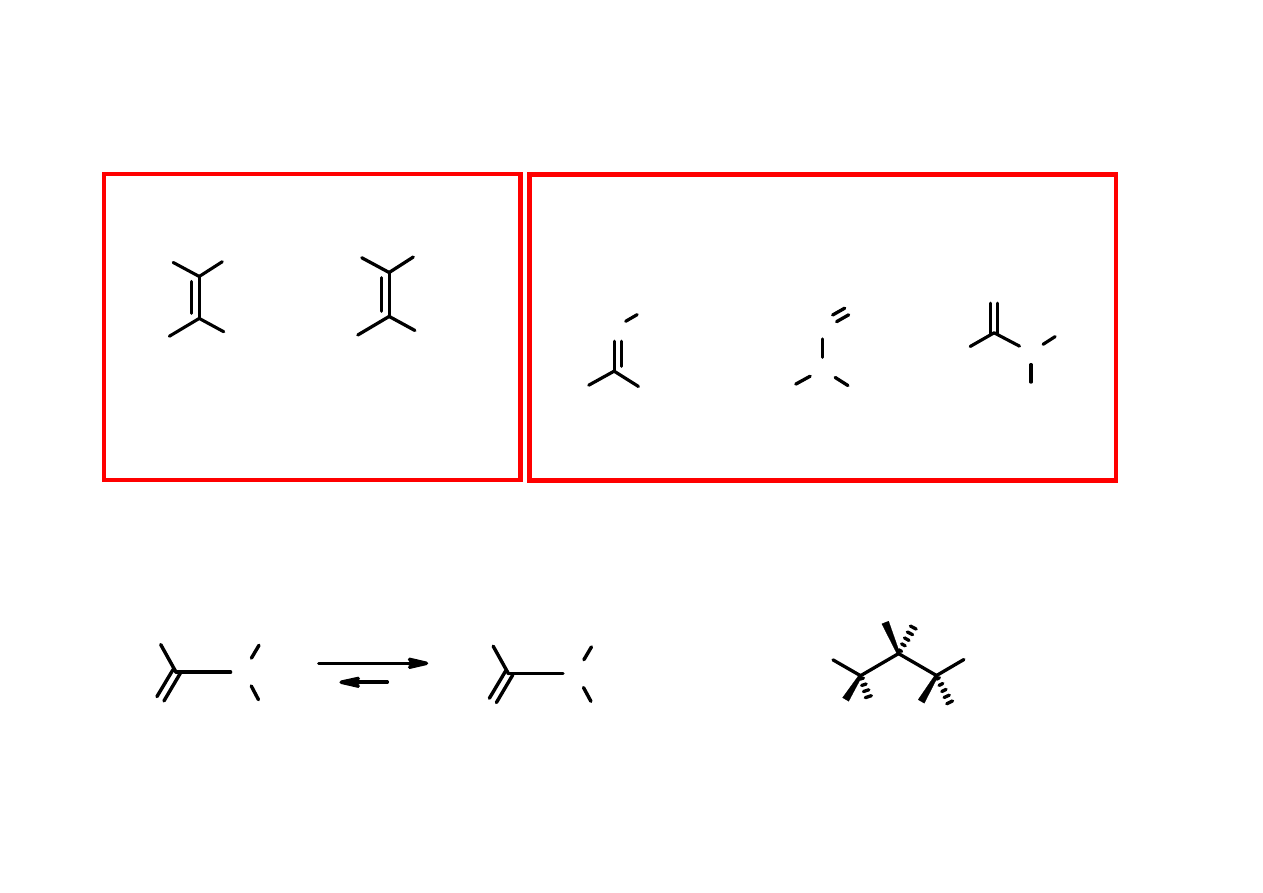
Równocenno
ść
/ nierównocenno
ść
chemiczna atomów
równocenne
(układ A
2
)
nierównocenne
(układ AB lub AX)
O
H
N
CH
3
CH
3
N
C
H
3
CH
3
N
O
C
H
3
CH
3
N
OR
H
H
Cl
Br
H
H
Cl
Cl
„Ukryte” wi
ą
zanie podwójne
N
H
O
R1
R2
N
H
O
R2
R1
H
R
R
X
Y
H
H
H

Rozpuszczalniki stosowane w
1
H NMR
Aceton-d
6
2.2 ppm
Acetonitryl-d
3
2.0 ppm
Benzen-d
6
7.4 ppm
Chlorek metylenu-d
2
5.3 ppm
Chloroform-d
7.3 ppm
Dimetyloformamid-d
6
(DMF)
2.9 ppm, 8.0 ppm
Dimetylosulfotlenek-d
6
(DMSO)
2.6 ppm
Metanol-d
4
3.5 ppm
Woda (D
2
O)
4.8 ppm
(Wg materiałów firmy BRUKER)
Wzorzec:
tetrametylosilan (TMS), (CH
3
)
4
Si
0.00 ppm
DSS
0.015 ppm
Wzorzec zewn
ę
trzny (external reference)
Wzorzec wewn
ę
trzny (internal reference)
Wzorzec wtórny (secondary reference)
Si
CH
3
C
H
3
CH
3
CH
3
Si
CH
3
C
H
3
CH
3
CH
2
CH
2
CH
2
SO
3
Na
TMS
DSS
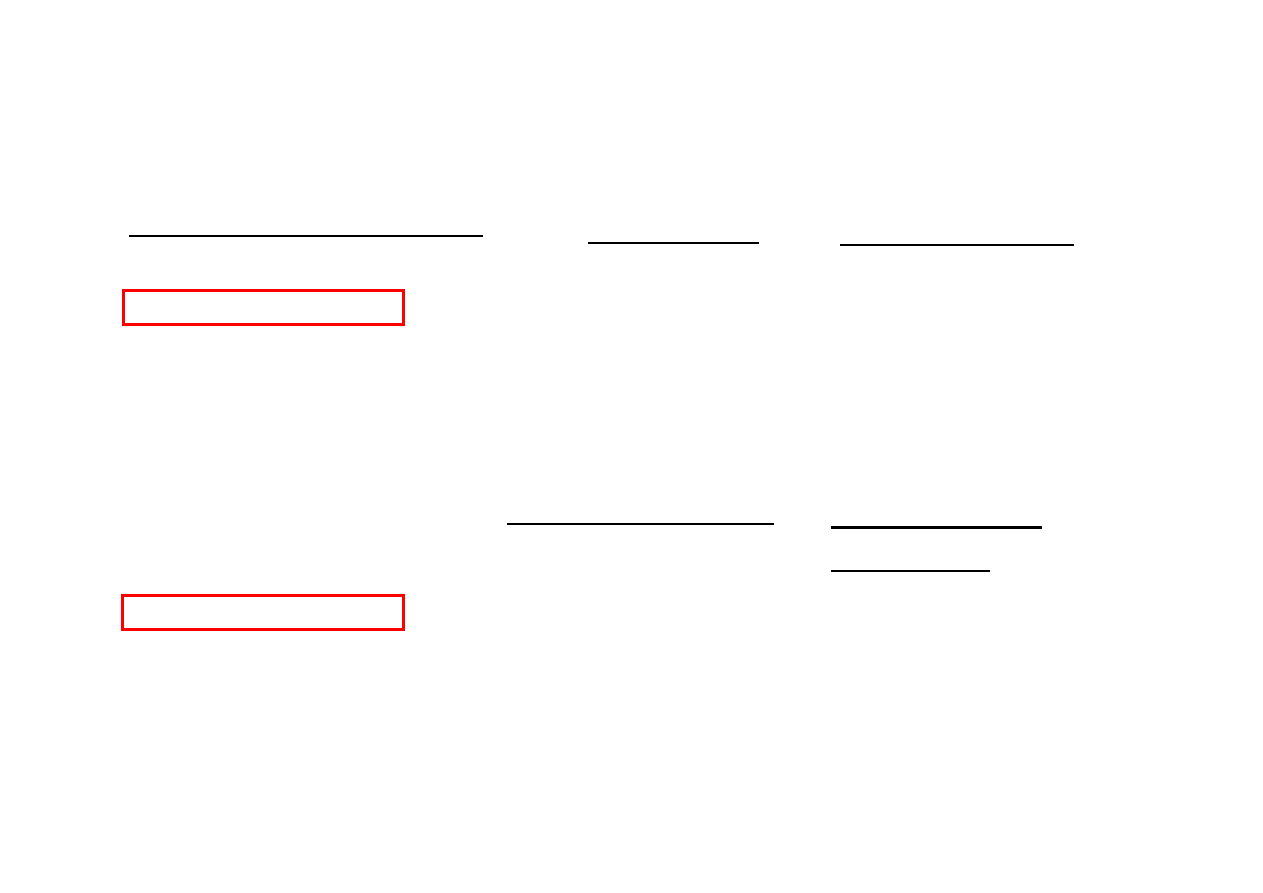
Kilka przesuni
ęć
chemicznych
1
H NMR (ppm)
Elektroujemno
ść
podstawnika:
CH
3
-H
0.23
CF
3
-F
4.26
CH
3
-Cl
3.05
CH
3
-Br
2.68
CH
3
-I
2.16
CH
3
-OCH
3
3.24
CH
3
-N(CH
3
)
2
2.12
CH
3
-SCH
3
2.08
CH
3
-Li
-1.30
(
CH
3
)
4
Si
0.00
Rz
ą
d wi
ą
zania:
CH
3
CH
3
0.86
CH
2
CH
2
5.32
CHCH
1.49
C
6
H
6
7.40
Ilo
ść
heteroatomów:
CH
4
0.23
CH
3
Cl
3.05
CH
2
Cl
2
5.35
CHCl
3
7.24
Ilo
ść
grup metylowych:
C
H
4
0.23
C
H
3
CH
3
0.86
CH
3
C
H
2
CH
3
1.33
CH
3
CH
2
C
H
(CH
3
)
2
1.47
Atom wodoru przy
heteroatomie:
OH (alif.)
1 – 5
OH (Ar)
4 – 10
OH (kwas)
9 – 12
SH
3 – 4
NH
2
3 – 5
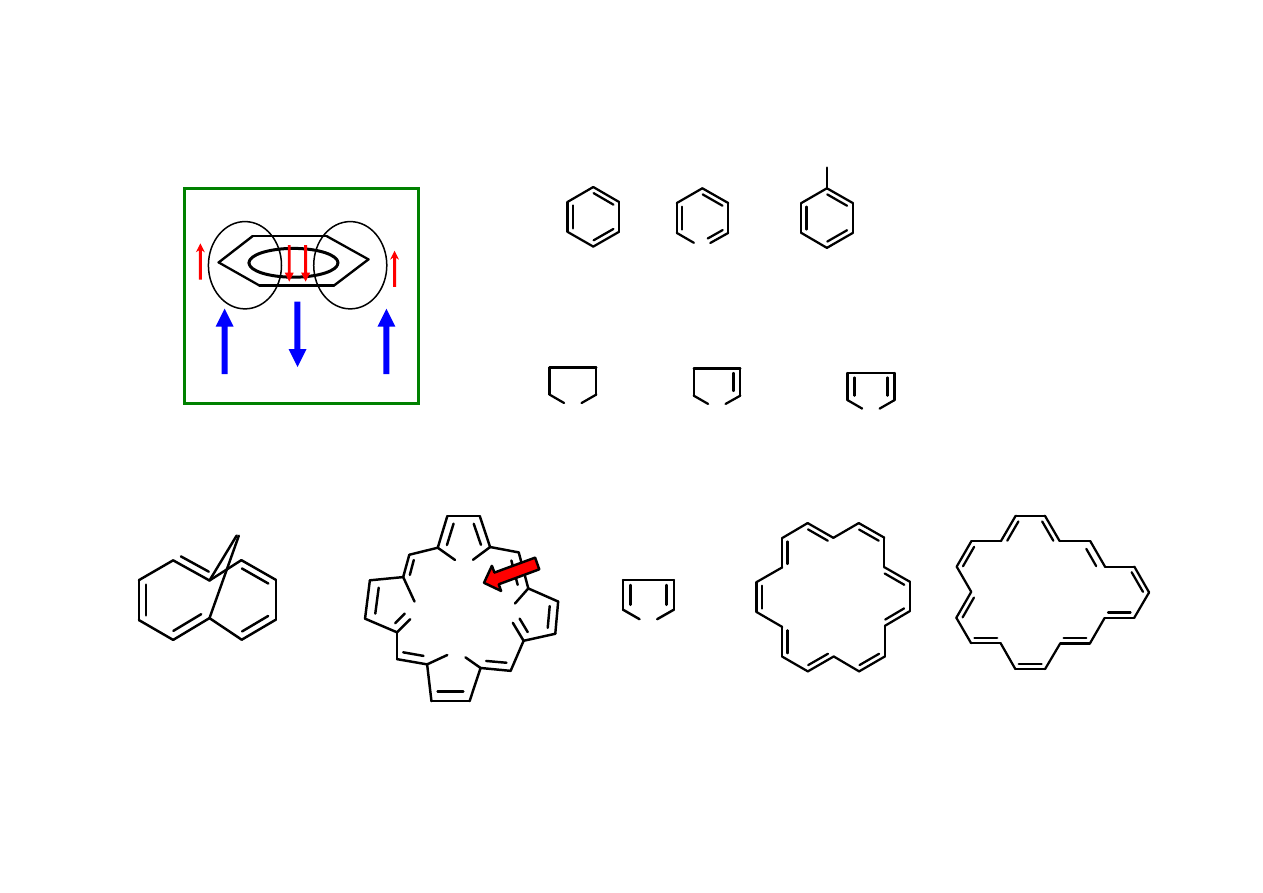
Kilka przesuni
ęć
chemicznych
1
H NMR (ppm)
N
X
7.3
8.6
7.3
7.6
6.5 - 8.2
7.0 - 7.5
6.8 - 7.6
O
O
O
1.9
3.8
4.8
6.2
6.3
7.4
CH
2
N
H
N
N
H
N
N
H
7.3
7.0
- 0.5
10 - 11
- 4
6.1
6.6
ca. 8
9.3
-3.0
18 elektronów
π
π
π
π
20 elektronów
π
π
π
π
11 - 14
4 - 7
Chaitanya S.Wannere, Paul von Ragué Schleyer, Organic Letters, 2003, 5(5), 605
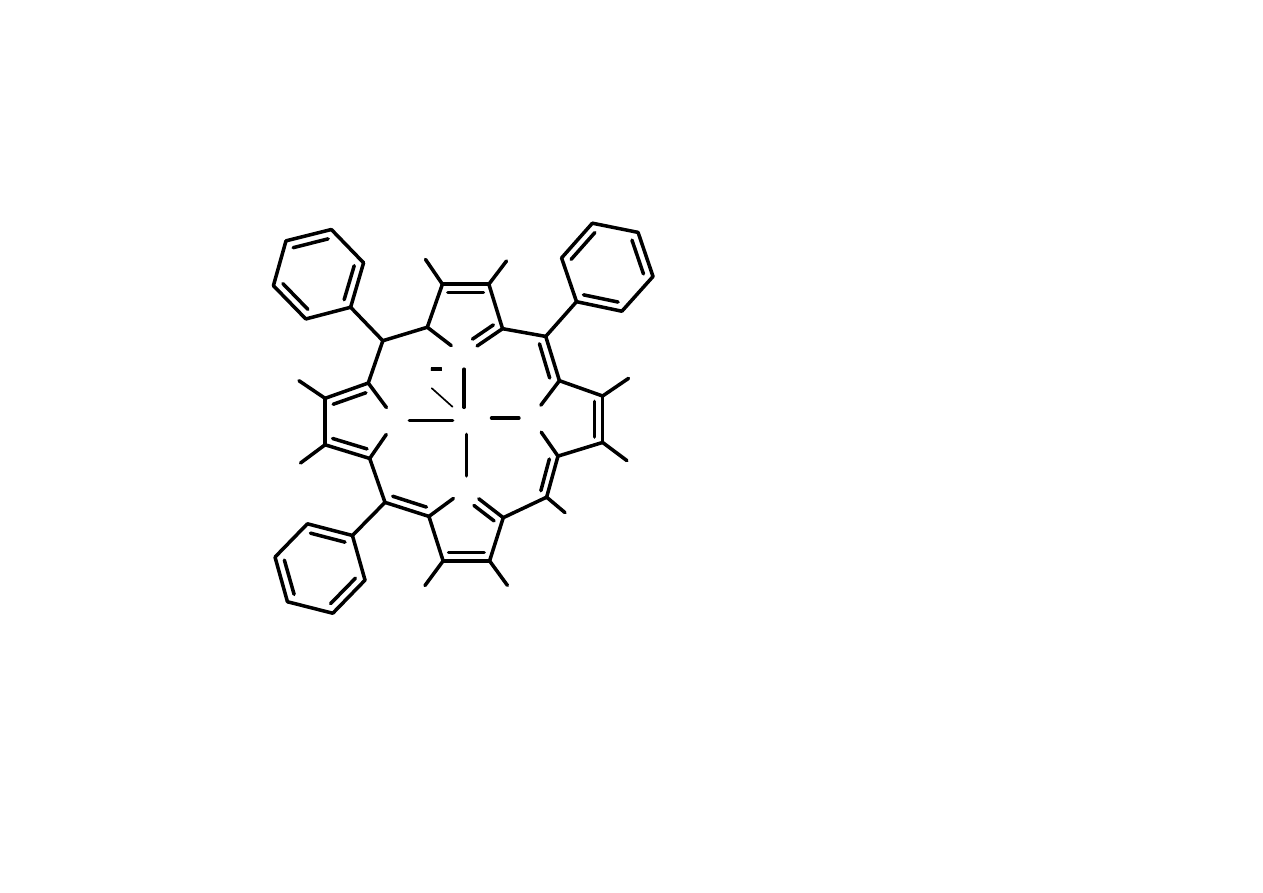
N
N
N
N
Fe
3+
H
H
H
H
H
H
H
H
H
Cl
1
H NMR (CDCl
3
)
protony pirolowe: 78.5
÷÷÷÷
81.1 ppm
proton mezo:
-72.4 ppm
protony Ar:
5.1
÷÷÷÷
13.5 ppm
(J.Wojaczy
ń
ski, Praca Doktorska, Wrocław, 1998)
Zmiany przesuni
ę
cia chemicznego
1
H NMR wywołane metalem przej
ś
ciowym: do ± 600 ppm
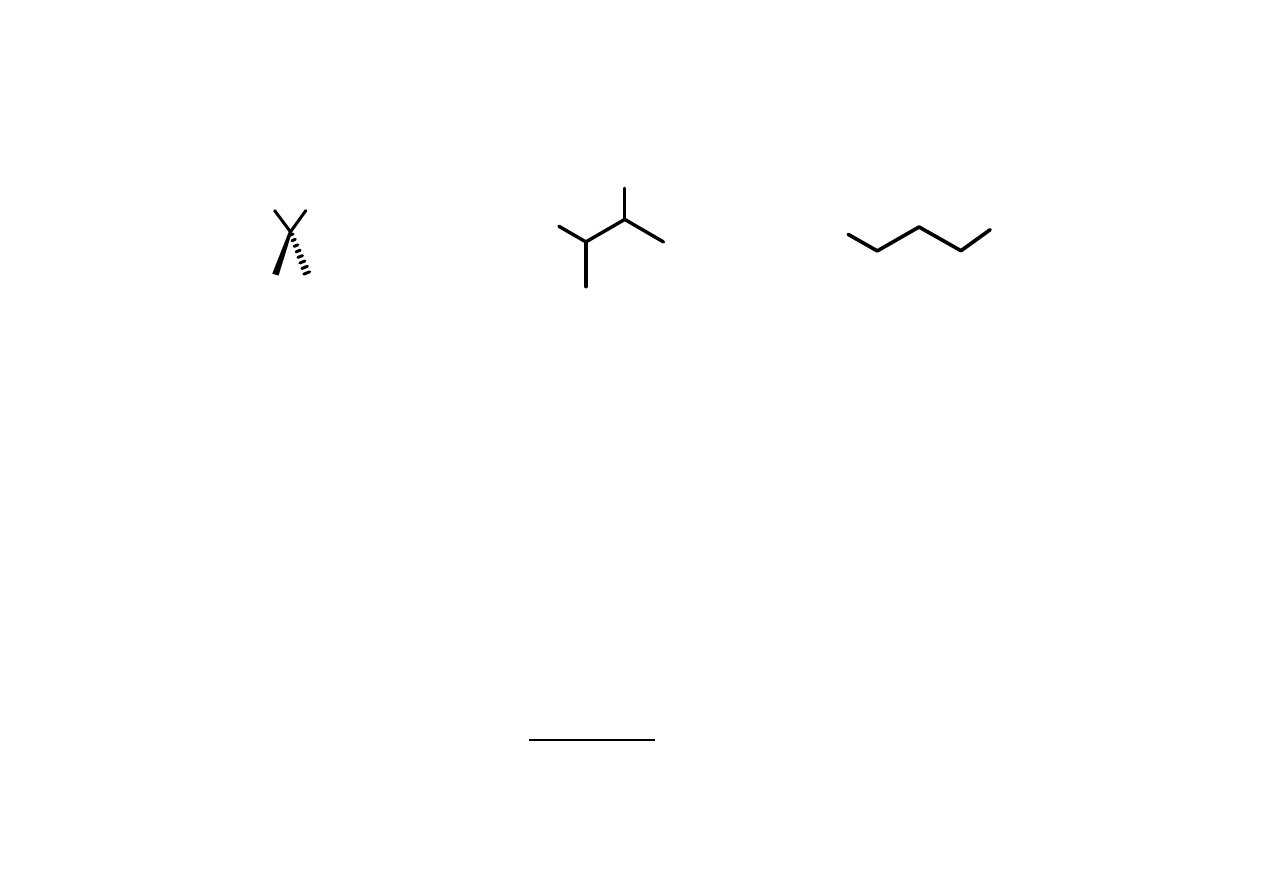
Sprz
ęż
enie po
ś
rednie (skalarne) J
H
H
H
H
H
H
sprz
ęż
enie
geminalne
2
J
gem
sprz
ęż
enie
wicynalne
3
J
vic
sprz
ęż
enie dalekiego
zasi
ę
gu
n
J
2
J
gem
2
J(
1
H-
1
H)
1
J(
13
C-
1
H)
3
J(5H-6H)
Stała sprz
ęż
enia J ma znak
Okre
ś
lenie znaku stałej sprz
ęż
enia wymaga dodatkowych eksperymentów
Nazwy sprz
ęż
e
ń
dotycz
ą
dwóch dowolnych j
ą
der, nie tylko protonów
Sprz
ęż
enia pomi
ę
dzy j
ą
drami równocennymi chemicznie nie wpływaj
ą
na struktur
ę
multipletów (w widmach I rz
ę
du !!)
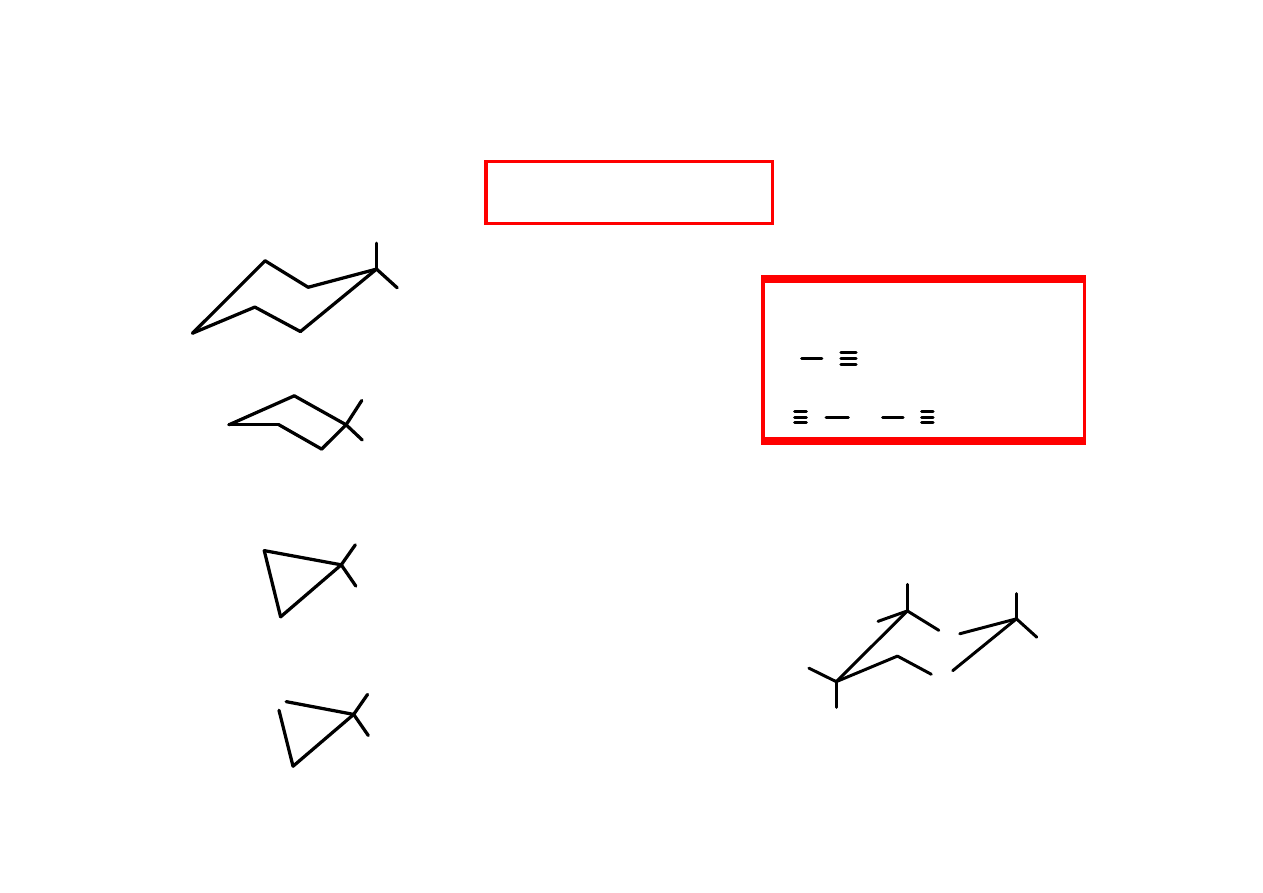
H
H
H
H
H
H
X
H
H
(- 12)
÷÷÷÷
(- 14)
(- 11)
÷÷÷÷
(- 18)
(- 3)
÷÷÷÷
(- 9)
(+ 6)
÷÷÷÷
(- 1.4)
(X = NR, J
≈
0 Hz)
O
O
H
H
H
H
H
H
- 6.1
- 12.9
- 11.2
Geminalna stała sprz
ęż
enia
2
J
gem
(atom sp
3
)
2
J
gem
= (+ 6)
÷÷÷÷
(- 20) Hz
CH
2
C
C
N
N
CH
3
C
N
CH
4
- 12.4
- 16.9
- 20.3
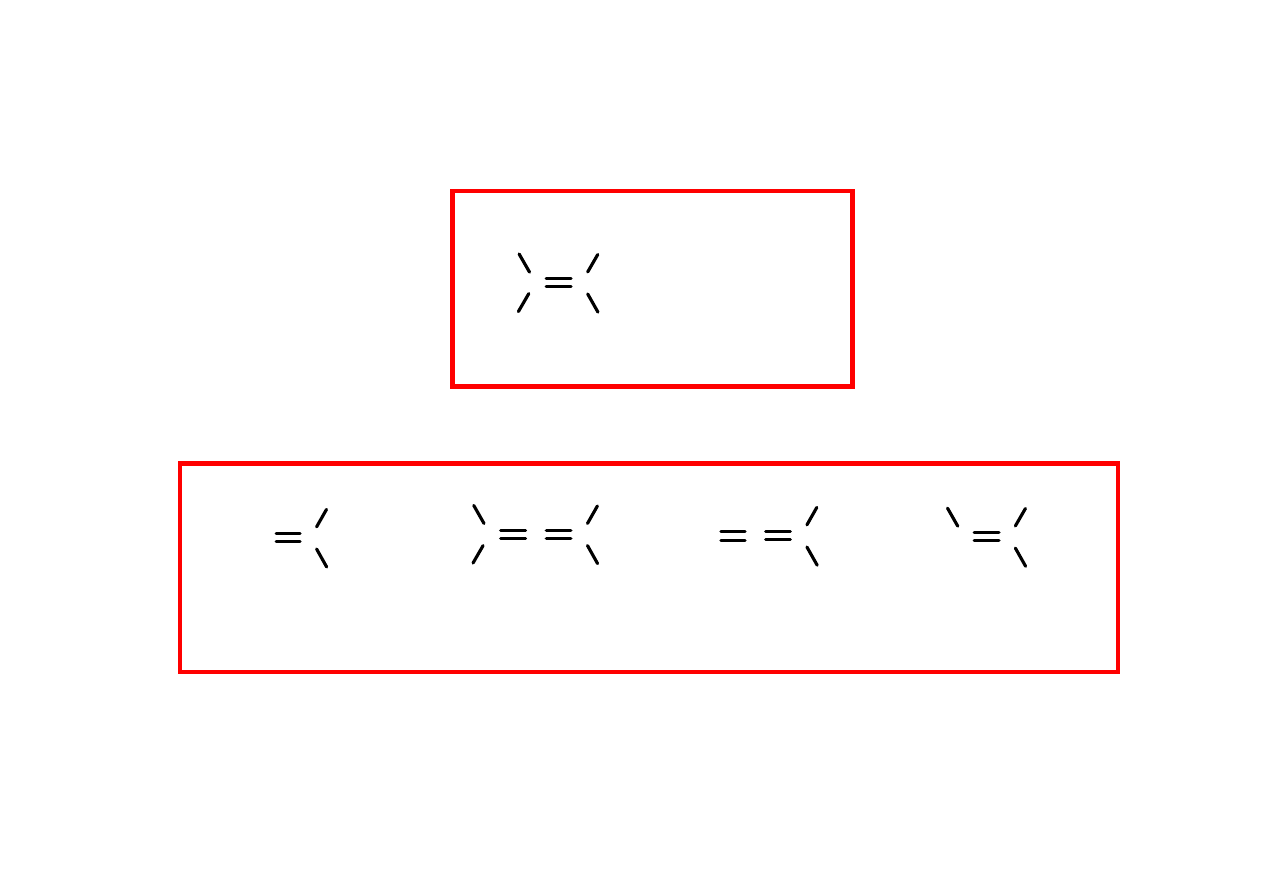
Geminalna stała sprz
ęż
enia
2
J
gem
(atom sp
2
)
C
C
H
H
R
X
X = F
- 3.2
NH
2
0
H
+ 2.5
Li
+ 7.1
O
C
H
H
C
C
H
H
C
C
H
3
C
H
3
C
C
H
H
O
N
C
H
H
R
+42
9.0
15.8
7
÷÷÷÷
17
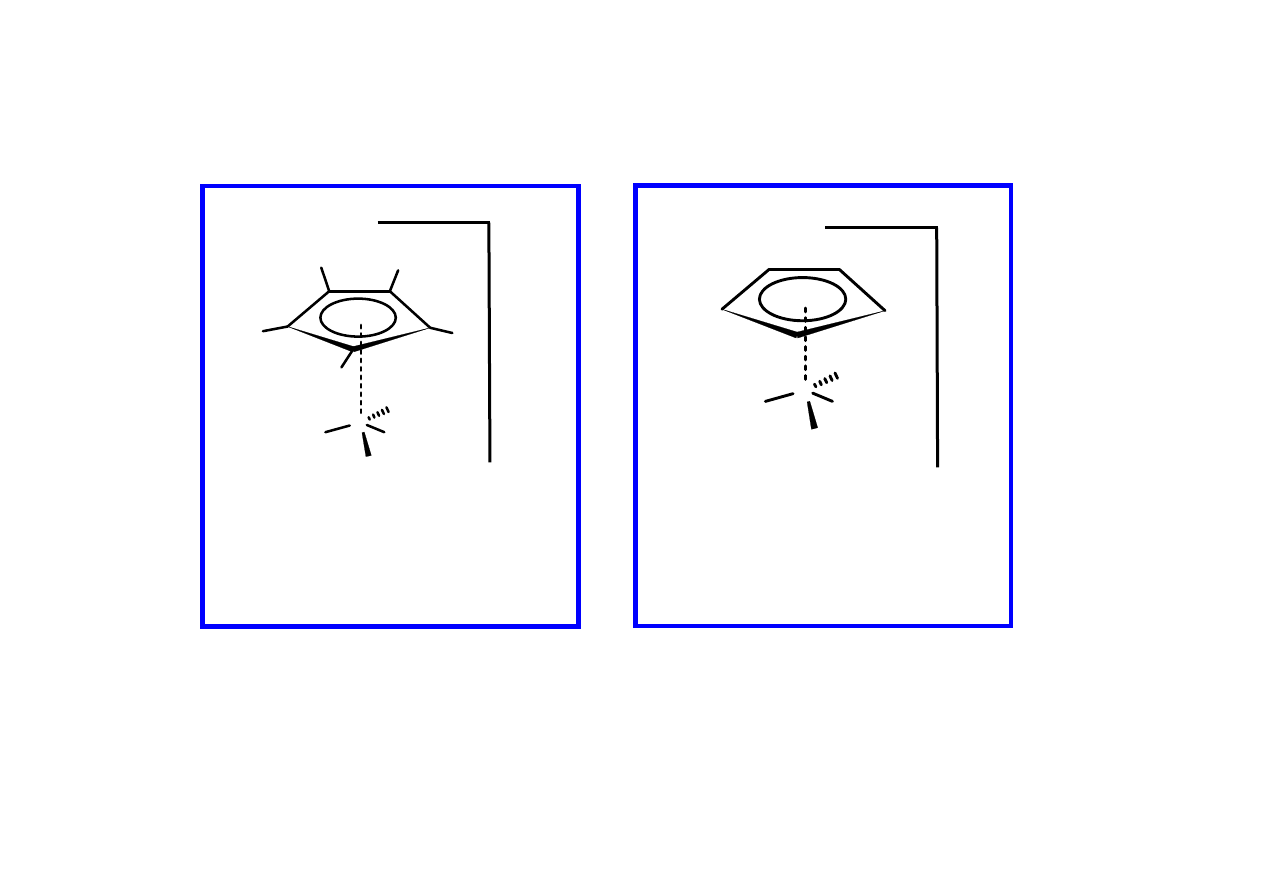
M.Heinekey, A.Hinkle, J.Close, J. Am. Chem. Soc., 1996, 118, 5353
Ir
H
H
H
Ph
3
P
Me
Me
Me
Me
Me
Ir
H
H
H
Ph
3
P
2
J(
H
,
H
) = 36.6 Hz (125 K)
99.0 Hz (201 K)
2
J(
H
,
H
) = 160 Hz (125 K)
533 Hz (201 K)
+
+
Nietypowe sprz
ęż
enia
2
J(
1
H,
1
H) w wodorkach niektórych metali
„Quantum Mechanical Exchange Coupling”
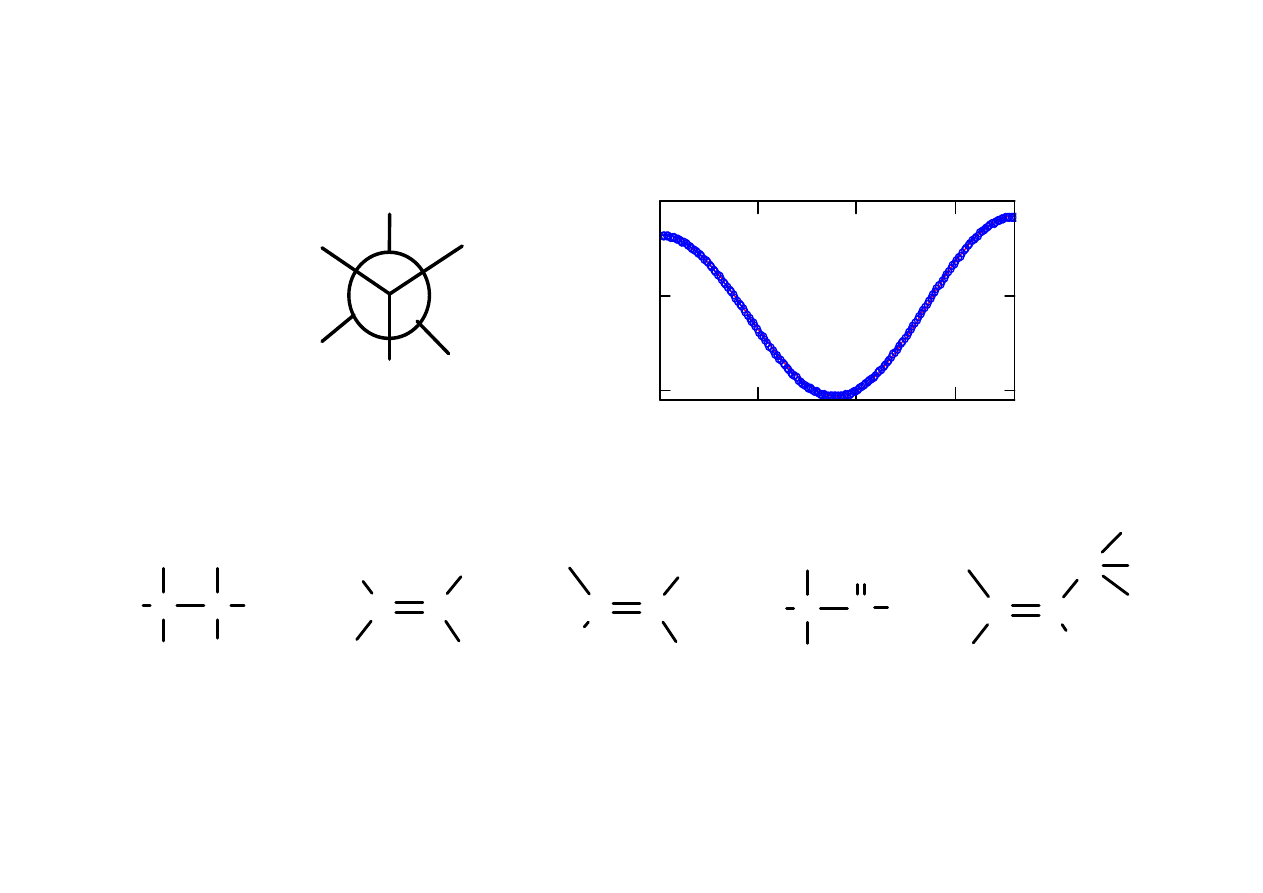
Zale
ż
no
ść
Karplusa
3
J = 8.5 cos
2
φφφφ
– 0.3 (0 – 90
o
)
3
J = 9.5 cos
2
φ
φ
φ
φ
– 0.3 (90 – 180
o
)
0
50
100
150
0
5
10
H
H
φφφφ
3
J [Hz]
k
ą
t
φφφφ
[
o
]
Wicynalna stała sprz
ęż
enia
3
J
vic
2
÷÷÷÷
9 Hz
6
÷÷÷÷
14 Hz
11
÷÷÷÷
18 Hz
4
÷÷÷÷
10 Hz
3
÷÷÷÷
7 Hz
C
C
H
H
C
C
H
H
C
C
H
H
C
C
C
H
H
C
C
H
H
O
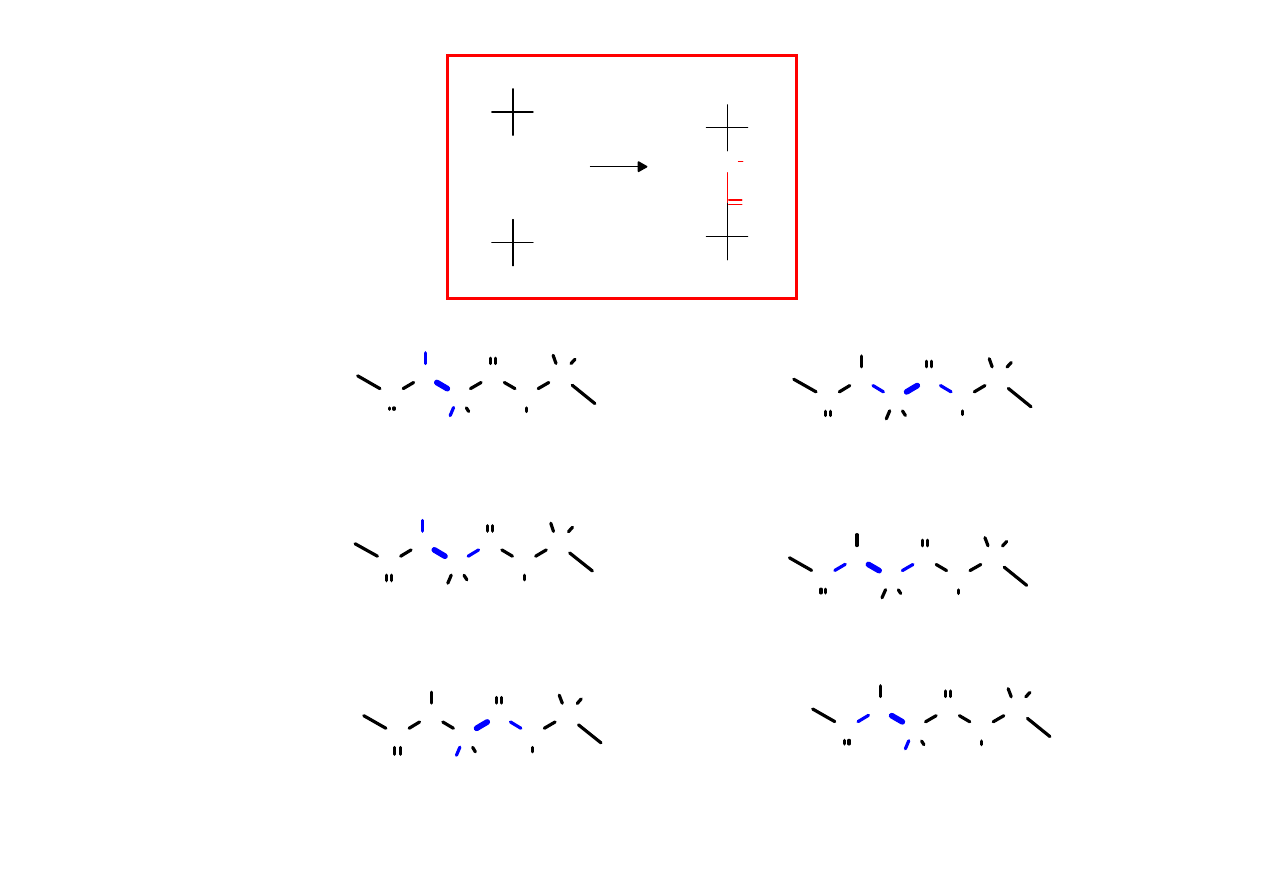
COOH
H
NH
2
R
COOH
H
NH
2
R
H
NH
2
R
COOH
H
R
O
N
H
C
N
H
C
R
C
N
O
H
C
R
H
O
H
C
N
H
C
R
C
N
O
H
C
R
H
O
H
C
N
H
C
R
C
N
O
H
C
R
H
O
H
C
N
H
C
R
C
N
O
H
C
R
H
O
H
C
N
H
C
R
C
N
O
H
C
R
H
O
H
C
N
H
C
R
C
N
O
H
C
R
H
O
H
3
J(
1
H-
1
H)
3
J(
13
C-
1
H)
3
J(
15
N-
1
H)
3
J(
15
N-
15
N)
3
J(
13
C-
13
C)
3
J(
13
C-
1
H)
3
J = Acos
2
(
φφφφ
+
αααα
) + Bcos(
φφφφ
+
αααα
) + C
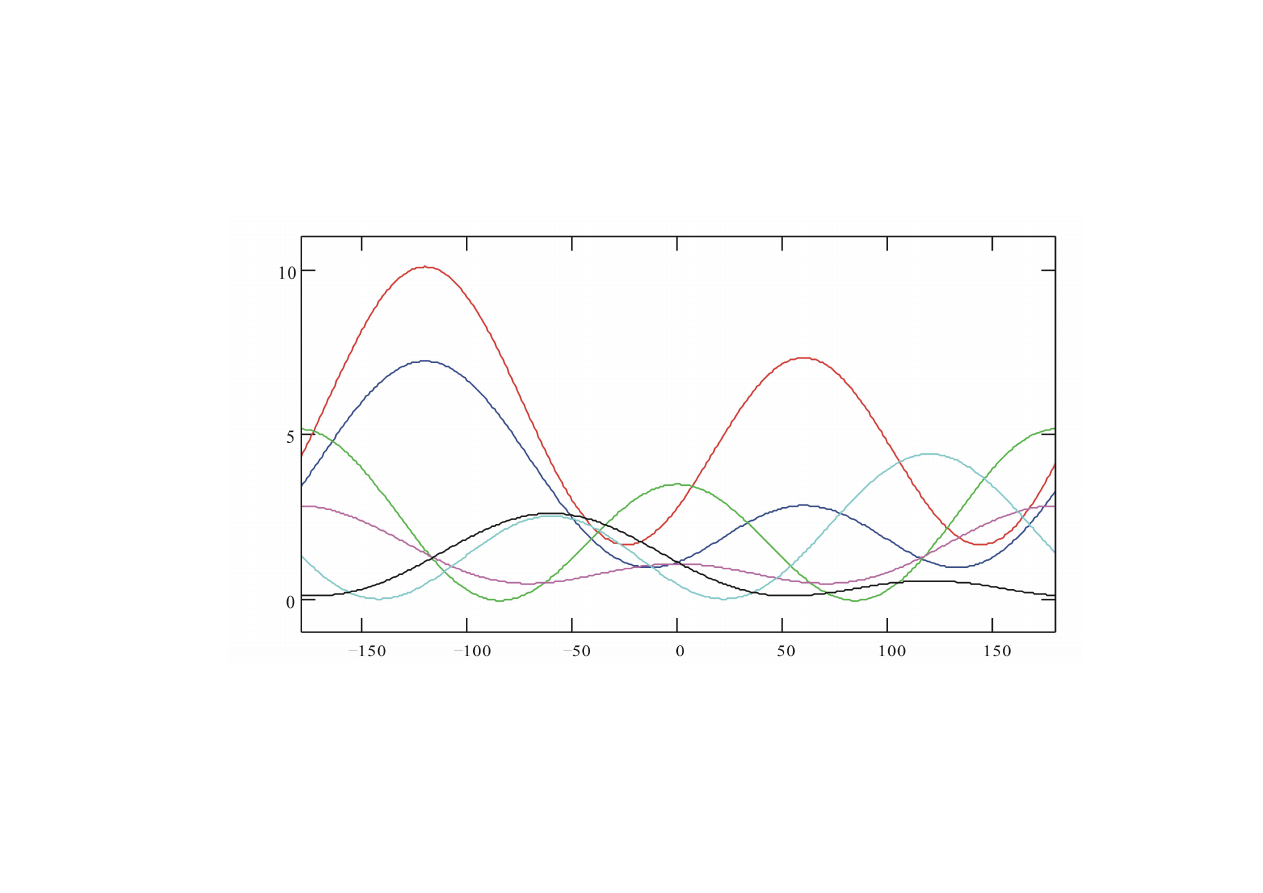
3
J [Hz]
k
ą
t
φ
φ
φ
φ
[
o
]
3
J = Acos
2
(
φφφφ
+
αααα
) + Bcos(
φφφφ
+
αααα
) + C
A.Ejchart, „Scalar Couplings in Structure Determination of Proteins”
Bulletin of the Polish Academy of Sciences; Chemistry, 1999, 47(1) 1
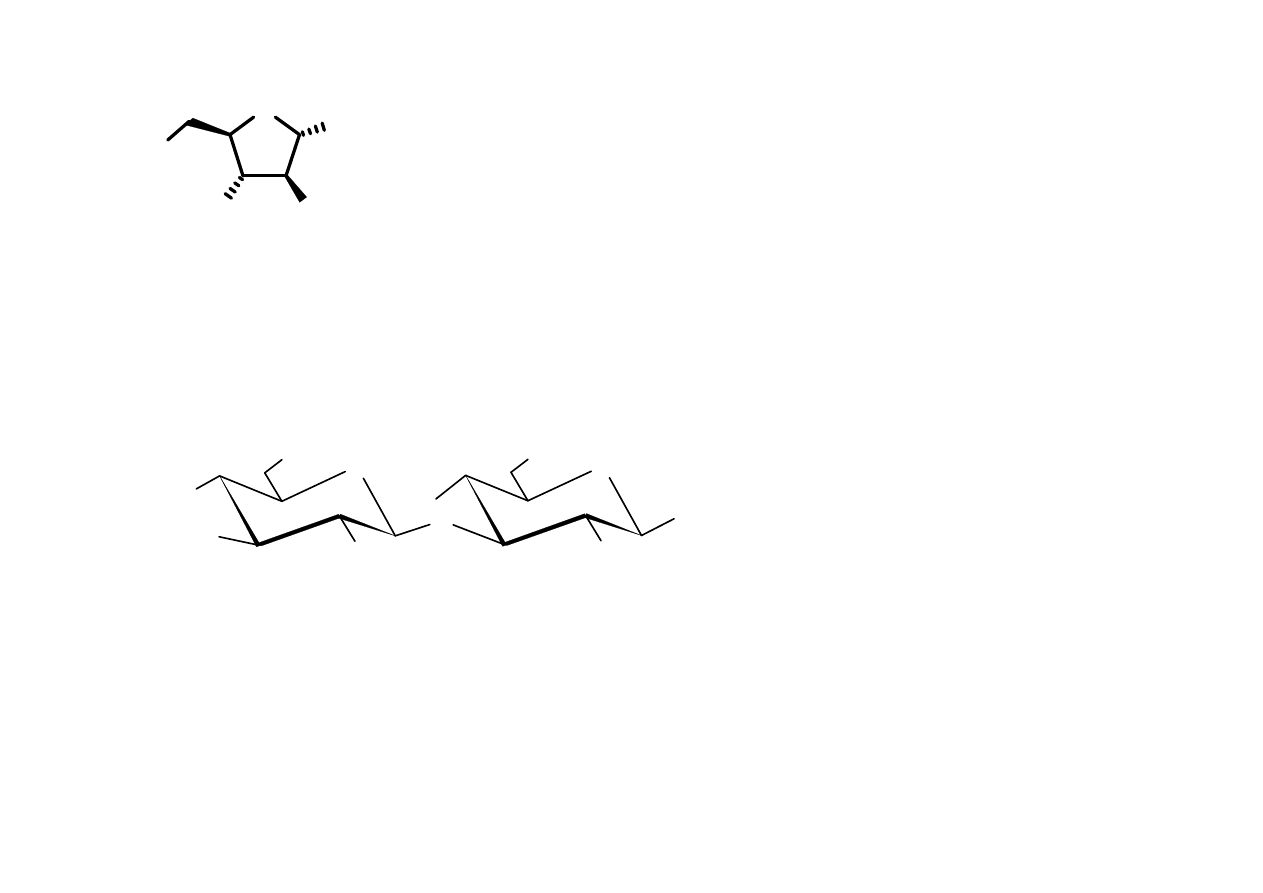
H. A. Taha, N. Castillo, D.N. Sears, R. E. Wasylishen, T. L. Lowary, P.-N. Roy, Journal of
Chemical Theory and Computation, 2010, 6, 212
O
O
H
OH
O
H
OMe
3
J(H,H) =
A
+
B
cos(
φφφφ
) +
C
cos (2
φφφφ
)
Parametryzacja równania: na podstawie 90 konformerów
O
OH
OH
O
H
O
H
O
O
H
O
OH
OH
OMe
N. J. Christensen, P. I. Hansen, F. H. Larsen, T. Folkerman, M. S. Motawia, S. B. Engelsen,
Carbohydrate Research, 2010, 345, 464
3
J(H,C) =
0.8
–
0.7
cos(
φφφφ
) +
5.3
cos
2
(
φφφφ
)
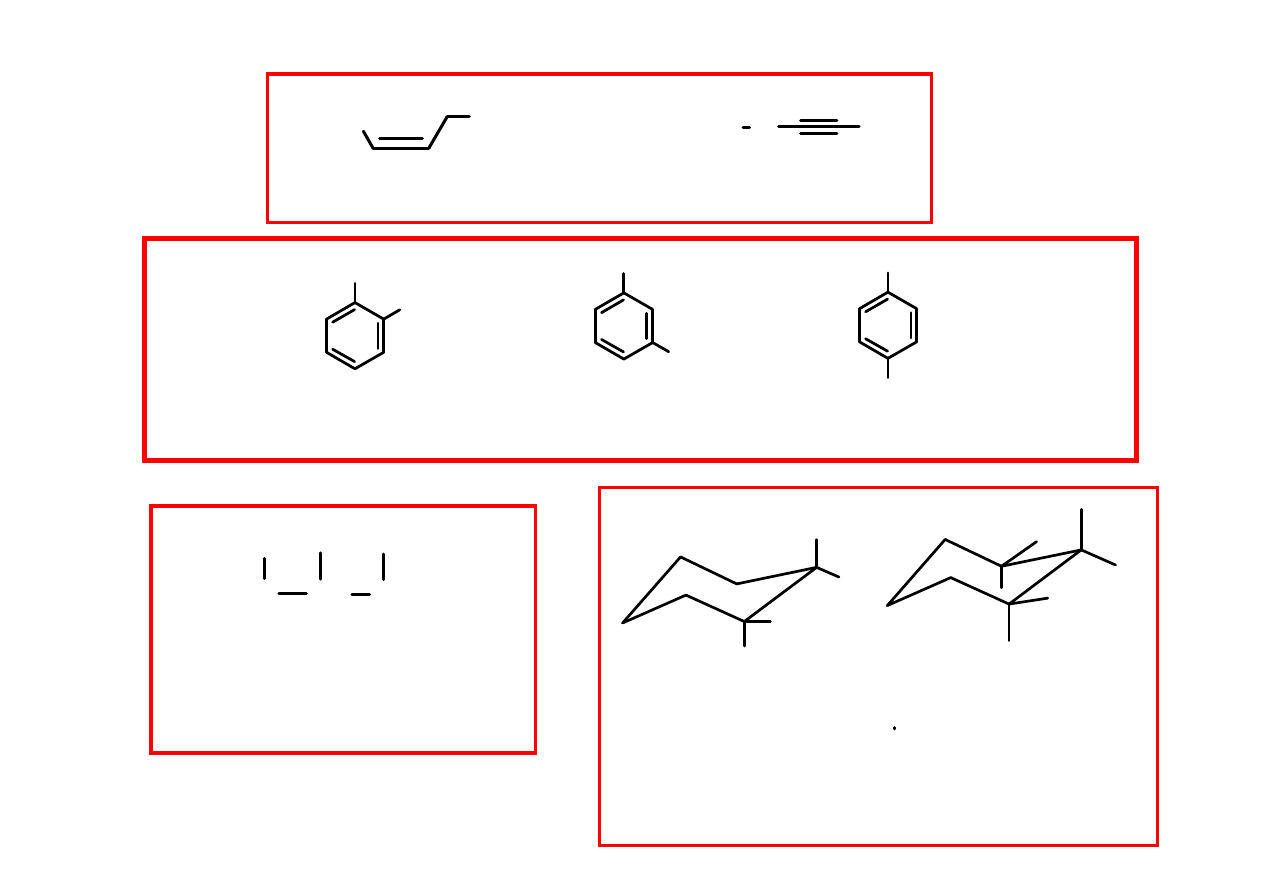
H
H
C
H
H
(- 3)
÷÷÷÷
(- 1) Hz
2
÷÷÷÷
3 Hz
H
H
H
H
H
H
3
J
orto
= 10
÷÷÷÷
13 Hz
5
J
para
= 0.1
÷÷÷÷
1 Hz
4
J
meta
= 2
÷÷÷÷
3 Hz
C
H
2
CH
H
CH
2
H
H
H
H
H
H
H
H
2
J
ax-eq
= (- 11)
÷÷÷÷
(- 13) Hz
3
J
ax-ax
= 11
÷÷÷÷
13 Hz
3
J
ax-eq
= 2
÷÷÷÷
5 Hz
3
J
eq-eq
= 2
÷÷÷÷
5 Hz
Sprz
ęż
enie „W”
ok. 1 Hz
3
J(
1
H
-
1
H
)
≠≠≠≠
0 Hz
4
J(
1
H-
1
H
)
≈≈≈≈
0 Hz

Widma NMR dziel
ą
si
ę
na widma
pierwszego
i
drugiego
rz
ę
du.
W widmach pierwszego rz
ę
du:
∆δ
∆δ
∆δ
∆δ
>> J
brak atomów magnetycznie nierównocennych
sprz
ęż
enia pomi
ę
dzy atomami chemicznie równocennymi
nie wpływaj
ą
na
krotno
ść
(multipletowo
ść
) sygnałów; np. sygnał grupy CH
3
jest singletem,
znak stałej sprz
ęż
enia nie wpływa na struktur
ę
multipletu,
δδδδ
i J mo
ż
na odczyta
ć
wprost z widma
W widmach drugiego rz
ę
du:
∆δ
∆δ
∆δ
∆δ ≈≈≈≈
J, i / lub s
ą
atomy nierównocenne magnetycznie
sprz
ęż
enia pomi
ę
dzy atomami chemicznie równocennymi i znak stałej
sprz
ęż
enia
wpływaj
ą
na struktur
ę
sygnałów
Trudna analiza multipletów
Konstrukcja multipletów

Praca domowa:
konstrukcja multipletów w widmach I rz
ę
du
ilo
ść
sygnałów vs. struktura zwi
ą
zku
przesuni
ę
cie chemiczne vs. struktura zwi
ą
zku

1
1
1
1
1
1
1
1
2
1
1
1
1
1
2
1
1
3
3
1
1
1
1
1
2
1
1
3
3
1
4
6
4
1
CH
CH
CH
CH
2
CH
CH
3
CH
CH
3
CH

C
H
C
H
3
CH
3
CH
3
Praca domowa: jak wygl
ą
da sygnał „czerwonego” atomu wodoru
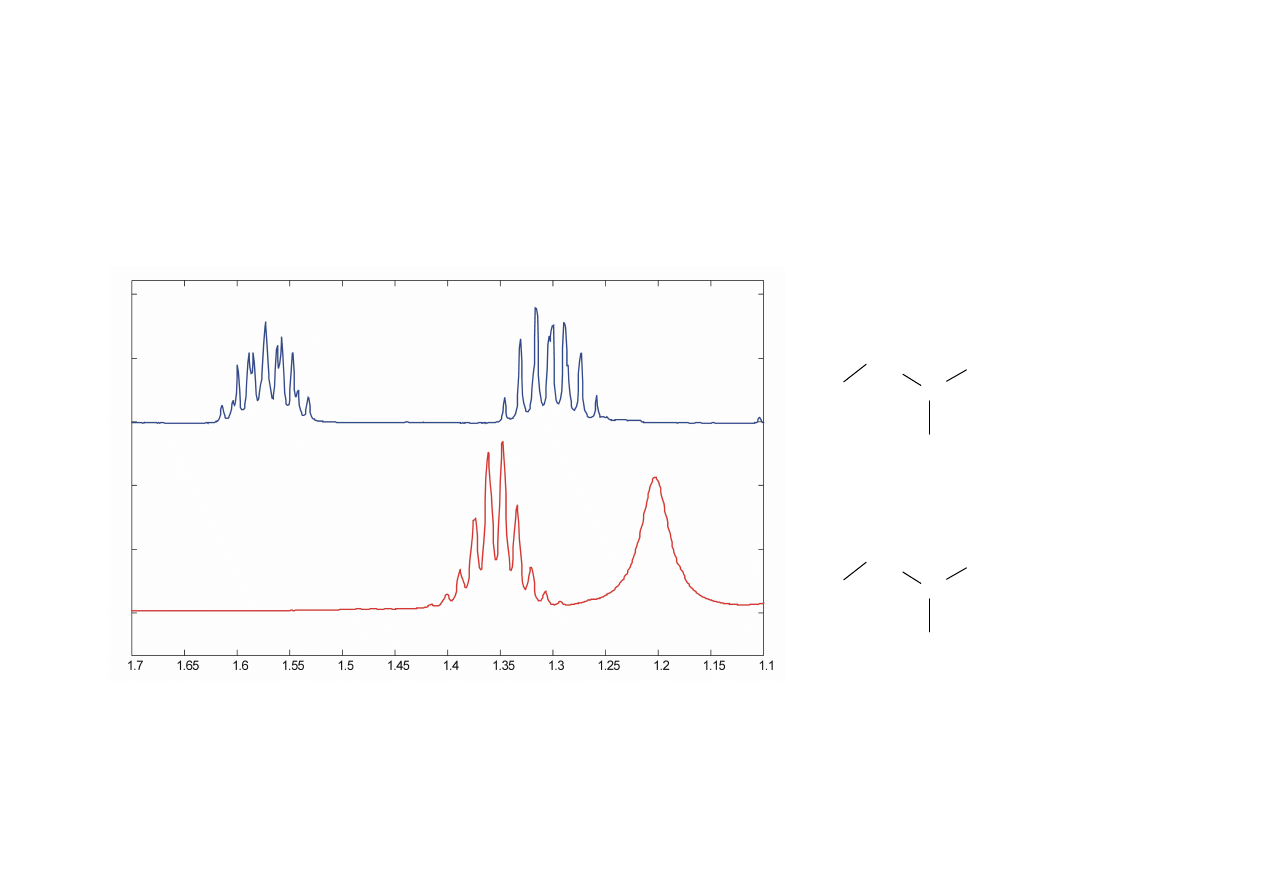
C
H
3
CH
2
CH
CH
3
NH
2
C
H
3
CH
2
CH
CH
3
N(CH
3
)
2
NH
Nierównocenno
ść
protonów w grupie CH
2
(widmo w CDCl
3
)
ppm
Układ A
3
MNX

Widma protonowe drugiego rz
ę
du
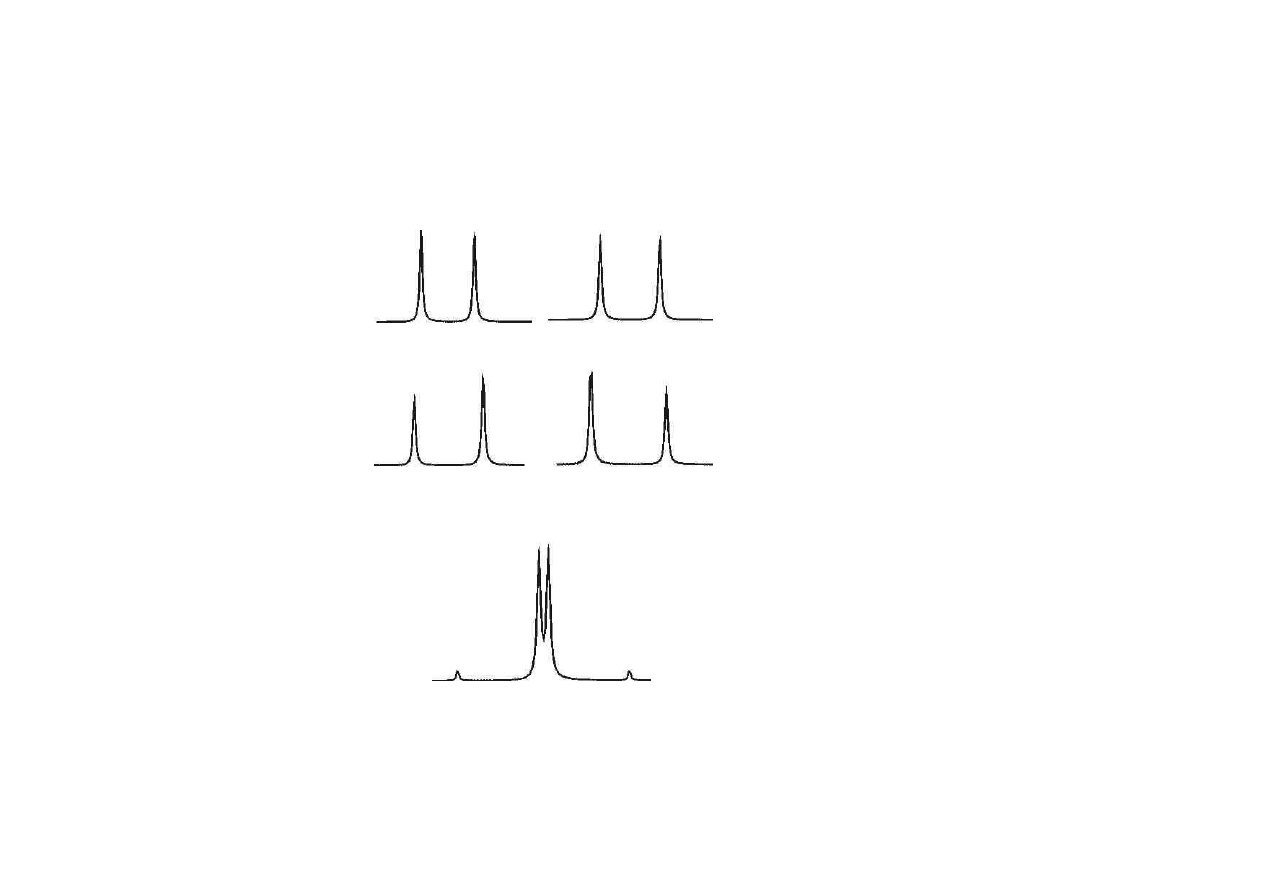
AX
AM
AB
J
≈≈≈≈ ∆δ
∆δ
∆δ
∆δ
widmo drugiego rz
ę
du
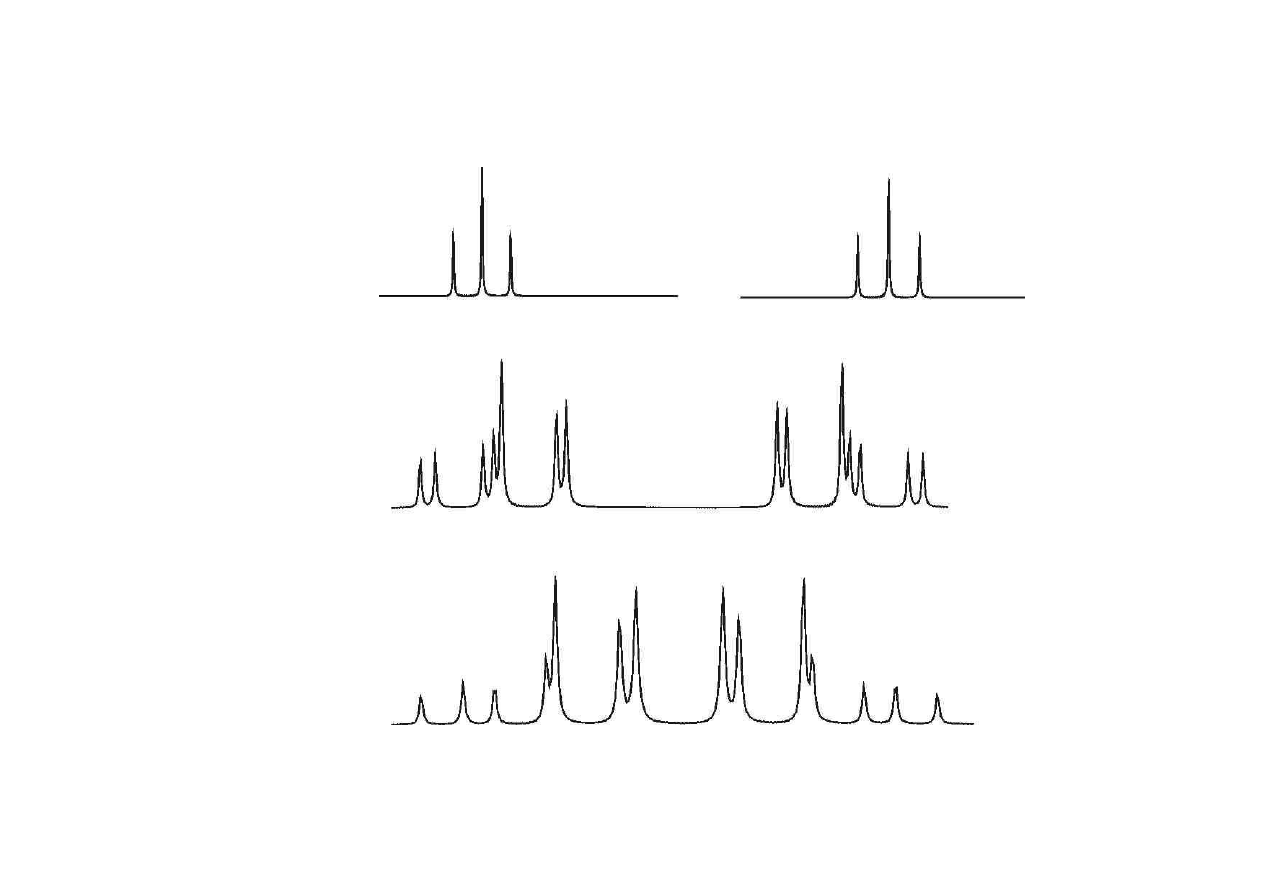
XCH
2
-CH
2
Y
A
2
X
2
A
2
M
2
A
2
B
2
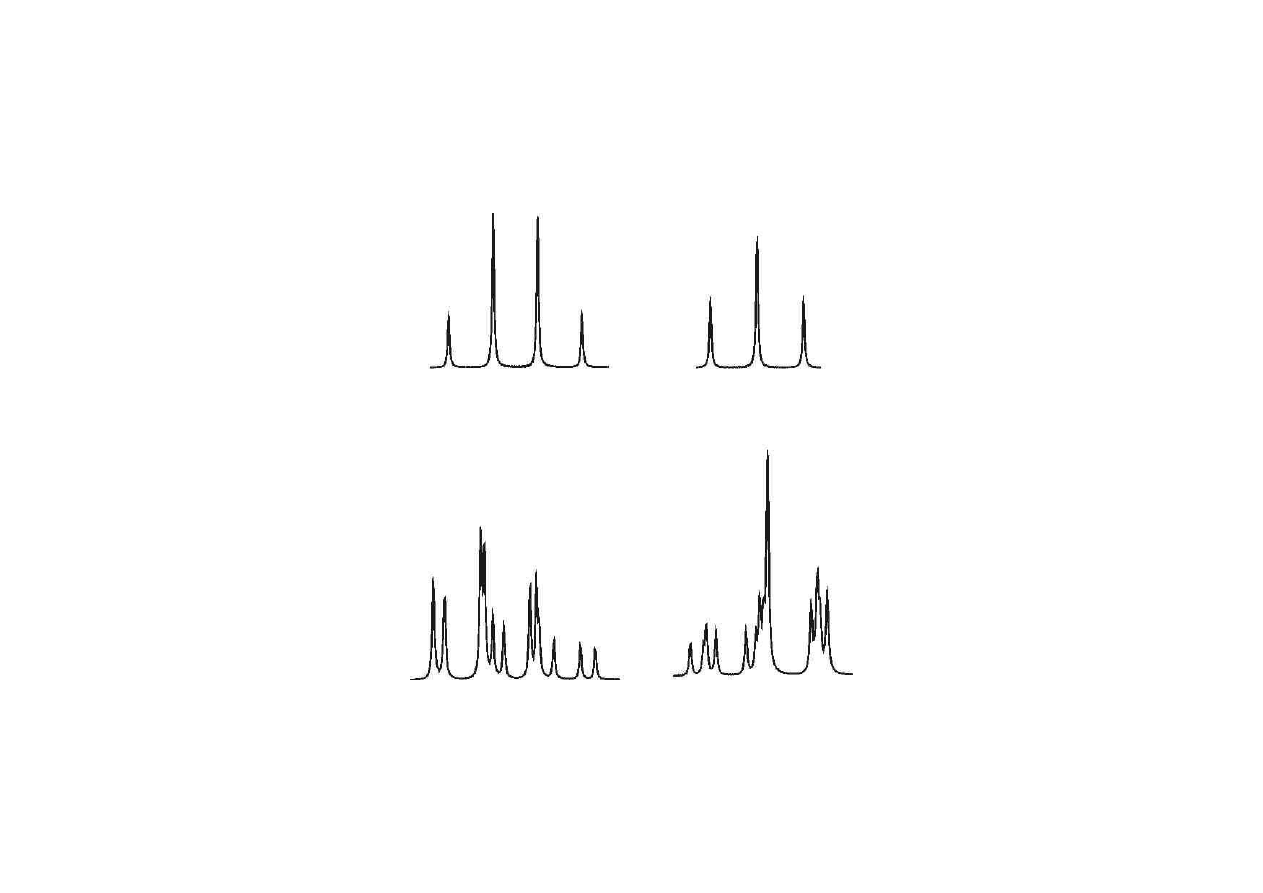
-CH
2
CH
3
A
2
X
3
A
2
B
3
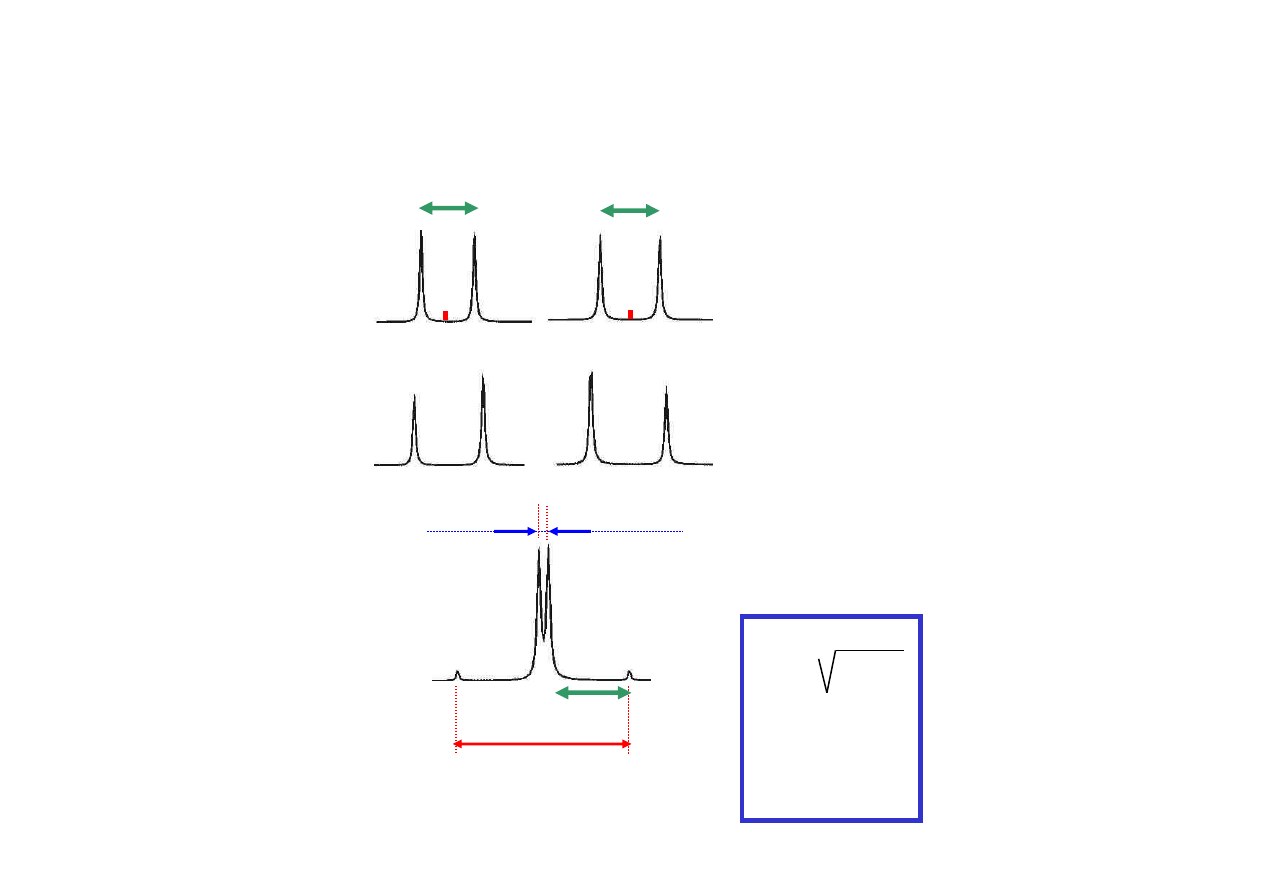
AX
AM
AB
J
≈≈≈≈ ∆δ
∆δ
∆δ
∆δ
widmo drugiego rz
ę
du
a
b
∆δ
∆δ
∆δ
∆δ =
=
=
=
a
*
b
δδδδ
x
=
δδδδ
0
–
∆δ
∆δ
∆δ
∆δ
/2
δδδδ
y
=
δδδδ
0
+
∆δ
∆δ
∆δ
∆δ
/2
J
J
J
δδδδ
x
δδδδ
y
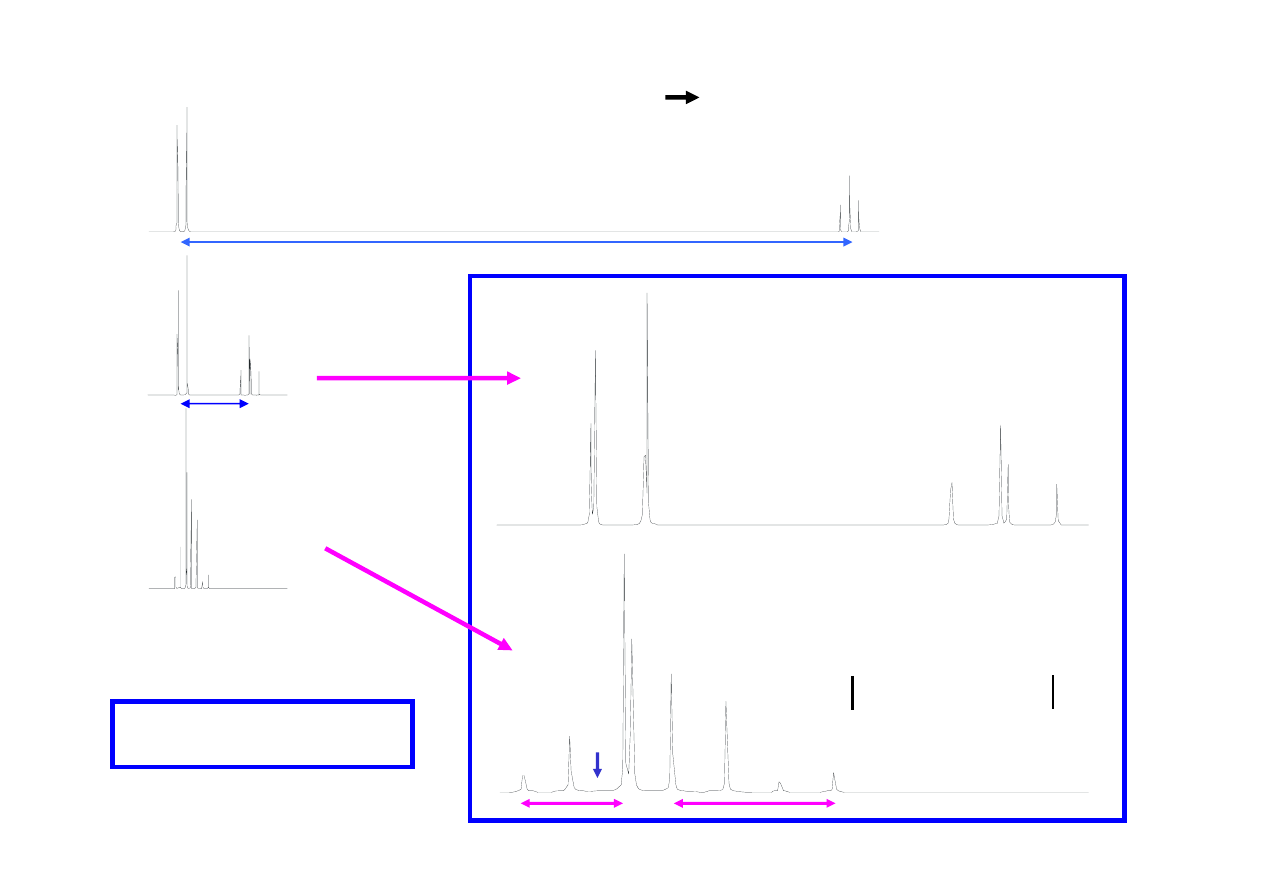
∆δ
∆δ
∆δ
∆δ
= 1 ppm (500 Hz)
J = 7 Hz
∆δ
∆δ
∆δ
∆δ
= 0.1 ppm (50 Hz)
∆δ
∆δ
∆δ
∆δ
= 0.02 ppm (10 Hz)
Układ spinowy AX
2
AB
2
A
X
! dla
∆δ
∆δ
∆δ
∆δ
= 0 ppm pozostanie
tylko jedna linia (układ A
3
)
6
5
6
1
2
3
4
8
7
1
2
3
4
5
8
7
δδδδ
A
δδδδ
B
= (
δδδδ
5
+
δδδδ
7
) / 2
δδδδ
B
J
AB
= (
νννν
1
-
νννν
4
) + (
νννν
6
–
νννν
8
) / 3
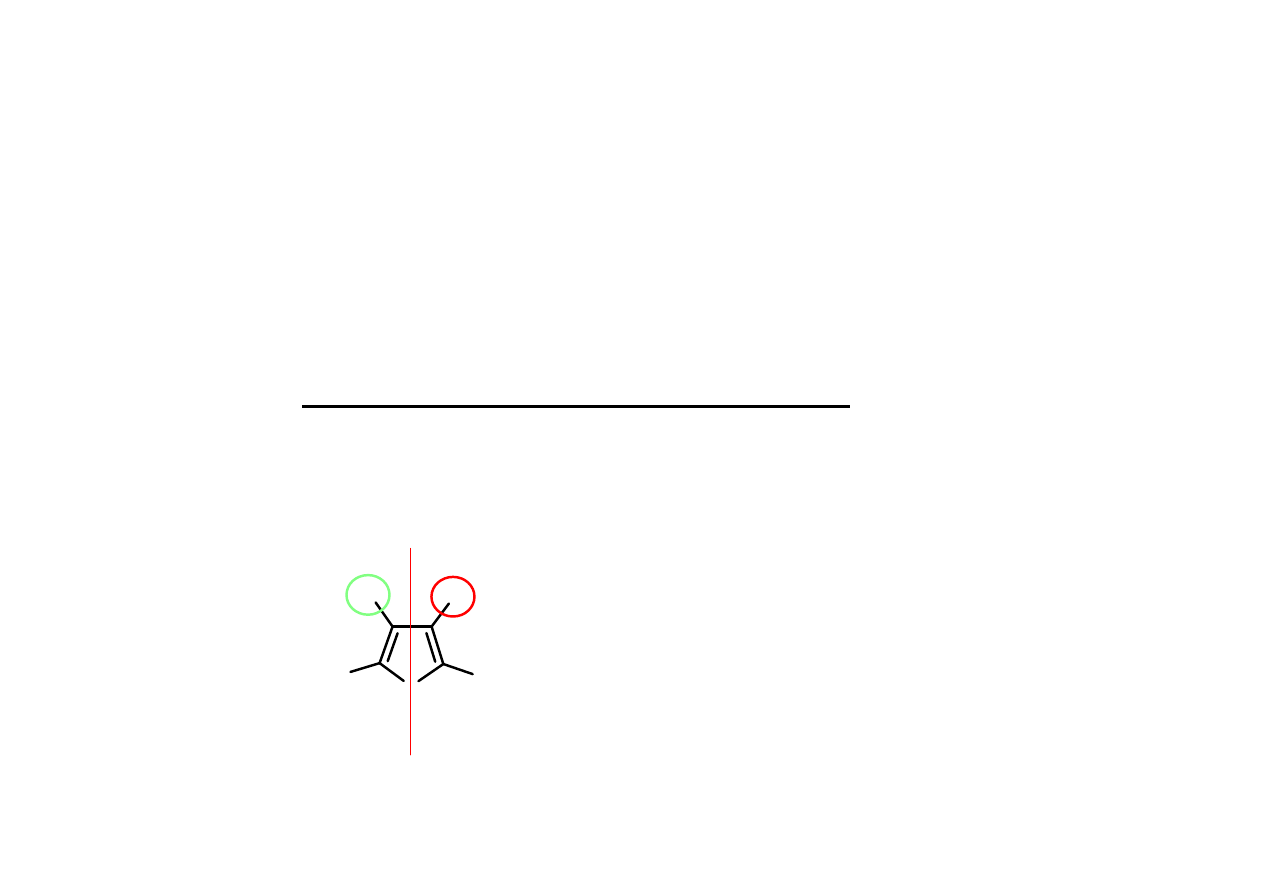
Dwa atomy s
ą
równocenne magnetycznie, kiedy:
s
ą
równocenne chemicznie
stałe sprz
ęż
enia tych atomów z dowolnym innym
atomem w cz
ą
steczce s
ą
identyczne
Równocenno
ść
/ nierównocenno
ść
magnetyczna: dotyczy atomów
równocennych chemicznie
NIERÓWNOCENNO
ŚĆ
MAGNETYCZNA
*
X
H
H
H
H
δδδδ
H
=
δδδδ
H
δδδδ
H
=
δδδδ
H
A
2
X
2
??
3
J(
H
H
)
≠≠≠≠
4
J(
H
H
) AA’XX’ (AA’BB’)
*
próbka w roztworze
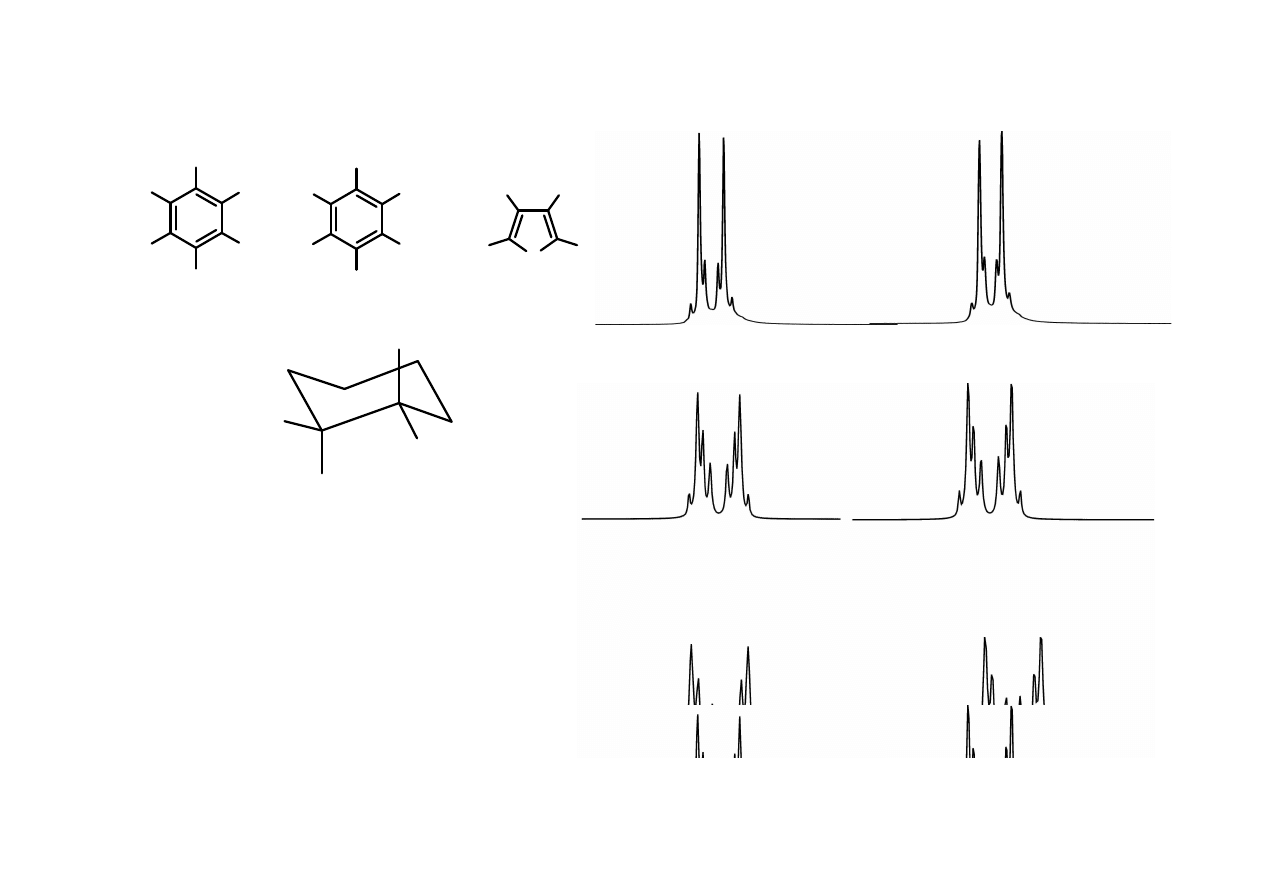
H
H
H
H
Z
Z
Z
Y
H
H
H
H
Z
H
H
H
H
H
H
H
H
Układ spinowy AA’XX’ (AA’BB’)
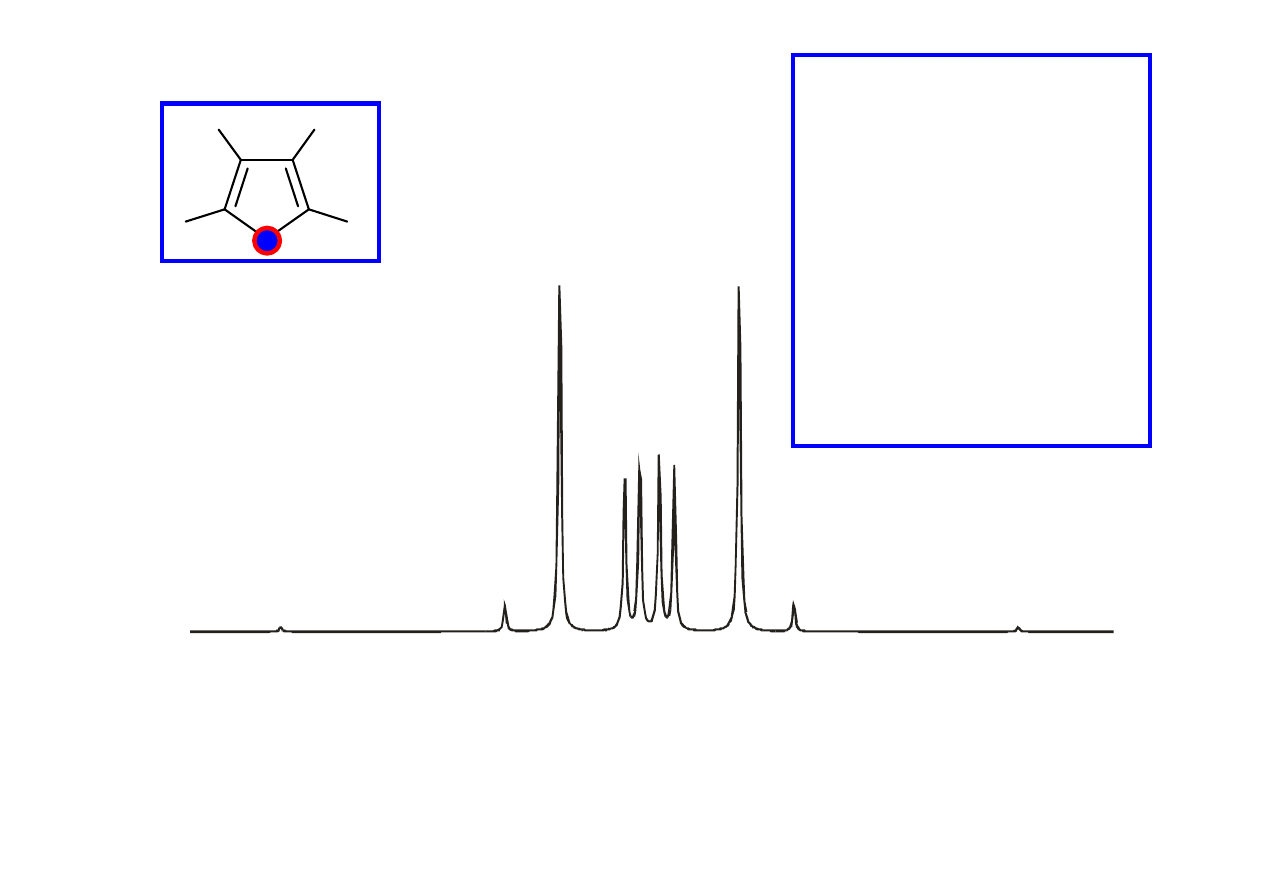
7,8
1,2
3
4
5
6
9
10
11
12
N =
νννν
1,2
–
νννν
7,8
K =
νννν
3
–
νννν
4
=
νννν
5
–
νννν
6
M =
νννν
9
–
νννν
10
=
νννν
11
–
νννν
12
(2O)
2
= (
νννν
3
–
νννν
5
)
2
= (
νννν
4
–
νννν
6
)
2
(2P)
2
= (
νννν
9
–
νννν
11
))))
2
= (
νννν
10
–
νννν
12
)
2
L = [(2O)
2
– K
2
]
0.5
= [(2P)
2
– M
2
]
0.5
N = J
AX
+ J
AX’
L = J
AX
– J
AX’
K = J
AA’
+ J
XX’
M = J
AA’
– J
XX’
E. W. Garbisch, Journal of Chemical Education,
1968, 45(5), 311 – 320
1968, 45(6), 402 – 416
1968, 45(7), 480 – 492
X
A
X
X'
A'
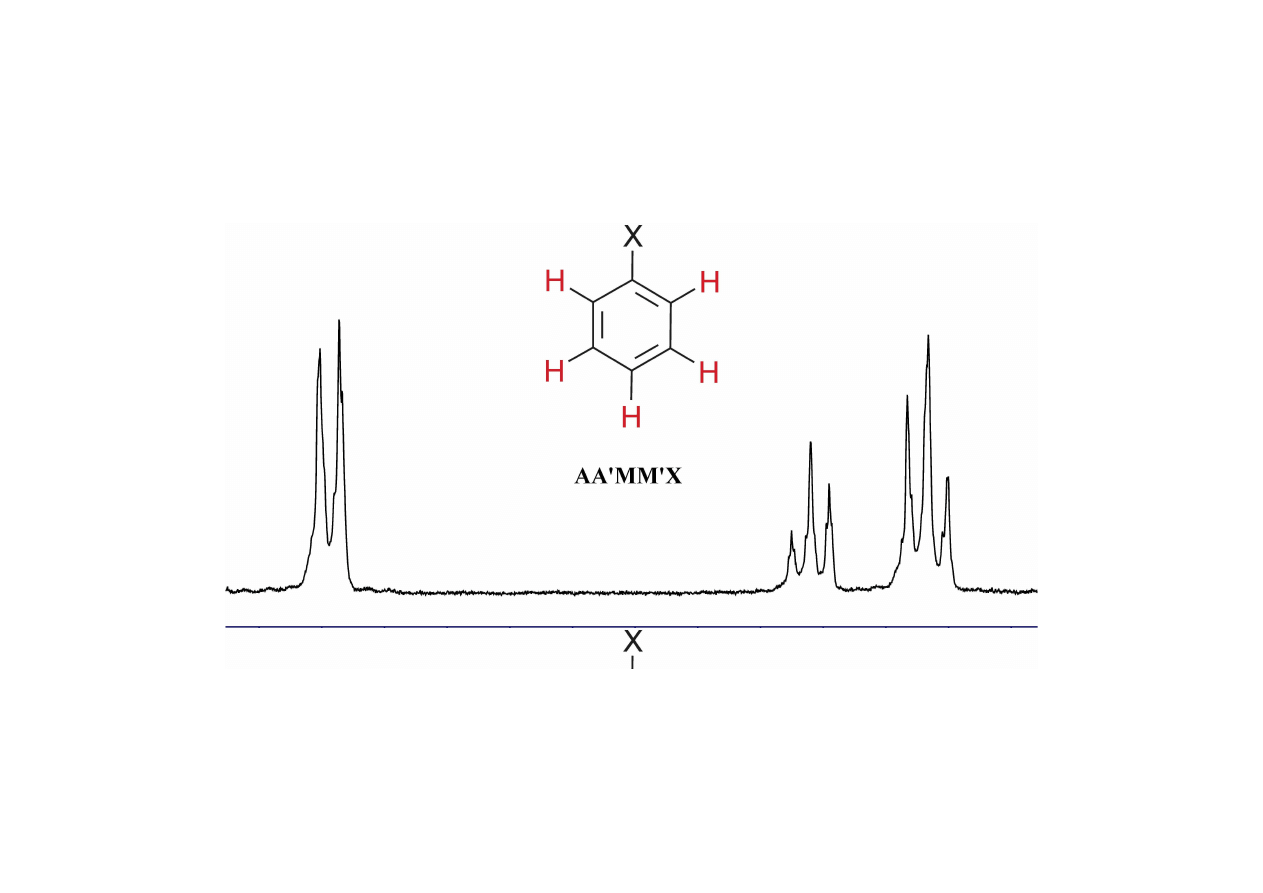
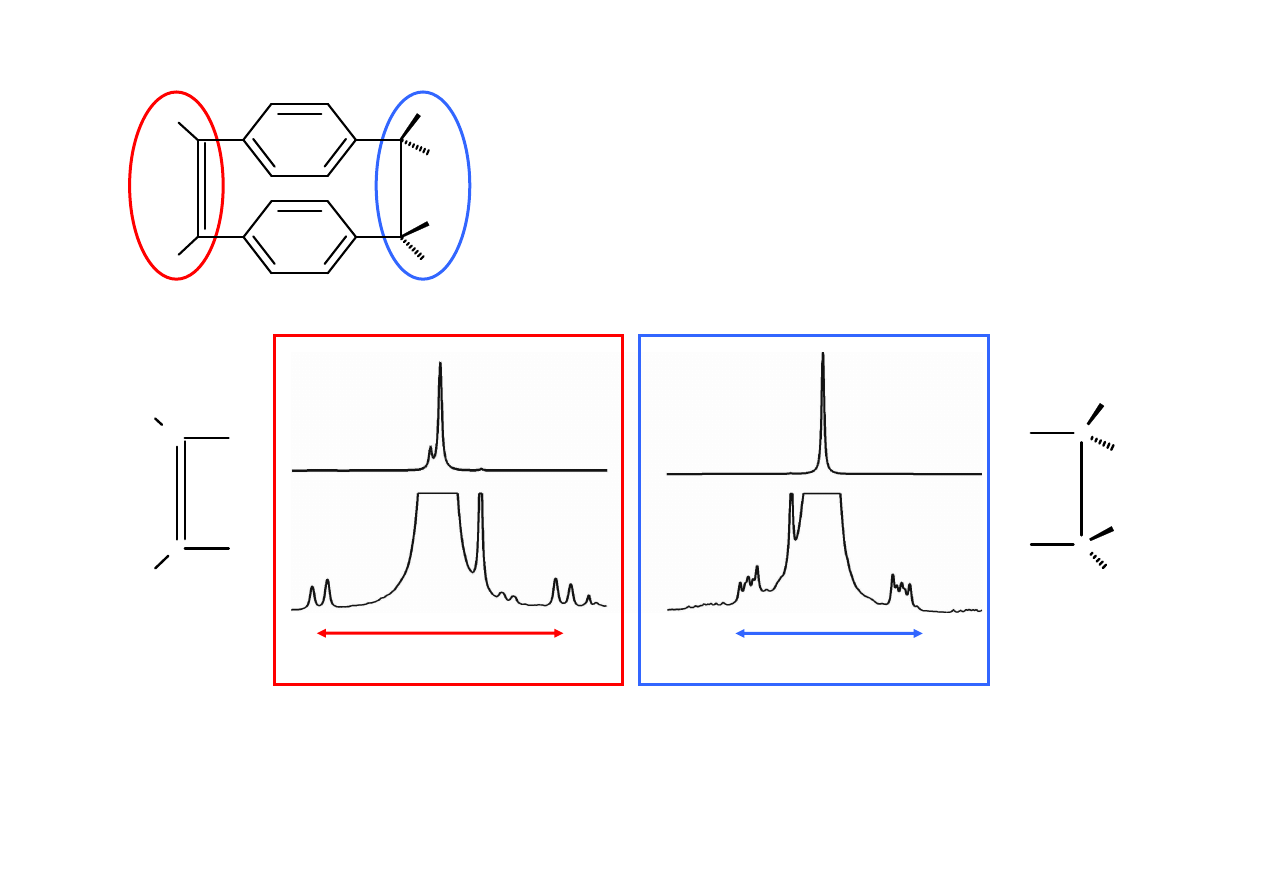
Układ AA’MM’X
≈≈≈≈
A
2
M
2
X
1
J(
13
C,
1
H)
3
J(
1
H,
1
H)
układ ABX
1
J(
13
C,
1
H)
*
*
*
*
*
H
H
H
H
H
H
C
12
C
13
H
H
H
H
układ AA’BB’ X
C
13
C
12
H
H
*
WIDMO SATELITARNE: POMIAR J(H,H)
~1%
~1%
dwa atomy
13
C obok siebie: ~0.01%
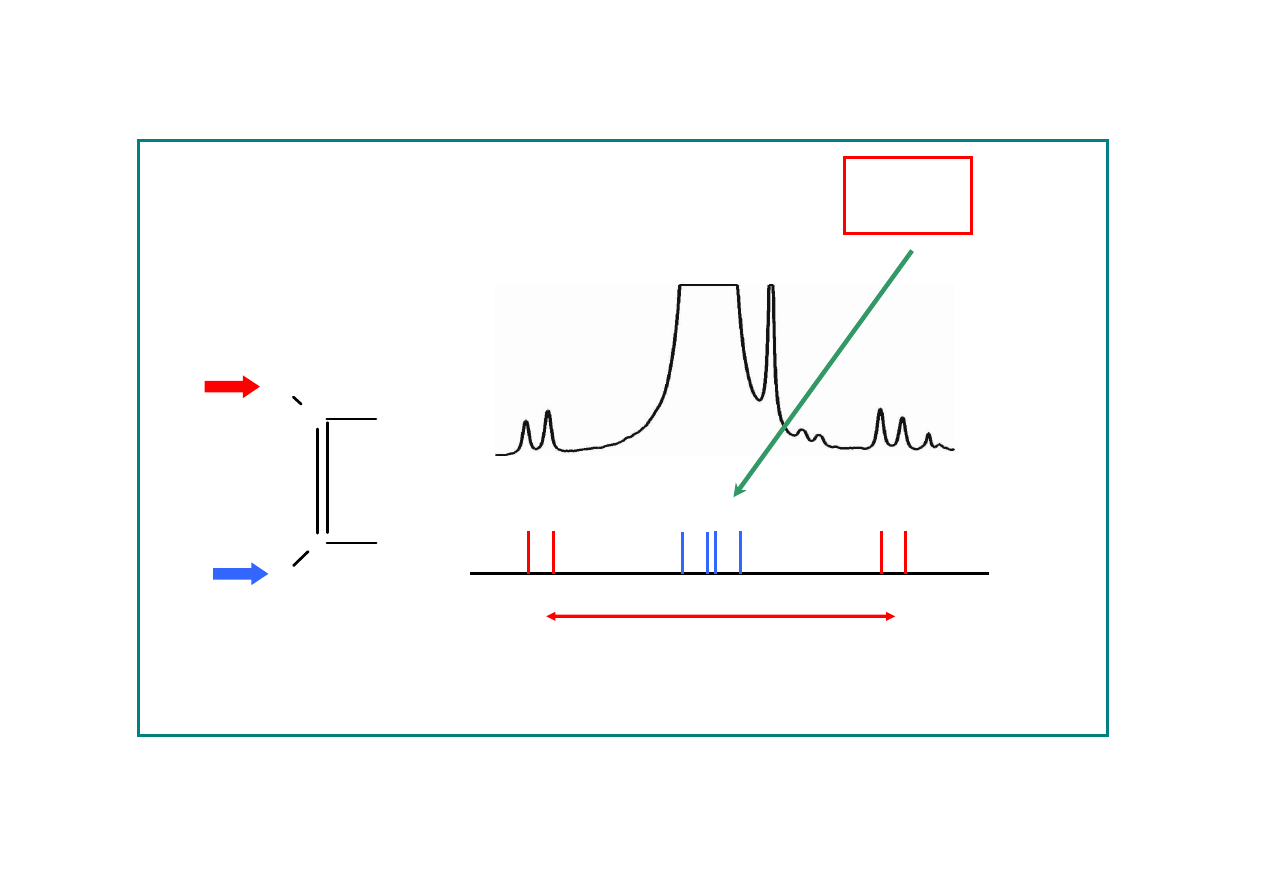
1
J(
13
C,
1
H)
3
J(
1
H,
1
H)
C
13
C
12
H
H
2
J(
13
C,
1
H)
3
J(
1
H,
1
H)
δδδδ
H
≠
δδδδ
H
efekt izotopowy !!

POMIAR
1
H NMR I PRZYCZYNY BŁ
Ę
DÓW
cz.2

Przygotowanie próbki
Próbka o odpowiednim st
ęż
eniu, rozpuszczona w odpowiedniej ilo
ś
ci
deuterowanego rozpuszczalnika, bez osadu i stałych zanieczyszcze
ń
.
Czy mo
ż
na u
ż
y
ć
rozpuszczalnika nie deuterowanego ?
Brak sygnału deuteru; brak sygnału u
ż
ywanego do regulacji jednorodno
ś
ci pola
i do stabilizacji pola. Mo
ż
na ewentualnie u
ż
y
ć
sygnału FID-u.
CHCl
3
, CH
2
Cl
2
.... – konieczno
ść
usuwania sygnału rozpuszczalnika.
CCl
4
, CS
2
, freon ... – mo
ż
na u
ż
y
ć
; ew. zastosowa
ć
rozpuszczalnik deuterowany
w kapilarze.
Wzorzec: zewn
ę
trzny lub wewn
ę
trzny. Mo
ż
na u
ż
y
ć
sygnału resztkowego
rozpuszczalnika.
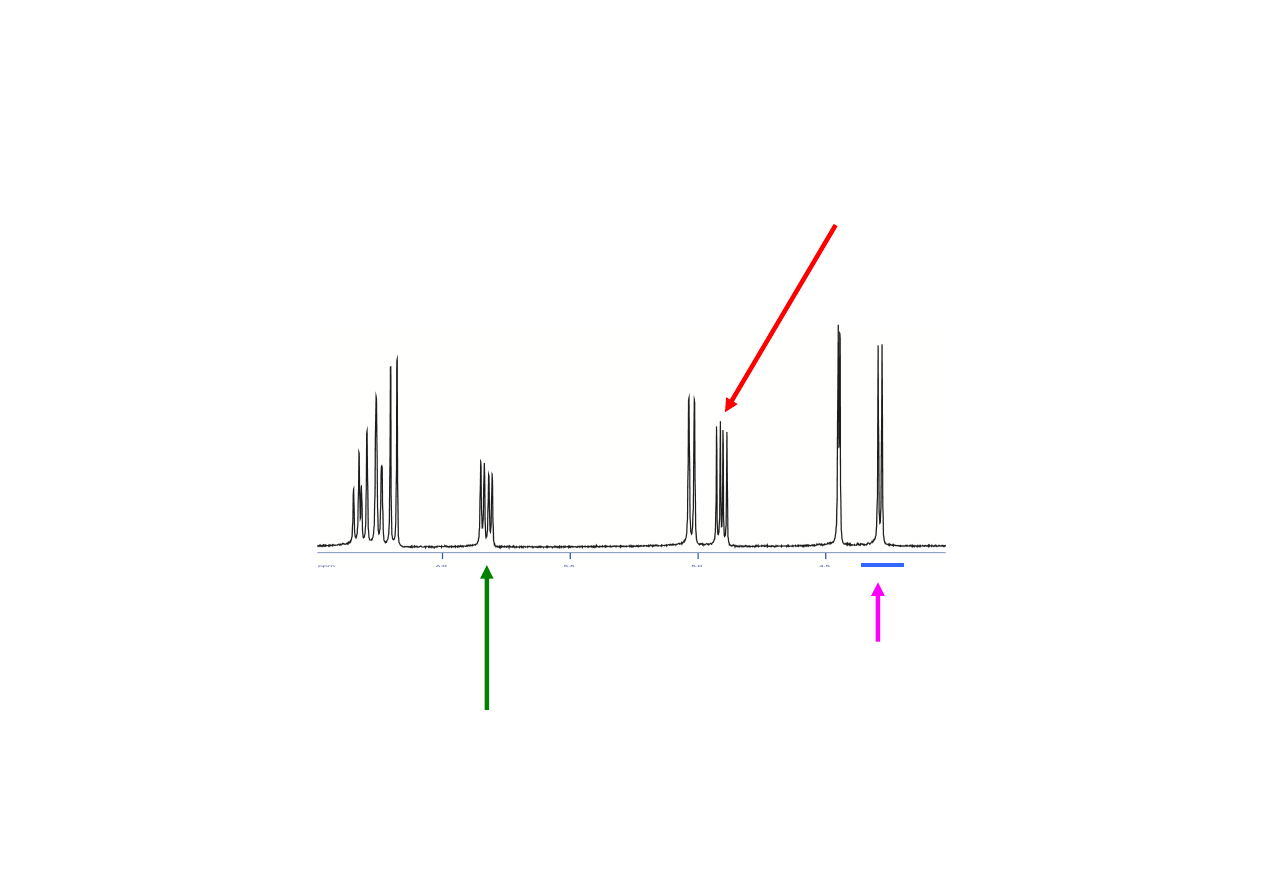
Przykładowe widmo
1
H NMR wykonane w roztworze:
stała sprz
ęż
enia J (Hz)
poło
ż
enie sygnału
(przesuni
ę
cie chemiczne)
intensywno
ść
integralna
„całka”
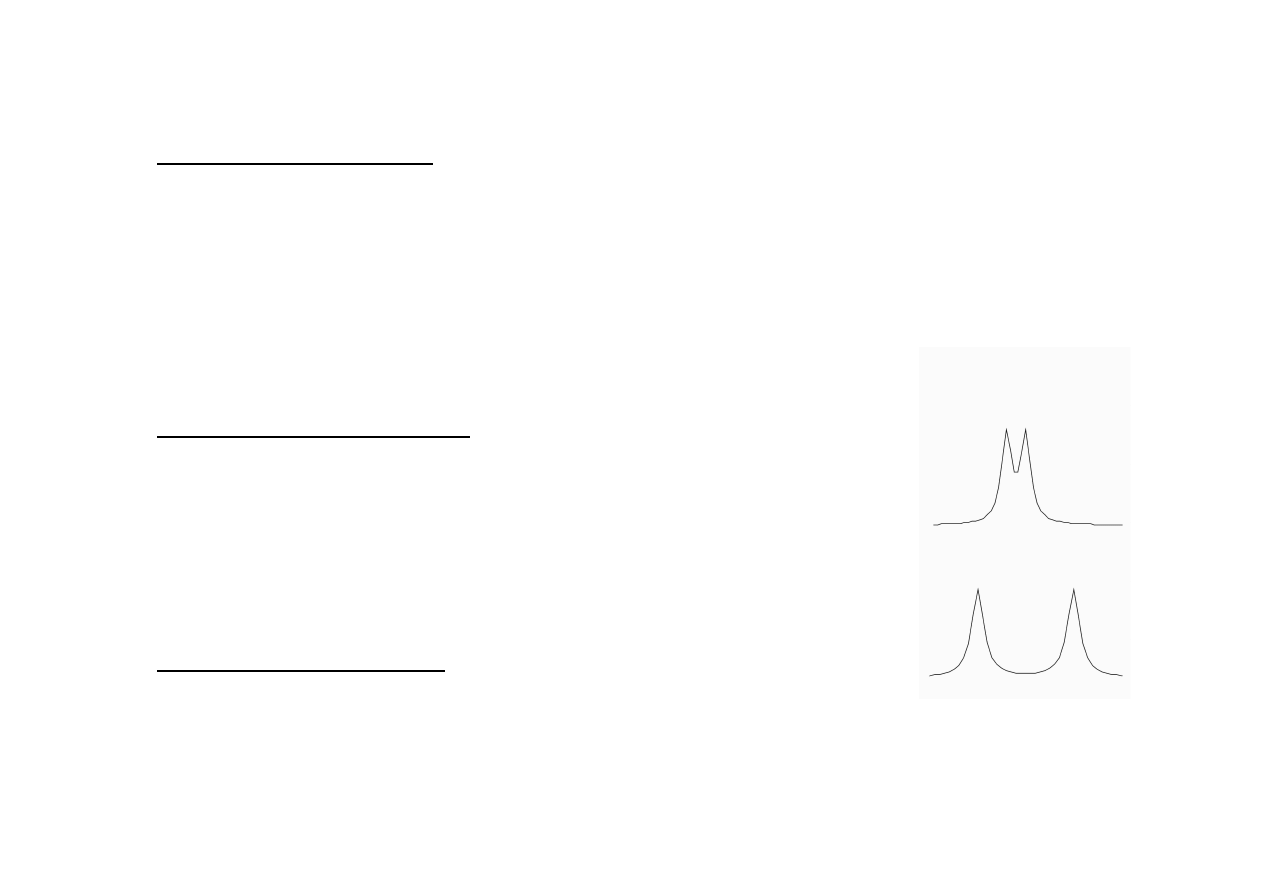
Przesuni
ę
cie chemiczne
niedoskonało
ść
wzorca („wewn
ę
trzny” TMS) – bł
ą
d do ± 0.5 ppm (
!!
). W precyzyjnych
pomiarach nale
ż
y stosowa
ć
wzorzec zewn
ę
trzny.
efekty st
ęż
eniowe, temperatura próbki, asocjacja zwi
ą
zku, itp.
rozdzielczo
ść
spektralna (0.3 – 0.8 Hz)
typowa dokładno
ść
δδδδ
(
1
H): nie wi
ę
cej ni
ż
± 0.01 ppm
Warto
ść
stałej sprz
ęż
enia J
rozdzielczo
ść
spektralna (0.3 – 0.8 Hz) (
!!!
)
nakładanie si
ę
sygnałów
typowa dokładno
ść
J: nie wi
ę
cej ni
ż
± 0.3 Hz
dokładno
ść
mo
ż
na zwi
ę
kszy
ć
poprzez optymalizacj
ę
pomiaru
Intensywno
ść
integralna:
niepełna relaksacja próbki
rozdzielczo
ść
spektralna
zaburzenia linii podstawowej widma, nieprawidłowa faza widma
typowy bł
ą
d: do 10%
BŁ
Ę
DY I ICH PRZYCZYNY
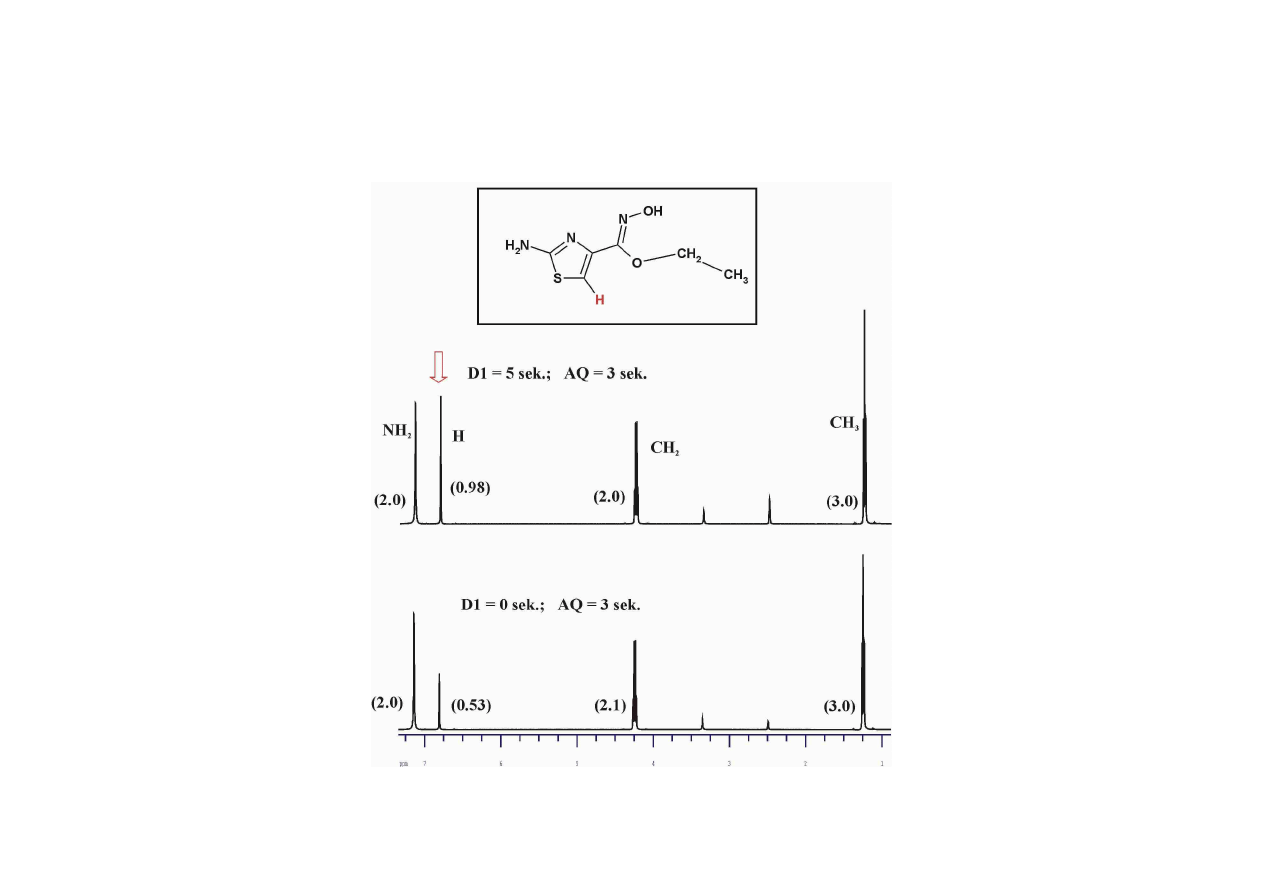
Niepełna relaksacja próbki
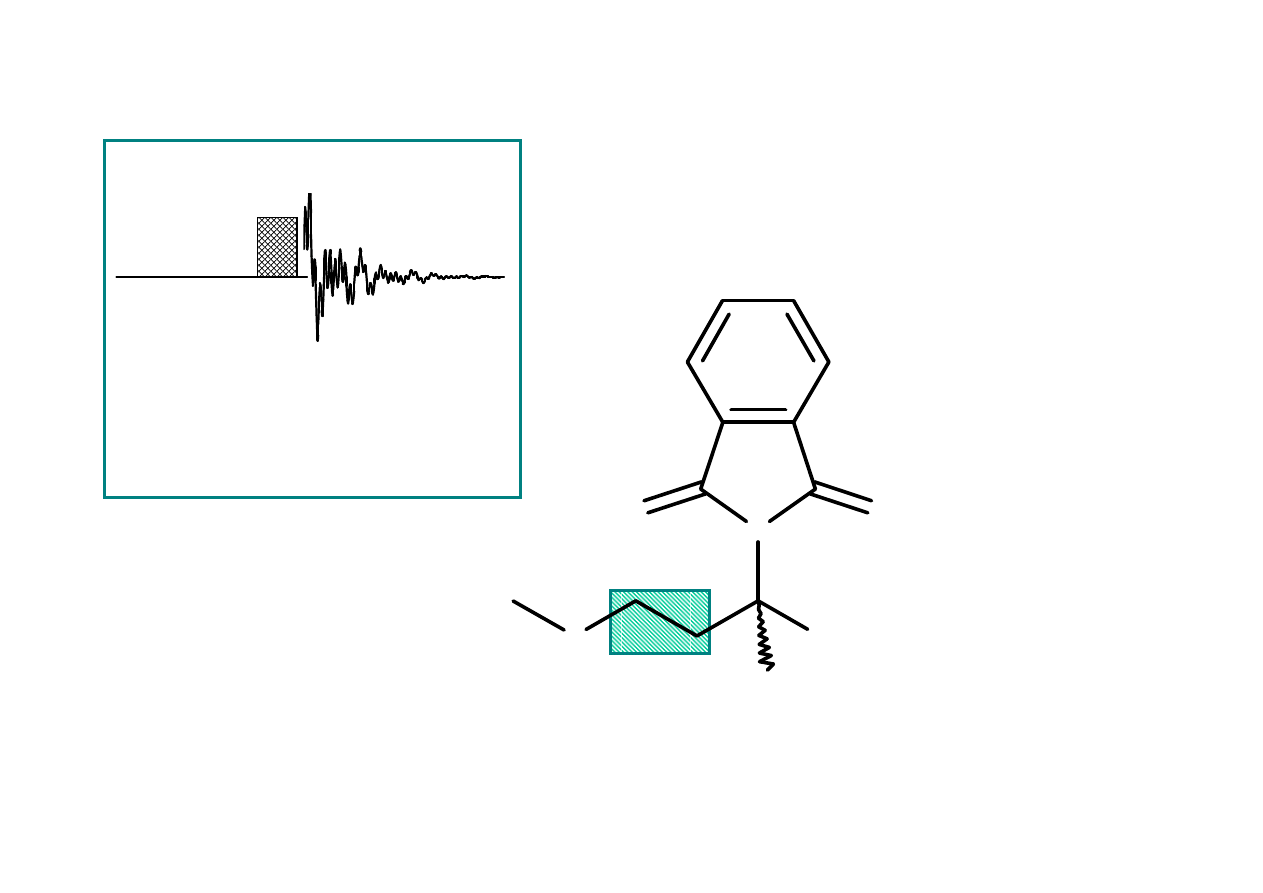
Widmo pochodnej metioniny w CDCl
3
– integracja sygnałów
AQ (at) = 2.34 s
d1 = 1 ms
d1 = 5 s
d1 = 10 s
S
N
O
O
COOMe
H
4H
df.
0.7
2.6
2.9
2.3
2.94
0.95
3.0
4.0
3.7
0.8
2.9
2.8
d1
pw
at
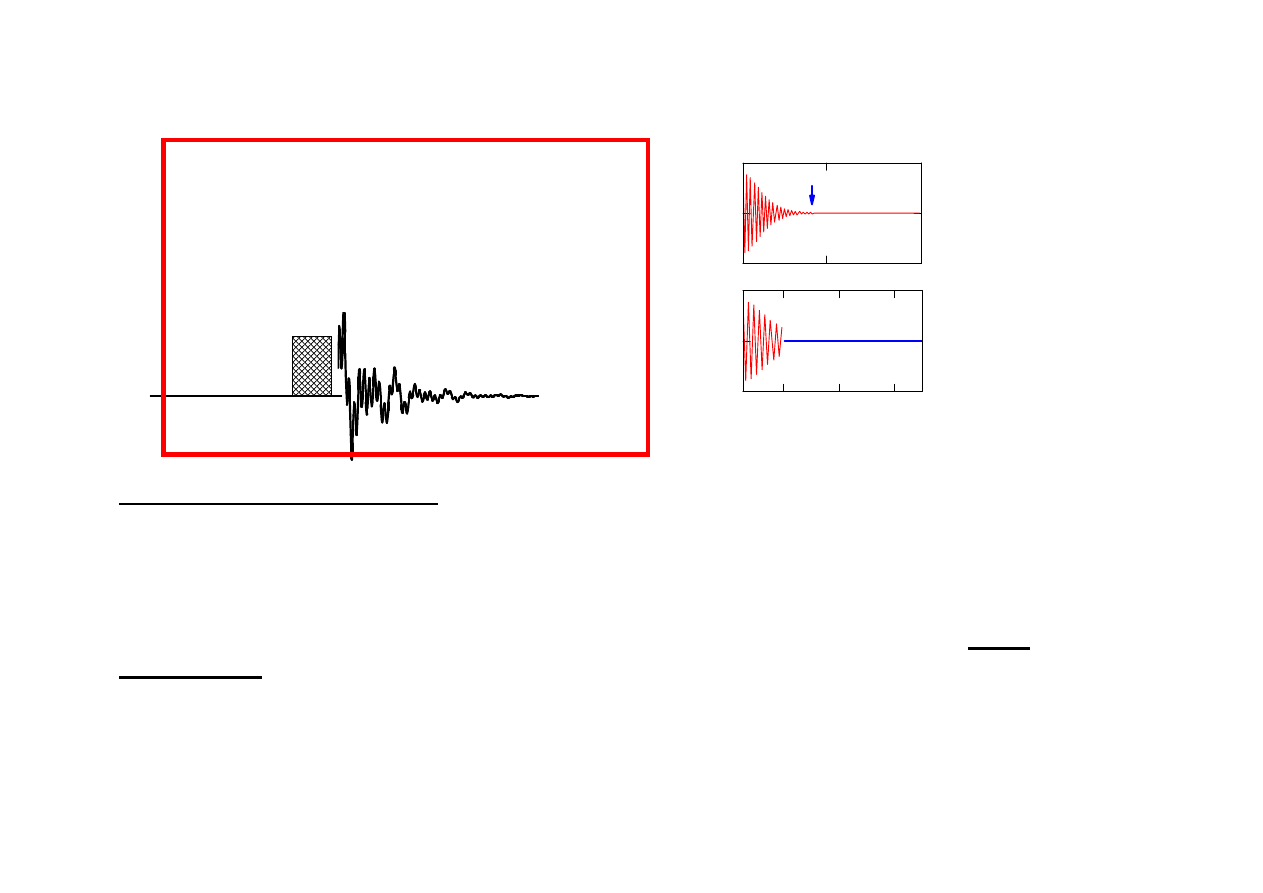
Optymalizacja pomiaru
1
H NMR
T1: dla
1
H 0.2 – 2 s lub dłu
ż
ej (!)
Typowe parametry:
1
H:
d1
= 0 s,
at
= 3 – 5 s,
pw
= 30 – 90
o
d1
pw
at
t (sek)
A
sygnał
szum
t (sek)
A
Parametry do optymalizacji:
d1
mo
ż
na wydłu
ż
y
ć
do kilkunastu sek. = bardziej wiarygodna intensywno
ść
integralna
at
powinien by
ć
optymalny (zazwyczaj nie trzeba zmienia
ć
) zmiana powoduje zmian
ę
np
np
ilo
ść
punktów FID-u; zmiana powoduje zmian
ę
at
fn
ilo
ść
punktów widma (
2
n
); zazwyczaj 32K lub 64K; mo
ż
na zwi
ę
kszy
ć
do 128 K.
Poprawia rozdzielczo
ść
spektraln
ą
widma; parametr wa
ż
ny przy pomiarze stałej
sprz
ęż
enia J i dokładnym całkowaniu.
!!
Rozdzielczo
ść
jest ograniczona „naturaln
ą
szeroko
ś
ci
ą
linii”
!!
sw
zakres wyst
ę
powania sygnałów; za du
ż
y = gorsza rozdzielczo
ść
; za mały = sygnały
zawini
ę
te (lub „zgubione”). Krótki
sw
= długi czas
at
pw
raczej nie zmienia
ć
, ew. skróci
ć
(
zbyt długi puls = mo
ż
liwo
ść
uszkodzenia aparatu !!)
gain
szczególnie wa
ż
ny przy pomiarach protonowych (za du
ż
y = deformacja widma)
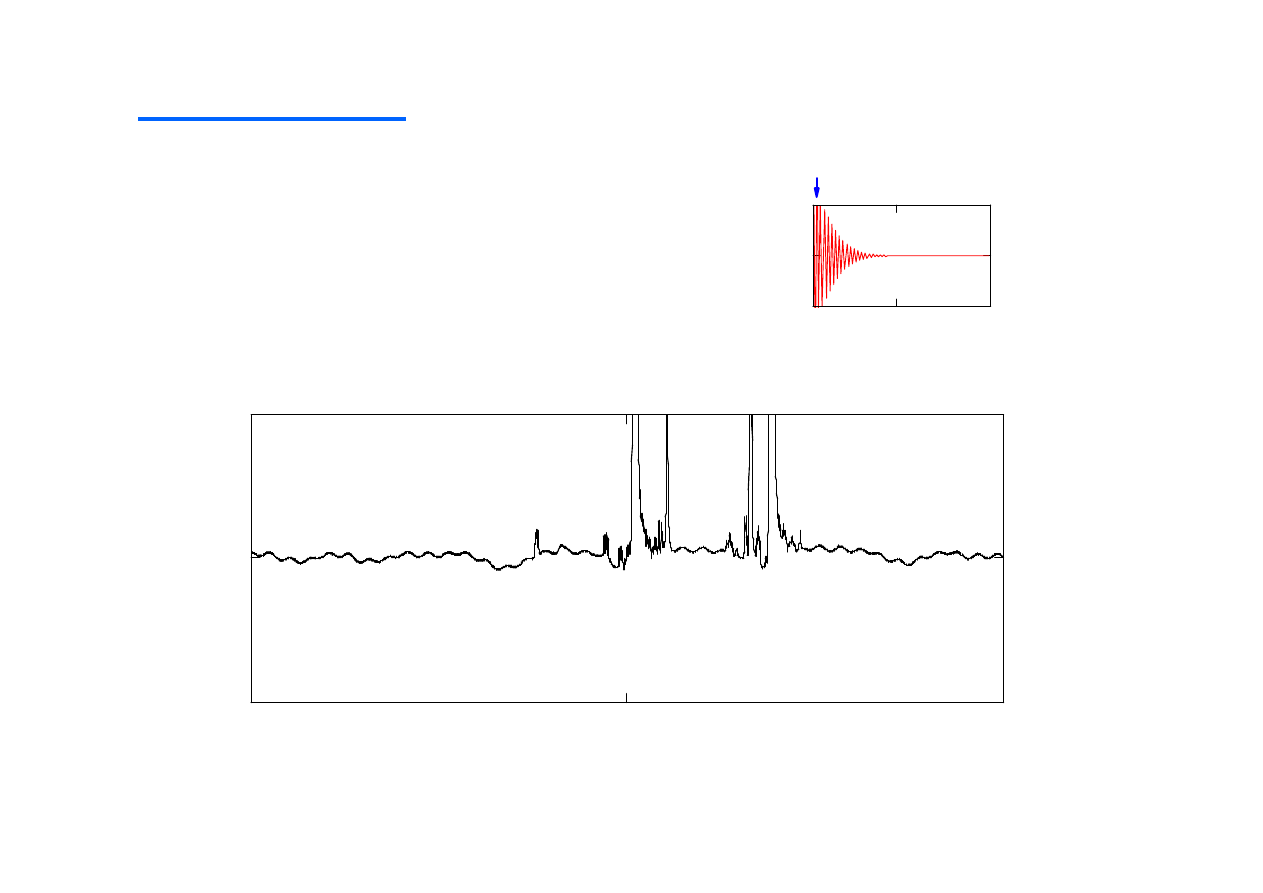
t (sek)
A
„
gain
” –
gain
= n lub 0 – 39
za mała warto
ść
–
ź
le wykorzystana czuło
ść
aparatu
za du
ż
a warto
ść
– obci
ę
cie sygnału
Je
ś
li
gain
= 0 za du
ż
y, nale
ż
y zmniejszy
ć
pw
(np. o 50%)
Przypomnienie:
dobór czuło
ś
ci odbiornika („receiver gain”)
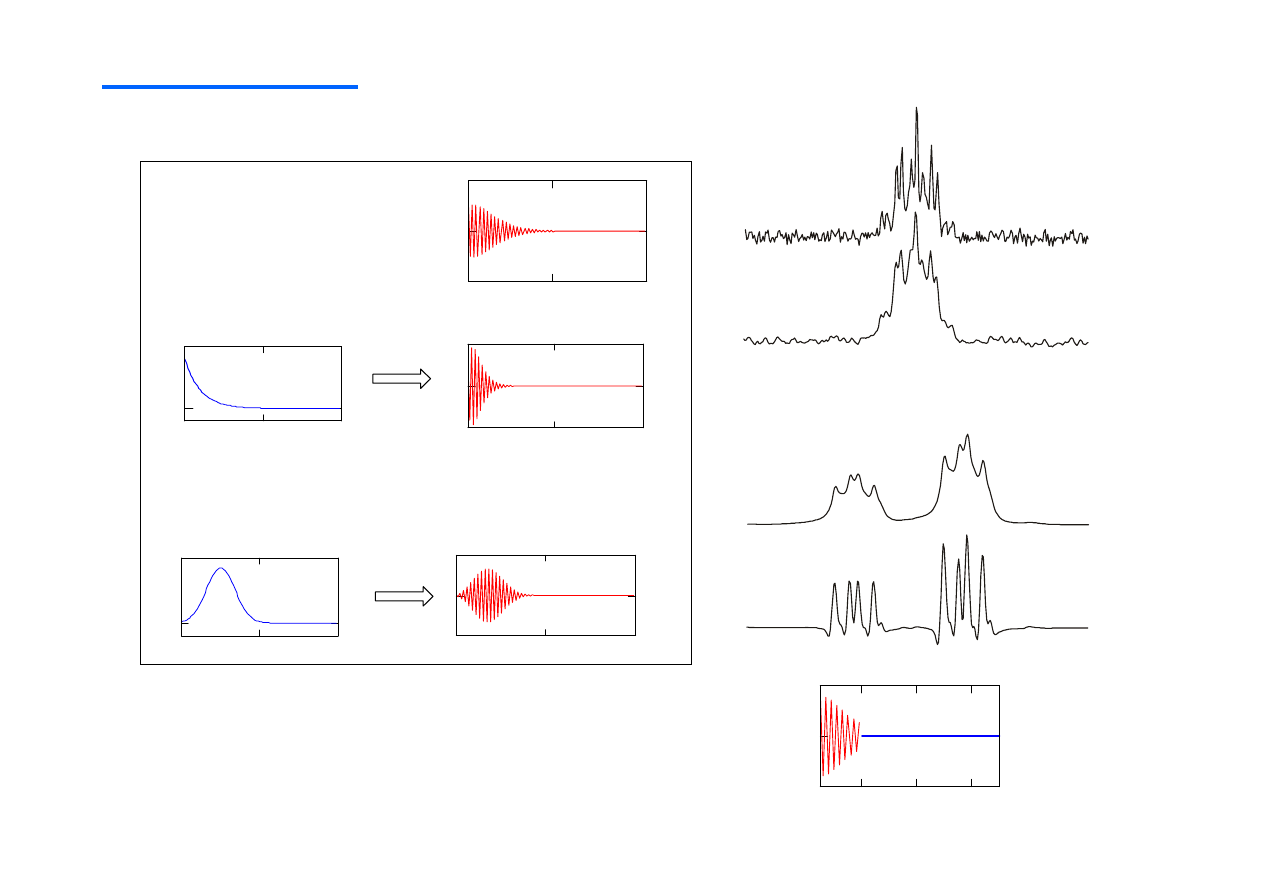
t (sek)
t (sek)
t (sek)
t (sek)
t (sek)
A
A
A
y
y
t (sek)
A
LB = 0.1 – 0.3 dla
1
H
EF lub EM i FT
LB = -1.2; GB = 0.1 – 1 (Bruker)
Mno
ż
enie przez funkcj
ę
wykładnicz
ą
(Exponential Multiplication, EM)
y = exp(-at/t
a
)
Mno
ż
enie przez funkcj
ę
Gaussa
(Lorentzian-to-Gauss Transformation)
y = exp(at/t
a
- bt
2
/t
a
2
))
FT
GM, EM, FT
LB = -1.2
GB = 0.5
FT
EM, FT
LB = 1
Przypomnienie
: funkcje wa
żą
ce stosowane w
1
H NMR (1D)

wpływ temperatury na widmo
efekt Overhausera
presaturacja sygnału (usuwanie sygnału rozpuszczalnika)
echo spinowe
rezonans podwójny („homodecoupling”)
Tematy zwi
ą
zane nie tylko z
1
H NMR
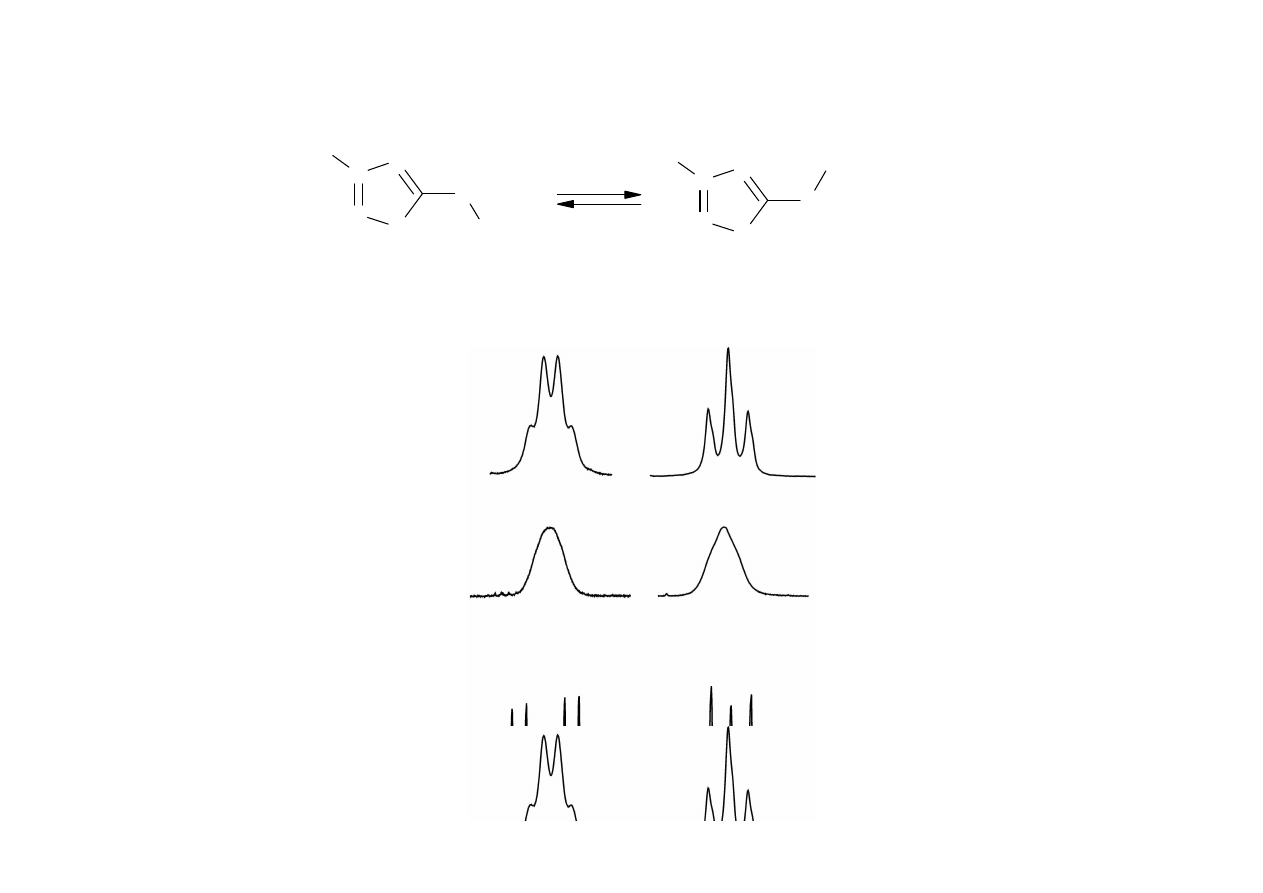
N
O
N
N
N
Ph
CH
2
CH
3
N
O
N
N
N
Ph
CH
2
CH
3
+
-
+
-
318 K
303 K
253 K
CH
2
CH
3
Wpływ temperatury na widmo
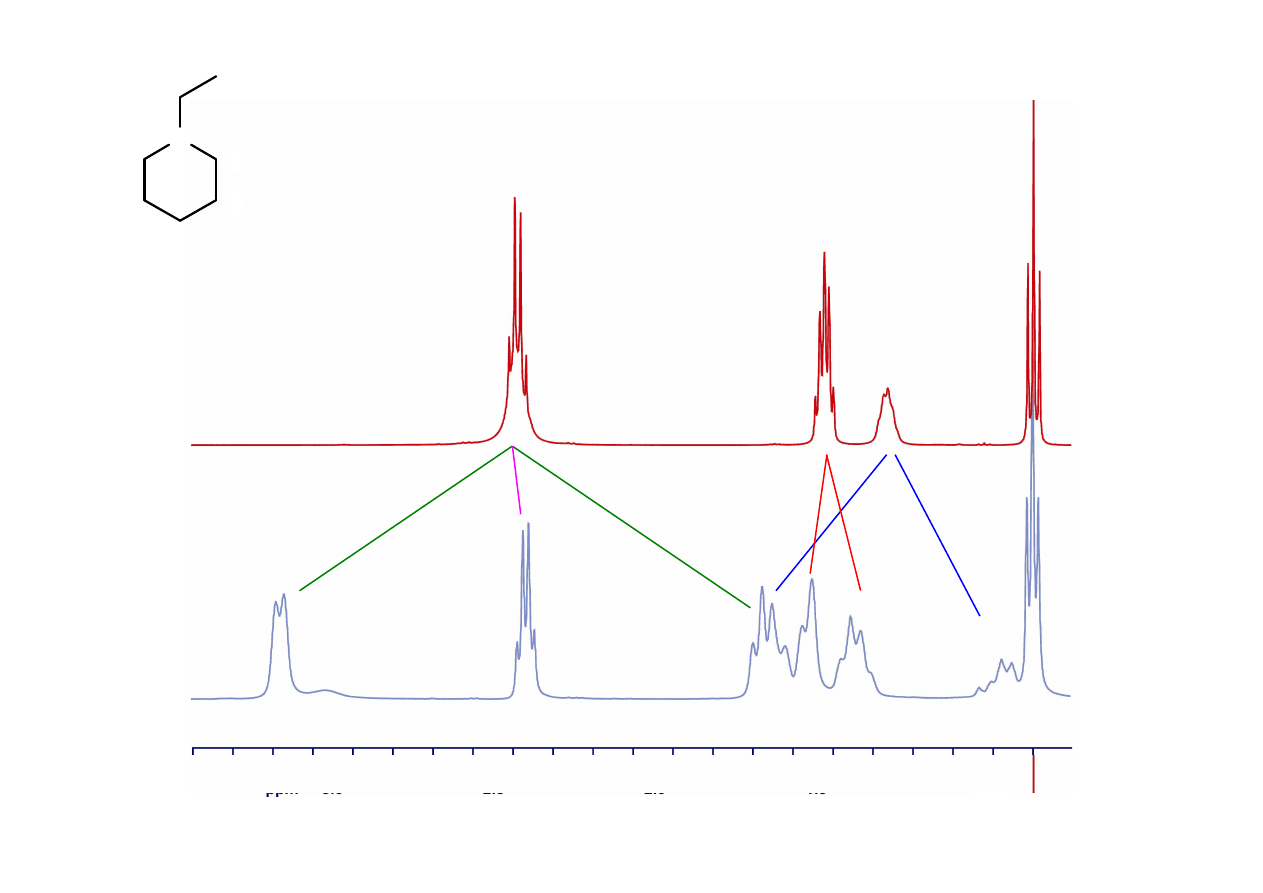
N
1
2
3
CH
2
CH
3
CH
2
+ 4 H1
4 H2
2 H3
H2
H2
H3
H1
, H3
H1
303 K
233 K
CDCl
3
Wpływ temperatury na widmo
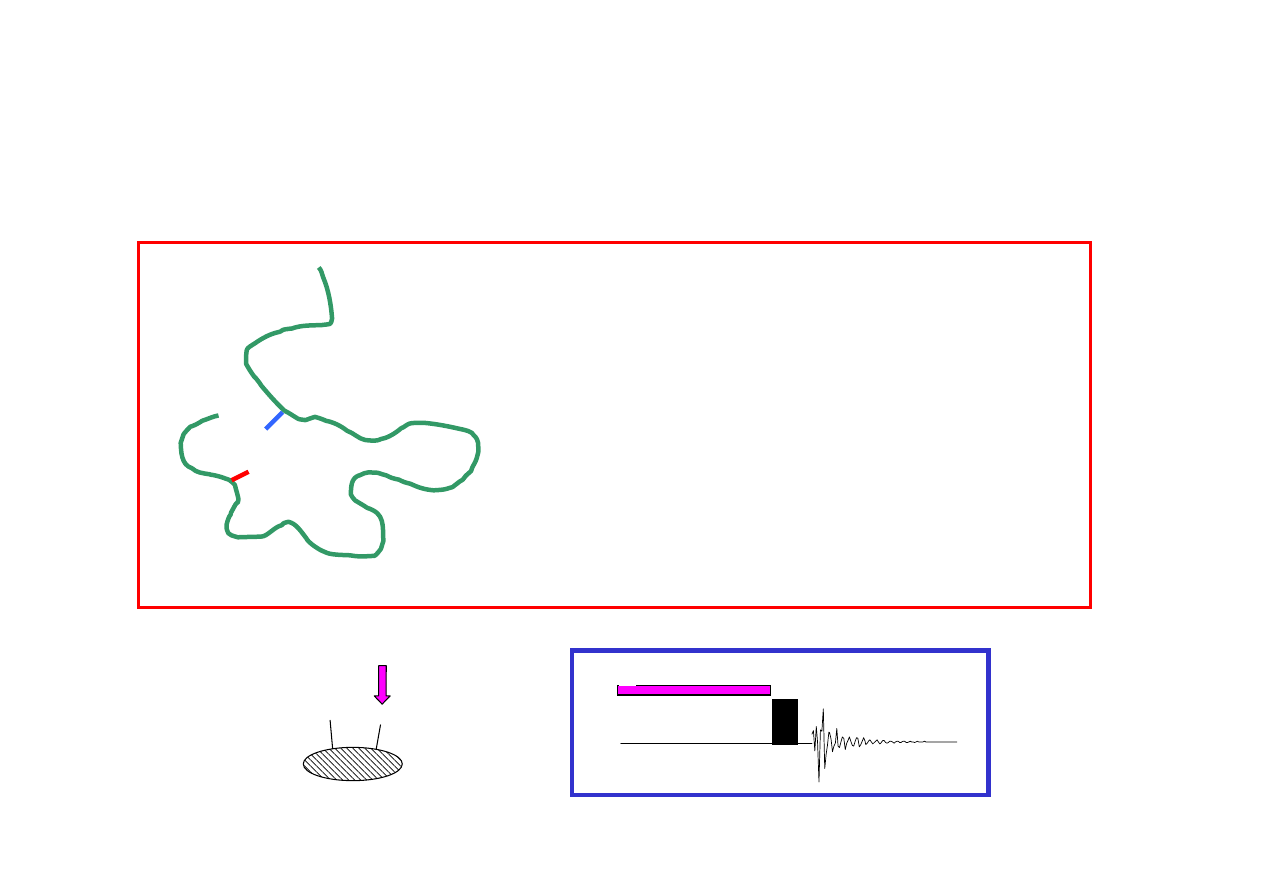
H
H
J
Ą
DROWY EFEKT OVERHAUSERA (Nuclear Overhauser Effect, NOE)
J(
H
,
H
) = 0 Hz (du
ż
a odległo
ść
liczona po wi
ą
zaniach)
D(
H
,
H
)
≠≠≠≠
0 Hz (mała odległo
ść
liczona poprzez przestrze
ń
)
H
H
υυυυ
0
Efekt Overhausera – zmiana intensywno
ś
ci sygnału atomu poło
ż
onego w pobli
ż
u innego atomu
na
ś
wietlanego jego cz
ę
sto
ś
ci
ą
rezonansow
ą
D.Neuhaus, M.Williamson „The Nuclear Overhauser Effect” (VCH 1989)
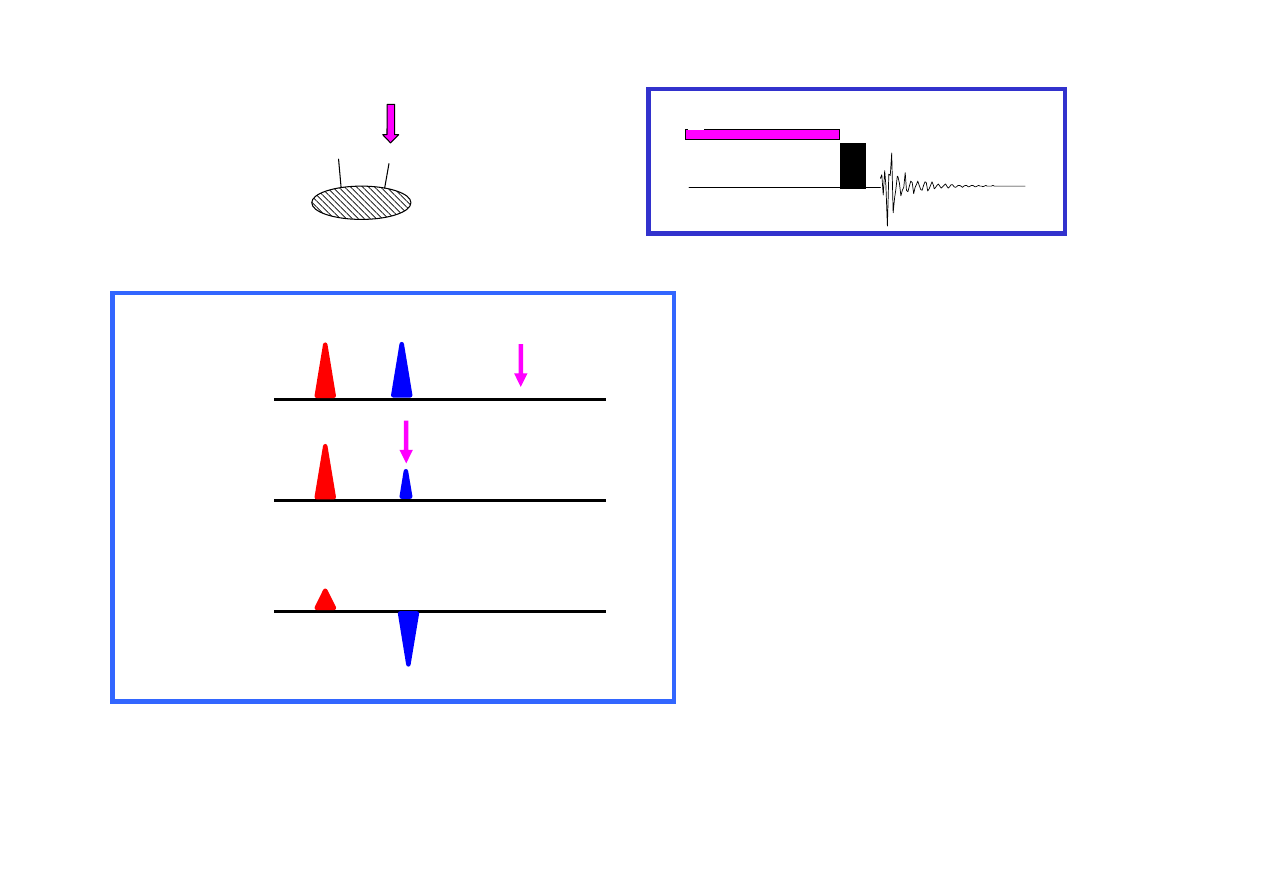
I – intensywno
ść
integralna sygnału
niezaburzonego
I
o
– intensywno
ść
integralna sygnału
zaburzonego
ηηηη
– współczynnik wzmocnienia
ηηηη
= (I – I
o
)/I
o
H
H
widmo odniesienia
widmo zaburzone
widmo ró
ż
nicowe
I
I
o
na
ś
w.
I - I
o
na
ś
w.
υυυυ
0
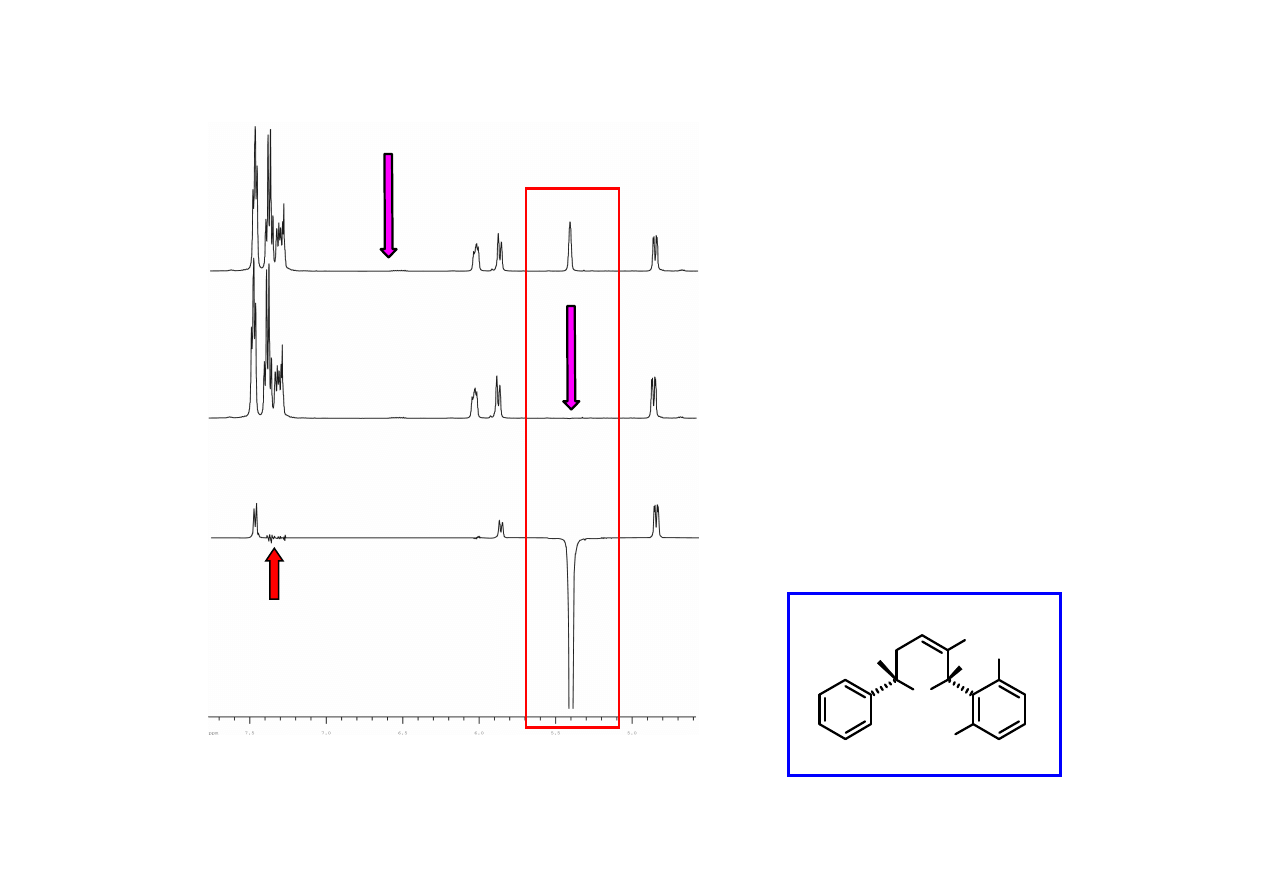
Widmo odniesienia
Widmo na
ś
wietlone
Widmo na
ś
wietlone - widmo odniesienia
Przykład pomiaru efektu Overhausera
(B.Furman et al.)
O
H
H
H
H
H
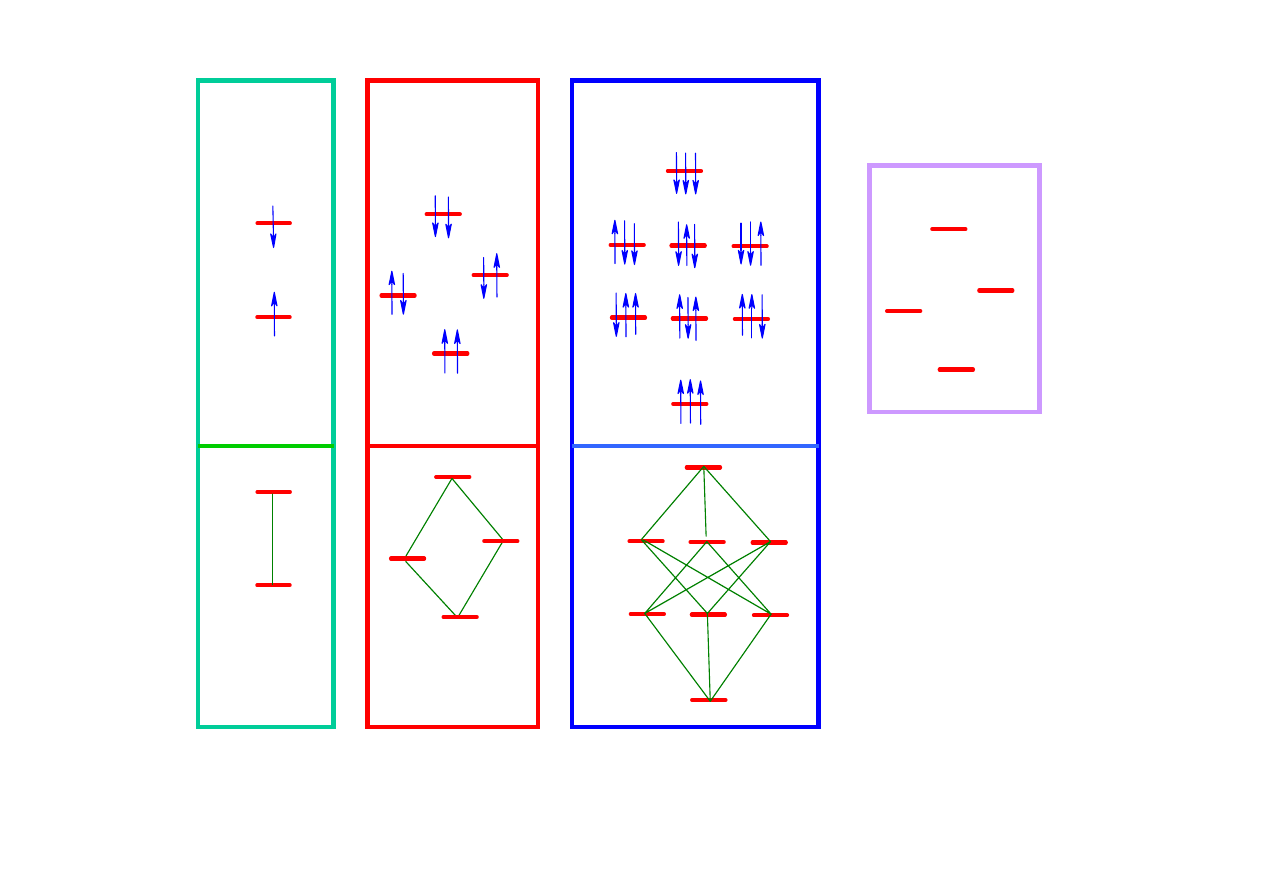
A
AX
AMX
αα
αβ
βα
ββ
W widmie NMR obserwowane s
ą
bezpo
ś
rednio wył
ą
cznie przej
ś
cia jednokwantowe
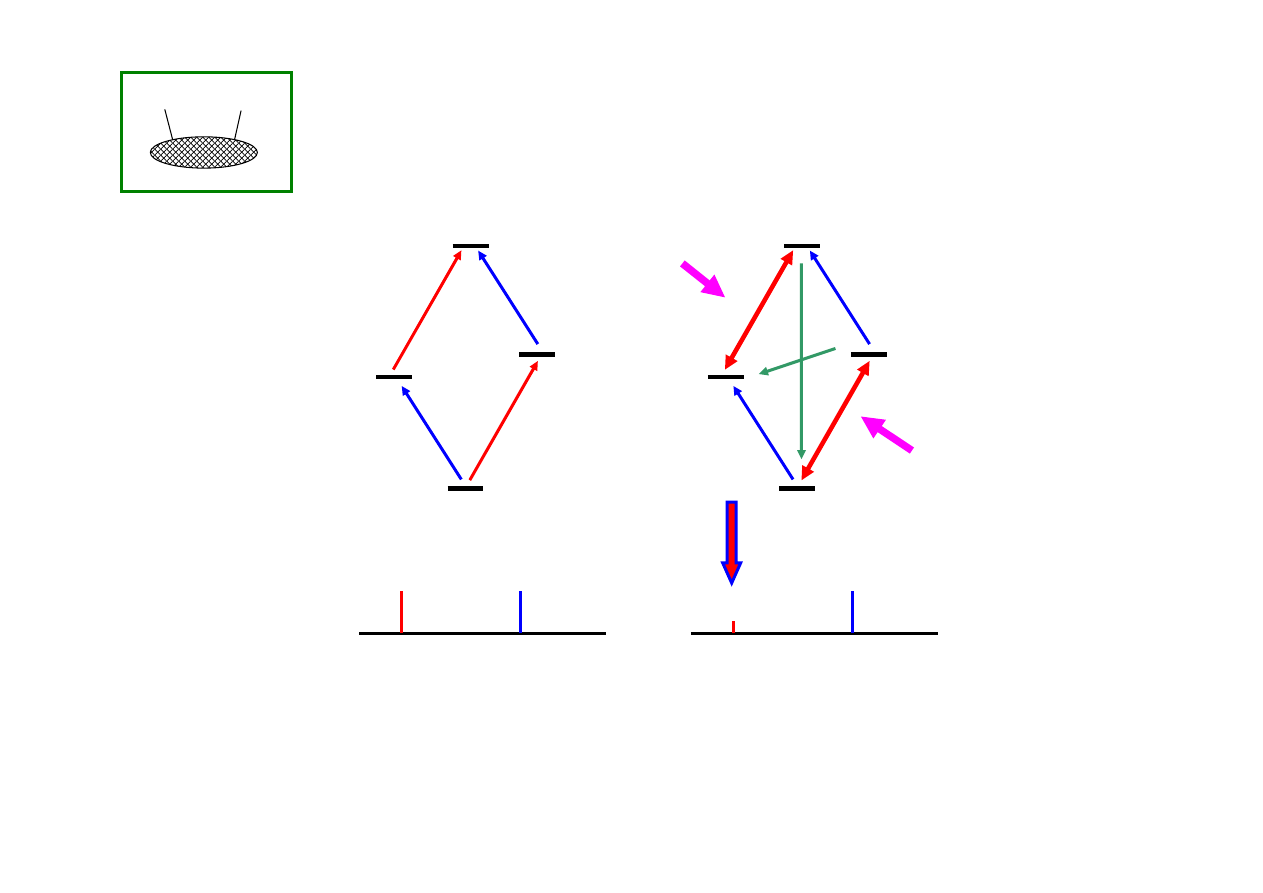
H
H
1 – 4 przej
ś
cia jednokwantowe
5 przej
ś
cie dwukwantowe
6 przej
ś
cie zerokwantowe
αα
αα
αα
αα
βα
βα
βα
βα
ββ
ββ
ββ
ββ
αβ
αβ
αβ
αβ
1
4
3
2
1,4
2,3
αα
αα
αα
αα
βα
βα
βα
βα
ββ
ββ
ββ
ββ
αβ
αβ
αβ
αβ
1
4
3
2
1,4
2,3
5
6
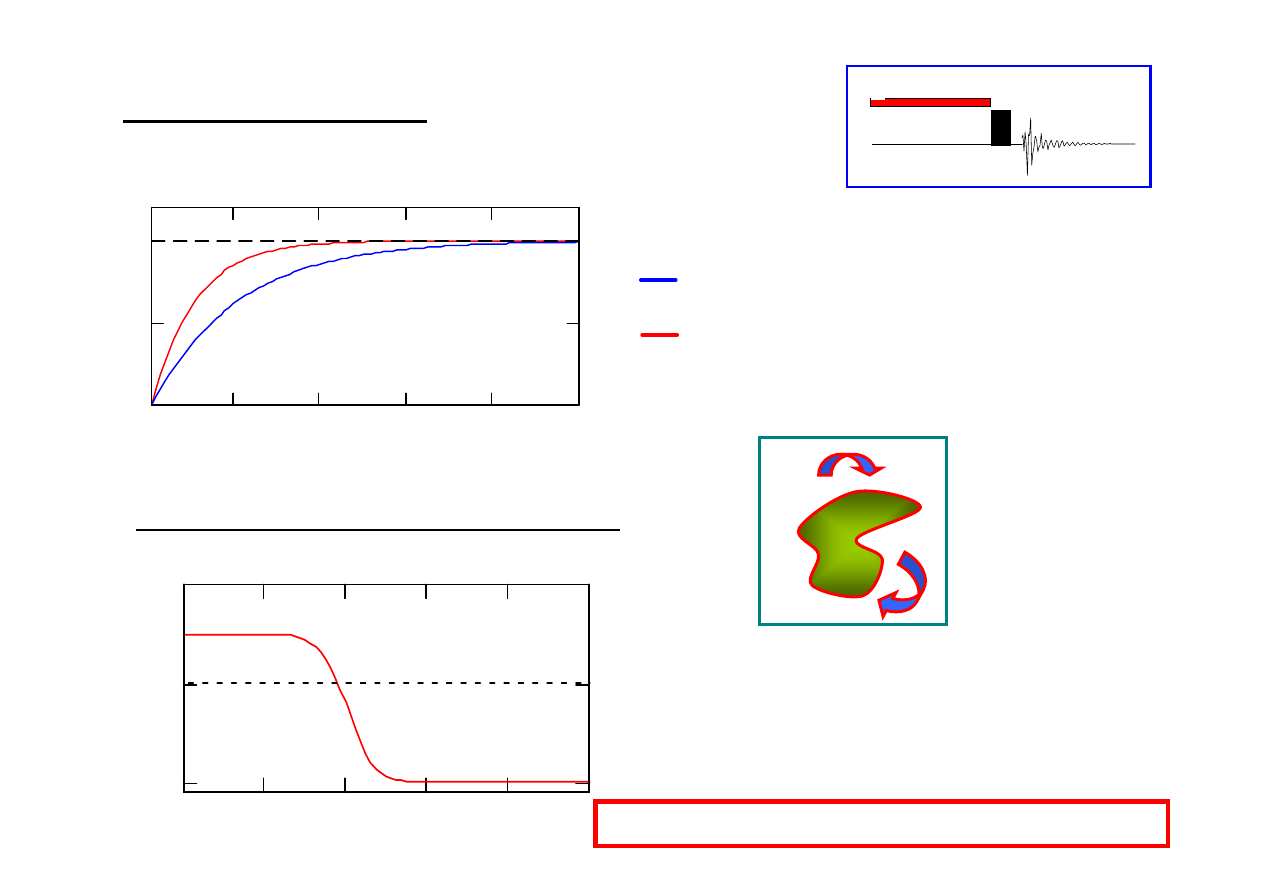
υυυυ
0
50%
ηηηη
czas na
ś
wietlania [s]
mała odległo
ść
mi
ę
dzy atomami
du
ż
a odległo
ść
mi
ę
dzy atomami
maksymalna warto
ść
ηηηη
dla układu
1
H –
1
H: 50%
Szybko
ść
narastania NOE:
Zale
ż
no
ść
ηηηη
od czasu korelacji cz
ą
steczki:
1
H{
1
H}
0.5
-1
ηηηη
log
ωτ
ωτ
ωτ
ωτ
c
ω
ω
ω
ω
– cz
ę
sto
ść
rezonansowa
1
H
ττττ
c
– czas korelacji cz
ą
steczki
0
!! Brak NOE nie jest potwierdzeniem struktury !!
+
+
-
-
ruch molekuły =
= fluktuacje B
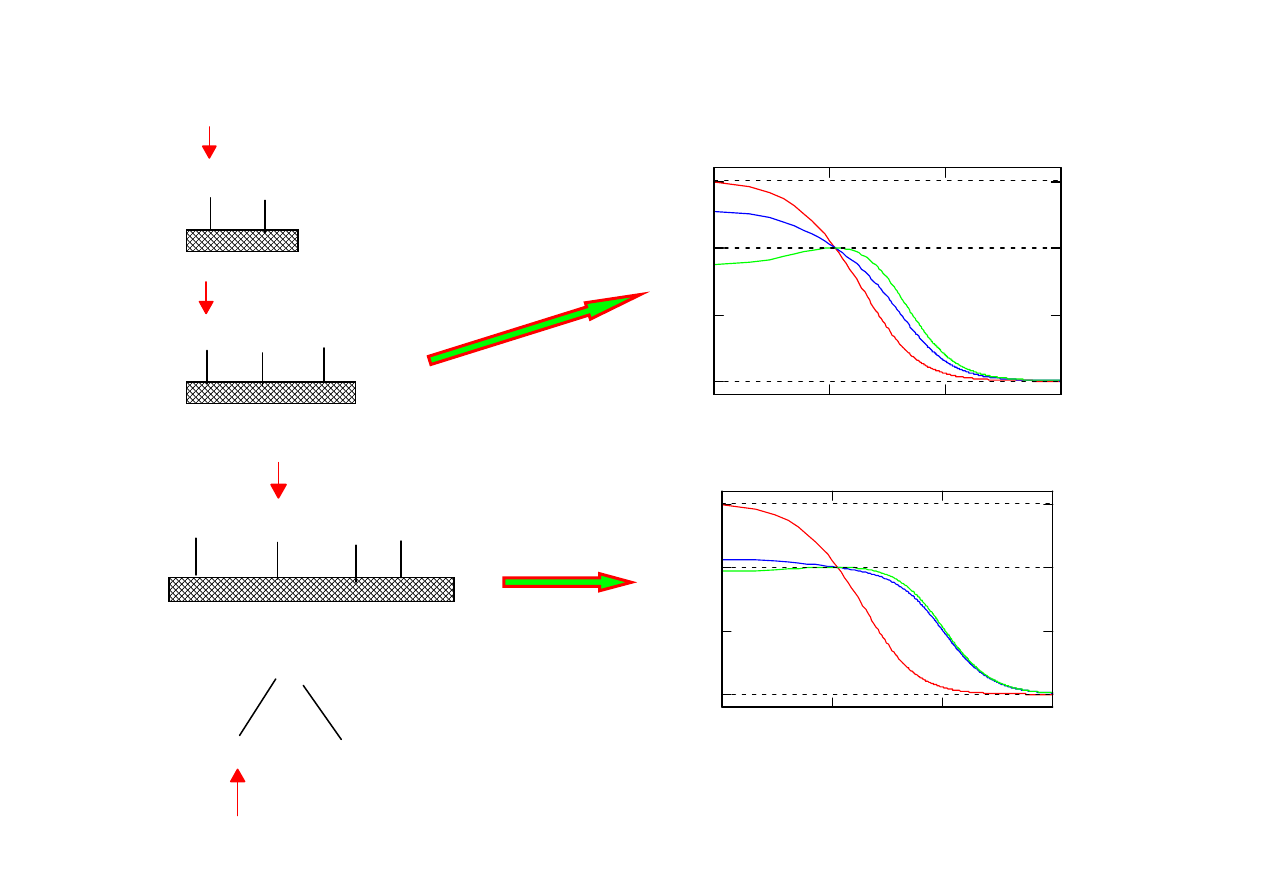
0.1
1
10
100
0.1
1
10
100
log
ωτ
ωτ
ωτ
ωτ
c
log
ωτ
ωτ
ωτ
ωτ
c
η [%]
η [%]
η [%]
η [%]
η [%]
η [%]
η [%]
η [%]
50 %
- 100 %
0 %
50 %
- 100 %
0 %
49 %
28 %
- 0.4 %
50 %
1 %
- 13 %
50 %
- 13 %
28 %
49 %
- 0.4 %
1 %
H
H
H
H
H
H
H
H
H
H
H
H
αααα
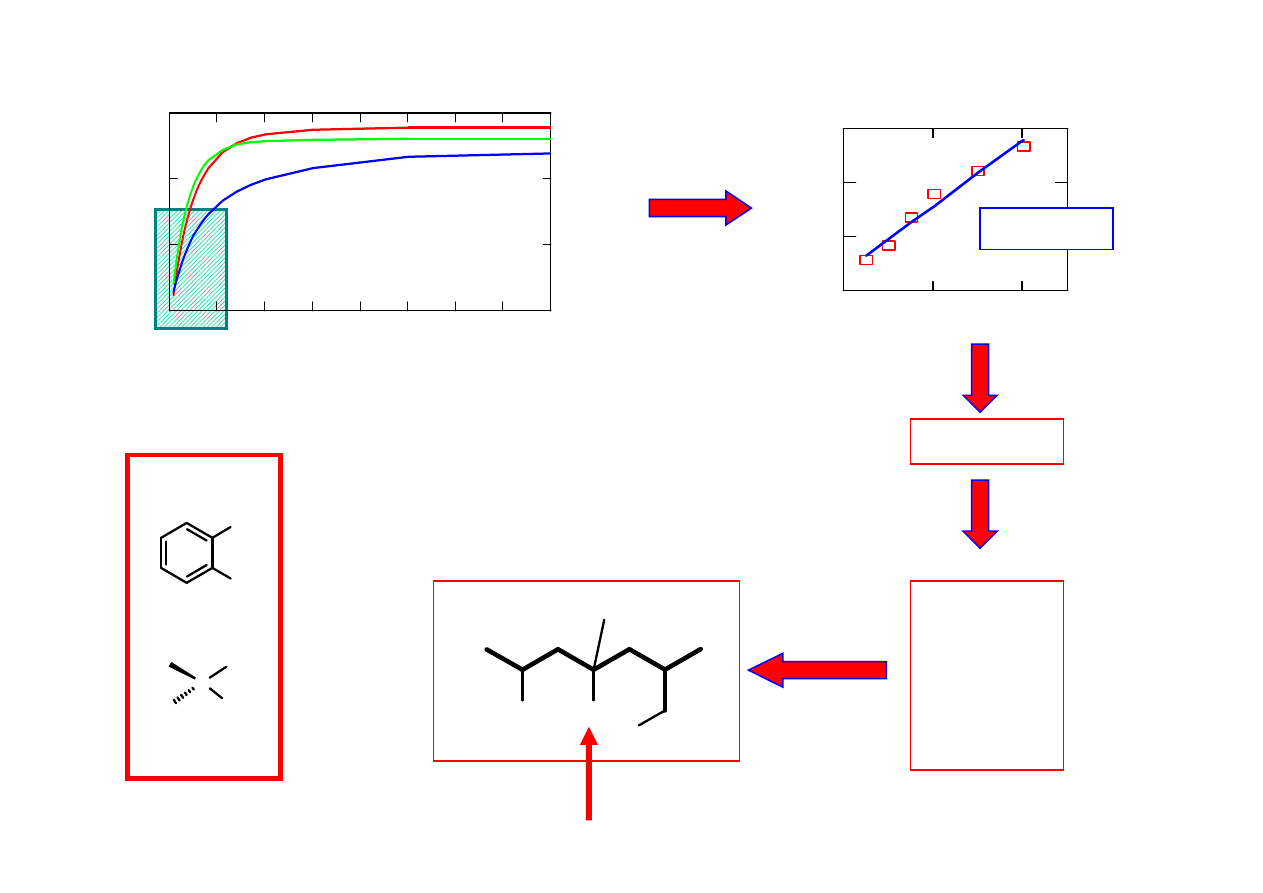
ηηηη
y = ax + b
H
H
H
H
a ~ 1/r
6
0
200 ms
ηηηη
czas na
ś
wietlania [`s]
a
1
,
a
2
,
a
3
H
H
C
H
H
wzorzec r
a
1
∝
∝
∝
∝
(1/r
1
)
6
a
2
∝
∝
∝
∝
(1/r
2
)
6
a
3
∝
∝
∝
∝
(1/r
3
)
6
eksperyment „NOE-build-up”
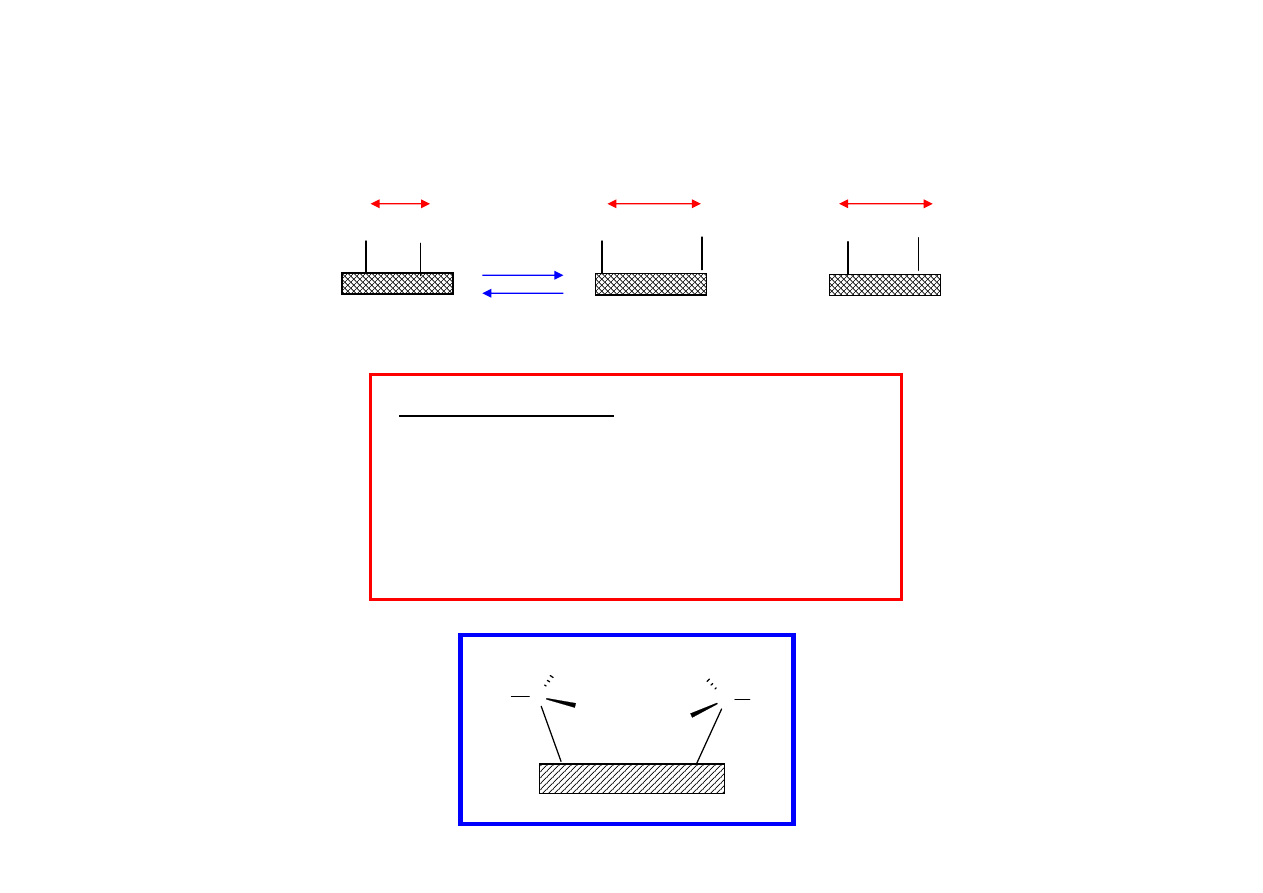
H
H
H
H
x
y
H
H
(x+y)/2
Odległo
ść
wg NOE: {[ (1/x
6
) + (1/y
6
) ] / 2}
-1/6
x = 0.4, y = 0.6
(x + y)/2 =
0.5
{[ (1/x
6
) + (1/y
6
) ] / 2}
-1/6
=
0.443
U
ś
rednianie odległo
ś
ci wg NOE <r
-6
>
C
H
H
H
C
H
H
H
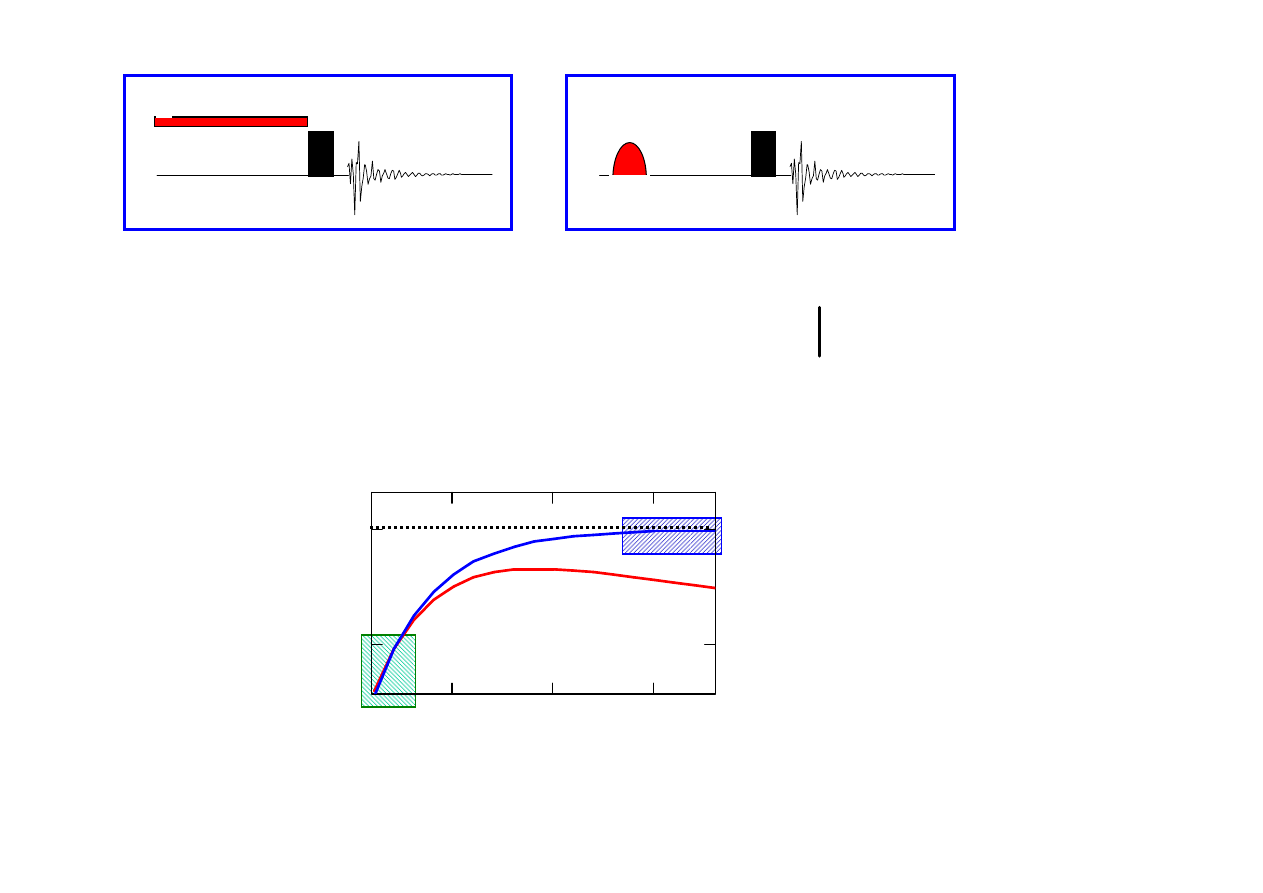
υυυυ
0
krótki czas na
ś
wietlania: „truncated driven NOE” (TOE)
długi czas na
ś
wietlania: „steady state NOE”
selektywny impuls 180
o
: „transient NOE”
d
ηηηη
/dt ~ 1/r
6
180
o
ηηηη
czas
90
o
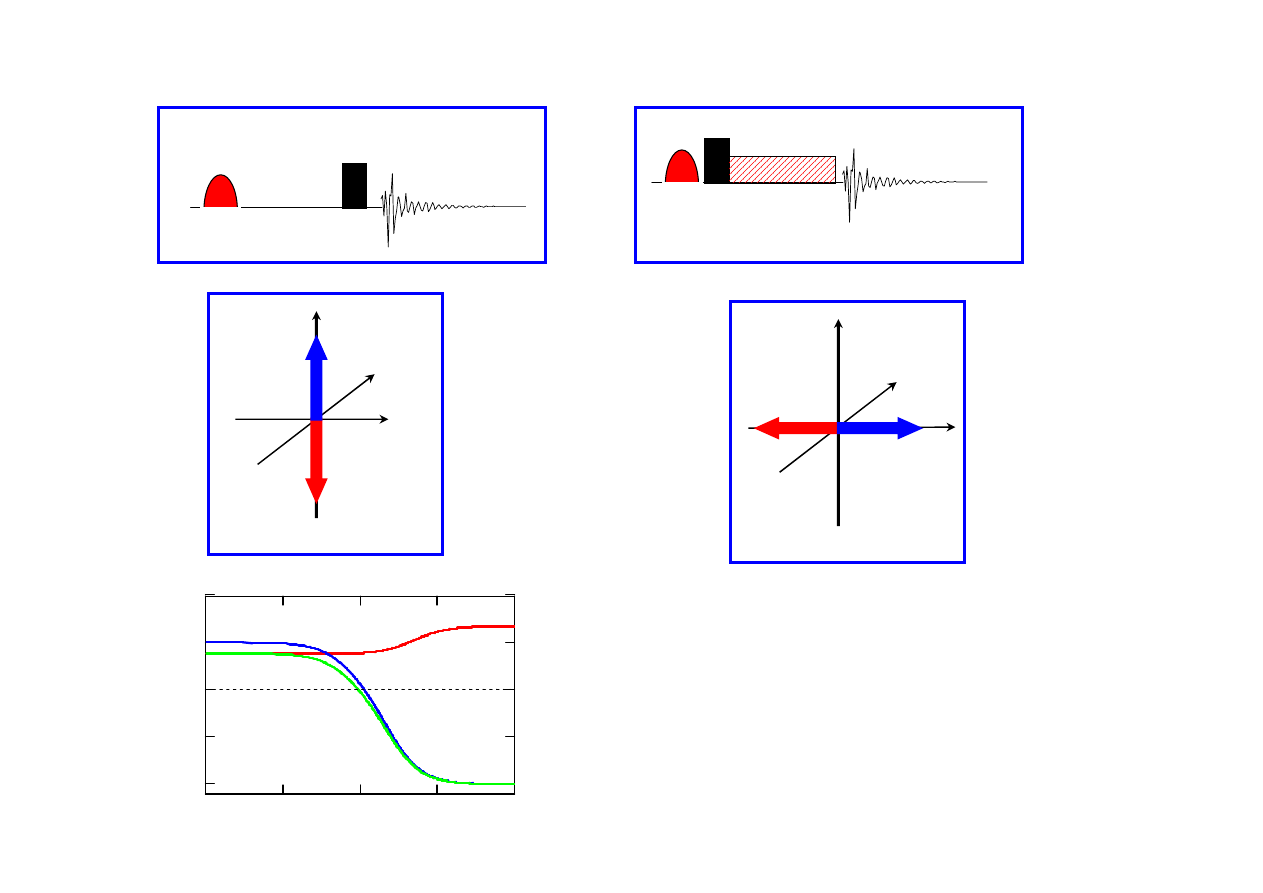
180
o
transient NOE
90
o
rotating-frame NOE (ROE)
spin lock
log(
ωτ
ωτ
ωτ
ωτ
c
)
ηηηη
steady state NOE
ηηηη
od 0.5 do -1
transient NOE
ηηηη
od 0.385 do -1
ROE
ηηηη
od 0.385 do 0.675
0
I.Bertini, Coord. Chem. Rev., 150 (1966) 163

NOE – wykonanie eksperymentu
Próbka:
eliminacja zanieczyszcze
ń
paramagnetycznych:
kationów metali przej
ś
ciowych (np. Cr
3+
z chromianki)
tlenu atmosferycznego rozpuszczonego w roztworze
Odgazowanie próbki:
przepuszczanie gazu oboj
ę
tnego – mało skuteczne
procedura „zamra
ż
anie – pró
ż
nia – rozmra
ż
anie” 3 – 5 razy
zastosowanie specjalnej probówki NMR
Pomiar:
wykona
ć
kilka pomiarów (co najmniej dwa)
brak NOE nie jest potwierdzeniem struktury
obecno
ść
NOE nie jest potwierdzeniem struktury

REZONANS PODWÓJNY
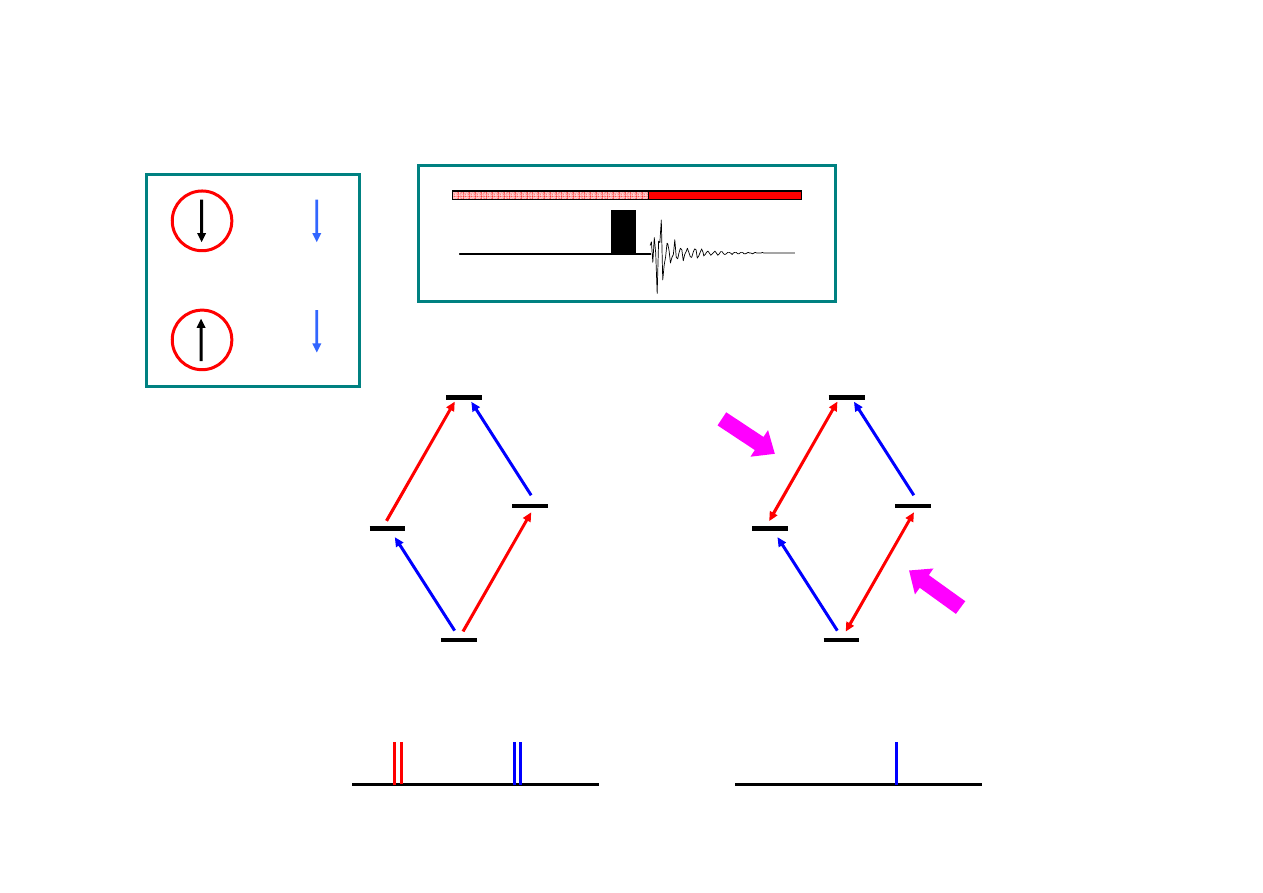
REZONANS PODWÓJNY
(homodecoupling, odsprz
ę
ganie)
νννν
o
αααα
αααα
ββββ
αααα
ββββ
ββββ
αααα
ββββ
1
4
3
2
1,4
2,3
αααα
αααα
ββββ
αααα
ββββ
ββββ
αααα
ββββ
1
4
3
2
1,4
2,3
νννν
0
νννν
0
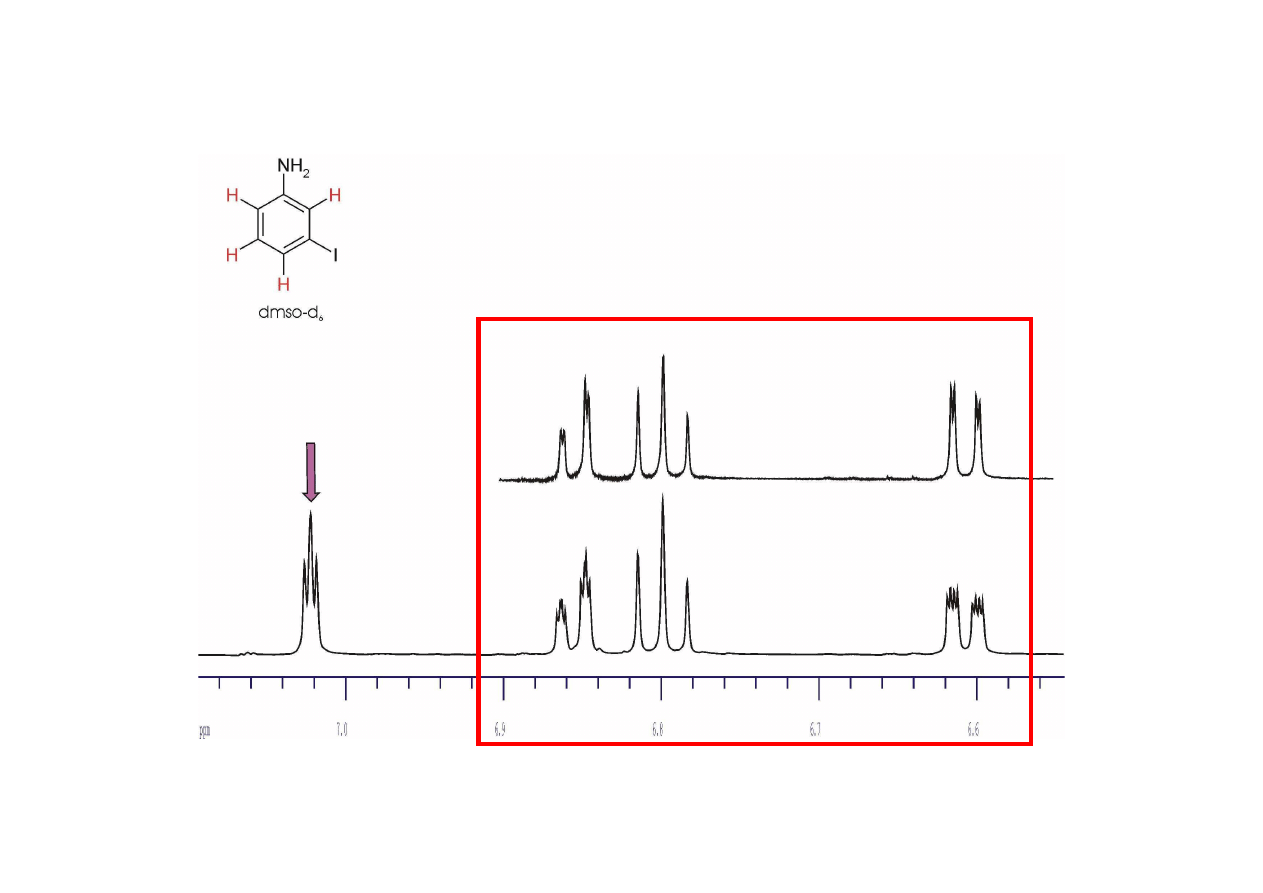

PRESATURACJA SYGNAŁU
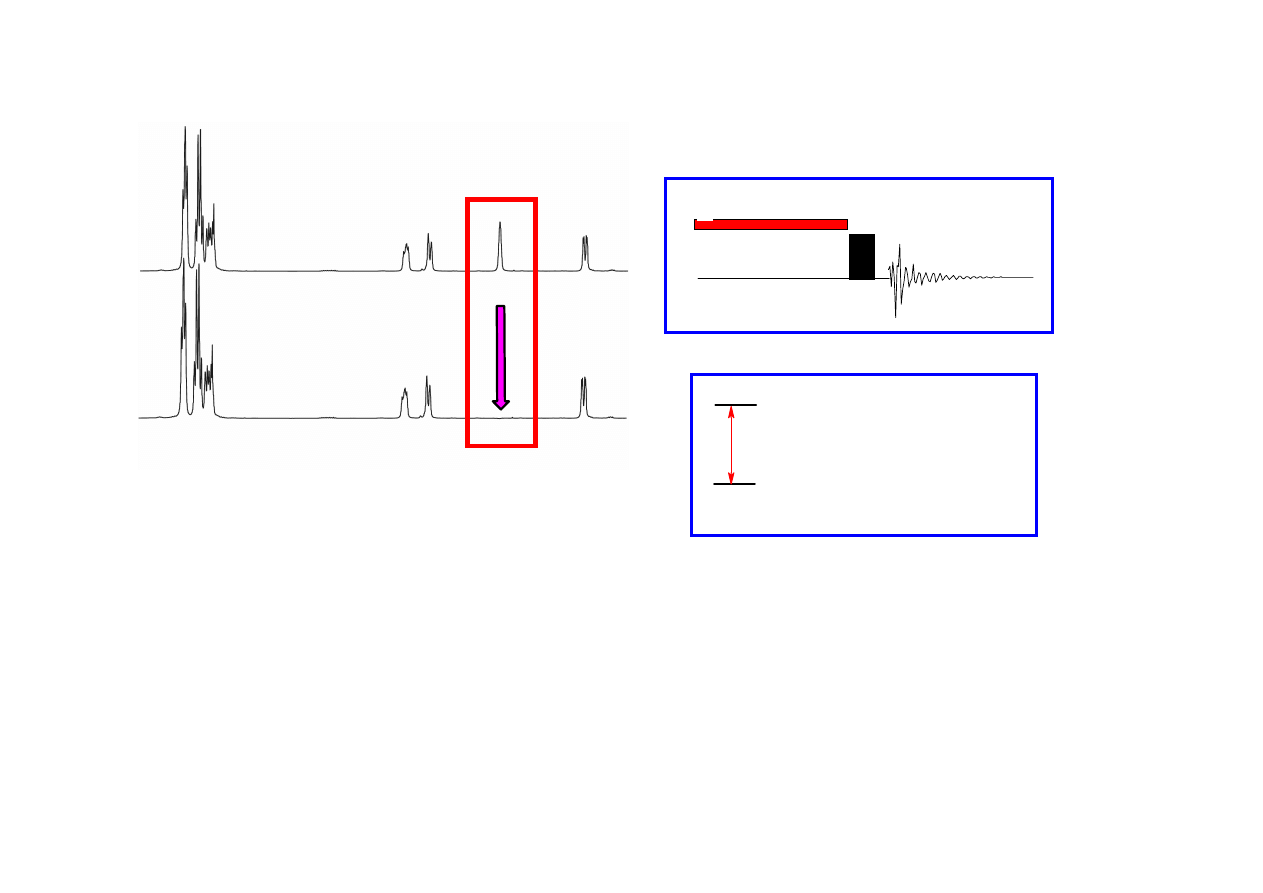
Widmo odniesienia
Widmo na
ś
wietlone
Uboczny skutek eksperymentu NOE: usuni
ę
cie sygnału z widma
PRESATURACJA SYGNAŁU – usuwanie sygnału rozpuszczalnika przez jego selektywne
na
ś
wietlanie.
ZASTOSOWANIE: usuwanie silnego sygnału rozpuszczalnika, np. w próbkach białek i DNA w
ś
rodowisku H
2
O (nie D
2
O !!)
υυυυ
0
Selektywne
na
ś
wietlanie:
wyrównanie obsadze
ń
poziomów
energetycznych
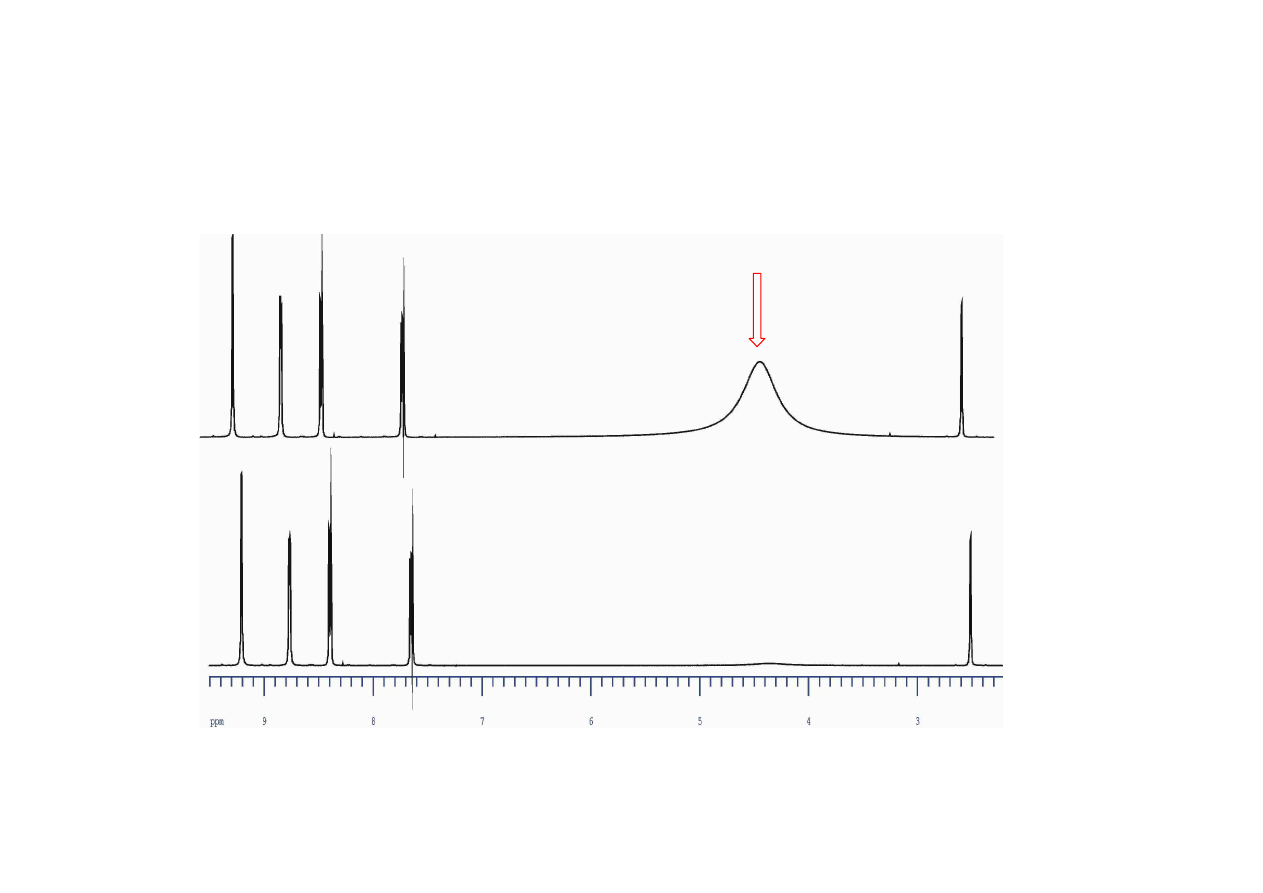
PRESATURACJA SYGNAŁU
(usuwanie sygnału rozpuszczalnika)
H
2
O
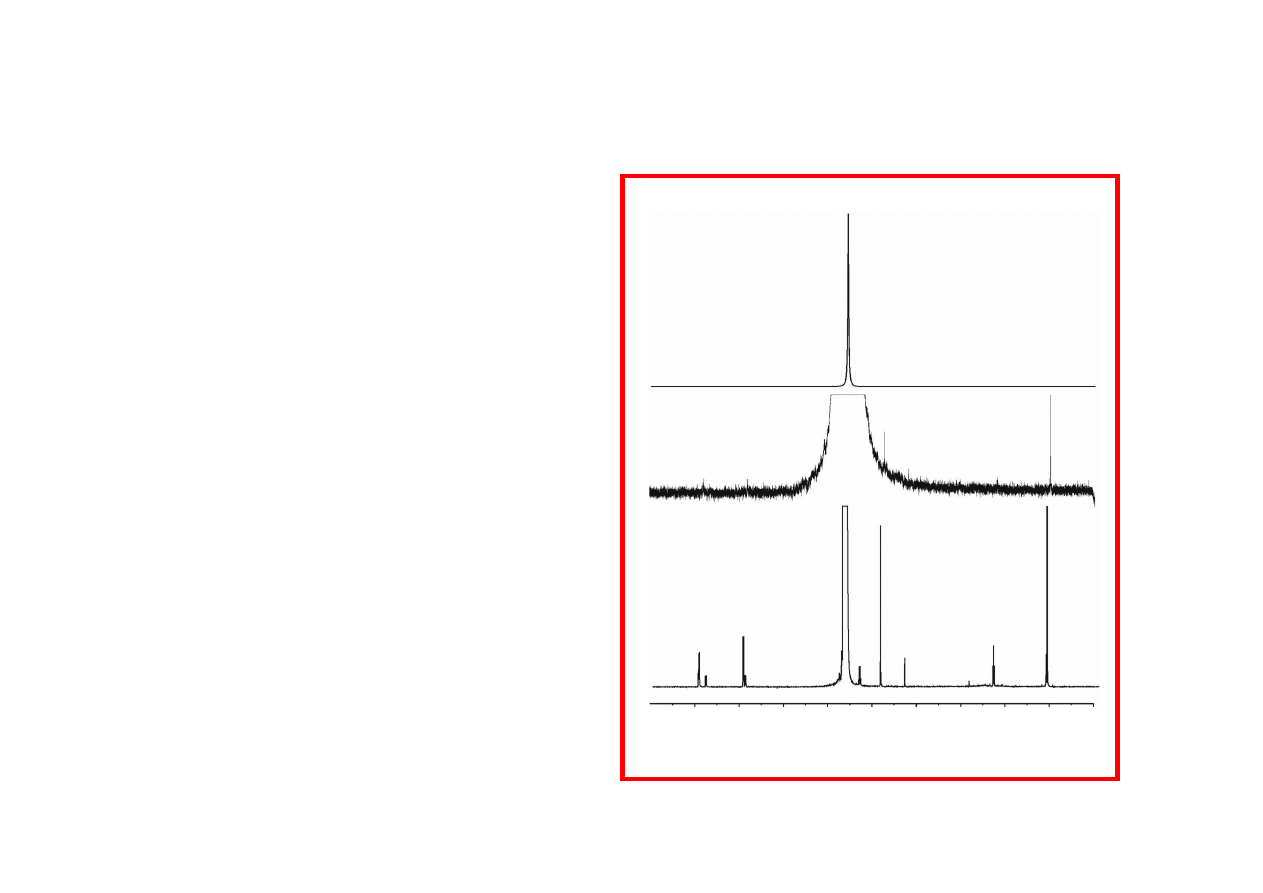
-1.0
9.0
ppm
H
2
O
Problem: 1% zwi
ą
zków organicznych
w wodzie; nie mo
ż
na odparowa
ć
wody
ani wydzieli
ć
zwi
ą
zku
Sygnał wody ponad 100 razy
silniejszy ni
ż
sygnały badane
Próbka: 60% roztworu + 40 % D
2
O
PRESATURACJA SYGNAŁU
(usuwanie sygnału rozpuszczalnika)
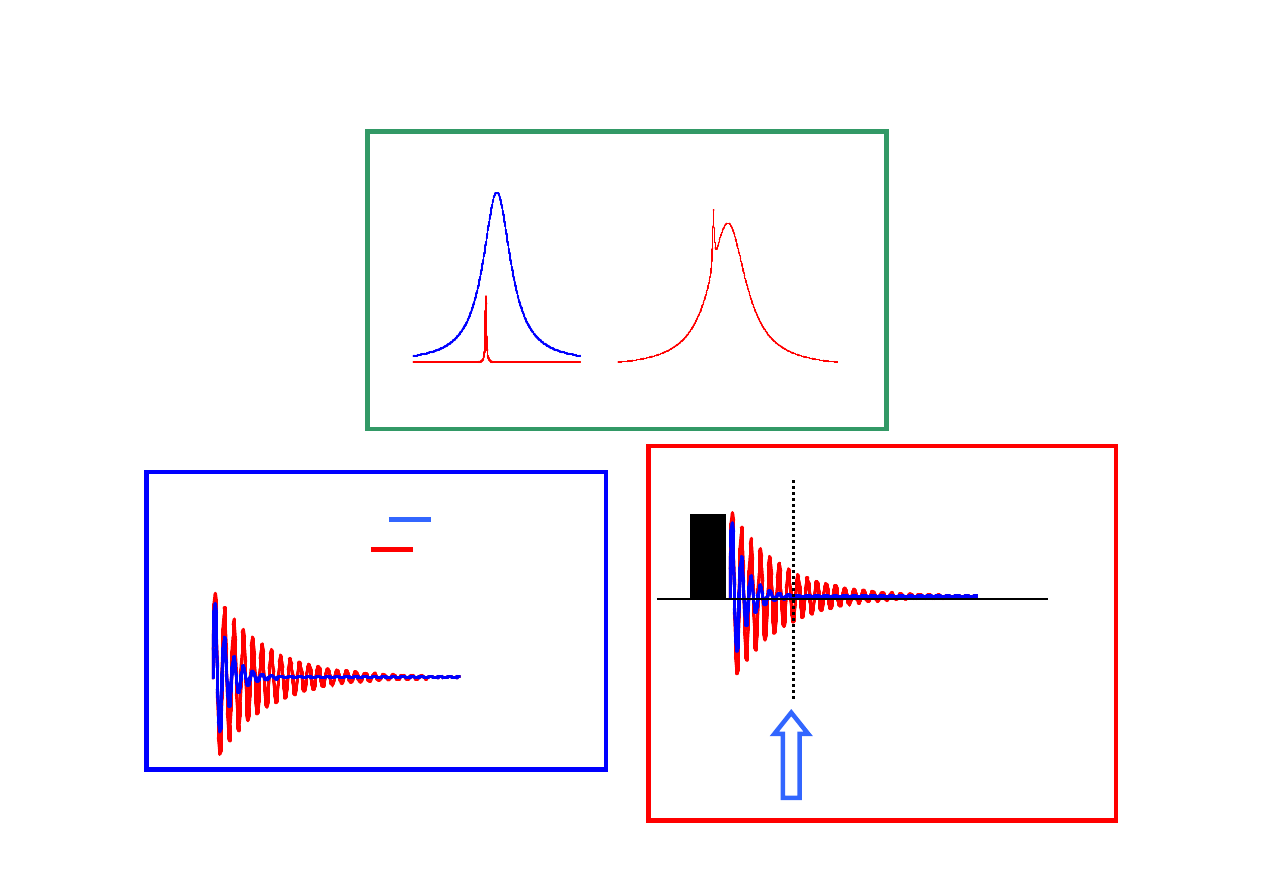
Szeroko
ść
sygnału zale
ż
y od czasu relaksacji T
2
Szeroki sygnał = krótki T
2
W
ą
ski sygnał = długi T
2
pocz
ą
tek rejestracji
sygnału
???
USUWANIE SZEROKIEGO SYGNAŁU

ECHO SPINOWE
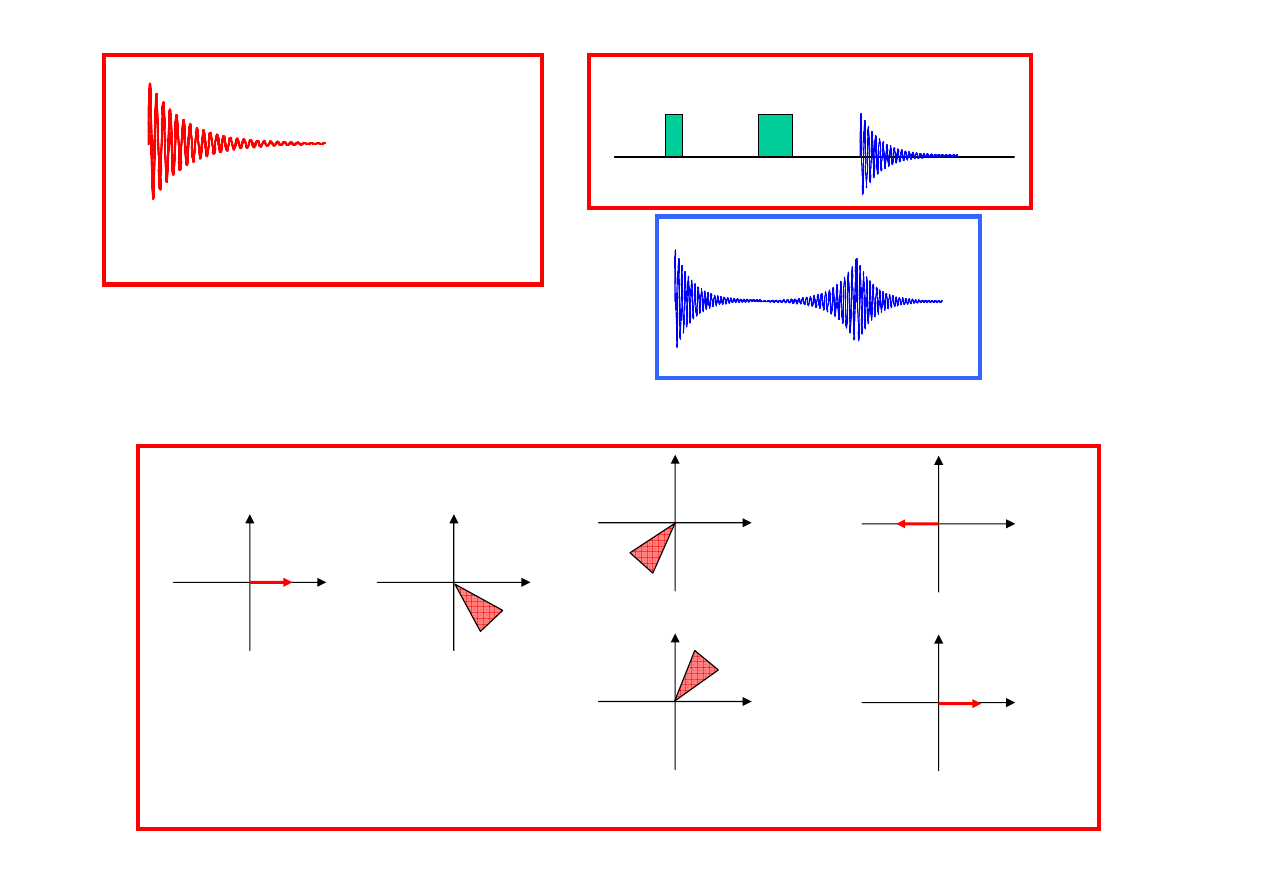
ττττ
ττττ
90
o
180
o
po impulsie 90
o
x
y
f
s
po czasie
ττττ
f
s
f
s
po impulsie 180
o
po czasie
ττττ
exp(-t / T
2
)
Dwie przyczyny zaniku sygnału:
czynniki aparaturowe (niejednorodno
ść
pola)
relaksacja spin-spin
Carr-Purcell-Meiboom-Gill
D1 – 90
o
– (
ττττ
– 180
o
–
ττττ
)
n
- FID
t = 0
ττττ
2
ττττ
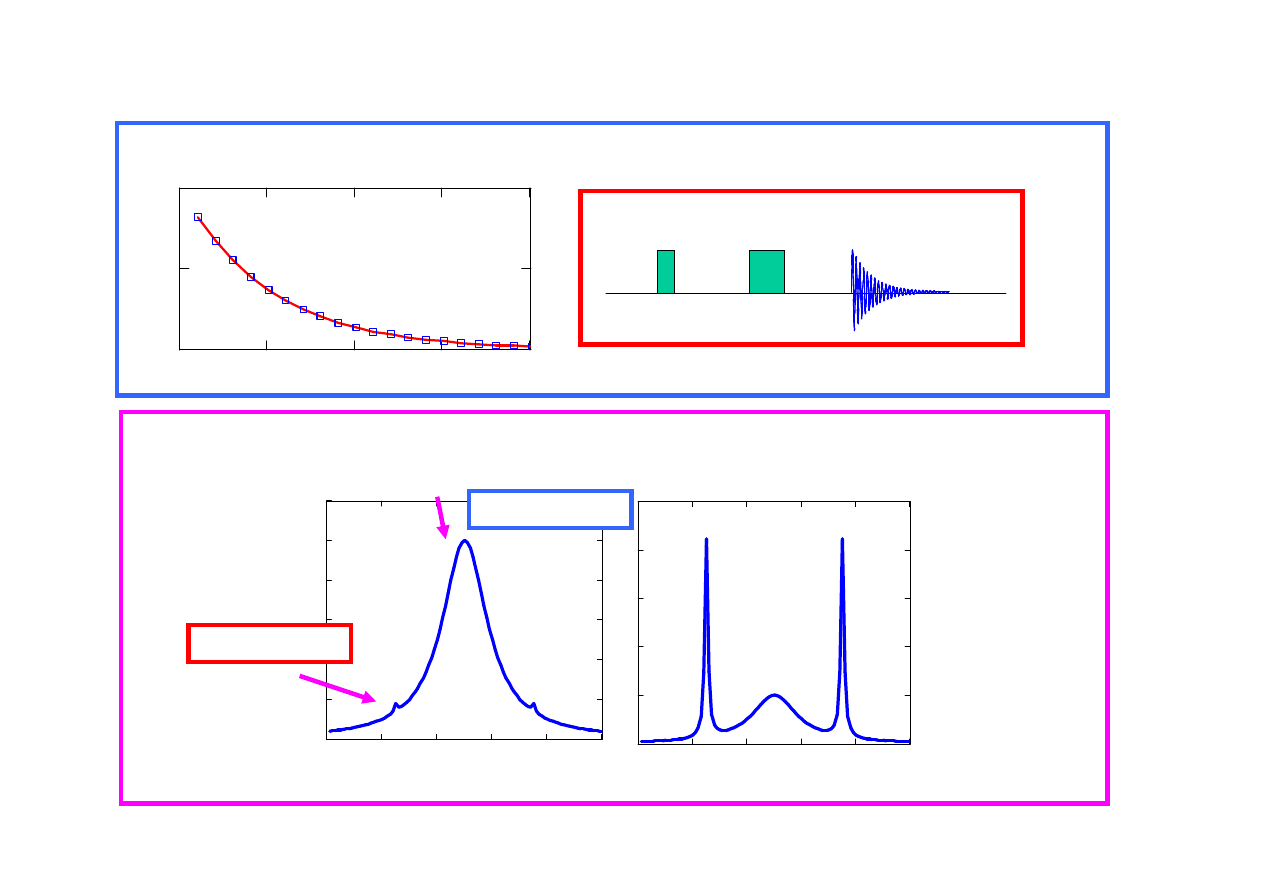
0
20
40
60
80
100
0
20
40
60
80
100
13
C-
14
N ok. 99%
13
C-
15
N ok. 1%
y = I
o
exp(-
τ
τ
τ
τ
/ T
2
)
ττττ
ττττ
ττττ
90
o
180
o
Dwa zastosowania echa spinowego
pomiar czasu T
2
Usuwanie szerokich sygnałów
Wyszukiwarka
Podobne podstrony:
NMR proton 2011
NMR wegiel 2011 (2)
2011 2 KOSZE
higiena dla studentów 2011 dr I Kosinska
Spektroskopia NMR
Plan pracy na 2011 pps
W 8 Hormony 2010 2011
wm 2011 zad 2
Zawal serca 20 11 2011
PRK 23 10 2011 org
PIW 4z 2011
pmp wykład podmioty 2011 2012
Widmo NMR
więcej podobnych podstron