
CHLORKI KWASOWE - REAKCJE
1. Przekształcenia w kwasy karboksylowe i ich pochodne
R C
OH
O
kwas
produkt
warunki
R C
OR
1
O
ester
H
2
O / zasada (pirydyna, NaOH)
reakcja hydrolizy
R
1
OH / zasada (pirydyna, NaOH)
reakcja alkoholizy
2. Redukcja
R C
Cl
O
1. LiAlH
4
(lub NaBH
4
)
2. H
2
O
R-CH
2
-OH
uwagi
a. do alkoholi
b. do aldehydów
R C
Cl
O
1. LiAlH[OC(CH
3
)
3
]
2. H
2
O
O
R
H
3. Reakcje ze związkami metaloorganicznymi
R C
Cl
O
1. R
1
MgX
2. H
2
O
a. związki Grignarda
b. związki kadmoorganiczne i miedzioorganiczne ( Gilmana)
R C
Cl
O
O
R
R
1
R
R
1
H
OH
R C
NH
2
O
amid
NH
3
lub aminy 1
0
i 2
0
reakcja aminolizy
bezwodnik
O
O
O
kwas karboksylowy w obecności zasady
lub sól kwasu karboksylowego
(R
1
)
2
CuLi
lub (R
1
)
2
Cd
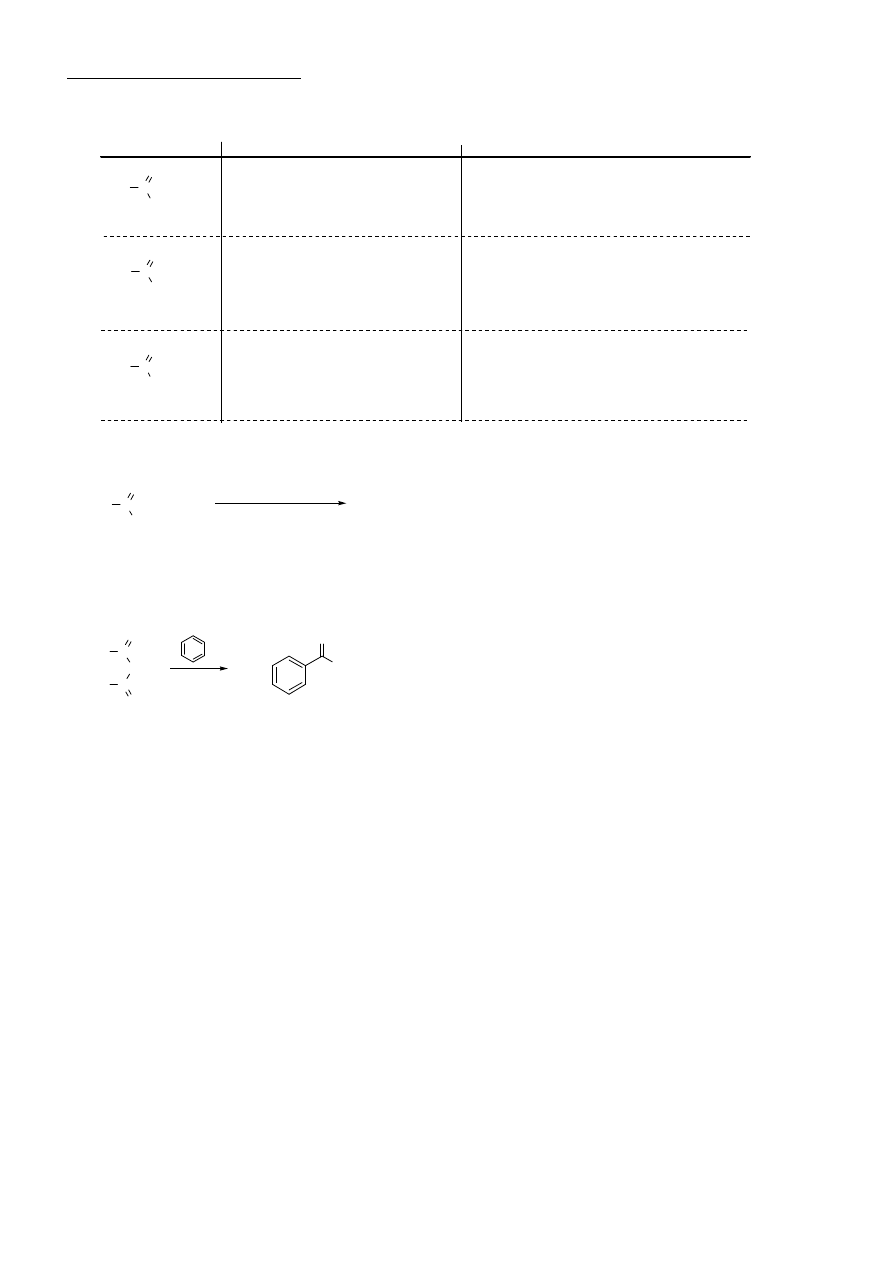
BEZWODNIKI KWASOWE - REAKCJE
1. Przekształcenia w kwasy karboksylowe i ich pochodne
R C
OH
O
kwas
związek
warunki
R C
OR
1
O
ester
R C
NH
2
O
amid
NH
3
lub aminy 1
0
i 2
0
H
2
O / zasada (pirydyna, NaOH)
reakcja hydrolizy - powstają dwie cząsteczki
kwasu karboksylowego
R
1
OH / zasada (pirydyna, NaOH)
reakcja alkoholizy
reakcja aminolizy
2. Redukcja
R C
OC(O)R
1
O
R-CH
2
-OH + R
1
OH
3. Acylowanie metodą Friedla-Craftsa
R C
O
O
AlCl
3
R
O
fenon
uwagi
C
O
R
+ R COOH
1. LiAlH
4
(lub NaBH
4
)
2. H
2
O
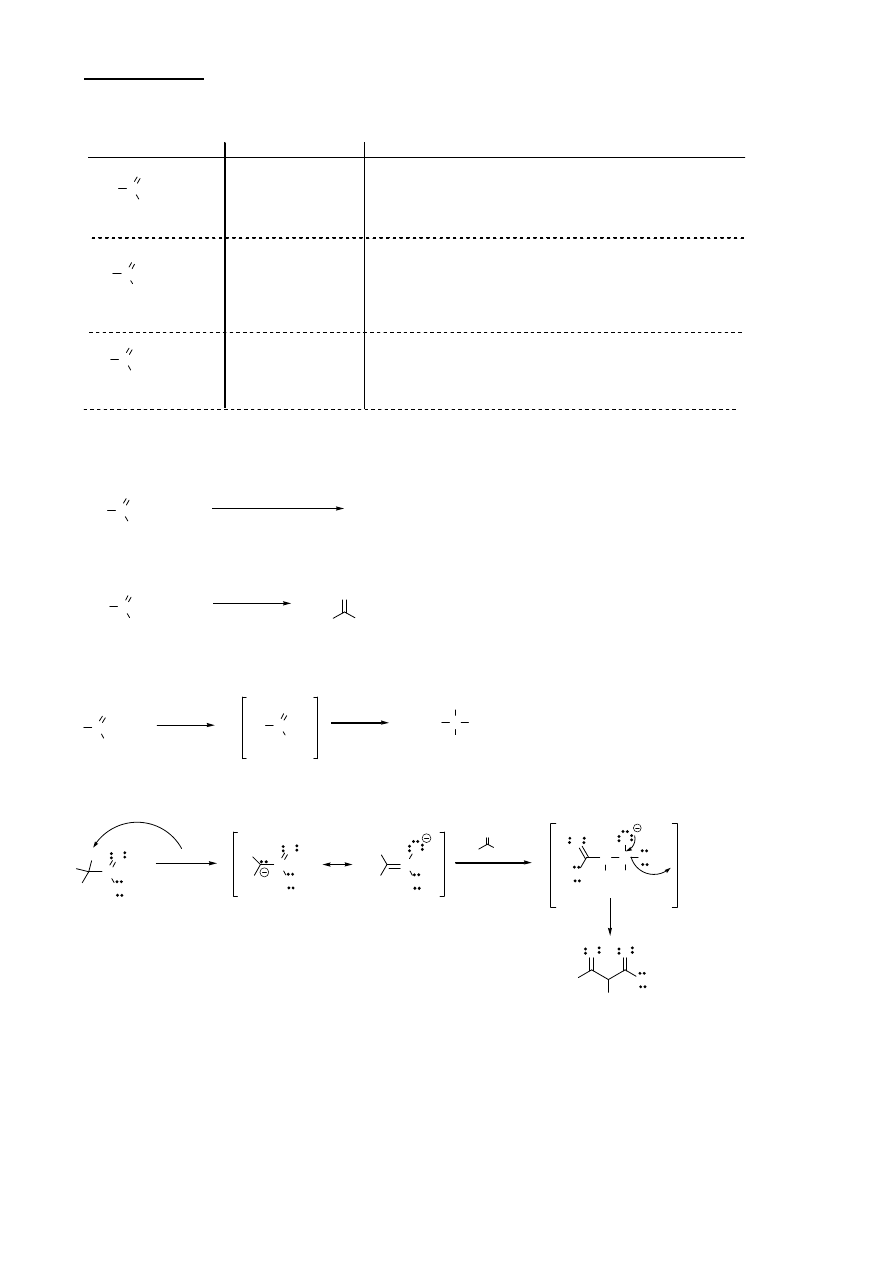
ESTRY - REAKCJE
1. Przekształcenia w kwasy karboksylowe i ich pochodne
R C
OH
O
kwas
związek
warunki
1. H
2
O / H
3
O
+
reakcja hydrolizy kwaśnej - odwracalna
reakcaj hydrolizy zasadowej (zmydlania) - praktycznie niodwracalna
2. Redukcja
3. Reakcje ze związkami magnezoorganicznymi
R C
OR'
O
R'MgX
R C
R'
O
R'MgX
OH
C
R
R'
R'
alkohol 3
0
uwagi
2. H
2
O / OH
-
R C
NH
2
O
amid
NH
3
lub aminy 1
0
i 2
0
reakcja aminolizy
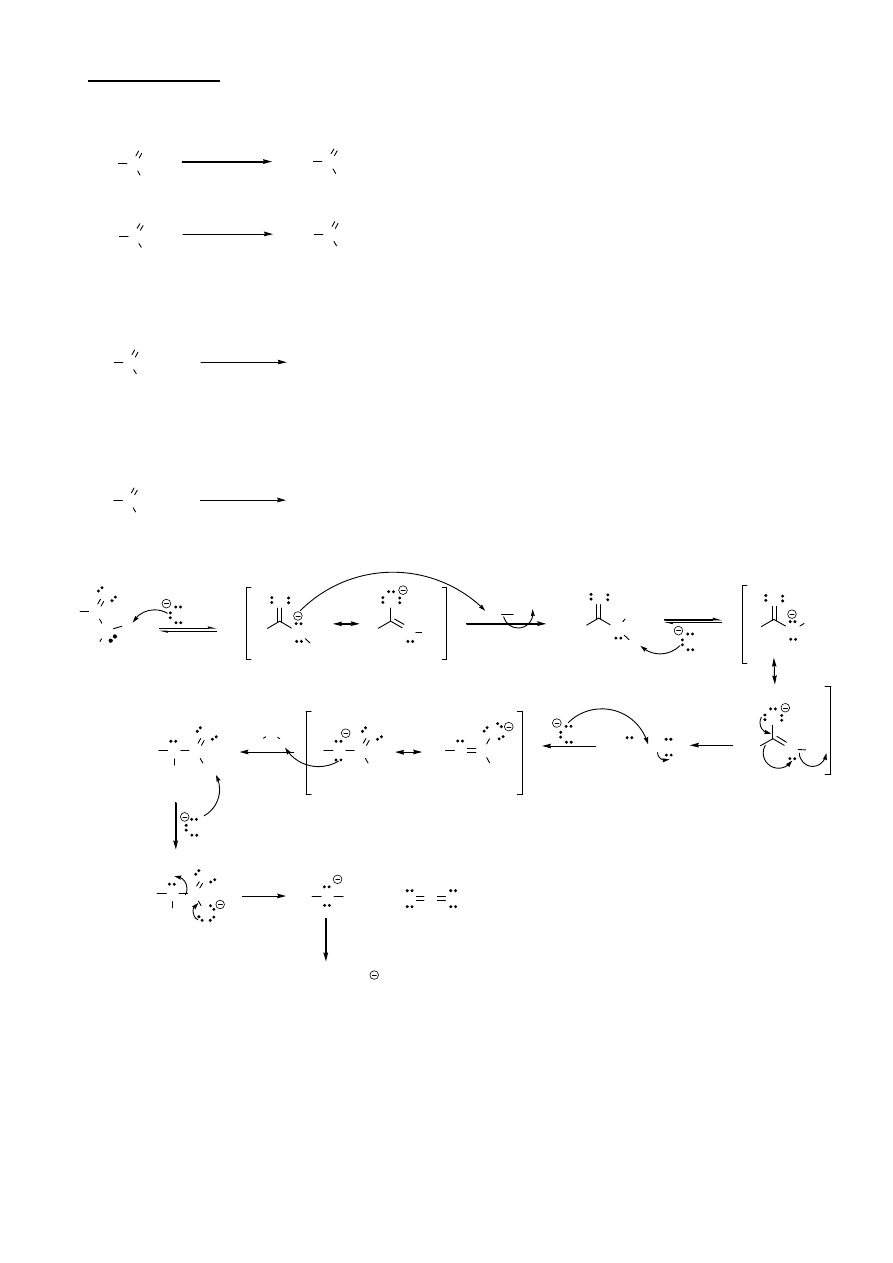
4. Kondensacja Claisena
C
OR'
O
R
EtO
-
Na
+
C
OR'
O
R
C
OR'
O
R
O
R
2
OR
1
O
C
H
C
OR
1
R
2
O
R'O
R
O
OR'
R
2
O
R
β-oksoester
R C
OR
1
O
ester
1. R
1
O / H
3
O
+
reakcja transestryfikacji katalizowana kwasem lub zasadą
2. R
1
OH / R
1
O
-
a. do alkoholi
b. do aldehydów
R C
OR
1
O
R-CH
2
-OH + R
1
OH
1. LiAlH
4
(lub NaBH
4
)
2. H
2
O
R C
OR
1
O
1. DIBAL
2. H
2
O
O
R
H
+ R
1
OH
H
H
H
H
AMIDY - REAKCJE
1. Hydroliza
2. Redukcja
R C
NH
2
O
R-CH
2
-NH
2
amina 1
0
R C
NH
2
O
H
2
O / H
3
O
+
R C
OH
O
R C
NH
2
O
H
2
O / OH
-
R C
OH
O
hydroliza kwasowa
hydroliza zasadowa
1. LiAlH
4
2. H
2
O
3. Przegrupowanie Hofmanna
R C
NH
2
O
R-NH
2
+ CO
2
amina 1
0
1. Br
2
/ OH
2. H
2
O
R C
N
O
H
H
OH
OH
O
R
N
O
R
N H
Br
Br
H
O
R
N
H
Br
N-bromoamid
OH
O
R
N
O
R
N Br
Br
R-N=C=O
nitryl
OH
R N C
OH
O
R N C
OH
O
O
H
H
R N C
OH
O
H
kwas
hydroksyamowy
R N C
O
O
H
R N H
C
O
O
+
H
2
O
R-NH
2
+ OH
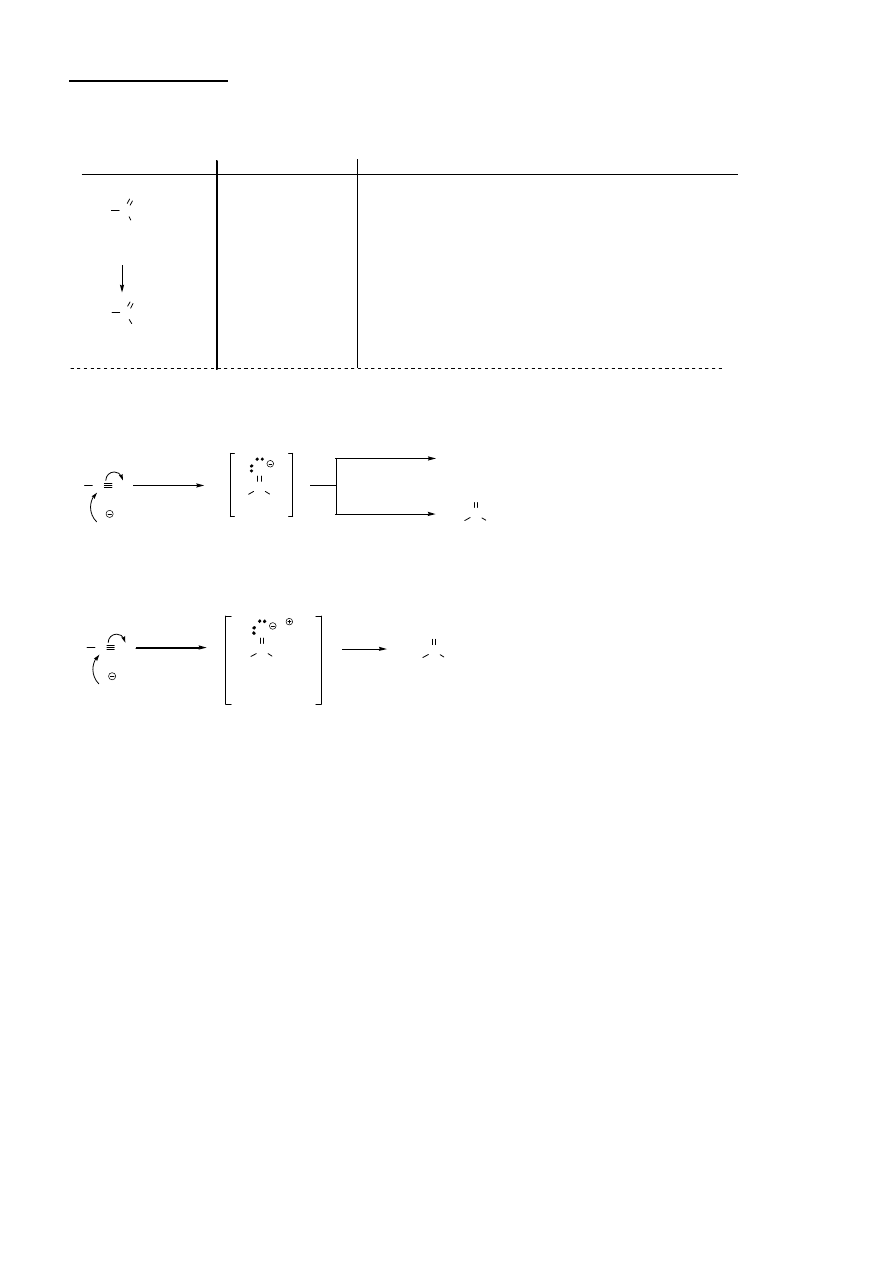
NITRYLE - REAKCJE
1. Przekształcenia w kwasy karboksylowe i ich pochodne
R C
OH
O
kwas
związek
warunki
R C
NH
2
O
amid
1 .H
2
O / H
3
O
+
reakcja hydrolizy w środowisku kwaśnym i zasadowym
w pierwszym etapie powstaje amid, który ulega dalszej hydrolizie
do kwasu karboksylowego
2. Redukcja
R C
LiAlH
4
(lub DIBAL-H)
uwagi
2. H
2
O / OH
-
N
N
C
R
H
anion iminy
H
1. LiAlH
4
/ eter
2. H
2
O
H
2
O
R-CH
2
-NH
2
O
C
R
H
amina 1
0
aldehyd
3. Reakcje z odczynnikami metaloorganicznymi
R C
R'MgX
N
N
C
R
R'
sól iminy
R'
MgX
H
3
O
+
O
C
R
R'
+ NH
3
keton
Wyszukiwarka
Podobne podstrony:
kwasy i pochodne Reakcja kwasów tłuszczowych z roztworem bromu i roztworem manganianu(VII) potasu
pochodne reakcje
Pochodne reakcje
kwasy i pochodne Reakcje z NaHCO3 i metalicznym magnezem
REAKCJE GRUPOWE I OTRZYMYWANIE POCHODNYCH
kwasy i pochodne Synteza?nzoesanu?nylu reakcja estryfikacji
Czynności obronne i reakcje stresowe
CZLOWIEK I CHOROBA – PODSTAWOWE REAKCJE NA
2 Pochodna calkaid 21156 ppt
Rozpuszczalniki organiczne pochodne alifatyczne (oprócz metanolu
W15 reakcje utlenienia redukcji
psychologiczna reakcja na katastrofy
potencjal spoczynkowy i jego pochodzenie
więcej podobnych podstron