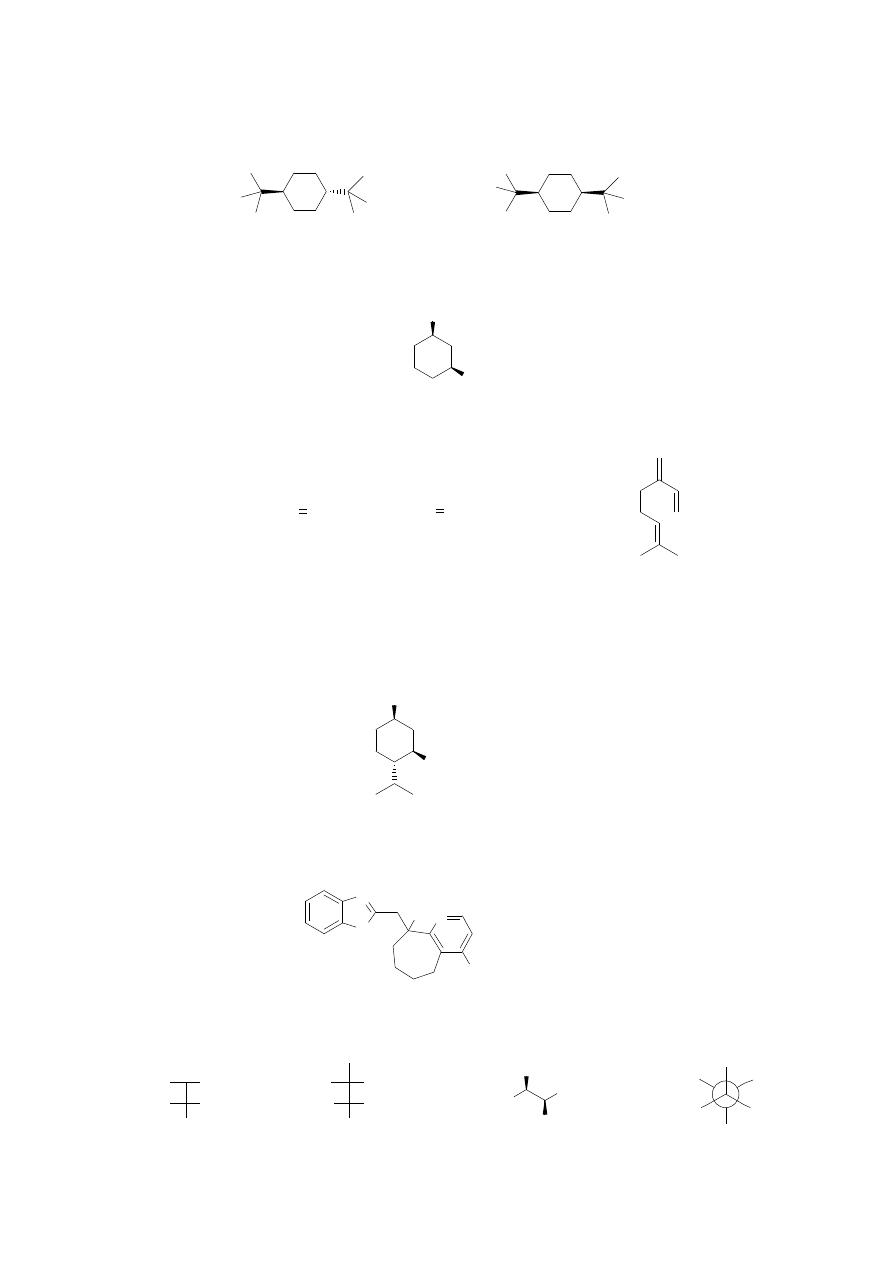
1. Związek A istnieje głównie w formie krzesłowej, a związek B w konformacji skręconej
łódki. Wyjaśnij dlaczego. (4)
A
B
2. Narysuj obie konformacje krzesłowe dla poniższego związku i uzasadnij, która z nich jest
bardziej trwała. (4)
CH
3
Br
3. Które z poniższych związków mogą istnieć jako izomery E i Z? Narysuj te izomery. (3)
(H
3
C)
2
C CHCH
2
CH
2
C(CH
3
) CHCH
2
OH
a.
b.
4. Dlaczego moment dipolowy dla CH
3
OCH
2
CH
2
OH jest znacznie większy niż dla
FCH
2
CH
2
F? (Wskazówka: przeanalizuj konformacje tych związków) (4)
5. Narysuj najniżej energetyczną konformację krzesłową mentolu. (4)
CH
3
OH
mentol
6. Nepaprazol jest racematem. Narysuj oba enancjomery Nepaprazolu z oznaczeniem, który
z nich jest R, a który S. (4)
N
H
N
N
OCH
3
H
Nepaprazol
7. Jaka jest relacja stereochemiczna związków B, C i D w stosunku do związku A. (4)
CH
3
H
OH
CH
3
H
Cl
H
Cl
CH
3
CH
3
H
OH
H
3
C
CH
3
Cl
OH
CH
3
H
Cl
H
HO
H
3
C
A
B
C
D
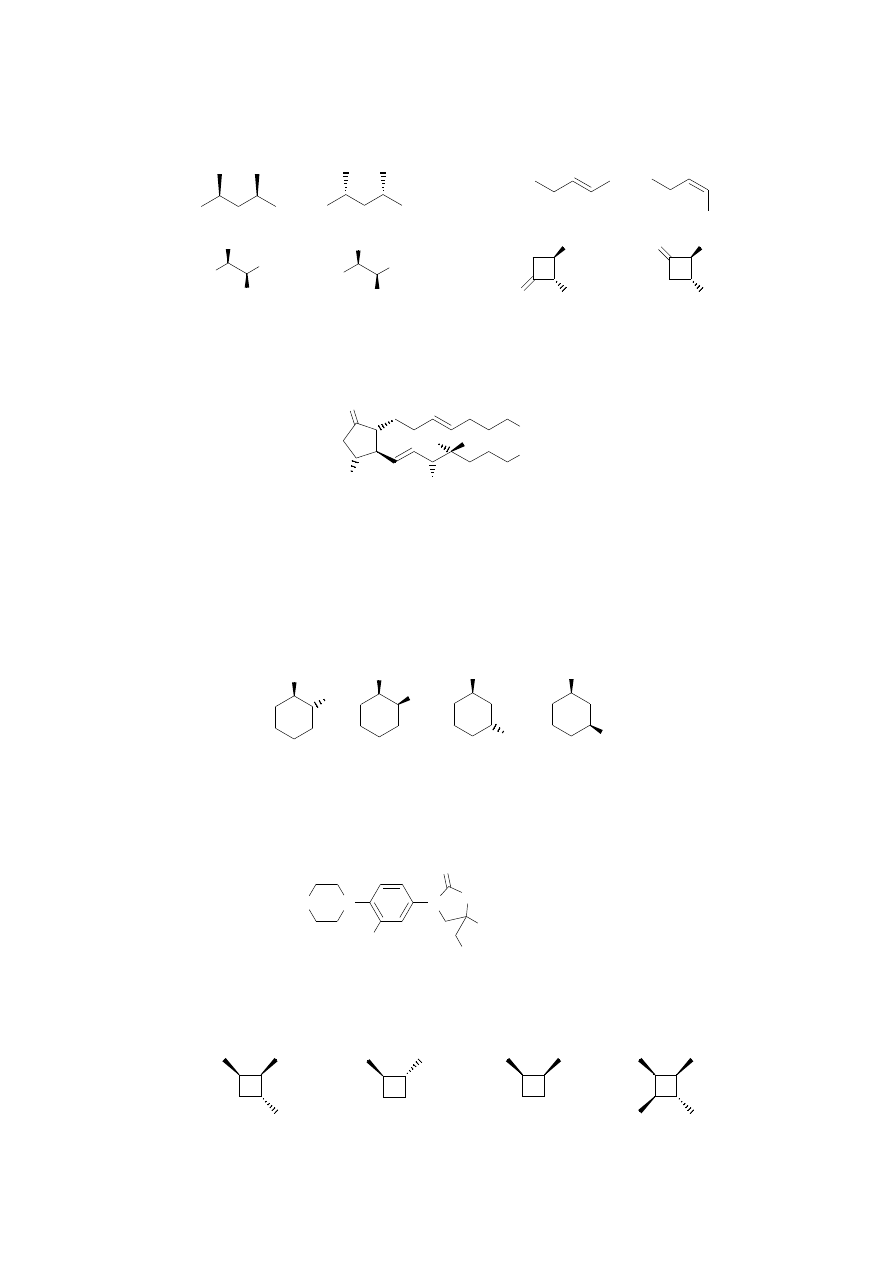
8. Jaka jest zależność stereochemiczna poszczególnych związków w parach? (4)
H
3
C
CH
3
Br
Cl
Br
CH
3
CH
3
Cl
O
CH
3
CH
3
CH
3
CH
3
O
a.
b.
c.
d.
9. Ile centrów chiralnych posiada Trimoprostic, lek przeciwwrzodowy? Ile może istnieć jego
chiralnych izomerów? Oznacz konfigurację R, S jednego z centrów stereogenicznych. (4)
COOH
CH
3
O
H
3
C
OH
H
3
C
CH
3
10. Narysuj projekcje Newmana dla następujących konformerów (4):
a. konformer gauche heksanu patrząc wzdłuż wiązania C3-C4;
b. konformer anti pentanu patrząc wzdłuż wiązania C2-C3.
11. Który(e) z poniższych związków ma oba atomy bromu w pozycji aksjalnej przynajmniej
konformacji krzesłowych? (4)
Br
Br
Br
Br
Br
Br
Br
Br
a.
b.
c.
d.
12. Syntetyczny Linezolid (antybiotyk) jest racematem. Narysuj oba enancjomery Linezolidu
z oznaczeniem, który z nich jest R, a który S. (4)
O
N
F
N
O
O
H
NHCOCH
3
Linezolid
13. Który(e) z poniższych związków jest chiralny? (3)
a.
b.
c
d.

14. (R )-Limonen jest składnikiem wielu olejków cytrusowych. Podaj jaka jest zależność
stereochemiczna związków A i B (enancjomery, diasteroizomery, takie same związki?) w
stosunku do (R )-limonenu. (4)
(R)-Limonen
A
B

15. Poniższe struktury przedstawiają 3-fluoro-2-fenylo-pentan-2-ol. Jaka jest ich relacja
stereochemiczna do (2R,3R)-3-fluoro-2-fenylo-pentan-2-olu? (4)
CH
2
CH
3
F
H
HO
CH
3
Ph
OH
Ph
H
3
C
F
A
B
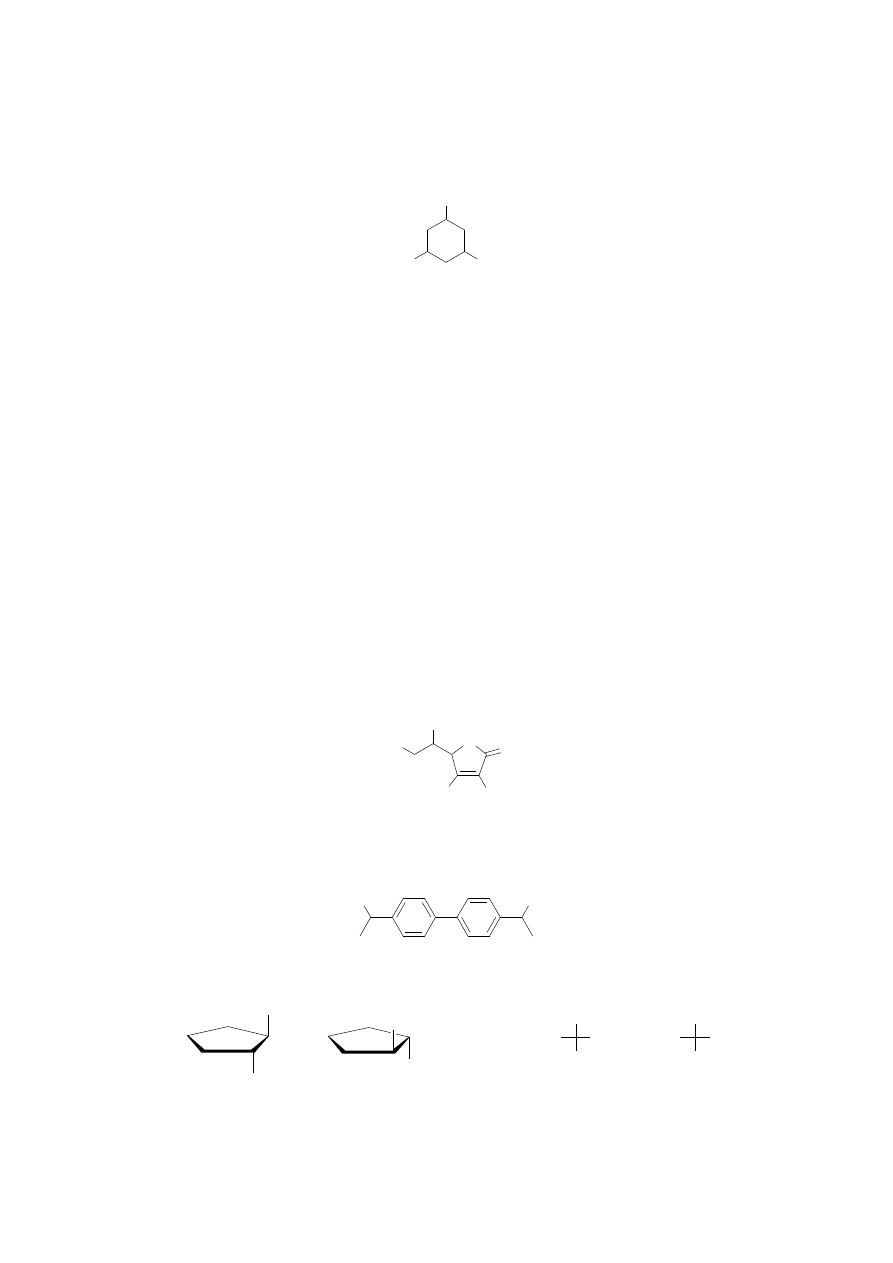
16. Dla poniższego wzoru można teoretycznie narysować osiem izomerów, ale faktycznie
istnieją tylko dwa i oba są optycznie nieczynne. Narysuj te izomery i wyjaśnij przyczynę
ich achiralności. (4)
CH
3
CH
3
H
3
C
17. Narysuj (R,R)-1,2-cyklopentanodiol oraz jego enancjomer. Związek ten posiada dwa
centra chiralne, powinny więc istnieć cztery izomery. Jednak są trzy, przy czym ten trzeci
jest nieaktywny optycznie. Narysuj go i wyjaśnij dlaczego nie jest on chiralny. (4)
18. Narysuj projekcję Fischera dla (3):
a. (S)-pentan-2-olu
b. Mezo-2,3-dihydroksybutanu.
19. Narysuj trójwymiarowy wzór (S)-2-bromobutanu. Jak wygląda jego enancjomer? (3)
20. Narysuj następujące struktury używając wzorów przestrzennych lub projekcji Fischera:
a. mezo-3,5-dibromoheptan; (2)
b. (S)-3-chloro-3-metyloheksan. (2)
21. Narysuj wzór przestrzenny oraz wzory Newmana i Fischera dla mezo-1,2-dibromo-1,2-
difenyloetanu. (3)
22. Znajdź centra stereogeniczne (chiralne atomy) na poniższym wzorze witaminy C i narysuj
jedną z par enancjomerów używając wzorów przestrzennych.(4)
O
HO
O
OH
HO
OH
23. Narysuj wszystkie możliwe stereoizomery dla poniższego związku. Które z nich są
chiralne? (3)
OH
HO
24. Jaka jest relacja stereochemiczna poniższych związków w parach? (4)
a.
CHO
OH
H
CH
3
H
CHO
HO
CH
3
b.
25. Jaka jest relacja stereochemiczna poniższych związków w parach? (4)

CH
3
H
Cl
CH
2
CH
3
H
Cl
H
3
CH
2
C
CH
3
CH
2
OH
HO
CHO
H
CHO
CH
2
OH
HO
H
a.
b.
Wyszukiwarka
Podobne podstrony:
Równania różniczkowe 13 doc
semquiz 13-4, 1
Doktryny PS wyklady 1 13 doc id 139353
semquiz 13-1, 1
Biochemia przedtermin 13 doc
77A (13) DOC
Åwiczenie 13 doc
378424464 La Roma Imperial 13 doc
II 13 doc
50A (13) DOC
CW 13 DOC
DYSKI 13 DOC
Sprawozdanie 2 (13) doc
WYKRESY (13) DOC
раздел 13 doc
ćwiczenie 13 doc
Fotoradary Opis 2009 10 13 doc
więcej podobnych podstron