Struktura
przestrzenna
kryształów metali
i stopów
Biszczanik Katarzyna
Czarnota Agnieszka
Rogala Katarzyna
Sobolewska Rebeka
Ogólne informacje o metalach
szlachetne
• odporność na korozję w ekstremalnych warunkach
(j. ustna)
• złoto, pallad, platyna
• drogie
nieszlachetne
• tytan, nikiel, miedź, srebro, cynk
• niezbędne składniki stopów dentystycznych
• wytrzymałe, odporne na ścieranie, elastyczne
• w czystej formie bardziej podatne na korozję w j.
ustnej
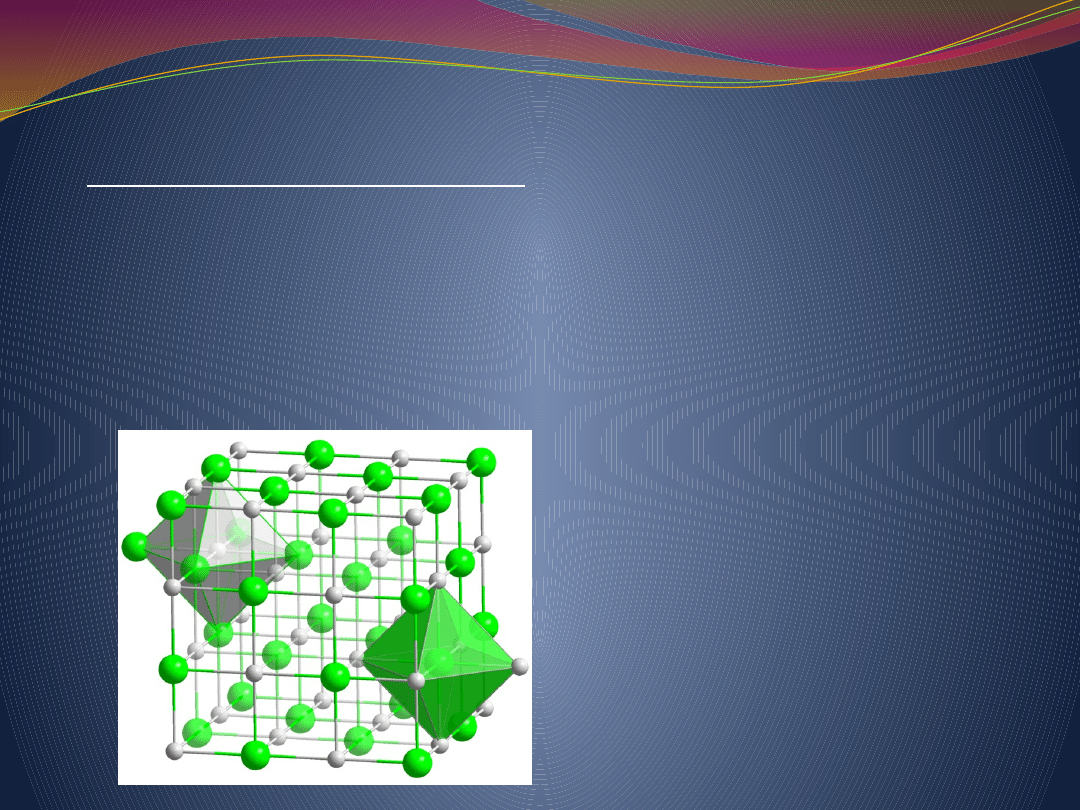
Krystalografia metali
•
krystalografia
– opis budowy ciał stałych
•
kryształ
– ciało stałe, anizotropowe, w którym
atomy ułożone są w równych powtarzających
się odstępach, w co najmniej trzech
nierównoległych kierunkach
Struktura krystaliczna azotku
tytanu
Każda prosta łącząca środki dwóch atomów w krysztale
nazywana jest
prostą sieciową
. Najbliższa odległość
atomów na prostej sieciowej w sieci prymitywnej nosi
nazwę podstawowego periodu identyczności lub
parametru sieci
. Przesunięcie, tzw. translacja prostej
sieciowej, o period identyczności w kierunku różnym od
kierunku prostej powoduje znalezienie
płaszczyzny
sieciowej
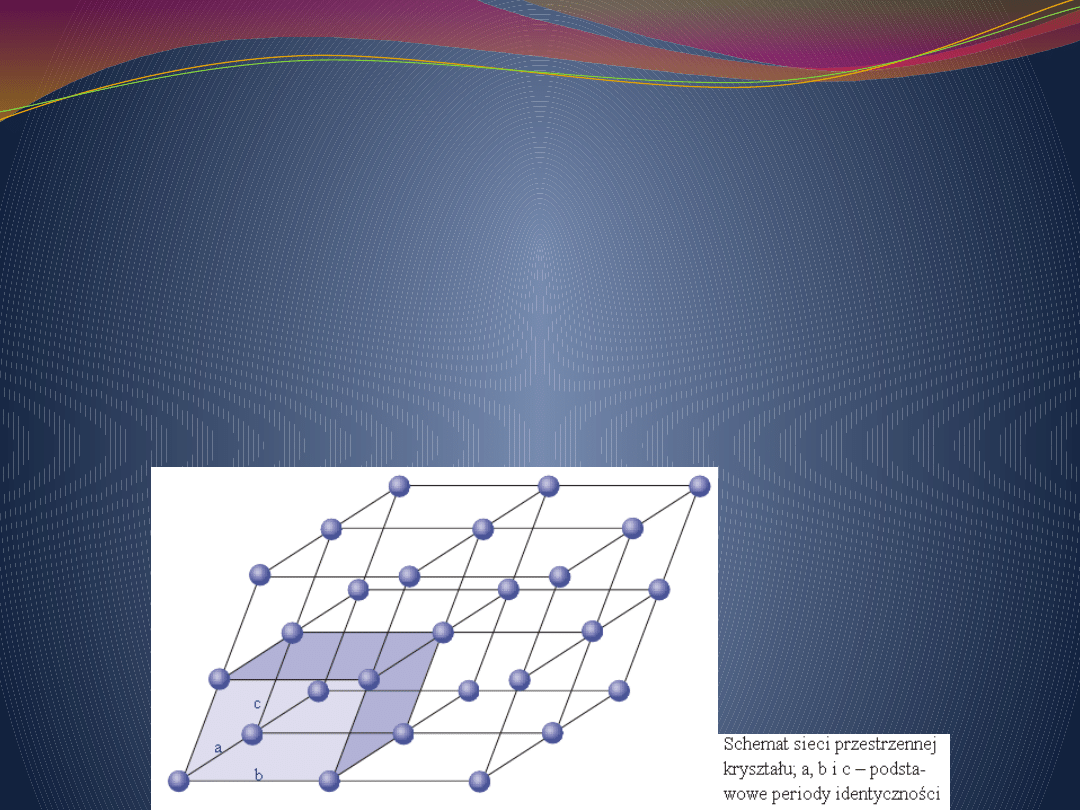
. Płaszczyzna sieciowa poddana translacjom w
kierunku do niej nierównoległym tworzy
sieć
przestrzenną
.
Elementami sieci przestrzennej są zat
em:
•
płaszczyzny sieciowe
•
proste sieciowe
, będące śladami
przecięcia płaszczyzn sieciowych,
•
węzły sieci
, stanowiące punkty przecięcia
prostych sieciowych; węzły sieci
prymitywnej odpowiadają położeniu
środków atomów kryształu.
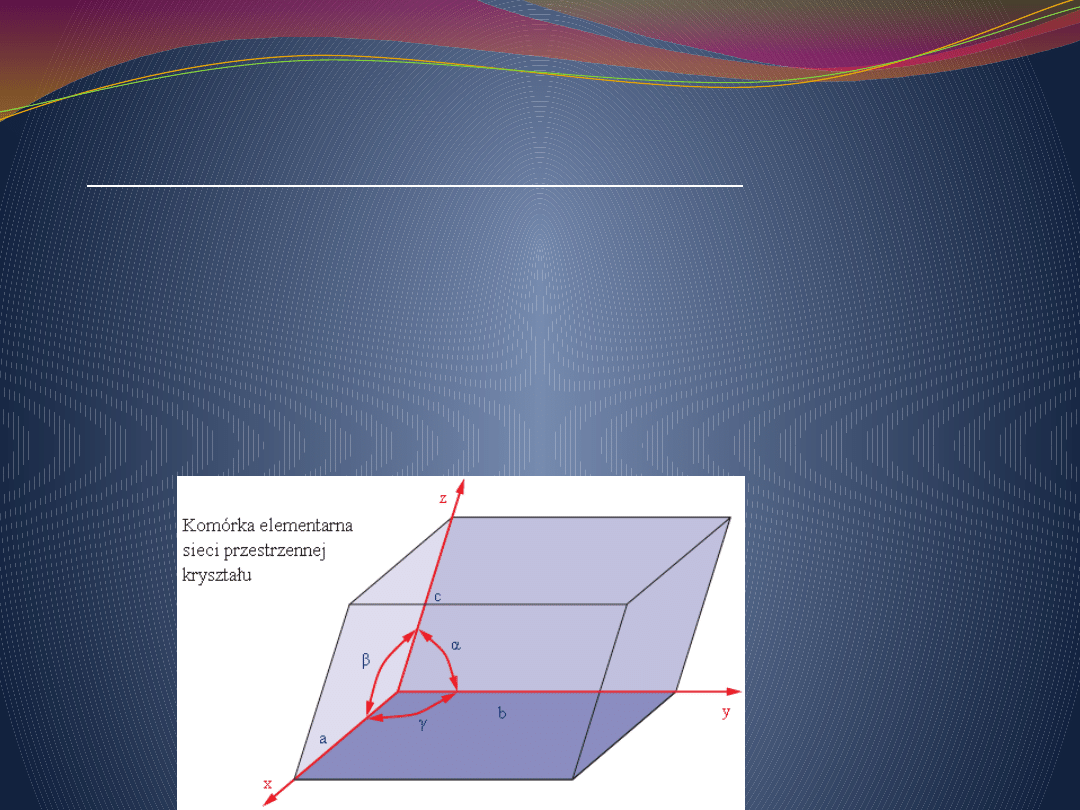
Elementarna komórka sieciowa
Trzy rodziny równoległych płaszczyzn sieciowych dzielą sieć
przestrzenną na identyczne równoległościany o
parametrach a, b i c, stanowiących podstawowe periody
identyczności (parametry) sieci. Równoległościany te są
nazwane
elementarnymi komórkami sieciowymi
i w pełni
charakteryzują dany kryształ. Komórka sieciowa może być
opisana przez jej podstawowe periody identyczności
(parametry sieci) a, b i c oraz kąty między nimi zawarte .
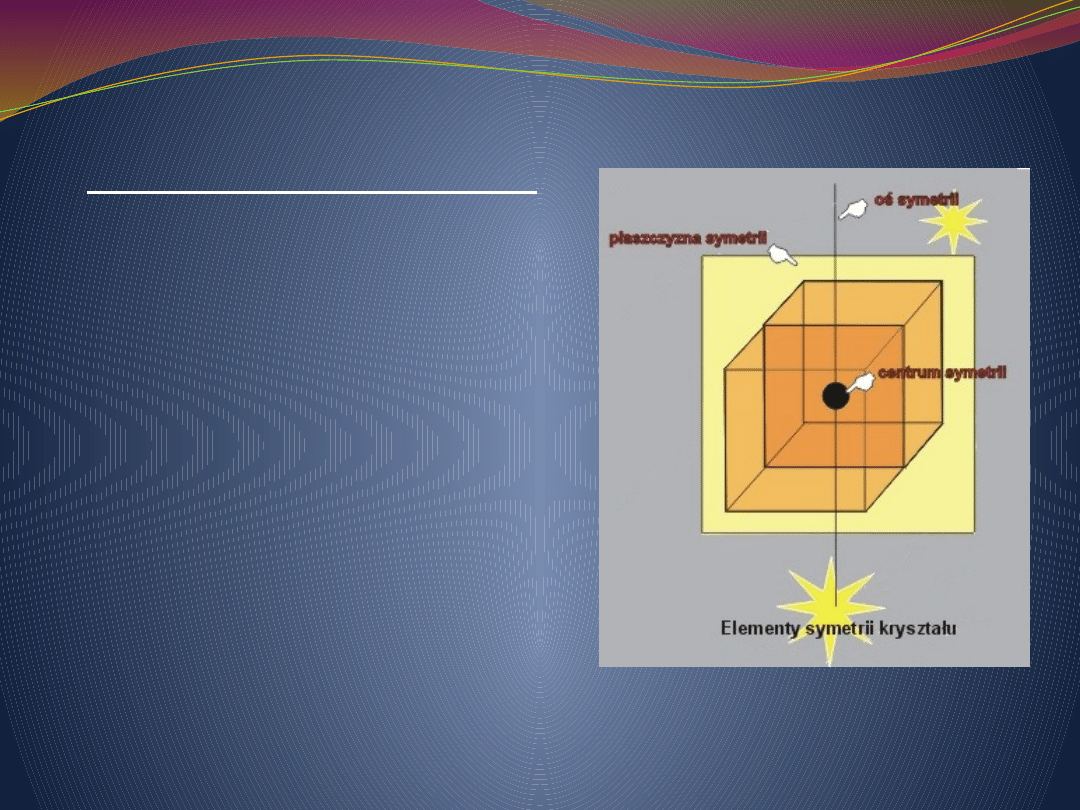
Symetria kryształu
Kryształ
charakteryzuje się
symetrycznym
ułożeniem elementów
sieci przestrzennej.
Proste elementy
symetrii jakie mogą
występować w
kryształach to
środek
,
osie
i
płaszczyzny
symetrii
.
Typy sieci przestrzennej
W zależności od tego czy elementarne
komórki sieciowe mają atomy wyłącznie na
narożach (komórki prymitywne), czy także
wewnątrz lub na ścianach bocznych
(komórki złożone), w ramach układów
krystalograficznych występuje
14 typów
sieci przestrzennej Bravais’go.
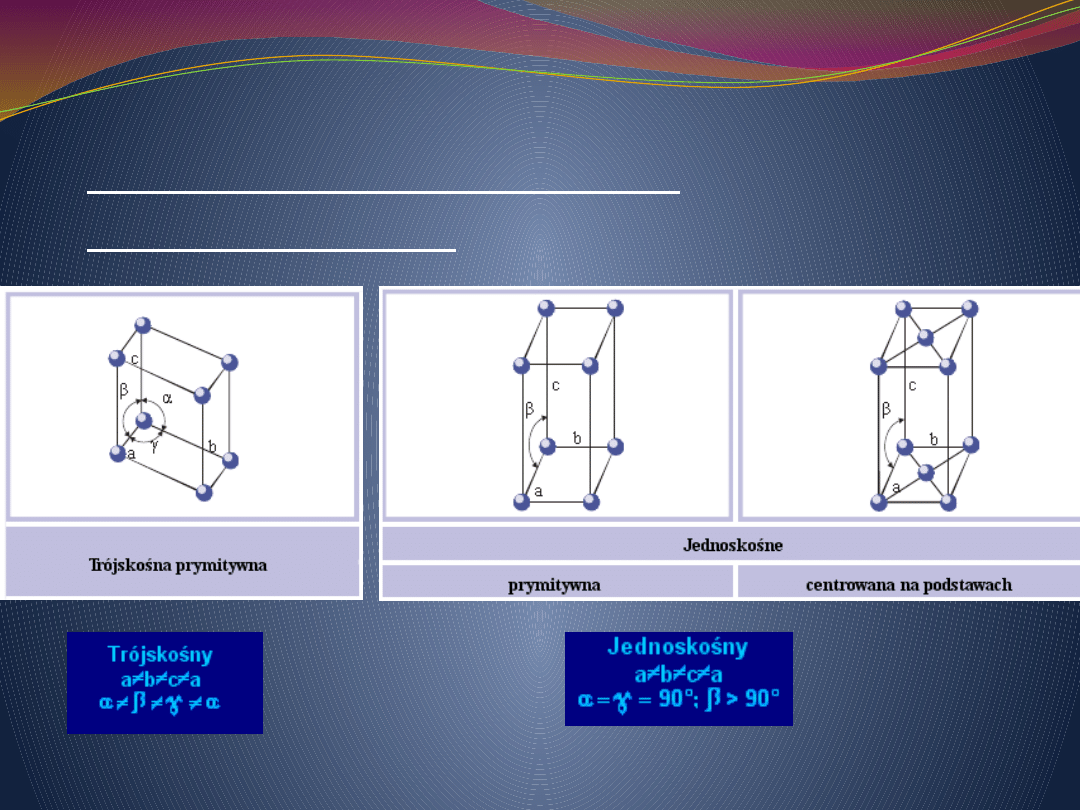
Schematy rodzajów sieci
przestrzennych
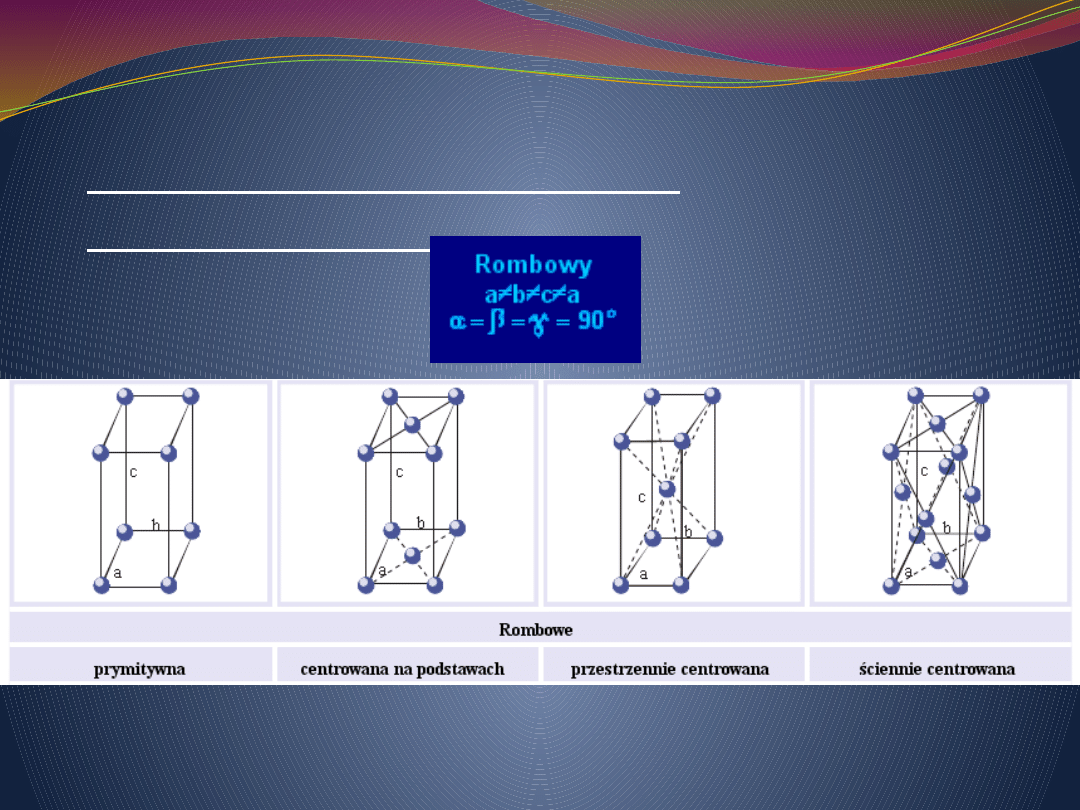
Schematy rodzajów sieci
przestrzennych
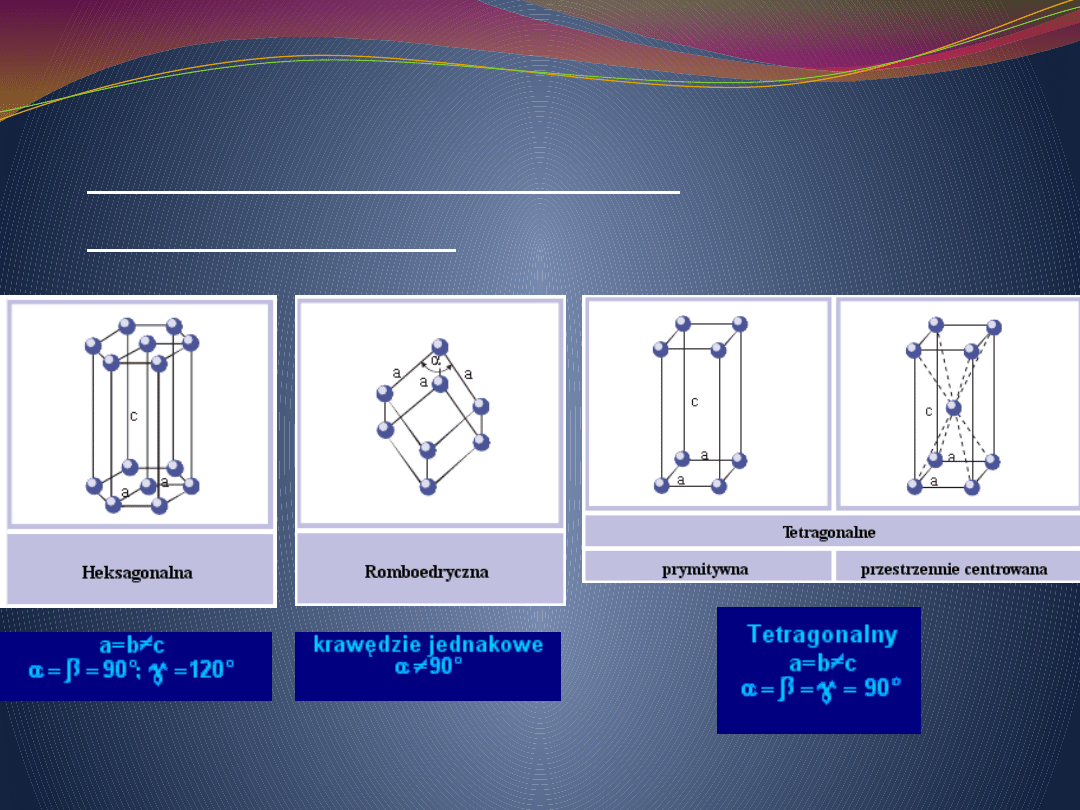
Schematy rodzajów sieci
przestrzennych
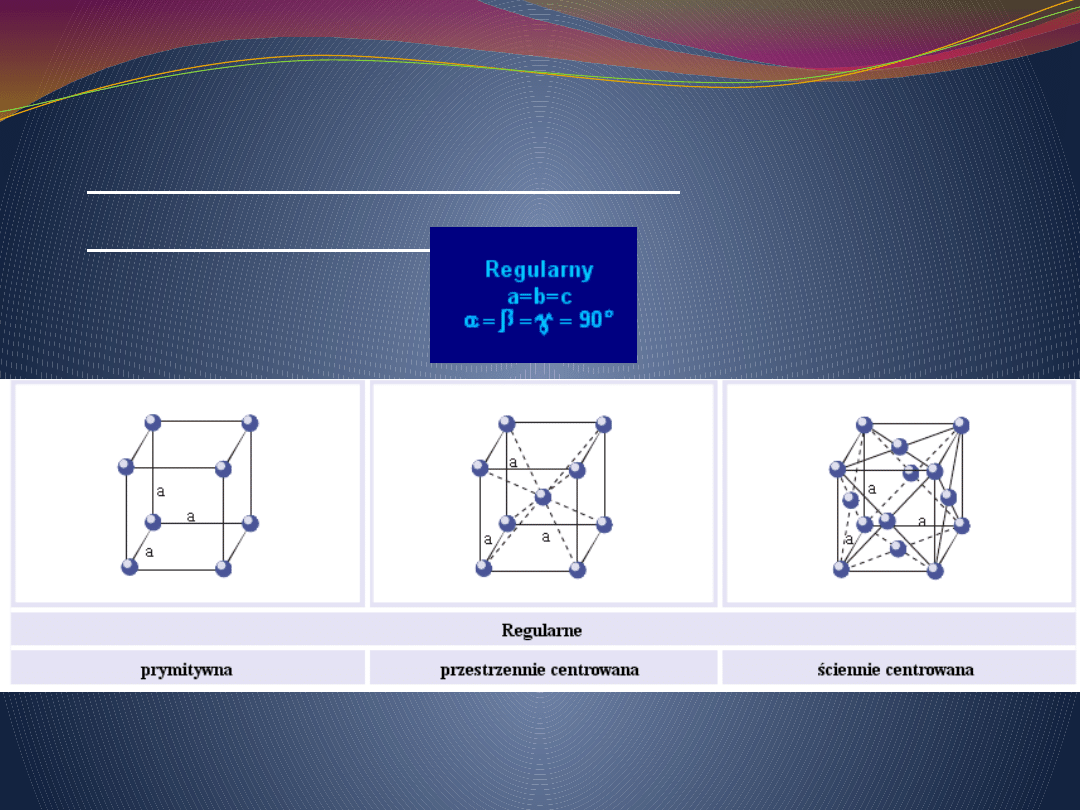
Schematy rodzajów sieci
przestrzennych
Pełzanie metali
Pełzanie metali przy
rozciąganiu – powolne, ciągłe
plastyczne wydłużanie się
metalu pod
stałym
obciążeniem
i przy
stałej
temperaturze.
Metale podstawowe stosowane w
protetyce:
-
Złoto
- Platyna
- Pallad
Metale pomocnicze stosowane w
protetyce:
- Nikiel
- Miedź
- Srebro
- Cynk

Złoto
– czyste charakteryzuje się ładnym, żółtym
połyskiem
- jest bardzo miękkie, kowalne, ciągliwe
- posiada dużą odporność chemiczną
- używa się go prawie wyłącznie w stopach z
innymi metalami
czyste złoto bywa używane do lutowania platyny
oraz jako folia złota do wypalania porcelany
do koron i płyt podstawowych używa się
22-karatowego złota, klamer i łuków – 18,
do wkładów koronowych 20-22- karatowego.
Platyna
duża odporność na działanie czynników
chemicznych
metal miękki, daje się łatwo kuć i walcować
jest barwy srebrzystobiałej
z platyny można wykonywać mosty i korony,
czystą platynę w postaci folii stosuje się na
czapeczki do wypalania wysoko topliwej masy
ceramicznej
platyna w postaci drutu oporowego ma
zastosowanie w elementach grzejnych pieców do
wypalania dentystycznej masy ceramicznej
Pallad
barwa palladu jest srebrzysta
niezbyt twardy, plastyczny, ciągliwy
ma własności wchłaniania wodoru
posiada wybitne właściwości odbarwiające stopy
jego stop ze srebrem (9:1) służy do wyrobu
ćwieczków do licówek porcelanowych
Nikiel
metal o silnym srebrzystobiałym połysku,
twardy, ciągliwy
odporny na działanie alkaliów, kwasów
organicznych
i wody
nadaje stopom odpowiednie właściwości
mechaniczne oraz zwiększa obojętność
chemiczną
jego stop służy do wyrobu drutu na uzwojenia
grzejne i oporowe pieców elektrycznych
dawniej używany był do powlekania narzędzi
żelaznych
Miedź
metal ciężki, kowalny, barwy czerwonej
daje się łatwo topić, stopiona charakteryzuje się
dużą płynnością
jako czysta miedź nie ma zastosowania w
protetyce jako materiał podstawowy
z czystej miedzi wyrabia się osłony do elektrod
węglowych, pierścienie miedziane do wycisków
pojedynczych zębów oraz modele metodą
galwanoplastyczną
Srebro
czyste jest barwy białej o silnym połysku
twarde, wytrzymałe, łatwe w obróbce
chemicznej i termicznej, ciągliwe, dające się
łatwo kuć i walcować
odporne na działanie tlenu z powietrza
ze względu na to, że sole srebra są trujące w
Polsce zakazane jest wykonywanie prac
dentystycznych ze srebra
może być stosowane jeśli nie będzie się stykało
bezpośrednio z płynami środowiska jamy ustnej
stosuje się do wykonywania wkładów
korzeniowych do koron akrylowych
Cynk
metal o niebieskawym połysku
kruchy, musi być ogrzany do temp. 100-150˚
przed obróbką, wtedy staje się kowalny i ciągliwy
metal chemiczni czynny
w czystej postaci nie jest stosowany w protetyce
tlenek cynkowy używany jest jako biała farba,
jest składnikiem wszystkich cementów
dentystycznych
z jego stopów wykonuje się tłocznie i
przeciwtłocznie
Stopy metali
Czyste metale są w technice stosowane
stosunkowo rzadko. Powszechne zastosowanie
znajdują stopy metali – w wielu przypadkach
wykazujące lepsze własności niż czyste
metale.
Stopy są substancjami dwu- lub
wieloskładnikowymi, makroskopowo
wykazującymi własności metaliczne. Co
najmniej jeden z głownych składnikow stopu
jest
metalem. Składnikami stopow są substancje
proste, np. pierwiastki, lub złożone –
np. związki nie ulegające przemianom.
Stopy mogą mieć strukturę jedno- lub wielofazową. Faza
to jednorodna część stopu, oddzielona od pozostałej
jego części granicą międzyfazową.
Poszczegolne fazy stopu zwykle dość znacznie rożnią się
między sobą własnościami.
Liczba, rodzaj i własności faz są uzależnione od składu
chemicznego stopu.
Zbior faz znajdujących się w stanie rownowagi
termodynamicznej jest nazywany układem.
Stopy metali są wytwarzane głownie przez topienie i
krystalizację ze stanu ciekłego. W wyniku tych
procesow z cieczy, będącej zwykle roztworem
wszystkich składnikow stopu, mogą powstać:
roztwory stałe,
fazy międzymetaliczne,
mieszaniny faz.
Roztwory stałe
Roztwor stały stanowi jednorodną fazę o
wiązaniu metalicznym i strukturze
krystalicznej o własnościach typowo
metalicznych.
Metal, którego atomy występują w sieci w
przewadze, jest rozpuszczalnikiem. Drugi
składnik jest nazywany pierwiastkiem
rozpuszczonym.
W przypadku gdy atomy pierwiastka rozpuszczonego są
usytuowane w sposób nieuporządkowany w
przestrzeniach międzywęzłowych sieci metalu
rozpuszczalnika, roztwór stały jest nazywany
roztworem stałym międzywęzłowym .
Atomy pierwiastka rozpuszczonego B powodują
ekspansję sieci rozpuszczalnika. Ponieważ w sieciach
A1, A2 i A3 przestrzenie
międzywęzłowe są niewielkie, mieszczą się w nich atomy
pierwiastków o niewielkich średnicach atomowych.
Roztwory te tworzą zwykle metale przejściowe
– w tym żelazo z niemetalami, głownie węglem, azotem,
wodorem
i borem. Roztwory stałe międzywęzłowe są roztworami
granicznymi, a rozpuszczalność graniczna zmienia się
zwykle
wraz ze zmianą temperatury.

Gdy atomy metalu rozpuszczonego zajmują przypadkowo
dowolne węzły w sieci krystalicznej metalu
rozpuszczalnika,
roztwór stały jest nazywany roztworem stałym
różnowęzłowym.
Obecność atomow innego pierwiastka w sieci
krystalicznej rozpuszczalnika, w zależności od stosunku
średnic atomów
rozpuszczalnika i pierwiastka rozpuszczonego, powoduje
odkształcenie sieci – ekspansję lub kontrakcję.
Roztwory stałe rożnowęzłowe mogą być ciągłe lub
graniczne. W roztworach stałych ciągłych liczba
węzłów sieci krystalicznej rozpuszczalnika zajętych
przez atomy drugiego składnika rośnie wraz ze
zwiększaniem się stężenia składnika rozpuszczonego
– od struktury czystego metalu A do struktury metalu B.
W niektórych roztworach stałych rożnowęzłowych o
określonych stosunkach stężenia atomowego
składników metalicznych
A i B, np. w wyniku wolnego chłodzenia lub wygrzewania
w stałej temperaturze, nieuporządkowany rozkład
obydwu składników
zmienia się na uporządkowany. Roztwór stały,
charakteryzujący się prawidłowym rozkładem atomów
obydwu składników w sieci, jest nazywany
nadstrukturą i powstaje w wyniku przemiany:
nieporządek porządek
Ponieważ przemiana ta jest odwracalna, przy nagrzaniu
do określonej temperatury następuje zanik
nadstruktury.
Fazy międzymetaliczne
Fazy międzymetaliczne są połączeniami metali lub metali z
niemetalami i wykazują własności metaliczne ze względu na
częściowy lub całkowity udział wiązania metalicznego
między atomami wchodzącymi w skład fazy.
Charakterystyczne cechy faz międzymetalicznych opisują
cztery zasady:
struktura krystaliczna faz międzymetalicznych rożni się od
struktury każdego ze składników,
atomy każdego ze składników wykazują uporządkowane
rozmieszczenie w sieci krystalicznej,
w oddziaływaniach między atomami występuje przewaga
wiązania metalicznego,
wzajemne stosunki ilościowe atomów składników rzadko
odpowiadają wartościowościom chemicznym pierwiastków,
jakie wykazują one w związkach chemicznych, chociaż
fazom można przypisać wzory podobne do wzorów związków
chemicznych.
Fazy międzymetaliczne występują przy ściśle
określonych stężeniach składników stopu,
chociaż mogą występować również w pewnym
zakresie stężeń
i tworzyć roztwory stałe wtórne.
Roztwory te mogą być:
różnowęzłowe,
międzywęzłowe,
pustowęzłowe.
W roztworach pustowęzłowych występuje
nadmiar atomów jednego ze składników, a w
węzłach sieci krystalicznej, które miałyby być
obsadzone atomami
drugiego składnika, powstają wakanse.
Fazy międzywęzłowe o strukturach prostych mają
własności metaliczne i krystalizują w sieciach
regularnej ściennie centrowanej i heksagonalnej
zwartej, a także regularnej przestrzennie
centrowanej i heksagonalnej prostej. Sieć
krystaliczna faz międzywęzłowych o strukturach
prostych jest przy tym zwykle rożna od sieci
czystego metalu.
Węzły sieci krystalicznej tych faz są zajęte przez
atomy ktoregoś metalu przejściowego M, a w
przestrzeniach międzywęzłowych są usytuowane
atomy niemetali X o małym promieniu atomowym,
tj. atomy węgla, azotu, wodoru lub boru.
Do faz międzywęzłowych o strukturach prostych są
więc zaliczane wodorki, niektore borki, a także
niektore węgliki i azotki metali przejściowych.
Fazy międzywęzłowe o strukturach złożonych
tworzone przez metale przejściowe i
niemetale zwykle mają znaczną liczbę atomów
w komórce strukturalnej.
Fazy te cechują się również własnościami
metalicznymi, są jednak mniej trwałe od faz
międzywęzłowych prostych.
Struktury złożone wykazuje większość borków
oraz niektóre azotki i węgliki żelaza, kobaltu,
niklu, manganu i chromu, a także węgliki
podwójne.
Mieszaniny faz
Stanem stopu, występującym bardzo często, jest
mieszanina faz. O mieszaninie faz mówi się wtedy,
gdy w stopie znajdują się co najmniej dwie fazy w
stanie rozdrobnienia, oddzielone od siebie granicami
międzyfazowymi.
Każda faza ma przy tym określone, właściwe sobie,
skład chemiczny, strukturę krystaliczną i własności.
Mieszaniny faz mają zwykle lepsze własności
wytrzymałościowe i mniejszą plastyczność od
poszczególnych faz.
Eutektyk
– mieszanina dwóch lub więcej faz
krystalicznych o określonym składzie, która
wydziela się z roztworów ciekłych lub stopów w
określonej temperaturze, zwanej temperaturą
eutektyczną. Jest ona na ogół znacznie niższa
od temperatury krzepnięcia czystych
składników. Kryształy eutektyku są czystymi
kryształami składników lub roztworami stałymi o
różnych składach.
Ziarna i struktura krystaliczna
stopów
Podczas tężenia roztopionego stopu
dochodzi do formowania i powiększania
kryształów. Stop metalu oglądany pod
mikroskopem zawiera widoczne kryształy,
nazywane w metalurgii także ziarnami.
Wielkość ziaren stanowi ważną cechę stopu,
szczególne zaś znaczenie maja kryształy małe.
Aby zmniejszyć wielkość kryształów w stopach
złota, dodaje się często specjalne składniki
uszlachetniające. Pierwiastkami o takich
właściwościach są iryt i ruten.
Struktura krystaliczna stopów, bardzo złożona , zależy
przede wszystkim od składu. W stopach o dużej
zawartości metali nieszlachetnych dominują ziarna
krystaliczne o większej średnicy; w takich stopach nie
można już stosowa składników obniżających średnicę
kryształu.
Podział stopów
•
Wysoko szlachetne
•
Szlachetne
•
Nieszlachetne
Wysoko Szlachetne
Stopy takie muszą zawiera przynajmniej
60% metali szlachetnych, w tym przynajmniej
40% złota. Do tego typu stopów należą:
•
Złoto-platyna (uzupełnienia złożone
metalowo-porcelanowe, odlewy pełne
metalowe),
•
Złoto-miedź-srebro (odlewy pełne
metalowe).
Szlachetne
W takich stopach zawartość metali
szlachetnych powinna wynosić co najmniej
25%, z tym że nie określono ilości złota, która
powinna znajdować się w stopie. Do tego typu
stopów należą:
•
Srebro-złoto-miedź (odlewy pełne
metalowe),
•
Pallad-miedź (odlewy pełne metalowe,
uzupełnienia złożone metalowo-
porcelanowe),
•
Srebro-pallad (odlewy pełne metalowe,
uzupełnienia złożone metalowo-
porcelanowe).
Nieszlachetne
Do trzeciej grupy należą stopy zawierające
w większości metale nieszlachetne; metali
szlachetnych jest w nim mniej niż 25%. Należą
do nich:
•
Stopy na bazie niklu (odlewy pełne
metalowe, protezy częściowe),
•
Stopy na bazie kobaltu (prefabrykowane
elementy poddawane obróbce plastycznej),
•
Stopy na bazie tytanu ( protezy częściowe,
implanty).
Cechy stopów:
•
Przedział topnienia,
•
Gęstość,
•
Wytrzymałość,
•
Twardość,
•
Biokompatybilność.
Przedział topnienia
Stopy matali nie ulegają topnieniu w
konkretnej temperaturze, lecz w ściśle
określonym przedziale topnienia, np. 950-
1000○C. Temperatura, w której stop w całości
przechodzi w postać płynną, nazywa się
„likwidusem”, podczas gdy temperatura, w
której stop podczas ochładzania przechodzi w
całości w postać stała, nosi miano „solidusa”.
Gęstość
Gęstość stopu oznacza ilość stopu, która
zajmuje objętość 1 cm³. Gęstość stopów
dentystycznych mieści się w przedziale od 4,5
g/cm³ (stopy tytanowe) do przeszło 18 g/cm³
(niektóre stopy wysoko szlachetne). Stopy o
dużej gęstości są łatwiejsze do odlewania,
ponieważ grawitacja przyspiesza napływanie
stopu do formy odlewniczej.
Wytrzymałość stopów
Elementy wykonane ze stopów
dentystycznych musza mieć odpowiednią
wytrzymałość, aby nie doszło do zmiany ich
kształtu w jamie ustnej.
Twardość stopu
Jest cechą umożliwiającą jego polerowanie.
Twardość stopów ma związek z granica
plastyczności. Stop o wyraźnej granicy
plastyczności jest twardy i zwykle trudniejszy
do polerowania niż stop o słabiej granicy
plastyczności. Jednostkę twardości stanowi
kg/mm².
Biokompatybilność
Biokompatybilność stopów dentystycznych
wiąże się przede wszystkim z nich podatnością
na korozję. Efektem korozji, w trakcie której
dochodzi do uwalniania elementów stopu,
mogą by niepożądane reakcje tkanek jamy
ustnej, np. nieprzyjemny smak, podrażnienie
czy alergia. Z dużym prawdopodobieństwem
można stwierdzić, że stopy wysoko szlachetne
uwalniają mniej elementów w procesie korozji
ze względu na dużą zawartość pierwiastków
szlachetnych.
Dziękujemy za uwagę
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Stopy metali
- Slide 23
- Roztwory stałe
- Slide 25
- Slide 26
- Slide 27
- Fazy międzymetaliczne
- Slide 29
- Slide 30
- Slide 31
- Mieszaniny faz
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
Wyszukiwarka
Podobne podstrony:
Struktura przestrzeni w instalacji wideo
Struktura przestrzenna transportu w Polsce i perspektywy jego rozwoju
Ontologia, 15. Struktura przestrzeni c.d., Rudolf Carnap - „Struktura przestrzeni”
Ontologia, 14. Struktura przestrzeni, Rudolf Carnap - „Struktura przestrzeni”
Bialka struktury przestrzenne
Struktura przestrzenna gospodarki
Struktura przestrzenna i funkcjonalna zakładów gastronomicznych, PWSZ, Wyposażenie techniczne
Pryzmatyczne struktury przestrzenne
Jak się ustrzec fałszywego stwierdzenia nielosowości struktury przestrzennej drzewostanu
3 Struktura przestrzenna białek
A Zoll Karalnosc i karygodnosc czynu jako odrebne elementy struktury przestepstwa
12 katarzyna prajzner wirtualne spacery struktury przestrzenne w grach komputerowych
Struktura przestrzeni pow i warunki korzystania
Struktura produkcyjna i podstawy jej tworzenia Projektowanie i organizacja struktury przestrzennej
więcej podobnych podstron