Podstawy Chemii Nieorganicznej kod kursu:
CHC012001 l
Sprawozdanie
ROZTWORY BUFOROWE
Nazwisko
Imię i nazwisko:
Nr indeksu:
Ocena
prowadzącego kurs:
Wyznaczanie pojemności buforowej roztworu buforowego (HA/A-;BOH/B+) Stężenia roztworów użytych w doświadczeniu C0CH3OOH = 0,20 mol/dm3 C0CH3OONa = 0,20 mol/dm3 pKa = 4,75
C0HCl = 0,25 mol/dm3 C0NaOH = 0,25 mol/dm3
Objętość roztworów użytych do sporządzenia roztworu buforowego: VCH3COOH = 9,5 cm3 VCH3COONa = 10,5 cm3
1. Pomiar pojemności buforowej w stosunku do HCl Lp
VHCl
nHCl
Vr-r
C
pH
a
Cs
obl
pHpom
[cm3]
[mmol]
[cm3]
[mol/dm3]
[mol/dm3]
1
0
0
20
0,095
0,105
4,79
4,84
2
1
0,25
21
0,102
0,088
4,69
4,66
3
2
0,5
22
0,109
0,072
4,58
4,58
4
3
0,75
23
0,115
0,059
4,46
4,46
5
4
1
24
0,121
0,046
4,33
4,34
6
5
1,25
25
0,126
0,034
4,18
4,20
7
6
1,5
26
0,131
0,023
3,99
4.03
8
7
1,75
27
0,135
0,013
3,73
3,82
9
8
2
28
0,139
0,0036
3,23
3,51
10
9
2,25
29
0,138
0
2,26
2,94
11
10
2,5
30
0,133
0
1,88
2,20
12
11
2,75
31
0,129
0
1,68
1,85
13
12
3
32
0,125
0
1,55
1,66
2. Pomiar pojemności buforowej w stosunku do NaOH
Lp
VNaOH
nNaOH
Vr-r
Ca
Cs
pHobl
pHpom
[cm3]
[mmol]
[cm3]
[mol/dm3]
[mol/dm3]
1
0
0
20
0,095
0,105
4,79
4,84
2
1
0,25
21
0,079
0,112
4,90
4,89
3
2
0,5
22
0,064
0,118
5,02
5,00
4
3
0,75
23
0,05
0,124
5,14
5,12
5
4
1
24
0,038
0,129
5,28
5,26
6
5
1,25
25
0,026
0,134
5,46
5,46
7
6
1,5
26
0,015
0,138
5,71
5,63
7
1,75
27
0,006
0,143
6,13
5,91
9
8
2
28
0
0,143
11,55
6,45
10
9
2,25
29
0
0,138
12,08
12,38
11
10
2,5
30
0
0,133
12,3
12,90
3. Pojemność roztworu buforowego w stosunku do kwasu Δn = cHCl • VHCl = 0,0,25mol/dm3 • 0,00700dm3 = 0,00175 mola ΔpH =4,03 – 4,84 = -0,81
Vbuforu = 20,0cm3 = 0,0200dm3
β = -Δn/(ΔpH•V) = -0,00175mol • 1,0dm3/(-0,81 • 0,0200dm3) = 0,108 = 0,11mola 4. Pojemność roztworu buforowego w stosunku do zasady Δn = cNaOH • VNaOH = 0,25mol/dm3 • 0,00700dm3 = 0,00175mol ΔpH = 5,63 - 4,84 = 0,79
Vbuforu = 20,0cm3 = 0,0200dm3
β = Δn/(ΔpH • V) = 0,00175mol • 1,0dm3/(0,79 • 0,0200dm3) = 0,110759 = 0,11mola 5. Do sprawozdania dołączamy obliczenia oraz wykresy.
6. Wnioski:
Wszystkie wyniki są obarczone błędem, ponieważ trudno jest uzyskać idealną objętość idealnie czystego roztworu, stąd różnice między pH mierzonym a obliczonym. Objętość rzeczywista mogła być niewiele większa lub mniejsza ze względu na niedokładność odmierzenia pipetą. Sam roztwór również mógł być minimalnie zanieczyszczony przez niedomyte szkło laboratoryjne bądź zanieczyszczenia z powietrza.
Jednak mimo tych niedokładności na podstawie doświadczenia mogliśmy się przekonać, że roztwór buforowy rzeczywiście jest „odporny” na dodatek mocnej zasady czy kwasu – jego pH ulega niewielkiej zmianie, ale jedynie do pewnego momentu. Zmiana jest zauważalna kiedy przekroczymy pewną granicę – czyli dodatek kwasu lub zasady zużyje całą sól lub kwas w buforze. Sama pojemność buforowa jest zależna od składników buforu.
WYKRESY
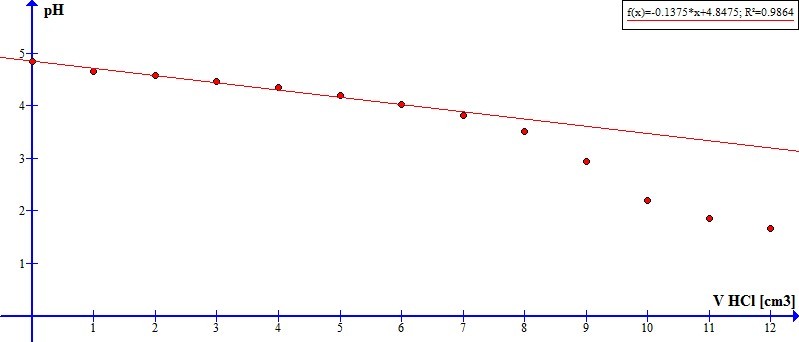
1. Pojemność względem HCl
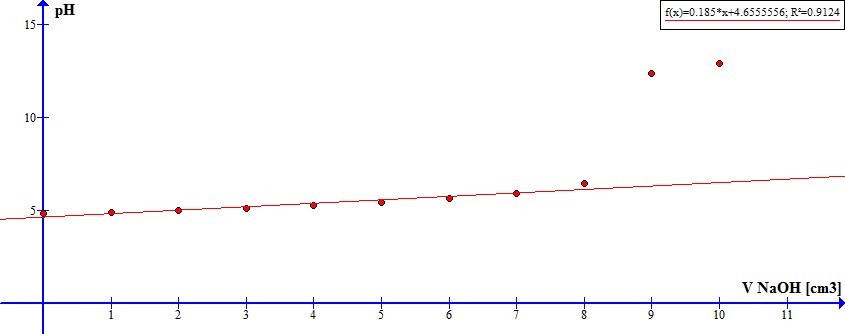
2. Pojemność względem NaOH
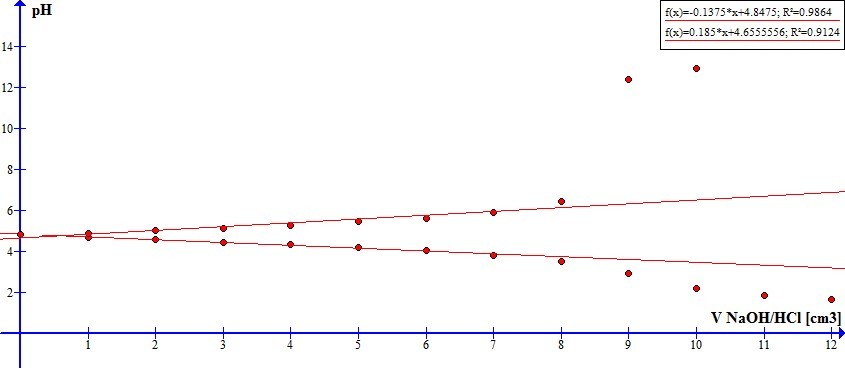
3. Wykresy nałożone na siebie