Sprawozdanie z ćwiczenia z biofizyki |
||||
Temat: Widma absorpcyjne. |
||||
Wykonujący:
|
Wydział Stomatologii Rok I Semestr I |
|||
Prowadzący: dr W. Podraza |
||||
Grupa i podgrupa |
Data wykonania ćwiczenia |
Data oddania sprawozdania |
Ocena |
Podpis |
L2B |
08.11.2006 |
22.11.2006 |
|
|
Wprowadzenie:
1. Widmo absorpcyjne jest to widmo uzyskane po przejściu przez środowisko absorbujące promieniowanie elektromagnetyczne np. światło. Po przejściu światła przez to środowisko jego natężenie maleje na skutek absorpcji, którą można podzielić na :
selektywną
nieselektywną
Podział absorpcji jest wykorzystywany do ilościowego i jakościowego badania substancji.
Doświadczenie przedstawione przez nas nawiązuje do prawa Bouguera- Lamberta. Prawo to określa zależność pomiędzy natężeniem wiązki światła padającej na jednorodną substancję, a grubością tej substancji. Prawo to można zapisać w postaci równania:
I = I e
Lub w postaci logarytmicznej:
E = log(I / I) = kd , gdzie
gęstość optyczna- ekstynkcja
k- współczynnik proporcjonalności
Prawo Bouguera- Lamberta spełnione jest dla wszystkich subsancji.
2. Spektrokolorymetria
Specol jest to jednowiązkowy fotometr spektralny z monochromatorem siatkowym, pracuje w zakresie długości fal od 330 do 850. Zaopatrzony jest we wskaźnik wychyleniowy.
Specol jako przyrząd wieloczynnościowy wykorzystywany jest do pomiarów:
absorpcji
fluorescencji
zmętnienia
remisji
miareczkowania fotometrycznego
fluorymetrycznego
turbidymetrycznego różnych roztworów
Cel ćwiczenia:
Wyznaczenie zależności transmisji i ekstynkcji od długości fali oraz od stężenia roztworu. Znalezienie stężenia badanego roztworu X.
Przebieg ćwiczenia:
I. Wyznaczanie zależności ekstynkcji i transmisji od długości fali.
Przesłonę P ustawić w pozycji 0 (do fotoelementu nie dochodzi światło).
Włączyć zasilacz do sieci. Po włączeniu zasilania odczekać 5 min.
Do jednej kuwety nalać wodę destylowaną, a do drugiej - roztwór wskazany przez prowadzącego ćwiczenia.
Następnie rozpoczynamy badanie całego obszaru widma absorpcji (450770 nm):
a/ ustawiamy bęben B na 450 nm;
b/ w bieg promieni wstawiamy kuwetę z wodą destylowaną;
c/ przy pomocy pokrętła 0 (górne z prawej strony przyrządu) ustawić wskazówkę miernika na przepuszczalność 0%.
d/ przy pomocy pokrętła 100 ustawiamy wskazówkę miernika na 100% transmisji;
e/ w bieg promieni wprowadzamy kuwetę z badanym roztworem - odczytujemy wartość ekstynkcji i transmisji (wyniki zapisujemy w tabeli I);
f/ zmieniamy długość fali światła o 10 nm i powtarzamy czynności b, c, d, e.
Sporządzamy wykresy E= f () i T = f ().
Powtarzamy czynności wymienione w pkt. 4 i 5 dla innego roztworu wskazanego przez prowadzącego ćwiczenia.
II. Wyznaczanie zależności ekstynkcji i transmisji od stężenia roztworu.
Ustawiamy bęben na długość fali, przy której ekstynkcja jest maksymalna.
Wprowadzamy w bieg promieni świetlnych kolejno roztwory o różnych stężeniach i odczytujemy wartości ekstynkcji i transmisji. Wyniki zapisujemy w tabeli II.
Sporządzamy wykresy E= f (c) i T = f (c). ( krzywe kalibracyjne).
Odczytując ekstynkcję roztworu badanego z otrzymanej krzywej kalibracyjnej odczytujemy jego stężenie.
I. Wyznaczanie zależności ekstynkcji i transmisji od długości fali.
Tabela I
DŁUGOŚĆ FALI [nm] |
EKSTYNKCJA E |
TRANSMISJA T |
450 |
0,03 |
90 |
460 |
0,03 |
96 |
470 |
0,03 |
96 |
480 |
0 |
100 |
490 |
0,01 |
99 |
500 |
0,02 |
98 |
510 |
0,02 |
97 |
520 |
0,03 |
95 |
530 |
0,03 |
94 |
540 |
0,04 |
93 |
550 |
0,05 |
91 |
560 |
0,05 |
90 |
570 |
0,07 |
85 |
580 |
0,11 |
78 |
590 |
0,15 |
72 |
600 |
0,17 |
68 |
610 |
0,21 |
62 |
620 |
0,25 |
56 |
630 |
0,35 |
45 |
640 |
0,4 |
40 |
650 |
0,35 |
45 |
660 |
0,24 |
57 |
670 |
0,14 |
72 |
680 |
0,08 |
85 |
690 |
0,04 |
91 |
700 |
0,03 |
95 |
710 |
0,02 |
96 |
720 |
0,15 |
96 |
730 |
0,15 |
97 |
740 |
0,1 |
97 |
750 |
0,1 |
97 |
760 |
0,15 |
97 |
770 |
0,15 |
97 |
Wykres I
E= f(λ)
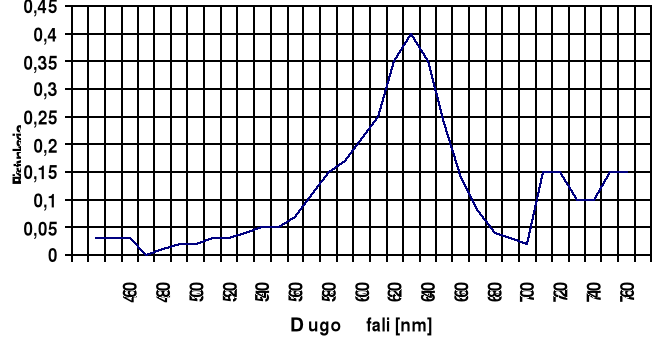
Wykres II
T= f(λ)
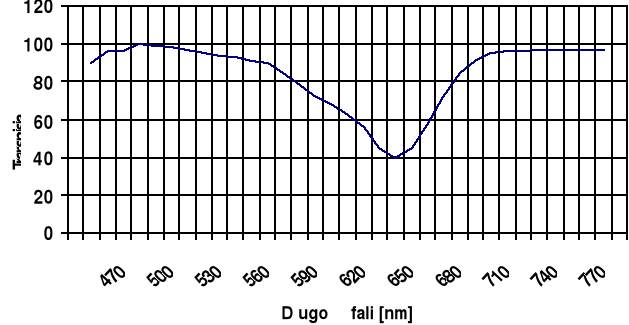
Największą ekstynkcję zanotowaliśmy dla fali o dł.650 nm
Pozostałe obliczenia w tabeli II i na wykresach III i IV zostały sporządzone dla fali 650nm.
II. Wyznaczanie zależności ekstynkcji i transmisji od stężenia roztworu.
Tabela II
STĘŻENIE C [mmol/L] |
EKSTYNKCJA E |
TRANSMISJA T |
X |
0,28 |
52 |
1 |
0,04 |
91 |
2 |
0,09 |
81 |
3 |
0,12 |
76 |
4 |
0,14 |
72 |
5 |
0,21 |
61 |
6 |
0,22 |
60 |
7 |
0,32 |
48 |
8 |
0,32 |
48 |
9 |
0,4 |
40 |
X - roztwór o nieznanym stężeniu
Wykres III
E= f(C)
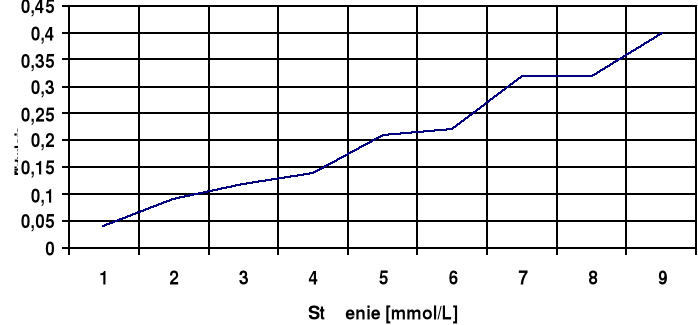
Wykres IV
T= f(C)
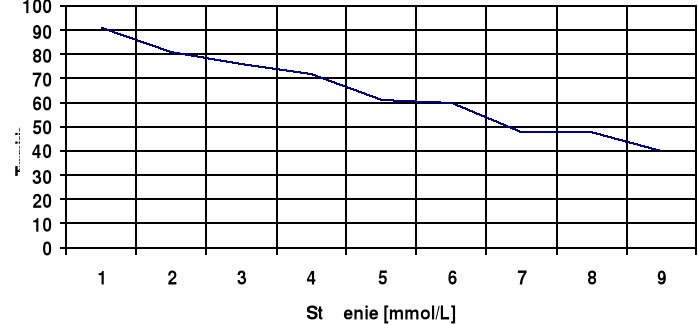
Analiza błędów:
Zaistniałe błędy w dokonywanych pomiarach mogły być spowodowane:
błędami ustawiania i małą częstotliwością sprawdzania miernika w pozycji 0%
nieprawidłowym ustawieniem bębna
błędami popełnionymi przy odczytywaniu uzyskanych wyników
Wnioski:
Stężenie roztworu X zawiera się w przedziale 6-7 mmol/L.
Podczas przeprowadzanego ćwiczenia zauważyłyśmy, że ekstynkcja i transmisja zachowywały się względem siebie odwrotnie proporcjonalnie.
Wyszukiwarka
Podobne podstrony:
sprawozdania-biofizyka, Sprawozdanie z cwiczenia z biofizyki 1[1], Sprawozdanie z ćwiczenia z biofiz
sprawozdania z fizyki, Sprawozdanie - Cwiczenie 2, Sprawozdanie z laboratorium z fizyki i biofizyki
sprawozdania-biofizyka, sprawozdanie 4 - audiometria[1], Sprawozdanie z ćwiczenia z biofizyki
sprawozdania-biofizyka, sprawozdanie 4 - audiometria[1], Sprawozdanie z ćwiczenia z biofizyki
sprawozdania-biofizyka, SPRAWOZDANIE Z ĆWICZENIA Z FIZYKI MEDYCZNEJ, SPRAWOZDANIE Z ĆWICZENIA Z FIZY
sprawka zrobione, Sprawozdanie z ćwiczenia z biofizyki2,2, Sprawozdanie z ćwiczenia z biofizyki
sprawozdania-biofizyka, Sprawozdanie z ćwiczenia z biofizyki, Sprawozdanie z ćwiczenia z biofizyki
sprawozdania z fizyki, Sprawozdanie - Cwiczenie 9, Sprawozdanie z laboratorium z fizyki i biofizyki
sprawozdania-biofizyka, mikroobiekty-lucidakamera2, Sprawozdanie z ćwiczenia z fizyki medycznej
sprawozdania-biofizyka, sprawozdanie mikroskop, Sprawozdanie z ćwiczenia z fizyki medycznej
sprawozdania z fizyki, Sprawozdanie - Cwiczenie 7, Sprawozdanie z laboratorium z fizyki i biofizyki
sprawka zrobione, Sprawozdanie z ćwiczenia z biofizyki2,1, Sprawozdanie z ćwiczenia z biofizyki
sprawozdania z fizyki, Sprawozdanie - Cwiczenie 10, Sprawozdanie z laboratorium z fizyki i biofizyki
sprawka zrobione, do wydrukowania, Sprawozdanie z ćwiczenia z biofizyki
sprawka zrobione, sprawko audiometria do oddania, Sprawozdanie z ćwiczenia z biofizyki
sprawka zrobione, biofizyki prady 11, Sprawozdanie z ćwiczenia z biofizyki
sprawka zrobione, 1sprawozdanie, Sprawozdanie z ćwiczenia z biofizyki
sprawozdania-biofizyka, 1Sprawozdanie z ćwiczenia z fizyki medycznej, Sprawozdanie z ćwiczenia z fiz
więcej podobnych podstron