ZESPOŁY PARKINSONOWSKIE
grupa schorzeń przebiegająca z objawami zespołu hipertoniczno-hipokinetycznego
należą do niej:
choroba Parkinsona (parkinsonizm pierwotny lub idiomatyczny)
objawowe zespoły parkinsonowskie (parkinsonizm wtórny)
mózgowe zespoły zwyrodnieniowe, przebiegające z parkinsonizmem, demencją i/lub innymi objawami towarzyszącymi (parkinsonizm plus)
CHOROBA PARKINSONA
opisana w 1817 roku przez Jamesa Parkinsona jako „drżączka poraźna”
pierwotne schorzenie zwyrodnieniowe ukł pozapiramidowego
zajmuje ukł nigrostrialny (zmniejszone przekaźnictwo dopaminy z istoty czarnej do rec D2 w prążkowiu)
cechy charakterystyczne:
sztywność mięśni (rigor)
spowolnienie ruchowe (hypokinesis)
drżenie spoczynkowe
częstość
1-2/ 1000 (populacja ogólna)
w Polsce w sumie ok. 50 000 osób chorych
najczęstszy wiek zachorowania to 55-60 lat (ale początek może być nawet przed 40rż)
po 70rż liczba zachorowań wzrasta dziesięciokrotnie, z niewielką przewagą wśród mężczyzn
etiopatogeneza
zwyrodnienie neuronów istoty czarnej śródmózgowia z ich zanikiem
drastyczny niedobór dopaminy w całym prążkowiu (stężenie dopaminy zmniejszone o ok. 80%)
hipotezy możliwych czynników etiologicznych:
genetyczne (wczesne zachorowania i występowanie rodzinne) np. mutacja genu kodującego białko α-synukleinę (4q), a także mutacje na chromosomach 2 i 6, lub apoptoza istoty czarnej
stres oksydacyjny- uszkodzenie bł kom przez wolne rodniki i niekontrolowany napływ jonów Ca do neuronów istoty czarnej, co prowadzi do ich obumierania, istotna rola jonów Fe
czynniki toksyczne egzo- i endogenne np. MPTP, powstająca przy produkcji heroiny => wybiórczo uszkadza istotę czarną (wykorzystana do tworzenia zwierzęcego modelu choroby)
wniosek: etiologia wieloczynnikowa ze szczególnym wpływem uwarunkowań genetycznych i wpływu stresu oksydacyjnego na istotę czarną
patomorfologia:
zwyrodnienie neuronów zawierających melaninę w części zbitej istoty czarnej w śródmózgowiu i miejscu sinawym
obecność wewnątrzkomórkowych wtrętów (ciała Lewy'ego) zawierające białko α-synukleinę
szczególne obniżenie ilości dopaminy w: jądrze ogoniastym, skorupie i istocie czarnej
OBJAWY KLINICZNE => stanowią podstawę rozpoznania choroby
drżenie spoczynkowe
częstotliwość 4-8Hz
obejmuje spoczynkowo odsiebne części kończyn górnych (rytmiczne ruchy palców rąk- „kręcenie pigułek” lub liczenie pieniędzy”, występuje też w kończynach dolnych oraz obejmuje brodę i język, nie dotyczy głowy
podczas wykonywania ruchów dowolnych i w wyniku niespodziewanego pobudzenia bodźcami emocjonalnymi lub zmysłowymi drżenie zanika
nasilane przez stres lub jego przewidywanie
w pierwszy okresie choroby często niesymetryczne
różnicowanie:
spoczynkowe- zesp Parkinsonowskie
zamiarowe, kinetyczne- samoistne, SM
„trzepotanie skrzydłami”- ch Wilsona
nieregularne, nierytmiczne, dziwaczne
spowolnienie ruchowe (bradykinezja)
wydłużony czas wykonywania sekwencji ruchowych „jak w zwolnionym filmie”)
trudności z rozpoczęciem ruchu dowolnego, zwłaszcza związanego z przemieszczaniem się
trudności z obracaniem się w łóżku
uogólnione zubożenie ruchowe (hipokinezja), z charakterystyczną maskowatością twarzy (hipomimią) i rzadkim mruganiem powiekami,
nieruchome spojrzenie
niechęć do podejmowania jakiejkolwiek aktywności ruchowej
pisanie powolne, z trudnością i zmniejszaniem wielkości liter (mikrografia)
mowa spowolnione, cicha (hipofonia), monotonna i niewyraźna (nie wymawianie spółgłosek i brak modulacji głosu)
sylwetka ciała pochylona do przodu, ze zgiętymi w stawach łokciowych kończynami górnymi
chód drobnymi kroczkami, bez fizjologicznych współruchów (balansowania) kończynami górnymi
zaburzenie odruchów podstawnych powodujące niemożność znalezienia środka ciężkości- natychmiastowe zatrzymywanie się po potknięciu lub lekkm popchnięciu do przodu (anteropulsja) lub do tyłu (retropulsja)
nagłe, przemijające zablokowanie czynności ruchowych- objaw „przymrożenia” (freezing)
sztywność mięśni (rigor)
podczas wykonywania ruchów biernych kończynami- charakter ciągły, plastyczny (objaw „rury ołowianej”) lub przerywany (objaw „koła zębatego” związany z nakładaniem się drżenia spoczynkowego na pozapiramidową sztywność)

charakterystyczna postawa zgięciowa- głowa i tułów zgięte do przodu a kończyny górne przywiedzione w stawie barkowym i zgięte w stawie łokciowymw ciężkich przypadkach- przykurcze zgięciowe palców
objaw „poduszki powietrznej”- wzmożone napięcie mięśni przykręgosłupowych powodujące pochylenie głowy do przodu (jak gdyby była podparta poduszką) → próba spojrzenia na wprost wymaga skieowania oczu ku górze
zaburzenia autonomiczne
obniżenie ciśnienia tętniczego
zaburzenia rytmu serca
nadmierne wydzielanie gruczołów łojowych i potowych (skóra wygładzona, naoliwiona)
dysuria
zaparcia
zaburzenia potencji
zaburzenia termoregulacji- zła tolerancja zimna
inne:
nadmierne gromadzenie śliny związane z zaburzeniem automatyzmów ruchowych połykania
zaburzenia czuciowe- parestezje, ból
zaburzenia węchu
objawy psychiczne:
spowolnienie myślenia (bradyfrenia)
zaburzenia snu
częste wahania nastroju ze stanami depresyjnymi
u ok. 20% chorych zaburzenia funkcji poznawczych
objawy psychotyczne- u osób w podeszłym wieku, związane gł z nietolerancją leków przeciwparkinsonowskich
diagnostyka
rozpoznanie na podstawie objawów klinicznych (obecność co najmniej 2 objawów osiowych)
w początkowej fazie- objawy jednostronne
brak innych objawów neurologicznych
postępujący przebieg
poprawa kliniczna po preparatach lewodopy (test farmakologiczny potwierdzający)
nie ma żadnych wskaźników biologicznych choroby
przy podejrzeniu chor Parkinsona- konieczne wykonanie CT w celu różnicowania
PET umożliwia wykazanie zmian w metabolizmie dopaminy

ocena przebiegu i leczenia- skala Hoehn i Jahra
I° |
Objawy jednostronne, zwykle z minimalnym zaburzeniem funkcji lub bez |
II° |
Objawy obustronne lub z zajęciem mięśni osiowych, bez zaburzeń postawnych |
III° |
Zaburzenia odruchów podstawnych, wyraźna niestabilność przy wykonywaniu obrotów oraz w wypadku popychania, gdy stoi ze złączonymi stopami i zamkniętymi oczami. Nieznaczne ograniczenie aktywności; możliwość wykonywania niektórych prac w zależności od rodzaju zatrudnienia. Chory zdolny do prowadzenia samodzielnego życia- stopień niepełnosprawności nieznaczny lub umiarkowany |
IV° |
W pełni rozwinięta choroba powodująca ciężką niesprawność, pacjent zdolny do chodzeniai stania bez pomocy, znaczny stopień inwalidztawa |
V° |
Chory leżący lub siedzący w fotelu, wymagający pomocy osób trzecich. |
badania dodatkowe
morfologia, OB., biochemia, bad ogólne moczu
chor tarczycy
odczyny kiłowe
poziom miedzi i ceruloplazminy (< 50rż, w różnicowaniu z chor Wilsona)
przedni odcinek oka w lampie szczelinowej (pierścień Kayera- Fleischera - w chor Wilsona)
bad neuroobrazujące (TK, MRI)
leczenie
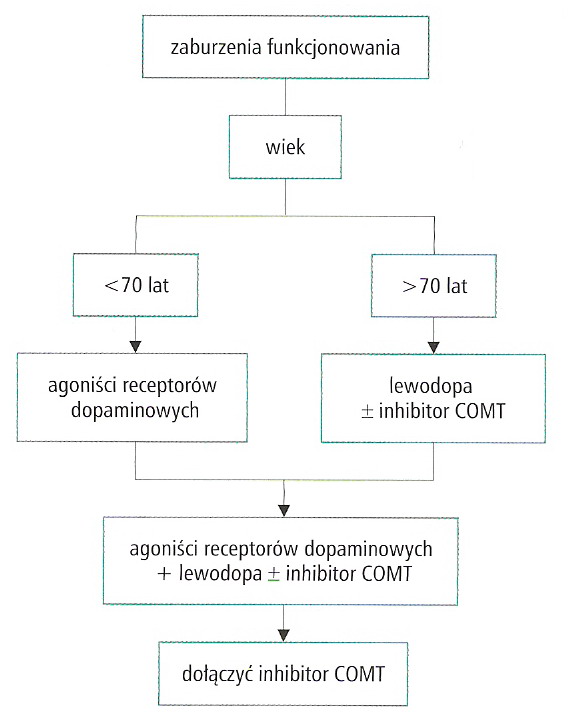
podstawą jest farmakoterapia, wspomagana fizjoterapią i zachowaniem codziennej higieny ruchowej
celem leczenia farmakologicznego jest zapewnienie pacjentom możliwie optymalnej sprawności ruchowej i poprawa komfortu życia przez zmniejszenie sztywności mięśni i drżenia oraz stymulację aktywności kinetycznej
stymulacja aktywności kinetycznej- preparaty o działaniu cholinolitycznym (atropinopodobnym), zwłaszcza w leczeniu drżenia spoczynkowego np. biperyden(Akineton) lub triheksyfenid (Parkopan) => działania niepożądane (zwłaszcza w podeszłym wieku): splątanie, zaburzenia pamięci, omamy, nieostre widzenie, zaparcia
leczenie substytucyjne za pomocą prekursora dopaminy- lewodopy
aby ograniczyć jej rozkład na obwodzie dodaje się inhibitor dekarboksylazy aminokwasów aromatycznych np. benzaseryd (Madopar) i karbidopę (Nakom) => pozwala to na zredukowanie dawki lewodopy i zmniejsza jej skutki niepożądane
zmiany w ukł. receptorowych :
↑ wrażliwości i liczby rec. D2 (wyraz procesów adaptacyjnych) :
jest przyczyną silnego początkowo reagowania na leki dopaminergiczne
↓ wrażliwości i liczby rec D2 :
w trakcie podawania leków dopaminergicznych
mogą być przyczyną silnych krańcowych reakcji na leki dopaminergiczne (zespół on - off) : występowanie reakcji hiperkinetycznych bezposrednio po podaniu leku, nagle ustępujacych po pewnym czasie, przechodzących w stan zahamowania ruchowego
wraz z postępem choroby preparaty lewodopy są coraz mniej skuteczne, a podwyższanie dawki prowadzi do dyskinez (ruchów mimowolnych o charakterze pląsawiczym) i czasem miokloni (zespół szczytu dawki)
skracanie czasu działania leku powoduje gwałtowne nasilenie objawów przed przyjęciem kolejnej dawki, występują stany przymrożenia
pojawiają się fluktuacje ruchowe tzw zespoły włączania i wyłączania (on-off) → nagłe maksymalne wzmaganie się sztywności i/lub drżenia, często z zaburzeniami wegetatywnymi (off), co powoduje unieruchomienie nawet na kilka godzin
decyzję o włączeniu do leczenia lewodopy rozważa się indywidualnie
hamowanie rozkładu dopaminy przez inhibitory monoaminooksydazy (MAO-B) np. selegilina i Oksy- metylo- transferazy katecholowej (COMT) np. tolkapon
stymulacja rec dopaminergicznych za pomocą agonistów dopaminy (bromokryptyna, pergoli, pramipeksol, kabergolina, lizuryd) → często jako pierwsze wprowadzane do leczenia; działania nieporządane: hipotonia ortostatyczna, zaburzenia psychiczne, zwłóknienie pozaotrzewnowe
hamowanie ukł glutaminergicznego przez blokowanie rec NMDA np. amantadyna (jednocześnie zwiększa uwalnianie endogennej dopaminy)
w razie potrzeby leki o działaniu przeciwdepresyjnym np. amitryptylina
w przypadku powikłań psychotycznych- zmniejszenie dawki lewodopy i/lub agonistów dopaminy, neuroleptyki nowej generacji np. klozapina
leczenie operacyjne
zwykle w późniejszym okresie choroby, gdy zawodzi farmakoterapia
gdy dominującym objawem jest drżenie, sztywność mięśni lub hiperkinezy o charakterze pląsawiczym, względnie dystonicznym
szczególnie dobre rezultaty przy objawach jednostronnych
stereotaktyczne zabiegi destrukcyjne, niszczące nadaktywne obszary wzgórza (talamotomia) w przypadku dominującego drżenia lub gałki bladej (pallidotomia) przy dominującej sztywności
stymulacja prądem o wysokiej częstotliwości, za pomocą elektrod wszczepianych do wzgórza lub jądra podwzgórzowego Luysa
przeszczepy istoty czarnej
wszczepianie kom macierzystych (eksperymentalnie)
rehabilitacja, wspomaganie grupowe i edukacja
u pacjentów z chor Parkinsona nie wolno stosować:
neuroleptyków (haloperidol, fenaktil, prometazyna) → można klozapinę
litu
neuroleptyków przeciwwymiotnych (Torecan, Metoclopramid) → można Dranperidol, Cisaprid
metyldopy
rezerpiny
flunaryzyny, cynnaryzyny
powikłania
zapalenia płuc- sztywność mięśni oddechowych powoduje osłabienie odruchu kaszlowego i podatność na zakażenia; zaburzenia połykania- aspiracja treści pokarmowej do dróg oddechowych → zachłystowe zapalenie płuc
zakażenia ukł moczowego- zaleganie moczu
następstwa upadków
PRZEŁOM AKINETYCZNY (ZŁOŚLIWY ZESP NEUROLEPTYCZNY)
pogorszenie stanu chorego zagrażające życiu np. w wyniku nagłego odstawienia leków przeciwparkinsonowskich
należy intensywnie podawać leki p/parkinsonowskie, zastosować hipotermię, nawodnienia, wyrównanie zaburzeń gospodarki elektrolitowej, heparynę i antybiotyki
OBJAWOWE ZESPOŁY PARKINSONOWSKIE
zatrucia
niepożądane działanie leków
zapalenia mózgu
zaburzenia metaboliczne
mózgowe zmiany naczyniowe (miażdżyca)
wodogłowie o prawidłowym ciśnieniu (normotensyjne)
guzy mózgu
urazy
parkinsonizm toksyczny
w następstwie zatrucia ostrego lub przewlekłego
zatrucie tlenkiem węgla
objawy po kilku tygodniach
objawy są obustronne
zatrucie związkami manganu:
przewlekłe
objawy po kilku latach
inne objawy to zaburzenia pamięci, orientacji oraz halucynacje i stany pobudzenia
drżenie zamiarowe
zatrucia: metanolem, talem, litem, dwusiarczkiem węgla, dwutlenkiem siarki, czterochlorkiem węgla, związkami ołowiu, substancjami fosforoorganicznymi i cyjankami
zespół po zatruciu MPTP → uszkodzenie neuronów dopaminergicznych istoty czarnej (przypomina idiomatyczną chorobę Parkinsona)- u osób uczestniczących w produkcji heroiny i narkomanów
parkinsonizm polekowy
powstaje w wyniku blokowania rec dopaminergicznych w prążkowiu przez klasyczne neuroleptyki (fenotiazyny i butyrofenony) → zesp poneuroleptyczny
α- metyldopa
diazoksyd
rezerpina
leki przeciwwymiotne np. metoklopramid
długotrwałe podawanie leków blokujących kanały Ca np. flunaryzyna, cynnaryzyna
dominujące objawy: sztywność i spowolnienie
drżenia pojawiają się w późniejszym okresie
leczenie: odstawienie leków wywołujących zesp Parkinsonowi i podawanie preparatów o działaniu antycholinergicznym
parkinsonizm pozapalny
w przebiegu zapalenia mózgu lub jako jego późne powikłanie
w latach 1919- 1926 podczas pandemi śpiączkowego zapalenia mózgu
obecnie sporadycznie
w ostrym okresie nacieki zapalne, zanik kom istoty czarnej, rzadko ciała Lewy'ego
typowe objawy parkinsonowskie i nasilone zaburzenia wegetatywne
napady przymusowego spozierania, przeważnie ku górze (napady wejrzeniowe), zaburzenia gałkoruchowe
dystonie, tiki, mioklonie
zaburzenia zachowania
duża wrażliwość na preparaty lewodopy
parkinsonizm w zaburzeniach metabolicznych
w niedoczynności przytarczyc, przebiegającej z zaburzeniami gospodarki wapniowo- fosforanowej i wtórnymi zwapnieniami w jądrach podstawy
rzekoma niedoczynność przytarczyc → oporność tkanek na parahormon
encefalopatie wątrobowe
parkinsonizm naczyniopochodny (miażdżycowy)
u osób starszych z nasilonymi objawami miażdżycy naczyń
MRI- drobne ogniska lakunarne (stan zatokowy)
dominują zaburzenia chodu i postawy, z objawami przymrożenia
drżenie spoczynkowe zazwyczaj nie występuje
postępujący przebieg
skuteczność preparatów lewodopy jest niewielka
parkinsonizm w przebiegu wodogłowia normotensyjnego (zesp Hakima)
dominują zaburzenia chodu (chód drobnymi kroczkami, przymrożenia), zaburzenia odruchów postawnych i spowolnienie
rzadko drżenia
w późniejszym okresie nieotrzymanie moczu i otępienie
znaczne poszerzenie ukł komorowego (np. w TK)
poprawę kliniczną wywołuje upust pmr
leczenie: wszczepienie dokomorowego ukł zastawkowego
parkinsonizm w przebiegu guza mózgu
w śródczaszkowych procesach rozrostowych przebiegających z efektem masy → bezpośrednie lub pośrednie poszerzenie ukł pozapiramidowego
w gliomatozie mózgu, torbieli śródmózgowia, dużych tętniakach śródczaszkowych i krwiaku podtwardówkowym
parkinsonizm pourazowy
najczęściej wielokrotne urazy głowy z towarzyszącym wstrząśnieniem mózgu np. u bokserów
zwykle z towarzyszącym otępieniem
parkinsonizm po porażeniu prądem elektrycznym
PARKINSONIZM PLUS
zanik wieloukładowy (MSA- multiple system atrophy)
postępujące porażenie nadjądrowe (chor Steela- Richardsona- Olszewskiego) PSP (progressive supranuclear palsy)
zwyrodnienie korowo- podstawne (corticobasal ganglionie degeneration)
otępienie z ciałami Lewy'ego
chor Wilsona (tylko wg seminarium, nie ma w żadnej książce)
mózgowe procesy zwyrodnieniowe, w których obok zespołu parkinsonowskiego występują inne objawy: otępienie, zaburzenia ukł autonomicznego, dystonia, dysartria lub objawy piramidowe
brak lub bardzo słaba reakcja na preparaty lewodopy i agonistów rec dopaminergicznego
zanik wieloukładowy (MSA)
oporny na lewodopę zesp parkinsonowski (zwyrodnienie prążkowoiowo- czarne)
objawy móżdżkowe (zanik oliwkowo- mostowo- móżdżkowy)
zaburzenia autonomiczne (dominują w zesp Shya- Dragera)
4/ 10000
patomorfologicznie: w oligodendrocytach i kom nerwowych - wtręty srebrochłonne zawierające ubikwitynę i białko tau
w przypadku dominacji zesp parkinsonowskiego- głównie zaburzenia odruchów postawnych z towarzyszącymi upadkami, bez drżeń
w dominujących objawach móżdżkowych- ataksja, drżenie kinetyczne, dysmetria
zesp Shya- Dragera: objawy dysautonomii (hipotonia ortostatyczna, dysfagia, zaburzenia w oddawaniu moczu i stolca (zaparcia) i impotencja)
czasem objawy piramidowe i otępienie podkorowe
leczenie
próby stosowania lewodopy, agonistów rec dopaminergicznego i amantadyny
przy nasilonych objawach hipotonii z omdleniami- zwiększona podaż płynów i soli, sympatykomimetyki (midodryna) i steroidy (fludrokortyzon)
postępujące porażenie nadjądrowe (PSP)
przewlekłe, szybko postępujące schorzenie zwyrodnieniowe mózgu
patomorfologicznie: zanik grzbietowej części śródmózgowiamostu i przedniej części płatów skroniowych (gałki bladej i jądra podwzgórzowego oraz odbarwienie istoty czarnej)
poszerzenie wodociągu i III i IV komory
klinicznie dominuje zesp hipertoniczno- hipokinetyczny, ze szczególnym nasileniem sztywności pozapiramidowej w mięśniach osiowych, hiperekstensją tułowia, zaburzeniami odruchów postawnych i częstymi upadkami
drżenia rzadko
zaburzenia gałkoruchowe (ograniczenie ruchów pionowych gałek ocznych, szczególnie ku dołowi) → upośledzona fiksacja wzroku
kurcz powiek i niemożność dowolnego otwierania i zamykania oczu (forma apraksji)
zaburzenia poznawcze o charakterze otępienia podkorowego
objawy zespołu rzekomoopuszkowego, z napadowym śmiechem i płaczem; dyzartria i dysfagia
PET- zmniejszony wychwyt w jądrze ogoniastym i skrupie
lewodopa szybko traci skuteczność
leki przeciwdepresyjne
zwyrodnienie korowo- podstawne(CBD)
tauopatia, w której dochodzi do tworzenia złogów białka MAP-τ w OUN, gł w korze tylnej okolicy czołowej, bruzdy środkowej mózgu i jądra kresomózgowia
kilkaset przypadków
klinicznie- asymetryczny zespół pozapiramidowy, ze sztywnością mięśni
korowe zaburzenia czucia
zespół „obcej ręki” (ALP)
objawy uszkodzenia drogi piramidowej
rzadziej zaburzenia gałkoruchowe (trudności z zapoczątkowaniem ruchów dowolnych), móżdżkowe oraz choreaotetoza i kurcz powiek
zachowany oczopląs optokinetyczny
odpowiednie ustawienie głowy ułatwia poruszanie gałkami → tzw synergia oczno- głowowa
zaburzenia funkcji poznawczych o typie otępienia skroniowo- czołowego
w początkowej fazie- korowe objawy z płata skroniowego (apraksja konstrukcyjna, dyskalkulia i zaburzenia przestrzenne)TK i MRI- asymetryczny zanik płata ciemieniowego i skroniowego
PET- przeciwstronne do ogniska spowolnienie metabolizmu w okolicy czołowo- ciemieniowej, jądrach podstawy i przyśrodkowej części kory płata skroniowgo
brak leczenia farmakologicznego
otępienie z ciałami Lewy'ego (DLBD- diffuse Lewy body disease)
częściej u mężczyzn
ciała Lewy'ego w korze płata skroniowego, ciemieniowego i ukł limbicznego
płytki starcze i zwyrodnienie neurofibrylarne (jak w chor Alzheimera)
klinicznie- zaburzenia funkcji poznawczych o zmiennym nasileniu, z okresami splątania, halucynacjami wzrokowymi i urojeniami
zespół parkinsonowski z częstymi upadkami
patologiczna reakcja na klasyczne neuroleptyki
leczenie: inhibitory cholinesterazy i lewodopa oraz neuroleptyki nowej generacji np. olenzapina
zwyrodnienie wątrobowo- soczewkowe (chor Wilsona)
AR, występuje w wieku 10-25 lat
zaburzenia przemiany białkowej i miedzi, ↓ ceruloplazminy
odkładanie Cu w tkankach np. wątrobie (marskość) i mózgu (jądro soczewkowate)
sztywność i drżenie (przypomina „trzepotanie skrzydłami”)
hiperkinezy, dyzartria
zaburzenia psychiczne
zielonkawobrunatny rąbek na obwodzie rogówki (pierścień Kaysera- Fleischera)
leczenie: D-penicylamina i siarczan cynku
Wyszukiwarka
Podobne podstrony:
Parkinsonizm - drżączka poraźna, Parkinsonizm - dr˙˙czka pora˙na - jest to zesp˙˙ chorobowy charakte
CHOROBA PARKINSONA 4
Reh amb w ch Parkinsona
Choroba Parkinsona
Liczby zesp razem
parking
Choroba Parkinsona jest to choroba postępująca, Fizjoterapia
6 Choroba Parkinsona
K zesp belka cz 2
Parkinson Prawo parkinsona
Leczenie farmakologiczne choroby Parkinsona
Parkingi podziemne o ścianach konstrukcyjnych wykonanych z grodzic(1)
CHOROBA PARKINSONA, Notatki Studia Fizjoterapia
Parking samochodowy. Klasyfikowanie, scenariusze zajęć - matematyka
funkcje zesp wykl
więcej podobnych podstron