Napisz wynik reakcji Michaela dla poniższego przykładu. Nazwij substraty.
Na przykładzie acetonu zapisz mechanizm reakcji kondensacji aldolowej.
Czym różnią się aldozy od ketoz? Zapisz wzorami po jednym przykładzie i podaj sposób ich rozróżniania na drodze chemicznej.
Przykład aldozy Przykład ketozy
(glukoza- aldoheksoza) (fruktoza-ketoheksoza)
Różnica między aldozą a ketozą
Występuje różnica w charakterze grupy karbonylowej: aldozy posiadają grupę aldehydową, a ketozy ketonową.
Rozróżnienie na drodze chemicznej
Reakcją pozwalającą odróżnić aldozy od ketoz jest reakcja z buforowanym wodnym roztworem Br2. Reakcja ta jest specyficzna dla aldoz (utleniają się do kwasu aldonowego), a ketozy nie ulegają utlenieniu przez wodny roztwór Br2
Reakcja z Br2 na przykładzie glukozy, która utlenia się do kwasu D-glukarowego:
Dla D-glukozy napisz reakcje tworzenia form cyklicznych i zaznacz pozycję anomeryczną.
Napisz reakcję zmydlania dowolnego tluszczu.
Co to są mydła? Jak się je otrzymuje i na czym polegają właściwości piorące (myjące) mydła?
Co oznacza określenie kwas tluszczowy omega-3 ?
W kwasie tłuszczowym ostatni atom węgla w łańcuchu jest oznaczany symbolem omega. Omega 3 oznacza, że pierwsze wiązanie podwójne znajduje się przy 3 atomie węgla licząc od atomu omega.
Jakie związki zaliczamy do lipidów, napisz odpowiednie wzory.
Lipidami nazywamy naturalne organiczne cząsteczki o nieznacznej rozpuszczalności w wodzie, izolowane z komórek lub tkanek przez ekstrakcję niepolarnymi rozpuszczalnikami organicznymi takimi jak np. eter czy chloroform. Przykładami lipidów są: tłuszcze, oleje, woski, prostaglandyny, steroidy, terpenoidy, wiele spośród witamin i hormonów oraz większość niebiałkowych składników błon komórkowych.
tłuszcz zwierzęcy- triester
(R, R', R''= łańcuchy C11-C19)
Jaka ważna cecha odróżnia węglowodany od lipidów.
Węglowodany, tak jak lipidy, to organiczne związki chemiczne składające się z atomów węgla, wodoru i tlenu. Są to związki zawierające jednocześnie liczne grupy hydroksylowe, karbonylowe oraz czasami mostki półacetalowe. Węglowodany możemy podzielić na: cukry proste (monosacharydy), oligosacharydy, wielocukry (polisacharydy) Najpowszechniejszym przykładem węglowodanów jest glukoza:
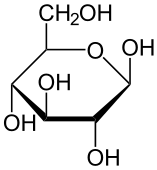
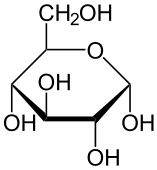
Ze względu na obecność licznych grup -OH węglowodany bardzo dobrze rozpuszczają się w wodzie - w przeciwieństwie do lipidów.
Lipidami nazywamy naturalnie występujące organiczne cząsteczki o nieznacznej rozpuszczalności w wodzie, izolowane z komórek i tkanek przez ekstrakcję niepolarnymi rozpuszczalnikami organicznymi. Przykładami lipidów są tłuszcze, oleje, woski, wiele witamin i hormonów. Zbudowane są z atomów węgla, wodoru, tlenu oraz innych pierwiastków, np. azotu czy fosforu. Są to związki składające się z alkoholi zestryfikowanych z resztami kwasów tłuszczowych lub kwasów tłuszczowych wraz z innymi związkami chemicznymi. Ze względu na budowę nie rozpuszczają się w wodzie, natomiast dobrze rozpuszczają się w rozpuszczalnikach niepolarnych.
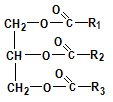
Tłuszcze możemy podzielić na: roślinne i zwierzęce lub nasycone i nienasycone lub stałe i ciekłe.
Ogólny wzór tłuszczu:
Podaj podział terpenów. Jaka reguła ma tu zastosowanie?
Terpeny klasyfikuje się zależnie od liczby jednostek izoprenowych, które zawierają. Tak więc monoterpeny to 10-węglowe substancje biosyntezowane z dwóch jednostek izoprenowych, seskwiterpeny są to 15-węglowe cząsteczki powstałe z trzech jednostek izoprenowych itd.
Liczba atomów węgla |
Liczba jednostek izoprenowych |
Klasyfikacja |
10 |
2 |
monoterpen |
15 |
3 |
seskwiterpen |
20 |
4 |
diterpen |
25 |
5 |
sesterterpen |
30 |
6 |
triterpen |
40 |
8 |
tetraterpen |
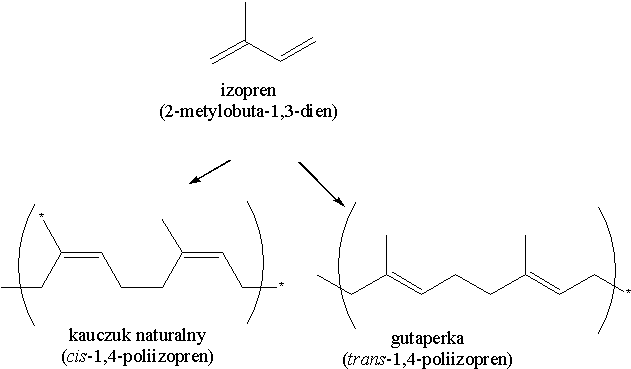
Ma tu zastosowanie reguła izoprenowa. Zgodnie z tą regułą terpeny mogą być rozpatrywane jako produkty kolejnego łączenia według mechanizmu „głowa do ogona” jednostek izoprenowych (2-metylobuta-1,3-dienowych). Atom węgla C1 nazywamy „głową” jednostki izoprenowej, a atom węgla C4 jest „ogonem”.
Co oznacza pojęcie mutarotacja?
Mutarotacja- polega na zmianie wartości liczbowej kąta skręcania płaszczyzny światła spolaryzowanegoprzechodzącego przez roztwory substancji ulegających epimeryzacji. W przypadku sacharydów spowodowana jest stopniowym przechodzeniem anomeru α w β. Jest wynikiem tautomerycznych równowag, ustalających się w roztworach cukrów (np. w stanie równowagi roztwór wodny D-glukozy zawiera 35,5% formy α i 64,5% formy β). (Przewaga formy β-D-glukozy wynika stąd, że odmiana ta jest korzystniejsza energetycznie, gdyż w konformacji krzesłowej wszystkie podstawniki są w pozycjach ekwatorialnych). Mutarotacja jest zjawiskiem, występującym u większości sacharydów (nie występuje np. w roztworze sacharozy, gdyż w tym disacharydzie oba anomeryczne atomy węgla są zablokowane wiązaniem O-glikozydowym). Jest charakterystyczna dla cukrów redukujących.
Mutarotacja przebiega przez odwracalne otwarcie pierścienia każdego z anomerów do otwartołańcuchowego aldehydu, a następnie zachodzi ponowne zamknięcie pierścienia.
Wyjaśnij, dlaczego pirydyna jest mocniejszą zasadą niż pirol?
Pirydyna pirol
Pirol jak i pirydyna mają wolną parę na atomie azotu . W pirolu wolna para jest wykorzystana do stworzenia układu aromatycznego , pirydyna ma układ aromatyczny więc para na azocie zostaje nie wykorzystana i to ona świadczy o większej zasadowości pirydyny nad pirolem.
Napisz wzór guaniny oraz tyminy.
Napisz wzór pirymidyny i puryny oraz zaznacz pozycje zasadowe w tych związkach. Napisz wzory co najmniej 2 zasad wchodzących w skład nukleotydów.
Napisz wzory i nazwij związki heterocykliczne zawierające azot i/lub tlen o 3, 5 i 6 atomach w pierścieniu.
Jakim elementem struktury różnią się rybonukleotydy od deoksyrybonukleotydów?
Różnią się one jedną zasadą (tymina - uracyl). Jak także obecnością grupy hydroksylowej w przypadku cukru w rybonukleotydzie.
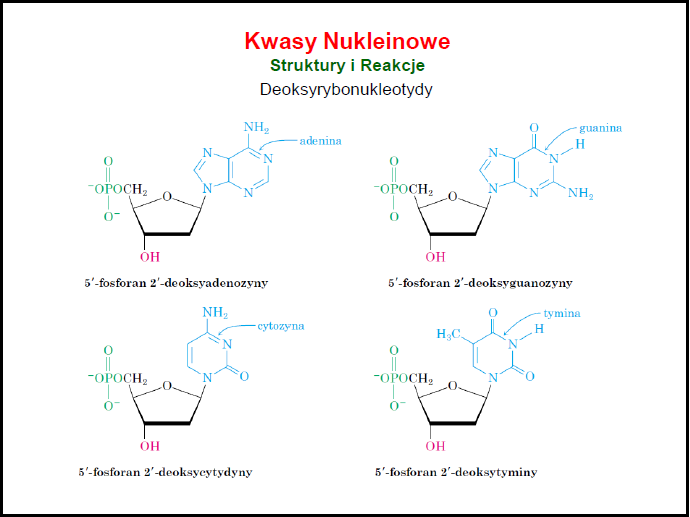
Napisz wzory odpowiednich rybonukleotydów zawierających adeninę oraz uracyl.
Na dowolnych przykładach napisz co najmniej 3 reakcje (różne metody) otrzymywania aminokwasów.
Synteza Streckera
Reakcja Hela- Wolharda- Zielińskiego
Synteza przez acetamidomalonian etylu
Redukcyjne aminowanie α-oksokwasów
Co to jest punkt izoelektryczny aminokwasu? Definicja.
W roztworze kwasowym, czyli przy niskim pH, cząsteczka aminokwasu jest protonowana i występuje głównie jako kation. W roztworze zasadowym, przy wysokim pH, aminokwas traci proton i występuje głównie jako anion. Pośrednie pH, przy którym istnieje dokładna równowaga między formą kationową i anionową aminokwasu i występuje on jedynie jako obojętny, dipolowy jon obojnaczy nazywamy punktem izoelektrycznym, pI, aminokwasu.
Na czym polega proces elektroforezy?
Elektroforeza to metoda separacji makrocząsteczek. Pod wpływem przyłożonego napięcia cząsteczki te, obdarzone ładunkiem elektrycznym, wędrują w polu elektrycznym. Prędkość przemieszczania zależy od ładunku makrocząsteczki, jej rozmiaru, kształtu, a także oporów ruchu środowiska. Technika ta jest najczęściej stosowana do rozdzielenia DNA i jego analizy w żelu, a także do rozdzielania RNA czy białek.
Wyróżnia się dwa rodzaje żeli:
żele agarozowe i żele poliakrylamidowe
Aparaty do elektroforezy:
aparat i żel poziomy - żel umieszcza się poziomo; nalewamy do zbiornika odpowiedni bufor i przykładamy napięcie - to wywołuje migrację DNA (ma ładunek ujemny) od elektrody ujemnej (katody) do elektrody dodatniej (anody);
aparat pionowy - stosuje się go głównie do rozdziału w żelach poliakrylamidowych; żel umieszcza się pionowo; od góry i od dołu żelu są zbiorniki z buforem; kierunek migracji jest od elektrody ujemnej do elektrody dodatniej.
Rozdział elektroforetyczny zależy od kilku czynników:
konformacji DNA;
wielkości DNA - im większe, tym wolniej migruje w żelu;
stężenia agarozy;
przyłożonego napięcia;
rodzaju buforu.
Przed nałożeniem próby DNA w żel podbarwiamy próbę barwnikiem śledzących, np. błękit bromofenolowy, który wędruje w tym samym kierunku co DNA, z prędkością taką jak około 1.000 par zasad. Do barwnika śledzącego dodaje się tak zwany roztwór obciążający. Najczęściej jest to stężony roztwór mocznika lub sacharozy albo fikol 400. Czynnik obciążający powoduje, że próbka opada na dno studzienki (kanału), wypychając z niej bufor na zewnątrz.
Wyniki rozdziału elektroforetycznego obserwuje się po wybarwieniu DNA bromkiem etydyny i wizualizacji w świetle UV przy długości fali α = 260 nm (maksimum absorpcji dla DNA). Żel można sfotografować przy zastosowaniu odpowiedniego filtra.
Rys. Schemat przebiegu procesu elektroforezy (źródło: wikipedia.pl, domena publiczna).
Żel agarozowy z uformowanymi w nim trzema studzienkami (S) na próbki.
Wstrzyknięcie markera DNA (wzorzec masowy) do pierwszej studzienki.
Wprowadzenie badanych próbek do drugiej i trzeciej studzienki.
Przyłożenie napięcia. DNA porusza się w kierunku anody ze względu na posiadany ładunek ujemny.
Małe fragmenty DNA poruszają się szybko przez żel, duże fragmenty DNA - powoli. Normalnie DNA nie jest widoczny w trakcie tego procesu, dlatego do próbki DNA dodawany jest barwnik.
Podaj definicje reakcji pericyklicznych oraz wyjaśnij znaczenie następujących oznaczeń [2+2], [2+4], itp.
Reakcje pericykliczne są to reakcje w których tworzenie nowych wiazan i zrywanie starych zachodzi równocześnie w cyklicznym stanie przejściowym, podczas reakcji nie tworzą się produkty pośrednie. Oznaczenia te charakteryzuja reakcje cykloaddycji- reakcje międzycząsteczkowe, w których 2 cząsteczki ulegają addycji , tworząc cykliczny produkt. Cyfry w nawiasie oznaczaja ilość elektronów pi biorących udział w reakcji. 2+2 pomiędzy dwoma alkenami(produktem jest cyklobutan lub pochodne), 4+2 dien + dienofil-r. Dielsa-Aldera(produktem jest cykloheksen lub pochodne).Opisz krótko (ilustrując dowolnymi równaniami reakcji) następujące procesy:
a) cykloaddycja [4+2] Dielsa-Aldera
b) przegrupowanie [3,3] Claisena
α-D-glukopiranoza β-D-glukopiranoza
C3
C4
„ogon”
C2
C1
„głowa”
Wyszukiwarka
Podobne podstrony:
Projekt z mechaniki część druga
Terenia, joanna2, CZĘŚĆ DRUGA
Słownik łaciński część druga
Kazusy czyny niedozwolone część druga, Prawo cywilne
czesc druga, AGH WIMIIP Metalurgia, semestr 2, nauka o materiałach
02 Część druga
Terpeny część druga
Część druga rocznika 2004, Politologia - materiały na zajęcia, Stosunki międzynarodowe
NIEOMYLNOŚĆ Kościoła Katolickiego część druga
pytania grupa A cześć druga, Studia Pwr, Semestr 1, Zintegrowane systeymy informatyczne - wykład
Temat Podatność związków organicznych na biodegradację część druga
część druga
METODY NUMERYCZNE CZESC DRUGA
pytania grupa B cześć druga, Studia Pwr, Semestr 1, Zintegrowane systeymy informatyczne - wykład
buddyjska tradycja gelug czesc druga i ostatnia eioba
Część druga z worda
Zadania 14 część druga
więcej podobnych podstron