Jacek Olender I rok KiR
ĆWICZENIE I - SPRAWOZDANIE
Część teoretyczna
Roztwór – nierozdzielająca się w długich okresach czasu mieszanina dwóch lub więcej związków chemicznych. Skład roztworów określa się przez podanie stężenia składników. W roztworach zwykle jeden ze związków chemicznych jest nazywany rozpuszczalnikiem, a drugi substancją rozpuszczaną. Rozpuszczalnikiem nazywa się substancję występującą w roztworze w największej ilości lub substancje określającą stan skupienia roztworu.
Podział roztworów:
Ze względu na doskonałość - roztwory dzieli się często na tzw. właściwe i niewłaściwe.
Roztwory właściwe są całkowicie jednorodne tzn. że dla objętości kilkakrotnie większych od wielkości cząsteczek, każda porcja zawiera taki sam skład ilościowy cząsteczek.
Roztwory niewłaściwe nie są całkowicie jednorodne. Są to np. trwałe emulsje, skrajnie rozproszone zawiesiny, zole i żele.
Ze względu na stopień nasycenia:
Roztwór nienasycony – to roztwór, w którym w danej temperaturze można rozpuścić jeszcze pewną ilość danej substancji.
Roztwór nasycony – to roztwór, który w określonych warunkach termodynamicznych (ciśnienie, temperatura) nie zmienia swego stężenia w kontakcie z substancją rozpuszczoną. W praktyce oznacza to, że bez zmian warunków termodynamicznych z roztworu nasyconego nie wypada żaden osad, ale nie można też w nim rozpuścić już więcej substancji.
Roztwór przesycony – to roztwór o stężeniu większym od stężenia roztworu nasyconego w danej temperaturze. Roztwory przesycone są przykładami substancji w stanie termodynamicznym niestabilnym metatrwałym.
Ze względu na stan skupienia:
Gazowy (mieszanina dwóch gazów)
Ciekły (ciecz w cieczy lub ciało stałe w cieczy)
Stały (kryształy mieszane – powstają podczas krystalizacji)
Ze względu na sposób oddziaływania cząsteczek związku rozpuszczanego i rozpuszczalnika:
Homodynamiczne – między cząsteczkami występują oddziaływania jednego rodzaju
Heterodynamiczne – między cząsteczkami występują oddziaływania różnego rodzaju
Rozpuszczalność – stężenie nasyconego roztworu substancji – maksymalna ilość substancji, która rozpuszcza się w określonej ilości rozpuszczalnika. Zależy od warunków fizycznych (np. temperatura rozpuszczalnika)
Stężenie – ilość substancji rozpuszczonej przypadająca na określona ilość roztworu lub rozpuszczalnika.
Stężenie molowe – liczba moli substancji rozpuszczonej w 1
dm3. Wzór:
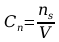 (jednostka [mol/dm3])
(jednostka [mol/dm3])
Mol (gramocząsteczka)-chemiczna jednostka ilości substancji; Jest to liczba cząsteczek równa liczbie atomów w 12g izotopu węgla 12C; (jest to liczba gramów substancji równa liczbowo masie cząsteczkowej). Mol każdej substancji zawiera jednakową liczbę cząsteczek: 6,023 * 1023 ( liczba Avogadra)
Stężenie procentowe- masa substancji rozpuszczonej w 100g
roztworu. Wzór:
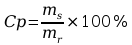 ,
gdzie
,
gdzie
Cp
- stężenie procentowe
ms
- masa substancji rozpuszczonej
mr
- masa roztworu
Można obliczać stężenie molowe z procentowego za pomocą wzoru:
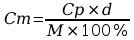
Natomiast odwrotnie za pomocą wzoru:
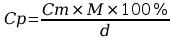 ,
gdzie:
,
gdzie:
Cm – stężenie molowe
Cp – stężenie procentowe
M – masa molowa
d – gęstość roztworu.
Wyszukiwarka
Podobne podstrony:
Lab 6 PMI Hartownosc Sprawozdan Nieznany
Mikrokontrolery Grodzki Sprawoz Nieznany
ProjektUnifikacja sprawozdanie Nieznany
Projekt zaliczeniowy Sprawozdan Nieznany
problematyka sprawozdawczosci M Nieznany
ProbabilistykaEND SprawozdanieA Nieznany
Sprawozdania Sprawozdanie1prakt Nieznany
Sprawozdania Sprawozdanie2teori Nieznany
konserwanty wzor sprawozdania v Nieznany
Elektroenergetyka sprawozdanie Nieznany
2012 03 KPP Mikolow sprawozdani Nieznany (2)
Sprawozdania Sprawozdanie5teori Nieznany
Sprawozdania Sprawozdanie3prakt Nieznany
PFM 3 Instrukcje pisania sprawo Nieznany
Mikrokontrolery Grodzki Sprawoz Nieznany (2)
ETD3070L01 Przykladowe sprawozd Nieznany
destylacja z para wodna sprawoz Nieznany
Sprawozdania Sprawozdanie3teori Nieznany
Sprawozdania Sprawozdanie4teori Nieznany
Sprawozdania Sprawozdanie6teori Nieznany