Zakład Chemii Fizycznej
Laboratorium Studenckie
ĆWICZENIE 12
TEMAT:RÓWNOWAGA FAZOWA CIECZ-CIECZ W UKŁADZIE TRÓJSKŁADNIKOWYM.
SPORZĄDZIŁY:
Tomasz Dziadosz
Łukasz Daniel
-->WYPOSAŻENIE: [Author ID1: at Wed Mar 10 18:40:00 1999 ]
-10 kolb stożkowych
-biurety
-termometr
-->ODCZYNNIKI: [Author ID1: at Wed Mar 10 18:40:00 1999 ]
-woda destylowana
-chloroform
-kwas octowy
Reguła faz przewiduje, że w układach trójskładnikowych suma liczby stopni swobody i liczby faz jest równa 5.
W układzie jednofazowym zmieniać się mogą niezależnie temperatura, ciśnienie i stężenia dwóch składników. Ułamek molowy lub wagowy trzeciego jest automatycznie ustalony. Ponieważ relacji między czterema zmiennymi nie daje się przedstawić graficznie, trzeba wprowadzić jakieś uproszczenia. Zazwyczaj przyjmuje się, że ciśnienie jest ustalone i wynosi 0,1Mpa. W ten sposób liczba stopni swobody zmniejsza się do trzech. Pozostałe 3 zmienne przedstawia się na wykresie trójwymiarowym, którego podstawą jest trójkąt równoboczny. Zmienne wyrażające skład odkłada się na osiach trójkąta, a temperaturę na osi pionowej. Otrzymuje się w ten sposób wykres przestrzenny w postaci prostopadłościanu, przekrój poziomy którego przedstawia układ trójskładnikowy w stałej temperaturze i pod stałym ciśnieniem.
-->CEL ĆWICZENIA.[Author ID1: at Wed Mar 10 18:40:00 1999 ]-->[Author ID1: at Wed Mar 10 18:40:00 1999 ]
W układzie trójskładnikowym chloroform - kwas octowy-woda obserwuje się zakres ograniczonej rozpuszczalności. Celem ćwiczenia jest określenie zakresu stężeń, w którym to zjawisko występuje, czyli wyznaczenie izotermy rozpuszczalności oraz cięciwy równowagi .
Wzajemna rozpuszczalność dwóch częściowo nie mieszających się cieczy ulega znacznym zmianom pod wpływem dodania trzeciego składnika. Jeżeli ten trzeci składnik jest rozpuszczalny tylko w jednej z dwóch cieczy to wzajemna rozpuszczalność maleje. Dodanie zaś składnika dobrze rozpuszczającego się w obu cieczach zwiększa ich wzajemną rozpuszczalność. Zjawiska te są doskonale ilustrowane w układzie CHCl3-CH3COOH-H2O. Gdy dodamy w określonej temperaturze CH3COOH do mieszaniny z CHCl3 to wzrasta wzajemna rozpuszczalność wody i CHCl3 przy określonej ilości CH3COOH mieszanina staje się jednorodna.
OPRACOWANIE WYNIKÓW POMIARÓW:
Nr pom. |
objętość w ml |
% wag. w roztworze |
% mol. w roztworze |
||||||
|
H2O |
CH3COOH |
CHCl3 |
H2O |
CH3COOH |
CHCl3 |
H2O |
CH3COOH |
CHCl3 |
1 |
0,2 |
5 |
30 |
0,004 |
0,105 |
0,891 |
0,0235 |
0,185 |
0,792 |
2 |
0,45 |
7 |
20 |
0,012 |
0,195 |
0,793 |
0,0629 |
0,308 |
0,629 |
3 |
1 |
8 |
14 |
0,033 |
0,278 |
0,689 |
0,15 |
0,378 |
0,427 |
4 |
3,1 |
11 |
10 |
0,105 |
0,391 |
0,504 |
0,352 |
0,393 |
0,255 |
5 |
3,4 |
14 |
10 |
0,103 |
0,445 |
0,452 |
0,338 |
0,438 |
0,224 |
6 |
5 |
12,5 |
6 |
0,185 |
0,485 |
0,330 |
0,486 |
0,383 |
0,131 |
7 |
6,85 |
13 |
4 |
0,259 |
0,516 |
0,225 |
0,578 |
0,346 |
0,076 |
8 |
11,7 |
14 |
2 |
0,398 |
0,5 |
0,101 |
0,706 |
0,266 |
0,027 |
9 |
16,9 |
14 |
1,5 |
0,499 |
0,434 |
0,066 |
0,780 |
0,204 |
0,016 |
10 |
33,5 |
14 |
1 |
0,674 |
0,296 |
0,03 |
0,878 |
0,116 |
0,006 |
1.Obliczanie % wagowego w roztworze pierwszym. Pozostałe obliczenia wykonano w taki sam sposób:
% wagA=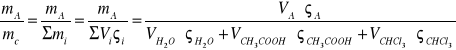
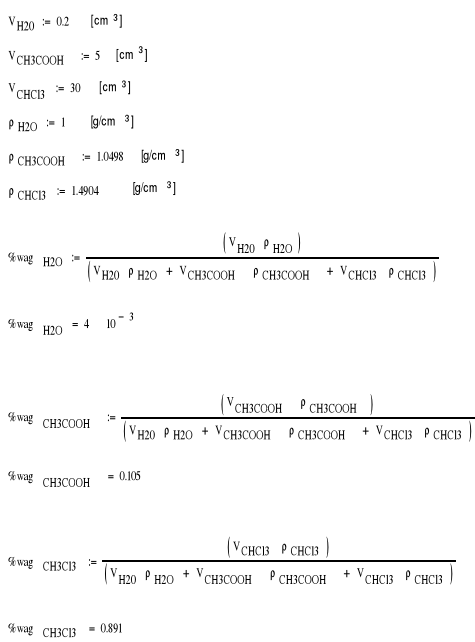
2.Obliczanie % molowego w roztworze pierwszym. Pozostałe obliczenia wykonano w taki sam sposób:
% molA = 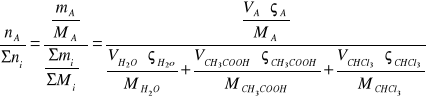
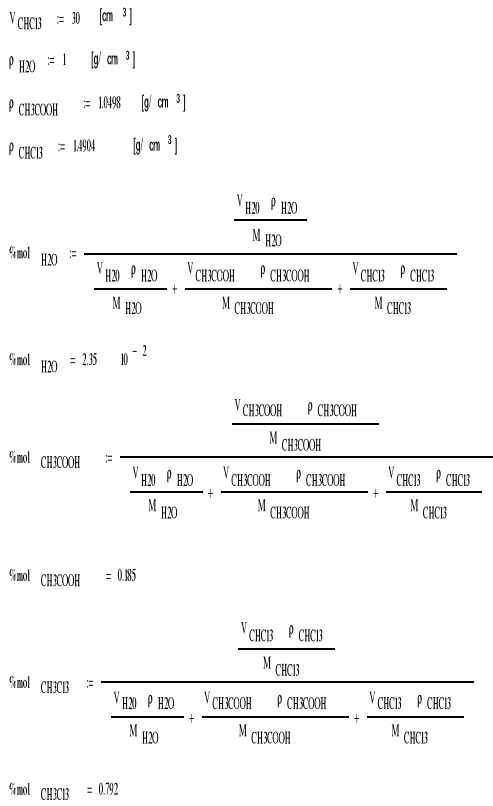
2
Wyszukiwarka
Podobne podstrony:
Lab 9 12, Studia - Politechnika Opolska, Semestr 2, Informatyka
Lab 7 12, Studia - Politechnika Opolska, Semestr 2, Informatyka
Lab 8 12, Studia - Politechnika Opolska, Semestr 2, Informatyka
materiaB do 12, Studia, Politechnika
SprawfizRE.-12-, Studia, Politechnika
fiza 12 odpowiedzi, Politechnika Slaska, studia zaoczne, rybnik, wydzial gornictwo i geologia, semes
O.12.3P, Politechnika Lubelska, Studia, Studia, fizyka
12. szlif, Politechnika Lubelska, Studia, Studia, Sprawka 5 semestr, technologia maszyn tuleja, BOCI
W 4 - 26.10.12, Studia, Praca Socjalna, Semestr 5, Rynek pracy
petrologia8 2.12, Studia (Geologia,GZMIW UAM), II rok, Petrologia, Wykłady, Wykłady
Prawo inżynierskie i ochrona własności intelektualnych. Wykład 3, Studia, Politechnika Łódzka - Pend
Ch w9 8.12, Studia (Geologia,GZMIW UAM), I rok, Chemia
Testy biodegradacji, Studia, Politechnika
Norek7-12, studia, Etyka
Chf9, Studia, Politechnika
Wyznaczanie stałej reakcji szybkości zmydlania estru, Studia, Politechnika
Kresowa księga sprawiedliwych T 12 Studia i materiały Warszawa 2007 ISBN 978 83 60464 61 8
CH.F.L9, Studia, Politechnika
ZAKAAD CHEMI FIZYCZNEJ, Studia, Politechnika
więcej podobnych podstron