TREŚĆ ZADAŃ I PRZYKŁADOWE ODPOWIEDZI
I ETAP
44 OGÓLNOPOLSKIEGO KONKURSU CHEMICZNEGO
IM. PROF. ANTONIEGO SWINARSKIEGO
Wersja II
ZAD. A (20 pkt)
1. Liczbami kwantowymi n = 3 i l = 0 opisany jest orbital …………… .
2. W pewnym tlenku azot łączy się z tlenem w stosunku masowym 7:4. Jest to tlenek o wzorze ............... .
3. Mieszanina złożona z 20 g argonu i 16 g tlenu zajmuje w warunkach normalnych objętość.............. .
4. Celem przeprowadzenia tlenku krzemu w metakrzemian sodu należy użyć
A. mocnego kwasu a potem zasady. B. mocnej zasady a potem kwasu.
C. mocnej zasady. D. wody.
5. W reakcji stężonego kwasem azotowego(V) z miedzią powstaje azotan(V) miedzi(II), woda oraz …………… .
6. Do probówek oznaczonych kolejno numerami od I do V z rozcieńczonym wodnym roztworem siarczanu(VI) miedzi(II) wprowadzono blaszki wykonane ze złota, żelaza, magnezu, srebra i cynku. Zmiana zabarwienia roztworu nastąpiła w probówkach ……………
7. Na rozcieńczony wodny roztwór manganianu(VII) potasu z dodatkiem rozc. kwasu siarkowego(VI) podziałano roztworem siarczanu(IV) sodu. Zaobserwowano zmianę zabarwienia z ……………….. na …………… .
8. W wyniku analizy elementarnej stwierdzono, że próbka 140 mg związku organicznego zawiera 90 mg węgla i 10 mg wodoru. Wzór elementarny tego związku to …………… .
9. W celu zobojętnienia 0,092 gramów pewnego kwasu zużyto 20 cm3 roztworu wodorotlenku sodu o stężeniu 0,1 mola/dm3. Zobojętnianiu poddano kwas
A. masłowy. B. propionowy.
C. octowy. D. metanowy.
10. Proces utwardzania tłuszczów ciekłych polega na reakcji tych związków z .......... wobec ……………. .
ODP. ZAD A/II:
1. 3s; 2. N2O; 3. 22,4 dm3; 4. C; 5. NO2; 6. I, III, V; 7. fioletowego na bezbarwną (lekko różową, różowawą); 8. C3H4O; 9. D; 10. wodorem wobec katalizatora.
ZAD. B (10 pkt)
Jednym z najważniejszych zastosowań kompleksometrii jest analiza środowiskowa mająca na celu między innymi oznaczanie zawartości metali w glebie. Do oznaczeń kompleksometrycznych używa się roztworu wodnego EDTA. Odczynnik ten kompleksuje wybrane jony metali w stosunku molowym 1:1.
W celu oznaczenia zawartości jonów wapnia i magnezu w glebie odważono 20,0 g wysuszonej, a wcześniej wyprażonej gleby, dodano 200,00 cm3 roztworu octanu amonu i mieszano przez 2 godziny. Następnie roztwór przesączono, pobrano 50,00 cm3 ekstraktu, zalkalizowano do pH = 12 i oznaczono zawartość jonów wapnia zużywając na miareczkowanie, w obecności mureksydu jako wskaźnika, 3,50 cm3 roztworu EDTA o stężeniu 0,01 mol/dm3. Roztwór po oznaczeniu jonów wapnia zobojętniono a następnie dodano buforu amoniakalnego i oznaczono jony magnezu miareczkując roztworem EDTA o stężeniu 0,01 mol/dm3 wobec czerni eriochromowej T jako wskaźnika. Na miareczkowanie zużyto 15,00 cm3 roztworu.
1. Obliczyć w analizowanej objętości ekstraktu zawartość (w mg):
a) wapnia,
b) magnezu.
2. Podać zawartość (w mg):
a) wapnia w przeliczeniu na kg gleby,
b) magnezu w przeliczeniu na kg gleby.
ODP. ZAD B/II:
1.a - 1,4 mg; 1.b - 3,6 mg.
2.a - 280 mg/kg gleby ; 2.b - 720 mg/kg gleby.
ZAD. C (10 pkt)
Zbudowano ogniwo z elektrody wodorowej i elektrody srebrowej zanurzonej w roztworze azotanu(V) srebra o stężeniu 0,01 mol/dm3. Elektrodę wodorową stanowił drucik platynowy pokryty czernią platynową, omywany gazowym wodorem pod ciśnieniem 1013,25 hPa zanurzony w roztworze kwasu solnego o temperaturze 25 oC i pH = 1.
1. Zapisać:
a) schemat tego ogniwa zgodnie z Konwencją Sztokholmską,
b) równania reakcji chemicznych zachodzących na elektrodach.
2. Podać, która z elektrod jest dodatnim biegunem ogniwa.
3. Obliczyć:
a) potencjał elektrody wodorowej w temp. 25 oC,
b) SEM ogniwa.
ODP. ZAD C/II:
1.a - (-) Pt,H2|H+||Ag+|Ag (+).
1.b - dodatnia: Ag+ + 1e → Ag ; ujemna: H2 → 2H+ + 2e.
2. - biegunem dodatnim jest elektroda srebrowa.
3.a - E H+/H2 = -0,059 V; 3.b - SEM = 0,740 V.
ZAD. D (15 pkt)
W szkolnej pracowni chemicznej znajdują się następujące odczynniki chemiczne i roztwory:
AgNO3(aq.), AgNO3, Ag2O, Br2(aq), CH3OH, C2H5OH, CaC2, Ca(OH)2(aq), CH3COOH, Cu, CuO, CuCl2, CuCl2(aq), CuSO4, CuSO4(aq), FeCl3.6H2O, FeCl3(aq), FeBr3, FeCl2, HCOOH, HCl(aq), H2SO4, jod, I2/KI(aq), KOH, KOH(aq), KMnO4, K2SO4, K2CrO4, Mg, NH3(aq), NH4Cl, NaOH, NaOH(aq), roztwór fenoloftaleiny, roztwór skrobi.
Wykorzystując niektóre z nich dokonać jednoznacznej identyfikacji następujących substancji : gliceryny, glukozy, hept-1-enu, kwasu mrówkowego i roztworu wodnego benzenolu,
Dla każdej z wymienionych substancji zaproponować chemiczny sposób identyfikacji poprzez podanie:
a) odpowiednich odczynników i warunków reakcji (na zimno, ciepło itp.),
b) obserwacji potwierdzających obecność danego związku
oraz
c) stosownego równania lub równań reakcji.
ODP. ZAD D/II:
Gliceryna - CuSO4(aq), NaOH(aq) na zimno; rozpuszczenie osadu, szafirowo zabarwiony roztwór;
C3H5(OH)3 + Cu(OH)2 C3H5(OH)O2Cu + 2H2O
Glukoza - Np.: CuSO4(aq), NaOH(aq) na zimno; rozpuszczenie osadu, szafirowo zabarwiony roztwór;
na ciepło; ceglasty osad;
C5H11O5CHO + 2Cu(OH)2 C5H11O5COOH + Cu2O + 2H2O.
Hept-1-en - Br2(aq) na zimno; odbarwienie;
CH3(CH2)3CH=CH2 + Br2 CH3(CH2)3CHBrCH2Br.
Kwas mrówkowy - Np.: NaOH(aq), roztwór fenoloftaleiny, na zimno; odbarwienie;
HCOOH + NaOH HCOONa + H2O
Benzenol - Np.: FeCl3(aq) na zimno; fioletowo (ciemno) zabarwiony roztwór;
6C6H5OH + FeCl3 ![]()
H3[(C6H5O)6Fe] + 3HCl
ZAD. E (15 pkt)
W chemii organicznej znana jest tzw reakcja Cannizzaro. Jest to reakcja utleniania-redukcji, której ulegają aldehydy nie posiadające atomu wodoru przy węglu bezpośrednio związanym z grupą aldehydową (tzw. węglu α). Reakcja ta zachodzi pod wpływem silnej zasady zgodnie ze schematem:
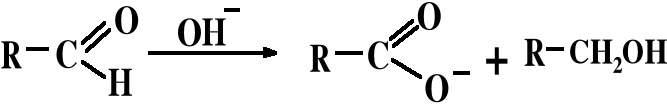
Poniżej przedstawiono wzory grupowe i strukturalne wybranych aldehydów:
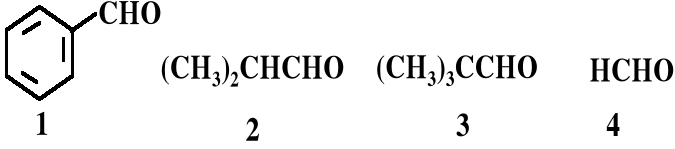
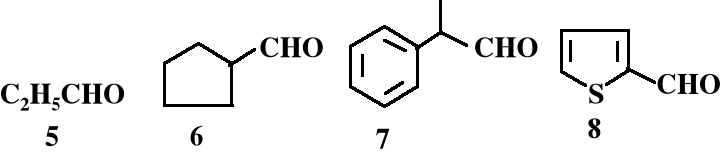
1. Spośród podanych aldehydów wybrać te, które ulegają reakcji Cannizzaro.
2. Dla jednego łańcuchowego i jednego cyklicznego aldehydu ulegających reakcji Cannizzaro zapisać odpowiednie równania reakcji.
3. Dla każdego z substratów i produktów organicznych występujących w równaniach (patrz pkt 2) podać stopnie utlenienia tych atomów, które je zmieniły.
4. Zapisać uproszczone równania reakcji połówkowych dla obu reakcji (patrz pkt 2).
5. Podać ogólną nazwę tego typu reakcji utleniania-redukcji i sformułować jej definicję.
6. Dla wybranego łańcuchowego aldehydu ulegającego reakcji Cannizaro (patrz. pkt 2) podać jego nazwę systematyczną oraz nazwy systematyczne produktów reakcji.
7. Dla wybranego cyklicznego substratu (patrz. pkt 2) podać masy produktów, które powstaną z 0,1 mola substratu, przy założeniu 60% wydajności całego procesu.
ODP. ZAD E/II:
1. Aldehydy ulegające reakcji Cannizzaro to związki 1,3, 4, 8.
2. Np.: 2HCHO + NaOH HCOONa + CH3OH,
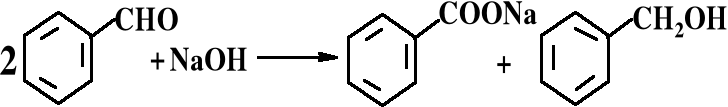
3. C w HCHO na 0; C w HCOOH na II; C w CH3OH na -II.
C w grupie aldehydowej związku C6H5CHO na I; C w grupie -COONa
związku C6H5COONa na III; C w grupie -CH2OH związku C6H5CH2OH
na -I.
4.
C0 - 2e CII i C0 + 2e C-II oraz CI - 2e CIII i CI + 2e C-I
5. Jest to reakcja dysproporcjonowania (dysmutacji). Jest to taka reakcja redoks, w której cześć atomów tego samego pierwiastka ulega utlenieniu a część redukcji.
6. Np.: metanal, metanian sodu, metanol.
7. Np.: 4,32 g benzoesanu sodu i 3,24 g alkoholu benzylowego.
DANE:
Masy atomowe: Ar - 40u; C - 12u; Ca - 40u; Cu -64u; H - 1u; K - 39u; Mg - 24u; N - 14u; Na - 23u; O - 16u.
Potencjały standardowe: E0Ag/Ag+ = 0,799 V.
4
44 Ogólnopolski Konkurs Chemiczny im. prof. A.Swinarskiego, Etap I, wersja II
Wyszukiwarka
Podobne podstrony:
strategie cenowe zad koło, FiR UMK Toruń 2010-2013, II FiR, Strategie cenowe
ZAD36, Medycyna, umk
ZAD35, Medycyna, umk
Dematologia czerwiec 2014, Medycyna CM UMK - materiały, IV ROK, DERMATOLOGIA, Giełdy
toksykologia w medycynie ratunkowej, Fizjoterapia CM UMK, Pierwsza pomoc
pytania moja BYŁA grupa-P radio, Medycyna CM UMK - materiały, V ROK, RADIOLOGIA, Giełdy, prof. Seraf
Giełda na 2 rok CM UMK, Medycyna, II rok
medycyna regeneracyjna, Dietetyka CM UMK, Biologia z genetyką
Idea medycyny paliatywnej, Pielęgniarstwo licencjat cm umk, III rok, Opieka paliatywna
chem2010 zad alkeny odp2
PARAZYTOLOGIA, Medycyna CM UMK - materiały, I ROK, BIOLOGIA MEDYCZNA, Przezentacje
Medycyna paliatywna, Pielęgniarstwo licencjat cm umk, III rok, Opieka paliatywna
więcej podobnych podstron