ZASTOSOWANIE POMIARÓW PRZEWODNICTWA WŁAŚCIWEGO (KONDUKTOMETRII) DO OZNACZANIA ZANIECZYSZCZEŃ
Ćwiczenie K-2
Ilościowe oznaczanie dwutlenku węgla w powietrzu.
Oznaczanie oparte jest na reakcji :
Ba(OH)2 + CO2 → BaCO3 + H2O (1 mol Ba(OH)2 reaguje z 1 molem CO2)
Na podstawie spadku przewodnictwa właściwego roztworu wodorotlenku barowego przed i po pochłonięciu CO2 obliczono zawartość dwutlenku węgla.
Odczynniki i aparatura
wodorotlenek barowy świeżo sporządzony o stężeniu około 0,01 mol/dm3 ,
konduktometr,
zestaw płuczek, aspirator.
Wykonanie ćwiczenia
napełniono cztery płuczki o pojemności 150 cm3 mianowanym roztworem Ba(OH)2, połączono szeregowo z aspiratorem i zatkano wylot zatyczką,
zmierzono przewodność właściwą wyjściowego roztworu Ba(OH)2 w jednej z płuczek,
zdjęto zatyczki z płuczki i przepuszczono przez płuczki 20 dm3 powietrza z szybkością 55dm3/h,
zmierzono przewodnictwo właściwe roztworu Ba(OH)2 w każdej z płuczek.
Wyniki pomiarów
W poniższej tabeli przedstawiono wyniki pomiarów przewodnictwa i stężenia, które zostało odczytane z krzywej zależności Ba(OH)2 od przewodnictwa κ = 464,86 * C + 0,1717.
Tabela 1
Numer płuczki |
Przewodnictwo [mS] |
Stężenie Ba(OH)2 [mol/dm3] |
Roztwór podstawowy |
6,0 |
0,0125 |
Płuczka I |
4,9 |
0,0102 |
Płuczka II |
4,8 |
0,0099 |
Płuczka III |
5,0 |
0,0104 |
Płuczka IV |
4,9 |
0,0102 |
Obliczono różnicę stężeń roztworu Ba(OH)2 :
Płuczka I 0,0125mol/dm3 - 0,0102mol/dm3 = 0,0023 mol/dm3
Płuczka II 0,0125mol/dm3 - 0,0099mol/dm3 = 0,0026 mol/dm3
Płuczka III 0,0125mol/dm3 - 0,0104mol/dm3 = 0,0021 mol/dm3
Płuczka IV 0,0125mol/dm3 - 0,0102mol/dm3 = 0,0023 mol/dm3
Do płuczek wlano po 150 cm3 Ba(OH)2 . Obliczono w ten sposób ilość moli dwutlenku węgla w każdej płuczce ![]()
:
Płuczka I 0,0023 mol/dm3 ⋅ 0,15 dm3 = 0,000345 mola
Płuczka II 0,0026 mol/dm3 ⋅ 0,15 dm3 = 0,00039 mola
Płuczka III 0,0021 mol/dm3 ⋅ 0,15 dm3 = 0,000315 mola
Płuczka IV 0,0023 mol/dm3 ⋅ 0,15 dm3 = 0,000345 mola
Σ = 0,001395 mola
Obliczono objętość pochłoniętego CO2:
1 mol - 22,4 dm3 CO2
0,001395 mol - x dm3 CO2
x = 0,001395 mol * 22,4 dm3/ 1 = 0,0313 dm3 CO2
Czas pochłaniania: 22,0 min
Prędkość przepływu: 55,0 dm3/h
Objętość przepuszczonego powietrza: 20,0 dm3
Współczynnik pochłonięcia k: 0,5 - (50%)
Obliczono objętość CO2 w przepuszczonym powietrzu:
0,0313 dm3 CO2 * 2= 0,0626 dm3 CO2
Obliczono objętość CO2 w przepuszczonym powietrzu:
20 dm3 powietrza - 100%
0,0626 dm3 CO2 - x%
x = 0,0626 dm3 ⋅ 100 / 20 dm3 = 0,313 % CO2
Wnioski
Przeprowadzone doświadczenie pozwoliło na oznaczenie dwutlenku węgla w powietrzu. Polegało ono na badaniu spadku przewodnictwa właściwego roztworu wodorotlenku barowego. W analizowanym powietrzu znajdowało się 0,0626 dm3 CO2, co stanowiło 0,313 % powietrza.
ZASTOSOWANIE POMIARÓW PRZEWODNICTWA WŁAŚCIWEGO (KONDUKTOMETRII) DO OZNACZANIA ZANIECZYSZCZEŃ
Ćwiczenie K-3
Konduktometryczne oznaczanie zawartości kwasu solnego i octowego w mieszaninie
Konduktometryczne oznaczanie równocześnie występujących dwóch kwasów jest możliwe tylko wówczas, gdy różnią się one dość znacznie wartościami stałych dysocjacji (mają różną moc).
Odczynniki i aparatura
wodorotlenek sodowy o natężeniu 0,1 mol/dm3
konduktometr
Wykonanie ćwiczenia
otrzymany roztwór kwasu solnego i kwasu octowego o nieznanym stężeniu rozcieńczono wodą destylowaną w kolbie miarowej do 100 cm3. Następnie pobrano do zlewki 20 cm3 tak przygotowanego roztworu i dodano 80 cm3 wody destylowanej,
zlewkę z tak przygotowaną próbką umieszczono na mieszadle magnetycznym i zmierzono przewodnictwo,
dodawano z biurety po 0,5 cm3 wodorotlenku sodowego o stężeniu 0,1 mol/dm3, mieszając po dodaniu każdej porcji i odczytywano wartość przewodnictwa,
miareczkowanie prowadzono do 6 - 7 punktów po przekroczeniu punktu końcowego (PK2!)
miareczkowanie wykonano dla próby nr 2 dwukrotnie.
Wyniki pomiarów
W poniższej tabeli przedstawiono wyniki pomiarów przewodnictwa dla próby nr 2.
Tabela nr 1
VNaOH [cm3] |
Wartości przewodnictwa [mS] |
|
|
Pomiar I |
Pomiar II |
0 |
2,3 |
2,5 |
0,5 |
2,2 |
2,3 |
1,0 |
2,1 |
2,3 |
1,5 |
1,9 |
2,2 |
2,0 |
1,8 |
1,9 |
2,5 |
1,7 |
1,7 |
3,0 |
1,6 |
1,6 |
3,5 |
1,4 |
1,5 |
4,0 |
1,3 |
1,3 |
4,5 |
1,2 |
1,2 |
5,0 |
1,1 |
1,0 |
5,5 |
0,9 |
0,9 |
6,0 |
0,8 |
0,8 |
6,5 |
0,7 |
0,7 |
7,0 |
0,7 |
0,7 |
7,5 |
0,7 |
0,7 |
8,0 |
0,8 |
0,8 |
8,5 |
0,8 |
0,8 |
9,0 |
0,8 |
0,8 |
9,5 |
0,8 |
0,8 |
10,0 |
0,9 |
0,9 |
10,5 |
0,9 |
0,9 |
11,0 |
0,9 |
1,0 |
11,5 |
0,9 |
1,0 |
12,0 |
1,0 |
1,1 |
12,5 |
1,0 |
1,2 |
13,0 |
1,1 |
1,2 |
13,5 |
1,1 |
1,4 |
14,0 |
1,2 |
1,5 |
14,5 |
1,3 |
1,5 |
15,0 |
1,4 |
1,6 |
15,5 |
1,5 |
1,7 |
16,0 |
1,6 |
1,8 |
16,5 |
1,7 |
1,9 |
17,0 |
1,8 |
2,0 |
17,5 |
1,9 |
2,1 |
18,0 |
2,0 |
2,2 |
18,5 |
2,1 |
2,3 |
Na dołączonym wykresie zobrazowano zależność przewodnictwa od objętości NaOH dla pomiaru I.
Jak widać z wykresu, pierwszy punkt końcowy (PK1) oznaczający koniec miareczkowania mocnego kwasu solnego (HCl) leży na pierwszym załamaniu krzywej miareczkowania. Ilość zużytego NaOH wynosi 6,67 cm3. Drugi punkt końcowy (PK2) oznacza koniec miareczkowania kwasu octowego (CH3COOH). Ilość zużytego NaOH wynosi: 13,11 cm3.
Obliczono zawartość obu kwasów w mieszaninie:
NaOH + HCl → NaCl + H2O
NaOH + CH3COOH → CH3COONa + H2O
NaOH reaguje z obydwoma kwasami w stosunku 1 : 1, więc:
![]()
![]()
gdzie:
![]()
więc:
![]()
![]()
MHCl = 36,4609 g/mol
MCH3COOH= 60,0534 g/mol
CNaOH = 0,1 mol/dm3
VNaOH (PK1) = 6,67 cm3
VNaOH (PK2) = 13,11 cm3
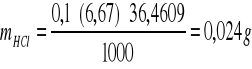
![]()
Wnioski
Przeprowadzone doświadczenie pozwoliło na jednoczesne oznaczenie kwasu solnego i kwasu octowego w mieszaninie. Polegało ono na badaniu przewodnictwa roztworu wodorotlenku sodowego podczas dodawania tego roztworu do próby. W analizowanym próbie znajdowało się 0,024 g HCl i 0,039 g CH3COOH.
Wyszukiwarka
Podobne podstrony:
spekrofotometria, SPEKTROFOTOMETRIA ABSORPCYJNA W ŚWIETLE WIDZIALNYM (VIS) I W NADFIOLECIE (UV)
SPEKTROFOTOMETRIA ABSORPCYJNA W ŚWIETLE WIDZIALNYMpat, Chemia 1
1 Absorpcjometria w świetle widzialnym
Spektrofotometria w swietle widzialnym
Sprawozdania, Spektrofotometria absorpcyjna, Spektrofotometria absorpcyjna
Sprawozdania z analizy instrumentalnej, AAS I, Atomowa Spektrometria Absorpcyjna
UV-vis, ZAKRESY UV- PRÓŻNIOWY (DALEKI) 100-200 nm 100000-50000 CM-1 UV-KWARCOWY (WŁAŚCIWY) 200-380 n
Sprawozdania z analizy instrumentalnej, AAS I, Atomowa Spektrometria Absorpcyjna
UV-vis, ZAKRESY UV- PRÓŻNIOWY (DALEKI) 100-200 nm 100000-50000 CM-1 UV-KWARCOWY (WŁAŚCIWY) 200-380 n
biofizyka-PROMIENIOWANIE NADFIOLETOWE UV, PROMIENIOWANIE NADFIOLETOWE UV (ultrafioletowe)
05 Spektrofotometria absorpcyjna (kolorymetria)
sprawozdanie Spektroskopia absorpcyjna w podczerwieni, spektroskopia
PROMIENIOWANIE NADFIOLETOWE UV, fizykoterapia(2)
CW2 3, POMIAR EFEKTÓW PODSTAWNIKOWYCH METODĄ SPEKTROSKOPII ABSORPCYJNEJ W PODCZERWIENI
testy chemia, pat sciąga chemia zerówka, II Spektrofotometria absorpcyjna
ATOMOWA SPEKTROFOTOMETRIA ABSORPCYJNA, Analiza Instrumentalna
Spektroskopia absorpcyjna
więcej podobnych podstron