Ab
so
rp
cja
W
świ
et
le
widz
ial
n
ym
1
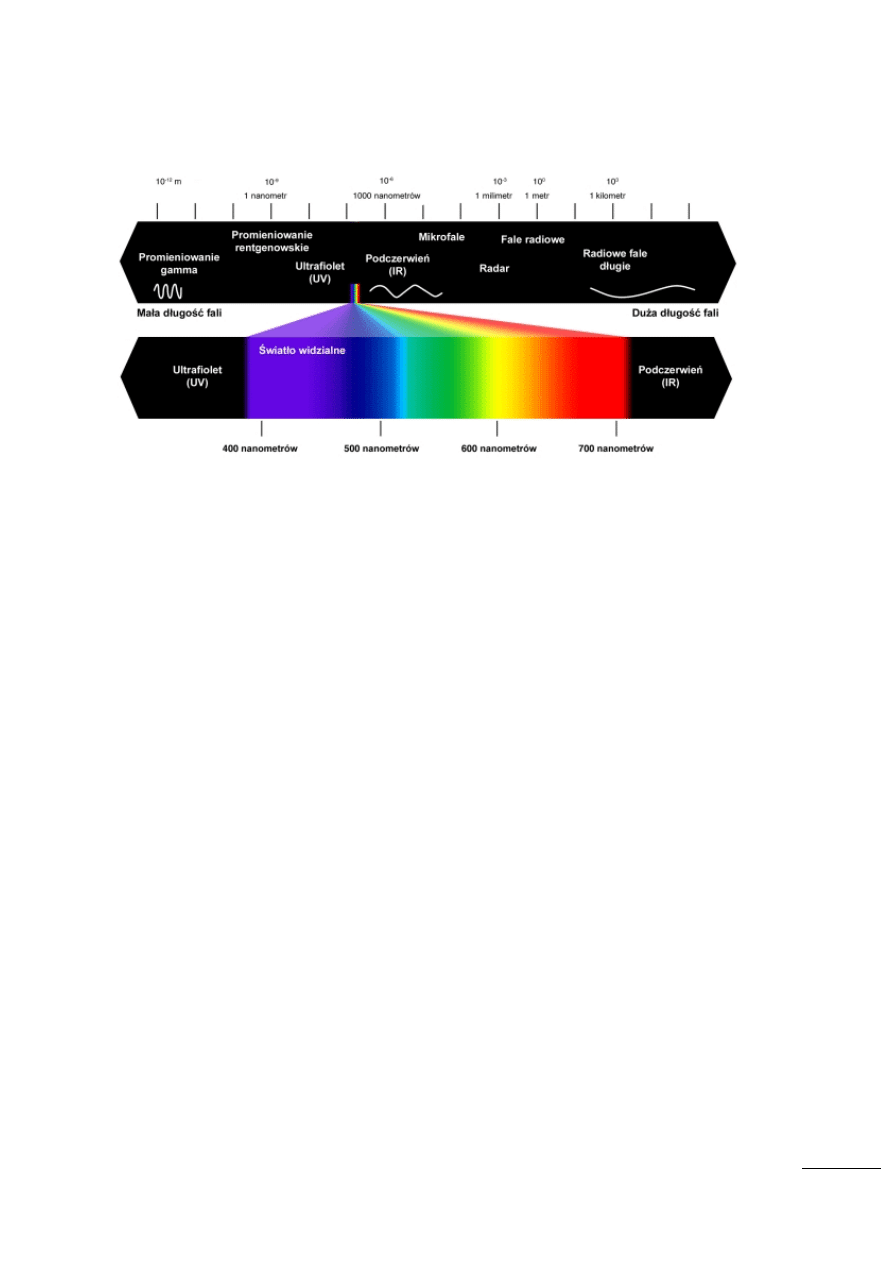
Absorpcjometria – metoda optyczna wykorzystujaca zjawisko selektywnej absorpcji promieniowania
elektromagnetycznego. Wykorzystuje się światło widzialne ( 380 – 780 nm)
Promieniowanie em. Przechodząc przez materię ulega pochłonięciu, czyli absorpcji.
Cząsteczki ulegają wielu procesom dynamicznym:
-obrót cząsteczki jako całośd rotacja
-drgania atomów w cząsteczce oscylacja
-ruchy atomów w polu nabojów ( towarzyszy zmiana energii zawartej w cząsteczce)
Widma absorpcyjne są wynikiem zmian energetycznych, zachodzących w cząsteczce danego związku
chemicznego. Przejścia między poziomami elektronowymi towarzyszy absorpcja w nadfiolecie i części
widzialnej; natomiast przejścia między podpoziomami oscylacyjnymi tego samego poziomu
elektronowego towarzyszy absorpcja w bliskiej i właściwej podczerwieni ( również przejścia między
sąsiadującymi podpoziomami rotacyjnymi). Dzięki odmiennym rozkładom poziomów energii ich
widma absorpcyjne różnią się między sobą, co daje duża możliwośd ich identyfikacji i oznaczeo.
Wrażenie barwy substancji związane jest z jej zdolnością absorpcji niektórych fal promieniowania em.
Przechodzące światło przepuszczamy substancję przeźroczystą następnie przez pryzmat szklany
otrzymując obraz widma p.em. w zakresie widzialnym z ciemnymi pasami wywołanymi
pochłanianiem promieniowaia o określonej długości fali.
Widmo absorpcyjne – wykres zależności absorpcji od długości fali. Uzyskujemy je za pomocą
spektrofotometru.
Przyczyną powstania barwy obecnośd sprzężonego układu elektronów π ( szczególnie latwo legają
wzbudzeniu; łatwiej im dłuższy układ)
PRAWA ABSORBCJI:

Ab
so
rp
cja
W
świ
et
le
widz
ial
n
ym
2
Padająca a warstwę roztworu wiązka promieniowania monochromatycznego ulega
- absorpcji
- przejściu przez roztwór
- odbiciu i rozproszeniu
Natężenie promieniowania padającego (Io) jest równe sumie natężeo promieniowania
zaabsorbowanego (Ia); natężenia promieniowani odbitego i rozproszonego (Ir) oraz natężeniu
promieniowania które przeszło przez roztwór (It)
I
0
= I
a
+ I
r
+ I
t
Transmitacja – stosunek światła wychodzącego z danego ośrodka (I
t
) do natęzenia światła
padającego (I
0
; określa jaka częśd promieniowania padającego została przepuszczona przez
substancję absorbującą. *%+
T= I
t
/ I
0
* 100%
Absorbancja – logarytm stosunku natężenia promieniowania padającego (I
o
) do promieniowania
wychodzącego (I
t
). (logarytm odwrotności transmitacji)
A= lg (1/ T)
A= lg (100/ T [%]

Ab
so
rp
cja
W
świ
et
le
widz
ial
n
ym
3
Prawo Bougera-Lamberta –określa zwiazek między absorbuj a grubościa ośrodka absorbującego
𝑑𝐼
𝐼
= −𝑘𝑑𝑙
I – natężenie światła wchodzącego do danej warstwy
k- współczynnik proporcjonalności
l- grubośd warstwy absorbującej [cm]
Prawo Beera – zależnośd absorbancji od stężenia substancji absorbującej przy stałej grubości
warstwy.
A= K’c
c- stężenie substancji
Prawo Bougera-Lamberta-Beera-Waltera - zależnośd absorbancji od stężenia substancji absorbującej
oraz grubości warstwy
𝐴 = 𝑙𝑔
𝐼
0
𝐼
𝑡
= 𝑎𝑐𝑙
a - Współczynnik absorpcji (a=A/cl)
Wyrażanie stężenia substancji
1) Stężenie molowe
A=εcl
ε – molowy współczynnik absorpcji ( L/mol*cm)
2) Stężenie masowe
A= ρa
s
l
a
s
– współczynnik absorpcji właściwej
Postad wykładnicza
I
t
=I
0
- ερl
Natężenie promieniowania zaabsorbowanego zależy od liczby cząsteczek znajdujących się w ośrodku
na drodze promieniowania oraz absorpcji kwantów przez te cząsteczki.
Pomiary absorbcji wykonuje się zawsze w zestawieniu z roztworem wzorcowym, w celu
wyeliminowania czynników dodatkowych.
Prawo addytywności absorbancji- absorbancja całkowita roztworu wieloskładnikowego jest równa
sumie absorbancji poszczególnych składników. (grubośd warstwy jest stała)

Ab
so
rp
cja
W
świ
et
le
widz
ial
n
ym
4
Odstępstwa od prawa absorpcji (widoczne na wykresie zależności absorbancji a stężenia, jako
odchylenia od prostej) spowodowane są:
1) Odstępstwa chemiczne ( zmiana kształtu widma absorpcyjnego)
a. Oddziaływanie cząsteczek między sobą (dysocjacja, asocjacja)
b. =||=
cząsteczkami rozpuszczalnika
c. Tworzenie kompleksów
d. Nieodpowiednia długośd fali użyta do badania próbki
2) Odstępstwa fizyczna
a. Niemonochromatycznośd promieniowania
Wyszukiwarka
Podobne podstrony:
SPEKTROFOTOMETRIA ABSORPCYJNA W ŚWIETLE WIDZIALNYMpat, Chemia 1
konduktometria, SPEKTROFOTOMETRIA ABSORPCYJNA W ŚWIETLE WIDZIALNYM (VIS) I W NADFIOLECIE (UV)
spekrofotometria, SPEKTROFOTOMETRIA ABSORPCYJNA W ŚWIETLE WIDZIALNYM (VIS) I W NADFIOLECIE (UV)
Spektrofotometria w swietle widzialnym
Absorpcja
Psychologia osobowości dr Kofta wykład 4 Osobowość w świetle teorii uczenia sie
Kolumna absorpcyjna z wypelnieniem
ŚWIETLICA WIEJSKA W ŁUSZKOWIEGYUIO
Kolumna absorpcyjna
IV SA Wa 198 08 Wyrok WSA w Warszawie ws zakazu reklamy świetlnej
Świetlówka inaczej Errata
Ćwiczenie 1 Badania strumienia świetlnego różnych źródeł światła
Oświetlenie, Podstawowe pojęcia techniki świetlnej
elektroniczny zapłonnik świetlówki
Czynne rozliczenia międzyokresowe kosztów w świetle ustawy o rachunkowości
Badania mikrobiologiczne żywności w świetle nowych przepisów UE
więcej podobnych podstron