Dla zbudowania trójskładnikowego układu składającego się z CaO, CO2, CaCO3 wystarczą dwa składniki np.: CaO i CO2 gdyż trzeci składnik w układzie pojawi się wskutek reakcji: CaO + CO2 → CaCO3 . Tak więc ilość składników niezależnych dla układu „CaO, CO2, CaCO3 ” jest równa ilości składników obecnych w układzie pomniejszonej o jeden (jedno równanie wiąże ze sobą składniki tworzące układ):
α = 2.
DLA DANEJ WARTOŚCI α MAKSYMALNA LICZBA FAZ W UKŁADZIE WYSTEPUJE, GDY s = 0 (tzw. układ inwariantny, niezmienny).
WÓWCZAS:
UKŁAD JEDNOSKŁADNIKOWY: βmax. = 3
UKŁAD DWUSKŁADNIKOWY: βmax. = 4
UKŁAD TRÓJSKŁADNIKOWY: βmax. = 5
W takim razie w warunkach stałego ciśnienia i temperatury w układzie jednoskładnikowym maksymalna liczba faz pozostających w równowadze może wynosić βmax. = 3 (gdy s = 0), oczywiście w zależności od wzajemnej rozpuszczalności składników istnieją również jedno- i dwufazowe układy jednoskładnikowe
Gdy układ zawiera α składników niezależnych, jego stan termodynamiczny opisują: temperatura, ciśnienie oraz stężenia (α - 1) składników w każdej z faz (stężenie ostatniego składnika jest jednoznacznie określone przez stężenia pozostałych składników). Gdy układ przy tym składa się z β faz, a temperatura i ciśnienie są w każdym punkcie jednakowe, to jego stan opisuje 2 + β(α-1) parametrów intensywnych.
Lp = 2 + β(α-1)
CZY WSZYSTKIE PATAMETRY INTENSYWNE MOGĄ PRZYJMOWAĆ DOWOLNE WARTOŚCI
??????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????
!!!!!!!!!!!!!!!NIE!!!!!!!!!!!!!!
STĘŻENIA MUSZĄ SPEŁNIAĆ WARUNKI RÓWNOWAGI UKŁADU
PRZY STAŁEJ TEMPERATURZE I CIŚNIENIU DLA KAŻDEGO ZE SKŁADNIKÓW UKŁADU W STANIE RÓWNOWAGI POTENCJAŁ CHEMICZNY MUSI BYĆ TAKI SAM WE WSZYSTKICH FAZACH, CZYLI MUSZĄ BYĆ SPEŁNIONE NASTĘPUJĄCE RÓWNANIA:
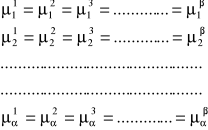
LICZBA TYCH RÓWNAŃ WYNOSI
Lr = α(β-1)
PO CO TO s ???????????????
LICZBA STOPNI SWOBODY UKŁADU OKREŚLA LICZBĘ ZMIENNYCH, KTÓRYCH WARTOŚCI MOŻNA ZMIENIAĆ, PRZY CZYM TA ZMIANA, WYWOŁUJĄC NARUSZENIE STANU RÓWNOWAGI, NIE POWDUJE JEDNAK ZMIANY LICZBY FAZ.
W NOWYM STANIE RÓWNOWAGI JAKI USTALI SIĘ W UKŁADZIE, WYSTEPUJĄ OBOK SIEBIE TE SAME FAZY, CO POPRZEDNIO, TYLKO W INNYCH ILOŚCIACH.
JEŻELI WYMUSI SIĘ NA UKŁADZIE PRZYJĘCIE CHOCIAŻBY JEDNEJ ZMIENNEJ PONAD LICZBĘ STOPNI SWOBODY, NASTĄPI NIEUCHRONNE ZMNIEJSZENIE SIĘ LICZBY FAZ W UKŁADZIE.
SKŁADNIKI NIEZALEŻNE CZYLI TE KTÓRYCH STĘŻENIA W KTÓREJKOLWIEK Z FAZ NIE SĄ POWIĄZANE MIĘDZY SOBĄ ZALEŻNOŚCIAMI STECHIOMETRYCZNYMI, WYNIKAJĄCYMI Z PRAWA DZIAŁANIA MAS. LICZBĘ NIEZALEŻNYCH SKŁADNIKÓW MOŻNA WIĘC OBLICZYĆ, ODEJMUJĄC OD LICZBY WSZYSTKICH SKŁADNIKÓW WYSTEPUJĄCYCH W UKŁADZIE LICZBĘ WZAJEMNIE NIEZALEŻNYCH RÓWNAŃ, JAKIMI MOŻNA POWIĄZAĆ STĘŻENIA POSZCZEGÓLNYCH SKŁADNIKÓW W OKREŚLONEJ FAZIE. JEŻELI W UKŁADZIE MOGĄ PRZEBIEGAĆ REKACJE CHEMICZNE, DOCHODZĄCE DO STANU RÓWNOWAGI, ZANIM ZOSTANIE OSIĄGNIETY STAN RÓWNOWAGI FAZOWEJ, TO KAŻDA Z TYCH REKACJI WNOSI JEDNO RÓWNANIE WIĄŻĄCE STĘŻENIA.
α = n - r - w
n - chemicznie różne składniki
r - liczba niezależnych równań stechiometrycznych
w - dodatkowe warunki stechiometrii
W
Q
W
Q
Składniki
Zamknięty
Otwarty
Otoczenie
Otoczenie
Otoczenie
Układ
Niezależne od ilości materii w układzie:
temperatura
ciśnienie
ułamek molowy
Proporcjonalne do ilości materii w układzie:
masa
objętość
Liczba stopni swobody
Intensywne
Ekstensywne
Parametry stanu układu
Stan układu
UKŁAD JEST DWUSKŁADNIKOWY, MIMO ŻE WYSTĘPUJE W NIM CO NAJMNIEJ 5 RÓŻNYCH INDYWIDUŁÓW CHEMICZNYCH. W TAKIM UKŁADZIE ISTNIEJE STAN RÓWNOWAGI REAKCJI.
H3O+1 + OH-1 = 2H2O
A PONAD TO SPEŁNIONE SĄ DWA DODATKOWE WARUNKI:
warunek stechiometryczny: [Na+1]=[Cl-1]
warunek elektroobojętności: [H3O+1]+[Na+1]=[OH-1]+[Cl-1]
zatem
α = 5 - 1 - 2 = 2
NaCl
Cl-1
H2O
H3O+1
OH-1
Na+1
FAZA - CZĘŚĆ LUB CAŁOŚĆ UKŁADU, KTÓRA WYKAZUJE W CAŁEJ SWEJ MASIE JEDNAKOWE WŁAŚCIOWOŚCI FIZYCZNE I CHEMICZNE I JEST WYRAŹNIE ODGRANICZONA OD RESZTY UKŁADU (OTOCZENIA).
SKŁADNIK - WSZYSTKIE SUBSTANCJE CHEMICZNE, Z KTÓRYCH ZBUDOWANY JEST UKŁAD.
SKŁADNIKI NIEZALEŻNE - SKŁADNIKI, KTÓRYCH ZNAJOMOŚĆ WYSTARCZA I JEST KONIECZNA DO
OKREŚLENIA SKŁADU UKŁADU.
11
B
A
![]()
Maksymalna liczba faz:
Reguła faz Gibbsa:
W stanie równowagi:
T1 = T2 = T3 = .... = T
(warunek równowagi termicznej)P1 = P2 = P3 = .... = P
(warunek równowagi mechanicznej)
....
jest zbudowany z
α - składników
β -faz
P
1
2
3
Układ wieloskładnikowy - wielofazowy...
Liczba stopni swobody:
2
s
max
2
Wyszukiwarka
Podobne podstrony:
Referaty, Stała gazowa R, Równanie stanu gazów doskonałych ( równanie Clapeyrona )
Równania EURELA, BĄKI referat fizyka
Rozwiązywanie układów równań
Referat Inżynieria Produkcji Rolniczej
Równanie Laplace’a
Rownanie Maxwella
referat solidy
statystyka referat MPrzybyl
referat 4
Referat 3 v3
Rozwiązywanie układów równań metodą wyznaczników
Referat 4
04 referat Pieprzyk szczelność powietrzna
więcej podobnych podstron