1.Anabolizm- (Es<Ep) A+B+EC endoergiczny; reakcje syntez związków bardziej złożonych z prostszych, wymagające dost.energii,która umożliwia podniesienie poziomu energet. zw. w czasie procesu chem. Produkt zaw. większą niż substraty ilość energii, magazyn. w postaci wiązań chemicznych. Np.:fotosynteza CO2+H2OC6H12O6+O2, reak.redukcji;
Katabolizm- (Es>Ep) CA+B+E obniżanie poziomu energet. substratów złoż. w wyniku ich rozkładu na zw. proste z wydziel.energii, która wyzwala się podczas rozrywania wiąz. wysokoenerget. substratów.Np.: oddychanie komórkowe (glikoliza-cytoplazma, cykl Krebsa-matriks mitochondrium, łańcuch oddechowy-bł.mitochondrium), reak.utleniania.
2.Gł. substraty energetyczne: węglowodany, białka, lipidy.
3.β-oksydacja kwasów tłuszczowych- Kw.tłuszczow ulegają aktywacji z (CoA i ATP) do acylo-CoA w obecności katalizatora- syntetazy acylo-CoA; w przenoszeniu acylów o dł.łańcuchy (>12C) przez błony mitchondrium pomaga karnityna: przejściowo powstaje acylokarnityna, która reaguje z CoA oddając acyl powst. acylo-CoA. Aktywne kw.tłuszcz nasycone, dzięki dehydrogenazie acylo-CoA przechodzą w nienasycone, a te z udziałem hydratazy enoilo-CoA w aktywe 3-hydroksykwasy (β-hydroksykw.). Te pod wpływem dehydrogenazy 3-hydroksyacylo-CoA, w obecności nowej cz.CoA ulegają rozpadowi na aktyw. kw.octowy (acetylo-CoA); aktywny kw.tłuszczowy nasycony (uboższy o 2atC w stos.do wyjściowego)

4. Katabolizm cukrowców: Hydrolityczny rozkuł.skrobii- enzymy (amylolityczne) α i β-amylaza: α-amylaza rozkłada wiąz. α-1,4-glikozydowe znajdujące się w środku łańcucha, rozbijając do na fragm. β-amylaza hydrolizuje te same wiąz., ale odszczepia fragm.od końców nieredukujących łańcucha. Powstała maltoza rozszczepiana przez maltazę do glukozy. Fosforoliza- rozkład w obecności fosforylazy. Wiąz. α-1,4-glikozydowe rozszczepiane przez ortofosforan: przeniesienie reszty glukozylowej oderwanej od nieredukcyjnego końca polisacharydu na akceptor (kw.fosfor.); od łańcucha sukcesywnie odszczepiają się cz. glukozo-1-fosforanu (w ten sposób przebiega depolimeryzacja skrobii w chloroplastach).
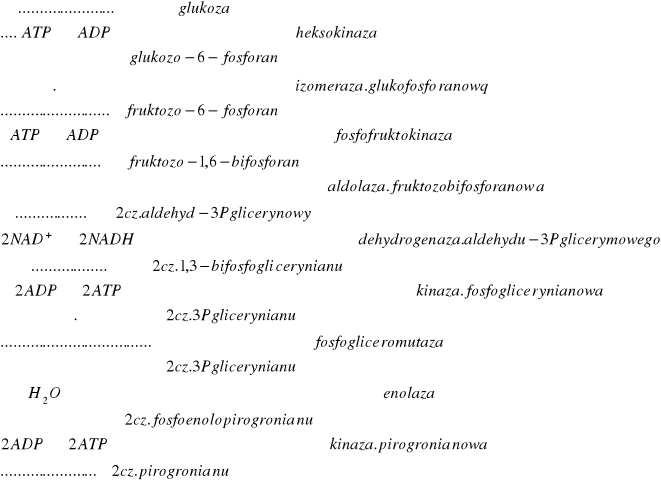
5.Glikoliza i jej przebieg w warunkach tlenowych i beztlenowych-Ietap oddychania kom; stopniowy rozklad glukozy do kw.pirogronowego. 1)fosforylacja glukozy=aktywacja (energia z ATP) do 6-fosforanu glukozy (heksokinaza) konwersja do 6-fosforanu fruktozy (izomeraza glukofosforan.) 1,6-bifosforan fruktozy (1-fruktokinaza,ATP)fosforan 1,3-dihydroksyacetonu i 1,3-dihydroksyacetonu2)wyzwolenie cz.energii; aldehyd-3P-glicerynowy (izomeraza triozofosforanowa)utlenienie i fosforylacja aldehydu (NAD)3-fosforan gliceroilu kinaza fosfoglicerynowa przenosi resztę fosforanową na ADP 3-Pglicerynian i ATP2-fosforoglicerymnian dehydratacja z enolaząfosfoenolopirogronianenolo fosforylacja ADPATP i pirogronian (węzłowy metabolit w metabol.węglowodanów).
6.Oksydacyjna dekarboksylacja kwasu pirogronowego-tworzenie acetylo-CoA, pirogronian w obecności O2 ulega dekarboksylacji do aldehydu octowego,a ten odwodornieniu do reszty arylowej, która wiąże się z CoA (acetylo-CoA), a odłączony H wiązany jest przez NAD+. W reak.biorą udział DPT i kw.LipS2. CH3COCOOH+CoA-SH+NAD+[LipS2, DPT] CH3CO-SCoA+NADH+H++CO2.Procesy kat.przez kompleks dehydrogenazy pirogronianowej: 1) deydrogenaza pirogronianowa E1-dekarboksylacja oksydacyjna pirogronianu. 2)acetylotransferaza dihydroliponianowa E2 przeniesienie gr.acetylowej na CoA. 3)dehydrogenaza liponianowa E3- regeneracja utlenionej formy lipoamidu

7.Bilans energetyczny glikolizy- oddychanie tlenowe-Zużywane 2 cz.ATP do przekształcenia 1 glukozy w bifosforan fruktozy, który ulega przekształceniu w 2 fosfotriozy (z każdej 2cz ATP z utleniania aldehydu fosfoglicer. do kwasu, i z przemiany fosfoenolopir. w pirogronian. Beztlenowe: z 1 glukozy powst 4 cz.ATP, netto 2 ATP. Tlenowe: 2NADH utleniając się dają 6cz ATP; ogółem 8 cz.ATP.
8.Centralna rola acetylo-CoA w przemianach energetycznych- wprowadza zw. 2C do cyklu Krebsa.
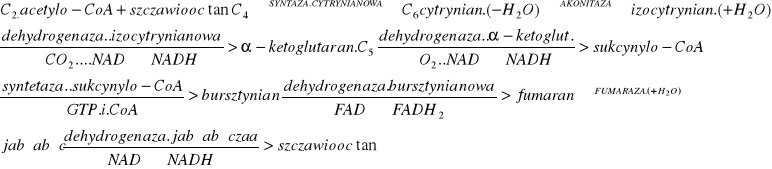
9.Cykl Krebsa- CH3CO-SCoA+ 3H2O+ 3 NAD++ FAD2CO2+ 3NADH+H++FADH2+CoA-SH. Kilkukrot. Przył H2O i 4x odwodornienie z wydziel.2 CO2. 1)acetyloCoA + szczawiooctan 6C kw.cytrynowy (syntaza), energia z odszczepienia CoA-SH od octanu z H2O. 2) izomeryzacja do izocytrynianu 3)utlenianie do szczawiobursztynianu (odwodor. Gr -CHOH do =CO) dehydrogenaza izocytr. 4)szczawiobursztynian |enzym ten sam| dekarboksyluje 5C kw.2-oksoglutarowy dekarbo.oksydac. do sukcynylo-CoA 5) +GDP+H3PO44C bursztynian+ GTP+ CoA-SH. 6)odwodom.do kw.fumarowego 7)hydratacja do jabłczanu 8) dehydrogen jabłczanowa 4C szczawioocotan.
10.Koenzymy dehydrogenaz uczestniczących w TCAC- dehydrogenaza z NAD: izocytrynianowa, 2-oksyglutaranowa, jabłczanowa; FAD: bursztynianowa.
11.Produkty TCAC- kw.cytrynowy, cis-Akonitan, Izocytrynian, Szczawiobursztynian, α-Ketoglutaran, bursztynylo-CoA, bursztynian, Fumaran, L-Jabłczan, Szczawiooctan
12. Łańcuch przenośników elektronów (oddechowy)- Pierwsze ogniwo stanowią dehydrogenazy NAD/FAD, które powodują wiąz. at.H z substratów na przez te koenzymy np.w c. Krebsa). Kolejnym przenośnikiem at. H sądehydrogenazy zredukowanego NAD (pobierające H z NADH), zawne flawoproteinami pośredniczącymi (białkowy kompleks siarkowo-żelazowy, mononukleotydem flawinowym (FMN) jako gr. prostetyczną. W kolejnym etapie flawoproteina pośrednicząca przekazuje at.H na ubichinon (CoQ)- redukcja do CoQH2, kóry dalej przekazuje już tylko e- na układ cytochromów (b, c1, c) i oksydazę cytochromową (a+a3), redukując cząst. tlenu do O2-. Protony natomiast przenikają do środowiska i poza łańcuchem łączą się z O2- dając H2O. Elektrony trafiają na cytochrom b, w tym czasie jon Fe3+ tego cytochromy redukuje się do Fe2+, który następnie przekazuje e- na cytochrom c redukując go, (sam wraca do Fe3+). Później dochodzi do redukcji oksydazy cytochromowej (a+a3), która przenosi 4e- na O2 redukując do O2- (tóry łączy się z 2H+ dając H2O). 4 kompleksy enzymatyczne: I- dehydrogenaza NADH (przenoszenie e i H z NADH na CoQ) II reduktaza bursztynian:CoQ III reduktaza CoQH2:cytochrom c. IV oksydaza cytochromowi (redukcja O2 do 2H2O w reak.4e-)
13.Bilans energetyczny TCAC- 4x dehydrogenacja (H 3xNADH i 1xFADH2); 2xdekarboksylacja (-2 CO2), uwolnienie energii: z 3NADH- 9ATP, z FADH2-2 ATP, fosforylacja substratowa- 1ATP= 12 ATP. 14. Wydajność energet. przemian tlen. i beztlen: Oddychanie tlenowe: Substraty: związki organiczne, Produkty: dwutlenek węgla, woda, energia, Ilość energii: 1cz glukozy 38 ATP; Lokalizacja: cytoplazma, mitochondriom. Oddychanie beztlenowe:Substraty: związki organiczne Produkty: alkohole, kwasy Ilość energii: 1 glukoza2 ATP Lokalizacja: cytoplazma
15.Budowa mitochondriów-podst.funk:prod. 2 form energii swobodnej, (protonowej siły motorycznej); przebiegają w nich podst.procesy związ z pobieraniem O2 i wydzieleniem energii, końcowe etapy utlenienia cukrów, lipidów i AA do CO2 i H2O. Dwie bł. białkowo-lipidowe, podobne w bud. do zwykłej bł. komórkowej, o różnych właściwościach. Bł.zewn- zaw. białka- poryny, które są dużymi (2-3 nm średnicy) kanałami, przejdą cząsteczki o masie 5-10kDa. Większe cz. przedost.się przy pomocy transportu aktywnego. ½ masy bł. stanowią fosfolipidy. Wśród białek budujących są enzymy odpowiadające za np. wydłużanie łańcuchów kw. tł., utlenianie adrenaliny i rozkład tryptofanu. Bł.wewn.- brak poryn, jest nieprzepuszczalna - transport jonów i innych cząst. wymaga specjalnych transporterów błonowych. Umożliwia to wytworz. gradientu protonowego niezbędnego do działania łańcucha oddechowego. Zawiera ponad 100 rozmaitych polipep., a białka stanowią ponad ¾ jej masy. Są to białka łańcucha oddechowego, syntaza ATP wytwarzająca ATP w matriks i białka transportujące metabolity do wnętrza i na zewnątrz. Tworzy wpuklenia- grzebienie mitocho.,(gdzie zakotwiczone są enzymy łańcucha oddech,),które zwiększają pow. bł. Wnętrze wypełnia matriks mitochondrialna- rodzaj żelu- wodny roztwór białek i metabolitów mitochondriom oraz modna, rybosomy mt. i tRNA mt.. Białkami wewn. mitoch. są wszystkie enzymy β-oksydacji kw. tł., cyklu Krebsa, syntezy steroidów itp. Mitochondria tworzą w kom. dynamiczną sieć łączących się i rozdzielających organelli. Kształt organelli, stopień pofałdowania wewnętrznej błony jest charakterystyczny dla poszczególnych tkanek. Poj. Kom. zaw. od kilku - kilku tys.sztuk mito.
16. Synteza ATP przez ATP-azę zlokalizowaną w wewn.bł. mitochondrialnej- fosforylacja oksydacyjna; odbywa się dzięki syntetazieATP-wielocząst.enzymowi złoż.z2 zasadniczych części: główki-F1, cz.katalityczna syntetazy, wystaje w kierunku matriks, hydrofilowa. Segment-FO; hydrofobowy; zakotwiczony w wewn.bł.mitochondrialnej; stanowi kanał protonowy całego kompleksu (transport H+). F1 i F0 zespolone białkowa szyjką.
Przepływ e- przez łańcuch oddechowy powoduje przepompowanie H+ z matriksowej na cytoplazmat.str. wewn.bł. mito. Stęż H+ zwiększa się po cytoplazmat.str.bł. wytwarzając potencjał elektryczny(+), wytworzenie ATP warunkuje siła protonomotoryczna. Synteza ATP zachodzi, gdy protony wracają przez kanał F0 ze str.cytoplazmat na matriksową. Rola siły protonomot.polega na wywołaniu zmian konformacyjnych w obrębie c.aktyw F1-niezbędne do uwalniania ATP ściśle związ.z centr.akt. (α i β) syntetazy. Gradient protonowy wytwarza się w 3 miejscah: 1.kompleks reduktazy NADH-ubichinowej; 2,pomiędzy CoQ a cytochromem c1; 3.kompleks oksydazy cytochromu c.
Siła protomotoryczna-wewn.bł.mito. nie przepuszcza H+, gromadzą się one w strefie międzybłonowej, co powoduje jej dodatnie naładowanie wytwarza się gradient elektrochem.(siła) który powoduje obniżenie pH po cytoplazmat str.bł.wewn, o 1,4 w strony matriks do przemieszczania H+ przez bł.prowadzi przepływ e- od (+) do (-).
17.Centralna rola ATP w magazynowaniu i przenoszeniu energii w kom.- uniwersalny akumulator i przenośnik energii skumulowanej w wiązaniach wysokoenerget. Wszystkie procesy energet. służą, osatecznie tworzeniu ATP/ jego redukcji. Nukleotyd, zawiera 3 reszty kwasu ortofosforowego(V), resztę adeniny i rybozy; wchodzi w reakcje tylko w obecności kationów metali 2-wart. (Mn2+, Mg2+), z którymi tworzy kompleksy; powstaje w wyniku fosforylacji substratowej, oksydacyjnej i fotosyntetycznej. ATP jest aktywnym czynnikiem fosforylującym - łatwo odszczepia 1 resztę kw. ortofosforowego(V) przechodząc w ADP i uwalniając z rozerwanego wiązania energię. Budowa ułatwia hydrolizę wiązań: jednoimienne (-) reszty odpychają się, bezwodnikowe wiąz.fosforowe jest silnie przyciągane przez at P.
18. Istota i przebieg fotosyntezy: Istotą jest redukcja CO2 (donor H to H2O) i wytworzenie materii organicznej oraz energii chem. z nieorganicznych substratów (CO2, H2O, sole min) przy udziale energii świetlnej i barwników fotosyntetycznych.
6CO2+6H2O (światło, chlorofil) C6H12O6 +6O2
FAZA JASNA-wytworzenie siły asymilacyjnej, wykorzyst. w fazie ciemnej; istotą jest zamiana enegii świetlnej na chemiczną.
Barwniki fotosyntetyczne tworzą fotosystemy: PS I-chlorofia a + karoteny; PS II- chlorofi a i b + ksantofile.
Reakcje fazy jasnej to fosforylacje cykliczna i niecykliczna. F.cykliczna- bierze udział PS I. Gdy cz.barwnika pochłoną światło, energia przenoszona jest do chlorofilu a, który przekazuje swoje wybite światłem, e-, pierwszemu ich akceptorowi, potem za pośrednictwem akceptorów e- wędrują z powrotem na chlorofil a. W miarę przesuwania e- wzdłuż łańcucha transportu, uwalnia się energia do syntezy ATP. Nie ma fotolizy H2O, więc nie uwalnia się NADPH.
F.niecykliczna- PS II pochłaniając światło przechodzi w stan wzbudzenia; e- przenoszone są wzdłuż łańcucha akceptorów e- i zostają przekazane na PS I, a ostatecznie na NADP+; PS II warunkuje fotolizę H2O i uwalnianie O2. W wyniku fotolizy H2O otrzymujemy e-, O2 i H+-tlen uwalniany jest do atmosfery, e- wypełnia lukę w PS II, a H+ łączy się z NADP+ NADPH
FAZA CIEMNA-niezależna od światła; cykl Calvina:
3C5 Rybulozo-1,5-difosforan [karbksylacja+rubisco+3H2O+3CO2] 6C3 kw.3P-glicerynowy [redukcja; -6NADPH, -6APT] 6C3 aldehyd 3P-glicerynowy {zysk pierwotny: 1 trioza} 5C3 [regeneracja; -3ATP)3 RudP.
Wyszukiwarka
Podobne podstrony:
biochemia egzamin1, Ogrodnictwo UP POZNAŃ
Pytania z Egzaminu biochemi, Ogrodnictwo UP POZNAŃ
ściąga na biochemię na 234kolo, Ogrodnictwo UP Lbn, Biochemia
metody 2 ostatnie cwiczenia, Ogrodnictwo UP Lbn, Ochrona roślin. Metody i środki, Egzamin
pod o war, Ogrodnictwo UP POZNAŃ
zestaw 4, Ogrodnictwo UP Lbn, Biochemia
zestaw 6 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
ostatni kolos, Ogrodnictwo, Ogrodnictwo UP Wro, ROK II, semestr IV, Ochrona roślin (z Fitopatopogia)
KOENZYMY zagadnienia na kolokwium, Ogrodnictwo UP Lbn, Biochemia
Zestawy z biochemie co były na egzamnie, OGRODNICTWO UP LUBLIN, BIOCHEMIA
KWASY NUKLEINOWE, Ogrodnictwo UP Lbn, Biochemia, kwasy nukl
zestaw 2 biochemia, OGRODNICTWO UP LUBLIN, BIOCHEMIA, zestawy
zestaw z pytaniami - biochemia, Ogrodnictwo UP Lbn, Biochemia
maltoza, Ogrodnictwo UP Lbn, Biochemia
więcej podobnych podstron