Zaawansowane metody analizy instrumentalnej
IV rok Ochrony Środowiska
TEMAT ĆWICZENIA:
Oznaczanie lotnych związków organicznych w powietrzu metodą chromatografii gazowej z kriogenicznym wzbogacaniem próbki
Wprowadzenie
Wśród ogromnej liczby organicznych zanieczyszczeń powietrza ważną grupę stanowią węglowodory. Obecność węglowodorów alifatycznych jest szczególnie niekorzystna ze względu na ich udział w fotolitycznym cyklu reakcji z udziałem tlenków azotu, czyli jednym z procesów tworzenia się smogu fotochemicznego. Z kolei niektóre węglowodory aromatyczne mają udowodnione właściwości mutagenne lub kancerogenne.
Głównym antropogenicznym źródłem węglowodorów w powietrzu jest komunikacja samochodowa (spaliny, transport i dystrybucja paliw), ale znaczne ilości wprowadza do atmosfery także przemysł, głównie petrochemiczny i chemiczny (produkcja farb, lakierów i rozpuszczalników). Emitowane są one również ze źródeł naturalnych, głównie przez drzewa, które emitują tylko specyficzne związki - izopren i węglowodory z grupy terpenów.
Stężenia niemetanowych węglowodorów w powietrzu wykazują duże wahania czasowe i przestrzenne, ale są zazwyczaj rzędu μg/m3. Czynniki meteorologiczne (takie jak kierunek i siła wiatru, stan równowagi atmosfery, opady i nasłonecznienie) mają bardzo istotny wpływ na rozprzestrzenianie się zanieczyszczeń w atmosferze, a co za tym idzie na poziom imisji. Zanieczyszczenia są usuwanie z atmosfery wskutek procesów fizycznych oraz reakcji chemicznych, co również ma wpływ na mierzone stężenia zanieczyszczeń w powietrzu.
Metodą stosowaną do znaczeń lotnych związków organicznych w powietrzu atmosferycznym jest chromatografia gazowa. Jest to metoda umożliwiająca rozdzielenie mieszaniny związków oraz w połączeniu z odpowiednim system detekcji dająca informacje o rodzaju i ilości oznaczanych związków. Chromatografię gazową stosuje się do rozdzielania substancji gazowych oraz takich, które można przeprowadzić w stan gazowy w warunkach chromatografowania - poprzez odparowanie lub na drodze przemian chemicznych.
Istotą rozdzielania chromatograficznego jest wielokrotny podział składników mieszaniny pomiędzy dwie nie mieszające się fazy: fazę stacjonarną i fazę ruchomą, którą w chromatografii jest gaz, zwany gazem nośnym. Analizowane substancje wraz z gazem nośnym przemieszczają się w kolumnie chromatograficznej, te które mają większe powinowactwo do fazy stacjonarnej wolniej przemieszczają się wzdłuż kolumny, później docierają do detektora. Rejestrowany jest sygnał detektora w funkcji czasu (lub objętości fazy ruchomej), czyli tzw. chromatogram, z którego po odpowiedniej kalibracji odczuje się informacje jakościową i ilościową składu próbki.
Cel ćwiczenia
Celem niniejszego ćwiczenia jest zapoznanie z metodą oznaczeń lotnych związków organicznych w powietrzu atmosferycznym, metodą chromatografii gazowej z kriogenicznym wzbogacaniem próbki, oraz oznaczenie zawartości węglowodorów w próbkach powietrza atmosferycznego. Część praktyczna ćwiczenia obejmuje: pobranie próbek powietrza do metalowych kanistrów, przygotowanie aparatury do badań, wykonanie analizy chromatograficznej, identyfikację pików na chromatogramie, obliczenie stężeń zidentyfikowanych węglowodorów i ocenę uzyskanych wyników.
Podstawowe pojęcia i definicje
Podstawowym parametrem odczytywanym z chromatogramu, będącym podstawą do identyfikacji związku jest czas retencji (tR), nazywany również całkowitym czasem retencji. Jest to czas mierzony od momentu zadozowania próbki do zarejestrowania maksimum piku chromatografowanej substancji. Całkowity czas retencji jest sumą czasu oddziaływania substancji z fazą stacjonarną (przebywania w fazie stacjonarnej) oraz czasu przemieszczenia się substancji wzdłuż kolumny z fazą ruchomą.
Czas retencji substancji wyznacza się w konkretnych warunkach pomiarowych mających wpływ na jego wartość. Te warunki to w szczególności rodzaj kolumny (jej wymiary i wypełnienie) oraz parametry analizy chromatograficznej (prędkość przepływu gazu nośnego, temperatura kolumny). Porównywanie czasu retencji oznaczanej substancji z wzorcem w celu identyfikacji jest uzasadnione tylko przy zachowaniu identycznych warunków analizy. Dlatego też oprócz tR stosuje się wielkości retencyjne obliczane względem substancji wzorcowych (np. względny czas retencji) lub z uwzględnieniem martwego czasu retencji (tM), np. zredukowany czas retencji.
Bardzo użytecznym parametrem retencji jest indeks retencji wprowadzony przez Kovatča. wyznaczany się w eddstosunku do retencji n-alkanów - jednego o „z” atomach węgla w cząsteczce, eluowanego z kolumny przed tą substancją i drugiego o „z+1” atomach węgla w cząsteczce, eluowanego za tą substancją: Indeks retencji n-alkanu jest iloczynem liczby atomów węgla w cząsteczce i liczby 100, czyli np. dla n-heksanu indeks retencji wynosi 600.
Indeks retencji dowolnej substancji ( Ix ) oblicza się według wzoru:
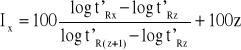
(1)
W przypadku programowania temperatury kolumny używa się temperaturowego indeksu retencji:
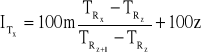
(2)
gdzie: ![]()
- temperatura retencji nieznanych związków,
![]()
- temperatura retencji alkanu zawierającego „z” atomów węgla,
![]()
- temperatura retencji alkanu zawierającego „z + 1” atomów węgla.
Temperatura retencji TR jest to temperatura, w której największa ilość składnika opuszcza kolumnę. Oblicza się ją w oparciu o czas retencji i szybkość grzania kolumny:
TR = T0 + (tR - t0)β (3)
gdzie: T0 - początkowa temperatura kolumny, przed rozpoczęciem ogrzewania [°C],
t0 - czas rozpoczęcia ogrzewania kolumny [min],
β - szybkość grzania [°C/min].
Sprawność rozdzielania
Jako miarę sprawności rozdzielania określonego analitu stosuje się pojęcie liczby półek teoretycznych N:
N = 5,54(tR / w0,5h)2 (4)
gdzie w0,5h jest szerokością piku w połowie jego wysokości,
lub wysokość równoważną półce teoretycznej, która jest definiowana jako :
WRPT = L/N (5)
gdzie L jest długością kolumny chromatograficznej.
Kolumnę cechuje tym lepsza sprawność rozdzielania im większa jest liczba półek teoretycznych i mniejsza wysokość odpowiadająca półce teoretycznej.
Miarą rozdzielenia dwóch składników jest rozdzielczość pików R definiowana wzorem:
Tt5555555![]()
(6)
gdzie: d - odległość między maksimami pików, w1 i w2 - szerokości podstawy pików.
Jeżeli zamiast szerokości pików przy podstawie wykorzystuje się do obliczenia rozdzielczości ich szerokość w połowie wysokości (wh0,5), to wzór powyższy przyjmie postać:
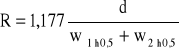
(7)
Piki są tym lepiej rozdzielone im większa jest wartość R. Rozdzielczość „od linii podstawowej” zazwyczaj ma miejsce przy wartości R=1,50, jednakże nie ma wtedy linii podstawy między pikami. Wartości mniejsze od 1,50 wskazują na koelucję piku.
Aparatura do chromatografii gazowej
Schemat aparatury do oznaczeń metodą chromatografii gazowej przedstawiono na rysunku 1. Główne elementy chromatografu gazowego to kolumna chromatograficzna, detektor oraz dozownik. W tym przypadku funkcję dozownika pełni pułapka kriogeniczna wraz z układem zaworów.
Rys. 1 Schemat aparatur do oznaczeń metodą chromatografii gazowej: 1 - butla z gazem nośnym, 2 - pułapka kriogeniczna, 3 - zawory, 4 - kanister z próbką powietrza, 5 - pompa ssąca, 6 - kolumna chromatograficzna, 7 - termostatowany piec kolumny, 8 - detektor,
9 - wzmacniacz, 10 - komputer lub rejestrator.
Pułapkę kriogeniczną (SPT, z ang. Sample Preconcentration Trap) stanowi metalowa rurka, która jest chłodzona ciekłym azotem. W czasie analizy powietrze pobierane z kanistra przepływa przez pułapkę, gdzie następuje wzbogacenie analitów. Przepływ powietrza wymuszony jest przez pompę ssącą. Po etapie wzbogacania do pułapki skierowany zostaje gaz nośny, pułapka jest ogrzewana i anality razem z gazem nośnym dostają się do kolumny.
W kolumnie zachodzi rozdzielenie mieszaniny. Składniki mieszaniny w różnym stopniu są zatrzymywane przez fazę stacjonarną, która może być ciało stałe lub ciecz naniesiona na stałym nośniku. Rozdzielenie składników mieszaniny jest możliwe dzięki procesom adsorpcji lub rozpuszczania. Substancje słabo adsorbujące i słabiej rozpuszczające się szybciej opuszczą kolumnę i dotrą do detektora znajdującego się na końcu kolumny. Detektor reaguje na zmiany składu gazów wypływających z kolumny. Sygnał z detektora jest wzmacniany i zapisywany przez komputer lub rejestrator.
Spośród wielu dostępnych detektorów stosowanych w chromatografii gazowej, do oznaczeń węglowodorów najlepszy jest detektor płomienio-jonizacyjny (FID, z ang. Flame Ionization Detektor). Zasada działania detektora opiera się na wykorzystaniu zmiany przewodnictwa elektrycznego płomienia wodoru w polu elektrycznym po wprowadzeniu substancji organicznej. Jeśli z kolumny do płomienia dochodzi tylko gaz nośny, to mierzony prąd jonowy bardzo mały. Gdy w płomieniu znajdzie się substancja organiczna, powstają karbojony i natężenie prądu jonowego wzrasta. Sygnał detektora jest proporcjonalny do liczby atomów węgla nie związanych z atomami tlenu. Wykrywalność detektora jest rzędu pg C/s, zakres liniowości 107.
Pobieranie próbek powietrza
Spośród znanych metod pobierania próbek powietrza najczęściej stosowane są: metoda izolacyjna i aspiracyjna. O zastosowaniu tych metod decyduje stopień zanieczyszczenia powietrza oraz metoda analizy, którą stosuje się do ilościowej oceny zanieczyszczeń.
Metoda izolacyjna polega na pobraniu powietrza do naczynia o określonej objętości. Takimi naczyniami mogą być:
strzykawki,
pipety gazowe - szklane lub metalowe rurki zakończone obustronnie kranami, zaworami lub zaciskami. Próbki można pobierać stosując technikę zastępowania cieczy przez gaz (wytwarza się podciśnienie), technikę przepływową (zastępowania gazu przez gaz) lub wcześniej wytworzyć podciśnienie pompą próżniową.
worki na próbki gazowe, wykonane z tworzyw sztucznych, np. z teflonu.
Metalowe pojemniki, tzw. kanistry - pojemniki o różnej pojemności, wykonane ze stali nierdzewnej i powierzchni wewnętrznej dezaktywowanej elektrolitycznie. Są to pojemniki wielokrotnego użytku. Przed pobraniem próbki należy je wypompować uzyskując odpowiednio niskie ciśnienie.
Metodą izolacyjną stosuje się zazwyczaj przy dużych stężeniach zanieczyszczeń. Jeśli stężenia są zbyt małe wówczas przed analizą trzeba przeprowadzić wzbogacanie analitów albo zastosować metodę aspiracyjną z równoczesnym wzbogacaniem próbki.
Metoda aspiracyjna polega na przepuszczaniu znanej objętości badanego powietrza przez odpowiednio dobrane ciekłe lub stałe substancje pochłaniające zwane sorbentami. W praktyce stosowane są najczęściej płuczki oraz rurki sorpcyjne. Podczas pobierania prób, oznaczana substancja łączy się z sorbentem w wyniku zjawisk fizycznych (rozpuszczanie, adsorpcja, absorpcja) lub reakcji chemicznych. Przy pobieraniu prób tą metodą istotne jest ustalenie optymalnej szybkości przepływu powietrza oraz odpowiedniej objętości próby.
Pobierając próbę metodą aspiracyjną dokonuje się wzbogacenia próbki oraz zmiany matrycy. Inne sposoby wzbogacania próbki to wzbogacania pasywne (dozymetry pasywne), denudacyjne oraz kriogeniczne. (więcej w literaturze [2])
W każdym z powyższych przypadków przed wykonaniem analizy chromatograficznej anality trzeba przenieść do fazy gazowej lub do ciekłej, co można przeprowadzić na drodze ekstrakcji rozpuszczalnikiem, termodesorpcji.
Obowiązujący zakres materiału naukowego
1. Węglowodory:
Węglowodory alifatyczne i aromatyczne - nazewnictwo, szeregi homologiczne, izomeria, właściwości chemiczne i fizyczne. [3]
Źródła antropogeniczne i naturalne węglowodorów w atmosferze. Czynniki wpływające na poziom imisji. [2]
Przemiany węglowodorów w atmosferze. Smog fotochemiczny. Toksyczność węglowodorów.[2,8]
2. Metody pobierania próbek powietrza. [7]
3. Podstawy teoretyczne chromatografii: [1]
Klasyfikacja metod chromatograficznych.
Pojęcia i definicje: chromatogram, całkowity czas retencji, martwy czas retencji
Od czego zależy wartość czasu retencji; optymalizacja warunków analizy chromatograficznej.
Sprawność kolumny, półka teoretyczna, wysokość równoważna półce teoretycznej, obliczanie liczby półek teoretycznych.
4. Aparatura do chromatografii gazowej [1]
(elementy chromatografu i zasada ich działania)
5. Metody kalibracji stosowane w chromatografii gazowej (metoda wzorca zewnętrznego, metoda wzorca wewnętrznego, sposoby obliczeń wyników końcowych analizy).
Obowiązująca literatura !!!
Szczepaniak W., Metody instrumentalne w analizie chemicznej, PWN, Warszawa 2002, rozdział 14 „Wprowadzenie do metod chromatograficznych” i 15 „Chromatografia gazowa”.
Chemia środowiska, praca zbiorowa pod red. E. Szczepaniec-Cięciak i P. Kościelniaka, t.1, Uniwersytet Jagielloński, Kraków 1999, rozdz. 2.3. i 2,4,
wykłady z chemii organicznej (zagadnienia dotyczące węglowodorów).
Literatura uzupełniająca
Witkiewicz Z.: Podstawy chromatografii, WNT, Warszawa 1995,
R*del W., W*lm G.: Chromatografia gazowa, PWN, Warszawa 1992.
Minczewski J., Marczenko Z.: Chemia analityczna, t. 3, PWN, Warszawa 1987, rozdz. 14.1-14.4.
Namieśnik J., Łukasiak J., Jamrógiewicz Z., Pobieranie próbek środowiskowych do analizy. PWN Warszawa 1995, rozdział III i IV.
Falkowska L., Chemia atmosfery, Wydaw. Uniwersytetu Gdańskiego, Gdańsk 1998.
Gomółka E., Szaynok A. Chemia wody i powietrza. Oficyna Wydawnicza Politechniki Wrocławskiej, Wrocław 1997.
„Węglowodory niemetanowe (NMHC) w powietrzu atmosferycznym.” Część I i II. Kurdziel M., Szczepaniec-Cięciak E. Wiadomości chemiczne 1997, 51, 5-6 oraz 11-12
http://www.pg.gda.pl/chem/Dydaktyka/Analityczna/GC/chrom.htm
Odczynniki, naczynia i przyrządy
Wyposażenie chromatografu zostało dobrane specjalnie pod kątem jego zastosowania do oznaczeń lotnych związków organicznych w próbkach gazowych:
Chromatograf gazowy Varian Star 3600CX, wyposażony w kolumnę kapilarną DB-1 (długość 60m, średnica 0,32 mm, film z polidimetylosiloksanu o grubości 3μm), pułapkę kriogeniczną, zawory iglicowe, zawór 4-drożny i 10-drożny, detektor płomieniowo-jonizacyjny.
pompa ssąca,
miernik przepływu Side-Trak typ 840 (Masowy kontroler przepływu),
naczynie Dewara na ciekły azot,
metalowe kanistry SUMMA® o pojemności 6 dm3,
komputer PC 486DX z zainstalowanym programem „Star Chromarografy Workstation” wersja 4,5,
przepływomierz pęcherzykowy,
Mieszanina wzorcowa 27-składnikowa,
Butle ze sprężonymi gazami (wodór, powietrze, azot, hel),
Ciekły azot.
Przebieg ćwiczenia
1. Omówienie zagadnień związanych z obecnością lotnych związków organicznych w powietrzu atmosferycznym.
2. Zapoznanie się z obsługą aparatury wykorzystywanej w niniejszym ćwiczeniu, kontrola parametrów metody analitycznej (przepływy gazów, temperatury stref grzanych, ustawienie zaworów) i przygotowanie chromatografu do wykonania analizy chromatograficznej.
3. Pobranie próbki powietrza.
4. Analiza próbki powietrza i zarejestrowanie chromatogramu.
5. Kalibracja układu analitycznego - utworzenie metody do identyfikacji pików i obliczania stężeń węglowodorów.
6. Opracowanie uzyskanego chromatogramu: identyfikacja i obliczenie stężeń węglowodorów w oparciu o przeprowadzoną wcześniej kalibrację.
7. Identyfikacja pików na chromatogramie z wykorzystaniem indeksów retencji Kovatca.
Sposób wykonania
Ad. 2.
Przygotowując chromatograf do wykonania analizy chromatograficznej trzeba wykonać następujące czynności:
Sprawdzić przepływów gazów: nośnego i gazów doprowadzanych do detektora.
Optymalne przepływy gazów:
hel (jako gaz nośny) 2,5 cm3/min
gaz nośny i make-up 30 cm3/min
powietrze 300 cm3/min
wodór 30 cm3/min
Włączyć chromatograf i program sterującego jego pracą - moduł „System Control”.
Zapalić płomień w detektorze płomieniowo-jonizacyjnym.
Wskazać metodę oznaczeń i wpisać nazwy analizowanej próbki.
Włączyć pompę i regulator przepływu oraz ustawić odpowiedniego natężenia przepływu.
Przykręcić kanister do układu dozującego i przepłukanie przewodów doprowadzających próbkę
Sprawdzić temperatury poszczególnych elementów chromatografu:
SPT: -175*C utrzymywane przez początkowe 5 min analizy, potem120*C,
kolumna: -60*C utrzymywane przez początkowe 6 min analizy, potem wzrost
temperatury 8*C/min do temp. 20*C i 5*C/min do temp. 180*C,
zawory: 160*C
detektor: 250*C
Ad. 3. Pobranie próbki powietrza
Do pobierania próbek powietrza służą kanistry SUMMA. Przed pobraniem próbki należy przykręcić filtr zapobiegający zasysaniu pyłów i innych stałych zanieczyszczeń. W miejscu pobierania próbki odkręca się lekko zawór i powietrze zostaje zassane do wnętrza kanistra wskutek różnicy ciśnień. Czas pobierania próbki zależy od tego jak mocno odkręci się zawór ale nie przekracza zwykle 5 minut. Po zakręceniu zaworu kanister przenosi się do laboratorium.
Ad. 4. Analiza próbki powietrza i zarejestrowanie chromatogramu
Po osiągnięciu stanu gotowości przez chromatograf można rozpocząć analizę.
Na początku analizy gaz nośny kierowany bezpośrednio do kolumny, a próbka powietrza przepływa przez pułapkę kriogeniczną, w której składniki próbki ulegają skropleniu i zestaleniu. Przepływ próbki wymuszany jest przez pompę ssącą, sprzężoną z regulatorem przepływu, pozwalającym na precyzyjne odmierzanie ilości pobieranej próbki. Składniki próbki powietrza nie ulegające wzbogaceniu są wypłukiwane na zewnątrz. Zazwyczaj natężenie przepływu próbki wynosi 40 cm3/min, a czas wymrażania 4 minuty. Po zakończeniu wzbogacania próbki strumień gazu nośnego zostaje skierowany do pułapki kriogenicznej, cały czas znajdującą się w temperaturze -175*C, wypłukując resztki gazowych substancji. Następnie temperatura pułapki wzrasta do 120*C i następuje desorpcja składników próbki i razem z gazem nośnym dostają się do kolumny. Ponieważ w tym czasie kolumna znajduje się w temperaturze - 60*C, składniki próbki zostają skupione na czole kolumny. W miarę wzrostu temperatury pieca kolumny następuje wymywanie analitów zgodnie ze wzrostem ich temperatur wrzenia.
Całkowity czas analizy wynosi ok. 60 minut. Następnie w celu oczyszczenia układu analitycznego ogrzewa się pułapkę kriogeniczną i kolumnę do temperatury 230 *C przez kilka minut.
Ad. 5. Kalibracja układu analitycznego
Do kalibracji jakościowej i ilościowej układu analitycznego stosuje się mieszaninę wzorcową, zawierającą 27 węglowodorów o stężeniach od 5 do 47 ppbV. Obliczenia wykonuje się metodą wzorca zewnętrznego. W ramach kalibracji wykonuje się następujące czynności:
Analiza mieszaniny wzorcowej na odpowiednich poziomach kalibracji (różne poziomy stężeń uzyskuje się zmieniając czas wzbogacania lub natężenie przepływu próbki przez pułapkę kriogeniczną).
Wypełnienie tzw. tabeli pików: wpisanie nazw pików, czasów retencji, stężeń dla poszczególnych poziomów kalibracyjnych.
Obliczenie współczynników kalibracyjnych dla poszczególnych substancji.
Ad. 6. Opracowanie uzyskanego chromatogramu
Korzystając z programu `Star Chromatography Workstation' należy zidentyfikować piki na otrzymanym chromatogramie porównując ich czasy retencji z czasami retencji składników mieszaniny wzorcowej oraz obliczyć stężenia węglowodorów w oparciu o przeprowadzoną wcześniej kalibrację. Obliczone współczynniki kalibracyjne pozwalają przeliczyć powierzchnie pików na stężenia.
Moduł obróbki danych umożliwia wielokrotne przeliczanie wyników, przy zmianie takich parametrów jak:
sposób wyznaczania linii podstawowej,
linia podziału dwóch pików słabo rozdzielonych,
szerokość okna czasowego piku,
stosunek sygnału do szumu (S/N).
Należy sprawdzić czy zaproponowany przez program dobór tych parametrów jest właściwy i czy ich zmiana wpływa na wyznaczone powierzchnie pików, a tym samym wynik końcowy oznaczenia.
Ad. 7. Identyfikacja pików na chromatogramie za pomocą indeksów retencji Kovatca.
W celu zwiększenia liczby zidentyfikowanych pików na chromatogramie próbki powietrza należy wykorzystać dane retencyjne mieszaniny 60-składnikowej i dokonać identyfikacji pików porównując indeksy retencji. Należy to wykonać w kolejnych krokach:
- obliczenie temperatur retencji dla pików na chromatogramie próbki powietrza,
- obliczenie temperaturowych indeksów retencji pików na chromatogramie próbki powietrza (uwzględnić piki od n-butanu do n-heksanu),
- porównanie obliczonych Iret z indeksami retencji związków występujących w 60-składnikowej mieszaninie wzorcowej,
- identyfikacja węglowodorów o zgodnych indeksach retencji.
Opracowanie wyników
Przygotować sprawozdanie z ćwiczenia zawierające:
Zwięzły opis metody analitycznej.
Opis metody kalibracji wraz z niezbędnymi obliczeniami.
Opracowanie wyników raportu z analizy próbki powietrza zawierające:
- listę zidentyfikowanych związków i ich stężenia,
- związki występujące w największych stężeniach,
- porównanie stężeń węglowodorów w próbce powietrza z dopuszczalnymi wartościami stężeń obowiązującymi na obszarze kraju (znaleźć odpowiednie rozporządzenie MŚ, np. na stronie http://isip.sejm.gov.pl/ ),
- obliczenie sumarycznych stężeń poszczególnych grup związków (alkany, węglowodory alifatyczne nienasycone i węglowodory aromatyczne) oraz udziałów procentowych wyróżnionych grup związków,
- obliczenie sumarycznego stężenia związków niezidentyfikowanych.Zastosowanie indeksów retencji Kovatca do identyfikacji pików na chromatogramie próbki powietrza:
- obliczenie temperatur retencji pików chromatograficznych,
- obliczenie temperaturowych indeksów retencji pików na chromatogramie próbki powietrza (dla pików od n-butanu do n-heksanu),
- porównanie obliczonych Iret z indeksami retencji związków występujących w 60-składnikowej mieszaninie wzorcowej i identyfikacja większej liczby związków.Określenie sprawności rozdzielania używanej kolumny dla wybranych związków - obliczenie liczby półek teoretycznych.
Obliczenie współczynników rozdzielczości R wybranych dwóch par pików.
7
Wyszukiwarka
Podobne podstrony:
CHROMATOGRAFIA CIECZOWA, I MU, Zaawansowana analiza
2010-11, I MU, Zaawansowana analiza
Chromatografia cieczowa egzamin, I MU, Zaawansowana analiza
wyniki MS, I MU, Zaawansowana analiza
CHROMATOGRAFIA CIECZOWA, I MU, Zaawansowana analiza
Prawdopod 2, Ir. ETI MU, Podstawy analizy danych eksperymentalnych
Prawdopod 3, Ir. ETI MU, Podstawy analizy danych eksperymentalnych
Pojencja Wstepne, Ir. ETI MU, Podstawy analizy danych eksperymentalnych
Spark Zaawansowana analiza danych
Spark Zaawansowana analiza danych sparkz
Spark Zaawansowana analiza danych sparkz
Spark Zaawansowana analiza danych
Spark Zaawansowana analiza danych 2
Analiza progu rentownoÂci, licencjat, rok 3, Zaawansowana rachunkowosc zarzadcza
Excel zaawansowany pobieranie i analiza zewnetrznych danych e
Analiza sledcza i powlamaniowa Zaawansowane techniki prowadzenia analizy w systemie Windows 7 Wydani
więcej podobnych podstron