OLEJKI ETERYCZNE
Historia
Termin ”essential oil” prawdopodobnie pochodzi od nazwy utworzonej w XVI wieku przez Paracelsusa, określającej działający składnik leku - Quinta essentia (łac. essentia - istota, byt).
Polska nazwa olejków - „eteryczne” podkreśla cechę ich lotności (łac. aether, gr. aither - substancja gazowa wypełniająca wszechświat).
Destylację, jako sposób otrzymywania olejków, znano już w starożytnym Egipcie i Persji, twórcą metody otrzymywania olejków eterycznych na drodze destylacji był arabski lekarz Awicenna (980-1037r).
Wraz z wiedzą medyczną świata arabskiego dotarła ona do Europy. Już w XV wieku niemiecki lekarz i botanik Valerius Cordus destylował olejek goździkowy. Od tego czasu notowano rozwój wiedzy na temat pozyskiwania olejków eterycznych i możliwości ich stosowania leczniczego.
W latach dwudziestych ubiegłego wieku francuski chemik Rene Gattefosse zainteresował się właściwościami terapeutycznymi olejków, doświadczając leczniczego działania olejku lawendowego zastosowanego w przypadku poparzenia skóry.
W roku 1937 Gattefosse jako pierwszy użył terminu aromaterapia łącząc olejki eteryczne z terapią.
Wystepowanie
Olejki eteryczne są lotnymi mieszaninami, zazwyczaj posiadającymi w swym składzie od kilkudziesięciu do kilkuset związków.
Jako metabolity wtórne, magazynowane są w specjalnej tkance wydzielniczej lub komórkach tkanki gruczołowej; znaleźć je można praktycznie w każdej części rośliny: korzeniach i kłączach (Levistici radix, Calami rhizoma),
zielu (Thymi herba),
liściach (Salviae folium),
kwiatach (Rosae flos, Chamomillae anthodium),
owocach i nasionach (Carvi fructus, Myristicae semen)
korze (Cinnamomi cortex).
W świecie roślinnym występują szczególnie często w rodzinach Lamiaceae, Rosaceae, Apiaceae, Asteraceae, Pinaceae, Cupressaceae, Poaceae, Myrtaceae, Lauraceae, Zingiberaceae, Piperaceae.
W roślinach olejkowych zawartość olejku najczęściej mieści się w granicach 1 - 3%, osiągając jednakże niekiedy nawet 18% (pąki goździkowca, tzw. goździki).
W wielu roślinach, których olejki wykorzystywane są w przemyśle perfumeryjnym, ich ilość nie przekracza 0.1% (np. olejek różany 0.009 - 0.06%).
Skład olejku eterycznego jest cechą gatunku, jednak procentowy udział poszczególnych składników może ulegać wahaniom w zależności od warunków glebowych, klimatycznych, stadium wegetacji i in. Może także zmieniać się w zależności od części rośliny, z której jest pozyskiwany.
Na przykład olejek z liści kolendry zawiera 26% linalolu , natomiast otrzymany z owoców 70% linalolu .
Rola olejków eterycznych w roślinie nie jest do końca poznana; olejki kwiatowe służą jako substancje wabiące owady. Wiele z nich posiada właściwości repelentów czyli substancji odstraszających mrówki, muchy, karaluchy, osy, stosowane są także w celach zwalczania mszyc, roztoczy czy grzybów. Olejki o aktywności przeciwdrobnoustrojowej określane są jako fitoncydy.
Metody otrzymywania
Olejki eteryczne otrzymuje się ze świeżych lub wysuszonych surowców roślinnych najczęściej
metodą destylacji z parą wodną lub hydrodestylacji,
niekiedy przez wyciskanie, dotyczy to jednak głównie olejków otrzymywanych z owoców cytrusowych.
W celach analitycznych lub przemysłowych prowadzi się ekstrakcję rozpuszczalnikami organicznymi (np. eterem etylowym, naftowym, alkoholem).
W perfumerii nadal stosowna jest dawna metoda nawaniania tłuszczów (enfleurage) dosyć pracochłonna jednakże nie powodująca zmian w budowie składników olejkowych.
Nowszą metodą jest ekstrakcja ciekłym dwutlenkiem węgla; tzw. nadkrytyczna, jednak ze względu na wysokie koszty, nie jest powszechnie stosowana.
W farmacji i przemyśle wykorzystuje się także pojedyncze składniki olejków, które otrzymuje się na drodze destylacji frakcjonowanej, lub przez wymrażanie z olejku dominujących związków (stearopteny) np.: mentol, tymol, azulen czy kamfora. Ze względu na prostą budowę, prowadzi się także półsyntezę lub pełną syntezę chemiczną niektórych ważnych składników olejków np.: aldehydu cynamonowego, eugenolu, geraniolu i in..
Własności fizyko-chemiczne
Olejki eteryczne są cieczami o wysokiej temperaturze wrzenia (ok. 150o) i charakteryzującymi się dużą lotnością. Najczęściej są lżejsze od wody o gęstości poniżej 1 g/cm3, gęstość powyżej 1g/cm3 posiadają olejki cynamonowy i goździkowy.
Bezpośrednio po destylacji są bezbarwne lub żółtawe poza nielicznymi wyjątkami olejki azulenowe (zabarwienie niebieskie lub zielone), żółte - olejek pomarańczowy czy brązowe - olejek paczulowy. Przechowywane dłuższy okres czasu zmieniają zabarwienie i konsystencję Silnie załamują światło oraz wykazują charakterystyczną skręcalność światła spolaryzowanego.
Jak podaje Farmakopea Polska VI w monografii ogólnej olejków (Aetherolea),
w wodzie rozpuszczają się słabo,
natomiast z etanolem i rozpusz-czalnikami lipofilnymi (toluen, chloroform, eter etylowy, disiarczek węgla i olejami tłustymi mieszają się w każdym stosunku.
Chemicznie olejki stanowią mieszaniny węglowodorów, alkoholi, aldehydów, ketonów, estrów i eterów, będących terpenami (głównie mono- i seskwiterpeny) a także pochodnymi fenylopropanu. Niekiedy towarzyszą im związki azotowe, siarkowe i inne. W niektórych surowcach (kolendra) składniki olejku mogą występować w formie połączeń glikozydowych. W procesie destylacji z udziałem kwasu siarkowego są hydrolizowane do lotnych aglikonów terpenowych lub fenolowych zwiększając tym samym zawartość składników w końcowym produkcie.
Olejki eteryczne należy przechowywać w naczyniach szklanych, możliwie wypełnionych (szkło oranżowe), szczelnie zamkniętych, w temperaturze nie niższej niż 4oC i chronić od światła.
Budowa wybranych składników olejków eterycznych
węglowodory monoterpenowe
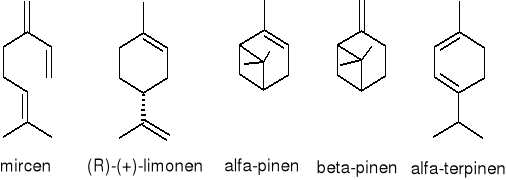
utlenione monoterpeny
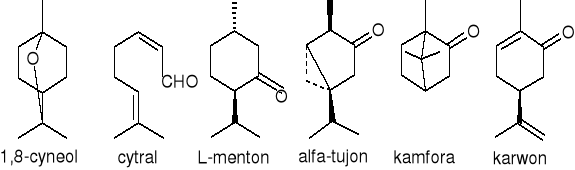
węglowodory seskwiterpenowe: (-)-trans-kariofylen i utlenione seskwiterpeny (+/-)-bisabolol
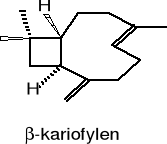
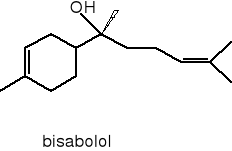
d) pochodne fenylopropanu
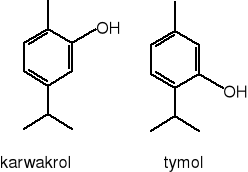
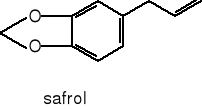
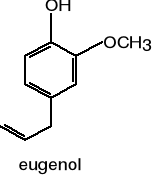
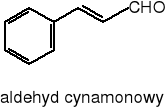
Aktywność biologiczna
Uwagi ogólne
Olejki eteryczne znajdują także zastosowanie w technologii postaci leku, jako tzw. promotory wchłaniania. Prawdopodobnie związki te zwiększają dyfuzję leku przez skórę poprzez wpływ na białka wewnątrzkomórkowe lub lipidy warstwy rogowej skóry (stratum corneum). Badana są możliwości wykorzystanie prostych terpenów, takich jak: D-limonen, L-mentol, (+/-)-linalol, karwakrol, 1,8-cineol jako związków ułatwiających absorpcję leków z maści, żeli oraz systemów transdermalnych.
Olejki wchłaniają się stosunkowo dobrze, praktycznie niezależnie od drogi podania obserwuje się szybkie pojawianie składników olejku we krwi np.: szybka dyfuzja olejków z płuc do krwioobiegu wykorzystywana jest w terapii klimatycznej w strefie specjalnie komponowanych skupisk różnych drzew iglastych. Po aplikacji na skórę, gdy warstwa rogowa nie stanowi wystarczającej bariery ochronnej, czyli kiedy naruszona jest ciągłość skóry, co ma miejsce w przypadku ran, oparzeń czy różnego rodzaju zmian skórnych, możliwe jest nawet całkowite wchłonięcie zaaplikowanego olejku. Doustne podanie, również ze względu na możliwe całkowite wchłonięcie podanej dawki oraz kontakt ze śluzówką przewodu pokarmowego stwarza największe ryzyko wystąpienia działań niepożądanych (działania toksycznego). Z tego też względu należy przestrzegać zasad podawania olejków eterycznych, które obowiązują również w aromaterapii.
Przyjmując olejki doustnie lub na skórę, stosować jedynie rozcieńczone roztwory olejków. Do masażu czy nacierań stosować oleje bazowe np.: olej ze słodkich migdałów lub olej z pestek winogron. Stosować roztwór - 1 kropla na 5 ml nośnika lub, doustnie, kropla na kostkę cukru i popić dużą ilością wody.
Do inhalacji stosować 1-3 kropli olejku, woda powinna być gorąca, lecz nie wrząca.
Dla optymalnego efektu nie mieszać więcej niż trzech olejków. Nie przekraczać jednorazowej dawki 8 kropli.
Działanie antyseptyczne olejków i niektórych ich składników obejmuje: bakterie Gram-(+) i Gram-(-), wirusy, grzyby pleśniowe, drożdże, promieniowce i pierwotniaki. Wart podkreślenia jest fakt, iż olejki działają także na bakterie oporne na antybiotyki. Aktywność przeciwdrobnoustrojowa rośnie wraz ze wzrostem stężenia olejku, jednak zależy głównie od charakteru chemicznego składnika wiodącego. Enancjomery mogą wykazywać różną aktywność. Kierując się aktywnością przeciwdrobnoustrojową składniki olejków eterycznych można uszeregować według następującej kolejności:
fenole > aldehydy > alkohole > ketony > etery > węglowodory.
Tak więc najsilniej przeciwbakteryjnie działają olejki zawierające fenole, takie jak tymol i karwakrol (olejek tymiankowy, cząbrowy, oregano), eugenol (olejek goździkowy i cynamonowy z liści), ale także olejek cynamonowy z kory zawierający aldehyd cynamonowy. Gram-(+) bakterie są bardziej wrażliwe na działanie olejków eterycznych niż Gram-(-). Lipofilny charakter olejków umożliwia przenikanie przez błony komórkowe, warunkując wielokierunkowe działanie przeciwdrobnoustrojowe. Składniki olejków mogą działać na drodze następujących mechanizmów: poprzez uszkodzenie ściany komórki lub błony cytoplazmatycznej, uszkodzenie białek transbłonowych, wyciek cytoplazmy czy zahamowanie pompy wodorowej.
Działanie wykrztuśne olejków związane jest z drażnieniem błony śluzowej oskrzeli, co powoduje wzmożenie wydzielania bardziej płynnego śluzu. Przesuwająca się wydzielina pobudza receptory, nasilając odruch kaszlu. Dodatkowo olejki działają dezynfekująco w obrębie dróg oddechowych. Najskuteczniejszą drogą podania są inhalacje, optymalnie przy użyciu inhalatorów (np. ultradźwiękowych), które produkują wystarczająco małe kropelki wody, by mogły one dotrzeć do najdrobniejszych oskrzelików. Inhalacje zapewniają także odpowiednie nawodnienie dróg oddechowych, na co należy zwracać uwagę szczególnie u dzieci i osób starszych, u których odruch kaszlu może być niewykształcony lub zaburzony. Spośród olejków eterycznych o działaniu wykrztuśnym stosuje się najczęściej: olejek eukaliptusowy, sosnowy, tymiankowy, jodłowy, anyżowy.
Konsekwencją drażnienia kanalików nerkowych jest także zwiększone wydalanie moczu, działanie diuretyczne olejków. Wyraźną aktywność posiadają: olejek jałowcowy, olejek z korzeni lubczyku i, obecnie nie stosowany, olejek z nasion pietruszki. Olejek z szyszkojagód jałowca, jeśli zawiera więcej α- i β-pinenu niż moczopędnego terpinenu-4-olu, działa silnie drażniąco, wywołując po przedawkowaniu uszkodzenie nerek; z tego względu częściej stosuje się połączenie owoców jałowca z inne surowcami o łagodnym działaniu moczopędnym.
Działanie spazmolityczne cechuje wiele olejków eterycznych. Obejmuje ono zmniejszenie napięcia mięśni gładkich, głównie przewodu pokarmowego, oraz przywrócenie prawidłowych ruchów perystaltycznych. Olejek lawendowy, oraz jego główny składnik linalol, wywołują wzrost stężenia wewnątrzkomórkowego cAMP. 1,8-cyneol rozluźnia mięśnie gładkie oskrzeli i naczyń mózgowych, działając także inotropowo ujemnie na mięsień sercowy (poprzez zahamowanie napływu jonów Ca2+ przez sarkoplazmę). Podobnie, jako antagonista wapnia, działa mentol; olejek miętowy w stężeniu 0.05μg/ml obniżał ilość i amplitudę spontanicznych skurczy fragmentów jelita cienkiego królika i kota, a także hamował skurcze wywołane działaniem chlorku baru, pilokarpiną i fizostygminą. Wiele olejków dodatkowo pobudza wydzielanie soku żołądkowego, hamuje nadmierne namnażanie się bakterii. Najczęściej stosowanymi olejkami są: olejek koprowy, olejek kminkowy, rumiankowy, miętowy, melisowy i lawendowy.
Surowcami olejkowymi o działaniu uspakajającym są liść melisy i kwiat lawendy. Do innych surowców, posiadających także aktywność sedatywną, należą: korzeń kozłka i szyszki chmielu, które zawierają w swoim składzie inne aktywne składniki synergizujące to działanie. Aktywność sedatywną olejku melisowego potwierdzono w badaniach na myszach; wykazano zależność od dawki (1 i 3 mg/kg), przy czym w niższej dawce olejek był aktywniejszy. Za działanie uspokajające melisy prawdopodobnie odpowiadają głównie aldehydy terpenowe. W innym badaniu na myszach, podając cytral, mircen i limonen (podanie dootrzewnowe dawek 100 i 200 mg/kg), potwierdzono działanie uspokajające. Linalol, działa prawdopodobnie poprzez hamowanie uwalniania acetylocholiny i wpływ na funkcję kanałów jonowych w połączeniach nerwowo-mięśniowych. Działanie sedatywne na centralny układ nerwowy obejmuje także aktywność nasenną, przeciwdrgawkową i hipotermiczną. Uważa się, że wynikają one z działania miejscowo znieczulającego. W badaniach na myszach potwierdzono znaczący wzrost czasu snu po podaniu dootrzewnowym linalolu w dawce 200 mg/kg. Działanie to było porównywalne do efektu po podaniu diazepamu w dawce 2 mg/kg. Inhalacja olejku lawendowego zmniejszyła mobilność myszy poddanych działaniu kofeiny.
Oprócz wymienionych aktywności, dla olejków eterycznych lub ich składników, w badaniach in vitro i in vivo, potwierdzono między innymi aktywność: przeciwwirusową, przeciwzapalną, przeciwwymiotną, cytotoksyczną, znieczulającą i własności anty-oksydacyjne. Niezwykle cenne są własności chemoprotekcyjne monoterpenów takich jak: limonen, jego metabolitu - alkoholu perilowego, karwonu czy geraniolu. Alkohol perilowy, jako najbardziej aktywny związek, jest obecnie w fazie I i II badań klinicznych nad możliwym zastosowaniem w terapii m.in. raka piersi, prostaty i trzustki.
Do najczęściej stosowanych zewnętrznie postaci leku, zawierających wyciągi roślinne, olejki eteryczne lub ich składniki, należą: maści, kremy, balsamy, żele, emulsje, roztwory oraz czopki i maści doodbytnicze. Wewnętrznie olejki podaje się m.in. jako napary, roztwory, krople czy kapsułki. W schorzeniach górnych dróg oddechowych poleca się inhalacje z czystych olejków lub ich mieszanin (gotowe preparaty).
PIŚMIENNICTWO
1. Góra J. Lis A. Najcenniejsze olejki eteryczne. Wydawnictwo Uniwersytetu Mikołaja
Kopernika Toruń 2004.
2. Delaquis P.J., Stanich, K., Girard B. i wsp.: Int J Food Microbiol 74,101,2002.
3. Farmakopea Polska VI, PTFarm Warszawa 2002.
4. Burt S.: Int J Food Microbiol 94, 223, 2004.
5. Słownik wyrazów obcych. PIW Warszawa 1967.
6. Jaroniewski W.: Wiad Ziel 11, 8, 1991.
7. Dudareva N., Pichersky E., Gershenon J.: Plant Physiol 135, 1893, 2004.
8. Inouye S., Takizawa T., Yamaguchi H.,: J. Antimicrob Chemother 47, 565, 2001.
9. Kalemba D., Lis A.: Aromater. 1,57, 2005.
10. Ochocka J.R., Lis-Balchin M., Deans S., i wsp.: Eur J Pharm Sci 4, 1, S105, 1996.
11. Kalemba D., Kunicka A.: Curr Med Chem 10, 813, 2003.
12. Lis-Balchin M., Hart S.: Phytother. Res. 13, 540, 1999.
13. Soares M.C.M.S., Damiani C.E.N., Moreira C.M. i wsp.: Braz J Med Biol Res 38, 453,
2005.
14. WHO Monograph on Selected Plant. Second edition. Genewa 2001.
15. Sorensen J.M.: Int J Aromather 10, 1/2, 7, 2002.
16. Vale T.G., Furtado E.C., Santos J.G. i wsp.: Phytomedicine 9, 709, 2002.
17. Re L., Barocci S., Sonnino S. i wsp.: Pharm. Res. 42, 2, 177, 2000.
18. Elizabetsky E., Cohelo De Souza G.P., Dos Santos M.A.C. i wsp.: Fitoterapia 66, 5, 407, 1995.
19. Schuhmacher A., Reichling J., Schnitzler P.: Phytomedicine 10, 6-7, 504, 2003.
20. Choi E.M, Hwang J.K.: Fitoterapia 75, 557, 2004.
21. Lutomski J., Kędzia B.: Post. Fitoter. 1, 32, 2000.
22. Peana A.T., D'Aquila P.S., Panin F.i wsp.: Phytomedicine 9, 8, 721, 2002.
23. Juergens U.R., Dethlefsen U., Steinkamp G. i wsp.: Respir Med. 97(3), 250, 2003.
24. Geiger J.: Int J Aromather 15(1), 7, 2005.
25. O'Brien Z.: Pharmacokinetics, in vitro absorption and metabolism of perillyl alcohol, a chemopreventive and chemotherapeutic agent. Dissertation, The Ohio State University 2004, http://www.ohiolink.edu/etd/view.cgi?osu1078118089.
26. Galeotti N., Ghelardini C., Mannelli L.C. i wsp.: Planta Med 67, 174, 2001.
27. Ghelardini C., Galeotti N., Salvatore G. i wsp.: Planta Med 65, 700, 1999.
28. Tomaino A., Cimino F., Zimbalatti V. i wsp.: Food Chem 89, 549, 2005.
29. Ruberto G., Baratta M.T.: Food Chem 69, 2, 167, 2000.
30. Crowell P.L.: J Nutr 129, 3, 775, 1999.
32. Makowska M., Alkiewicz J.: Post. Fitoter. 3, 38, 2000.
33. Cal K.:. Aromater. 3/4(33/34), 9, 20,2003.
34. Lee S., Tsao R., Peterson C., i wsp.: J Econ Entom 90(4), 883, 1997.
35. Ngoh S.P., Choo L.E.W., Pang F.Y. i wsp.: Pestic. Sci. 54, 261, 1999.
36. Isman M.B.: Crop Protection 19, 603, 2000.
37. Enan E.: Comp Biochem Physiol C 130, 325, 2001.
38. Kunta J., Goskonda V.R., Brotherton H.O. i wsp.: J Pharm Sci 86,12, 1369, 1997.
39. Buck P.: Int J Aromather 14, 70, 2004.
40. Krishnaiah Y.S.R., Bhaskar P., Satyanarayana V.: Pharmazie 59, 12, 942, 2004.
Wyszukiwarka
Podobne podstrony:
giełda na koła, oddechowka2, Wysłany: Wto 16 Sty, 2007 11:20 FIZJOLOGIA - giełda ODDECHÓWKA
Wykład I; 16.09.2007, Uczelnia - notatki, dr Dorota Piontek
olejki eteryczne cz3
olejki eteryczne
16 09 2013
16 09 Przyczyny zaburzeń psychicznych
egzamin poprawkowy teoria 16 09 10
OLEJKI ETERYCZNE id 335075 Nieznany
16 424 plan ii rok 14 15 zimowy, 16 09
09 2007 pol 2 odp
Izolacyjnosc ogniowa lekkich przegrod warstwowych calosc 16[1] 11 2007
Olejki eterycznych w kosmetyce Nieznany
5. PATOMORFOLOGIA KOLO 5 2006.2007 (16.12.2007), patomorfologia, pato testy, koło 6
Konspekt 10 16.09 1k., Konspekty klasy 1-3
Teoria egzamin 16.09, 34-36, Zadanie 34
Teoria egzamin 16.09, 27-29, Zadanie 27
Teoria egzamin 16.09, 13-16, Zadanie 13
Olejki eteryczne
więcej podobnych podstron