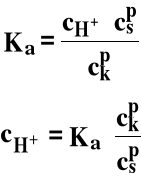XIb. ELEKTROLITY cd.
6. Wodorotlenki
Wodorotlenkami nazywa się związki nieorganiczne, w których we wzorze wyróżnia się kation metalu lub kation amonowy (NH4+) oraz grupę wodorotlenową (OH-).
Np: NaOH, Ca(OH)2, Al(OH)3, Fe(OH)3.
Wodorotlenki, których wodne roztwory mają odczyn wyraźnie zasadowy, nazywamy zasadami. Są to wodorotlenki mocne.
Przykłady: NaOH, KOH, Ca(OH)2.
Ale zasadą jest również wodny roztwór amoniaku (NH3⋅H2O).
Reakcje dysocjacji elektrolitycznej:
NaOH → Na+ + OH-
NH3∙H2O ⇔ NH4+ + OH-
Wodorotlenki dzielimy na:
- wodorotlenki zasadowe - reagują tylko z kwasami;
np: NaOH, Ca(OH)2:
Ca(OH)2 + 2HCl = CaCl2 + 2H2O
- wodorotlenki amfoteryczne - reagują z kwasami i zasadami;
np: Al(OH)3, Zn(OH)2.
Stechiometryczny zapis reakcji roztwarzania wodorotlenku cynku w
kwasach i zasadach:
Zn(OH)2 + 2HCl = ZnCl2 + 2H2O
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4]
7. Sole
W wyniku reakcji kwasu z wodorotlenkiem (tzw. reakcja zobojętnienia) powstają sole.
Przykłady:
HCl + NaOH = NaCl + H2O
chlorek sodu
2HNO3 + Ca(OH)2 = Ca(NO3)2 + H2O
azotan wapnia
H2SO4 + 2NH3·H2O = (NH4)2SO4 + 2H2O
siarczan amonu
2H3PO4 + 3Mg(OH)2 = Mg3(PO4)2 + 6H2O
fosforan magnezu
Sole są związkami stałymi o budowie krystalicznej.
W węzłach ich sieci są kationy metali i aniony reszt kwasowych.
♦ Sole mogą też powstać w reakcjach:
- tlenek kwasowy + tlenek zasadowy
np: CO2 + CaO = CaCO3
- tlenek zasadowy + kwas
np: CaO + 2HCl = CaCl2 + H2O
- tlenek kwasowy + zasada
np: SO2 + 2NaOH = Na2SO3 + H2O
Poznane tutaj sole są solami obojętnymi.
Są też wodorosole i hydroksosole.
♦ Wodorosole (inaczej sole kwaśne) powstają przez niecałkowite
zobojętnienie kwasu wieloprotonowego zasadą.
Przykłady:
H2SO4 + NaOH = NaHSO4 + H2O
wodorosiaczan sodu
H3PO4 + Ca(OH)2 = CaHPO4 + 2H2O
wodorofosforan wapnia
2H3PO4 + Ca(OH)2 = Ca(H2PO4)2 + 2H2O
dwuwodorofosforan wapnia
Hydroksosole (inaczej sole zasadowe) powstają przez niecałkowite zobojętnienie kwasem wodorotlenku posiadającym więcej niż jedną grupę OH-
Przykłady:
Mg(OH)2 + HCl = Mg(OH)Cl + H2O
chlorek hydroksomagnezu
♦ Niektóre sole są bardzo trudno rozpuszczalne w wodzie. Przykłady:
- większość siarczków np. CuS, HgS,
- większość fosforanów np. Ca3(PO4)2 ,
- niektóre chlorki np. AgCl,
- niektóre siarczany np. CaSO4.
8. Hydroliza soli
Odczyn roztworów wodnych
kwasów → kwaśny; pH < 7,0
zasad → zasadowy; pH > 7,0
Jaki jest odczyn roztworu wodnego soli - obojętny?
(1) NaCl → Na+ + Cl- pH = 7,0
(2) NH4Cl → NH4+ + Cl- pH < 7,0
(3) CH3COONa → CH3COO- + Na+ pH > 7,0
Dlaczego odczyn soli (2) i (3) nie jest obojętny?
Przyczyną jest zjawisko hydrolizy
Definicja:
Hydrolizą nazywamy proces rozkładu jakiejś substancji (soli) następujący pod wpływem wody. Ściślej: hydrolizie ulegają jony wywodzące się z danej soli. |
I tak hydrolizie ulegają jony:
reakcja (2) NH4+
(3) CH3COO-
hydrolizie nie ulegają natomiast jony Na+ czy Cl-
b) Opis ilościowy reakcji hydrolizy
1o NH4+ + H2O ⇔ NH3·H2O + H+
odczyn słabo kwaśny
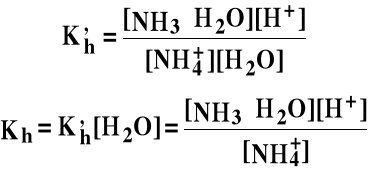
Pomnóżmy obie strony przez [OH-]
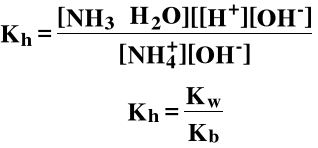
Jeżeli nie ma dodatkowych jonów "wspólnych":
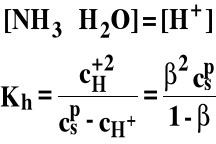
β - stopień hydrolizy, 0 < β < 1
Dla β << 1 Kh = β2 csp
2o CH3COO- + H2O ⇔ CH3COOH + OH-
odczyn słabo zasadowy
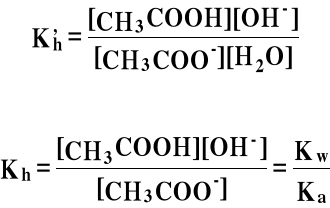
Jeżeli nie ma dodatkowych jonów "wspólnych":
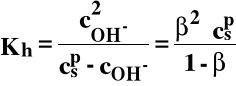
3o NH4+ + CH3COO- + H2O ⇔ NH3⋅H2O + CH3COOH
Odczyn tego typu soli zależy od tego co jest „mocniejsze”, tj. kwas czy zasada:
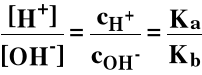
W przypadku CH3COONH4: pKa = pKb, [H+] = [OH-] i dla
pKw = 14,00 mamy pH = 7,0
Inne jony ulegające hydrolizie:
Zn2+ + H2O = [ZnOH]+ + H+
Al3+ + H2O = [AlOH]2+ + H+
![]()
+ H2O = HCO3- + OH-
9. Roztwory buforowe (bufory)
Bufory są to roztwory wodne, których pH nie zmienia się przy dość znacznych rozcieńczeniach, oraz w których dodatek niewielkich ilości mocnego kwasu lub mocnej zasady powoduje małe zmiany kwasowości (zasadowości) roztworu. |
||
Roztworem buforowym może być roztwór wodny: - słabej zasady i jej soli,
- roztwór dwóch soli słabego kwasu wieloprotonowego. |
||
a) Bufor: Słaby kwas + jego sól, np.
CH3COOH + CH3COONa
Równowagę w tej mieszaninie opisuje reakcja:
CH3COOH = CH3COO- + H+
Wpływ jonów octanowych pochodzących od octanu sodu - cofa się dysocjacja.
Stała równowagi kwasu octowego. Ka, w obecności octanu sodu przyjmuje postać:
|
csp, ckp - stężenia początkowe octanu sodu i kwasu octowego |
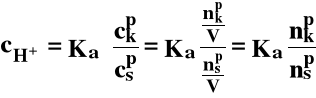
1o Wpływ rozcieńczenia (w określonych granicach) - [H+] nie zmienia się
2o Wpływ dodatku niewielkiej ilości mocnego kwasu - niewielka zmiana pH roztworu
CH3COOH = CH3COO- + H+
H+ z mocnego kwasu
Dysocjacja cofa się - równowaga przesuwa się w lewo
3o Wpływ dodatku niewielkiej ilości mocnej zasady
CH3COOH = CH3COO- + H+
OH- z mocnej zasady
Dysocjacja zwiększa się - równowaga przesuwa się w prawo
b) Bufor: słaba zasada + jej sól:
NH3 ⋅ H2O + NH4Cl
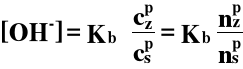
c) Bufor: mieszanina dwóch soli tego samego kwasu:
NaH2PO4 + Na2HPO4
(kwas) (sól)
H2PO4- ⇔ HPO42- + H+ (Ka2)
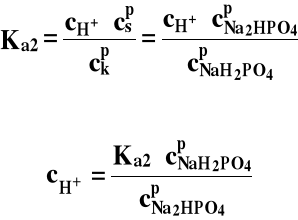
10. Iloczyn rozpuszczalności
Niektóre elektrolity cechuje niska lub bardzo niska rozpuszczalność w wodzie.
Weźmy nasycony roztwór wodny AgCl:
AgCl ⇔Ag+ + Cl-
dla I = const.
|
|
Ag+, Cl- |
← roztwór nasycony |
|
←osad AgCl |
W roztworze nasyconym [AgCl] = const.
[Ag+][Cl-] = K ⋅ [AgCl] = Ir
Ir - iloczyn rozpuszczalności dla I = const. i T = const.
Dla siarczku cyny(IV): ![]()
Ir = [Sn4+][S2-]2
Dla fosforanu wapnia: ![]()
Ir = [Ca2+]3[PO43-]2
Definicja: Iloczyn rozpuszczalności jest iloczynem ze stężeń najprostszych postaci jonów związku słabo rozpuszczalnego i jest wielkością stałą w danej temperaturze i sile jonowej. |
W tabelach często zamiast Ir podaje się pIr : pIr = -logIr
Tabela rozpuszczalności wybranych związków nieorganicznych:
|
|
|
|
|
|
|
|
|
|
Na+ |
|
|
|
|
|
|
|
|
|
K+ |
|
|
|
|
|
|
|
|
|
Mg2+ |
B |
B |
|
|
|
|
|
B |
B |
Ca2+ |
|
B |
|
|
|
|
B |
B |
B |
Al3+ |
B |
B |
|
|
|
B |
|
B |
B |
Pb2+ |
B |
B |
B |
B |
Ż |
Cza |
B |
B |
B |
Zn2+ |
B |
B |
|
|
|
B |
|
B |
B |
Ag+ |
Br |
|
B |
Ż |
Ż |
Cza |
|
Ż |
Ż |
Cu2+ |
N |
|
|
|
Br |
Cza |
|
N |
N |
Fe2+ |
B |
|
|
|
|
Cza |
|
B |
N |
Fe3+ |
Br |
|
|
|
Br |
Br |
|
Br |
Ż |
Ni2+ |
Z |
|
|
|
|
Cza |
|
Z |
Z |
Co2+ |
R |
|
|
|
|
Cza |
|
Cze |
Fi |
Cr3+ |
Z |
Z |
|
|
|
Cza |
|
|
Z |
Kolory związków trudnorozpuszczalnych:
B - biały Cza - czarny Cze - czerwony Br - brązowy
R - różowy Z - zielony N - niebieski Fi - fioletowy
Ż - żółty
Puste pole oznacza iż dany związek chemiczny jest rozpuszczalny w wodzie.
Przykładowe wartości pIr dla I = 0 w temp. 298 K
|
Ag+ 11,09
Mg2+ 4,05 |
Ba2+ 8,69
Ni2+ 8,18 |
Ca2+ 8,41
Pb2+ 13,13 |
Cd2+ 12,00
Zn2+ 10,84 |
Co2+ 9,98
|
Fe2+ 10,46
|
|
|
Ag+ 19,89
Pb2+ 42,10 |
Al3+ 18,24
Mg2+ 25,20 |
Zn2+ 32,04 |
Bi3+ 22,89
|
Cr3+ 26,0
|
CaH3+ 6,66
|
Fe3+ 21,89
|
AsO43- |
Ag+ 22,0 |
Al3+ 15,80 |
Ba2+ 50,11 |
Bi3+ 9,36 |
Ca2+ 18,17 |
Cd2+ 32,66 |
Co2+ 28,12 |
|
Cu2+ 35,12 |
Cr3+ 20,11 |
Fe3+ 20,24 |
Mg2+ 19,68 |
Mn2+ 28,72 |
Ni2+ 25,51 |
Pb2+ 35,39 |
|
Ag+ 49,2 |
Bi3+ 97,0 |
Cd2+ 26,1 |
Co2+ 20,4 |
Cu+ 47,6 |
Cu2+ 35,2 |
|
S2- |
Hg2+ 49,2 |
Fe2+ 17,2 |
Mn2+ 9,6 |
Ni2+ 18,5 |
|
|
|
|
Pb2+ 26,6 |
Sn2+ 25,9 |
Zn2+ 23,8 |
|
|
|
|
SO42- |
Ba2+ 9,77 |
Ca2+ 4,37 |
Pb2+ 7,78 |
Sr2+ 6,49 |
|
|
|
F- |
Ca2+ 10,40 |
Mg2+ 8,19 |
Pb2+ 7,57 |
|
|
|
|
Cl- |
Pb2+ 4,79 |
Ag+ 9,75 |
|
|
|
|
|
Jak obliczyć rozpuszczalność związku słaborozpuszczalnego w czystej wodzie?
(brak dodatkowych jonów wspólnych)
Przykład:
wodny nasycony roztwór Ag2CrO4:
Ag2CrO4 ⇔ 2Ag+ + CrO42-
Uwaga:
Ag2CrO4 należy traktować jako związek "złożony" z Ag+ i CrO42-
- inaczej więc należałoby pisać Ag2[CrO4]
Stężenie molowe Ag2CrO4 w roztworze wodnym nad osadem to tzw. rozpuszczalność tej soli w wodzie - R =
Ir = [Ag+]2 [CrO42-] = (2R)2 R = 4R3
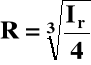
Stąd:
Uwaga: W tych rozważaniach nie uwzględniono hydrolizy jonów Ag+ i CrO42-
Rozpuszczalność w obecności elektrolitu zawierającego jony wspólne
Rozpuszczalność Ag2CrO4 w obecności K2CrO4 (jony wspólne, tj. ![]()
) oznaczane są jako R1:
Ir = [Ag+]2[CrO42-] = (2R)2 ⋅ (R + cK2CrO4)
Rozpuszczalność zmaleje, więc:
R1 << cK2CrO4
Ir = (2R1)2 ⋅ cK2CrO4
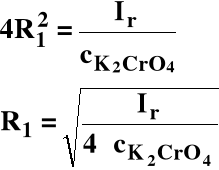
R1 << R
Władysław Walkowiak - Chemia Ogólna. WPC1002w
19
Rozdział 11b. Równowagi w roztworach wodnych elektrolitów. Kwasy. Zasady. Sole.
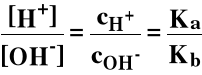
Wyszukiwarka
Podobne podstrony:
Wyklad 6. Uklad okresowy pierwiastkow, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wyklad 12. Reakcje jadrowe, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
WYKŁAD 1. Wstepne pojecia chemiczne, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wyklad 4. Reakcje utleniajaco-redukcyjne, pwr biotechnologia(I stopień), I semestr, Chemia ogó
Wyklad 11a. Elektrolity, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wykład VI, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wykład VIII, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wykład X, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wykład V, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
wykład XIV, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Wyklad XIII, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Test z WPC1002w Walkowiak, pwr biotechnologia(I stopień), I semestr, Chemia ogólna
Egzamin (2), pwr biotechnologia(I stopień), V semestr, Biologia molekularna, Egzamin
Wykład 11b. Elektrolity - cd., chemia, CHEMIA OGÓLNA -Walkowiak- (WPC 1002w) DOC
Wyklad 11b Elektrolity cd , hydroliza, bufory, iloczyn rozpuszczaln
egzamin (11), pwr biotechnologia(I stopień), VI semestr, Inżynieria genetyczna - wykład, Egzamin
więcej podobnych podstron