Poch kw barbiturowego
Działanie nasenne
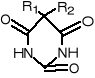
R1-C2H5 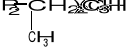
pentobarbital
R1-C2H5 ![]()
cyklobarbital
R1-C2H5 ![]()
fenobarbital
Krotkotrwałe dział nasenne i p/drgawkowe
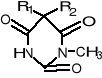
R1-C2H5 ![]()
heksobarbital
![]()
metylofenobarbital
Dział narkotyczne o krótkim okresie działania
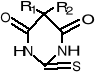
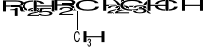
tiopental
![]()
tialbarbital
![]()
butalital
Retrosynteza-odwrócona synteza
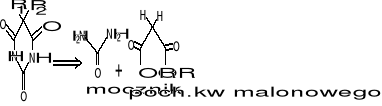
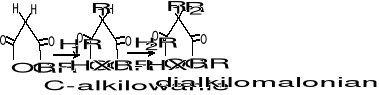

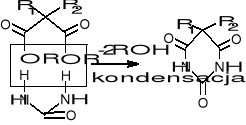
Związki typu II i III ![]()
N-metylomocznik tiomocznik
Bardzo efektywna metoda dla podstawników alkilowych lub allilowych (poch. 5,5-dialkilowe)
Schemat produkcji kw dietylobarbiturowego
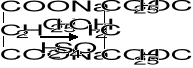
C6H6 temp 25-60º
↓
rozdzielanie warstw: fazy wodnej i benzenowej
↓
przemywanie wyciągu benzenowego rocz. NaOH, suszenie bezw Na2CO3
↓
Destylacja pod zmn ciś estru etylowego kw malonowego 94-96 stop C
↓

↓
Destylacja frakcyjna - wydzielenie gł produktu
↓
Dodajemy wodę Rozdzielanie warstw estru etylowego kw dietylomalonowego od r-ru NaBr
↓
Destylacja pod ciś 18mm w temp 132-135
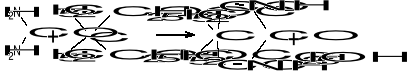
↓
Odestylowanie EtOH + H2O + steż HCl
↓
Odwirowanie surowego kwasu i przemycie H2O
↓
Rozpuszczenie w H2O + wegiel, ogrzewanie , odfiltrowanie
↓
Krystalizacja, odwirowanie i suszenie 40-50stop C
5-arylo, 5-alkilowe pochodne kw. barbiturowego
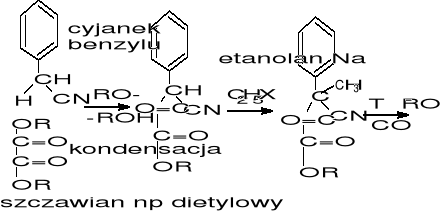
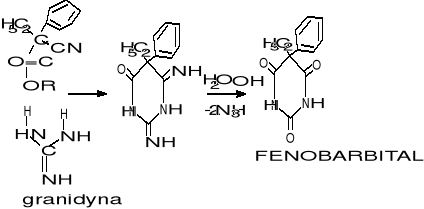
5-alkenylo, 5-alkilowe poch kw barbit
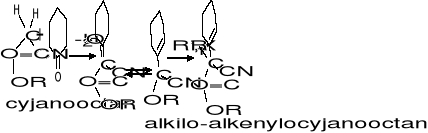
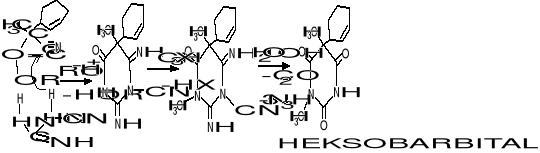
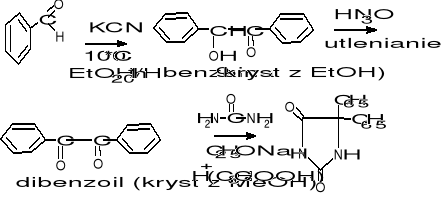
Pochodne hydantoiny 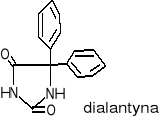
1 METODA
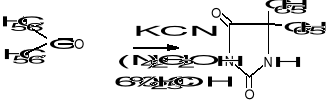
2 METODA Bucherera-Bergsa
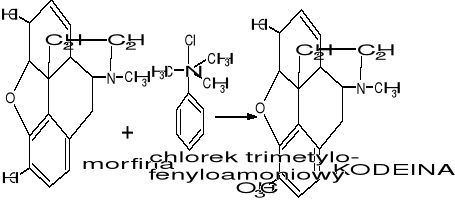
Otrzymywanie kodeiny
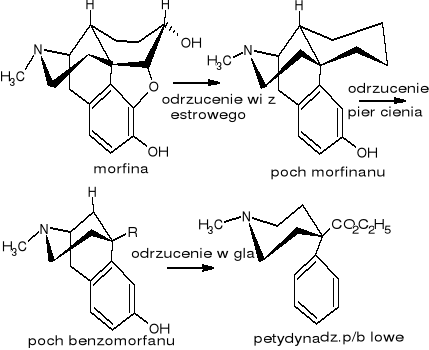
Otrzymywanie petydyny
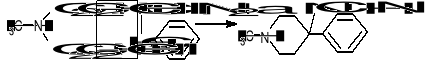
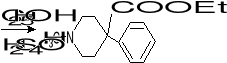
NaNH2-otrzym przez rozpuszczenie Na w ciekłym amoniaku; silniejsza zasad od NaOH; pod wpływem NaOH rozkłada się
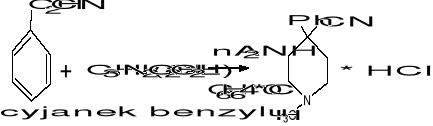
↓
+NaOH ekstrakcja estrem
↓
oddestylowanie eteru, oczyszczanie przez dest próżniową
↓
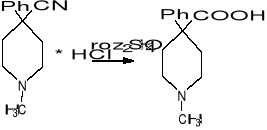
↓
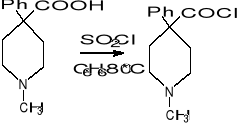
↓
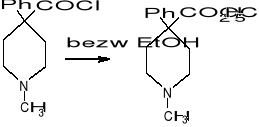
↓
oczyszcz przez kilkakrotną krystal
Otrzymywanie lewometadonu
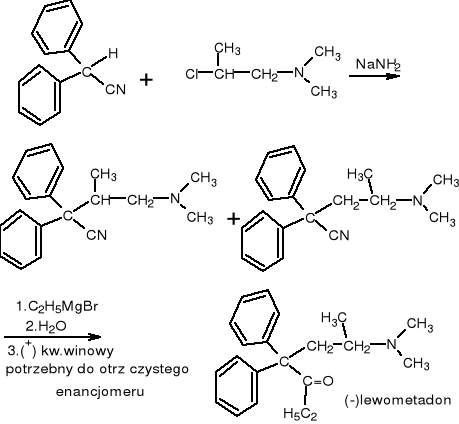
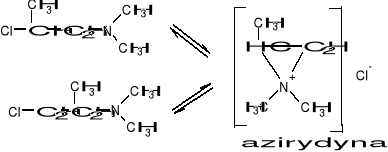
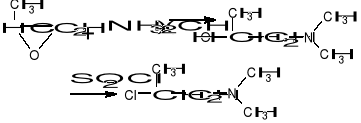
Otrzymywanie lewometadonu
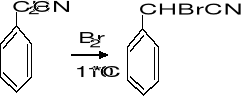
↓
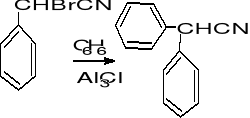
↓
+ HCl , oddestylowanie benzenu
krystalizacja(izopropanol)
↓
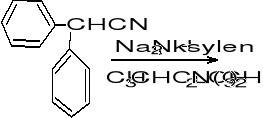
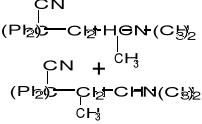
↓
+woda , oddestylowanie ksylenu
+ heksan, krystalizacja
↓

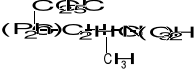
↓
+NaOH , ekstrakcja eterem
krystalizacja
↓
rozdzielenie izomerów optycznych
przy pomocy(+)kw winowego
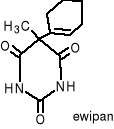
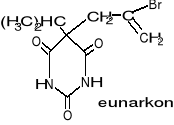
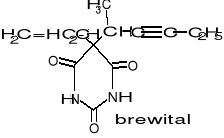
Narkotyki wziewne poch kw barbitur
Wyszukiwarka
Podobne podstrony:
7981
7981
7981
7981
7981
7981
7981
7981
praca-magisterska-wa-c-7981, Dokumenty(2)
7981
7981
09 PODSTAWY PRAWNE FUNKCJONOWANIA ZOZid 7981 pptx
więcej podobnych podstron