Andrzej Michalski 17.12.2009 r.
Robert Jała
Dominika Machul
SPRAWOZDANIE
Ćwiczenie 8
Wyznaczanie parametrów kinetyki reakcji enzymatycznej
Cel ćwiczenia
Celem ćwiczenia jest wyznaczenie stałej Km, Vmax, oraz stworzenie odpowiednich wykresów. W tym celu wykorzystano właściwość zmiany skręcalności roztworu podczas hydrolizy sacharozy do glukozy i fruktozy.
Przebieg ćwiczenia
Przygotowanie rozcieńczeń
Do kolby na 100 ml wsypano 10g sacharozy, dolano wody destylowanej do kreski i dokładnie rozpuszczono. 50 ml roztworu przelano do osobnej kolby - w ten sposób posiadamy 10% roztwór sacharozy. Do pozostałych 50 ml dolano wody do kreski, wymieszano i odlano kolejne 50 ml - stężenie 5%. Następnie znowu dolano wody do kreski i w ten sposób otrzymano stężenie 2,5%.
Pomiar skręcalności
Do 10% roztworu sacharozy dodano 0,1 ml enzymu inwertazy i dobrze wymieszano. Roztwór szybko wlano do rurki polarymetrycznej i rozpoczęto pomiar skręcalności. Pierwszy pomiar przeprowadzono po 30 sekundach po dodaniu inwertazy, a kolejne co 4 minuty od dodania enzymu. Pomiary dokonano dla każdego ze stężeń sacharozy. Wyniki pomiarów notowano i wyliczono dzięki nim odpowiednie wartości.
Tabele wyników
Stężenie 10% |
||||||
Czas |
Skręcalność α[◦] |
Stężenie substratu Cs [g/100ml] |
Stężenie produktu C0-Cs [g/100ml] |
Początkowa szybkość reakcji v0 [g/100 ml *min] |
1/C0 |
1/v0 |
35 |
11,95 |
9,23 |
0,77 |
1,32 |
0,10 |
0,76 |
240 |
10,6 |
8,45 |
1,55 |
|
|
|
480 |
9,55 |
7,84 |
2,16 |
|
|
|
720 |
8,85 |
7,43 |
2,57 |
|
|
|
960 |
8,05 |
6,97 |
3,03 |
|
|
|
Stężenie 5% |
||||||
Czas |
Skręcalność α[◦] |
Stężenie substratu Cs [g/100ml] |
Stężenie produktu C0-Cs [g/100ml] |
Początkowa szybkość reakcji v0 [g/100 ml *min] |
1/C0 |
1/v0 |
30 |
5,7 |
4,46 |
0,54 |
1,02 |
0,20 |
0,98 |
240 |
5,1 |
4,11 |
0,89 |
|
|
|
480 |
4,35 |
3,67 |
1,33 |
|
|
|
720 |
3,6 |
3,24 |
1,76 |
|
|
|
960 |
3 |
2,89 |
2,11 |
|
|
|
Stężenie 2.5% |
||||||
Czas |
Skręcalność α[◦] |
Stężenie substratu Cs [g/100ml] |
Stężenie produktu C0-Cs [g/100ml] |
Początkowa szybkość reakcji v0 [g/100 ml *min] |
1/C0 |
1/v0 |
20 |
3 |
2,32 |
0,19 |
0,56 |
0,40 |
1,80 |
240 |
2,35 |
1,94 |
0,56 |
|
|
|
480 |
1,8 |
1,62 |
0,88 |
|
|
|
720 |
1,35 |
1,36 |
1,14 |
|
|
|
960 |
1,1 |
1,21 |
1,29 |
|
|
|
Wykresy
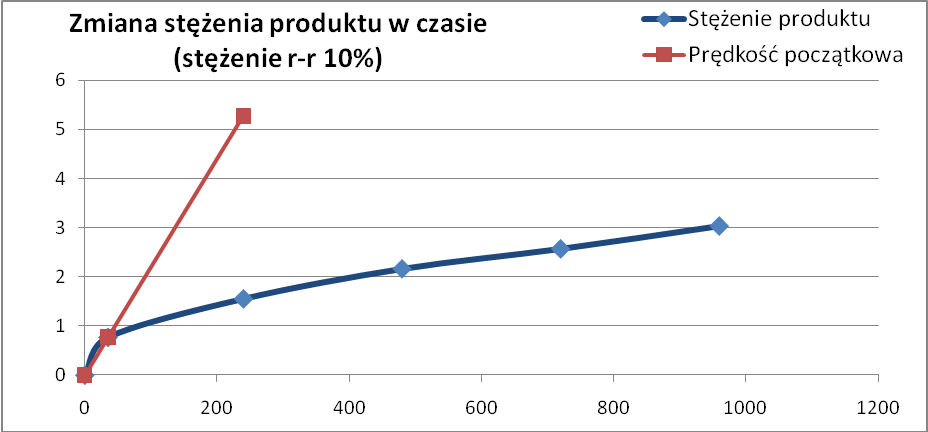
Obliczanie stałych Km oraz Vmax
Wzór lini trendu dla wykresu Lineweavera - Burka:
Aby obliczyć Vmax należy obliczyć f(0), a następnie odwrócić wynik:
Aby obliczyć stałą Km należy obliczyć f(x)=0, a następnie odwrócić wynik:
Wnioski
Wykresy zmian produktów w czasie na początku szybko rosną, natomiast później prędkość spada. Spowodowane jest to ciągłym zmniejszaniem się stężenie sacharozy w roztworze, a co za tym Idze - zmniejszeniem prędkości jej rozkładu.
Wyliczona wartość stałej Km , (która jest dosyć wysoka i wynosi 10,2), jest to stężenia substratu przy którym prędkość wynosi połowę prędkości maksymalnej Vmax. Nasze stężenia (10, 5, 2.5 %) są trochę zbyt niskie. Brakuje nam stężenia powyżej 10%, aby lepiej pokazać wszystkie zależności na wykresie.
Wysoka wartość stałej Km, (a więc słabe powinowactwo substratu do enzymu) może być spowodowane słabą jakością enzymu - inwertazy.
Prędkości początkowe zostały wyliczone na podstawie początkowych zmian stężeń sacharozy. Dla stężenia 10% pierwszy pomiar odbył się po około 35 sekundach i prędkość została policzona właśnie dla tych pierwszych sekund. Dla kolejnego stężenia pomiar odbył się już szybciej (ze względu na nabieranie wprawy ). Dla ostatniego stężenia pierwszy pomiar zrobiliśmy już po 20 sekundach. Niestety możliwe, że te wartości mogą nie być bardzo dokładne, ponieważ występowały opóźnienia czasowe podczas włączania stopera.
Vmax
Km
1/Vmax
-1/Km
Wykres Km
Vmax/2
Wyszukiwarka
Podobne podstrony:
Sprawozdanie Biochemia Kinetyka reakcji polarymetr
Biotech enzym Kinetyka reakcji hydrolizy sacharozy katalizowanej przez inwerazę Sprawozdanie gr
Egzamin2007, Biotechnologia, Semestr III, Biochemia
z, Biotechnologia, Semestr III, Biochemia
09-BIOCHEMIA-Pomiar-aktywnosci-dr, Biotech, BIOTECHNOLOGIA, Semestr V, Biochemia, Wykłady, Aktualne
reakcje z analitycznej, Biotechnologia PWR, Semestr 4, Podstawy chemii analitycznej - Laboratorium,
zerowka z biochemii, Biotechnologia, Semestr III, Biochemia
sss teoria, Biotech, BIOTECHNOLOGIA, Semestr V, Spec. Bioinf, SSS, Egzamin
Atmosfera, Biotechnologia, Semestr I, Ochrona Środowiska
cw1 Zadania, Biotech, BIOTECHNOLOGIA, Semestr V, Spec. Bioinf, SSS, LAB, Lab 2
opracowanie skanow, Biotechnologia, Semestr III, Biologia molekularna
SPRAWOZDANIE Z LABOLATORIUM Z FIZYKI I BIOFIZYKI cw.5, biotechnologia inż, sem2, FiB, laborki, spraw
Wyznaczanie parametrów kinetyki reakcji enzymatycznej za pomocą metod polarymetrycznych 5x
Program kursu ch.og.-cw wer. II, Biotechnologia, SEMESTR 1, Chemia ogólna
14.10, Studia Biotechnologia, Semestr 7 - II stopnia - mikrobiologia molekularna, Metagenomika
Pytania z PCR 2, Studia Biotechnologia, Semestr 7 - II stopnia - mikrobiologia molekularna, Metody P
Rozdział mieszanin i roztworów, Biotechnologia, Semestr 1, Chemia ogólna, Egzamin
Zadania na 2 kolokwium z algebry, Biotechnologia, SEMESTR 1, Algebra liniowa z geometrią analityczną
Związki organiczne ChOgol, Biotechnologia, Semestr 1, Chemia ogólna, Egzamin
więcej podobnych podstron